트리글리세리드
Triglyceride| 식품의 지방 종류 |
|---|
| 「 」를 참조해 주세요. |
트리글리세리드(TG, 트리아실글리세롤, TAG 또는 트리아실글리세리드)는 글리세롤 및 세 가지 지방산(트리글리세리드 및 글리세리드)[1]에서 유래한 에스테르이다.트리글리세라이드는 식물성 [2]지방뿐만 아니라 인간과 다른 척추 동물들의 체지방의 주요 성분입니다.그것들은 또한 간에서 지방과 혈당의 양방향 전달을 가능하게 하기 위해 혈액에 존재하며, 인간 피부 [3]오일의 주요 성분이다.
많은 종류의 트리글리세리드들이 존재한다.한 가지 특정 분류는 포화 및 불포화 유형에 초점을 맞춘다.포화지방은 C=C기를 가지지 않으며, 불포화지방은 하나 이상의 C=C기를 특징으로 한다.불포화지방은 포화유사체보다 녹는점이 낮은 경향이 있습니다. 그 결과, 종종 상온에서 액체 상태가 됩니다.
화학 구조
트리글리세라이드는 3개의 지방산 분자에 결합된 글리세롤로 구성된 트리 에스테르입니다.알코올에는 수산기(HO-)가 있습니다.유기산은 카르복실기(–COOH)를 가지고 있다.알코올과 유기산이 결합하여 에스테르를 형성합니다.글리세롤 분자는 3개의 수산기(HO-)를 가지고 있고 각 지방산은 카르복실기(-COOH)를 가지고 있다.트리글리세리드에서는 글리세롤의 수산기가 지방산의 카르복실기와 결합하여 에스테르 결합을 형성합니다.
- HOCH2(OH)CHOH2 + RCOH2 + RcoCOH2 + RcoCOH2 → RCOCH22(OCR2)CHCOR22 + 3HO2
세 가지 지방산(위2 식에서는 RCOH, RcoCOH2, RcoCOH2)은 많은 종류의 트리글리세라이드가 알려져 있기 때문에 보통 다르다.자연적으로 발생하는 트리글리세리드 지방산의 사슬 길이는 다양하지만, 대부분은 16, 18 또는 20개의 탄소 원자를 포함합니다.식물과 동물에서 발견되는 천연 지방산은 전형적으로 짝수 탄소 원자로만 구성되어 있으며, 이는 2탄소 빌딩 블록 아세틸 CoA로부터의 생합성 경로를 반영한다.그러나 박테리아는 홀수 사슬 지방산과 분기 사슬 지방산을 합성하는 능력을 가지고 있다.그 결과 반추동물의 지방은 반추동물의 세균 작용에 의해 15 등의 홀수지방산을 함유하고 있다.많은 지방산은 불포화이다; 어떤 지방산은 다불포화이다.[4]
대부분의 천연 지방은 개별 트리글리세리드 혼합물을 포함하고 있습니다.이것 때문에, 그것들은 광범위한 온도에서 녹는다.코코아 버터는 글리세롤의 1, 2, 3단계에서 [4]팔미트산, 올레인산 및 스테아린산으로부터 파생된 소수의 트리글리세리드만으로 구성되어 있다는 점에서 특이하다.
호모 및 헤테로트리글리세리드
가장 단순한 트리글리세라이드는 세 가지 지방산이 동일한 것입니다.스테아린에서 유래한 스테아린, 팔미틴에서 유래한 팔미틴 등의 지방산을 나타낸다.이들 화합물은 α, β, β의 세 가지 결정 형태(다형체)로 얻어질 수 있으며, [4][5]이 세 가지 형태는 녹는점이 다르다.
글리세롤의 첫 번째 지방산과 세 번째 지방산이 다르면 트리글리세라이드는 [6]키랄이다.
컨피규레이션
지방과 지방산 분자의 모양은 대개 잘 정의되지 않는다.단 하나의 결합으로 연결된 분자의 두 부분은 그 결합을 중심으로 자유롭게 회전할 수 있습니다.따라서 n개의 단순 결합을 가진 지방산 분자는 n-1 독립적인 방식으로 변형될 수 있다(말단 메틸기의 회전도 계산).
이러한 회전은 분자의 절반 중 하나를 180도 회전시켜 분해하고 다시 변형하는 경우를 제외하고는 이중 결합을 통해 발생할 수 없으며, 이는 상당한 에너지 장벽을 넘어야 합니다.따라서 이중 결합을 가진 지방 또는 지방산 분자(사슬의 맨 끝부분 제외)는 유의하게 다른 화학적 및 생물학적 특성을 가진 여러 cis-trans 이성질체를 가질 수 있다.각 이중 결합은 구조 자유도를 1개씩 감소시킵니다.각각의 3중 결합은 가장 가까운 4개의 탄소를 일직선으로 배치하여 2개의 자유도를 제거한다.
따라서 이중 결합(스테아린과 같은)이 없는 "포화" 지방산과 하나의 시스 결합(올레산과 같은)이 "팔꿈치" 모양으로 구부러지는 것은 다소 오해의 소지가 있다.후자는 약간 덜 유연하지만, 둘 다 비슷한 직선 또는 팔꿈치 모양을 가정하기 위해 비틀 수 있습니다.사실, 결정이나 양층막과 같은 특정한 맥락 밖에서는, 두 형태 모두 두 형태 중 어느 한 형태보다 무작위로 뒤틀린 형태로 발견될 가능성이 더 높습니다.
예
| 스테아린산 포화상태의 | |
|---|---|
| 올레인산 불포화 cis-8 |  |
| 엘라이드산 불포화 트랜스-8 | |
| 박센산 불포화 트랜스11 |
스테아린산은 동물성 지방에서 발견되는 포화 지방산(단일 결합만 있음)이며, 완전한 수소화에서 의도된 제품입니다.
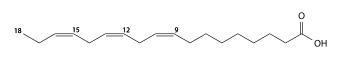
올레인산은 사슬의 중간쯤에 시스 형상과 이중 결합(따라서 "불포화")을 가지고 있으며, 올리브유의 55~80%를 차지한다.
엘라이드산은 트랜스 이성질체로 부분적으로 수소화된 식물성 기름에 존재할 수 있으며, 두리안 과일의 지방(약 2%)과 유지방(0.1%)에서도 발생합니다.
박센산은 이중 결합의 위치에서만 엘라이드와 다른 또 다른 트랜스산이다. 또한 유지방(약 1~2%)에서도 발생한다.
명명법
일반적인 지방 이름
지방은 보통 그 공급원의 이름을 따서 지어지거나 그들만의 전통적인 이름을 가지고 있다.이 이름들 중 일부는 적절한 지방 외에 상당한 양의 다른 성분이 포함된 제품들을 가리킨다.
화학적 지방산 명칭
화학과 생화학에서, 수십 개의 포화 지방산과 수백 개의 불포화 지방산은 보통 그들의 소스 지방(부틸릭, 카프릴릭, 스테아릭, 올레산, 팔미틱, 신경학)에서 영감을 얻은 전통적인 과학/기술적 이름을 가지고 있지만, 때때로 그들의 발견자(마드, 오스본드)를 가지고 있다.
그런 다음 트리글리세리드는 글리세릴 1,2-디올레이트 [7]3-팔미테이트와 같은 해당 산의 에스테르로 명명됩니다.
IUPAC
IUPAC(International Union of Pure and Applied Chemistry)가 개발한 일반 화학명칭에서 해당 탄화수소의 이름에서 파생된 지방산의 권장 명칭은 탄소수 및 이중결합의 수와 위치를 규정함으로써 그 구조를 완전히 기술한다.따라서 올레산은 예를 들어 "(9Z)-옥데틱-9-에노산"이라고 불리며, 이는 한 끝에 카복실기가 있는 18개의 탄소 사슬("옥데틱")과 카복실("9-en")에서 계수되는 탄소 9에 이중 결합을 가지며, 이중 결합에 인접한 단일 결합의 구성은 (9Z)이다.lso는 수소 원자가 다른 화학 그룹에 의해 대체되는 분기 사슬과 유도체를 다룬다.
트리글리세라이드는 일반적인 에스테르 규칙에 따라 예를 들어 "프로판-1,2,3-트릴 1,2-비스(9Z)-옥데덱-9-에노에이트) 3-(헥사데카노에이트)"로 명명된다.
지방산코드
IUPAC만큼 정밀하지만 해석하기 쉬운 분기 사슬이 없는 지방산 특유의 표기법은 "{N}:{D} cis-{CC} trans-{TTT}), {N}은 탄소수(카르복실기 1 포함), {D}은 이중결합수, {CC}은 시스 이중결합의 위치 목록, {TT}은 트랜스결합의 위치 목록입니다.해당 유형의 결합이 없는 경우 목록과 레이블은 생략됩니다.
따라서 예를 들어 스테아린산, 올레산, 엘라이드산 및 박센산의 코드는 각각 "18:0", "18:1 cis-9", "18:1 trans-9" 및 "18:1 trans-11"이 될 것이다.IUPAC 명명법의 α-올레오스테아린산 코드(9E,11E,13Z)-옥타데카-9,11,13-트리에노산)는 코드 '18:3 트랜스-9,11 cis-13'이다.
분류
체인 길이별
지방은 구성 지방산의 탄소 사슬 길이에 따라 분류될 수 있다.녹는점이나 산도와 같은 대부분의 화학적 성질은 이 매개변수에 따라 서서히 변하기 때문에 급격한 구분이 없다.화학적으로 포름산(1탄소)과 아세트산(2탄소)은 가장 짧은 지방산으로 볼 수 있으며, 트리폼린은 가장 단순한 트리글리세리드이다.그러나, "지방산"과 "지방"이라는 용어는 일반적으로 상당히 긴 [citation needed]사슬을 가진 화합물들을 위해 남겨져 있다.
생화학 및 영양학에서 일반적으로 만들어지는 부문은 다음과 같다.[citation needed]
- 탄소가 6개 미만인 짧은 사슬 지방산(SCFA)입니다(예: 낙산).
- 6~12개의 탄소를 가진 중쇄 지방산(MCFA)입니다(예: 염소산).
- 13~21개의 탄소를 가진 긴 사슬 지방산(LCFA)입니다(예: 페트로셀린산).
- 22개 이상의 탄소를 가진 매우 긴 사슬 지방산(VLCFA) (예: 26개의 세로틴산)
트리글리세리드 분자는 길이가 다른 지방산 요소를 가질 수 있으며, 지방 제품은 종종 다양한 트리글리세리드 혼합물이 될 것이다.식물이든 동물이든 음식에서 발견되는 대부분의 지방은 보통 같거나 거의 같은 길이의 중간에서 긴 사슬 지방산으로 구성되어 있습니다.
포화 및 불포화 지방
인간의 영양을 위해, 지방의 중요한 분류는 구성 지방산의 이중 결합의 수와 위치에 기초한다.포화 지방은 이중 결합이 없는 포화 지방산이 우세한 반면, 불포화 지방은 이중 결합이 있는 불포화 산이 주를 이룬다.(이중결합은 화학식 중 수소원자가 2개 적다는 것을 의미한다.따라서, 이중 결합을 가지지 않는 포화 지방산은 주어진 수의 탄소 원자에 대해 수소 원자의 최대 수를 가지고 있다. 즉, 수소 원자와 함께 "포화"된다.)[8][9]
불포화지방산은 단일 이중 결합을 가진 단일 불포화(MUFAs)와 2개 이상의 [8][9]다불포화(PUFAs)로 더욱 분류된다.자연 지방은 같은 분자에도 여러 개의 다른 포화산과 불포화산을 함유하고 있습니다.예를 들어 대부분의 식물성 기름에서 포화 팔미트산(C16:0) 및 스테아린산(C18:0) 잔류물은 보통 글리세롤 허브의 위치 1 및 3(sn1 및 sn3)에 부착되며, 중간 위치(sn2)는 보통 올레산(C18:1, δ–9-18) 또는 L:2와 같은 불포화산에 의해 점유된다.
| 스테아린산(포화, C18:0) | |
| 팔미톨레산(단일불포화, C16:1 cis-9, 오메가-7) | |
| 올레산(단일불포화, C18:1 cis-9, 오메가9) | |
| α-리놀렌산(다불포화, C18:3 cis-9, 12, 15, 오메가-3) | |
| γ-리놀렌산(다불포화, C18:3 cis-6, 9, 12, 오메가-6) |
일반적으로 가장 큰 관심을 끄는 것은 다불포화 지방산의 영양 측면이지만, 이러한 물질들은 비식품적인 용도도 가지고 있다.그것들은 아마인(아마씨), 텅, 양귀비씨, 들깨, 호두기름과 같은 고체막을 형성하기 위해 산소에 노출되면 중합되는 건조유를 포함하고 페인트와 바니시를 만드는 데 사용된다.
포화지방은 일반적으로 분자량이 같은 불포화지방보다 녹는점이 높기 때문에 상온에서 고체가 될 가능성이 높다.예를 들어 동물성 지방인 티로우와 라드는 포화지방산 함량이 높고 고형물이다.반면에 올리브 오일과 아마인 오일은 불포화 및 액체입니다.불포화 지방은 공기에 의해 산화되기 쉬운데, 이것은 그것들을 상하고 먹을 수 없게 만든다.
불포화 지방의 이중 결합은 촉매에 의해 영향을 받는 수소와 반응하여 단일 결합으로 전환될 수 있습니다.수소화라고 불리는 이 과정은 식물성 기름을 마가린과 같은 고형 또는 반고형 식물성 지방으로 바꾸는데 사용되는데, 마가린은 타우와 버터를 대체할 수 있고 (불포화 지방과 달리) 썩지 않고 무기한으로 저장될 수 있습니다.그러나 부분 수소화는 또한 [11]시스산으로부터 원치 않는 트랜스산을 생성한다.
세포 대사에서 불포화 지방 분자는 동등한 양의 포화 지방보다 약간 더 적은 에너지(즉, 더 적은 칼로리)를 생산한다.포화, 모노, 디 및 트라이 불포화 18-탄소 지방산 에스테르 연소열은 각각 2859, 2828, 2794 및 2750 kcal/mol로 측정되었으며, 중량 기준으로는 10.75, 10.71, 10.66, 10.58 kcal/g – 각각 이중 [12]결합에 대해 약 0.6% 감소하였다.
지방산의 불포화 정도가 클수록(즉, 지방산의 이중 결합이 많을수록) 지질 과산화(란산성)에 취약하다.항산화제는 지질 과산화로부터 불포화 지방을 보호할 수 있다.
시스 및 트랜스 지방
불포화 지방산의 또 다른 중요한 분류는 이중 결합에 인접한 C–C 단일 결합의 공간적 배열인 cis-trans 이성질체를 고려한다.자연에서 발생하는 대부분의 불포화 지방산은 시스("같은 면") 구성에서 이러한 결합을 가지고 있습니다.시스 지방의 부분적인 수소화는 지방산의 일부를 트랜스("대면") 품종으로 바꿀 수 있습니다.
엘라이드산은 인간의 식단에서 가장 흔한 지방산 중 하나인 올레인산의 트랜스 이성질체이다.하나의 이중 결합에서 구성이 한 번 바뀌면 화학적, 물리적 특성이 달라집니다.엘라이드산은 13.4°C가 아닌 45°C로 올레인산보다 녹는점이 훨씬 높습니다.이러한 차이는 일반적으로 트랜스 분자가 더 단단하게 채워져 [13]분해하기 더 어려운 고체를 형성할 수 있는 추정된 능력에 기인한다.
오메가 수
또 다른 분류는 사슬의 끝(카르복실기 반대)에 상대적인 이중 결합의 위치를 고려한다.위치는 "θ-k" 또는 "n-k"로 표시되며, 이는 탄소 k와 k+1 사이에 이중 결합이 있다는 것을 의미한다.예를 들어, α-리놀렌산은 "γ-3" 또는 "n-3" 산이며, 이는 세 번째와 네 번째 탄소 사이에 이중 결합이 있다는 것을 의미한다. 즉, 구조식은 –CH=CH-CH-CH-CH로
2
3 [14]끝난다.
포화지방산의 예
지방산의 일반적인 예는 다음과 같습니다.
- 4개의 탄소 원자를 가진 낙산(버터에 함유)
- 12개의 탄소 원자를 가진 라우르산(코넛 오일, 팜 커널 오일 및 모유에 포함)
- 14개의 탄소 원자를 가진 미리스트산(우유 및 유제품에 포함)
- 16개의 탄소 원자를 가진 팔미트산(야자유 및 육류에 포함)
- 18개의 탄소 원자를 가진 스테아린산(고기 및 코코아 버터에도 포함)
불포화지방산의 예
- 미리스톨레산 C14:1, γ-5, cis-9-테트라데센산
- 사피엔산 C16:1γ-10, cis-6-헥사데센산
- 팔미톨레산 C16:1, γ-7, cis-9-헥사데센산
- 올레인산 C18:1γ-9, 시스-9-옥데세논산
- 페트로셀린산 C18:1γ-12, 시스옥데덱-6-에노산
- 시스-바센산, C18:1γ-7, 시스-11-옥데세논산
- 박센산 C18:1γ-7, 트랜스-11-옥데세논산
- 엘라이드산 18:1µ-9, 트랜스-9-옥데데센산(트랜스올레산)
- 리놀산
- 리놀렌산
- 폴린산 C20:1µ-7, 시스-13-에이코센산
- 가돌레산 C20:1γ-11, 시스-9-이코센산
- 곤도산 20:1µ-9, 시스-11-에이코센산
- 에루크산 C22:1γ-9, 시스-15-도코센산
- 브라시드산 C22:1γ-9, 트랜스-15-도코센산
- 네르본산 C24:1γ-9, cis-15-테트라코센산
- 아라키돈산
산업용도
아마인 오일 및 관련 오일은 유화 페인트 및 관련 코팅에 사용되는 유용한 제품의 중요한 성분입니다.아마인 오일은 산소 존재 하에서 굳어지는 경향이 있는 디 및 삼불포화 지방산 성분이 풍부합니다.이 열을 발생시키는 경화 과정은 소위 말하는 건조유에 특이합니다.그것은 산소 분자가 탄소 골격을 공격하면서 시작되는 중합 과정에 의해 발생합니다.
트리글리세리드도 바이오디젤 제조 과정에서 에스테르 분해를 통해 성분으로 분해된다.생성된 지방산에스테르를 디젤 엔진의 연료로 사용할 수 있습니다.글리세린은 식품 제조나 의약품 제조 등 다양한 용도로 사용된다.
염색
지방산, 트리글리세리드, 리포단백질 및 기타 지질에 대한 염색은 리소크롬(지방용성 염료)을 사용하여 이루어집니다.이 염료들은 재료를 특정 색상으로 염색함으로써 특정 관심 지방을 선별할 수 있습니다.몇 가지 예:수단 IV, 오일 레드 O, 수단 블랙 B.
인터랙티브 패스 맵
아래의 유전자, 단백질 및 대사물을 클릭하여 각각의 기사와 연결하세요. [§ 1]
- ^ 대화형 경로 맵은 WikiPathways에서 편집할 수 있습니다."Statin_Pathway_WP430".
「 」를 참조해 주세요.
- 디글리세리드아실전달효소, 트리글리세리드생합성효소
- 중쇄 트리글리세리드
- 지질 프로파일
- 지질
- 수직 자동 프로파일
레퍼런스
- ^ "Nomenclature of Lipids". IUPAC-IUB Commission on Biochemical Nomenclature (CBN). Retrieved 2007-03-08.
- ^ Nelson, D. L.; Cox, M. M. (2000). Lehninger, Principles of Biochemistry (3rd ed.). New York: Worth Publishing. ISBN 1-57259-153-6.
- ^ Lampe, M. A.; Burlingame, A. L.; Whitney, J.; Williams, M. L.; Brown, B. E.; Roitman, E.; Elias, M. (1983). "Human stratum corneum lipids: characterization and regional variations". J. Lipid Res. 24 (2): 120–130. doi:10.1016/S0022-2275(20)38005-6. PMID 6833889.
- ^ a b c Alfred Thomas (2002). "Fats and Fatty Oils". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a10_173. ISBN 3527306730.
- ^ Charbonnet, G. H.; Singleton, W. S. (1947). "Thermal properties of fats and oils". J. Am. Oil Chem. Soc. 24 (5): 140. doi:10.1007/BF02643296. S2CID 101805872.
- ^ Lok, C.M.; Ward, J.P.; van Dorp, D.A. (1976). "The synthesis of Chiral Glycerides starting from D- and L-serine". Chemistry and Physics of Lipids. 16 (2): 115–122. doi:10.1016/0009-3084(76)90003-7. PMID 1269065.
- ^ N. Koeniger와 H. J. Veith(1983) : "Glyserl-1, 2-dioleate-3-palmitate, 꿀벌(Apismellifera L)"경험치, 제39권, 1051~1052쪽 doi:10.1007/BF01989801
- ^ a b "Essential Fatty Acids". Micronutrient Information Center, Oregon State University, Corvallis, OR. May 2014. Retrieved 24 May 2017.
- ^ a b "Omega-3 fatty acids, fish oil, alpha-linolenic acid". Mayo Clinic. 2017. Retrieved 24 May 2017.
- ^ Institute of Shortenings and Edible oils (2006). "Food Fats and oils" (PDF). Archived from the original (PDF) on 2007-03-26. Retrieved 2009-02-19.
- ^ Marchand, V (2010). "Trans fats: What physicians should know". Canadian Paediatric Society. 6 (15): 373–375. doi:10.1093/pch/15.6.373. PMC 2921725. PMID 21731420.
- ^ Krisnangkura, Kanit (1991). "Estimation of heat of combustion of triglycerides and fatty acid methyl esters". Journal of the American Oil Chemists' Society. 68: 56–58. doi:10.1007/BF02660311. S2CID 84433984.
- ^ "Section 7: Biochemistry" (PDF). Handbook of chemistry and physics. 2007–2008 (88th ed.). Taylor and Francis. 2007. Retrieved 19 November 2007.
- ^ 카렌 둘리 (2008) : "오메가 3 지방산과 당뇨병"플로리다 대학 UFHealt 웹사이트의 온라인 기사.2020-08-30에 접속.