글리코겐
Glycogen글리코겐은 포도당의 다당류로 동물,[2] 곰팡이, 박테리아에서 에너지 저장의 한 형태 역할을 한다.[3]다당체 구조는 체내 포도당의 주요 저장 형태를 나타낸다.
글리코겐은 두 가지 형태의 에너지 비축물 중 하나로, 글리코겐은 단기용이고 다른 형태는 장기 저장을 위한 지방 조직(즉, 체지방)에 트리글리세리드 저장소로 기능한다.인간에서 글리코겐은 주로 간과 골격근의 세포에 만들어 저장된다.[4][5]간에서 글리코겐은 장기의 신선한 무게의 5~6%를 차지할 수 있고, 1.5kg의 성인의 간은 약 100~120g의 글리코겐을 저장할 수 있다.[4][6]골격근육에서 글리코겐은 낮은 농도(근육량의 1~2%)에서 발견되며 몸무게 70kg인 성인의 골격근은 약 400g의 글리코겐을 저장한다.[4]
특히 근육과 간 내에 있는 글리코겐의 양은 대부분 신체 훈련, 기초 대사율, 식습관[7](특히 산화 타입 1 섬유[8][9])에 따라 달라진다.휴식의 대부분의 글리코겐 입자는 이론적 최대치보다 작지만 기존 입자의[10] 크기를 증가시키기보다는 글리코겐 입자의 수를 변화시킴으로써 휴식의 근육 글리코겐의 다른 수준에 도달한다.[11]소량의 글리코겐은 또한 신장, 적혈구,[12][13][14] 백혈구,[15] 뇌의 활혈구 등 다른 조직과 세포에서도 발견된다.[16]자궁은 또한 태아에게 영양을 공급하기 위해 임신 중에 글리코겐을 저장한다.[17]
약 4그램의 포도당이 인간의 혈액에 항상 존재한다.[4] 단식하는 개인에서는 간 및 골격근에 있는 글리코겐 저장소의 희생으로 이 수준에서 일정하게 유지된다.[4]골격근에 있는 글리코겐 저장소는 근육 자체를 위한 에너지 저장의 한 형태로 작용하지만,[4] 근육 글리코겐의 파괴는 혈액으로부터 근육 포도당을 흡수하는 것을 방해하여 다른 조직에서 사용할 수 있는 혈당의 양을 증가시킨다.[4]간 글리코겐 저장소는 몸 전체, 특히 중추신경계를 위한 포도당 저장소의 역할을 한다.[4]인간의 뇌는 약 60%의 혈당량을 금식, 좌식성 개인에게서 소비한다.[4]
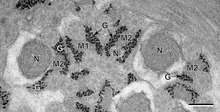
글리코겐은 식물에서 에너지 저장 역할을 하는 포도당 중합체인 전분의 아날로그다.아밀로펙틴(전분 성분)과 비슷한 구조를 가지고 있지만 전분보다 더 넓게 갈고 압축된다.둘 다 건조한 상태의 백색 가루다.글리코겐은 많은 세포 유형에서 시토솔/사이토플라즘의 과립 형태로 발견되며 포도당 주기에 중요한 역할을 한다.글리코겐은 포도당의 갑작스러운 필요를 충족시키기 위해 빠르게 동원될 수 있는 에너지 비축량을 형성하지만 트리글리세리드(지질)의 에너지 비축량보다 압축성이 떨어지는 것을 말한다.이와 같이 많은 기생 원생동물에서도 저장보존물로 발견된다.[18][19][20]
구조
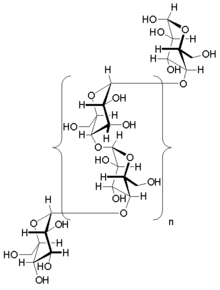
글리코겐은 포도당 평균 길이 약 8–12의 포도당 잔류물과 글리코겐 1개 분자당 2000-60,000개의 잔류물을 가진 포도당 잔류물의 선형 사슬로 구성된 분기형 생물폴리머다.[21][22]
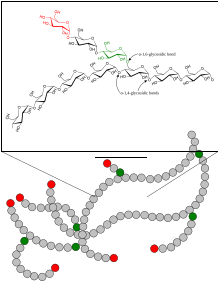
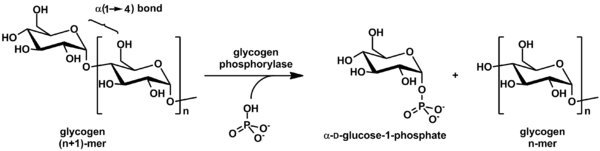
포도당 단위는 한 포도당에서 다음 포도당으로 α(1→4) 당질 결합에 의해 선형적으로 연결된다.가지들은 새로운 가지의 첫 번째 포도당과 줄기 체인의 포도당 사이의 α(1→6) 당귀 결합에 의해 분기되는 사슬에 연결된다.[23]
글리코겐을 합성하는 방법 때문에, 모든 글리코겐 과립은 핵심에 글리코겐 단백질을 가지고 있다.[24]
근육, 간, 지방 세포의 글리코겐은 글리코겐의 그램 당 0.45밀리몰(18mg)의 칼륨과 연관된 글리코겐의 부분당 서너 부분으로 구성된 수분 형태로 저장된다.[5]
포도당은 삼투압 분자로, 고농도의 삼투압에 심대한 영향을 미칠 수 있으며, 수정되지 않고 세포에 저장하면 세포 손상이나 사망으로 이어질 수 있다.[3]글리코겐은 비삼투압 분자여서 삼투압에 지장을 주지 않고 세포에 포도당을 저장하는 용액으로 사용할 수 있다.[3]
기능들
간
탄수화물이나 단백질을 함유한 식사를 먹고 소화하면 혈당 수치가 올라가고 췌장은 인슐린을 분비한다.관문맥에서 혈당이 간세포(혈구세포)로 들어간다.인슐린은 간세포에 작용하여 글리코겐 싱타아제를 포함한 여러 효소의 작용을 자극한다.포도당 분자는 인슐린과 포도당이 모두 풍부하게 남아 있는 한 글리코겐의 사슬에 첨가된다.이 식후 또는 "식사 후" 상태에서 간은 혈액에서 방출되는 것보다 더 많은 포도당을 섭취한다.
식사가 소화되고 포도당 수치가 떨어지기 시작하면 인슐린 분비가 감소하고 글리코겐 합성이 중단된다.에너지에 필요할 때 글리코겐은 분해되어 다시 포도당으로 전환된다.글리코겐인산화효소는 글리코겐 분해의 1차 효소다.향후 8-12시간 동안 간 글리코겐에서 도출된 포도당은 나머지 신체에서 연료로 사용하는 혈당의 일차 공급원이 된다.
췌장에 의해 생성되는 또 다른 호르몬인 글루카곤은 많은 면에서 인슐린에 대항하는 역할을 한다.인슐린 수치가 정상 이하(글루코겐의 혈중 수치가 정상 범위 이하로 떨어지기 시작할 때)에 반응하여 글루카곤은 증가하는 양에 분비되어 글리코겐 분해(글리코겐의 분해)와 글루코네제시스(다른 소스로부터 포도당 생산)를 모두 자극한다.
근육
근육 세포 글리코겐은 근육 세포에 이용 가능한 포도당의 즉각적인 예비 공급원으로 기능하는 것으로 보인다.소량을 포함하는 다른 세포들도 그것을 국소적으로 사용한다.근육세포는 혈중으로 포도당을 전달하는데 필요한 포도당-6-인산화효소가 부족하기 때문에 이들이 저장하는 글리코겐은 내부용으로만 사용할 수 있고 다른 세포와 공유되지 않는다.이는 간세포가 요구하면 저장한 글리코겐을 포도당으로 분해해 혈류를 통해 다른 장기의 연료로 보내는 것과 대조적이다.[25]
역사
글리코겐은 클로드 버나드에게 발견되었다.그의 실험은 간에서 "발효"의 작용으로 당분을 감소시킬 수 있는 물질을 간에서 함유하고 있다는 것을 보여주었다.1857년까지 그는 "라 마티에르 글리코겐" 또는 "설탕 형성 물질"이라고 불리는 물질의 격리를 묘사했다.간에서 글리코겐이 발견된 직후, A. 샌슨은 근육 조직에도 글리코겐이 들어 있다는 것을 발견했다.(CHO
6
10
5)n의 글리코겐에 대한 경험적 공식은 1858년 케쿨레에 의해 제정되었다.[26]
신진대사
합성
글리코겐 합성은 그것의 분해와 달리 내구성이다. 그것은 에너지의 투입을 필요로 한다.글리코겐 합성을 위한 에너지는 UTP(Uridine triphosphate, UTP)에서 나오는데, UTP는 글루코스-1-인산염(Glucose-1-phosphate uridylyltransferase)에 의해 촉매된 반응으로 UDP-글루코스를 형성한다.글리코겐은 글리코겐이 호모디머이기 때문에 글리코겐의 감소를 위해 두 개의 티로신 닻을 가진 단백질 글리코겐에 의해 초기에 UDP-글루코겐의 단량체로부터 합성된다.티로신 잔여물에 약 8개의 포도당 분자가 첨가된 후, 글리코겐 신타아제는 UDP-글루코스를 사용하여 글리코겐 체인을 점진적으로 연장하고, 글리코겐 체인의 비절감 끝에 α(1→4)-결합 포도당을 첨가한다.[27]
글리코겐 분자 효소는 6개 또는 7개 포도당 잔류물의 단자 조각이 비절감 끝에서 글리코겐 분자 내부로 더 깊이 포도당 잔류물의 C-6 히드록실 그룹으로 전달되도록 촉진한다.분지 효소는 최소 11개의 잔여물이 있는 가지에만 작용하며, 효소는 동일한 포도당 체인이나 인접한 포도당 체인으로 전달될 수 있다.
고장
글리코겐은 글리코겐인산화효소에 의해 사슬의 비절감 끝에서 분해되어 포도당-1인산염의 단모체를 생성한다.
체내에서는 인산염과 포도당-1-인산염의 비율이 대개 100보다 크기 때문에 인산염은 글리코겐 분해 방향으로 진행된다.[28]포도당-1 인산염은 인광글루코무타제에 의해 포도당 6 인산염(G6P)으로 변환된다.갈겨진 글리코겐에서 α(1-6) 가지를 제거하고 체인을 선형 중합체로 재편하기 위해서는 특수 괴사조직화 효소가 필요하다.생산된 G6P 모노머에는 세 가지 운명의 가능성이 있다.
- G6P는 당분해 경로에서 계속하여 연료로 사용될 수 있다.
- G6P는 효소 포도당-6-인산염 탈수소효소를 통해 펜토오스 인산염 경로로 진입해 NADPH와 5개의 탄소를 생성할 수 있다.
- 간이나 신장에서 G6P는 효소 포도당 6-인산염에 의해 다시 포도당으로 탈인화 될 수 있다.이것이 글루코네제네시스 경로의 마지막 단계다.
임상 관련성
글리코겐 대사 장애
글리코겐 신진대사가 비정상적으로 되는 가장 흔한 질환은 당뇨병으로, 이 경우 인슐린의 비정상적인 양 때문에 간 글리코겐이 비정상적으로 축적되거나 고갈될 수 있다.정상 포도당 신진대사의 회복은 글리코겐 신진대사를 정상화시킨다.
과도한 인슐린에 의한 저혈당증에서는 간 글리코겐 수치가 높지만 인슐린 수치가 높으면 정상 혈당 수치를 유지하는 데 필요한 글리코겐 분해를 예방한다.글루카곤은 이런 종류의 저혈당증의 흔한 치료법이다.
신진대사의 다양한 선천적 오류는 글리코겐 합성이나 분해에 필요한 효소의 결핍에 의해 발생한다.이를 총칭하여 글리코겐 저장성 질환이라고 한다.
글리코겐 고갈 및 지구력 운동
마라톤 선수, 크로스컨트리 스키어, 사이클 선수 등 장거리 선수들도 충분한 탄수화물 섭취 없이 오랜 시간 노력 끝에 거의 모든 선수 글리코겐 매장이 고갈되는 글리코겐 고갈을 경험하는 경우가 많다.이 현상을 "벽에 박는 것"이라고 한다.
글리코겐 고갈은 다음 세 가지 방법으로 방지될 수 있다.
- 첫째, 운동 중에는 혈당 전환율이 가장 높은 탄수화물을 지속적으로 섭취한다(혈당지수 높음).이 전략의 가능한 최선의 결과는 최대 80% 이상의 심장 박동수로 소비되는 포도당의 약 35%를 대체한다.
- 둘째, 지구력 훈련 적응법 및 특수 요법(예: 단식, 저강도 지구력 훈련)을 통해 인체는 I형 근육 섬유를 연료 사용 효율과 작업 부하 용량을 모두 개선하여 연료로 사용되는 지방산의 비율을 증가시켜 모든 공급원에서 탄수화물 사용을 절약할 수 있다.[29][30]
- 셋째, 운동이나 식이요법의 결과로 글리코겐 저장소를 고갈시킨 후 많은 양의 탄수화물을 섭취함으로써 인체는 근육내 글리코겐 저장소의 저장 용량을 증가시킬 수 있다.[31][32][33][34]이 과정은 탄수화물 부하로 알려져 있다.일반적으로 일시적인 글리코겐 고갈로 근육 인슐린 민감도가 높아지기 때문에 탄수화물 선원의 당혈지수는 문제가 되지 않는다.[35][36]
운동선수들이 철저한 운동 후에 탄수화물과 카페인을 모두 섭취할 때, 글리코겐 상점은 더 빨리 보충되는 경향이 있다.[37][38] 그러나 글리코겐 재충전에 임상적으로 유의미한 효과가 있는 카페인의 최소 복용량은 아직 확립되지 않았다.[38]
참고 항목
참조
- ^ McArdle, William D.; Katch, Frank I.; Katch, Victor L. (2006). Exercise physiology: Energy, nutrition, and human performance (6th ed.). Lippincott Williams & Wilkins. p. 12. ISBN 978-0-7817-4990-9.
- ^ Sadava, David E.; Purves, William K.; Hillis, David M.; Orians, Gordon H.; Heller, H. Craig (2011). Life (9th, International ed.). W. H. Freeman. ISBN 9781429254311.
- ^ a b c Berg JM, Tymoczko JL, Gatto GJ, Stryer L (8 April 2015). Biochemistry (Eighth ed.). New York: W. H. Freeman. ISBN 9781464126109. OCLC 913469736.
- ^ a b c d e f g h i Wasserman DH (January 2009). "Four grams of glucose". American Journal of Physiology. Endocrinology and Metabolism. 296 (1): E11–21. doi:10.1152/ajpendo.90563.2008. PMC 2636990. PMID 18840763.
Four grams of glucose circulates in the blood of a person weighing 70 kg. This glucose is critical for normal function in many cell types. In accordance with the importance of these 4 g of glucose, a sophisticated control system is in place to maintain blood glucose constant. Our focus has been on the mechanisms by which the flux of glucose from liver to blood and from blood to skeletal muscle is regulated. ... The brain consumes ~60% of the blood glucose used in the sedentary, fasted person. ... The amount of glucose in the blood is preserved at the expense of glycogen reservoirs (Fig. 2). In postabsorptive humans, there are ~100 g of glycogen in the liver and ~400 g of glycogen in muscle. Carbohydrate oxidation by the working muscle can go up by ~10 fold with exercise, and yet after 1 h, blood glucose is maintained at ~4 g.
- ^ a b Kreitzman SN, Coxon AY, Szaz KF (1992). "Glycogen storage: Illusions of easy weight loss, excessive weight regain, and distortions in estimates of body composition" (PDF). The American Journal of Clinical Nutrition. 56 (1, Suppl): 292s–293s. doi:10.1093/ajcn/56.1.292S. PMID 1615908.
- ^ Guyton, Arthur C.; Hall, John Edward (2011). Guyton and Hall Textbook of Medical Physiology. New York, New York: Saunders/Elsevier. ISBN 978-5-98657-013-6.
- ^ Bergström, Jonas; Hermansen, Lars; Hultman, Eric; Saltin, Bengt (1967). "Diet, Muscle Glycogen and Physical Performance". Acta Physiologica Scandinavica. 71 (2–3): 140–150. doi:10.1111/j.1748-1716.1967.tb03720.x. ISSN 1365-201X. PMID 5584523.
- ^ Jensen, Rasmus; Ørtenblad, Niels; Stausholm, Marie-Louise Holleufer; Skjærbæk, Mette Carina; Larsen, Daniel Nykvist; Hansen, Mette; Holmberg, Hans-Christer; Plomgaard, Peter; Nielsen, Joachim (2020). "Heterogeneity in subcellular muscle glycogen utilisation during exercise impacts endurance capacity in men". The Journal of Physiology. 598 (19): 4271–4292. doi:10.1113/JP280247. ISSN 1469-7793. PMID 32686845. S2CID 220653138.
- ^ Jensen, Rasmus; Ørtenblad, Niels; Stausholm, Marie-Louise H.; Skjærbæk, Mette C.; Larsen, Daniel N.; Hansen, Mette; Holmberg, Hans-Christer; Plomgaard, Peter; Nielsen, Joachim (May 2021). "Glycogen supercompensation is due to increased number, not size, of glycogen particles in human skeletal muscle". Experimental Physiology. 106 (5): 1272–1284. doi:10.1113/EP089317. ISSN 0958-0670. PMID 33675088. S2CID 232131416.
- ^ Jensen, Rasmus; Ørtenblad, Niels; Stausholm, Marie-Louise H.; Skjærbæk, Mette C.; Larsen, Daniel N.; Hansen, Mette; Holmberg, Hans-Christer; Plomgaard, Peter; Nielsen, Joachim (May 2021). "Glycogen supercompensation is due to increased number, not size, of glycogen particles in human skeletal muscle". Experimental Physiology. 106 (5): 1272–1284. doi:10.1113/EP089317. ISSN 0958-0670. PMID 33675088. S2CID 232131416.
- ^ Marchand, I.; Chorneyko, K.; Tarnopolsky, M.; Hamilton, S.; Shearer, J.; Potvin, J.; Graham, T. E. (1 November 2002). "Quantification of subcellular glycogen in resting human muscle: granule size, number, and location". Journal of Applied Physiology. 93 (5): 1598–1607. doi:10.1152/japplphysiol.00585.2001. ISSN 8750-7587. PMID 12381743.
- ^ Moses SW, Bashan N, Gutman A (December 1972). "Glycogen metabolism in the normal red blood cell". Blood. 40 (6): 836–843. doi:10.1182/blood.V40.6.836.836. PMID 5083874.
- ^ Ingermann RL, Virgin GL (1987). "Glycogen content and release of glucose from red blood cells of the sipunculan worm themiste dyscrita" (PDF). J Exp Biol. 129: 141–149. doi:10.1242/jeb.129.1.141.
- ^ Miwa I, Suzuki S (November 2002). "An improved quantitative assay of glycogen in erythrocytes". Annals of Clinical Biochemistry. 39 (Pt 6): 612–13. doi:10.1258/000456302760413432. PMID 12564847.
- ^ Murray, Bob (April 2018). "Fundamentals of glycogen metabolism for coaches and athletes". Nutrition Reviews. 76 (4): 243–259. doi:10.1093/nutrit/nuy001. PMC 6019055. PMID 29444266.
- ^ Oe Y, Baba O, Ashida H, Nakamura KC, Hirase H (June 2016). "Glycogen distribution in the microwave-fixed mouse brain reveals heterogeneous astrocytic patterns". Glia. 64 (9): 1532–1545. doi:10.1002/glia.23020. PMC 5094520. PMID 27353480.
- ^ Campbell, Neil A.; Williamson, Brad; Heyden, Robin J. (2006). Biology: Exploring Life. Boston, MA: Pearson Prentice Hall. ISBN 978-0-13-250882-7.
- ^ Ryley, J.F. (March 1955). "Studies on the metabolism of the protozoa. 5: Metabolism of the parasitic flagellate Trichomonas foetus". The Biochemical Journal. 59 (3): 361–369. doi:10.1042/bj0590361. PMC 1216250. PMID 14363101.
- ^ Benchimol, Marlene; Elias, Cezar Antonio; de Souza, Wanderley (December 1982). "Tritrichomonas foetus: Ultrastructural localization of calcium in the plasma membrane and in the hydrogenosome". Experimental Parasitology. 54 (3): 277–284. doi:10.1016/0014-4894(82)90036-4. ISSN 0014-4894. PMID 7151939.
- ^ Mielewczik, Michael; Mehlhorn, Heinz; al Quraishy, Saleh; Grabensteiner, E.; Hess, M. (1 September 2008). "Transmission electron microscopic studies of stages of histomonas meleagridis from clonal cultures". Parasitology Research. 103 (4): 745–750. doi:10.1007/s00436-008-1009-1. ISSN 0932-0113. PMID 18626664. S2CID 2331300.
- ^ Manners, David J. (1991). "Recent developments in our understanding of glycogen structure". Carbohydrate Polymers. 16 (1): 37–82. doi:10.1016/0144-8617(91)90071-J. ISSN 0144-8617.
- ^ Ronner, Peter (2018). Netter's Essentials Biochemistry. USA: Elsevier. p. 254. ISBN 978-1-929007-63-9.
- ^ Berg, Tymoczko, & Stryer (2012). Biochemistry (7th, International ed.). W. H. Freeman. p. 338. ISBN 978-1429203142.
{{cite book}}: CS1 maint: 작성자 매개변수 사용(링크) - ^ Berg; et al. (2012). Biochemistry (7th, International ed.). W. H. Freeman. p. 650.
- ^ "Glycogen Biosynthesis; Glycogen Breakdown". oregonstate.edu. Retrieved 28 February 2018.
- ^ Young, F.G. (22 June 1957). "Claude Bernard and the discovery of glycogen". British Medical Journal. 1 (5033): 1431–1437. doi:10.1136/bmj.1.5033.1431. JSTOR 25382898. PMC 1973429. PMID 13436813.
- ^ Nelson, D. (2013). Lehninger Principles of Biochemistry (6th ed.). W.H. Freeman and Company. p. 618.
- ^ Stryer, L. (1988). Biochemistry (3rd ed.). Freeman. p. 451.
- ^ "Methods of endurance training, Part 1". 30 October 2009.
- ^ "Steady state vs. tempo training and fat loss". 2 June 2008.
- ^ Jensen, Rasmus; Ørtenblad, Niels; Stausholm, Marie-Louise Holleufer; Skjærbæk, Mette Carina; Larsen, Daniel Nykvist; Hansen, Mette; Holmberg, Hans-Christer; Plomgaard, Peter; Nielsen, Joachim (2020). "Heterogeneity in subcellular muscle glycogen utilisation during exercise impacts endurance capacity in men". The Journal of Physiology. 598 (19): 4271–4292. doi:10.1113/JP280247. ISSN 1469-7793. PMID 32686845. S2CID 220653138.
- ^ McDonald, Lyle (25 July 2012). "Research review: An in-depth look into carbing up on the cyclical ketogenic diet". Retrieved 19 February 2017.
- ^ McDonald, Lyle (1998). The Ketogenic Diet: A complete guide for the dieter and the practitioner. Lyle McDonald.
- ^ Costill DL, Bowers R, Branam G, Sparks K (December 1971). "Muscle glycogen utilization during prolonged exercise on successive days". J Appl Physiol. 31 (6): 834–838. doi:10.1152/jappl.1971.31.6.834. PMID 5123660.
- ^ Zorzano A, Balon TW, Goodman MN, Ruderman NB (December 1986). "Glycogen depletion and increased insulin sensitivity and responsiveness in muscle after exercise". Am. J. Physiol. 251 (6, Part 1): E664–E669. doi:10.1152/ajpendo.1986.251.6.E664. PMID 3538900.
- ^ McDonald, Lyle (2003). The Ultimate Diet 2.0. Lyle McDonald.
- ^ Pedersen, D.J.; Lessard, S.J.; Coffey, V.G.; et al. (July 2008). "High rates of muscle glycogen resynthesis after exhaustive exercise when carbohydrate is coingested with caffeine". Journal of Applied Physiology. 105 (1): 7–13. doi:10.1152/japplphysiol.01121.2007. PMID 18467543.
- ^ a b Beelen, M.; Burke, L.M.; Gibala, M.J.; van Loon, L.J.C. (December 2010). "Nutritional strategies to promote post-exercise recovery". International Journal of Sport Nutrition and Exercise Metabolism. 20 (6): 515–532. doi:10.1123/ijsnem.20.6.515. PMID 21116024. S2CID 13748227.
외부 링크
| 위키미디어 커먼즈에는 글리코겐과 관련된 미디어가 있다. |
- "Glycogen storage disease". McArdle's Diseases.
- 미국 국립 의학 도서관 글리코겐(MesH) 제목