리보오스
Ribose
| | |||
| | |||
| 이름 | |||
|---|---|---|---|
| IUPAC 이름 (2R,3R,4S,5R)-5-(히드록시메틸)옥솔란-2,3,4-트리올 | |||
| 기타 이름 d-리보스 | |||
| 식별자 | |||
3D 모델(JSmol) |
| ||
| 첸블 | |||
| 켐스파이더 |
| ||
| 드러그뱅크 | |||
| EC 번호 |
| ||
PubChem CID | |||
| 유니 | |||
| |||
| |||
| 속성[1][2] | |||
| C5H10O5 | |||
| 몰 질량 | 150.13 | ||
| 외모 | 흰색 솔리드 | ||
| 녹는점 | 95 °C (203 °F, 368 K) | ||
| 100g/L(25°C, 77°F) | |||
키랄 회전([α])D | -21.5°(HO2) | ||
| 관련 화합물 | |||
관련 알도펜토스 | 아라비노스 자일로스 리소스 | ||
관련 화합물 | 디옥시리보스 | ||
달리 명시되지 않은 한 표준 상태(25°C[77°F], 100kPa)의 재료에 대한 데이터가 제공됩니다. | |||
리보스는 분자식이5105 CHO이고 선형 조성이 H-(C=O)-(CHOH)-4H인 단당 및 탄수화물이다.자연적으로 발생하는 형태인 d-리보스는 RNA가 만들어지는 리보뉴클레오티드의 구성요소이며, 따라서 이 화합물은 유전자의 부호화, 해독, 조절 및 발현에 필요하다.디옥시리보스는 DNA의 유사한 필수 성분이다.[3] l-리보스는 에밀 피셔와 오스카 필로티에 의해 1891년에 처음 제조된 부자연스러운 설탕이다.1909년이 되어서야 피버스 레베네와 월터 제이콥스는 d-리보스가 천연물이며 피셔와 필로티 제품의 에난티오머이며 핵산의 [4][5][6]필수 성분이라는 것을 알게 되었다.피셔는 "리보스"라는 이름을 선택했는데, 이는 리보스가 2' 탄소의 에피머인 또 다른 당인 아라비노스의 이름의 부분적인 재배열이기 때문입니다; 두 이름 모두 아라비노스가 처음 분리되었고 그들이 리보스를 [6][7]준비했던 아라비아 고무와도 관련이 있습니다.
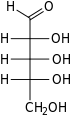
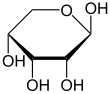
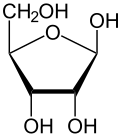
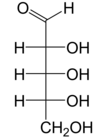
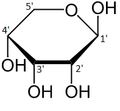
대부분의 설탕과 마찬가지로 리보스는 선형 형태와 평형 상태에서 순환 형태의 혼합물로 존재하며, 이것들은 특히 [8]수용액에서 쉽게 상호 변환됩니다."리보스"라는 이름은 생화학 및 생물학에서 이러한 모든 형태를 지칭하기 위해 사용되지만, 필요할 때 각각에 대한 더 구체적인 이름이 사용됩니다.그것의 선형 형식에, ribose는 피셔 투영식에서 같은 면에 대한 수산화 기능적인 그룹의 펜토오스 설탕처럼. d-Ribose과(2R,3R,4R)[9]는 동안 l-ribose은 수산화 그룹에 나타나고 있는 체계적인 이름과 관련된 오른쪽에 이러한 수산화들을 인식할 수 있다. t피셔 투영법에서 왼손을 잡았어요리보스의 환화는 C4' 하이드록실기의 알데히드 공격에 의한 헤미아세탈 형성을 통해 일어나 푸라노스 형태를 생성하거나 C5' 하이드록실기를 통해 피라노스 형태를 생성한다.각각의 경우, 헤미아세탈 탄소 원자('아노머 탄소')의 입체 화학에 따라 α와 β-로 명명되고 아노머로 알려진 두 가지 기하학적 결과가 있을 수 있다.실온에서 d-리보스의 약 76%는 피라노스[8]: 228 형태(α:β = 1:[10]2)로, 24%는 플루노스 형태[8]: 228 (α:β = 1:3)[10]로 존재하며,[11][12] 선형 형태의 약 0.1%만이 존재한다.
리보뉴클레오시드 아데노신, 시티딘, 구아노신 및 우리딘은 모두 β-d-리보퓨라노스의 유도체이다.인산화 리보스를 포함하는 대사적으로 중요한 종에는 ADP, ATP, 조효소 [8]: 228–229 A 및 NADH가 포함된다. cAMP와 cGMP는 일부 신호 경로에서 2차 전달자로 작용하며 리보스 유도체이기도 하다.리보스 부분은 항생제인 네오마이신과 파로마이신을 [10]포함한 일부 의약품에서 나타난다.
합성 및 소스
5-인산 에스테르로서의 리보스는 일반적으로 펜토오스 인산 경로를 통해 포도당으로부터 생성된다.적어도 일부 고고학에서는 대체 경로가 확인되었다.[13]
리보스는 화학적으로 합성될 수 있지만, 상업적인 생산은 포도당의 발효에 의존한다.유전자 변형 B. subtilis 균주를 사용하여 200g의 포도당으로부터 90g/l의 리보스를 생성할 수 있습니다.이 변환은 글루콘산염과 [14]리불로오스의 중간을 수반한다.
구조.
리보스는 열린 사슬 형태로 한쪽 끝에 알데히드 관능기를 가진 알도펜토스(탄소 원자 5개를 포함하는 단당류)이다.기존의 단당류 번호부여 방식에서 탄소원자는 C1'(알데히드기 중)에서 C5'까지 번호가 매겨진다.DNA에서 발견되는 디옥시리보스 유도체는 C2'에서 수산기 대신 수소 원자를 갖는 것으로 리보스와 다르다.이 히드록실기는 RNA 스플라이싱에서 기능을 수행합니다.
d-리보스라는 이름의 "d-"는 알데히드기(C4')에서 가장 멀리 떨어진 키랄 탄소 원자의 입체 화학을 의미한다.모든 d-설탕과 마찬가지로 d-리보스에서 이 탄소원자는 d-글리세랄알데히드와 동일한 구성을 가진다.
용액 중 리보오스 형태의 상대적 풍부도는 β-d-리보피라노스(59%), α-d-리보피라노스(20%), β-d-리보피라노스(13%), α-d-리보피라노스(7%), 개방사슬(0.1%)[11]이다.
뉴클레오시드와 뉴클레오티드의 리보오스 잔기에 대해서는 결합을 포함하는 회전에 대한 비틀림 각도가 각각의 뉴클레오시드와 뉴클레오티드의 구성에 영향을 준다.핵산의 2차 구조는 7개의 비틀림 [17]각도의 회전에 의해 결정됩니다.비틀림 각도가 크면 유연성이 높아집니다.
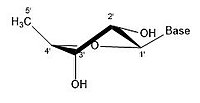
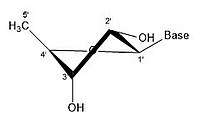
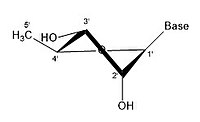
닫힌 링 리보이스에서는 링 사이클이 [17]구조에서 가능한 비틀림 각도의 수에 제한을 가하기 때문에 위에서 언급한 관측된 유연성은 관찰되지 않는다.폐쇄형 리보스의 컨포머는 분자 내의 외로운 산소가 리보스에 부착된 질소 염기(핵염기 또는 단지 염기라고도 함)에 대해 각각 어떻게 위치하는지에 대해 다르다.카본이 베이스 쪽을 향하고 있는 경우는, 리보스는 엔도라고 하는 라벨이 붙어 있습니다.만약 탄소가 베이스에서 떨어져 있다면, 리보스는 엑소라고 라벨이 붙여집니다.폐쇄 사이클 리보스의 2' 탄소에 산소 분자가 붙어 있으면 산소와 [17]염기의 상호작용을 감소시키기 때문에 엑소 확인이 더 안정적입니다.차이 자체는 매우 작지만, RNA의 전체 사슬을 볼 때 약간의 차이는 상당한 영향을 미칩니다.
- 리보스의 일부 퍼커 구성
리보오스 분자는 전형적으로 종이 위에 평면 분자로 표현된다.그럼에도 불구하고, 그것은 전형적으로 평면이 아니다.수소 원자 사이에서도, 리보오스 분자상의 많은 성분들은 스테릭 장애와 긴장감을 일으킨다.이러한 혼잡과 링 변형을 완화하기 위해 링 퍽(즉,[18] 비평면)이 퍼커링은 평면에서 원자를 변위시켜 왜곡을 완화시키고 보다 안정적인 [17]구성을 생성함으로써 달성됩니다.당환 형태(특히 리보스 설탕)로 알려진 퍽킹은 퍼커의 진폭과 의사 회전 각도로 설명할 수 있습니다.의사 회전 각도는 "북(N)" 또는 "남(S)" 범위로 설명할 수 있습니다.두 범위 모두 이중 나선형으로 발견되는 반면, 북쪽 범위는 일반적으로 RNA와 A 형태의 DNA와 관련이 있습니다.대조적으로, 남쪽 범위는 B 형태의 DNA와 연관되어 있다. Z-DNA는 북쪽과 남쪽 [19]범위에 모두 당을 포함하고 있다.단 하나의 원자만 변위하는 경우, 그것은 "봉투" 퍼커라고 불립니다.두 원자가 변위할 때, 지그재그 [20]방향과 관련하여, 그것은 "트위스트" 퍼커라고 불립니다."내부" 퍼커에서 원자의 주요 변위는 C4'-C5' 결합 및 베이스와 같은 면인 β면에 있다."exo" pucker에서 원자의 주요 변위는 고리의 반대편인 α 면에 있습니다.리보스의 주요 형태는 3'-엔도 퍼커(RNA와 A형 DNA에 의해 일반적으로 채택됨)와 2'-엔도 퍼커(B형 [21]DNA에 의해 일반적으로 채택됨)이다.이러한 링 퍼커는 링 비틀림 각도의 변화로부터 개발됩니다. 각도의 무한한 조합이 있기 때문에 각각 다른 활성화 에너지에 의해 분리된 트랜스포저블 퍼커 구성이 무한히 존재합니다.
기능들
ATP는 리보오스로부터 유도되며, 리보오스 1개, 인산기 3개, 아데닌 염기 1개를 포함한다.ATP는 아데노신 이인산(인산기가 하나 적은 ATP)으로부터 세포 호흡 중에 생성된다.
시그널링 패스
리보스는 ATP에서 파생된 고리형 아데노신 일인산(cAMP)과 같은 2차 신호 분자의 구성 요소이다.cAMP가 사용되는 구체적인 경우는 cAMP 의존 시그널링 경로입니다.cAMP 시그널링 경로에서 자극 호르몬 수용체 또는 억제 호르몬 수용체는 신호 분자에 의해 활성화된다.이러한 수용체는 자극적 또는 억제적 조절 G단백질과 연결되어 있다.자극적인 G-단백질이 활성화되면 아데닐릴 사이클라아제는 Mg2+ 또는 2차 전달자인 Mn. cAMP를2+ 사용하여 ATP를 cAMP로 촉매한 다음 세포 대사를 조절하는 효소인 단백질 키나제 A를 활성화시킵니다.단백질인산화효소A는 원래 신호분자에 따라 세포의 변화를 일으키는 인산화로 대사효소를 조절한다.억제성 G단백질이 활성화되면 그 반대 현상이 발생하는데, G단백질은 아데닐환원효소를 억제하고 ATP는 cAMP로 변환되지 않는다.
대사
리보스는 세포 내 에너지 [citation needed]전달에 관여하기 때문에 "분자 통화"라고 불립니다.예를 들어 니코틴아미드아데닌디뉴클레오티드(NAD), 플라빈아데닌디뉴클레오티드(FAD) 및 니코틴아미드아데닌디뉴클레오티드인산(NADP)은 모두 d-리보푸라노스 부분을 포함한다.리보키나아제 [22][23]효소에 의해 d-리보오스 5-인산으로 전환된 후 각각 d-리보오스로부터 유도될 수 있다.NAD, FAD 및 NADP는 해당과정, 구연산 회로, 발효 및 전자전달 사슬을 포함한 주요 대사 경로에서 생화학적 산화환원 반응에서 전자수용체 역할을 한다.
뉴클레오티드생합성
뉴클레오티드는 회수 또는 탈노보 [24]합성을 통해 합성된다.뉴클레오티드 인양은 이전에 만들어진 뉴클레오티드의 조각들을 사용하고 미래에 사용하기 위해 그것들을 재합성한다.데노보에서는 아미노산,[24] 이산화탄소, 엽산유도체 및 포스포리보실피로인산(PRPP)을 사용하여 뉴클레오티드를 합성한다.de novo와 survage 모두 PRPP [24]합성효소라고 불리는 효소에 의해 ATP와 리보오스 5-인산으로부터 합성되는 PRPP를 필요로 한다.
변경 사항
본성의 변경
리보키나아제는 d-리보스의 d-리보오스 5-인산으로의 전환을 촉매한다.변환 후 d-리보스-5-인산은 아미노산 트립토판 및 히스티딘의 제조 또는 펜토스 인산 경로에서 사용할 수 있다.d-리보스의 흡수는 소장에서 88~100%이다(최대 200mg/kg/h).[25]
리보오스 분자의 C2' 위치에서 한 가지 중요한 변형이 일어난다.O-알킬기를 첨가함으로써 추가적인 안정화력에 의해 RNA의 핵저항을 증가시킨다.이러한 힘은 분자 내 수소 결합의 증가와 글리코사이드 결합의 [26]안정성 증가로 인해 안정화되고 있습니다.그 결과 저항성의 증가는 세포와 [27]동물에서 siRNA의 반감기와 잠재적 치료 잠재력 증가로 이어진다.특정 부위에서의 리보스의 메틸화는 면역 [28]자극의 감소와 관련이 있다.
합성 수정
인산화와 함께, 리보푸라노스 분자는 4' 위치에서만 변화하는 유사한 당을 생성하기 위해 셀레늄과 유황과 산소를 교환할 수 있습니다.이 유도체들은 원래 분자보다 더 친유성이 있다.친유성이 높아짐에 따라 PCR, RNA 압타머 사후 수정, 안티센스 기술 및 X선 결정학 데이터의 [27]단계화와 같은 기술에 사용하기에 더 적합합니다.
2'의 성질과 마찬가지로 리보스의 합성 개조는 2' 위치에 불소를 첨가하는 것을 포함한다.이 불소화 리보스는 DNA [26]가닥에서 리보스의 위치에 따라 면역 자극을 억제할 수 있기 때문에 메틸화 리보스와 유사하게 작용합니다.메틸화와 불소의 가장 큰 차이는 후자가 합성 변형을 통해서만 발생한다는 것이다.불소의 첨가는 글리코시드 결합의 안정화와 분자 내 [26]수소 결합의 증가로 이어진다.
의료 용도
d-리보스는 울혈성 심부전[29] 관리와 만성피로증후군(CFS)에 사용할 것을 제안받았습니다. 만성피로증후군은 개방 라벨 비시각, 비랜덤화 및 비크로스 주관적 [30]연구에서 골수성 뇌척수염(ME)이라고도 합니다.
보충적 d-리보스는 에너지 생산 경로인 펜토오스 인산 경로의 일부를 우회하여 d-리보스-5-인산을 생성할 수 있다.포도당-6-인산탈수소효소(G-6-PDH)는 세포에서 종종 부족하지만 심장병 환자의 심근 세포와 같은 질병 조직에서는 더 많다.미토콘드리아에서 d-리보스의 공급은 ATP 생산과 직접적으로 관련이 있다; d-리보스의 공급 감소는 ATP 생산량을 감소시킨다.연구에 따르면 d-리보스를 조직 허혈(예: 심근 허혈)에 이어 보충하면 심근 ATP 생산이 증가하여 미토콘드리아 기능이 향상된다.본질적으로 보충적 d-리보스를 투여하는 것은 ATP 생산을 위한 5-포스포-d-리보스 1-피로인산염 대체원을 제공함으로써 펜토스 인산 경로의 효소 단계를 우회한다.보충적인 d-리보스는 사람과 다른 동물들의 세포 손상을 줄이면서 ATP 수치의 회복을 강화합니다.한 연구는 보조적인 d-리보스의 사용이 진단된 [31]관상동맥질환을 가진 남성들에게 협심증의 발생을 감소시킨다고 제안했다. d-리보스는 만성피로증후군, 섬유근육통, 그리고 심근기능장애와 같은 많은 병리학적 질환들을 치료하는데 사용되어 왔다.운동 후 경련, 통증, 뻣뻣함 등의 증상을 줄이고 운동 능력을[citation needed] 향상시키는 데도 사용된다.
레퍼런스
- ^ The Merck Index: An Encyclopedia of Chemicals, Drugs, and Biologicals (11th ed.), Merck, 1989, ISBN 091191028X, 8205
- ^ Weast, Robert C., ed. (1981). CRC Handbook of Chemistry and Physics (62nd ed.). Boca Raton, FL: CRC Press. p. C-506. ISBN 0-8493-0462-8.
- ^ Fischer, Emil; Piloty, Oscar (1891). "Ueber eine neue Pentonsäure und die zweite inactive Trioxyglutarsäure" [About a new pentonic acid and the second inactive trioxyglutaric acid]. Berichte der deutschen chemischen Gesellschaft (in German). 24 (2): 4214–4225. doi:10.1002/cber.189102402322.
- ^ Levene, P. A.; Jacobs, W. A. (1909). "Über Inosinsäure" [About inosic acid]. Berichte der deutschen chemischen Gesellschaft (in German). 42 (1): 1198–1203. doi:10.1002/cber.190904201196.
- ^ Levene, P. A.; Jacobs, W. A. (1909). "Über die Pentose in den Nucleinsäuren" [About the pentose in the nucleic acids]. Berichte der deutschen chemischen Gesellschaft (in German). 42 (3): 3247–3251. doi:10.1002/cber.19090420351.
- ^ a b Jeanloz, Roger W.; Fletcher, Hewitt G. (1951). "The Chemistry of Ribose". In Hudson, Claude S.; Cantor, Sidney M. (eds.). Advances in Carbohydrate Chemistry. Vol. 6. Academic Press. pp. 135–174. doi:10.1016/S0096-5332(08)60066-1. ISBN 9780080562650. PMID 14894350.
- ^ Nechamkin, Howard (1958). "Some interesting etymological derivations of chemical terminology". Science Education. 42 (5): 463–474. Bibcode:1958SciEd..42..463N. doi:10.1002/sce.3730420523.
- ^ a b c d Dewick, Paul M. (2013). "Oxygen as a Nucleophile: Hemicetals, Hemiketals, Acetals and Ketals". Essentials of Organic Chemistry: For Students of Pharmacy, Medicinal Chemistry and Biological Chemistry. John Wiley & Sons. pp. 224–234. ISBN 9781118681961.
- ^ Leigh, Jeffery (July–August 2012). "Non-IUPAC Nomenclature Systems". Chemistry International. International Union of Pure and Applied Chemistry. 34 (4). Retrieved 15 December 2019.
- ^ a b c Bhutani, S. P. (2019). "Aldopentoses—The Sugars of Nucleic Acids". Chemistry of Biomolecules (2nd ed.). CRC Press. pp. 63–65. ISBN 9781000650907.
- ^ a b Drew, Kenneth N.; Zajicek, Jaroslav; Bondo, Gail; Bose, Bidisha; Serianni, Anthony S. (February 1998). "13C-labeled aldopentoses: detection and quantitation of cyclic and acyclic forms by heteronuclear 1D and 2D NMR spectroscopy". Carbohydrate Research. 307 (3–4): 199–209. doi:10.1016/S0008-6215(98)00040-8.
- ^ de Wulf, P.; Vandamme, E. J. (1997). "Microbial Synthesis of ᴅ-Ribose: Metabolic Deregulation and Fermentation Process". Advances in Applied Microbiology. 44: 167–214. doi:10.1016/S0065-2164(08)70462-3. ISBN 9780120026449.
- ^ Tumbula, D. L.; Teng, Q.; Bartlett, M. G.; Whitman, W. B. (1997). "Ribose biosynthesis and evidence for an alternative first step in the common aromatic amino acid pathway in Methanococcus maripaludis". Journal of Bacteriology. 179 (19): 6010–6013. doi:10.1128/jb.179.19.6010-6013.1997. PMC 179501. PMID 9324245.
- ^ Wulf, P. De; Vandamme, E. J. (1997). "Production of d -ribose by fermentation". Applied Microbiology and Biotechnology. 48 (2): 141–148. doi:10.1007/s002530051029. PMID 9299771. S2CID 34340369.
- ^ Steigerwald, Bill; Jones, Nancy; Furukawa, Yoshihiro (18 November 2019). "First Detection of Sugars in Meteorites Gives Clues to Origin of Life". NASA. Retrieved 18 November 2019.
- ^ Furukawa, Yoshihiro; Chikaraishi, Yoshito; Ohkouchi, Naohiko; Ogawa, Nanako O.; Glavin, Daniel P.; Dworkin, Jason P.; Abe, Chiaki; Nakamura, Tomoki (2019). "Extraterrestrial ribose and other sugars in primitive meteorites". Proceedings of the National Academy of Sciences of the United States of America. 116 (49): 24440–24445. Bibcode:2019PNAS..11624440F. doi:10.1073/pnas.1907169116. PMC 6900709. PMID 31740594.
- ^ a b c d Bloomfield, Victor; Crothers, Donald; Tinoco, Ignacio (2000). Nucleic Acids: Structures, Properties, and Functions. University Science Books. pp. 19–25. ISBN 9780935702491.
- ^ Voet, Donald; Voet, Judith (2011). Biochemistry. John Wiley & Sons, Inc. pp. 1152, 1153. ISBN 978-0470570951.
- ^ Foloppe, Nicolas; MacKerell, Alexander D. (August 1998). "Conformational Properties of the Deoxyribose and Ribose Moieties of Nucleic Acids: A Quantum Mechanical Study". The Journal of Physical Chemistry B. 102 (34): 6669–6678. doi:10.1021/jp9818683. ISSN 1520-6106.
- ^ "Nucleic acid architecture". fbio.uh.cu. Retrieved 8 October 2019.
- ^ Neidle, Stephen (2008). "The Building-Blocks of DNA and RNA". In Neidle, Stephen (ed.). Principles of Nucleic Acid Structure. Academic Press. pp. 20–37. doi:10.1016/B978-012369507-9.50003-0. ISBN 9780123695079.
- ^ Bork, Peer; Sander, Chris; Valencia, Alfonso (1993). "Convergent evolution of similar enzymatic function on different protein folds: The hexokinase, ribokinase, and galactokinase families of sugar kinases". Protein Science. 2 (1): 31–40. doi:10.1002/pro.5560020104. PMC 2142297. PMID 8382990.
- ^ Park, Jae; Gupta, Radhey S. (2008). "Adenosine kinase and ribokinase – the RK family of proteins". Cellular and Molecular Life Sciences. 65 (18): 2875–2896. doi:10.1007/s00018-008-8123-1. PMID 18560757. S2CID 11439854.
- ^ a b c Puigserver, Pere (2018). "Signaling Transduction and Metabolomics". In Hoffman, Ronald; Benz, Edward J.; Silberstein, Leslie E.; Heslop, Helen E. (eds.). Hematology (7th ed.). Elsevier. pp. 68–78. doi:10.1016/B978-0-323-35762-3.00007-X. ISBN 9780323357623.
- ^ "Herbal Remedies, Supplements A-Z Index". PDRHealth.com. PDR, LLC. Archived from the original on 11 October 2008.
- ^ a b c Hamlow, Lucas; He, Chenchen; Fan, Lin; Wu, Ranran; Yang, Bo; Rodgers, M. T.; Berden, Giel; Oomens, J. (June 2015). Structual [sic] Effects of Cytidine 2'-Ribose Modifications as Determined by Irmpd Action Spectroscopy. 70th International Symposium on Molecular Spectroscopy. University of Illinois Urbana-Champaign. Bibcode:2015isms.confEMI13H. doi:10.15278/isms.2015.MI13.
- ^ a b Evich, Marina; Spring-Connell, Alexander M.; Germann, Markus W. (27 January 2017). "Impact of modified ribose sugars on nucleic acid conformation and function". Heterocyclic Communications. 23 (3): 155–165. doi:10.1515/hc-2017-0056. ISSN 2191-0197. S2CID 91052034.
- ^ Peacock, Hayden; Fucini, Raymond V.; Jayalath, Prasanna; Ibarra-Soza, José M.; Haringsma, Henry J.; Flanagan, W. Michael; Willingham, Aarron; Beal, Peter A. (2011). "Nucleobase and Ribose Modifications Control Immunostimulation by a MicroRNA-122-mimetic RNA". Journal of the American Chemical Society. 133 (24): 9200–9203. doi:10.1021/ja202492e. PMC 3116021. PMID 21612237.
- ^ Omran, Heyder; McCarter, Dean; St Cyr, John; Lüderitz, Berndt (2004). "ᴅ-Ribose aids congestive heart failure patients". Experimental & Clinical Cardiology. Summer (9(2)): 117–118. PMC 2716264. PMID 19641697.
- ^ Teitelbaum, Jacob E.; Johnson, Clarence; St Cyr, John (26 November 2006). "The use of ᴅ-ribose in chronic fatigue syndrome and fibromyalgia: a pilot study". The Journal of Alternative and Complementary Medicine. 12 (9): 857–862. CiteSeerX 10.1.1.582.4800. doi:10.1089/acm.2006.12.857. PMID 17109576.
- ^ "Ribose". wa.kaiserpermanente.org. Retrieved 7 October 2019.