크론병
Crohn's disease| 크론병 | |
|---|---|
| 기타이름 | 크론병, 크론증후군, 육아종성 장염, 국소 장염, 레 ś스키-크론병 |
 | |
| 궤양성 대장염의 영향을 받는 부위(대장염 궤양, 우측)에 비해 크론병의 장 침범이 가장 흔한 3개 부위(좌측) | |
| 전문 | 소화기내과 |
| 증상 | 복통, 설사(피가 날 수 있음), 발열, 체중감소,[1] 피로감, 입덧, 식욕감소[2] |
| 합병증 | 빈혈, 피부발진, 관절염, 장암[1] |
| 보통발병 | 20~30개[3] |
| 지속 | 장기[1] |
| 위험요소 | 담배 흡연[4] |
| 진단방법 | 조직검사, 의료영상검사[1] |
| 감별진단 | 과민성 장증후군, 셀리악병, 베체트병, 비스테로이드성 소염제 장병증, 장결핵[1][5] |
| 약 | 코르티코스테로이드, 생물학적 치료, 아자티오프린과 같은 면역억제제[1], 메토트렉세이트 |
| 예후 | 사망[6] 위험이 약간 증가함 |
| 빈도수. | 1,000명당 3.2명(선진국)[7] |
| 이름은 다음과 같습니다. | |
크론병은 위장관의 어떤 부분에도 영향을 미칠 수 있는 염증성 장질환의 한 종류입니다.[3] 증상으로는 복통, 설사, 발열, 복부 팽만감, 체중 감소 등이 종종 발생합니다.[1][3] 위장관 밖의 합병증으로는 빈혈, 피부 발진, 관절염, 눈의 염증, 피로감 등이 있을 수 있습니다.[1] 피부 발진은 농피증이나 홍반 노도섬 뿐만 아니라 감염 때문일 수도 있습니다.[1] 장폐색은 만성 염증의 합병증으로 발생할 수 있으며, 해당 질환이 있는 사람은 대장암과 소장암의 위험이 더 큽니다.[1]
크론병(CD)의 정확한 원인은 알려지지 않았지만 유전적으로 취약한 개인의 환경, 면역, 박테리아 요인이 복합적으로 작용하여 발생하는 것으로 추정됩니다.[3][8][9][10] 이로 인해 인체의 면역 체계가 위장관을 방어하는 만성 염증성 질환이 발생하여 미생물 항원을 표적으로 삼을 가능성이 있습니다.[9][11] 크론병은 면역과 관련된 질환이지만 자가면역질환은 아닌 것으로 보입니다.[12] 정확한 기저 면역 문제는 명확하지 않지만 면역 결핍 상태일 수 있습니다.[11][13][14]
전체 위험의 절반 정도는 유전자와 관련이 있으며, 70개 이상의 유전자가 관련되어 있습니다.[1][15] 담배를 피우는 사람들은 비흡연자들에 비해 크론병에 걸릴 확률이 3배나 높습니다.[4] 위장염 이후에 시작되는 경우가 많습니다.[1] 비슷한 증상을 보이는 다른 질환으로는 과민성 장증후군, 베체트병 등이 있습니다.[1]
크론병에 대한 알려진 치료법은 없습니다.[1][3] 치료 옵션은 증상을 돕고 관해를 유지하며 재발을 방지하기 위한 것입니다.[1] 새로 진단된 환자의 경우 증상을 빠르게 개선하기 위해 짧은 기간 동안 코르티코스테로이드를 사용할 수 있으며, 재발을 방지하기 위해 메토트렉세이트나 티오푸린과 같은 다른 약물을 사용할 수 있습니다.[1] 크론병을 앓고 있는 사람들에게는 금연이 권장됩니다.[1] 매년 이 병에 걸린 사람 5명 중 1명이 병원에 입원하고 있으며, 이 병에 걸린 사람의 절반은 10년 이상의 기간 동안 어느 시점에서 수술을 받아야 합니다.[1] 수술은 가능한 한 적게 사용해야 하지만 일부 농양, 특정 장폐색, 암을 해결해야 합니다.[1] 대장 내시경 검사를 통해 장암 여부를 확인하는 것은 질병이 시작된 지 8년 후부터 시작하는 것이 좋습니다.[1]
크론병은 유럽과 북미에서 인구 1,000명당 약 3.2명에게 영향을 미치며 아시아와 아프리카에서는 덜 흔합니다.[7][16][17] 역사적으로 선진국에서 더 흔했습니다.[18] 그러나 1970년대 이후 특히 개발도상국에서 비율이 증가하고 있습니다.[17][18] 염증성 장질환으로 2015년에 47,400명이 사망했고 [19]크론병 환자들은 기대수명이 조금 줄었습니다.[1] 어느 연령에서나 발생할 수 있지만 청소년기와 젊은 성인기에 시작되는 경향이 있습니다.[20][1][3][21] 수컷과 암컷은 똑같이 영향을 받습니다.[3]
이름논란
이 질병의 이름은 1932년 레온 긴즈버그(Leon Ginzubz, 1898-1988), 고든 D와 함께 소화기내과 의사 버릴 버나드 크론(Burrill Bernard Cron)의 이름을 따서 지어졌습니다. 뉴욕 마운트 사이나이 병원의 오펜하이머(1900~1974)는 소장 말단 회장에 염증이 있는 일련의 환자들에 대해 설명했는데, 이는 질병의 가장 일반적인 영향을 받는 부위입니다.[22] 이 병의 이름이 크론의 이름을 따서 지어진 이유에 대해서는 논란이 있습니다.[23][24] 크론이 그의 회고록에서 그 병에 대한 그의 최초의 조사를 설명하는 반면, 긴츠부르크는 어떻게 그와 오펜하이머가 그 병을 처음으로 연구했는지에 대한 강력한 증거를 제공했습니다.[25]
징후 및 증상
| 크론병 | 궤양성 대장염 | |
|---|---|---|
| 배변 | 죽 같은 경우가 종종 있는데,[26] 때때로 지방질 | 점액질 같은 경우가 많습니다. 피를[26] 흘리며 |
| 테네스무스 | 일반적이지[26] 않음 | 더 일반적인[26] |
| 열. | 공통[26] | 중증을[26] 나타냅니다. |
| 피스툴래 | 공통[27] | 드물게 |
| 체중감량 | 자주 | 더 드물게 |
위장

크론병에 걸린 많은 사람들은 진단 전 수년간 증상이 있습니다.[28] 일반적인 발병 시기는 10대와 20대이지만 어느 연령대에서나 발생할 수 있습니다.[21][1] 위장관 질환의 '패치'한 특성과 조직 침범 깊이 때문에 궤양성 대장염보다 초기 증상이 더 미묘할 수 있습니다. 크론병을 앓고 있는 사람들은 만성적으로 반복되는 발작과 관해를 경험합니다.[29] 경험하는 증상은 염증이 증가하고 확산됨에 따라 시간이 지남에 따라 변화할 수 있습니다. 어떤 장기가 관련되느냐에 따라 증상도 달라질 수 있습니다. 일반적으로 크론병의 발현은 증상의 변동성, 장기 침범, 초기 발현 등이 높아 환자마다 다른 것으로 생각됩니다.
페리아날
항문주위 불편감은 크론병에서도 두드러질 수 있습니다. 항문 주위의 가려움증이나 통증은 항문의 염증을 암시하거나 항문 주위의 치루, 누공 또는 농양과 같은 항문 주위의 합병증을 시사할 수 있습니다.[1] 항문주위 피부 태그는 크론병에서도 흔하며, 대장 용종의 유무와 상관없이 나타날 수 있습니다.[30] 변실금은 항문주위 크론병에 동반될 수 있습니다.
창자
장, 특히 대장과 말단 회장은 신체에서 가장 흔하게 영향을 받는 부위입니다. 복통은 [3]크론병의 흔한 초기 증상으로, 특히 우하복부에 발생합니다.[31] 편평, 팽만감, 복부 팽만감은 부가적인 증상이며 장의 불편함을 가중시킬 수도 있습니다. 통증은 종종 피가 날 수도 있고 아닐 수도 있는 설사를 동반합니다. 장관의 여러 부위에 염증이 생기면 대변의 질에 영향을 줄 수 있습니다. 장염은 일반적으로 다량의 수분이 있는 대변을 초래하는 반면 대장염은 더 높은 빈도의 적은 양의 대변을 초래할 수 있습니다. 대변의 농도는 고체에서 수분까지 다양할 수 있습니다. 심할 경우 개인은 하루에 20개 이상의 배변이 있을 수 있으며, 배변을 위해 밤에 깨어 있어야 할 수도 있습니다.[1][32][33][34] 대변에서 보이는 출혈은 궤양성 대장염보다 크론병에서 덜 흔하지만 특이한 것은 아닙니다.[1] 혈변은 대개 간헐적으로 나타나며, 밝은 빨간색, 어두운 색, 심지어 검은색일 수도 있습니다. 혈변의 색깔은 출혈 위치에 따라 다릅니다. 크론 대장염이 심할 경우 출혈이 심할 수 있습니다.[32]
위와 식도
위는 CD의 유일하거나 우세한 부위인 경우는 거의 없습니다. 현재까지 분리된 위 CD를 가진 성인에 대한 문서화된 증례 보고는 소수에 불과하며 소아 인구에서는 보고가 없습니다. 고립된 위 침범은 전체 위장관 CD의 0.07% 미만을 차지하는 매우 특이한 양상입니다.[35] 드물게 식도와 위가 크론병에 관여할 수 있습니다. 삼키기 곤란( 연하 곤란), 상복부 통증, 구토 등의 증상이 나타날 수 있습니다.[36]
오로인두 (입)
입은 반복적인 상처(진통성 궤양)에 의해 영향을 받을 수 있습니다. 재발성 아프타성 궤양은 흔하지만 이것이 크론병 때문인지 단순히 일반 인구에게 흔한 것인지는 명확하지 않습니다. 다른 소견으로는 입의 미만성 또는 결절성 부종, 입 안의 조약돌 모양, 육아종성 궤양 또는 화농성 식물염이 있을 수 있습니다. CD를 치료하기 위해 일반적으로 처방되는 항염증제 및 설파 함유 약물은 입에서 리체노이드 약물 반응을 일으킬 수 있습니다. 칸디다증과 같은 진균 감염도 질병의 치료에 필요한 면역 억제로 인해 흔히 발생합니다. 영양 흡수 장애로 창백·각성 구순염 등 빈혈 증상이나 광택염 증상도 흔히 나타납니다.[37]
크론병에 걸린 사람들은 입꼬리에 염증이 생기는 각성 구내염과 식물성 골수염에도 걸리기 쉽습니다.[38]
시스템적
다른 많은 만성 염증성 질환과 마찬가지로 크론병은 다양한 전신 증상을 유발할 수 있습니다.[1] 아이들 사이에서는 성장 실패가 흔합니다. 많은 어린이들이 성장을 유지하지 못하는 것을 근거로 크론병을 먼저 진단받습니다.[39] 사춘기에 성장이 싹트는 시기에 나타날 수 있는 것처럼 크론병 어린이의 최대 30%는 성장이 지연될 수 있습니다.[40] 38.5°C(101.3°F) 이상의 열은 농양과 같은 합병증이 없는 한 흔하지 않습니다.[1] 나이가 많은 사람들 사이에서 크론병은 체중 감소로 나타날 수 있는데, 크론병으로 인한 장 증상이 있는 사람들은 음식을 먹지 않을 때 기분이 좋아지고 식욕이 떨어질 수 있기 때문입니다.[39] 광범위한 소장 질환을 앓고 있는 사람도 탄수화물이나 지질의 흡수 장애가 있어 체중 감소를 더욱 악화시킬 수 있습니다.[41]
장외
크론병은 위장관을 넘어 많은 장기 시스템에 영향을 미칠 수 있습니다.[42]
| 크론스 질병 | 궤양성 대장염 | ||
|---|---|---|---|
| 영양결핍 | 고위험군 | ||
| 대장암 위험도 | 약간 | 고려하는 | |
| 장외 합병증의[43][44][45] 유병률 | |||
| 홍채염/포도막염 | 여성 | 2.2% | 3.2% |
| 남성 | 1.3% | 0.9% | |
| 원발성 경화증 담관염 | 여성 | 0.3% | 1% |
| 남성 | 0.4% | 3% | |
| 강직성 척추염 | 여성 | 0.7% | 0.8% |
| 남성 | 2.7% | 1.5% | |
| 표더마 괴저노섬 | 여성 | 1.2% | 0.8% |
| 남성 | 1.3% | 0.7% | |
| 홍반노도섬 | 여성 | 1.9% | 2% |
| 남성 | 0.6% | 0.7% | |
시각.
포도막염으로 알려진 눈의 내부 부분에 염증이 생기면 특히 빛에 노출되면 시야가 흐려지고 눈이 아플 수 있습니다.[46] 포도막염은 치료하지 않으면 시력을 잃을 수 있습니다.[42]
염증은 또한 눈의 하얀 부분(sclera)이나 위에 있는 결합 조직(epclera)을 포함할 수 있으며, 이는 각각 공막염과 상공막염이라고 불리는 질환을 유발합니다.[46]
그 밖에 매우 드문 안과적 증상으로는 결막염, 녹내장, 망막혈관질환 등이 있습니다.[47]
담낭과 간
회장에 영향을 미치는 크론병은 담석의 위험을 증가시킬 수 있습니다. 회장에서 담즙산의 흡수가 감소하여 담즙이 대변으로 배출되기 때문입니다. 그 결과 담낭 내 콜레스테롤/담즙 비율이 증가하여 담석의 위험도가 증가하게 됩니다.[46] 궤양성 대장염의 맥락에서 연관성이 더 크지만 크론병은 담관의 염증의 일종인 원발성 경화성 담관염과도 관련이 있을 수 있습니다.[48]
크론병의 간 침범은 간경변과 지방증을 포함할 수 있습니다. 비알코올성 지방간 질환(비알코올성 지방간염, NAFLD)은 비교적 흔하며 서서히 말기 간질환으로 진행될 수 있습니다. NAFLD는 간을 손상에 민감하게 만들고 또 다른 간 손상에 이어 급성 또는 만성 간부전으로 발전할 위험을 높입니다.[47]
크론병의 다른 드문 간담도 소견으로는 담관암, 육아종성 간염, 담석증, 자가면역 간염, 간농양, 담관 주위염 등이 있습니다.[47]
신장 및 비뇨기과
신장염, 폐쇄성 요로병증, 요로 누공은 기저질환 과정에서 직접적으로 발생합니다. 신장염은 옥살산칼슘이나 요산결석에 의한 것입니다. 옥살산칼슘은 전형적으로 말단 회장 CD 또는 회장 절제술과 관련된 고옥살뇨로 인한 것입니다. 대장에서 흡수되지 않은 지방산이 있으면 옥살산염 흡수가 증가합니다. 지방산은 칼슘과 결합하기 위해 옥살산과 경쟁하여 옥살산을 대체하고 대장세포를 가로질러 결합되지 않은 옥살산나트륨으로 흡수되어 소변으로 배출될 수 있습니다. 옥살산나트륨은 대장에서만 흡수되기 때문에 대장이 온전한 환자에게만 칼슘-옥살산 결석이 형성됩니다. 회장루절제술을 받은 환자는 탈수가 잦아 요산결석이 생기기 쉽습니다. IBD 환자에서 특히 일반적인 불편함과 다를 경우 갑자기 심한 복부, 등 또는 옆구리 통증이 시작되면 감별 진단에 신장 결석이 포함되어야 합니다.[47]
IBD 환자의 비뇨기학적 징후에는 요관 계산, 장루, 경막 감염, 뇌주위 농양 및 수신증이 있는 폐쇄성 요로병증이 포함될 수 있습니다. 요관 압박은 말단 회장과 맹장을 포함하는 가래성 염증 과정의 후복막 확장과 관련이 있으며, 고혈압을 유발할 정도로 심한 수신증을 유발할 수 있습니다.[47]
단백뇨 및 혈뇨를 동반하는 면역 복합 사구체신염은 CD 또는 UC를 가진 소아 및 성인에서 설명되었습니다. 진단은 신장 생검에 의한 것이며, 치료는 기저 IBD와 유사합니다.[47]
크론병에 이차적인 아밀로이드증(내분비학적 관여 참조)이 기술되었으며 신장에 영향을 미치는 것으로 알려져 있습니다.[47]
췌장의
췌장염은 UC와 CD 모두와 관련이 있을 수 있습니다. 가장 흔한 원인은 의인성이며, 설파살라진, 메살라민, 6-메르캅토푸린 및 아자티오프린을 포함한 IBD 치료에 사용되는 약물(환자의 3%)에 대한 민감성을 포함합니다. 췌장염은 IBD를 가진 성인에서 증상(2%) 또는 더 일반적으로 무증상(8-21%) 질환으로 나타날 수 있습니다.[47]
심혈관 및 순환기
IBD가 있는 어린이와 성인은 초기 발표 시 또는 활동성 또는 정지성 질환 중 흉막 주위염이 발생하는 것으로 보고된 경우가 거의 없습니다(<1%). 흉막성 심막염의 발병기전은 알려져 있지 않지만, 일부 경우에는 특정 약물(예: 설파살라진 및 메살라민 유도체)이 관련되어 있습니다. 임상적 소견으로는 흉통, 호흡곤란 또는 심한 경우 신속한 배액이 필요한 심낭 탐포나이드가 포함될 수 있습니다. 비스테로이드성 항염증제가 치료제로 사용되었지만 이것은 기저 IBD를 악화시키는 가상의 위험과 비교해야 합니다.[47]
드물게 심근병증, 심내막염, 심근염 등이 기재되어 있습니다.[47]
크론병은 또한 혈전의 위험을 증가시킵니다;[46] 아래 다리의 고통스러운 부종은 깊은 정맥 혈전증의 징후일 수 있고, 호흡 곤란은 폐색전증의 결과일 수 있습니다.
호흡기
염증성 장질환에 후두가 침범하는 경우는 극히 드물어요. 2019년[update] 현재까지 보고된 크론병의 후두 침범 사례는 12건에 불과합니다. 더욱이 궤양성 대장염에서 후두에 발현된 증례는 해당 날짜 현재 1건만 보고되고 있습니다.[49] 9명의 환자가 후두에서 인두하부까지 부종과 궤양으로 호흡 곤란을 호소했습니다.[50] 쉰 목소리, 인후통, 연하통은 크론병의 후두 침범의 다른 증상입니다.[51]
CD의 장외 증상을 고려할 때 폐와 관련된 증상은 비교적 드뭅니다. 그러나, 다양한 폐 증상들이 있는데, 이는 무증상의 변화, 기도 질환 및 폐 실질 질환에서부터 흉막 질환 및 약물 관련 질환에 이르기까지 다양합니다. 가장 빈번한 증상은 기관지확장증 유무에 관계없이 기관지 염증 및 진정입니다. 폐가 CD에 관여할 수 있는 여러 메커니즘이 있습니다. 여기에는 조상의 장에 의한 폐와 위장관의 동일한 발생학적 기원, 폐와 장 점막의 유사한 면역 체계, 순환하는 면역 복합체 및 자가 항체의 존재, 일부 약물의 폐 부작용 등이 포함됩니다.[52] 알려진 폐 증상의 완전한 목록은 섬유화 폐염, 폐혈관염, 정점 섬유화, 기관지확장증, 기관지염, 기관지염, 기관지 협착, 육아종성 폐질환 및 비정상적인 폐 기능을 포함합니다.[47]
근골격계
크론병은 혈청 음성 척추관절병증으로 알려진 류마티스 질환의 한 종류와 관련이 있습니다.[46] 이 질환군은 하나 이상의 관절(관절염)이나 근육 삽입(장염)에 염증이 생기는 것이 특징입니다.[46] 크론병의 관절염은 두 가지로 나눌 수 있습니다. 첫 번째 유형은 무릎(가장 일반적인), 엉덩이, 어깨, 손목 또는 팔꿈치와 같은 더 큰 체중을 견디는 관절에 영향을 미칩니다.[46] 두 번째 유형은 손과 발의 작은 관절 중 5개 이상을 대칭적으로 포함합니다.[46] 관절염도 척추를 침범해 척추 전체가 침범하면 강직성 척추염으로 이어지거나, 천 장관절만 침범하면 단순 천 장염으로 이어지기도 합니다.[46]
크론병은 골다공증이나 뼈가 얇아질 위험을 증가시킵니다.[46] 골다공증이 있는 사람들은 뼈 골절의 위험이 증가합니다.[53]
피부과
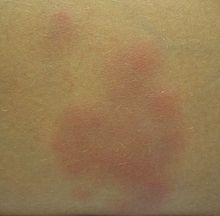
크론병은 또한 피부, 혈액 및 내분비계를 포함할 수 있습니다. 홍반성 결절증은 크론병 환자의 약 8%에서 발생하는 가장 흔한 유형의 피부 문제로 정강이에 주로 나타나는 융기되고 부드러운 붉은 결절을 생성합니다.[46][54][55] 홍반성 결절증은 기저 피하조직의 염증에 의한 것으로, 중격성 지방층염이 특징입니다.[54]
Pyoderma gerrenosum은 2% 미만에서 [55]발생하는 덜 흔한 피부 문제이며 일반적으로 고통스러운 궤양 결절입니다.[54][42]
손가락 끝의 기형인 클럽빙도 크론병의 결과일 수 있습니다.
다른 매우 희귀한 피부과 증상은 식물성 골수염, 건선, 홍반 다형, 표피 용혈성 불로사 아퀴스타(사례 보고서에 설명됨) 및 전이성 CD(크론 염증이 피부로 전이됨[38])를 포함합니다.[47] 스위트 증후군이 크론병과 관련이 있는지는 알 수 없습니다.[47]
신경학
크론병은 신경학적 합병증을 유발할 수도 있습니다(최대 15%).[56] 이 중 가장 흔한 것은 발작, 뇌졸중, 근병증, 말초신경병증, 두통, 우울증입니다.[56]
중추 및 말초 신경 장애는 IBD 환자에서 설명되며 말초 신경병증, 근병증, 초점 중추 신경계 결함, 경련, 혼란 에피소드, 뇌수막염, 실신, 시신경염 및 감각 신경 손실을 포함합니다. IBD와 관련된 자가면역 기전이 제안됩니다. 비타민 B12 결핍과 같은 신경학적 증상과 관련된 영양 결핍을 조사해야 합니다. 척추농양은 경막외 공간에서 지주막하 공간으로 압통이 확장되어 초기에 심한 요통을 호소한 소아와 성인 모두에서 보고되었습니다.[47]
정신과 및 심리학
크론병은 우울증과 불안, 자신의 질병에 대한 부정, 의존 또는 의존적인 행동의 필요성, 압도감, 좋지 않은 자아상을 포함한 많은 심리적 장애와 관련이 있습니다.[57]
많은 연구에서 IBD 환자가 일반 인구보다 더 높은 빈도의 우울증 및 불안 장애를 보고한다는 것을 발견했습니다. 대부분의 연구는 IBD를 가진 여성이 남성보다 정의적 장애에 걸릴 가능성이 더 높다는 것을 확인하고 그들 중 최대 65%가 우울증 및 불안 장애를 가지고 있을 수 있다는 것을 보여줍니다.[58][59]
내분비학적 또는 혈액학적
면역계가 적혈구를 공격하는 질환인 자가면역용혈성빈혈도 크론병에서 더 흔하며 피로감, 창백한 외모 등 빈혈에서 흔히 나타나는 증상을 유발할 수 있습니다.
이차성 아밀로이드증(AA)은 크론병에서 일반적으로 나타나는 염증성 장질환(IBD)의 또 다른 드물지만 심각한 합병증입니다. 크론병 환자의 최소 1%에서 아밀로이드증이 발생합니다. 문헌에서 크론병 발병과 아밀로이드증 진단 사이의 시간 경과는 1년에서 21년 사이로 보고되었습니다.
백혈구 증가증과 혈소판 감소증은 대개 면역억제제 치료나 설파살라진 때문입니다. 심각한 빈혈과 함께 IBD 환자의 혈장 에리트로포이에틴 수치가 예상보다 낮은 경우가 많습니다.[47]
IBD 환자의 과응고 상태로 인한 혈전증 및 혈전색전증 사건은 폐색전증 또는 신체의 다른 곳에서 혈전증을 유발할 수 있습니다. UC 환자의 1.8%, CD 환자의 3.1%에서 혈전증이 보고되었습니다. 혈전색전증과 혈전증은 소아 환자들 사이에서 덜 빈번하게 보고되며, UC 환자는 3명, CD 환자는 1명이 증례 보고에 기술되어 있습니다.[47]
드물게 과응고 장애와 간문맥 혈전증이 설명되었습니다.[47]
영양실조증상
크론병에 걸린 사람은 비타민 B12, 엽산, 철분 결핍으로 인해 빈혈이 발생하거나 만성 질환의 빈혈로 인해 빈혈이 발생할 수 있습니다.[60][61] 가장 흔한 것은 만성적인 혈액 손실로 인한 철분 결핍성 빈혈[60], 식이 섭취 감소, 지속적인 염증으로 인해 헵시딘 수치가 증가하여 십이지장 내 철분 흡수가 제한됩니다.[61] 크론병은 비타민 B12/내인성 인자 복합체가 흡수되는 말단 회장에 가장 흔하게 영향을 미치므로 B12 결핍을 볼 수 있습니다.[61] 이것은 특히 회장을 제거하는 수술 후에 흔히 발생합니다.[60] 십이지장과 공장의 침범은 엽산을 포함한 다른 많은 영양소의 흡수를 손상시킬 수 있습니다. 크론병에 걸린 사람들은 종종 미세영양소 결핍을 일으킬 수 있는 소장 세균 과증식 증후군에 문제가 있습니다.[62][63]
합병증
장상해

크론병은 장 내에서 폐색,[64][65] 누공, 농양 등 여러 기계적 합병증을 유발할 수 있습니다.[66] 폐색은 일반적으로 내강을 좁히는 협착이나 유착에서 발생하여 장 내용물의 통과를 막습니다. 누공은 장과 방광 사이, 장과 질 사이, 장과 피부 사이의 두 고리 사이에서 발생할 수 있습니다. 농양은 복부나 항문주위에 발생할 수 있는 감염의 장벽이 있는 농도입니다. 크론병은 소포장 누공의 10%를 담당하며, 회장성 누공의 가장 흔한 원인입니다.[67]
장협착으로 인한 증상, 즉 장이 조여지고 좁아지는 증상도 크론병에서 흔히 나타납니다. 복통은 협착이 있는 장 부위가 가장 심한 경우가 많습니다. 지속적인 구토와 메스꺼움은 소장 폐쇄로 인한 협착이나 위, 유문 또는 십이지장과 관련된 질병을 나타낼 수 있습니다.[32]
장 육아종은 감염을 분리하기 위해 대식세포에 의해 장의 벽으로 둘러싸인 부분입니다. 육아종 형성은 젊은 환자에서 더 자주 나타나며, 주로 중증의 활동성 침투성 질환에서 나타납니다.[68] 육아종은 크론병(CD)에서 현미경 진단의 특징으로 여겨지지만, 육아종은 CD 환자의 21-60%에서만 발견될 수 있습니다.[68]
암
크론병은 염증 부위의 암 발생 위험도 증가시킵니다. 예를 들어 소장과 관련된 크론병 환자는 소장암에 걸릴 위험이 더 높습니다.[69] 마찬가지로 크론 대장염에 걸린 사람들은 대장암에 걸릴 상대적 위험이 5.6입니다.[70] 최소 8년 이상 크론 대장염에 걸린 사람은 대장 내시경으로 대장암 검진을 받는 것이 좋습니다.[71]
일부 연구는 대장과 관련된 크론의 대장암 예방에 화학적 보호의 역할이 있음을 시사합니다; 엽산과 메살라민 제제의 두 가지 제제가 제안되었습니다.[72] 또한, 이 질병을 치료하기 위해 사용되는 면역 조절제와 생물학적 제제는 장 외 암 발생을 촉진할 수 있습니다.[73]
급성 골수성 백혈병과 같은 일부 암은 크론병의 경우에 기술되었습니다.[47] 간비장염 T세포 림프종(HSTCL)은 염증성 장질환을 가진 젊은 남성 환자들에게 일반적으로 나타나는 희귀하고 치명적인 질병입니다. TNF-α 억제제 치료제(infliximab, adalimumab, certolizumab, natalizumab, etanercept)가 이 희귀 질환의 원인으로 생각됩니다.[74]

주요 합병증
크론병의 주요 합병증으로는 장폐색, 농양, 유리천공, 출혈 등이 있는데, 드물게는 치명적일 수도 있습니다.[75][76]
기타합병증
크론병에 걸린 사람들은 음식 섭취 감소와 흡수 장애를 포함한 많은 이유로 영양실조의 위험에 처해 있습니다. 소장을 절제한 후 위험이 증가합니다. 이러한 사람들은 칼로리 섭취량을 증가시키기 위해 경구 보충제를 필요로 하거나 심한 경우 총비경구영양법(TPN)을 필요로 할 수 있습니다. 보통 또는 심각한 크론병을 앓고 있는 대부분의 사람들은 영양 보조를 위해 영양사에게 의뢰됩니다.[77]
소장세균과다증식(small interest bacterial overgrowth, SIBO)은 소장에서 대장세균종이 과도하게 증식하는 것이 특징입니다. SIBO의 잠재적인 원인은 누공, 협착 또는 운동 장애를 포함합니다. 따라서 크론병 환자는 특히 SIBO가 발생하기 쉽습니다. 이로 인해 CD 환자는 흡수 장애를 경험하고 체중 감소, 수분 설사, 유성증, 풍만감, 복통 등의 증상을 보고할 수 있으며, 이러한 환자에서 급성 발적을 모방합니다.[63]
임신
크론병은 임신 중에 문제가 될 수 있으며 일부 약물은 태아나 산모에게 좋지 않은 결과를 초래할 수 있습니다. 크론병과 모든 약물에 대해 산부인과 및 소화기내과 전문의와 상담하면 예방 조치가 용이합니다. 임신 중에 관해가 발생하는 경우도 있습니다. 특정 약물은 정자 수를 낮추거나 그렇지 않으면 남성의 생식력에 악영향을 미칠 수 있습니다.[78]
항문 절제술(크론병에서 흔히 볼 수 있는 수술)의 흔한 합병증은 점막 부종, 연동 피부염, 후퇴, 장루 탈출, 점막/피부 박리, 혈종, 괴사, 하반신 탈장 및 협착입니다.[79]
병인학
크론병의 병인은 알려지지 않았습니다. 크론병의 주요 기전으로 4개의 주요 이론이 가설되는 등 많은 이론들이 논란이 되고 있습니다. 자가면역질환에서 항체와 T림프구는 염증의 주된 방식입니다. 이 세포들과 신체들은 적응 면역 체계의 일부, 혹은 처음 확인되었을 때 이물질과 싸우는 법을 배우는 면역 체계의 일부입니다.[80] 자가 염증성 질환은 선천성 면역 체계, 즉 유전적으로 암호화된 면역 체계가 우리 자신의 세포를 공격하도록 설계된 질병입니다.[81] 크론병은 적응성 면역체계와 선천성 면역체계를 모두 포함하고 있습니다.[82]
자가염증이론
크론병은 다인성 자가염증성 질환으로 설명할 수 있습니다. 크론병의 특발성은 아직 알려지지 않았습니다. 어쨌든, 면역 기구의 조절 능력의 상실은 질병의 발병과 관련이 있을 것입니다. 이 점에서 흥미롭게도 블라우병(단일성 자가염증성 질환)의 경우, NOD2 유전자 돌연변이가 크론병과 연관되어 있습니다. 그러나 크론병에서는 NOD2 변이가 위험인자로 작용하여 배경집단보다 크론병 환자들에게 더 많이 나타나는 반면, 블라우병에서는 NOD2 변이가 상염색체 우성 질환이기 때문에 이 증후군과 직접적으로 연관되어 있습니다. 크론병의 발병기전에 대한 이 모든 새로운 지식은 우리가 이 다인성 질환을 자가염증 증후군의 그룹에 넣을 수 있게 해줍니다.[81]
선천성 면역 체계가 장 염증에 어떤 영향을 미치는지에 대한 몇 가지 예를 설명했습니다.[82] CD 유전체 전체 연관 연구의 메타 분석에서 71개의 별개의 CD 민감도 유전자좌가 밝혀졌습니다. 흥미롭게도, 3개의 매우 중요한 CD-민감성 유전자(세포내 병원체 인식 수용체, NOD2; 자가포식 관련 16-유사 1, ATG16L1 및 면역 관련 GTPase M, IRGM)는 장내 미생물에 대한 선천적 면역 반응에 관여합니다. 하나(X-box 결합 단백질 1)는 MHC 그룹 II를 통한 [적응적] 면역 경로의 [83]조절에 관여하여 자가 염증을 유발합니다. 연구에 따르면 ILC3의 증가는 주요 조직적합성 복합체(MHC) II를 과발현할 수 있습니다. MHC 클래스 II는 CD4+ T 세포 사멸을 유도하여 정상적인 장내 미생물에 대한 T 세포 반응을 피할 수 있습니다. 비IBD 환자와 비교한 IBD 환자에 대한 추가 연구에서 ILC3에 의한 MHC II의 발현이 IBD 환자에서 현저하게 감소하여 장 세포 또는 정상적인 장 세균에 대한 면역 반응을 유발하고 장을 손상시키는 것으로 나타났습니다. 이것은 또한 장을 음식이나 박테리아와 같은 환경적 요인에 더 취약하게 만들 수 있습니다.[82]
크론병은 선천성 면역체계의 관여가 강하고 NOD2 돌연변이를 소인으로 가지고 있기 때문에 자가면역질환보다는 자가염증성 질환일 가능성이 높다는 생각입니다.[82]
면역결핍설
최근 몇 년 동안 크론병의 주요 결함이 실제로 상대적인 면역 결핍 중 하나임을 시사하는 상당한 데이터가 나타났습니다.[84] 이러한 견해는 최근 선천성 면역 기능에 중요한 분자를 강조한 후속 유전 연구와 일치하는 초기 반응에서 심각한 이상을 확인한 새로운 면역학 및 임상 연구에 의해 강화되었습니다. 따라서 제안은 크론의 병인이 실제로 부분 면역결핍에서 비롯된다는 것인데, 이는 식세포 기능을 손상시키는 선천성 단성 질환 환자에서 발생하는 사실상 동일한 비감염성 염증성 장 질환의 빈번한 인식과 일치하는 이론입니다.[84]
위험요소
| 크론병 | 궤양성 대장염 | |
|---|---|---|
| 흡연석을 부탁해요. | 흡연자의 위험도가 높음 | 흡연자의[85] 위험 감소 |
| 나이 | 사이의 일반적인 발병 15년과[86] 30년 | 사이의 최고 발생률 15년과 25년 |
정확한 원인이나 원인은 알려지지 않았지만 크론병은 환경적 요인과 유전적 성향이 복합적으로 작용한 것으로 보입니다.[87] 크론병은 유전적 위험인자와 면역체계의 관계가 상당히 구체적으로 이해되는 최초의 유전적 복합질환입니다.[88] 각 개별 위험 돌연변이는 크론병의 전체 위험에 작은 기여를 합니다(약 1:200). 면역력에 대한 직접적인 평가, 즉 유전적 데이터는 선천적인 면역체계의 오작동을 나타냅니다.[89] 이 관점에서 크론병의 만성 염증은 적응성 면역체계가 결핍된 선천성 면역체계를 보완하려고 할 때 발생합니다.[90]
유전학

크론은 유전적인 요소를 가지고 있습니다.[92] 이 때문에 크론병에 걸린 것으로 알려진 사람들의 형제자매들은 일반인들보다 크론병에 걸릴 확률이 30배나 높습니다.[93]
크론과 관련이 있는 것으로 밝혀진 첫 번째 돌연변이는 NOD2 유전자(일명 CARD15 유전자)의 프레임 시프트였고,[94] 이어서 점 돌연변이가 발견되었습니다.[95] 30개 이상의 유전자가 크론과 관련이 있습니다; 대부분 생물학적 기능이 알려져 있습니다. 예를 들어, 한 가지 연관성은 소포체의 펼쳐진 단백질 반응 경로에 관여하는 XBP1 유전자의 돌연변이와 관련이 있습니다.[96][97] NOD2/CARD15의 유전자 변이는 소장 침범과 관련이 있는 것으로 보입니다.[98] 크론병 발병 위험을 높이는 다른 잘 문서화된 유전자는 ATG16L1,[99] IL23R,[100][101] IRGM 및 SLC11A1입니다.[102] IBD에 대한 민감도 유전자좌와 마이코박테리아 감염 사이에는 상당한 중복이 있습니다.[103] 유전체 전체의 연관성 연구는 크론병이 유전적으로 실장골 질환과 관련이 있다는 것을 보여주었습니다.[104]
크론스는 유전자 LRRK2와 관련이 있으며 한 변이체는 잠재적으로 질병 발병 위험을 70%까지 증가시키는 반면 다른 변이체는 25%까지 낮춥니다. 이 유전자는 단백질을 만드는 역할을 하는데, 이 단백질은 세포의 노폐물을 모으고 제거하며, 파킨슨병과도 연관이 있습니다.[105]
면역체계
크론병은 원발성 T세포 자가면역질환이라는 견해가 지배적이었지만, 새로운 이론은 크론병이 선천성 면역력의 손상으로 인한 것이라는 가설을 세웠습니다.[106] 나중의 가설은 대식세포에 의한 사이토카인 분비 장애를 설명하는데, 이는 선천성 면역 장애에 기여하고 박테리아 부하가 높은 대장에서 지속적인 미생물 유발 염증 반응으로 이어집니다.[9][89] 또 다른 이론으로는 크론병의 염증이 T1과 T17hh 사이토카인의 과활성 반응에 의해 발생했다는 것입니다.[107][108]
2007년 ATG16L1 유전자는 자가포식을 유도하고 침습성 박테리아를 공격하는 신체의 능력을 방해할 수 있는 크론병과 관련이 있습니다.[99] 또 다른 연구에서는 인간의 면역 체계가 전통적으로 몸 안에 기생충이 존재하면서 진화했으며 현대의 위생 기준으로 인해 기생충이 부족하여 면역 체계가 약화되었다고 이론을 세웠습니다. 실험 대상자들은 다시 무해한 기생충에 도입되었고, 긍정적인 반응을 보였습니다.[109]
미생물
GI관에서 공생 미생물 성장의 유지는 면역 조절 장애의 결과 또는 원인으로 조절 장애를 일으킨다는 가설이 있습니다.[110][111]
크론병, 마이코박테리움, 다른 병원성 세균, 그리고 유전자 표지 사이에는 명백한 연관성이 있습니다.[112][113] 많은 연구에서 소에서 유사한 질병인 존병을 유발하는 MAP(Mycobacterium avium subspecies paratuberculosis)의 인과적 역할을 제시했습니다.[114][115] 많은 사람들에게 유전적 요인은 Mycobacterium avium subsp. paratuberculosis 감염의 소인이 됩니다. 이 박테리아는 만노스를 포함하는 특정 화합물을 생성할 수 있으며, 이는 식균 작용으로부터 자신과 다양한 다른 박테리아를 보호하여 다양한 2차 감염을 유발할 수 있습니다.[116]
NOD2는 크론의 유전적 감수성에 관여하는 유전자입니다. 이는 대식세포의 MAP 식세포화 능력 저하와 관련이 있습니다. 이와 같은 유전자는 위장 조직의 선천성 및 적응성 면역을 감소시키고 MAP 박테리아에 의한 감염에 저항하는 능력을 손상시킬 수 있습니다.[117] MAP 박테리아를 섭취하는 대식세포는 TNF-α의 높은 생산과 관련이 있습니다.[118][119]
다른 연구들은 특정 종류의 장부착성 대장균을 이 질병과 연관시켰습니다.[120] CD를 가진 사람들에게 더 흔한 부착 침습성 대장균([121][122][120]AIEC)은 호중구의 높은 부착 및 침입 지수와[123][124] 관련된 비-AIEC 균주에 비해 강력한 생물막을 만드는 능력과 자가포식을 자가포식 단계에서 차단하는 능력을 가지고 있습니다. 박테리아의 세포 내 생존과 염증 유도를 가능하게 합니다.[125] 염증은 유전자형에 관계없이 회장에서 AIEC의 증식과 세균 불균형을 유발합니다.[126] AIEC 균주는 대식세포 내부에서 광범위하게 복제되어 매우 많은 양의 TNF-α의 분비를 유도합니다.[127]
쥐 연구에 따르면 크론병, 궤양성 대장염, 과민성 장증후군의 일부 증상이 근본 원인과 같다고 합니다. 세 환자 그룹의 결장에서 채취한 생검 샘플은 높은 수준의 세린 단백질분해효소를 생성하는 것으로 나타났습니다.[128] 세린 프로테아제를 쥐에게 실험적으로 도입하면 과민성 장증후군과 관련된 광범위한 통증을 유발하는 것으로 밝혀졌으며, 이는 세 가지 질병 모두와 관련이 있습니다.[129] 이러한 질병의 지역적 및 시간적 변화는 원생동물 배반포낭염 감염과 관련된 질병을 따릅니다.[130]
"콜드체인" 가설은 여시니아와 리스테리아 종과 같은 정신성 박테리아가 이 질병에 기여한다는 것입니다. 미국과 유럽 여러 지역에서 냉장고 사용이 시작되고 질병이 증가하는 사이에 통계적 상관관계가 발견되었습니다.[131][132][133]
칸디다 집락화와 크론병 사이에는 잠정적인 연관성도 있습니다.[134]
여전히 특정 병원체와 크론병 사이의 이러한 관계는 불분명합니다.[135][136]
환경적 요인
산업화된 세계에서 크론병의 발병률이 증가하는 것은 환경적 요소를 나타냅니다. 크론병은 동물성 단백질, 우유 단백질의 섭취 증가, 오메가-6 대 오메가-3 고도 불포화 지방산의 비율 증가와 관련이 있습니다.[137] 식물성 단백질을 섭취하는 사람들은 크론병의 발병률이 낮은 것으로 보입니다. 생선 단백질 섭취는 연관성이 없습니다.[137] 흡연은 활동성 질환(불꽃)의 복귀 위험을 증가시킵니다.[4] 1960년대 미국에서 호르몬 피임법이 도입된 것은 발병률의 급격한 증가와 관련이 있으며, 한 가지 가설은 이러한 약물이 흡연과 유사한 방식으로 소화기에 작용한다는 것입니다.[138] 이소트레티노인은 크론병과 관련이 있습니다.[139][140][141]
스트레스가 크론병을 악화시킨다고 주장하기도 하지만, 그러한 주장을 뒷받침할 구체적인 증거는 없습니다.[3] 그래도 면역 기능이 스트레스와 관련이 있다는 것은 잘 알려져 있습니다.[142] 치약에서 발견되는 것과 같은 식이성 미세입자는 면역력에 영향을 미치기 때문에 연구되어 왔지만 크론병 환자들에게는 더 많은 양이 섭취되지 않았습니다.[143][144] 독시사이클린의 사용은 또한 염증성 장 질환의 발병 위험 증가와 관련이 있습니다.[145][146][147] 한 대규모 후향적 연구에서 여드름으로 독시사이클린을 처방받은 환자는 크론병에 걸릴 위험이 2.25배 더 높았습니다.[146]
병태생리학
| 크론병 | 궤양성 대장염 | |
|---|---|---|
| 사이토카인반응 | T17h[148] 관련 | T2와h 모호하게 연관됨 |
대장 내시경 검사 중에는 진단을 확인하기 위해 대장 생검을 하는 경우가 많습니다. 보이는 병리학의 특정한 특징은 크론병을 가리킵니다. 그것은 염증의 경벽 패턴을 보여주는데, 이것은 염증이 장벽의 전체 깊이에 걸쳐 있을 수 있다는 것을 의미합니다.[1]
거대세포로 알려진 대식세포 유도체의 응집체인 육아종은 사례의 50%에서 발견되며 크론병에 가장 특이적입니다. 크론병의 육아종은 결핵과 같은 감염과 관련된 육아종의 현미경 검사에서 치즈와 같은 모양인 "caseation"을 보이지 않습니다. 생검은 또한 장 융모의 둔탁, 음와의 비정형 분지 및 조직 유형의 변화(화생)에 의해 입증되는 만성 점막 손상을 보일 수 있습니다. 이러한 대사증후군의 한 예인 Paneth cell metaplasia는 위장계의 다른 부분에서 Paneth cells (일반적으로 소장에서 발견되며 장내 미생물의 주요 조절인자)의 발달을 포함합니다.[149][150]
진단.
크론병의 진단은 때때로 어려울 수 있으며,[28] 의사가 진단을 내리는 데 도움을 주기 위해 많은 검사가 필요합니다.[32] 전체 검사 배터리를 사용하더라도 완전한 확실성으로 크론병을 진단할 수는 없을 수도 있습니다. 대장 내시경 검사는 질병 진단에 약 70% 효과적이며, 추가 검사는 효과적이지 않습니다. 소장의 질병은 특히 진단이 어렵습니다. 전통적인 대장내시경 검사는 대장과 소장 하부에만 접근할 수 있기 때문입니다. 캡슐내시경[151] 검사를 도입하면 내시경 진단에 도움이 됩니다. 크론병 병변에서 흔히 발견되는 거대(다핵) 세포는 지의류 병변에서는 덜 흔합니다.[152]
분류

크론병은 염증성 장질환의 한 종류입니다. 일반적으로 위장관에서 나타나며 영향을 받는 특정 부위에 따라 분류할 수 있습니다.
위십이지장 크론병은 위와 십이지장이라는 소장의 첫 부분에 염증을 일으킵니다. 공장성 장염은 소장의 위쪽 절반에 점박이 염증을 유발하는데, 이를 공장이라고 합니다.[153] 이 질병은 입에서 항문에 이르기까지 소화관의 모든 부분을 공격할 수 있습니다. 그러나 이 질병의 영향을 받는 개인은 다른 영역에서 발표와 함께 이 세 가지 분류를 벗어나는 경우는 거의 없습니다.[1]
크론병은 진행됨에 따라 질병의 행동에 따라 분류될 수도 있습니다. 이러한 분류는 질병의 비엔나 분류에서 공식화되었습니다.[154] 크론병은 협착, 침투, 염증 등 세 가지로 분류됩니다. 협착성 질환은 장이 좁아져 장폐색이나 대변의 질에 변화가 생길 수 있습니다. 침투성 질환은 장과 피부와 같은 다른 구조물 사이에 비정상적인 통로(누공)를 만듭니다. 염증성 질환(또는 비협착성, 비침투성 질환)은 협착이나 누공을 일으키지 않고 염증을 유발합니다.[154][155]
내시경
대장내시경 검사는 대장과 말단 회장을 직접 시각화하여 질병의 침범 패턴을 식별할 수 있기 때문에 크론병 진단을 위한 최고의 검사입니다. 간혹 대장내시경은 말단 회장을 지나칠 수 있지만 사람마다 다릅니다. 시술 중에는 소화기내과 전문의가 조직 검사를 수행하여 실험실 분석을 위해 소량의 조직 샘플을 채취할 수도 있어 진단을 확인하는 데 도움이 될 수 있습니다. 크론병의 30%는 회장만 침범하기 때문에 진단을 내리는 데 말단 회장의 캐뉼러 삽입이 필요합니다.[1] 결장이나 회장을 포함하지만 직장을 포함하지 않는 부분적인 질병 분포를 발견하는 것은 다른 내시경 스티그마타와 마찬가지로 크론병을 암시합니다.[156] 그러나 이를 위한 캡슐 내시경의 효용성은 여전히 불확실합니다.[157]
방사선학적 검사
소장 추적 검사는 크론병의 진단을 시사할 수 있으며 소장만 관련된 질병일 때 유용합니다. 대장내시경과 위내시경은 말단 회장과 십이지장 시작 부분만 직접 시각화할 수 있기 때문에 소장의 나머지 부분을 평가하는 데 사용할 수 없습니다. 그 결과 황산바륨 현탁액을 섭취하고 장을 투시하여 시간이 지남에 따라 장을 촬영하는 바륨 추적 X선은 소장의 염증 및 협착을 찾는 데 유용합니다.[156][158] 바륨을 직장에 삽입하고 형광 투시를 통해 장을 촬영하는 바륨 관장제는 대장내시경 검사의 등장으로 크론병의 정밀검사에는 거의 사용되지 않습니다. 대장의 협착이 너무 작아서 대장 내시경이 통과할 수 없을 때나 대장 누공을 감지할 때 해부학적 이상을 식별하는 데 유용합니다(이 경우 요오드산염 물질로 조영술을 수행해야 합니다).[159]
CT 및 MRI 스캔은 장용해 프로토콜로 소장을 평가하는 데 유용합니다.[160] 이들은 또한 농양, 소장 폐쇄 또는 누공과 같은 크론병의 복강 내 합병증을 찾는 데 유용합니다.[161] 자기공명영상(MRI)은 소장을 촬영하고 합병증을 찾는 또 다른 방법이지만 비용이 많이 들고 쉽게 구할 수 없습니다.[162] 확산가중영상, 고해상도영상 등 MRI 기법은 CT에 비해 궤양과 염증을 감지하는 데 더 민감합니다.[163][164]
혈액검사
완전한 혈구 수는 빈혈을 나타낼 수 있는데, 빈혈은 일반적으로 혈액 손실이 철분 결핍으로 이어지거나 비타민 B12 결핍으로 발생하는데, 대개 회장 질환이 비타민 B12 흡수를 손상시킴으로써 발생합니다. 드물게 자가면역 용혈이 발생할 수 있습니다.[165] 페리틴 수치는 철분 결핍이 빈혈에 기여하는지 평가하는 데 도움이 됩니다. 적혈구침강속도(ESR)와 C반응성 단백질은 염증의 정도를 평가하는 데 도움이 되는데, 페리틴도 염증에서 상승할 수 있어 중요합니다.[166]
빈혈의 다른 원인으로는 염증성 장질환 치료에 사용되는 약물, 예를 들어 세포감소증을 유발할 수 있는 아자티오프린, 엽산 결핍을 유발할 수 있는 설파살라진 등이 있습니다. Saccharomyces[167] cerevisiae antibody(ASCA)와 항호중구 세포질 항체(ANCA)에 대한 검사는 장의 염증성 질환을 확인하고 크론병을 궤양성 대장염과 구별하기 위해 평가되었습니다.[168] 또한, ASCA, 항아미나리바이오사이드[Glc(β1,3)Glb(β); ALCA], 항시토바이오사이드[GlcNAc(β1,4)GlcNAc(β); ACCA], 항만노바이오사이드[Man(α1,3)Man(α)] 등의 혈청학적 항체의 양 및 수준 증가AMCA], 항Laminarin[(Glc(β1,3))3n(Glc(β1,6)n; 항-L] 및 항-티틴[GlcNAc(β1,4)n; 항-C]은 질병 행동 및 수술과 관련이 있으며, 크론병의 예후에 도움이 될 수 있습니다.[169][170][171][172]
낮은 혈청 수치의 비타민 D는 크론병과 관련이 있습니다.[173] 이 연관성의 중요성을 결정하기 위해서는 추가 연구가 필요합니다.[173]
궤양성 대장염과의 비교
크론병의 증상을 모방하는 가장 흔한 질병은 궤양성 대장염인데, 둘 다 비슷한 증상으로 대장에 영향을 줄 수 있는 염증성 장질환입니다. 질병과 치료 과정이 다를 수 있기 때문에 이러한 질병을 구별하는 것이 중요합니다. 하지만 경우에 따라서는 그 차이를 구분할 수 없을 수도 있는데, 이 경우 질병은 불확정 대장염으로 분류됩니다.[1][32][33]
| 크론병 | 궤양성 대장염 | |
|---|---|---|
| 말단 회장 침범 | 일반적으로 | 드물게 |
| 대장 침범 | 보통 | 항상 |
| 직장 침범 | 드물게 | 보통(95%)[85] |
| 주변의 관여 항문 | 공통[174] | 드물게 |
| 담관 침범 | 원발성 경화성 담관염의 증가는 없습니다 | 고율[175] |
| 질병의 분포 | 염증이 있는 부위(슬립병변) | 염증의 연속부위[85] |
| 내시경 | 깊은 지리적, 농포성(뱀 모양) 궤양 | 지속성 궤양 |
| 염증의 깊이 | 경벽성일 수도 있고[174][176], 조직 깊숙이 있을 수도 있습니다. | 얕은 점막 |
| 협착증 | 흔한 | 드물게 |
| 조직검사상 육아종 | 비괴사성 장 주위 음와 육아종이[174][177][178] 있을 수 있습니다 | 비장내 음와립종은 보이지[179] 않습니다 |
감별진단
크론병과 유사한 증상을 보이는 다른 질환으로는 장결핵, 베체트병, 궤양성 대장염, 비스테로이드성 소염제 장병증, 과민성 장증후군, 셀리악병 등이 있습니다.[5] 과민성 장증후군은 염증성 변화가 있을 때는 제외됩니다.[5] 셀리악병은 특정 항체(항-트랜스글루타미나제 항체)가 음성이거나 [180][181]장 융모 위축이 없는 경우 배제할 수 없습니다.[182][183]
관리
| 크론병 | 궤양성 대장염 | |
|---|---|---|
| 메살라진 | 유용성이[184] 떨어짐 | 더[184] 유용한 |
| 항생제 | 장기적으로[185] 효과적입니다. | 일반적으로 유용하지[186] 않음 |
| 수술. | 종종 다음과 같이 반환됩니다. 환부 제거 | 보통 제거로 치료됩니다. 대장의 |
크론병은 치료법이 없으며, 완치가 불가능하거나 달성될 경우 장기화될 수 있습니다. 관해가 가능한 경우에는 약물치료, 생활습관 및 식이요법의 변화, 식습관의 변화(적은 양을 더 자주 섭취), 스트레스의 감소, 적당한 활동, 운동 등으로 재발을 예방하고 증상을 조절할 수 있습니다. 수술은 일반적으로 금기이며 재발을 예방하는 것으로 나타나지 않았습니다. 적절히 조절되면 크론병은 일상생활을 크게 제한하지 않을 수 있습니다.[187] 크론병의 치료는 먼저 급성 문제와 증상을 치료한 다음 질병의 관해를 유지하는 것을 포함합니다.
생활양식의 변화
특정 생활 습관 변화는 식이 조절, 기본 식단, 적절한 수분 공급 및 금연을 포함하여 증상을 줄일 수 있습니다. 크론병 환자들은 다이어트에 관심이 많습니다. 최근 리뷰에서는 이러한 환자에게 미치는 식단의 영향에 대해 거의 알려져 있지 않더라도 증거에 의해 가장 잘 뒷받침되는 식단을 채택하는 것이 중요하다고 강조했습니다.[188][189] 섬유질과 과일을 더 많이 포함한 식단은 위험 감소와 관련이 있는 반면, 총 지방, 다중 불포화 지방산, 육류 및 오메가-6 지방산이 풍부한 식단은 크론병의 위험을 증가시킬 수 있습니다.[190] 적절한 비율 조절로 균형 잡힌 식단을 유지하는 것은 질병의 증상을 관리하는 데 도움이 될 수 있습니다. 큰 식사 대신 작은 식사를 자주 하는 것도 식욕 부진에 도움이 될 수 있습니다. 음식 일기는 증상을 유발하는 음식을 식별하는 데 도움이 될 수 있습니다. 장 건강을 위한 식이섬유의 중요성이 인식되고 있음에도 불구하고, 일부 사람들은 특히 불용성 섬유질이 많은 음식이 장의 폐색이나 자극으로 인해 증상을 일으키는 경우 급성 증상을 조절하기 위해 저잔류 식이요법을 따라야 합니다.[187] 어떤 사람들은 식단에서 카제인(젖에서 발견되는 단백질)과 글루텐(밀, 호밀, 보리에서 발견되는 단백질)을 제거하는 것이 도움이 된다고 생각합니다. 그들은 (알레르기가 아닌) 특정 식이 과민증을 가지고 있을 수 있습니다(예: 유당).[191] 피로는 규칙적인 운동과 건강한 식단, 충분한 수면으로 도움을 받을 수 있으며, 질병으로 인한 비타민 B의12 흡수 장애나 말단 회장의 외과적 절제로 인한 코발아민 주사 등이 있습니다. 흡연은 증상과 병의 경과를 악화시킬 수 있으며, 중단하는 것이 좋습니다. 알코올 섭취 또한 증상을 악화시킬 수 있으며, 절제 또는 중단이 권장됩니다.[187]
약
급성 치료는 모든 감염(보통 항생제)을 치료하고 염증(보통 아미노살리실레이트 소염제 및 코르티코스테로이드)을 줄이기 위해 약물을 사용합니다. 증상이 완화되면 증상의 재발을 방지하기 위한 목적으로 치료가 유지됩니다. 코르티코스테로이드를 장기간 사용하면 심각한 부작용이 발생하므로 일반적으로 장기 치료에는 사용되지 않습니다. 대안에는 아미노살리실레이트 단독이 포함되지만 소수만이 치료를 유지할 수 있고 많은 사람들이 면역억제제를 필요로 합니다.[174] 또한 항생제가 장내 세균총을 변화시키고 지속적으로 사용하면 Clostridium difficile와 같은 병원체와의 과증식 위험이 있을 수 있다고 제안되었습니다.[192]
크론병의 증상을 치료하는 데 사용되는 약물에는 5-아미노살리실산(5-ASA) 제제, 프레드니손, 아자티오프린(6-메르캅토푸린의 전구약물로 제공)과 같은 면역 조절제, 메토트렉세이트,[193] 항-TNF 치료제 및 인플릭시맙, 아달리무맙,[33] 세르톨리주맙,[194] 베돌리주맙, 우스테키누맙과 같은 단일 클론 항체가 포함됩니다.[195] 나탈리주맙,[196][197] 리산키주맙-rzaa 및 우파다시티닙[198] 하이드로코르티손은 크론병의 심각한 공격에 사용되어야 합니다.[199] 생물학적 치료법은 장기간 스테로이드 사용을 피하고 염증을 줄이고 농양이 있는 누공을 치료하는 데 사용되는 약물입니다.[31] 단일클론항체 우스테키누맙은 안전한 치료법으로 보이며, 중등도에서 중증의 활동성 크론병 환자에게 도움이 될 수 있습니다.[200] 단일클론항체 치료의 장기적인 안전성과 효과는 알려져 있지 않습니다.[200] 단클론항체 브리아키누맙은 활동성 크론병 환자에게는 효과가 없고 더 이상 제조되지 않습니다.[200]
만성 염증 뿐만 아니라 위장관에서 혈액이 점차 손실되면서 빈혈이 발생하는 경우가 많은데, 이에 대한 정기적인 모니터링을 전문 가이드라인에서 제안하고 있습니다.[201][202][203]
면역억제제 치료, 감염 위험 및 예방접종
크론병의 영향을 받는 많은 환자들은 면역억제제 치료를 필요로 하는데, 이 치료는 기회 감염성 질환에 걸릴 위험이 더 높고 자궁경부 고등급 이형성증 및 암과 같은 종양 전 또는 종양성 병변의 위험과 관련이 있는 것으로 알려져 있습니다.[204][205] B형 간염, 인플루엔자, 수두, 대상포진 바이러스, 폐렴구균 폐렴 또는 인유두종 바이러스와 같은 잠재적으로 해로운 질병의 대부분은 백신으로 예방할 수 있습니다. IBD 치료에 사용되는 각 약제는 환자에게 유도된 면역억제 정도에 따라 분류되어야 합니다. 여러 지침에서는 치료를 시작하기 전에 환자의 백신 접종 상태를 조사하고 필요할 때 백신 예방 가능한 질병에 대한 백신 접종을 수행할 것을 제안합니다.[206][207] IBD의 영향을 받는 환자들은 다른 인구들에 비해 독감이나 폐렴 같은 백신 예방 가능한 질병에 걸릴 위험이 더 높은 것으로 알려져 있습니다.[208] 그럼에도 불구하고 감염 위험이 증가했음에도 불구하고 IBD 환자의 백신 접종률은 최적이 아닌 것으로 알려져 있으며 일반인의 백신 접종률보다 낮을 수도 있습니다.[209][210]
수술.
크론병은 장의 일부 또는 전체가 막힌 경우에 사용되지만 결국 재발하기 때문에 수술로 치료할 수 없습니다.[211] 또한 폐색, 누공, 농양과 같은 합병증이나 질병이 약물에 반응하지 않는 경우에도 수술이 필요할 수 있습니다. 첫 번째 수술 후, 크론병은 보통 병든 장을 제거하고 건강한 말단을 다시 결합한 부위로 돌아옵니다; 그것은 다른 장소에서도 돌아올 수 있습니다. 절제 후 흉터 조직이 쌓이게 되는데, 이로 인해 장이 너무 작아져서 배설물이 쉽게 통과하지 못할 때 생기는 협착이 발생하여 폐색이 될 수 있습니다. 첫 번째 절제 후 5년 이내에 또 다른 절제가 필요할 수 있습니다.[212] 협착으로 인해 폐쇄된 환자의 경우 두 가지 치료 방법은 협착 성형술과 장 부위 절제술입니다. 십이지장 침범의 경우 협착성형술 단독과 협착성형술 및 절제술 사이에는 통계적 유의성이 없습니다. 이들의 경우 재수술률이 각각 31%, 27%로 나타나 십이지장 침범이 있는 선별된 사람들에게 협착성형술이 안전하고 효과적인 치료법임을 알 수 있었습니다.[213]
크론병의 수술 후 재발은 비교적 흔합니다. 크론병변은 거의 항상 절제된 장 부위에서 발견됩니다. 일반적으로 대장 내시경 검사 중에 수술 후 관절(또는 문합)을 검사하고 질병 활동을 등급화할 수 있습니다. "루트게르트 점수"는 크론병의 수술 후 질병 재발에 대한 내시경 점수 체계입니다. 크론병의 가벼운 수술 후 재발은 i1 및 i2 등급, 중등도에서 중증 재발은 i3 및 i4 등급입니다.[214] 병변이 적으면 등급이 낮아집니다. 점수를 기반으로 환자에게 질병의 재발을 관리할 수 있는 최상의 기회를 제공하도록 치료 계획을 설계할 수 있습니다.[215]
짧은 장 증후군(SBS, 또한 짧은 장 증후군 또는 간단히 짧은 장 증후군)은 소장의 일부를 외과적으로 제거함으로써 발생합니다. 대개 소장의 절반 이상을 제거한 환자에게서 발병합니다.[216] 설사가 주요 증상이지만 체중 감소, 경련, 더부룩함, 속 쓰림 등이 있을 수 있습니다. 단장증후군은 식단의 변화, 정맥투여, 비타민 및 미네랄 보충제, 약물치료 등으로 치료합니다. SBS의 경우에는 장 이식 수술을 고려할 수 있습니다. 비록 이 시술을 제공하는 이식 센터의 수가 상당히 적고, 이식된 장의 감염 및 거부반응의 가능성으로 인해 높은 위험이 뒤따릅니다.[217]
담즙산 설사는 말단 회장이 제거된 크론병 수술 후 또 다른 합병증입니다. 이것은 과도한 물 설사로 이어집니다. 일반적으로 말단 회장의 절제 후 회장이 담즙산을 재흡수하지 못하기 때문으로 생각되며, 담즙산 흡수 장애의 첫 번째 유형으로 인식되었습니다.[218]
마이크로바이옴 변형
경구 프로바이오틱스 보충제를 사용하여 위장 마이크로바이옴의 구성과 행동을 수정하는 것이 크론병 환자의 관해율을 개선하는 데 도움이 될 수 있는지를 이해하기 위해 연구되었습니다. 그러나 2020년에 단 두 번의 통제된 시험만이 가능했으며, 프로바이오틱스 보충을 받는 크론병 환자에서 관해가 더 높거나 부작용이 더 낮다는 명확한 전반적인 증거는 없었습니다.[219]
정신건강
크론병은 특히 변실금으로 인해 성장이 둔화되거나 당황할 수 있는 젊은 사람들에게 불안이나 기분 장애를 초래할 수 있습니다.[220] 상담뿐만 아니라 항우울제나 항불안제를 복용하는 것도 몇몇 사람들의 관리에 도움이 될 수 있습니다.[220]
2017년[update] 현재 마음 챙김 기반 치료, 최면 치료, 인지 행동 치료 등을 살펴본 연구는 적은 편입니다.[221]
대체의학
크론병에 걸린 사람들은 보완요법이나 대체요법을 시도하는 것이 일반적입니다.[222] 여기에는 다이어트, 프로바이오틱스, 어유 및 기타 허브 및 영양 보충제가 포함됩니다.
- 침술은 중국에서 염증성 장질환을 치료하는 데 사용되며, 서구 사회에서 더 많이 사용되고 있습니다.[223] 이때 침술의 사용을 권장하기에는 근거가 부족합니다.[222]
- 2006년 독일의 한 조사에 따르면 IBD를 가진 사람들의 약 절반이 어떤 형태의 대체 의학을 사용했으며 가장 흔한 것은 동종 요법이며 프랑스의 한 연구에서는 약 30%가 대체 의학을 사용하는 것으로 나타났습니다.[224] 동종 요법 제제는 이것 또는 다른 어떤 조건으로도 입증되지 않으며 [225][226][227]대규모 연구에서 위약보다 더 효과적이지 않은 것으로 밝혀졌습니다.[228][229][230]
- 의료용 대마초가 염증성 장질환에 미치는 영향에 대해서는 상반된 연구가 있고,[231] 관리에 미치는 영향은 불확실합니다.[232]
예후
크론병은 알려진 치료법이 없는 만성 질환입니다. 증상이 호전되는 기간과 증상이 발현되는 에피소드가 특징입니다. 치료를 통해 대부분의 사람들은 건강한 체중을 달성하고 질병의 사망률은 상대적으로 낮습니다. 양성에서 매우 심한 경우까지 다양하게 나타날 수 있으며, CD를 가진 사람들은 단 한 번의 증상을 경험하거나 지속적인 증상을 보일 수 있습니다. 일부 사람들은 수년 또는 수십 년 동안 질병이 없을 수 있지만 일반적으로 재발합니다. 크론병 환자의 최대 80%가 질병 경과 중 어느 시점에 입원하며, 진단 후 첫 1년 동안 가장 높은 비율로 발생합니다.[6] 크론병을 앓고 있는 대부분의 사람들은 정상적인 수명을 삽니다.[233] 그러나 크론병은 소장암과 대장암(장암)의 위험이 약간 증가하는 것과 관련이 있습니다.[234]
역학
크론병에 걸린 사람들의 비율은 노르웨이와 미국에서 결정되었으며 6에서 7.1:100,000으로 유사합니다. 미국 크론 & 대장염 재단은 이 숫자를 약 149:100,000으로 인용하고 NIH는 100,000명당 28에서 199를 인용합니다.[235][236] 크론병은 북부 국가에서 더 흔하며, 이들 국가의 북부 지역에서는 여전히 발병률이 더 높습니다.[237] 크론병의 발병률은 유럽에서는 비슷하지만 아시아와 아프리카에서는 낮은 것으로 생각됩니다.[235] 또한 아슈케나지 유대인과[1][238] 흡연자에게서 발병률이 더 높습니다.[239]
크론병은 10~20대, 50~70대에서 가장 흔하게 시작됩니다.[1][32][21] 유아기에는 거의 진단되지 않습니다. 보통 남자보다 여자 아이들에게 더 심하게 영향을 미칩니다.[240] 하지만, 남성보다 약간 더 많은 여성만이 크론병을 가지고 있습니다.[241] 크론병에 걸린 사람의 부모, 형제자매 또는 자녀는 크론병에 걸릴 확률이 3배에서 20배까지 높습니다.[242] 쌍둥이 연구에 따르면 한 사람이 질병에 걸리면 다른 사람도 질병에 걸릴 확률이 55%입니다.[243]
크론병의 발병률은 유럽과[244] 신생 산업화 국가에서 증가하고 있습니다.[245] 예를 들어 브라질에서는 1990년 이후 매년 11%씩 크론병 발병률이 증가하고 있습니다.[245]
역사
염증성 장질환은 조반니 바티스타 모르가니(Giovanni Battista Morgagni, 1682–1771)와 1913년 스코틀랜드 의사 토마스 케네디 달지엘(Thomas Kennedy Dalziel)에 의해 기술되었습니다.[246]
말단 장염은 1904년 폴란드 외과의사 Antoni Le ś스키에 의해 처음 기술되었지만 장 결핵과 결정적으로 구별되지는 않았습니다. 폴란드에서는 여전히 레 ś노프스키-크론병(폴란드어: choroba Le ś노프스키에고-크론나)이라고 불립니다. 뉴욕의 마운트 사이나이 병원의 미국 소화기내과 의사인 버릴 버나드 크론은 1932년에 14건의 사례를 기술하고 "말기 회장염: 새로운 임상 실체"라고 설명했습니다. 그해 말, 그는 동료 레온 긴즈부르크, 고든 오펜하이머와 함께 "지역성 장염: 병리학적 및 임상적 실체"라는 사례 시리즈를 출판했습니다. 그러나, 크론의 이름이 알파벳에 우선하는 것으로 인해, 나중에 세계적인 문헌에서 크론병으로 알려지게 되었습니다.[22]
참고문헌
- ^ a b c d e f g h i j k l m n o p q r s t u v w x y z aa ab ac ad ae af ag ah Baumgart DC, Sandborn WJ (August 2012). "Crohn's disease". Lancet. 380 (9853): 1590–605. doi:10.1016/S0140-6736(12)60026-9. PMID 22914295.
- ^ "Crohn's disease". Autoimmune Registry Inc. Archived from the original on June 15, 2022. Retrieved June 15, 2022.
- ^ a b c d e f g h i "Crohn's Disease". National Institute of Diabetes and Digestive and Kidney Diseases (NIDDK). Archived from the original on December 8, 2019. Retrieved December 8, 2019.
- ^ a b c Cosnes J (June 2004). "Tobacco and IBD: relevance in the understanding of disease mechanisms and clinical practice". Best Practice & Research. Clinical Gastroenterology. 18 (3): 481–96. doi:10.1016/j.bpg.2003.12.003. PMID 15157822.
- ^ a b c "Inflammatory Bowel Disease" (PDF). World Gastroenterology Organization. August 2015. Archived from the original (PDF) on March 14, 2016. Retrieved March 13, 2016.
- ^ a b Lichtenstein GR, Loftus EV, Isaacs KL, Regueiro MD, Gerson LB, Sands BE (April 2018). "ACG Clinical Guideline: Management of Crohn's Disease in Adults". The American Journal of Gastroenterology. 113 (4): 481–517. doi:10.1038/ajg.2018.27. PMID 29610508. S2CID 4568430.
- ^ a b Molodecky NA, Soon IS, Rabi DM, Ghali WA, Ferris M, Chernoff G, Benchimol EI, Panaccione R, Ghosh S, Barkema HW, Kaplan GG (January 2012). "Increasing incidence and prevalence of the inflammatory bowel diseases with time, based on systematic review". Gastroenterology. 142 (1): 46–54.e42, quiz e30. doi:10.1053/j.gastro.2011.10.001. PMID 22001864. S2CID 206223870. Archived from the original on October 7, 2022. Retrieved October 7, 2022.
- ^ Cho JH, Brant SR (May 2011). "Recent insights into the genetics of inflammatory bowel disease". Gastroenterology. 140 (6): 1704–12. doi:10.1053/j.gastro.2011.02.046. PMC 4947143. PMID 21530736.
- ^ a b c Dessein R, Chamaillard M, Danese S (September 2008). "Innate immunity in Crohn's disease: the reverse side of the medal". Journal of Clinical Gastroenterology. 42 (Suppl 3 Pt 1): S144–7. doi:10.1097/MCG.0b013e3181662c90. PMID 18806708.
- ^ Stefanelli T, Malesci A, Repici A, Vetrano S, Danese S (May 2008). "New insights into inflammatory bowel disease pathophysiology: paving the way for novel therapeutic targets". Current Drug Targets. 9 (5): 413–8. doi:10.2174/138945008784221170. PMID 18473770.
- ^ a b Marks DJ, Rahman FZ, Sewell GW, Segal AW (February 2010). "Crohn's disease: an immune deficiency state". Clinical Reviews in Allergy & Immunology. 38 (1): 20–31. doi:10.1007/s12016-009-8133-2. PMC 4568313. PMID 19437144.
- ^ Casanova JL, Abel L (August 2009). "Revisiting Crohn's disease as a primary immunodeficiency of macrophages". The Journal of Experimental Medicine. 206 (9): 1839–43. doi:10.1084/jem.20091683. PMC 2737171. PMID 19687225.
- ^ Lalande JD, Behr MA (July 2010). "Mycobacteria in Crohn's disease: how innate immune deficiency may result in chronic inflammation". Expert Review of Clinical Immunology. 6 (4): 633–41. doi:10.1586/eci.10.29. PMID 20594136. S2CID 25402952.
- ^ Yamamoto-Furusho JK, Korzenik JR (November 2006). "Crohn's disease: innate immunodeficiency?". World Journal of Gastroenterology. 12 (42): 6751–5. doi:10.3748/wjg.v12.i42.6751. PMC 4087427. PMID 17106921.
- ^ Barrett JC, Hansoul S, Nicolae DL, Cho JH, Duerr RH, Rioux JD, et al. (August 2008). "Genome-wide association defines more than 30 distinct susceptibility loci for Crohn's disease". Nature Genetics. 40 (8): 955–62. doi:10.1038/ng.175. PMC 2574810. PMID 18587394.
- ^ Prideaux L, Kamm MA, De Cruz PP, Chan FK, Ng SC (August 2012). "Inflammatory bowel disease in Asia: a systematic review". Journal of Gastroenterology and Hepatology. 27 (8): 1266–80. doi:10.1111/j.1440-1746.2012.07150.x. PMID 22497584. S2CID 205468282.
- ^ a b Hovde Ø, Moum BA (April 2012). "Epidemiology and clinical course of Crohn's disease: results from observational studies". World Journal of Gastroenterology. 18 (15): 1723–31. doi:10.3748/wjg.v18.i15.1723. PMC 3332285. PMID 22553396.
- ^ a b Burisch J, Munkholm P (July 2013). "Inflammatory bowel disease epidemiology". Current Opinion in Gastroenterology. 29 (4): 357–62. doi:10.1097/MOG.0b013e32836229fb. PMID 23695429. S2CID 9538639.
- ^ GBD 2015 Mortality Causes of Death Collaborators (October 2016). "Global, regional, and national life expectancy, all-cause mortality, and cause-specific mortality for 249 causes of death, 1980–2015: a systematic analysis for the Global Burden of Disease Study 2015". The Lancet. 388 (10053): 1459–1544. doi:10.1016/S0140-6736(16)31012-1. PMC 5388903. PMID 27733281.
- ^ Shih, I-Lun; Lee, Tsung-Chun; Tu, Chia-Hung; Chang, Chin-Chen; Wang, Yu-Fen; Tseng, Yao-Hui; Chiu, Han-Mo; Wu, Ming-Shiang; Wang, Hsiu-Po; Shih, Tiffany Ting-Fang; Liu, Kao-Lang (December 1, 2016). "Intraobserver and interobserver agreement for identifying extraluminal manifestations of Crohn's disease with magnetic resonance enterography". Advances in Digestive Medicine. 3 (4): 174–180. doi:10.1016/j.aidm.2015.05.004. S2CID 70796090.
- ^ a b c "Crohn's Disease: Get Facts on Symptoms and Diet". eMedicineHealth. Archived from the original on October 20, 2007.
- ^ a b Crohn BB, Ginzburg L, Oppenheimer GD (May 2000). "Regional ileitis: a pathologic and clinical entity. 1932". The Mount Sinai Journal of Medicine, New York. 67 (3): 263–8. PMID 10828911.
- ^ Van Hootegem, Philippe; Travis, Simon (July 9, 2020). "Is Crohn's Disease a Rightly Used Eponym?". Journal of Crohn's and Colitis. 14 (6): 867–871. doi:10.1093/ecco-jcc/jjz183. ISSN 1873-9946. PMID 31701137.
- ^ Mulder, Daniel J.; Noble, Angela J.; Justinich, Christopher J.; Duffin, Jacalyn M. (May 2014). "A tale of two diseases: The history of inflammatory bowel disease". Journal of Crohn's and Colitis. 8 (5): 341–348. doi:10.1016/j.crohns.2013.09.009. PMID 24094598. S2CID 13714394.
- ^ Ginzburg, Leon (May 1986). "Regional enteritis: Historical perspective". Gastroenterology. 90 (5): 1310–1311. doi:10.1016/0016-5085(86)90419-1. PMID 3514360.
- ^ a b c d e f 인터넷 약se > 염증 위험 tarmsjukdom, kronisk, IBD by Robert Löfberg. 2010년 10월 번역 검색.
- ^ Hanauer SB, Sandborn W (March 2001). "Management of Crohn's disease in adults". The American Journal of Gastroenterology. 96 (3): 635–43. doi:10.1111/j.1572-0241.2001.3671_c.x (inactive August 1, 2023). PMID 11280528. S2CID 31219115.
{{cite journal}}: CS1 maint: 2023년 8월 기준 DOI 비활성화 (링크) - ^ a b Pimentel M, Chang M, Chow EJ, Tabibzadeh S, Kirit-Kiriak V, Targan SR, Lin HC (December 2000). "Identification of a prodromal period in Crohn's disease but not ulcerative colitis". The American Journal of Gastroenterology. 95 (12): 3458–62. doi:10.1111/j.1572-0241.2000.03361.x. PMID 11151877. S2CID 2764694.
- ^ National Research Council (2003). "Johne's Disease and Crohn's Disease". Diagnosis and Control of Johne's Disease. Washington, DC: National Academies Press. doi:10.17226/10625. ISBN 978-0-309-08611-0. PMID 25032299. Bookshelf ID: NBK207651. Archived from the original on September 6, 2017. Retrieved August 30, 2017.
- ^ Taylor BA, Williams GT, Hughes LE, Rhodes J (August 1989). "The histology of anal skin tags in Crohn's disease: an aid to confirmation of the diagnosis". International Journal of Colorectal Disease. 4 (3): 197–9. doi:10.1007/BF01649703. PMID 2769004. S2CID 7831833.
- ^ a b "What I need to know about Crohn's Disease". www.niddk.nih.gov. Archived from the original on November 21, 2015. Retrieved December 11, 2015.
- ^ a b c d e f 전자 의학에서 크론병
- ^ a b c Podolsky DK (August 2002). "Inflammatory bowel disease". The New England Journal of Medicine (Submitted manuscript). 347 (6): 417–29. doi:10.1056/NEJMra020831. PMID 12167685. Archived from the original on April 28, 2021. Retrieved September 4, 2018.
- ^ Mueller MH, Kreis ME, Gross ML, Becker HD, Zittel TT, Jehle EC (August 2002). "Anorectal functional disorders in the absence of anorectal inflammation in patients with Crohn's disease". The British Journal of Surgery. 89 (8): 1027–31. doi:10.1046/j.1365-2168.2002.02173.x. PMID 12153630. S2CID 42383375.
- ^ Ingle, Sachin B; Hinge, Chitra R; Dakhure, Sarita; Bhosale, Smita S (May 16, 2013). "Isolated gastric Crohn's disease". World Journal of Clinical Cases. 1 (2): 71–73. doi:10.12998/wjcc.v1.i2.71. ISSN 2307-8960. PMC 3845940. PMID 24303469.
- ^ Fix OK, Soto JA, Andrews CW, Farraye FA (December 2004). "Gastroduodenal Crohn's disease". Gastrointestinal Endoscopy. 60 (6): 985. doi:10.1016/S0016-5107(04)02200-X. PMID 15605018.
- ^ Antonelli E, Bassotti G, Tramontana M, Hansel K, Stingeni L, Ardizzone S, Genovese G, Marzano AV, Maconi G (January 2021). "Dermatological Manifestations in Inflammatory Bowel Diseases". J Clin Med. 10 (2): 364. doi:10.3390/jcm10020364. PMC 7835974. PMID 33477990.
- ^ a b Aberumand, Babak; Howard, Jessica; Howard, John (January 3, 2017). "Metastatic Crohn's Disease: An Approach to an Uncommon but Important Cutaneous Disorder". BioMed Research International. 2017: e8192150. doi:10.1155/2017/8192150. ISSN 2314-6133. PMC 5239966. PMID 28127561.
- ^ a b Beattie RM, Croft NM, Fell JM, Afzal NA, Heuschkel RB (May 2006). "Inflammatory bowel disease". Archives of Disease in Childhood. 91 (5): 426–32. doi:10.1136/adc.2005.080481. PMC 2082730. PMID 16632672.
- ^ Büller HA (February 1997). "Problems in diagnosis of IBD in children". The Netherlands Journal of Medicine (Submitted manuscript). 50 (2): S8–11. doi:10.1016/S0300-2977(96)00064-2. PMID 9050326. Archived from the original on August 28, 2021. Retrieved September 4, 2018.
- ^ O'Keefe SJ (1996). "Nutrition and gastrointestinal disease". Scandinavian Journal of Gastroenterology. Supplement. 220: 52–9. doi:10.3109/00365529609094750. PMID 8898436.
- ^ a b c Harbord M, Annese V, Vavricka SR, Allez M, Barreiro-de Acosta M, Boberg KM, et al. (March 2016). "The First European Evidence-based Consensus on Extra-intestinal Manifestations in Inflammatory Bowel Disease". Journal of Crohn's & Colitis. 10 (3): 239–54. doi:10.1093/ecco-jcc/jjv213. PMC 4957476. PMID 26614685.
- ^ Greenstein AJ, Janowitz HD, Sachar DB (September 1976). "The extra-intestinal complications of Crohn's disease and ulcerative colitis: a study of 700 patients". Medicine. 55 (5): 401–412. doi:10.1097/00005792-197609000-00004. PMID 957999.
- ^ Bernstein CN, Blanchard JF, Rawsthorne P, Yu N (April 2001). "The prevalence of extraintestinal diseases in inflammatory bowel disease: a population-based study". The American Journal of Gastroenterology. 96 (4): 1116–1122. doi:10.1111/j.1572-0241.2001.03756.x. PMID 11316157.
- ^ Harbord M, Annese V, Vavricka SR, Allez M, Barreiro-de Acosta M, Boberg KM, et al. (March 2016). "The First European Evidence-based Consensus on Extra-intestinal Manifestations in Inflammatory Bowel Disease". Journal of Crohn's & Colitis. 10 (3): 239–254. doi:10.1093/ecco-jcc/jjv213. PMID 26614685.
- ^ a b c d e f g h i j k Trikudanathan G, Venkatesh PG, Navaneethan U (December 2012). "Diagnosis and therapeutic management of extra-intestinal manifestations of inflammatory bowel disease". Drugs. 72 (18): 2333–49. doi:10.2165/11638120-000000000-00000. PMID 23181971. S2CID 10078879.
- ^ a b c d e f g h i j k l m n o p q r Jose, Folashade A.; Heyman, Melvin B. (February 2008). "Extraintestinal Manifestations of Inflammatory Bowel Disease". Journal of Pediatric Gastroenterology and Nutrition. 46 (2): 124–133. doi:10.1097/MPG.0b013e318093f4b0. ISSN 0277-2116. PMC 3245880. PMID 18223370.
- ^ Kumar V, Abbas AK, Fausto N (July 30, 2004). "The Gastrointestinal Tract". Robbins and Cotran: Pathologic Basis of Disease (7th ed.). Philadelphia, Pennsylvania: Elsevier Saunders. p. 847. ISBN 978-0-7216-0187-8.
- ^ Loos, Elke; Lemkens, Peter; Poorten, Vincent Vander; Humblet, Evelien; Laureyns, Griet (January 2019). "Laryngeal Manifestations of Inflammatory Bowel Disease". Journal of Voice. 33 (1): 1–6. doi:10.1016/j.jvoice.2017.09.021. ISSN 1873-4588. PMID 29605161. S2CID 4565046. Archived from the original on October 7, 2022. Retrieved September 6, 2021.
- ^ Hasegawa, Naoko; Ishimoto, Shin-Ichi; Takazoe, Masakazu; Tsunoda, Koichi; Fujimaki, Youko; Shiraishi, Aiko; Kinoshita, Makoto; Okada, Kazunari (July 2009). "Recurrent hoarseness due to inflammatory vocal fold lesions in a patient with Crohn's disease". The Annals of Otology, Rhinology, and Laryngology. 118 (7): 532–535. doi:10.1177/000348940911800713. ISSN 0003-4894. PMID 19708494. S2CID 8472904. Archived from the original on September 6, 2021. Retrieved September 6, 2021.
- ^ Li, Cong J.; Aronowitz, Paul (March 2013). "Sore throat, odynophagia, hoarseness, and a muffled, high-pitched voice". Cleveland Clinic Journal of Medicine. 80 (3): 144–145. doi:10.3949/ccjm.80a.12056. ISSN 0891-1150. PMID 23456463. S2CID 31002546.
- ^ Lu, De-Gan; Ji, Xiao-Qing; Liu, Xun; Li, Hong-Jia; Zhang, Cai-Qing (January 7, 2014). "Pulmonary manifestations of Crohn's disease". World Journal of Gastroenterology. 20 (1): 133–141. doi:10.3748/wjg.v20.i1.133. ISSN 1007-9327. PMC 3886002. PMID 24415866.
- ^ Bernstein M, Irwin S, Greenberg GR (September 2005). "Maintenance infliximab treatment is associated with improved bone mineral density in Crohn's disease". The American Journal of Gastroenterology. 100 (9): 2031–5. doi:10.1111/j.1572-0241.2005.50219.x. PMID 16128948. S2CID 28982700.
- ^ a b c Thrash B, Patel M, Shah KR, Boland CR, Menter A (February 2013). "Cutaneous manifestations of gastrointestinal disease: part II". Journal of the American Academy of Dermatology. 68 (2): 211.e1-33, quiz 244–6. doi:10.1016/j.jaad.2012.10.036. PMID 23317981. S2CID 1819416.
- ^ a b Roth N, Biedermann L, Fournier N, Butter M, Vavricka SR, Navarini AA, et al. (2019). "Occurrence of skin manifestations in patients of the Swiss Inflammatory Bowel Disease Cohort Study". PLOS ONE. 14 (1): e0210436. Bibcode:2019PLoSO..1410436R. doi:10.1371/journal.pone.0210436. PMC 6347222. PMID 30682031. S2CID 59275029.
- ^ a b 2007년 8월 5일 Wayback Machine에 보관된 크론병. professionals.epilepsy.com . 뇌전증 2007년 7월 13일 회수.
- ^ "Mental and Emotional Well-Being". Crohn's & Colitis Foundation. Archived from the original on October 7, 2022. Retrieved September 6, 2021.
- ^ 프라카스 E, 코스탄티노 A, 벡치 M, 부올리 M. 염증성 장질환 환자의 우울증 및 불안장애: 성별에 차이가 있습니까? 국제 환경 연구 및 공중 보건 저널. 2023; 20(13):6255. https://doi.org/10.3390/ijerph20136255
- ^ 바베리오 B, 자마니 M, 블랙 CJ, 사바리노 EV, 포드 AC. 염증성 장질환 환자의 불안 및 우울 증상 유병률: 체계적 검토 및 메타분석 랜싯 위장간질 헤파톨. 2021 May;6(5):359-370. doi: 10.1016/S2468-1253(21)00014-5
- ^ a b c Lomer MC (August 2011). "Dietary and nutritional considerations for inflammatory bowel disease". The Proceedings of the Nutrition Society. 70 (3): 329–35. doi:10.1017/S0029665111000097. PMID 21450124.
- ^ a b c Gerasimidis K, McGrogan P, Edwards CA (August 2011). "The aetiology and impact of malnutrition in paediatric inflammatory bowel disease". Journal of Human Nutrition and Dietetics (Review). 24 (4): 313–26. doi:10.1111/j.1365-277X.2011.01171.x. PMID 21564345.
- ^ MedlinePlus 백과사전: 소장세균과다증식
- ^ a b Klaus, Jochen; Spaniol, Ulrike; Adler, Guido; Mason, Richard A.; Reinshagen, Max; von Tirpitz C, Christian (July 30, 2009). "Small intestinal bacterial overgrowth mimicking acute flare as a pitfall in patients with Crohn's Disease". BMC Gastroenterology. 9 (1): 61. doi:10.1186/1471-230X-9-61. ISSN 1471-230X. PMC 2728727. PMID 19643023.
 Text was copied from this source, which is available under a Creative Commons Attribution 2.0 Generic (CC BY 2.0) Archived February 23, 2011, at the Wayback Machine license.
Text was copied from this source, which is available under a Creative Commons Attribution 2.0 Generic (CC BY 2.0) Archived February 23, 2011, at the Wayback Machine license. - ^ "Intestinal Obstruction". MERCK MANUAL Consumer Version. Archived from the original on July 10, 2016. Retrieved June 27, 2016.
- ^ "Anorectal Fistula". MERCK MANUAL Consumer Version. Archived from the original on July 10, 2016. Retrieved June 27, 2016.
- ^ "Anorectal Abscess". MERCK MANUAL Consumer Version. Archived from the original on June 14, 2016. Retrieved June 27, 2016.
- ^ e-Medicine에서 체외 누공 삽입
- ^ a b Molnár, Tamás; Tiszlavicz, László; Gyulai, Csaba; Nagy, Ferenc; Lonovics, János (May 28, 2005). "Clinical significance of granuloma in Crohn's disease". World Journal of Gastroenterology. 11 (20): 3118–3121. doi:10.3748/wjg.v11.i20.3118. ISSN 1007-9327. PMC 4305850. PMID 15918200.
- ^ Bye WA, Nguyen TM, Parker CE, Jairath V, East JE (September 2017). "Strategies for detecting colon cancer in patients with inflammatory bowel disease". The Cochrane Database of Systematic Reviews. 2017 (9): CD000279. doi:10.1002/14651858.CD000279.pub4. PMC 6483622. PMID 28922695.
- ^ Ekbom A, Helmick C, Zack M, Adami HO (August 1990). "Increased risk of large-bowel cancer in Crohn's disease with colonic involvement". Lancet. 336 (8711): 357–9. doi:10.1016/0140-6736(90)91889-I. PMID 1975343. S2CID 2046255. Archived from the original on August 5, 2020. Retrieved September 4, 2018.
- ^ Itzkowitz SH, Present DH, et al. (Crohn's and Colitis Foundation of America Colon Cancer in IBD Study Group) (March 2005). "Consensus conference: Colorectal cancer screening and surveillance in inflammatory bowel disease". Inflammatory Bowel Diseases. 11 (3): 314–21. doi:10.1097/01.mib.0000160811.76729.d5. PMID 15735438.
- ^ Zisman TL, Rubin DT (May 2008). "Colorectal cancer and dysplasia in inflammatory bowel disease". World Journal of Gastroenterology. 14 (17): 2662–9. doi:10.3748/wjg.14.2662. PMC 2709054. PMID 18461651.
- ^ Axelrad JE, Lichtiger S, Yajnik V (May 2016). "Inflammatory bowel disease and cancer: The role of inflammation, immunosuppression, and cancer treatment". World Journal of Gastroenterology (Review). 22 (20): 4794–801. doi:10.3748/wjg.v22.i20.4794. PMC 4873872. PMID 27239106.
- ^ Parakkal, Deepak; Sifuentes, Humberto; Semer, Rumi; Ehrenpreis, Eli Daniel (November 2011). "Hepatosplenic T-cell lymphoma in patients receiving TNF-α inhibitor therapy: expanding the groups at risk". European Journal of Gastroenterology & Hepatology. 23 (12): 1150–1156. doi:10.1097/MEG.0b013e32834bb90a. ISSN 1473-5687. PMID 21941193. S2CID 27267004. Archived from the original on October 3, 2021. Retrieved October 3, 2021.
- ^ Carrillo M (September 1, 1985). "Man of Many Problems Comes to City for Help". Richmond Times-Dispatch. Richmond, Virginia, USA. p. B1.
- ^ "Kay, Laura Lynn". Richmond Times-Dispatch. Richmond, Virginia, USA. April 3, 2014.
Loebenberg P (March 2, 2014). "Doris L. Johnson, 82, of Westminster". Carroll County Times. Westminster, Maryland, USA.
Berrier Jr R (December 31, 2013). "In memoriam: Dan Hodges Jr". The Roanoke Times. Roanoke, Virginia, USA.
"Cynthia Meredith Routt". Daily Press. Newport News, Virginia, USA. May 4, 2014. p. A11. - ^ Evans JP, Steinhart AH, Cohen Z, McLeod RS (2003). "Home total parenteral nutrition: an alternative to early surgery for complicated inflammatory bowel disease". Journal of Gastrointestinal Surgery. 7 (4): 562–566. doi:10.1016/S1091-255X(02)00132-4. PMID 12763417. S2CID 195305419.
- ^ Kaplan C (October 21, 2005). "IBD and Pregnancy: What You Need to Know". Crohn's and Colitis Foundation of America. Archived from the original on February 17, 2012. Retrieved November 7, 2009.
- ^ Rodrigues, Francielle Profeta; Novaes, Jane Andrea Vieira; Pinheiro, Marcela Monteiro; Martins, Paula; Cunha-Melo, José Renan (October 23, 2019). Intestinal Ostomy Complications and Care. IntechOpen. ISBN 978-1-78984-186-2. Archived from the original on October 7, 2022. Retrieved September 6, 2021.
- ^ "Definition of Autoimmunity & Autoimmune Disease - Autoimmune Disease Johns Hopkins Pathology". pathology.jhu.edu. Archived from the original on October 3, 2021. Retrieved October 3, 2021.
- ^ a b Ciccarelli, F.; Martinis, M. De; Ginaldi, L. (January 2013). "An Update on Autoinflammatory Diseases". Current Medicinal Chemistry. 21 (3): 261–269. doi:10.2174/09298673113206660303. ISSN 0929-8673. PMC 3905709. PMID 24164192.
- ^ a b c d Li, Na; Shi, Rui-Hua (January 7, 2018). "Updated review on immune factors in pathogenesis of Crohn's disease". World Journal of Gastroenterology. 24 (1): 15–22. doi:10.3748/wjg.v24.i1.15. ISSN 1007-9327. PMC 5757119. PMID 29358878.
- ^ Roggenbuck, D.; Reinhold, D.; Baumgart, D. C.; Schierack, P.; Conrad, K.; Laass, M. W. (January 1, 2016), Makowski, Gregory S. (ed.), "Chapter Two - Autoimmunity in Crohn's Disease—A Putative Stratification Factor of the Clinical Phenotype", Advances in Clinical Chemistry, Elsevier, 77: 77–101, doi:10.1016/bs.acc.2016.06.002, PMID 27717419, retrieved November 4, 2021
- ^ a b Marks, Daniel J. B.; Rahman, Farooq Z.; Sewell, Gavin W.; Segal, Anthony W. (February 2010). "Crohn's Disease: an Immune Deficiency State". Clinical Reviews in Allergy & Immunology. 38 (1): 20–31. doi:10.1007/s12016-009-8133-2. ISSN 1080-0549. PMC 4568313. PMID 19437144.
- ^ a b c Rubin DT, Ananthakrishnan AN, Siegel CA, Sauer BG, Long MD (March 2019). "ACG Clinical Guideline: Ulcerative Colitis in Adults". The American Journal of Gastroenterology. 114 (3): 384–413. doi:10.14309/ajg.0000000000000152. PMID 30840605. S2CID 73473272.
- ^ Nachimuthu S. "Crohn's disease". eMedicineHealth. Archived from the original on December 9, 2019. Retrieved December 8, 2019.
- ^ Braat H, Peppelenbosch MP, Hommes DW (August 2006). "Immunology of Crohn's disease". Annals of the New York Academy of Sciences. 1072 (1): 135–54. Bibcode:2006NYASA1072..135B. doi:10.1196/annals.1326.039. PMID 17057196. S2CID 2627465.
- ^ Henckaerts L, Figueroa C, Vermeire S, Sans M (May 2008). "The role of genetics in inflammatory bowel disease". Current Drug Targets. 9 (5): 361–8. doi:10.2174/138945008784221161. PMID 18473763.
- ^ a b Marks DJ, Harbord MW, MacAllister R, Rahman FZ, Young J, Al-Lazikani B, Lees W, Novelli M, Bloom S, Segal AW (February 2006). "Defective acute inflammation in Crohn's disease: a clinical investigation". Lancet. 367 (9511): 668–78. doi:10.1016/S0140-6736(06)68265-2. PMID 16503465. S2CID 13898663.
- ^ Comalada M, Peppelenbosch MP (September 2006). "Impaired innate immunity in Crohn's disease". Trends in Molecular Medicine. 12 (9): 397–9. doi:10.1016/j.molmed.2006.07.005. PMID 16890491.
- ^ Nakagome S, Mano S, Kozlowski L, Bujnicki JM, Shibata H, Fukumaki Y, et al. (June 2012). "Crohn's disease risk alleles on the NOD2 locus have been maintained by natural selection on standing variation". Molecular Biology and Evolution. 29 (6): 1569–85. doi:10.1093/molbev/mss006. PMC 3697811. PMID 22319155.
- ^ "Crohn's disease has strong genetic link: study". Crohn's and Colitis Foundation of America. April 16, 2007. Archived from the original on May 2, 2007. Retrieved November 7, 2009.
- ^ Liu JZ, Anderson CA (June 2014). "Genetic studies of Crohn's disease: past, present and future". Best Practice & Research. Clinical Gastroenterology. 28 (3): 373–86. doi:10.1016/j.bpg.2014.04.009. PMC 4075408. PMID 24913378.
- ^ Ogura Y, Bonen DK, Inohara N, Nicolae DL, Chen FF, Ramos R, et al. (May 2001). "A frameshift mutation in NOD2 associated with susceptibility to Crohn's disease". Nature. 411 (6837): 603–6. Bibcode:2001Natur.411..603O. doi:10.1038/35079114. hdl:2027.42/62856. PMID 11385577. S2CID 205017657.
- ^ Cuthbert AP, Fisher SA, Mirza MM, King K, Hampe J, Croucher PJ, et al. (April 2002). "The contribution of NOD2 gene mutations to the risk and site of disease in inflammatory bowel disease". Gastroenterology. 122 (4): 867–74. doi:10.1053/gast.2002.32415. PMID 11910337.
- ^ Kaser A, Lee AH, Franke A, Glickman JN, Zeissig S, Tilg H, et al. (September 2008). "XBP1 links ER stress to intestinal inflammation and confers genetic risk for human inflammatory bowel disease". Cell. 134 (5): 743–56. doi:10.1016/j.cell.2008.07.021. PMC 2586148. PMID 18775308.
- ^ Clevers H (February 2009). "Inflammatory bowel disease, stress, and the endoplasmic reticulum". The New England Journal of Medicine. 360 (7): 726–7. doi:10.1056/NEJMcibr0809591. PMID 19213688.
- ^ Vermeire S (June 2004). "NOD2/CARD15: relevance in clinical practice". Best Practice & Research. Clinical Gastroenterology (Review). 18 (3): 569–75. doi:10.1016/j.bpg.2003.12.008. PMID 15157828.
- ^ a b Prescott NJ, Fisher SA, Franke A, Hampe J, Onnie CM, Soars D, et al. (May 2007). "A nonsynonymous SNP in ATG16L1 predisposes to ileal Crohn's disease and is independent of CARD15 and IBD5". Gastroenterology. 132 (5): 1665–71. doi:10.1053/j.gastro.2007.03.034. PMID 17484864.
- ^ Diegelmann J, Czamara D, Le Bras E, Zimmermann E, Olszak T, Bedynek A, et al. (2013). "Intestinal DMBT1 expression is modulated by Crohn's disease-associated IL23R variants and by a DMBT1 variant which influences binding of the transcription factors CREB1 and ATF-2". PLOS ONE. 8 (11): e77773. Bibcode:2013PLoSO...877773D. doi:10.1371/journal.pone.0077773. PMC 3818382. PMID 24223725.
- ^ Prescott NJ, Dominy KM, Kubo M, Lewis CM, Fisher SA, Redon R, et al. (May 2010). "Independent and population-specific association of risk variants at the IRGM locus with Crohn's disease". Human Molecular Genetics. 19 (9): 1828–39. doi:10.1093/hmg/ddq041. PMC 2850616. PMID 20106866.
- ^ Chermesh I, Azriel A, Alter-Koltunoff M, Eliakim R, Karban A, Levi BZ (July 2007). "Crohn's disease and SLC11A1 promoter polymorphism". Digestive Diseases and Sciences. 52 (7): 1632–5. doi:10.1007/s10620-006-9682-3. PMID 17385031. S2CID 11429585.
- ^ Jostins L, Ripke S, Weersma RK, Duerr RH, McGovern DP, Hui KY, et al. (November 2012). "Host-microbe interactions have shaped the genetic architecture of inflammatory bowel disease". Nature. 491 (7422): 119–24. Bibcode:2012Natur.491..119.. doi:10.1038/nature11582. PMC 3491803. PMID 23128233.
- ^ Walker MM, Murray JA (August 2011). "An update in the diagnosis of coeliac disease". Histopathology (Review). 59 (2): 166–79. doi:10.1111/j.1365-2559.2010.03680.x. PMID 21054494. S2CID 5196629.
Recent genome-wide association studies have shown that chronic inflammatory and autoimmune diseases are linked genetically to coeliac disease; for example, type 1 diabetes mellitus, Grave's disease and Crohn's disease.
- ^ Coghlan A (January 10, 2018). "A single gene can either raise or lower Crohn's disease risk". New Scientist. Archived from the original on November 9, 2020. Retrieved November 5, 2020.
- ^ Marks DJ, Segal AW (January 2008). "Innate immunity in inflammatory bowel disease: a disease hypothesis". The Journal of Pathology. 214 (2): 260–6. doi:10.1002/path.2291. PMC 2635948. PMID 18161747.
- ^ Cobrin GM, Abreu MT (August 2005). "Defects in mucosal immunity leading to Crohn's disease". Immunological Reviews. 206 (1): 277–95. doi:10.1111/j.0105-2896.2005.00293.x. PMID 16048555. S2CID 37353838.
- ^ Elson CO, Cong Y, Weaver CT, Schoeb TR, McClanahan TK, Fick RB, Kastelein RA (June 2007). "Monoclonal anti-interleukin 23 reverses active colitis in a T cell-mediated model in mice". Gastroenterology. 132 (7): 2359–70. doi:10.1053/j.gastro.2007.03.104. PMID 17570211.
- ^ Velasquez-Manoff M (June 29, 2008). "The Worm Turns". The New York Times. Archived from the original on January 7, 2017.
- ^ Sartor RB (July 2006). "Mechanisms of disease: pathogenesis of Crohn's disease and ulcerative colitis". Nature Clinical Practice. Gastroenterology & Hepatology. 3 (7): 390–407. doi:10.1038/ncpgasthep0528. PMID 16819502. S2CID 3329677.
- ^ Dogan B, Scherl E, Bosworth B, Yantiss R, Altier C, McDonough PL, Jiang ZD, Dupont HL, Garneau P, Harel J, Rishniw M, Simpson KW (January 2013). "Multidrug resistance is common in Escherichia coli associated with ileal Crohn's disease". Inflammatory Bowel Diseases. 19 (1): 141–50. doi:10.1002/ibd.22971. PMID 22508665. S2CID 25518704.
- ^ Subramanian S, Roberts CL, Hart CA, Martin HM, Edwards SW, Rhodes JM, Campbell BJ (February 2008). "Replication of Colonic Crohn's Disease Mucosal Escherichia coli Isolates within Macrophages and Their Susceptibility to Antibiotics". Antimicrobial Agents and Chemotherapy. 52 (2): 427–34. doi:10.1128/AAC.00375-07. PMC 2224732. PMID 18070962.
- ^ Mpofu CM, Campbell BJ, Subramanian S, Marshall-Clarke S, Hart CA, Cross A, Roberts CL, McGoldrick A, Edwards SW, Rhodes JM (November 2007). "Microbial mannan inhibits bacterial killing by macrophages: a possible pathogenic mechanism for Crohn's disease" (PDF). Gastroenterology. 133 (5): 1487–98. doi:10.1053/j.gastro.2007.08.004. PMID 17919633.
- ^ Naser SA, Collins MT (December 2005). "Debate on the lack of evidence of Mycobacterium avium subsp. paratuberculosis in Crohn's disease". Inflammatory Bowel Diseases. 11 (12): 1123. doi:10.1097/01.MIB.0000191609.20713.ea. PMID 16306778.
- ^ Naser SA, Sagramsingh SR, Naser AS, Thanigachalam S (June 2014). "Mycobacterium avium subspecies paratuberculosis causes Crohn's disease in some inflammatory bowel disease patients". World Journal of Gastroenterology. 20 (23): 7403–15. doi:10.3748/wjg.v20.i23.7403. PMC 4064085. PMID 24966610.
- ^ "New insights into Crohn's Disease". Archived from the original on September 23, 2013.
- ^ Glubb DM, Gearry RB, Barclay ML, Roberts RL, Pearson J, Keenan JI, et al. (June 2011). "NOD2 and ATG16L1 polymorphisms affect monocyte responses in Crohn's disease". World Journal of Gastroenterology. 17 (23): 2829–37. doi:10.3748/wjg.v17.i23.2829 (inactive August 1, 2023). PMC 3120942. PMID 21734790.
{{cite journal}}: CS1 maint: 2023년 8월 기준 DOI 비활성화 (링크) - ^ Clancy R, Ren Z, Turton J, Pang G, Wettstein A (May 2007). "Molecular evidence for Mycobacterium avium subspecies paratuberculosis (MAP) in Crohn's disease correlates with enhanced TNF-alpha secretion". Digestive and Liver Disease. 39 (5): 445–51. doi:10.1016/j.dld.2006.12.006. PMID 17317344.
- ^ Nakase H, Tamaki H, Matsuura M, Chiba T, Okazaki K (November 2011). "Involvement of mycobacterium avium subspecies paratuberculosis in TNF-α production from macrophage: possible link between MAP and immune response in Crohn's disease". Inflammatory Bowel Diseases. 17 (11): E140–2. doi:10.1002/ibd.21750. PMID 21990211.
- ^ a b Baumgart M, Dogan B, Rishniw M, Weitzman G, Bosworth B, Yantiss R, et al. (September 2007). "Culture independent analysis of ileal mucosa reveals a selective increase in invasive Escherichia coli of novel phylogeny relative to depletion of Clostridiales in Crohn's disease involving the ileum". The ISME Journal. 1 (5): 403–18. Bibcode:2007ISMEJ...1..403B. doi:10.1038/ismej.2007.52. PMID 18043660.
- ^ Sasaki M, Sitaraman SV, Babbin BA, Gerner-Smidt P, Ribot EM, Garrett N, Alpern JA, Akyildiz A, Theiss AL, Nusrat A, Klapproth JM (October 2007). "Invasive Escherichia coli are a feature of Crohn's disease". Laboratory Investigation; A Journal of Technical Methods and Pathology. 87 (10): 1042–54. doi:10.1038/labinvest.3700661. PMID 17660846.
- ^ Darfeuille-Michaud A, Boudeau J, Bulois P, Neut C, Glasser AL, Barnich N, Bringer MA, Swidsinski A, Beaugerie L, Colombel JF (August 2004). "High prevalence of adherent-invasive Escherichia coli associated with ileal mucosa in Crohn's disease". Gastroenterology. 127 (2): 412–21. doi:10.1053/j.gastro.2004.04.061. PMID 15300573.
- ^ Nickerson KP, McDonald C (2012). Mizoguchi E (ed.). "Crohn's disease-associated adherent-invasive Escherichia coli adhesion is enhanced by exposure to the ubiquitous dietary polysaccharide maltodextrin". PLOS ONE. 7 (12): e52132. Bibcode:2012PLoSO...752132N. doi:10.1371/journal.pone.0052132. PMC 3520894. PMID 23251695.
- ^ Martinez-Medina M, Naves P, Blanco J, Aldeguer X, Blanco JE, Blanco M, Ponte C, Soriano F, Darfeuille-Michaud A, Garcia-Gil LJ (September 2009). "Biofilm formation as a novel phenotypic feature of adherent-invasive Escherichia coli (AIEC)". BMC Microbiology. 9 (1): 202. doi:10.1186/1471-2180-9-202. PMC 2759958. PMID 19772580.
- ^ Chargui A, Cesaro A, Mimouna S, Fareh M, Brest P, Naquet P, Darfeuille-Michaud A, Hébuterne X, Mograbi B, Vouret-Craviari V, Hofman P (2012). "Subversion of autophagy in adherent invasive Escherichia coli-infected neutrophils induces inflammation and cell death". PLOS ONE. 7 (12): e51727. Bibcode:2012PLoSO...751727C. doi:10.1371/journal.pone.0051727. PMC 3522719. PMID 23272151.
- ^ Craven M, Egan CE, Dowd SE, McDonough SP, Dogan B, Denkers EY, Bowman D, Scherl EJ, Simpson KW (2012). "Inflammation drives dysbiosis and bacterial invasion in murine models of ileal Crohn's disease". PLOS ONE. 7 (7): e41594. Bibcode:2012PLoSO...741594C. doi:10.1371/journal.pone.0041594. PMC 3404971. PMID 22848538.
- ^ Barnich N, Darfeuille-Michaud A (January 2007). "Adherent-invasive Escherichia coli and Crohn's disease". Current Opinion in Gastroenterology. 23 (1): 16–20. doi:10.1097/MOG.0b013e3280105a38. PMID 17133079. S2CID 23564986.
- ^ Cenac N, Andrews CN, Holzhausen M, Chapman K, Cottrell G, Andrade-Gordon P, Steinhoff M, Barbara G, Beck P, Bunnett NW, Sharkey KA, Ferraz JG, Shaffer E, Vergnolle N (March 2007). "Role for protease activity in visceral pain in irritable bowel syndrome". The Journal of Clinical Investigation. 117 (3): 636–47. doi:10.1172/JCI29255. PMC 1794118. PMID 17304351.
- ^ Cenac N, Coelho AM, Nguyen C, Compton S, Andrade-Gordon P, MacNaughton WK, Wallace JL, Hollenberg MD, Bunnett NW, Garcia-Villar R, Bueno L, Vergnolle N (November 2002). "Induction of intestinal inflammation in mouse by activation of proteinase-activated receptor-2". The American Journal of Pathology. 161 (5): 1903–15. doi:10.1016/S0002-9440(10)64466-5. PMC 1850779. PMID 12414536.
- ^ Boorom KF, Smith H, Nimri L, Viscogliosi E, Spanakos G, Parkar U, Li LH, Zhou XN, Ok UZ, Leelayoova S, Jones MS (October 2008). "Oh my aching gut: irritable bowel syndrome, Blastocystis, and asymptomatic infection". Parasites & Vectors. 1 (1): 40. doi:10.1186/1756-3305-1-40. PMC 2627840. PMID 18937874.
- ^ Hugot JP, Alberti C, Berrebi D, Bingen E, Cézard JP (December 2003). "Crohn's disease: the cold chain hypothesis". Lancet. 362 (9400): 2012–5. doi:10.1016/S0140-6736(03)15024-6. PMID 14683664. S2CID 10254395.
- ^ "Fridges blamed for Crohn's disease rise". Medical News Today. December 12, 2003. Archived from the original on January 3, 2009.
- ^ Forbes A, Kalantzis T (July 2006). "Crohn's disease: the cold chain hypothesis". International Journal of Colorectal Disease. 21 (5): 399–401. doi:10.1007/s00384-005-0003-7. PMID 16059694. S2CID 13271176.
- ^ Kumamoto CA (August 2011). "Inflammation and gastrointestinal Candida colonization". Current Opinion in Microbiology. 14 (4): 386–91. doi:10.1016/j.mib.2011.07.015. PMC 3163673. PMID 21802979.
- ^ "Possible links between Crohn's disease and Paratuberculosis" (PDF). European Commission Directorate-General Health & Consumer Protection. Archived from the original (PDF) on December 17, 2008. Retrieved November 7, 2009.
- ^ Gui GP, Thomas PR, Tizard ML, Lake J, Sanderson JD, Hermon-Taylor J (March 1997). "Two-year-outcomes analysis of Crohn's disease treated with rifabutin and macrolide antibiotics". The Journal of Antimicrobial Chemotherapy. 39 (3): 393–400. doi:10.1093/jac/39.3.393. PMID 9096189.
- ^ a b Shoda R, Matsueda K, Yamato S, Umeda N (May 1996). "Epidemiologic analysis of Crohn disease in Japan: increased dietary intake of n-6 polyunsaturated fatty acids and animal protein relates to the increased incidence of Crohn disease in Japan". The American Journal of Clinical Nutrition. 63 (5): 741–5. doi:10.1093/ajcn/63.5.741. PMID 8615358.
- ^ Lesko SM, Kaufman DW, Rosenberg L, Helmrich SP, Miller DR, Stolley PD, Shapiro S (November 1985). "Evidence for an increased risk of Crohn's disease in oral contraceptive users". Gastroenterology. 89 (5): 1046–9. doi:10.1016/0016-5085(85)90207-0. PMID 4043662.
- ^ Reddy D, Siegel CA, Sands BE, Kane S (July 2006). "Possible association between isotretinoin and inflammatory bowel disease". The American Journal of Gastroenterology. 101 (7): 1569–73. doi:10.1111/j.1572-0241.2006.00632.x. PMID 16863562. S2CID 27663573.
- ^ Borobio E, Arín A, Valcayo A, Iñarrairaegui M, Nantes O, Prieto C (2004). "[Isotretinoin and ulcerous colitis]". Anales del Sistema Sanitario de Navarra (in Spanish). 27 (2): 241–3. doi:10.4321/S1137-66272004000300009. PMID 15381956.
- ^ Reniers DE, Howard JM (October 2001). "Isotretinoin-induced inflammatory bowel disease in an adolescent". The Annals of Pharmacotherapy. 35 (10): 1214–6. doi:10.1345/aph.10368. PMID 11675849. S2CID 22216642. Archived from the original on June 29, 2012. Retrieved November 1, 2010.
- ^ Segerstrom, Suzanne C.; Miller, Gregory E. (July 2004). "Psychological Stress and the Human Immune System: A Meta-Analytic Study of 30 Years of Inquiry". Psychological Bulletin. 130 (4): 601–630. doi:10.1037/0033-2909.130.4.601. ISSN 0033-2909. PMC 1361287. PMID 15250815.
- ^ Lomer MC, Hutchinson C, Volkert S, Greenfield SM, Catterall A, Thompson RP, Powell JJ (December 2004). "Dietary sources of inorganic microparticles and their intake in healthy subjects and patients with Crohn's disease". The British Journal of Nutrition. 92 (6): 947–55. doi:10.1079/bjn20041276. PMID 15613257.
- ^ Powell JJ, Thoree V, Pele LC (October 2007). "Dietary microparticles and their impact on tolerance and immune responsiveness of the gastrointestinal tract". The British Journal of Nutrition. 98 (Suppl 1): S59–63. doi:10.1017/S0007114507832922. PMC 2737314. PMID 17922962.
- ^ Lee TW, Russell L, Deng M, Gibson PR (August 2013). "Association of doxycycline use with the development of gastroenteritis, irritable bowel syndrome and inflammatory bowel disease in Australians deployed abroad". Internal Medicine Journal. 43 (8): 919–26. doi:10.1111/imj.12179. PMID 23656210. S2CID 9418654.
- ^ a b Margolis DJ, Fanelli M, Hoffstad O, Lewis JD (December 2010). "Potential association between the oral tetracycline class of antimicrobials used to treat acne and inflammatory bowel disease". The American Journal of Gastroenterology. 105 (12): 2610–6. doi:10.1038/ajg.2010.303. PMID 20700115. S2CID 20085592.
- ^ Garrett JP, Margolis DJ (March 2012). "Impact of Long-Term Antibiotic Use for Acne on Bacterial Ecology and Health Outcomes: A Review of Observational Studies". Current Dermatology Reports. 1 (1): 23–28. doi:10.1007/s13671-011-0001-7.
- ^ Elson CO, Cong Y, Weaver CT, Schoeb TR, McClanahan TK, Fick RB, Kastelein RA (2007). "Monoclonal anti-interleukin 23 reverses active colitis in a T cell-mediated model in mice". Gastroenterology. 132 (7): 2359–70. doi:10.1053/j.gastro.2007.03.104. PMID 17570211.
- ^ 크로포드 JM "위장관 17장" 코트란 RS에서, 쿠마르 V, 로빈스 SL 로빈스 질병의 병리학적 기초: 5판. W.B. 손더스 앤 컴퍼니, 필라델피아, 1994.
- ^ Zhang T, DeSimone RA, Jiao X, Rohlf FJ, Zhu W, Gong QQ, et al. (June 13, 2012). "Host genes related to paneth cells and xenobiotic metabolism are associated with shifts in human ileum-associated microbial composition". PLOS ONE. 7 (6): e30044. Bibcode:2012PLoSO...730044Z. doi:10.1371/journal.pone.0030044. PMC 3374611. PMID 22719822.
- ^ HCP: Pill Cam, 캡슐 내시경, 식도 내시경, 2008년 6월 16일 Wayback Machine에서 보관
- ^ Scheinfeld NS, Teplitz E, McClain SA (November 2001). "Crohn's disease and lichen nitidus: a case report and comparison of common histopathologic features". Inflammatory Bowel Diseases. 7 (4): 314–8. doi:10.1097/00054725-200111000-00006. PMID 11720321. S2CID 35892792.
- ^ Tan WC, Allan RN (October 1993). "Diffuse jejunoileitis of Crohn's disease". Gut. 34 (10): 1374–8. doi:10.1136/gut.34.10.1374. PMC 1374544. PMID 8244104.
- ^ a b Gasche C, Scholmerich J, Brynskov J, D'Haens G, Hanauer SB, Irvine EJ, Jewell DP, Rachmilewitz D, Sachar DB, Sandborn WJ, Sutherland LR (February 2000). "A simple classification of Crohn's disease: report of the Working Party for the World Congresses of Gastroenterology, Vienna 1998". Inflammatory Bowel Diseases. 6 (1): 8–15. doi:10.1002/ibd.3780060103. PMID 10701144.
- ^ Dubinsky MC, Fleshner PP (June 2003). "Treatment of Crohn's Disease of Inflammatory, Stenotic, and Fistulizing Phenotypes". Current Treatment Options in Gastroenterology. 6 (3): 183–200. doi:10.1007/s11938-003-0001-1. PMID 12744819. S2CID 21302609.
- ^ a b Hara AK, Leighton JA, Heigh RI, Sharma VK, Silva AC, De Petris G, Hentz JG, Fleischer DE (January 2006). "Crohn disease of the small bowel: preliminary comparison among CT enterography, capsule endoscopy, small-bowel follow-through, and ileoscopy". Radiology. 238 (1): 128–34. doi:10.1148/radiol.2381050296. PMID 16373764.
- ^ Triester SL, Leighton JA, Leontiadis GI, Gurudu SR, Fleischer DE, Hara AK, Heigh RI, Shiff AD, Sharma VK (May 2006). "A meta-analysis of the yield of capsule endoscopy compared to other diagnostic modalities in patients with non-stricturing small bowel Crohn's disease". The American Journal of Gastroenterology. 101 (5): 954–64. doi:10.1111/j.1572-0241.2006.00506.x. PMID 16696781. S2CID 25684863.
- ^ Dixon PM, Roulston ME, Nolan DJ (January 1993). "The small bowel enema: a ten year review". Clinical Radiology. 47 (1): 46–8. doi:10.1016/S0009-9260(05)81213-9. PMID 8428417.
- ^ Carucci LR, Levine MS (March 2002). "Radiographic imaging of inflammatory bowel disease". Gastroenterology Clinics of North America. 31 (1): 93–117, ix. doi:10.1016/S0889-8553(01)00007-3. PMID 12122746.
- ^ Rajesh A, Maglinte DD (January 2006). "Multislice CT enteroclysis: technique and clinical applications". Clinical Radiology. 61 (1): 31–9. doi:10.1016/j.crad.2005.08.006. PMID 16356814.
- ^ Zissin R, Hertz M, Osadchy A, Novis B, Gayer G (February 2005). "Computed tomographic findings of abdominal complications of Crohn's disease--pictorial essay". Canadian Association of Radiologists Journal. 56 (1): 25–35. PMID 15835588. Archived from the original on October 7, 2022. Retrieved May 18, 2022.
- ^ Mackalski BA, Bernstein CN (May 2006). "New diagnostic imaging tools for inflammatory bowel disease". Gut. 55 (5): 733–41. doi:10.1136/gut.2005.076612. PMC 1856109. PMID 16609136.
- ^ Sinha R, Rajiah P, Murphy P, Hawker P, Sanders S (October 2009). "Utility of high-resolution MR imaging in demonstrating transmural pathologic changes in Crohn disease". Radiographics. 29 (6): 1847–67. doi:10.1148/rg.296095503. PMID 19959525.
- ^ Sinha R, Rajiah P, Ramachandran I, Sanders S, Murphy PD (May 2013). "Diffusion-weighted MR imaging of the gastrointestinal tract: technique, indications, and imaging findings". Radiographics. 33 (3): 655–76, discussion 676–80. doi:10.1148/rg.333125042. PMID 23674768.
- ^ Goh J, O'Morain CA (February 2003). "Review article: nutrition and adult inflammatory bowel disease". Alimentary Pharmacology & Therapeutics. 17 (3): 307–20. doi:10.1046/j.1365-2036.2003.01482.x. PMID 12562443. S2CID 72099458.
- ^ Chamouard P, Richert Z, Meyer N, Rahmi G, Baumann R (July 2006). "Diagnostic value of C-reactive protein for predicting activity level of Crohn's disease". Clinical Gastroenterology and Hepatology. 4 (7): 882–7. doi:10.1016/j.cgh.2006.02.003. PMID 16630759.
- ^ Kaila B, Orr K, Bernstein CN (December 2005). "The anti-Saccharomyces cerevisiae antibody assay in a province-wide practice: accurate in identifying cases of Crohn's disease and predicting inflammatory disease". Canadian Journal of Gastroenterology. 19 (12): 717–21. doi:10.1155/2005/147681. PMID 16341311.
- ^ Israeli E, Grotto I, Gilburd B, Balicer RD, Goldin E, Wiik A, Shoenfeld Y (September 2005). "Anti-Saccharomyces cerevisiae and antineutrophil cytoplasmic antibodies as predictors of inflammatory bowel disease". Gut. 54 (9): 1232–6. doi:10.1136/gut.2004.060228. PMC 1774672. PMID 16099791.
- ^ Ferrante M, Henckaerts L, Joossens M, Pierik M, Joossens S, Dotan N, Norman GL, Altstock RT, Van Steen K, Rutgeerts P, Van Assche G, Vermeire S (October 2007). "New serological markers in inflammatory bowel disease are associated with complicated disease behaviour". Gut. 56 (10): 1394–403. doi:10.1136/gut.2006.108043. PMC 2000264. PMID 17456509.
- ^ Papp M, Altorjay I, Dotan N, Palatka K, Foldi I, Tumpek J, et al. (March 2008). "New serological markers for inflammatory bowel disease are associated with earlier age at onset, complicated disease behavior, risk for surgery, and NOD2/CARD15 genotype in a Hungarian IBD cohort". The American Journal of Gastroenterology. 103 (3): 665–81. doi:10.1111/j.1572-0241.2007.01652.x. PMID 18047543. S2CID 6015339.
- ^ Seow CH, Stempak JM, Xu W, Lan H, Griffiths AM, Greenberg GR, Steinhart AH, Dotan N, Silverberg MS (June 2009). "Novel anti-glycan antibodies related to inflammatory bowel disease diagnosis and phenotype". The American Journal of Gastroenterology. 104 (6): 1426–34. doi:10.1038/ajg.2009.79. PMID 19491856. S2CID 25021606.
- ^ Dotan I (December 2007). "Serologic markers in inflammatory bowel disease: tools for better diagnosis and disease stratification". Expert Review of Gastroenterology & Hepatology. 1 (2): 265–74. doi:10.1586/17474124.1.2.265. PMID 19072419. S2CID 32035337.
- ^ a b Del Pinto R, Pietropaoli D, Chandar AK, Ferri C, Cominelli F (November 2015). "Association Between Inflammatory Bowel Disease and Vitamin D Deficiency: A Systematic Review and Meta-analysis". Inflammatory Bowel Diseases. 21 (11): 2708–17. doi:10.1097/MIB.0000000000000546. PMC 4615394. PMID 26348447.
- ^ a b c d Hanauer SB, Sandborn W (March 2001). "Management of Crohn's disease in adults". The American Journal of Gastroenterology. 96 (3): 635–43. doi:10.1111/j.1572-0241.2001.3671_c.x (inactive August 1, 2023). PMID 11280528. S2CID 31219115.
{{cite journal}}: CS1 maint: 2023년 8월 기준 DOI 비활성화 (링크) - ^ Broomé U, Bergquist A (February 2006). "Primary sclerosing cholangitis, inflammatory bowel disease, and colon cancer". Seminars in Liver Disease. 26 (1): 31–41. doi:10.1055/s-2006-933561. PMID 16496231.
- ^ Baumgart DC, Sandborn WJ (May 2007). "Inflammatory bowel disease: clinical aspects and established and evolving therapies". Lancet. 369 (9573): 1641–57. doi:10.1016/S0140-6736(07)60751-X. PMID 17499606. S2CID 35264387.
- ^ Shepherd NA (August 2002). "Granulomas in the diagnosis of intestinal Crohn's disease: a myth exploded?". Histopathology. 41 (2): 166–8. doi:10.1046/j.1365-2559.2002.01441.x. PMID 12147095. S2CID 36907992.
- ^ Mahadeva U, Martin JP, Patel NK, Price AB (July 2002). "Granulomatous ulcerative colitis: a re-appraisal of the mucosal granuloma in the distinction of Crohn's disease from ulcerative colitis". Histopathology. 41 (1): 50–5. doi:10.1046/j.1365-2559.2002.01416.x. PMID 12121237. S2CID 29476514.
- ^ DeRoche TC, Xiao SY, Liu X (August 2014). "Histological evaluation in ulcerative colitis". Gastroenterology Report. 2 (3): 178–92. doi:10.1093/gastro/gou031. PMC 4124271. PMID 24942757.
- ^ Lewis NR, Scott BB (July 2006). "Systematic review: the use of serology to exclude or diagnose coeliac disease (a comparison of the endomysial and tissue transglutaminase antibody tests)". Alimentary Pharmacology & Therapeutics (Review). 24 (1): 47–54. doi:10.1111/j.1365-2036.2006.02967.x. PMID 16803602. S2CID 16823218.
Both the endomysial antibody and tissue transglutaminase antibody have very high sensitivities (93% for both) and specificities (>99% and >98% respectively) for the diagnosis of typical coeliac disease with villous atrophy. (...) As the detection of at least partial villous atrophy was used to make a diagnosis of coeliac disease in the vast majority of studies, we can't assume that the same LRs apply to coeliac patients with lesser abnormality such as an increase in intraepithelial lymphocytes or electron-microscopic changes only. In fact, if such lesser abnormalities were used as criteria for diagnosing (and excluding) coeliac disease, the sensitivity of the tests could be lower (i.e. more false negatives), especially since a number of studies suggest that the EMA and tTG antibody tests are less sensitive with lesser degrees of mucosal abnormality
- ^ Rodrigo L, Garrote JA, Vivas S (September 2008). "[Celiac disease]". Medicina Clinica (Review) (in Spanish). 131 (7): 264–70. doi:10.1016/S0025-7753(08)72247-4. PMID 18775218. Archived from the original on March 19, 2016. Retrieved March 13, 2016.
Estos marcadores presentan en general una elevada sensibilidad y especificidad (cercanas al 90%) en presencia de atrofia marcada de las vellosidades intestinales. Sin embargo, muestran una notable disminución de la sensibilidad (del orden del 40-50%) en casos con atrofia vellositaria leve o cambios mínimos. These markers generally have high sensitivity and specificity (around 90%) in the presence of marked atrophy of the villi. However, they show a marked decrease in sensitivity (of the order of 40-50%) in cases with mild villous atrophy or minimal changes.
- ^ Rostami Nejad M, Hogg-Kollars S, Ishaq S, Rostami K (2011). "Subclinical celiac disease and gluten sensitivity". Gastroenterology and Hepatology from Bed to Bench (Review). 4 (3): 102–8. PMC 4017418. PMID 24834166.
- ^ Bold J, Rostami K (2011). "Gluten tolerance; potential challenges in treatment strategies". Gastroenterology and Hepatology from Bed to Bench (Review). 4 (2): 53–7. PMC 4017406. PMID 24834157.
- ^ a b Agabegi ED, Agabegi SS (2008). "Inflammatory bowel disease (IBD)". Step-Up to Medicine (Step-Up Series). Hagerstwon, MD: Lippincott Williams & Wilkins. pp. 152–156. ISBN 0-7817-7153-6.
- ^ Feller M, Huwiler K, Schoepfer A, Shang A, Furrer H, Egger M (February 2010). "Long-term antibiotic treatment for Crohn's disease: systematic review and meta-analysis of placebo-controlled trials". Clinical Infectious Diseases. 50 (4): 473–80. doi:10.1086/649923. PMID 20067425.
- ^ Prantera C, Scribano ML (July 2009). "Antibiotics and probiotics in inflammatory bowel disease: why, when, and how". Current Opinion in Gastroenterology. 25 (4): 329–33. doi:10.1097/MOG.0b013e32832b20bf. PMID 19444096.
- ^ a b c Fries WS, Nazario B (May 16, 2007). "Crohn's Disease: 54 Tips to Help You Manage". WebMD. Archived from the original on February 8, 2008. Retrieved February 14, 2008.
- ^ 론코로니L, 고리R, 엘리L, 톤티니GE, 도네다L, 노르사L, 쿠오모M, 롬바르도V, 스크리치올로A, 카프리올리F, 코스탄티노A, 스카라멜라L, 벡치M. 염증성 장질환 환자의 영양상태: 내러티브 리뷰 영양소 2022년 2월 10일 14(4):751
- ^ 아난타크리쉬난 AN, 카플란 GG, 번스타인 CN, 버크 KE, 록헤드 PJ, 새슨 AN, 아그라왈 M, 티옹 JHT, 스타인버그 J, 크루이스 W, 스타인부르즈 F, 아후자 V, Ng SC, 루빈 DT, 콜롬벨 JF, 기어리 R; 염증성 장 질환 연구를 위한 국제 기구. 염증성 장질환 환자 관리를 위한 생활습관, 행동, 환경의 변화: 국제 염증성 장질환 연구기구 합의 랜싯 위장간질 헤파톨. 2022 Apr 26:S2468-1253(22)00021-8.
- ^ Hou JK, Abraham B, El-Serag H (April 2011). "Dietary intake and risk of developing inflammatory bowel disease: a systematic review of the literature". The American Journal of Gastroenterology. 106 (4): 563–73. doi:10.1038/ajg.2011.44. PMID 21468064. S2CID 10337669.
- ^ Escott-Stump S (2008). Nutrition and Diagnosis-Related Care, 7th edition. Baltimore, MD: Lippincott Williams & Wilkins. pp. 1020 (pp 431). ISBN 978-1-60831-017-3.
- ^ Shanahan F (January 2002). "Crohn's disease". Lancet. 359 (9300): 62–9. doi:10.1016/S0140-6736(02)07284-7. PMID 11809204. S2CID 743620.
- ^ Djurić Z, Šaranac L, Budić I, Pavlović V, Djordjević J (August 2018). "Therapeutic role of methotrexate in pediatric Crohn's disease". Bosnian Journal of Basic Medical Sciences. 18 (3): 211–216. doi:10.17305/bjbms.2018.2792. PMC 6087553. PMID 29338679.
- ^ "FDA Approves Cimzia to Treat Crohn's Disease" (Press release). Food and Drug Administration (FDA). April 22, 2008. Archived from the original on October 20, 2009. Retrieved November 5, 2009.
- ^ "Prescribing information ustekinumab" (PDF). FDA. Archived (PDF) from the original on October 18, 2020. Retrieved May 23, 2019.
- ^ Sandborn WJ, Colombel JF, Enns R, Feagan BG, Hanauer SB, Lawrance IC, et al. (International Efficacy of Natalizumab as Active Crohn's Therapy (ENACT-1) Trial Group; Evaluation of Natalizumab as Continuous Therapy (ENACT-2) Trial Group) (November 2005). "Natalizumab induction and maintenance therapy for Crohn's disease". The New England Journal of Medicine. 353 (18): 1912–25. doi:10.1056/NEJMoa043335. PMID 16267322.
- ^ Nelson SM, Nguyen TM, McDonald JW, MacDonald JK (August 2018). "Natalizumab for induction of remission in Crohn's disease". The Cochrane Database of Systematic Reviews. 2018 (8): CD006097. doi:10.1002/14651858.CD006097.pub3. PMC 6513248. PMID 30068022.
- ^ "Discover RINVOQ® (upadacitinib)". RINVOQ. Archived from the original on May 18, 2023. Retrieved May 29, 2023.
- ^ Longmore M, Wilkinson I, Turmezei T, Cheung CK (2007). Oxford Handbook of Clinical Medicine (7th ed.). Oxford University Press. pp. 266–7. ISBN 978-0-19-856837-7.
- ^ a b c MacDonald JK, Nguyen TM, Khanna R, Timmer A (November 2016). "Anti-IL-12/23p40 antibodies for induction of remission in Crohn's disease". The Cochrane Database of Systematic Reviews. 2016 (11): CD007572. doi:10.1002/14651858.CD007572.pub3. PMC 6464484. PMID 27885650.
- ^ Mowat C, Cole A, Windsor A, Ahmad T, Arnott I, Driscoll R, Mitton S, Orchard T, Rutter M, Younge L, Lees C, Ho GT, Satsangi J, Bloom S, et al. (IBD Section of the British Society of Gastroenterology) (May 2011). "Guidelines for the management of inflammatory bowel disease in adults". Gut. 60 (5): 571–607. doi:10.1136/gut.2010.224154. PMID 21464096. S2CID 8269837.
- ^ Goddard AF, James MW, McIntyre AS, Scott BB (October 2011). "Guidelines for the management of iron deficiency anaemia". Gut. 60 (10): 1309–16. doi:10.1136/gut.2010.228874. PMID 21561874.
- ^ Gasche C, Berstad A, Befrits R, Beglinger C, Dignass A, Erichsen K, et al. (December 2007). "Guidelines on the diagnosis and management of iron deficiency and anemia in inflammatory bowel diseases". Inflammatory Bowel Diseases. 13 (12): 1545–53. doi:10.1002/ibd.20285. PMID 17985376.
- ^ 보제리, L.; 이츠코위츠, S.H. 암은 염증성 장질환을 악화시킵니다. N. 영어. J. Med. 2015, 372, 1441–1452
- ^ Toruner, M., Loftus, E.V., Harmsen, W.S., Zinsmeister, A.R., Orenstein, R., Sandborn, W.J., Colombel, J., Egan, L.J. 염증성 장 질환 환자의 기회 감염 위험 인자. 소화기내과 2008, 134, 929–936
- ^ F.A., Melmed, G.Y., 리히텐슈타인, G.R., Kane, S.V. ACG 임상 지침: 염증성 장 질환의 예방 관리. Am. J. Gastroenterol. 2017, 112, 241–258.
- ^ Kucharzik, T.; Ellul, P.; Greuter, T.; Rahier, J.F.; 버스토크, B., 아브레우, C., 앨버커키, A., 올리카, M., 에스테브, M., 파라예, F.A., et al. 염증성 장질환의 감염 예방, 진단 및 관리에 관한 ECCO 지침. J. 크론 대장염 2021, 15, 879–913.
- ^ A.N.의 Anthakrishnan; E.L.의 McGinley 감염 관련 입원은 염증성 장 질환 환자의 사망률 증가와 관련이 있습니다. J. 크론 대장염 2013, 7, 107–112.
- ^ 말히, G., 럼먼, A., R. 타나발란, K. 크로이토루, M.S. 실버버그, A.H. 스타인하트, G.C. 염증성 장 질환 환자의 백신 접종: 태도, 지식, 그리고 이해. J. 크론 대장염 2015, 9, 439–444
- ^ A. Costantino, A., Michelon, M., Noviello, D., F.M., Macaluso, Leon, S., Bonaccorso, N., Costantino, C., Vecchi, M., Caprioli, A., AMICI Scientific Board를 대표하여. 이탈리아 국립 염증성 장질환 환자 집단의 백신 접종에 대한 태도 백신 2023년, 11, 1591년.
- ^ Kristo I, Stift A, Bergmann M, Riss S (May 2015). "Surgical recurrence in Crohn's disease: Are we getting better?". World Journal of Gastroenterology. 21 (20): 6097–100. doi:10.3748/wjg.v21.i20.6097. PMC 4445088. PMID 26034346.
- ^ Tresca AJ (January 12, 2007). "Resection Surgery for Crohn's Disease". About.com. Archived from the original on November 13, 2007. Retrieved February 14, 2008.
- ^ Ozuner G, Fazio VW, Lavery IC, Milsom JW, Strong SA (November 1996). "Reoperative rates for Crohn's disease following strictureplasty. Long-term analysis". Diseases of the Colon and Rectum. 39 (11): 1199–203. doi:10.1007/BF02055108. PMID 8918424. S2CID 33628350.
- ^ Rutgeerts P, Geboes K, Vantrappen G, Beyls J, Kerremans R, Hiele M (October 1990). "Predictability of the postoperative course of Crohn's disease". Gastroenterology. 99 (4): 956–63. doi:10.1016/0016-5085(90)90613-6. PMID 2394349.
- ^ Yamamoto T, Bamba T, Umegae S, Matsumoto K (August 2013). "The impact of early endoscopic lesions on the clinical course of patients following ileocolonic resection for Crohn's disease: A 5-year prospective cohort study". United European Gastroenterology Journal. 1 (4): 294–8. doi:10.1177/2050640613495197. PMC 4040796. PMID 24917974.
- ^ "Short Bowel Syndrome". National Institute of Diabetes and Digestive and Kidney Diseases (NIDDK). July 2015. Archived from the original on December 9, 2019. Retrieved December 8, 2019.
- ^ Rhodes M (October 24, 2006). "Intestinal transplant for Crohn's disease". Everyday Health. Archived from the original on October 8, 2008. Retrieved March 22, 2009.
- ^ Hofmann AF (April 1967). "The syndrome of ileal disease and the broken enterohepatic circulation: cholerheic enteropathy". Gastroenterology. 52 (4): 752–7. doi:10.1016/S0016-5085(67)80140-9. PMID 5337211.
- ^ Limketkai, Berkeley N; Akobeng, Anthony K; Gordon, Morris; Adepoju, Akinlolu Adedayo (July 17, 2020). Cochrane Gut Group (ed.). "Probiotics for induction of remission in Crohn's disease". Cochrane Database of Systematic Reviews. 2020 (7): CD006634. doi:10.1002/14651858.CD006634.pub3. PMC 7389339. PMID 32678465.
- ^ a b Szigethy E, McLafferty L, Goyal A (April 2010). "Inflammatory bowel disease". Child and Adolescent Psychiatric Clinics of North America (Submitted manuscript). 19 (2): 301–18, ix. doi:10.1016/j.chc.2010.01.007. PMID 20478501. Archived from the original on April 28, 2021. Retrieved September 4, 2018.
- ^ Ballou S, Keefer L (January 2017). "Psychological Interventions for Irritable Bowel Syndrome and Inflammatory Bowel Diseases". Clinical and Translational Gastroenterology. 8 (1): e214. doi:10.1038/ctg.2016.69. PMC 5288603. PMID 28102860.
- ^ a b Caprilli R, Gassull MA, Escher JC, Moser G, Munkholm P, Forbes A, et al. (European Crohn's Colitis Organisation) (March 2006). "European evidence based consensus on the diagnosis and management of Crohn's disease: special situations". Gut. 55 (Suppl 1): i36–58. doi:10.1136/gut.2005.081950c. PMC 1859996. PMID 16481630.
the colitis activity index fell significantly in the treatment group compared to the sham acupuncture group. However, recruitment did not reach its target and the number of patients was small.
- ^ Joos S, Brinkhaus B, Maluche C, Maupai N, Kohnen R, Kraehmer N, Hahn EG, Schuppan D (2004). "Acupuncture and moxibustion in the treatment of active Crohn's disease: a randomized controlled study". Digestion. 69 (3): 131–9. doi:10.1159/000078151. PMID 15114043. S2CID 7852406.
- ^ Joos S (June 2011). "Review on efficacy and health services research studies of complementary and alternative medicine in inflammatory bowel disease". Chinese Journal of Integrative Medicine. 17 (6): 403–9. doi:10.1007/s11655-011-0758-3. PMID 21660673. S2CID 207298246.
- ^ Smith K (2012). "Homeopathy is Unscientific and Unethical". Bioethics. 26 (9): 508–512. doi:10.1111/j.1467-8519.2011.01956.x. S2CID 143067523. Archived from the original on October 29, 2017. Retrieved October 28, 2017.
- ^ Ladyman J (2013). "Towards a Demarcation of Science from Pseudoscience". In Pigliucci M, Boudry M (eds.). Philosophy of Pseudoscience: Reconsidering the Demarcation Problem. University of Chicago Press. pp. 45–59. ISBN 978-0-226-05182-6.
Yet homeopathy is a paradigmatic example of pseudoscience. It is neither simply bad science nor science fraud, but rather profoundly departs from scientific method and theories while being described as scientific by some of its adherents (often sincerely).
- ^ Baran GR, Kiani MF, Samuel SP (2014). "Science, Pseudoscience, and Not Science: How do They Differ?". Healthcare and Biomedical Technology in the 21st Century. pp. 19–57. doi:10.1007/978-1-4614-8541-4_2. ISBN 978-1-4614-8540-7.
within the traditional medical community it is considered to be quackery
- ^ Ernst E (December 2002). "A systematic review of systematic reviews of homeopathy". British Journal of Clinical Pharmacology. 54 (6): 577–82. doi:10.1046/j.1365-2125.2002.01699.x. PMC 1874503. PMID 12492603.
- ^ Shang A, Huwiler-Müntener K, Nartey L, Jüni P, Dörig S, Sterne JA, Pewsner D, Egger M (2005). "Are the clinical effects of homoeopathy placebo effects? Comparative study of placebo-controlled trials of homoeopathy and allopathy". Lancet. 366 (9487): 726–32. doi:10.1016/S0140-6736(05)67177-2. PMID 16125589. S2CID 17939264.
- ^ "Evidence Check 2: Homeopathy - Science and Technology Committee". British House of Commons Science and Technology Committee. February 22, 2010. Archived from the original on September 19, 2015. Retrieved April 5, 2014.
- ^ Naftali T, Mechulam R, Lev LB, Konikoff FM (2014). "Cannabis for inflammatory bowel disease". Digestive Diseases. 32 (4): 468–74. doi:10.1159/000358155. PMID 24969296. S2CID 25309621.
- ^ Kafil TS, Nguyen TM, MacDonald JK, Chande N (November 2018). "Cannabis for the treatment of Crohn's disease". The Cochrane Database of Systematic Reviews. 11 (11): CD012853. doi:10.1002/14651858.CD012853.pub2. PMC 6517156. PMID 30407616.
- ^ "Crohn's disease - Prognosis". University of Maryland Medical Centre. Archived from the original on August 29, 2012. Retrieved October 19, 2012.
- ^ a b Hiatt RA, Kaufman L (November 1988). "Epidemiology of inflammatory bowel disease in a defined northern California population". The Western Journal of Medicine. 149 (5): 541–6. PMC 1026530. PMID 3250100.
- ^ Moum B, Vatn MH, Ekbom A, Aadland E, Fausa O, Lygren I, Stray N, Sauar J, Schulz T (April 1996). "Incidence of Crohn's disease in four counties in southeastern Norway, 1990-93. A prospective population-based study. The Inflammatory Bowel South-Eastern Norway (IBSEN) Study Group of Gastroenterologists". Scandinavian Journal of Gastroenterology. 31 (4): 355–61. doi:10.3109/00365529609006410. PMID 8726303.
- ^ Shivananda S, Lennard-Jones J, Logan R, Fear N, Price A, Carpenter L, van Blankenstein M (November 1996). "Incidence of inflammatory bowel disease across Europe: is there a difference between north and south? Results of the European Collaborative Study on Inflammatory Bowel Disease (EC-IBD)". Gut. 39 (5): 690–7. doi:10.1136/gut.39.5.690. PMC 1383393. PMID 9014768.
- ^ Yang H, McElree C, Roth MP, Shanahan F, Targan SR, Rotter JI (April 1993). "Familial empirical risks for inflammatory bowel disease: differences between Jews and non-Jews". Gut. 34 (4): 517–24. doi:10.1136/gut.34.4.517. PMC 1374314. PMID 8491401.
- ^ Seksik P, Nion-Larmurier I, Sokol H, Beaugerie L, Cosnes J (May 2009). "Effects of light smoking consumption on the clinical course of Crohn's disease". Inflammatory Bowel Diseases. 15 (5): 734–41. doi:10.1002/ibd.20828. PMID 19067428. S2CID 10988974.
- ^ "Crohn's disease manifests differently in boys and girls". Crohn's and Colitis Foundation of America. Archived from the original on February 16, 2008.
- ^ "Who is affected by Crohn's disease". Healthwise. Archived from the original on January 23, 2009.
- ^ Satsangi J, Jewell DP, Bell JI (May 1997). "The genetics of inflammatory bowel disease". Gut. 40 (5): 572–4. doi:10.1136/gut.40.5.572. PMC 1027155. PMID 9203931.
- ^ Tysk C, Lindberg E, Järnerot G, Flodérus-Myrhed B (July 1988). "Ulcerative colitis and Crohn's disease in an unselected population of monozygotic and dizygotic twins. A study of heritability and the influence of smoking". Gut. 29 (7): 990–6. doi:10.1136/gut.29.7.990. PMC 1433769. PMID 3396969.
- ^ Burisch J, Jess T, Martinato M, Lakatos PL (May 2013). "The burden of inflammatory bowel disease in Europe". Journal of Crohn's & Colitis. 7 (4): 322–37. doi:10.1016/j.crohns.2013.01.010. PMID 23395397.
- ^ a b Ng SC, Shi HY, Hamidi N, Underwood FE, Tang W, Benchimol EI, Panaccione R, Ghosh S, Wu JC, Chan FK, Sung JJ, Kaplan GG (December 2018). "Worldwide incidence and prevalence of inflammatory bowel disease in the 21st century: a systematic review of population-based studies". Lancet. 390 (10114): 2769–2778. doi:10.1016/S0140-6736(17)32448-0. PMID 29050646. S2CID 32940.
- ^ Kirsner JB (June 1988). "Historical aspects of inflammatory bowel disease". Journal of Clinical Gastroenterology. 10 (3): 286–97. doi:10.1097/00004836-198806000-00012. PMID 2980764.
- ^ Lichtarowicz AM, Mayberry JF (August 1988). "Antoni Lésniowski and his contribution to regional enteritis (Crohn's disease)". Journal of the Royal Society of Medicine. 81 (8): 468–70. doi:10.1177/014107688808100817. PMC 1291720. PMID 3047387.
더보기
- Lichtenstein GR, Loftus EV, Isaacs KL, Regueiro MD, Gerson LB, Sands BE (April 2018). "ACG Clinical Guideline: Management of Crohn's Disease in Adults". Am. J. Gastroenterol. 113 (4): 481–517. doi:10.1038/ajg.2018.27. PMID 29610508.
외부 링크
- "Crohn's disease". MedlinePlus. U.S. National Library of Medicine.





