치주병
Periodontal disease| 치주병 | |
|---|---|
| 기타 이름 | 잇몸질환,열병,치주염 |
 | |
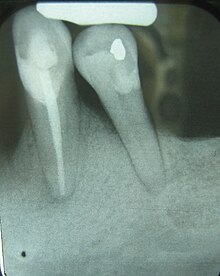
| 치아(검은색 부위)의 두 뿌리 사이의 뼈 손실을 보여주는 방사선 사진. 치아의 감염으로 인해 해면골이 빠지면서 치아에 대한 뼈 지지대가 줄어들었다. | |
| 발음 |
|
| 전문 | 치의학 |
| 증상 | 빨갛고, 붓고, 아프고, 잇몸에서 피가 나고, 이가 헐고, 입냄새가[1] 심하다. |
| 합병증 | 치아 손실, 잇몸 종기[1][2] |
| 원인들 | 박테리아 관련 명판이 쌓이다[1]. |
| 위험요소 | 흡연,[3] 당뇨병, 에이즈, 특정 약물[1] |
| 진단법 | 치과 검진, 엑스레이 검사[1] |
| 치료 | 구강위생 증진, 정기적인 전문 청소[4] |
| 약물 | 구술의 |
| 빈도 | 5억3800만(2015년)[5] |
잇몸질환으로도 알려진 치주질환은 치아를 둘러싼 조직에 영향을 미치는 염증성 질환의 집합체다.[4] 잇몸염이라고 불리는 초기에는 잇몸이 붓고 빨갛게 되며 피가 날 수도 있다.[4] 전 세계 성인들의 치아 상실의 주요 원인으로 꼽힌다.[6][7] 치주염이라고 불리는 더 심각한 형태에서는 잇몸이 치아에서 빠져 나갈 수 있고, 뼈가 없어질 수 있으며, 치아가 느슨해지거나 빠질 수 있다.[4] 입냄새도 날 수 있다.[1]
치주질환은 일반적으로 입 안의 박테리아가 치아 주변 조직을 감염시키기 때문이다.[4] 질병의 위험을 높이는 요인으로는 흡연,[3] 당뇨병,[1] 에이즈, 가족력, 특정 약물 등이 있다. 진단은 치아 주변의 잇몸 조직을 육안으로 모두 검사하고, 치아 주변의 뼈 손실을 찾아 탐침과 엑스레이로 검사하는 것이다.[1][8]
치료는 좋은 구강 위생과 정기적인 전문적인 치아 세척을 포함한다.[4] 권장 구강위생에는 매일 양치질, 치실 등이 포함된다.[4] 어떤 경우에는 항생제나 치과 수술을 권할 수도 있다.[9] 2015년 전 세계 5억3800만 명이 영향을 받은 것으로 추정됐으며, 전체 인구의 10~15%에 영향을 미치는 것으로 알려져 있다.[10][11][5] 미국에서는 30세 이상 인구의 거의 절반이 어느 정도 영향을 받고 있으며 65세 이상 인구의 약 70%가 이 질환을 앓고 있다.[4] 수컷이 암컷보다 더 자주 영향을 받는다.[4]
징후 및 증상
초기 치주염은 증상이 거의 없으며, 많은 개인에서 치료를 받기 전에 병이 현저하게 진전되었다.
증상에는 다음이 포함될 수 있다.
- 이를 닦는 동안 잇몸이 붉어지거나 피가 나는 경우, 치실을 사용하거나 딱딱한 음식을 물어뜯는 경우(예: 사과) (이것은 부착력 상실 잇몸 질환이 없는 치염에서도 발생할 수 있다)
- 잇몸 붓기가 재발하다.
- 양치질 후 피 뱉기
- 구토증, 즉 입냄새, 그리고 입안의 지속적인 금속 맛
- 치아가 길어 보이는 징기벌적 불황(이것은 또한 칫솔을 심하게 칫솔질하거나 뻣뻣하게 칫솔질을 해서 생길 수도 있다)
- 치아와 잇몸 사이의 깊은 주머니(포켓은 콜라겐을 파괴하는 효소로 인해 부착물이 점차적으로 파괴된 부위, 콜라겐아제라고 알려져 있다.
- 느슨한 톱니(다른 이유에서도 발생할 수 있음)
Gingival 염증과 뼈 파괴는 대부분 통증이 없다. 따라서, 사람들은 치아 세척이 대수롭지 않은 후에 무통 출혈로 잘못 추정할 수 있지만, 이는 치주염이 진행되는 증상일 수 있다.
관련 조건
치주염은 C-reactive 단백질과 인터루킨-6의 증가된 수치로 나타나는 것과 같이 체내 염증 증가와 연관되어 있다.[12][13][14][15] 뇌졸중,[16][17] 심근경색,[18] 아테롬성[19][20][21][22][23][24][25] 동맥경화증, 고혈압의 위험 증가와 관련이 있다.[26] 그것은 또한 60세 이상의 나이에도 지연된 기억력과 계산능력의 장애로 연결되었다.[27][28] 단식 포도당과 당뇨가 손상된 사람은 치주염의 정도가 높으며, 치주염으로 인한 지속적인 전신 염증 상태 때문에 혈당수치의 균형을 잡는 데 어려움을 겪는 경우가 많다.[29][30] 인과관계가 입증된 것은 아니지만 만성 치주염과 발기부전,[31] 염증성 장질환,[32] 심장질환,[33] 췌장암과의 연관성이 있다.[34]
원인들
치주염은 치주염, 즉 치아를 떠받치는 조직의 염증이다. 치주석은 네 개의 조직으로 구성되어 있다.
치경염의 1차 원인은 구강위생이 부실하거나 비효율적이기 때문에 치아 [35]플라그라고 불리는 잇몸선에 근종과[36][37][38][39] 박테리아 기질이 축적된다. 다른 기여자들은 영양 상태가 좋지 않고 당뇨병과 같은 근본적인 의학적 문제들이다.[40] 당뇨병 환자들은 치주질환을 다스리기 위해 가정 관리에 꼼꼼해야 한다.[41] 새로운 손가락 찌르기 테스트는 미국 식품의약국(FDA)의 승인을 받았으며, 치과에서 당뇨병과 같은 잇몸 질환의 원인이 될 수 있는 원인을 확인하고 검사하기 위해 사용되고 있다.
어떤 사람들에게는, 치주염이 치주염으로 진행되는데, 치주섬유가 파괴되면서 치주 주머니라고 불리는 잇몸 조직과 잇몸 조직이 분리되고 심화된 설커스가 발생한다. 서브진화 미생물(껌선 아래에 존재하는 미생물)은 치주 주머니를 식민지화하여 잇몸 조직에 더 많은 염증을 유발하고 진행성 뼈 손실을 일으킨다. 2차 원인의 예로는 복구 돌출부, 뿌리 근접성 등 정의상 미세균 플라그 누적을 일으키는 것들이 있다.
흡연은 치주염의 발생을 직접적이든 간접적이든 증가시키고,[42][43][44] 치주염 치료에 지장을 주거나 악영향을 미칠 수 있는 또 다른 요인이다.[45][46][47] 그것은 치주염에 있어 가장 중요한 환경적 위험인자다. 흡연자가 비흡연자에 비해 골절, 애착감소, 치아감소가 더 많다는 연구결과가 나왔다.[48] 이는 흡연이 상처 치유 감소, 항체 생산 억제, 중성미자에[48] 의한 포자세포증 감소 등 면역반응에 미치는 여러 영향 때문일 가능성이 높다.
Ellers-Danlos 증후군과 Papillon-Lefébre 증후군(일명 팜플로판타 케라토르마)도 치주염의 위험 요인이다.
방해를 받지 않고 방치하면 미생물 플라그가 미적분해 미적분을 형성하는데, 이를 흔히 타르타르라고 한다. 잇몸선 위와 아래의 미적분은 치위생사나 치과의사가 완전히 제거하여 치주염과 치주염을 치료해야 한다. 치주염과 치주염의 주된 원인은 치아 표면에 달라붙는 미생물 명판이지만, 다른 많은 변형 요인들이 있다. 매우 강한 위험요인은 사람의 유전적 민감성이다. 다운증후군, 당뇨병, 그리고 감염에 대한 저항력에 영향을 미치는 다른 질병들을 포함한 몇몇 조건과 질병들 또한 치주염에 대한 민감성을 증가시킨다.
치주염은 더 높은 스트레스와 관련이 있을 수 있다.[49] 치주염은 사회경제적 규모의 상위 계층의 사람들보다 하위 계층의 사람들에게 더 자주 발생한다.[50]
유전학은 치주염의 위험을 결정하는 데 역할을 하는 것으로 보인다. 유전학적으로 볼 때 명판 조절이 잘 된 사람이 치주염에 걸린 반면 구강 위생이 잘 되지 않은 사람이 치주염에 걸리는 이유를 설명할 수 있을 것으로 생각된다. 치주염에 걸린 사람의 위험을 수정할 수 있는 유전적 요인은 다음과 같다.
- Pagocytosis의 결함: 사람은 저자극성 Phagocells를 가지고 있을 수 있다.
- 인터루킨, 프로스타글란딘, 사이토카인 등의 초생산성으로 인해 면역반응이 과장되었다.
- 인터루킨 1 (IL-1) 유전자 다형성: 이러한 다형성을 가진 사람들은 더 많은 IL-1을 생산하고, 그 후에 만성 치주염에 걸릴 위험이 더 높다.[48]
당뇨병은 치주염의 시작, 진행, 심각성을 악화시키는 것으로 보인다.[51] 대부분의 연구가 제2형 당뇨병에 초점을 맞추고 있지만 제1형 당뇨병은 치주염의 위험성에 동일한 영향을 미치는 것으로 보인다.[52] 치주염의 위험 증가 정도는 당혈 조절 수준에 따라 달라진다. 그러므로 잘 관리된 당뇨병에서는 치주염의 위험성에 대한 당뇨병의 영향이 작은 것 같다. 그러나 글리코믹스 통제가 악화됨에 따라 위험은 기하급수적으로 증가한다.[52] 전체적으로 당뇨병 환자의 치주염 위험 증가율은 2~3배 정도 높은 것으로 추정된다.[51] 지금까지 연결의 기초가 되는 메커니즘은 완전히 이해되지는 않지만 염증, 면역 기능, 중성미 활동, 사이토카인 생물학 등의 측면을 수반하는 것으로 알려져 있다.[52][53]
메커니즘
치석이나 바이오 필름이 잇몸 근처와 아래 치아에 축적되면서 정상적인 구강 미세생물들의 이상증세가 나타난다.[54] 2017년 현재, 어떤 종들이 해를 끼쳤는지 확실하지 않지만, 그램 음성 혐기성 박테리아, 스피로체, 바이러스 등이 제안되었다.; 한 종 이상의 종들이 질병을 일으키고 있다는 것은 때때로 명백하다.[54] 2004년 연구는 3 그램의 음의 혐기성 종을 나타냈다. 아그레가티박터 액티노미세템코미탄스, 포르피로모나스 칭기발리스, 박테로이드스 개나리, 에이케넬라 등이 부식한다.[48]
플라크는 부드럽고 정제되지 않은 것, 딱딱하고 석회화 된 것, 또는 둘 다일 수 있다; 치아에 있는 플라크의 경우 칼슘은 침에서 나온다; 잇몸선 아래의 플라크의 경우, 그것은 염증이 난 잇몸의 배출을 통한 혈액에서 나온다.[54]
치아와 잇몸의 손상은 구강조직과 구강 미생물군 사이의 정상적인 공생을 방해하는 미생물들을 파괴하려 할 때 면역체계에서 온다. 다른 조직에서와 마찬가지로 상피 속의 랑게르한스 세포는 미생물로부터 항원을 받아 면역계에 제시하여 백혈구가 영향을 받는 조직으로 이동하게 된다. 이 과정은 차례로 뼈를 파괴하기 시작하는 골수성형을 활성화하고 인대를 파괴하는 매트릭스 금속단백질을 활성화시킨다.[54] 그래서 요컨대 병을 일으키는 것은 박테리아지만, 주요 파괴적인 사건은 숙주의 면역체계의 과장된 반응에 의해 야기된다.[48]
분류
1989년, 1993년, 1999년,[55] 2017년 등 치주질환에 대한 합의된 분류체계를 도입하려는 시도가 여러 차례 있었다.
1999년 분류
1999년 치주질환 및 질환 분류체계에는 7가지 주요 치주질환 범주가 열거되어 있는데,[55] 이 중 2~6은 근본적으로 돌이킬 수 없는 손상이기 때문에 파괴적인 치주질환으로 불린다. 7가지 범주는 다음과 같다.
더욱이 치주질환의 정도와 심각성을 모두 표현하는 용어는 특정인이나 특정인 집단의 구체적인 진단을 나타내기 위해 위의 용어에 첨부된다.
심각도
질병의 "결함성"은 "임상부착감소"라고 불리는 치주 인대섬유의 양을 말한다. 1999년 분류에 따르면 만성 치주염의 중증도는 다음과 같이 등급이 매겨진다.[56]
- 경미: 부착물 손실의 1–2mm(0.039–0.079인치)
- 보통: 부착물 손실의 3–4mm(0.12–0.16인치)
- 심각: 부착력 손실 5mm(0.20인치)
범위
질병의 "확장"은 부위의 퍼센트로 볼 때 질병의 영향을 받는 의치의 비율을 가리킨다. 부위는 각 치아를 중심으로 프로빙 측정을 하는 위치로 정의되며, 일반적으로 다음과 같이 각 치아를 중심으로 6개의 프로빙 부위가 기록된다.
- 메시오부칼
- 중간 부칼
- 디스토부크칼
- 중간 언어
- 중간 언어
- 원위법
입안에 있는 부위의 최대 30%가 영향을 받는 경우 발현을 "지역화"로 분류하고, 30% 이상에서는 "일반화"라는 용어를 사용한다.
2017년 분류
2017년 치주질환 분류는 다음과 같다.[57][58][59]
치주 건강, 징기발병 및 질환
- 치주 건강 및 징기발 건강
- 온전한 치주머니즘에 대한 임상적 징기벌 건강
- 온전한 치주머니즘에 대한 임상적 징기벌 건강
- 안정 치주염
- 비 치주염인
- Gingivitis - 치과용 바이오필름 유도
- 치과 바이오 필름에만 관련됨
- 체계적 및 국소적 위험 요인에 의해 매개됨
- 약물 유발 깅기벌 확대.
- Gingival 질환 - 치과용 바이오 필름이 유발되지 않음
- 유전적/발달적 장애
- 특정 감염
- 염증 및 면역 상태
- 반응형 프로세스
- 네오플라스움속
- 내분비, 영양 및 대사
- 외상성 병변
- Gingival 색소 침착.
치주염
치주름에 영향을 미치는 기타 조건
(조직성 질환과 발달 및 후천 조건의 주기적 징후)
- 치주 지지 조직에 영향을 미치는 질환의 전신 질환
- 기타 치주 조건
- 뮤코징 기형 및 조건
- 징기발 표현형
- Gingival/소프트티슈 침체
- 깅기바 부족
- 전정 깊이 감소
- 애버런트 프레넘/근육 위치
- Gingival 초과
- 비정상적 색상
- 노출된 뿌리 표면의 상태
- 외상의 외과적 힘
- 1차 외상
- 2차 외상
- 치아 및 보형물 관련 요인
- 국부적 치아 관련 요인
- 국부적인 치과 보형물 관련 요인
주엽식물 질병 및 질환
스테이징
치주염의 발생 목표는 손상의 심각성을 분류하고 경영에 영향을 미칠 수 있는 특정 요인을 평가하는 것이다.[59]
2017년 분류에 따르면 치주염은 다음과 같은 몇 가지 요인을 고려한 후 4단계로 구분된다.
- 방사선 촬영으로 뼈 손실 양 및 백분율
- 임상 부착 손실, 프로빙 깊이
- 퍼지션 유무
- 수직 뼈 결점
- 치주염 관련 치아 상실 이력
- 2차 막힘 외상으로[59] 인한 치아 과다 이동성
채점
2017년 분류에 따르면 치주염 등급제는 다음 3가지 등급으로 구성된다.[60]
- A등급: 질병의 느린 진행; 지난 5년간 뼈의 손실에 대한 증거는 없다.
- B급 : 적당한 진행, < 최근 5년간 뼈 손실 2mm
- C등급 : 고위험 시 신속한 진행 또는 향후 진행, ≥ 5년간 2mm 뼈 손실
개인이 분류되는 등급에 영향을 미치는 위험 요소에는 다음이 포함된다.[60]
- 흡연석을 부탁해요.
- 당뇨병
예방
치주질환 예방을 위한 일일 구강위생 조치에는 다음이 포함된다.
- 정기적으로(적어도 매일 두 번) 올바른 양치질을 하면, 칫솔모 밑의 칫솔모에 대한 방향을 잡아주는 사람이 있으면 박테리아 균의 성장과 부조화판의 형성을 방해하는 데 도움이 된다.[citation needed]
- 매일 치실질을 하고 치간칫솔(치아 사이의 공간이 충분히 큰 경우)을 사용하며, 마지막 치아인 세 번째 어금니를 분기마다 청소한다[citation needed].
- 소독용 구강 세척제 사용: 클로로헥시딘 글루콘산염 기반 구강청정기와 치주염으로 인한 부착손실을 되돌릴 수는 없지만 치주염은 조심스러운 구강위생을 병행하면 치주염을 치료할 수 있다.[citation needed]
- 필요에 따라 정기적인 치과 검진 및 전문 치아 세척: 치과 검진은 치아의 구강위생 방법과 치아 주변 부착 정도를 모니터링하고 치주염 초기 징후를 파악하며 치료에 대한 반응을 모니터링하는 역할을 한다.
일반적으로 치과 위생사(또는 치과의사)는 특수한 기구를 사용하여 거미줄 아래 치아를 청소(디브라이드)하고 거미줄 아래에서 자라는 치석을 교란시킨다. 이것은 확립된 치주염이 더 이상 진행되지 않도록 하기 위한 표준 치료법이다. 이런 전문 세척(주기적 괴사조직 제거) 후 미생물 플라그가 3~4개월 정도 지나면 사전 세척 수준으로 다시 커지는 경향이 있다는 연구결과가 나왔다. 그럼에도 불구하고, 사람의 치주 상태를 지속적으로 안정시키는 것은 주로 그렇지는 않지만, 이동 중뿐만 아니라 가정에서의 구강 위생에 크게 좌우된다. 매일 구강위생을 하지 않으면 치주질환을 극복하지 못할 것이며, 특히 치주질환이 광범위한 경우 더욱 그러하다.[citation needed]
관리

치주치료를 성공적으로 하는 초석은 훌륭한 구강위생을 확립하는 데서 출발한다. 이것은 매일 두 번 치실로 양치질을 하는 것을 포함한다. 또한 치아 사이의 공간이 허락한다면 치간 브러시를 사용하는 것도 도움이 된다. 좁은 공간에 부드러운 고무털이 달린 좁은 픽과 같은 제품들은 훌륭한 수동 세척을 제공한다. 관절염과 같은 손재주 문제가 있는 사람은 구강 위생이 어려울 수 있으며 전문적인 관리 및/또는 전동 칫솔 사용이 더 자주 필요할 수 있다. 치주염에 걸린 사람은 만성 염증성 질환이라는 것을 알아야 하며, 치주염에 걸린 치아를 유지하기 위해서는 치주염과 치주염의 평생치료가 필요하며 치주/치주염 전문의와 함께 전문적 유지관리를 해야 한다.
초기요법
치주건강을 확립하기 위해서는 미생물 명판과 미적분 제거가 필요하다. 치주염 치료의 첫 단계는 "뿌리 표면 계측" 또는 "RSI"라고 불리는 절차로 잇몸선 아래의 비수술적 세척을 수반하며, 이는 잇몸선 아래의 박테리아 바이오필름에 기계적 장애를 일으킨다.[48] 이 절차에는 치석과 미적분을 거름선 아래에서 기계적으로 제거하기 위한 전문 치료제의 사용이 포함되며, 적절히 완료하기 위해서는 여러 번의 방문과 국소 마취가 필요할 수 있다. 초기 RSI 외에도 뼈 지지대가 줄어든 치아에 과도한 힘이 가해지지 않도록 폐색(물림)을 조절해야 할 수도 있다. 또한 거칠고 명석한 복원술의 교체, 치아 사이의 열린 접촉의 폐쇄 및 초기 평가에서 진단된 다른 요구 조건과 같은 다른 치과 요구 사항을 완료해야 할 수 있다. RSI는 스케일링과 루트플랜팅과는 다르다는 점에 유의해야 한다: RSI는 미적분만을 제거하는 반면, 스케일링과 루트플랜팅은 미적분뿐만 아니라 밑부분이 부드러운 덴틴을 제거하는데, 이는 치주치유의 필수요건이 되지 않는다. 그러므로, RSI는 현재 뿌리 계획보다 주창되고 있다.[48]
재평가
비수술적 스케일링과 뿌리 평면화는 치주 주머니가 4~5mm(0.16-0.20인치)보다 낮은 경우 일반적으로 성공적이다.[61][62][63] 치과주치의나 위생사는 초기 스케일링과 뿌리계획 후 4~6주 후에 재평가를 실시하여 구강위생이 호전되고 염증이 퇴행하였는지를 판단해야 한다. 그 때 프로빙을 피해야 하며, gingival 지수에 의한 분석으로 염증의 유무를 판단해야 한다. 치주치료의 월별 재평가는 치료의 성공 여부를 더 잘 나타내는 것으로 치주 차트 작성과 다른 치료 과정이 확인될 수 있는지 확인해야 한다. 초기 치료 후 남아 있는 5-6mm(0.20–0.24인치) 이상의 주머니 깊이는 탐침 시 출혈이 있는 활성 질환을 나타내며 시간이 지남에 따라 추가적인 뼈 손실로 이어질 가능성이 매우 높다. 이는 특히 어금니 부위 중 뿌리(뿌리 사이의 영역)가 노출된 곳에서는 더욱 그러하다.
수술
비수술적 치료법이 질병 활동의 징후 관리에 실패한 것으로 판명될 경우, 가능한 경우 진행성 뼈 손실을 막고 잃어버린 뼈를 재생하기 위한 치주 수술이 필요할 수 있다. 개방 플랩 괴사조직 제거술, 삼지 수술 등 고도 치주염 치료에 많은 외과적 접근법이 사용되고 있으며, 유도 조직 재생과 뼈 이식술도 있다. 치주 수술의 목표는 가능한 한 주머니를 줄이기 위해 질병 과정에서 발생한 뼈 부위의 명확한 미적분 제거와 외과적 관리를 위한 접근이다. 장기간에 걸친 연구에 따르면, 중간에서 발달한 치주염에서, 수술로 치료된 케이스는 종종 시간이 지남에 따라 더 이상 분해되지 않으며, 정기적인 치료 후 유지 관리 요법과 결합하면, 거의 85%의 진단받은 사람들의 치아 상실을 막는 데 성공한다.[64][65]
현지 의약품 전달
치주학에서의 국소 약물 전달은 저항성 식물성 및 기타 부작용의 발생 위험 감소로 전신 약물에 비해 수용성과 인기를 얻었다.[66] 국소 테트라사이클린의 메타 분석 결과 개선이 발견되었다.[67] 스타틴의 국소적 응용이 유용할 수 있다.[68]
전신 약물전달
비수술적 치료와 연계한 전신 약물 전달은 구강 내 박테리아 플라그 부하 비율을 줄이기 위한 수단으로 사용될 수 있다. 많은 다양한 항생제와 항생제 조합이 검사되었지만, 비수술 치료에만 비해 장단기적으로 유의미한 차이가 있다는 확률은 매우 낮다. 박테리아는 항생제 내성을 발달시킬 수 있고 특정한 항생제는 메스꺼움, 설사, 위장 장애와 같은 일시적인 가벼운 부작용을 일으킬 수 있기 때문에 전신 약물의 사용을 제한하는 것이 유익할 수 있다.[69]
부가적인 전신 항균 처리
현재 보조 전신 항균제가 치주염의 비수술적 치료에 이로운지를 제시하는 낮은 품질의 증거가 있다.[70] 스케일링과 뿌리 플랜팅과 함께 사용할 때 일부 항생제가 다른 항생제보다 나은지는 확실하지 않다.
유지 관리
수술이 있든 없든 간에 성공적인 치주 치료가 완료되면, "치주기 유지 관리"의 지속적인 요법이 필요하다. 여기에는 치주염 유발 미생물의 재포용을 예방하고, 치주염이 재발할 경우 조기에 치료할 수 있도록 3개월에 한 번씩 정기검진과 세밀한 세척이 필요하다. 보통 치주질환은 부적절한 칫솔질로 인한 플라그 조절 불량으로 인해 발생한다. 따라서 브러싱 기법을 수정하지 않으면 치주 재발 가능성이 높다.
기타
대부분의 대안적인 "가정 내" 잇몸 질환 치료는 과산화수소와 같은 항균 용액을 가느다란 도포기나 구강 관개기를 통해 치주 주머니에 주입하는 것을 포함한다. 이 과정은 혐기성 미생물 군락을 교란시키고 매일 사용할 때 감염과 염증을 줄이는 데 효과적이다. 기능상 과산화수소와 동등한 많은 다른 제품들이 상업적으로 이용가능하지만, 훨씬 더 높은 비용으로 이용가능하다. 그러나 혐기성 미생물 군락은 미적분 내부와 주변에서 빠르게 재생되기 때문에 이러한 치료법은 미적분 형성을 다루지 못하고, 수명이 짧다.
Doxyclin은 스케일링의 1차 요법과 함께 제공될 수 있다(§ 초기 요법 참조).[71] Doxycyline은 질병 진행의 지표를 향상시키는 것으로 나타났다(명칭 탐식 깊이와 부착 수준).[71] 그것의 작용 메커니즘은 염증 조건 하에서 치아의 지지 조직(페리오돈튬)을 저하시키는 매트릭스 메탈로프로테아제(콜라겐아제 등)의 억제를 포함한다.[71] 유익한 구강 미생물을 죽이지 않기 위해 소량의 독시사이클린(20mg)만 사용한다.[71]
페이지 요법은 새로운 치료 대안이 될 수 있다.[72]
예후
치과의사와 치위생사는 치주검침이라는 장치를 사용하여 치주질환을 측정한다. 이 얇은 '측정봉'은 잇몸과 치아 사이의 공간에 부드럽게 놓이고, 잇몸선 아래로 미끄러진다. 탐침이 거미줄 아래로 3mm(0.12인치) 이상 미끄러질 수 있는 경우 상피부착의 이주가 발생하지 않은 경우 징기벌 주머니, 비정형 이주가 발생한 경우 치주 주머니가 있다고 한다. 이것은 본질적으로 어떤 깊이가 주머니인 것처럼 다소 오식적인 것으로, 그 깊이에 의해, 즉 2mm 포켓이나 6mm 포켓으로 정의된다. 그러나 주머니의 깊이가 3mm 이하일 경우 일반적으로 자기반복(집에서, 사람이, 칫솔로, 칫솔로)으로 인정된다. 이는 주머니가 치아 주변 3mm 이상 깊을 경우 홈케어로 주머니를 청소할 수 없어 전문적 관리를 구해야 하기 때문에 중요하다. 주머니 깊이가 6~7mm(0.24~0.28인치)에 이르면 치과 전문의들이 사용하는 손기구나 초음파 메스 등이 주머니 깊숙이 닿지 않아 징기발 염증을 일으키는 미생물 플라그를 제거하지 못할 수 있다. 이러한 상황에서, 치아 주변의 뼈나 잇몸은 수술로 변형되어야 하며 그렇지 않으면 항상 염증이 생겨 치아 주변의 뼈가 더 많이 손실될 가능성이 있다. 염증을 멈추기 위한 추가적인 방법은 그 사람이 부기질 항생제(미네소시클린과 같은)를 받거나 어떤 형태의 징기질 수술을 받아 주머니 깊이에 접근하고 어쩌면 주머니 깊이를 바꿔서 3mm이하로 만들고 다시 한 번 집에 있는 사람에 의해 적절하게 세척될 수 있게 하는 것이다. 아니면 그녀의 칫솔.
만약 사람들이 치아 주위에 7mm 혹은 더 깊은 주머니를 가지고 있다면, 그들은 수년 동안 결국 치아 상실의 위험을 무릅쓸 것이다. 만약 이 치주 질환이 확인되지 않고 사람들이 병의 진행적 특성을 모르고 있다면, 몇 년이 지난 후, 그들은 심각한 감염이나 심지어 고통으로 인해 일부 치아가 점차 느슨해지고 뽑혀질 필요가 있다는 사실에 놀랄지도 모른다.
스리랑카 차노동자 연구에 따르면 구강위생 활동이 없을 경우 약 10%가 심한 치주질환에 걸리며, 급속한 부착력 상실(>2mm/년)을 겪게 된다. 약 80%는 중간 손실(1~2mm/년)을 겪게 되고 나머지 10%는 손실에 걸리지 않게 된다.[73][74]
역학
치주염은 매우 흔하며, 충치 다음으로 세계적으로 두 번째로 흔한 치주질환으로 널리 알려져 있으며, 미국에서는 인구의 30~50%의 유병률을 보이고 있지만, 약 10%만이 심각한 형태를 가지고 있다.
만성 치주염은 2010년 현재 세계 인구의 약 10.8%인 약 7억 5천만 명의 사람들에게 영향을 미친다.[76]
치주염은 위생 및 기본적인 의료 감시 및 관리와 밀접하게 관련된 다른 조건과 마찬가지로 경제적 약자인 인구 또는 지역에서 더 흔한 경향이 있다. 그 발생은 높은 생활수준과 함께 감소한다. 이스라엘 인구의 경우 예멘인, 북아프리카인, 남아시아인, 지중해 출신 개인이 유럽계 출신 개인보다 치주질환 유병률이 높다.[77] 치주염은 흔히 사회적으로 패턴이 있다고 보고되는데, 즉 사회경제적 척도 하단의 사람들이 사회경제적 척도 상단의 사람들보다 치주염으로부터 더 자주 고통을 받는다는 것이다.[50]
역사
300만년 전의 고대 호민관은 잇몸 질환을 가지고 있었다.[78] 고고학 연구와 함께 중국과 중동의 기록을 보면 인류가 적어도 수천 년 동안 치주병을 앓아왔다는 것을 알 수 있다. 고대 플라크 DNA를 살펴본 유럽과 중동 고고학 연구는 고대 수렵-채집자의 생활 방식에서 잇몸 질환이 적었지만, 더 많은 시리얼을 먹었을 때 잇몸 질환이 더 흔해졌다는 것을 보여준다. Otzi Iceman은 심각한 잇몸 질환을 가지고 있는 것으로 밝혀졌다.[citation needed] 나아가 영국의 로마시대에는 현대에 비해 치주질환이 적었다는 연구결과가 나왔다. 연구원들은 흡연이 이것의 열쇠가 될 수 있다고 제안한다.[79]
사회와 문화
어원
periodontitis (그리스어: περιδδδ))))))))))))))))는 의학용어 "인플레이션"에서 그리스어 peri, "around", oodous (GEN odos), "toth", 접미사 -itis에서 유래한다.[80] 피오르헤아(대안 철자: pyorrhoea)라는 단어는 그리스 치질(πυόρρααα), "물질의 배출"이라는 단어 자체, 피온에서 "염소에서 배출", rhoē, "흐름", 접미사 -ia에서 유래한다.[81] 영어에서 이 용어는 그리스어처럼 고름이 분비되는 것을 묘사할 수 있다. 즉, 치아의 이러한 질병에 국한되지 않는다.[82]
경제학
심한 치주염으로 인한 생산성 손실은 세계 경제에 매년 약 540억 달러의 손실을 줄 것으로 추산된다.[83]
다른동물
치주질환은 개에게서 발견되는 가장 흔한 질병으로 3세 이상 개의 80% 이상이 걸리는 질환이다. 애완견의 유병률은 나이가 들수록 증가하지만 체중이 증가함에 따라 감소한다. 즉, 장난감과 미니어처 품종은 더 심각한 영향을 받는다. 최근 Waltham Centre for Pet Nutrition에서 실시된 연구는 개의 잇몸 질환과 관련된 박테리아가 인간과 같지 않다는 것을 입증했다.[84] 잇몸이 혈관이 매우 좋기 때문에 전신 질환이 발병할 수도 있다. 혈류에는 이러한 혐기성 미생물이 흐르고, 그것들은 신장과 간으로 걸러지며, 그곳에서 식민지화하여 미생물을 만들어낼 수도 있다. 혈액을 통해 이동하는 미생물은 심장 판막에도 부착되어 식물성 감염성 심내막염(감염된 심장 판막)을 일으킬 수 있다. 치주염으로 인해 발생할 수 있는 추가적인 질병은 만성 기관지염과 폐섬유화증이다.[85]
각주
- ^ a b c d e f g h "Gum Disease". National Institute of Dental and Craniofacial Research. February 2018. Retrieved 13 March 2018.
- ^ "Gum Disease Complications". nhs.uk. Retrieved 13 March 2018.
- ^ a b Albandar, Jasim M.; Adensaya, Margo R.; Streckfus, Charles F.; Winn, Deborah M. (December 2000). "Cigar, Pipe, and Cigarette Smoking as Risk Factors for Periodontal Disease and Tooth Loss". Journal of Periodontology. American Academy of Periodontology. 71 (12): 1874–1881. doi:10.1902/jop.2000.71.12.1874. ISSN 0022-3492. PMID 11156044. S2CID 11598500.
- ^ a b c d e f g h i "Periodontal Disease". CDC. 10 March 2015. Retrieved 13 March 2018.
- ^ a b GBD 2015 Disease and Injury Incidence and Prevalence Collaborators (October 2016). "Global, regional, and national incidence, prevalence, and years lived with disability for 310 diseases and injuries, 1990–2015: a systematic analysis for the Global Burden of Disease Study 2015". Lancet. 388 (10053): 1545–1602. doi:10.1016/S0140-6736(16)31678-6. PMC 5055577. PMID 27733282.
{{cite journal}}:author=일반 이름 포함(도움말) - ^ 브이. 바엘럼과 R. 로페즈, "주기적 역학: 사회과학이나 분자생물학을 지향하는가?"커뮤니티 치과 및 구강 역학, 32권, 4, 페이지 239–249, 2004.
- ^ 니키오 1세, 치렐리 T, 네포무체노 R 등 지질대사의 유전자에 있는 다형성들은 제2형 당뇨병성 감미료와 치주염과 연관되어 있으며, 대상자들의 당뇨병 연구의 치주, 당혈성 및 지질 프로파일 저널 2021년 1월 2021년 1월. PMCID: PMC8601849.
- ^ Savage A, Eaton KA, Moles DR, Needleman I (June 2009). "A systematic review of definitions of periodontitis and methods that have been used to identify this disease". Journal of Clinical Periodontology. 36 (6): 458–67. doi:10.1111/j.1600-051X.2009.01408.x. PMID 19508246.
- ^ "Gum Disease Treatment". nhs.uk. Retrieved 13 March 2018.
- ^ 브이. 바엘럼과 R. 로페즈, "주기적 역학: 사회과학이나 분자생물학을 지향하는가?"커뮤니티 치과 및 구강 역학, 32권, 4, 페이지 239–249, 2004.
- ^ 니키오 1세, 치렐리 T, 네포무체노 R 등 지질대사의 유전자에 있는 다형성들은 제2형 당뇨병성 감미료와 치주염과 연관되어 있으며, 대상자들의 당뇨병 연구의 치주, 당혈성 및 지질 프로파일 저널 2021년 1월 2021년 1월. PMCID: PMC8601849.
- ^ D'Aiuto F, Parkar M, Andreou G, Suvan J, Brett PM, Ready D, Tonetti MS (February 2004). "Periodontitis and systemic inflammation: control of the local infection is associated with a reduction in serum inflammatory markers". Journal of Dental Research. 83 (2): 156–60. doi:10.1177/154405910408300214. PMID 14742655. S2CID 34329326.
- ^ Nibali L, D'Aiuto F, Griffiths G, Patel K, Suvan J, Tonetti MS (November 2007). "Severe periodontitis is associated with systemic inflammation and a dysmetabolic status: a case-control study". Journal of Clinical Periodontology. 34 (11): 931–7. doi:10.1111/j.1600-051X.2007.01133.x. PMID 17877746.
- ^ Paraskevas S, Huizinga JD, Loos BG (April 2008). "A systematic review and meta-analyses on C-reactive protein in relation to periodontitis". Journal of Clinical Periodontology. 35 (4): 277–90. doi:10.1111/j.1600-051X.2007.01173.x. PMID 18294231.
- ^ D'Aiuto F, Ready D, Tonetti MS (August 2004). "Periodontal disease and C-reactive protein-associated cardiovascular risk". Journal of Periodontal Research. 39 (4): 236–41. doi:10.1111/j.1600-0765.2004.00731.x. PMID 15206916.
- ^ Pussinen PJ, Alfthan G, Jousilahti P, Paju S, Tuomilehto J (July 2007). "Systemic exposure to Porphyromonas gingivalis predicts incident stroke". Atherosclerosis. 193 (1): 222–8. doi:10.1016/j.atherosclerosis.2006.06.027. PMID 16872615.
- ^ Pussinen PJ, Alfthan G, Rissanen H, Reunanen A, Asikainen S, Knekt P (September 2004). "Antibodies to periodontal pathogens and stroke risk". Stroke. 35 (9): 2020–3. doi:10.1161/01.STR.0000136148.29490.fe. PMID 15232116.
- ^ Pussinen PJ, Alfthan G, Tuomilehto J, Asikainen S, Jousilahti P (October 2004). "High serum antibody levels to Porphyromonas gingivalis predict myocardial infarction". European Journal of Cardiovascular Prevention and Rehabilitation. 11 (5): 408–11. doi:10.1097/01.hjr.0000129745.38217.39. PMID 15616414. S2CID 34400631.
- ^ Ford PJ, Gemmell E, Timms P, Chan A, Preston FM, Seymour GJ (January 2007). "Anti-P. gingivalis response correlates with atherosclerosis". Journal of Dental Research. 86 (1): 35–40. doi:10.1177/154405910708600105. PMID 17189460. S2CID 5567995.
- ^ Beck JD, Eke P, Heiss G, Madianos P, Couper D, Lin D, Moss K, Elter J, Offenbacher S (July 2005). "Periodontal disease and coronary heart disease: a reappraisal of the exposure". Circulation. 112 (1): 19–24. doi:10.1161/CIRCULATIONAHA.104.511998. PMID 15983248.
- ^ Scannapieco FA, Bush RB, Paju S (December 2003). "Associations between periodontal disease and risk for atherosclerosis, cardiovascular disease, and stroke. A systematic review". Annals of Periodontology. 8 (1): 38–53. doi:10.1902/annals.2003.8.1.38. PMID 14971247.
- ^ Wu T, Trevisan M, Genco RJ, Dorn JP, Falkner KL, Sempos CT (October 2000). "Periodontal disease and risk of cerebrovascular disease: the first national health and nutrition examination survey and its follow-up study". Archives of Internal Medicine. 160 (18): 2749–55. doi:10.1001/archinte.160.18.2749. PMID 11025784.
- ^ Beck JD, Elter JR, Heiss G, Couper D, Mauriello SM, Offenbacher S (November 2001). "Relationship of periodontal disease to carotid artery intima-media wall thickness: the atherosclerosis risk in communities (ARIC) study". Arteriosclerosis, Thrombosis, and Vascular Biology. 21 (11): 1816–22. doi:10.1161/hq1101.097803. PMID 11701471.
- ^ Elter JR, Champagne CM, Offenbacher S, Beck JD (June 2004). "Relationship of periodontal disease and tooth loss to prevalence of coronary heart disease". Journal of Periodontology. 75 (6): 782–90. doi:10.1902/jop.2004.75.6.782. PMID 15295942.
- ^ Humphrey LL, Fu R, Buckley DI, Freeman M, Helfand M (December 2008). "Periodontal disease and coronary heart disease incidence: a systematic review and meta-analysis". Journal of General Internal Medicine. 23 (12): 2079–86. doi:10.1007/s11606-008-0787-6. PMC 2596495. PMID 18807098.
- ^ Martin-Cabezas R, Seelam N, Petit C, Agossa K, Gaertner S, Tenenbaum H, Davideau JL, Huck O (October 2016). "Association between periodontitis and arterial hypertension: A systematic review and meta-analysis". American Heart Journal. 180: 98–112. doi:10.1016/j.ahj.2016.07.018. PMID 27659888.
- ^ Noble JM, Borrell LN, Papapanou PN, Elkind MS, Scarmeas N, Wright CB (November 2009). "Periodontitis is associated with cognitive impairment among older adults: analysis of NHANES-III". Journal of Neurology, Neurosurgery, and Psychiatry. 80 (11): 1206–11. doi:10.1136/jnnp.2009.174029. PMC 3073380. PMID 19419981.
- ^ Kaye EK, Valencia A, Baba N, Spiro A, Dietrich T, Garcia RI (April 2010). "Tooth loss and periodontal disease predict poor cognitive function in older men". Journal of the American Geriatrics Society. 58 (4): 713–8. doi:10.1111/j.1532-5415.2010.02788.x. PMC 3649065. PMID 20398152.
- ^ Zadik Y, Bechor R, Galor S, Levin L (May 2010). "Periodontal disease might be associated even with impaired fasting glucose". British Dental Journal. 208 (10): E20. doi:10.1038/sj.bdj.2010.291. PMID 20339371.
- ^ Soskolne WA, Klinger A (December 2001). "The relationship between periodontal diseases and diabetes: an overview". Annals of Periodontology. 6 (1): 91–8. doi:10.1902/annals.2001.6.1.91. PMID 11887477.
- ^ Zadik Y, Bechor R, Galor S, Justo D, Heruti RJ (April 2009). "Erectile dysfunction might be associated with chronic periodontal disease: two ends of the cardiovascular spectrum". The Journal of Sexual Medicine. 6 (4): 1111–1116. doi:10.1111/j.1743-6109.2008.01141.x. PMID 19170861.
- ^ Poyato-Borrego, M.; Segura-Egea, J.-J.; Martín-González, J.; Jiménez-Sánchez, M.-C.; Cabanillas-Balsera, D.; Areal-Quecuty, V.; Segura-Sampedro, J.-J. (27 August 2020). "Prevalence of endodontic infection in patients with Crohn´s disease and ulcerative colitis". Medicina Oral, Patologia Oral y Cirugia Bucal. 26 (2): e208–e215. doi:10.4317/medoral.24135. ISSN 1698-6946. PMC 7980298. PMID 32851982.
- ^ Perk, J.; De Backer, G.; Gohlke, H.; Graham, I.; Reiner, Z.; Verschuren, M. (3 May 2012). "European Guidelines on cardiovascular disease prevention in clinical practice (version 2012): The Fifth Joint Task Force of the European Society of Cardiology and Other Societies on Cardiovascular Disease Prevention in Clinical Practice (constituted by representatives of nine societies and by invited experts) Developed with the special contribution of the European Association for Cardiovascular Prevention & Rehabilitation (EACPR)". European Heart Journal. 33 (13): 1635–1701. doi:10.1093/eurheartj/ehs092. PMID 22555213.
- ^ Michaud, Dominique S.; Izard, Jacques (2014). "Microbiota, Oral Microbiome, and Pancreatic Cancer". The Cancer Journal. 20 (3): 203–206. doi:10.1097/PPO.0000000000000046. PMC 4160879. PMID 24855008.
- ^ "Gingivitis". Mayo Clinic. Rochester, Minnesota: MFMER. 4 August 2017. Retrieved 10 May 2018.
- ^ Crich A (June 1932). "Blastomycosis of the Gingiva and Jaw". Canadian Medical Association Journal. 26 (6): 662–5. PMC 402380. PMID 20318753.
- ^ Urzúa B, Hermosilla G, Gamonal J, Morales-Bozo I, Canals M, Barahona S, Cóccola C, Cifuentes V (December 2008). "Yeast diversity in the oral microbiota of subjects with periodontitis: Candida albicans and Candida dubliniensis colonize the periodontal pockets". Medical Mycology. 46 (8): 783–93. doi:10.1080/13693780802060899. PMID 18608938.
- ^ Matsuo T, Nakagawa H, Matsuo N (1995). "Endogenous Aspergillus endophthalmitis associated with periodontitis". Ophthalmologica. Journal International d'Ophtalmologie. International Journal of Ophthalmology. Zeitschrift für Augenheilkunde. 209 (2): 109–11. doi:10.1159/000310592. PMID 7746643.
- ^ Migliari DA, Sugaya NN, Mimura MA, Cucé LC (1998). "Periodontal aspects of the juvenile form of paracoccidioidomycosis". Revista do Instituto de Medicina Tropical de Sao Paulo. 40 (1): 15–8. doi:10.1590/S0036-46651998000100004. PMID 9713132.
- ^ Lalla E, Cheng B, Lal S, Kaplan S, Softness B, Greenberg E, Goland RS, Lamster IB (April 2007). "Diabetes mellitus promotes periodontal destruction in children". Journal of Clinical Periodontology. 34 (4): 294–8. doi:10.1111/j.1600-051X.2007.01054.x. PMID 17378885.
- ^ "Diabetes and Periodontal Disease". WebMD.
- ^ Obeid P, Bercy P (2000). "Effects of smoking on periodontal health: a review". Advances in Therapy. 17 (5): 230–7. doi:10.1007/BF02853162. PMID 11186143. S2CID 2227017.
- ^ Tomar SL, Asma S (May 2000). "Smoking-attributable periodontitis in the United States: findings from NHANES III. National Health and Nutrition Examination Survey". Journal of Periodontology. 71 (5): 743–51. doi:10.1902/jop.2000.71.5.743. PMID 10872955.
- ^ Ryder MI (2007). "The influence of smoking on host responses in periodontal infections". Periodontology 2000. 43 (1): 267–77. doi:10.1111/j.1600-0757.2006.00163.x. PMID 17214844.
- ^ Pauletto NC, Liede K, Nieminen A, Larjava H, Uitto VJ (January 2000). "Effect of cigarette smoking on oral elastase activity in adult periodontitis patients". Journal of Periodontology. 71 (1): 58–62. doi:10.1902/jop.2000.71.1.58. PMID 10695939.
- ^ Persson L, Bergström J, Gustafsson A (October 2003). "Effect of tobacco smoking on neutrophil activity following periodontal surgery". Journal of Periodontology. 74 (10): 1475–82. doi:10.1902/jop.2003.74.10.1475. PMID 14653394.
- ^ Bergström J, Boström L (July 2001). "Tobacco smoking and periodontal hemorrhagic responsiveness". Journal of Clinical Periodontology. 28 (7): 680–5. doi:10.1034/j.1600-051x.2001.028007680.x. PMID 11422590.
- ^ a b c d e f g "Current Concepts in Periodontal Pathogenesis". DentalUpdate. 31 (10): 570–578. December 2004.
- ^ Peruzzo DC, Benatti BB, Ambrosano GM, Nogueira-Filho GR, Sallum EA, Casati MZ, Nociti FH (August 2007). "A systematic review of stress and psychological factors as possible risk factors for periodontal disease". Journal of Periodontology. 78 (8): 1491–504. doi:10.1902/jop.2007.060371. PMID 17668968.
- ^ a b Watt, RG; Listl, S; Peres, MA; Heilmann, A, eds. (2015). Social inequalities in oral health: from evidence to action (PDF). London: UCL.
- ^ a b Teeuw WJ, Kosho MX, Poland DC, Gerdes VE, Loos BG (1 January 2017). "Periodontitis as a possible early sign of diabetes mellitus". BMJ Open Diabetes Research & Care. 5 (1): e000326. doi:10.1136/bmjdrc-2016-000326. PMC 5337701. PMID 28316794.
- ^ a b c Casanova L, Hughes FJ, Preshaw PM (October 2014). "Diabetes and periodontal disease: a two-way relationship". British Dental Journal. 217 (8): 433–7. doi:10.1038/sj.bdj.2014.907. PMID 25342350.
- ^ Taylor JJ, Preshaw PM, Lalla E (April 2013). "A review of the evidence for pathogenic mechanisms that may link periodontitis and diabetes". Journal of Clinical Periodontology. 40 Suppl 14: S113–34. doi:10.1111/jcpe.12059. PMID 23627323.
- ^ a b c d Kinane DF, Stathopoulou PG, Papapanou PN (June 2017). "Periodontal diseases". Nature Reviews. Disease Primers. 3: 17038. doi:10.1038/nrdp.2017.38. PMID 28805207. S2CID 28018694.
- ^ a b Armitage GC (December 1999). "Development of a classification system for periodontal diseases and conditions". Annals of Periodontology. 4 (1): 1–6. doi:10.1902/annals.1999.4.1.1. PMID 10863370. S2CID 24243752.
- ^ "The Periodontal Disease Classification System of the American Academy of Periodontology – An Update". American Academy of Periodontology.
- ^ Jepsen S, Caton JG, Albandar JM, Bissada NF, Bouchard P, Cortellini P, Demirel K, de Sanctis M, Ercoli C, Fan J, Geurs NC, Hughes FJ, Jin L, Kantarci A, Lalla E, Madianos PN, Matthews D, McGuire MK, Mills MP, Preshaw PM, Reynolds MA, Sculean A, Susin C, West NX, Yamazaki K (June 2018). "Periodontal manifestations of systemic diseases and developmental and acquired conditions: Consensus report of workgroup 3 of the 2017 World Workshop on the Classification of Periodontal and Peri-Implant Diseases and Conditions" (PDF). Journal of Clinical Periodontology. 45 Suppl 20: S219–S229. doi:10.1111/jcpe.12951. PMID 29926500.
- ^ Berglundh T, Armitage G, Araujo MG, Avila-Ortiz G, Blanco J, Camargo PM, Chen S, Cochran D, Derks J, Figuero E, Hämmerle CH, Heitz-Mayfield LJ, Huynh-Ba G, Iacono V, Koo KT, Lambert F, McCauley L, Quirynen M, Renvert S, Salvi GE, Schwarz F, Tarnow D, Tomasi C, Wang HL, Zitzmann N (June 2018). "Peri-implant diseases and conditions: Consensus report of workgroup 4 of the 2017 World Workshop on the Classification of Periodontal and Peri-Implant Diseases and Conditions". Journal of Clinical Periodontology. 45 Suppl 20: S286–S291. doi:10.1111/jcpe.12957. PMID 29926491.
- ^ a b c Caton JG, Armitage G, Berglundh T, Chapple IL, Jepsen S, Kornman KS, Mealey BL, Papapanou PN, Sanz M, Tonetti MS (June 2018). "A new classification scheme for periodontal and peri-implant diseases and conditions – Introduction and key changes from the 1999 classification" (PDF). Journal of Periodontology. 89 Suppl 1: S1–S8. doi:10.1002/jper.18-0157. PMID 29926946. S2CID 49353912.
- ^ a b "Staging and Grading Periodontitis" (PDF).
- ^ Stambaugh RV, Dragoo M, Smith DM, Carasali L (1981). "The limits of subgingival scaling". The International Journal of Periodontics & Restorative Dentistry. 1 (5): 30–41. PMID 7047434.
- ^ Waerhaug J (January 1978). "Healing of the dento-epithelial junction following subgingival plaque control. I. As observed in human biopsy material". Journal of Periodontology. 49 (1): 1–8. doi:10.1902/jop.1978.49.1.1. PMID 340634.
- ^ Waerhaug J (March 1978). "Healing of the dento-epithelial junction following subgingival plaque control. II: As observed on extracted teeth". Journal of Periodontology. 49 (3): 119–34. doi:10.1902/jop.1978.49.3.119. PMID 288899.
- ^ Kaldahl WB, Kalkwarf KL, Patil KD, Molvar MP, Dyer JK (February 1996). "Long-term evaluation of periodontal therapy: II. Incidence of sites breaking down". Journal of Periodontology. 67 (2): 103–8. doi:10.1902/jop.1996.67.2.103. PMID 8667129.
- ^ Hirschfeld L, Wasserman B (May 1978). "A long-term survey of tooth loss in 600 treated periodontal patients". Journal of Periodontology. 49 (5): 225–37. doi:10.1902/jop.1978.49.5.225. PMID 277674.
- ^ Kalsi R, Vandana KL, Prakash S (October 2011). "Effect of local drug delivery in chronic periodontitis patients: A meta-analysis". Journal of Indian Society of Periodontology. 15 (4): 304–9. doi:10.4103/0972-124X.92559. PMC 3283924. PMID 22368351.
- ^ Nadig PS, Shah MA (2016). "Tetracycline as local drug delivery in treatment of chronic periodontitis: A systematic review and meta-analysis". Journal of Indian Society of Periodontology. 20 (6): 576–583. doi:10.4103/jisp.jisp_97_17. PMC 5713079. PMID 29238136.
- ^ Bertl K, Parllaku A, Pandis N, Buhlin K, Klinge B, Stavropoulos A (December 2017). "The effect of local and systemic statin use as an adjunct to non-surgical and surgical periodontal therapy-A systematic review and meta-analysis". Journal of Dentistry. 67: 18–28. doi:10.1016/j.jdent.2017.08.011. hdl:2043/23307. PMID 28855141.
- ^ Khattri S, Kumbargere Nagraj S, Arora A, Eachempati P, Kusum CK, Bhat KG, Johnson TM, Lodi G (2020). "Adjunctive systemic antimicrobials for the non‐surgical treatment of periodontitis". Cochrane Database of Systematic Reviews. 11 (11): 1465–1858. doi:10.1002/14651858.CD012568.pub2. PMID 33197289. S2CID 226990528. CD012568.
- ^ Khattri, Shivi; Kumbargere Nagraj, Sumanth; Arora, Ankita; Eachempati, Prashanti; Kusum, Chandan Kumar; Bhat, Kishore G; Johnson, Trevor M; Lodi, Giovanni (16 November 2020). "Adjunctive systemic antimicrobials for the non-surgical treatment of periodontitis". Cochrane Database of Systematic Reviews. 11: CD012568. doi:10.1002/14651858.cd012568.pub2. ISSN 1465-1858. PMID 33197289. S2CID 226990528.
- ^ a b c d Caton J, Ryan ME (February 2011). "Clinical studies on the management of periodontal diseases utilizing subantimicrobial dose doxycycline (SDD)". Pharmacological Research. 63 (2): 114–20. doi:10.1016/j.phrs.2010.12.003. PMID 21182947.
- ^ . Liviu Steier, Silvia Dias de Oliveira, José Antonio Poli de Figueiredo. "Bacteriophages in Dentistry—State of the Art and Perspectives". Dent J (Basel). 7 (1): 6. 2019. doi:10.3390/dj7010006. PMC 6473837. PMID 30634460.
{{cite journal}}: CS1 maint : 기타(링크) - ^ Preus HR, Anerud A, Boysen H, Dunford RG, Zambon JJ, Löe H (September 1995). "The natural history of periodontal disease. The correlation of selected microbiological parameters with disease severity in Sri Lankan tea workers". Journal of Clinical Periodontology. 22 (9): 674–8. doi:10.1111/j.1600-051X.1995.tb00825.x. PMID 7593696.
- ^ Ekanayaka A (April 1984). "Tooth mortality in plantation workers and residents in Sri Lanka". Community Dentistry and Oral Epidemiology. 12 (2): 128–35. doi:10.1111/j.1600-0528.1984.tb01425.x. PMID 6584263.
- ^ "Mortality and Burden of Disease Estimates for WHO Member States in 2002" (xls). World Health Organization. 2002.
- ^ Vos T, Flaxman AD, Naghavi M, Lozano R, Michaud C, Ezzati M, et al. (December 2012). "Years lived with disability (YLDs) for 1160 sequelae of 289 diseases and injuries 1990–2010: a systematic analysis for the Global Burden of Disease Study 2010". Lancet. 380 (9859): 2163–96. doi:10.1016/S0140-6736(12)61729-2. PMC 6350784. PMID 23245607.
- ^ Zadik Y, Bechor R, Shochat Z, Galor S (April 2008). "[Ethnic origin and alveolar bone loss in Israeli adults]". Refu'at Ha-Peh Veha-Shinayim (in Hebrew). 25 (2): 19–22, 72. PMID 18780541.
- ^ Forshaw, R. J. (April 2009). "Dental health and disease in ancient Egypt". British Dental Journal. 206 (8): 421–424. doi:10.1038/sj.bdj.2009.309. PMID 19396207. S2CID 24832214.
- ^ "Roman-Britons had less gum disease than modern Britons". HeritageDaily – Archaeology News. 24 October 2014. Retrieved 22 April 2020.
- ^ Harper, Douglas. "periodontitis". Online Etymology Dictionary. Harper, Douglas. "periodontal". Online Etymology Dictionary. ὀδούς, ὀδών. 리델, 헨리 조지; 스콧, 로버트; 페르세우스 프로젝트의 그리스-영어 렉시콘.
- ^ πυόρροια, πύον, ῥοή; cf. 리델과 스콧에서 πυρρωωωωωωωωωω. Harper, Douglas. "-ia". Online Etymology Dictionary.
- ^ "pyorrhea". Merriam-Webster Online.
- ^ Listl S, Galloway J, Mossey PA, Marcenes W (October 2015). "Global Economic Impact of Dental Diseases". Journal of Dental Research. 94 (10): 1355–61. doi:10.1177/0022034515602879. PMID 26318590. S2CID 39147394.
- ^ Dewhirst FE, Klein EA, Thompson EC, Blanton JM, Chen T, Milella L, Buckley CM, Davis IJ, Bennett ML, Marshall-Jones ZV (2012). "The canine oral microbiome". PLOS ONE. 7 (4): e36067. Bibcode:2012PLoSO...736067D. doi:10.1371/journal.pone.0036067. PMC 3338629. PMID 22558330.
- ^ Muller-Esnault, Susan (2009). "Periodontal Disease in the Dog and Cat". Critterology. Veterinary Internet Company. Archived from the original on 27 August 2014. Retrieved 12 March 2009.