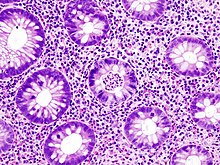
궤양성 대장염
Ulcerative colitis| 궤양성 대장염 | |
|---|---|
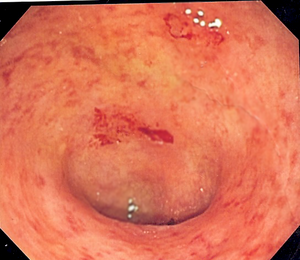 | |
| 궤양성 대장염에 걸린 결장의 내시경 영상.결장의 안쪽 표면이 얼룩지고 군데군데 부러져 있다.가벼운 병. | |
| 전문 | 위장병학 |
| 증상 | 복통, 설사, 혈액 혼합, 체중 감소, 발열,[1] 빈혈, 탈수, 식욕부진, 피로, 피부 통증, 급변, 급변에도 배변 불능, 직장[2] 통증 |
| 합병증 | 메가콜론, 눈, 관절, 간 염증, 대장암[1][3] |
| 통상적인 개시 | 15~30년 또는 60년[1] 이상 |
| 지속 | 장기[1] |
| 원인들 | 불명[1] |
| 진단 방법 | 조직 생체[1] 검사를 통한 대장 내시경 검사 |
| 차동 진단 | 이질, 크론병, 허혈성 대장염[4] |
| 치료 | 식생활의 변화, 약물, 수술[1] |
| 약 | 술파살라진, 메살라진, 스테로이드, 아자티오프린 등의 면역억제제, 생물학적 치료제[1] |
| 빈도수. | 100,000개당[5] 2개씩 |
| 사망. | 47,400과 Crohn's(2015년)[6]를 합친수 |
궤양성 대장염은 대장과 [1][7]직장에 염증과 궤양을 일으키는 장기 질환이다.활동성 질환의 주요 증상은 복통과 피가 [1]섞인 설사이다.체중 감소, 발열, 빈혈도 발생할 [1]수 있다.종종, 증상은 천천히 나타나며 가벼운 것부터 심각한 [1]것까지 다양합니다.증상은 보통 플레어 사이에 증상이 없는 [1]기간 동안 간헐적으로 발생합니다.합병증에는 대장(메가콜론), 눈, 관절, 간 등의 염증, 대장암이 [1][3]포함될 수 있습니다.
UC의 원인은 불명.[1]이론에는 면역 체계 기능 장애, 유전학, 정상적인 장내 세균의 변화, 그리고 환경적 [1][8]요인이 포함됩니다.선진국에서 발병률이 더 높은 경향이 있는데, 일부는 이것이 장내 감염이나 서구식 식단과 [7][9]생활습관에 덜 노출된 결과라고 주장한다.어린 나이에 맹장을 제거하는 것이 [9]보호적일 수 있습니다.진단은 일반적으로 조직 생체검사와 함께 대장내시경 검사를 [1]통해 이루어집니다.그것은 크론병, 현미경 [1]대장염과 함께 염증성 대장 질환의 일종이다.
고열량 식단이나 무유당 식단을 유지하는 것과 같은 식단 변화는 [1]증상을 개선할 수 있습니다.메살라진이나 술파살라진과 같은 아미노살리실산염, 스테로이드제, 아자티오프린과 같은 면역억제제, 그리고 생물학적 [1]치료를 포함한 여러 약물이 증상을 치료하고 완화를 가져오고 유지하기 위해 사용된다.병이 심하거나 치료에 효과가 없거나 대장암과 같은 [1]합병증이 생기면 수술로 결장을 제거해야 할 수도 있다.결장과 직장의 제거는 일반적으로 [1][9]그 상태를 낫게 한다.
크론병과 함께,[10] 2015년[update] 현재 약 1,120만 명의 사람들이 영향을 받았다.매년 인구 10만명당 1~20명꼴로 발생하며,[7][9] 10만명당 5~500명꼴로 발병한다.이 병은 다른 [9]지역보다 북미와 유럽에서 더 흔하다.종종 15세에서 30세 사이 또는 [1]60세 이상의 사람들에게서 발병한다.남성과 여성은 동일한 [7]비율로 영향을 받는 것으로 보입니다.그것은 또한 1950년대부터 [7][9]더 흔해졌다.궤양성 대장염과 크론병은 미국에서 [11]약 100만 명의 사람들에게 영향을 미친다.적절한 치료를 받으면 사망 위험은 일반 인구의 [3]사망 위험과 동일하게 나타난다.궤양성 대장염에 대한 최초의 [9]설명은 1850년대에 발생했다.
징후 및 증상
| 크론병 | 궤양성 대장염 | |
|---|---|---|
| 배변 | 종종 죽과 [12]같기도 하고 때때로 지방질 | 점액과 같은 경우가 많다. 그리고[12] 피로 |
| 테네스무스 | 일반적이지[12] 않다 | 보다[12] 일반적인 |
| 열. | 공통[12] | 중증질환을[12] 나타냅니다. |
| 피스툴레 | 공통[13] | 드물게 |
| 체중 감량 | 자주 | 거의 없다 |
위장
궤양성 대장염을 가진 사람들은 대개 [14]피를 섞은 설사를 하며 장기간(주) 지속되는 점진적 발병을 보인다.추가적인 증상으로는 변실금, 배변 빈도 증가, 점액 배출, 야간에 [14]배변 등이 있을 수 있다.항문염(직장의 염증)과 함께, UC를 앓고 있는 사람들은 긴급성이나 직장 테네스를 경험할 수 있는데,[14] 이것은 변이 거의 나오지 않는 긴급한 욕구이다.텐스무스는 변이 적은데도 변비가 되고 싶은 충동으로 인해 변비로 오인될 수 있다.유혈 설사와 복통은 심각한 질병에서 [14]더 두드러진 특징일 수 있다.UC의 복통의 심각도는 가벼운 불편함에서 매우 고통스러운 배변과 복부 [15]경련에 이르기까지 다양하다.높은 빈도의 배변, 체중 감소, 메스꺼움, 피로, 발열 또한 질병 플레어 동안 흔하다.만성 GI기관 출혈, 만성 염증, 철분 결핍은 종종 빈혈로 이어져 삶의 [16]질에 영향을 미칠 수 있다.
궤양성 대장염의 임상적 징후는 질병 [17]진행의 정도에 따라 달라진다.증상의 [14]최초 발생 시 최대 15%의 사람들이 심각한 질병을 가질 수 있다.진행 중인 증상(임상적 완화) 없이 UC 병력이 있는 사람 중 상당수(45%)가 진행 중인 [18]염증의 객관적 증거를 가지고 있다.궤양성 대장염은 신체의 많은 부분에 영향을 미칠 수 있는 일반적인 염증 과정과 관련이 있다.때때로, 이러한 연관된 장외 증상들은 질병의 [19]초기 징후이다.
관여 범위
대장 밖의 위장관에 영향을 미칠 수 있는 크론병과는 대조적으로 궤양성 대장염은 보통 대장에만 국한된다.궤양성 대장염의 염증은 일반적으로 직장과 관련되며 근위부(S자형 결장, 상행 결장 등)[20]로 확장된다.이와는 대조적으로, 크론병에 의한 염증은 소위 "건너뛰기 병변"[21]과 함께 종종 부분적이다.
이 질병은 질병의 [15]확장에 따라 관련 정도에 따라 분류된다: 항문염(직장염), 좌뇌대장염(하행결장염), 그리고 광범위한 대장염(하행결장에 [20]가까운 염증).항문암염은 직장과 S자 결장의 염증을 말합니다.판콜리티스는 직장부터 맹장까지 전체 결장의 관여를 말한다.보통 크론병과 관련이 있지만, 회장염(회장의 염증)도 UC에서 발생한다.UC를 가진 사람들의 약 17%가 회장염을 [22]가지고 있다.회장염은 판콜리티스의 환경에서 더 흔하게 발생하며,[14] 대장염의 활동과 관련이 있는 경향이 있다.소위 "역류성 회장염"이라고 불리는 이 질환은 판골염을 가진 사람의 10-20%에서 발생할 수 있으며 임상적으로 거의 [23]중요하지 않은 것으로 여겨진다.
질환의 심각도
UC는 관련 정도에 더하여 질병의 [20]심각성을 특징으로 합니다.질병의 심각도는 증상, 염증의 객관적 지표(내시경 소견, 혈액 검사), 질병 과정, 그리고 질병이 [20]일상생활에 미치는 영향에 의해 정의된다.가벼운 질병은 하루에 4개 미만의 대변과 관련이 있으며, 또한 가벼운 긴급성과 직장 출혈이 [20]간헐적으로 발생할 수 있습니다.가벼운 질병은 전신 독성의 징후가 없고 혈청 염증 마커(적혈구 침강 속도 및 C 반응 단백질)[citation needed]의 정상 수준을 보인다.
중간에서 심각한 질병은 하루에 6개 이상의 대변, 잦은 혈변, [20]긴급성과 관련이 있다.중간 정도의 복통, 저열, 38~39°C(100~102°F), 빈혈(정상 75%)이 [20]나타날 수 있다.발열, 빈맥, 빈혈 또는 ESR 또는 [20]CRP 상승으로 나타나는 독성이 존재한다.
극성 질환은 매일 10회 이상의 배변, 지속적인 출혈, 독성, 복부 압통 및 확장, 수혈 필요성, 대장 확장(확장)과 관련이 있다.극성 UC를 가진 사람들은 점막층 너머로 확장되는 염증을 가지고 있을 수 있으며, 이는 결장운동성 장애를 유발하고 독성 메가콜론으로 이어질 수 있다.장막과 관련된 경우 결장 천공이 [citation needed]발생할 수 있습니다.
궤양성 대장염은 호전되어 완화될 수 있다.질병의 완화는 대변의 형성, 혈청 설사의 부재, 긴급성의 해결, 혈청 염증 [20]마커의 정상 수치에 의해 특징지어진다.
제한적 증상 및 합병증
| 크론스 질병 | 궤양 대장염 | ||
|---|---|---|---|
| 영양소 결핍 | 리스크가 높다 | ||
| 대장암 위험 | 경미하다 | 고려하는 | |
| 근막외 합병증의[24][25][26] 유병 | |||
| 홍채염/포막염 | 여성 | 2.2% | 3.2% |
| 남성 | 1.3% | 0.9% | |
| 일차 경화 담관염 | 여성 | 0.3% | 1% |
| 남성 | 0.4% | 3% | |
| 안킬로징 척추염 | 여성 | 0.7% | 0.8% |
| 남성 | 2.7% | 1.5% | |
| 표피목 신경절 | 여성 | 1.2% | 0.8% |
| 남성 | 1.3% | 0.7% | |
| 홍반결절 | 여성 | 1.9% | 2% |
| 남성 | 0.6% | 0.7% | |
UC는 면역 조절 장애와 전신 염증으로 특징지어지는데, 이는 대장 밖에서 증상과 합병증을 일으킬 수 있다.일반적으로 영향을 받는 장기는 눈, 관절, 피부, [27]간이다.그러한 제한적 증상 빈도는 6~47%[28][29]로 보고되었다.
UC는 입안에 영향을 줄 수 있습니다.UC에 걸린 사람들의 약 8%가 구강 [30]증상을 보인다.가장 흔한 두 가지 구강 증상은 애프터성 구내염과 각질성 [30]구강염이다.애프터성 구내염은 양성이고, 화끈거리지 않으며 종종 재발하는 구강 궤양이 특징입니다.각질 킬레이트염은 입꼬리가 붉어지는 것이 특징이며,[30] 이는 피부에 아픈 상처나 골절을 포함할 수 있다.매우 드물게, 양성 농포가 입안에서 발생할 수 있다.[30]
UC는 눈에 영향을 줄 수 있습니다.눈 안쪽에서 염증이 발생하여 포도막염과 [31]홍채염이 발생할 수 있습니다.포도막염은 특히 빛에 노출되었을 때 시야가 흐릿해지고 눈의 통증을 유발할 수 있습니다.포도막염은 치료하지 않으면 영구적인 시력 [31]감퇴를 초래할 수 있다.염증은 또한 눈의 흰 부분(스크레라)이나 위에 덮인 결합 조직(에피소라)[32]을 포함할 수 있으며, 강막염과 회백염이라고 불리는 상태를 야기합니다.포도막염과 홍채염은 궤양성 대장염과 [33]더 흔하게 연관되어 있는 반면, 회백염은 크론병과 [33]더 흔하게 연관되어 있다.
UC는 혈청성 관절염으로 알려진 류마티스 질환의 유형을 포함하여 몇 가지 관절 증상을 일으킬 수 있으며, 이는 소수의 큰 관절(고관절염), 척추(강직성 척추염), 손발의 여러 작은 관절(말초 관절염)[27]에 영향을 미칠 수 있습니다.종종 근육이 뼈에 붙는 삽입 부위가 염증(관절염)을 일으킨다.염증은 천골관절에 영향을 미칠 수 있다.[19]관절염의 증상에는 관절통, 붓기, 삼출 등이 있으며 종종 상당한 [19]질병으로 이어진다.
궤양성 대장염은 피부에 영향을 미칠 수 있다.피부 증상의 가장 흔한 유형인 홍반 결절은 [33]융기하면서 정강이에 나타나는 부드러운 붉은 결절을 나타냅니다.결절 홍반은 피하조직의 염증(범결막염)에 의한 것이다.더 심각한 피부 증상인 화피강개막은 궤양이 되는 고통스러운 농포 또는 결절이 특징이며, 이는 점차적으로 성장한다.결절 홍반은 궤양성 대장염의 활동과 관련이 있고 종종 대장염의 치료와 함께 개선되는 경향이 있는 반면, 화피증은 UC 질환의 [27]활동과는 독립적으로 발생할 수 있다.몇몇 경우에, 화피강개노섬은 [27]코르티코스테로이드를 주입해야 할 수 있다.
궤양성 대장염은 혈액과 내분비계에 영향을 미칠 수 있다.UC는 [34][35][36]혈전의 위험을 증가시킨다; 아랫다리의 통증은 깊은 정맥 혈전증의 징후일 수 있는 반면 호흡곤란은 폐색전증(폐의 혈전)의 결과일 수 있다.혈전의 위험은 [35]IBD가 있는 사람에게서 약 3배 더 높다.정맥혈전 색전증의 위험은 염증으로 인한 응고성,[34] 특히 활동적이거나 광범위한 질병으로 인해 궤양성 대장염에서 높다.추가적인 위험 요소로는 수술, 입원, 임신, 코르티코스테로이드 및 토파치티니브의 [34]사용이 포함될 수 있다.면역체계가 적혈구를 공격하여 자가면역성 용혈성 빈혈로 이어질 수 있다.자가면역 파괴 외에도 직장출혈로 인한 만성 출혈과 염증으로 인한 골수 억제(지질병 빈혈)로 빈혈이 발생할 수 있다.골다공증은 [19]골절의 위험을 높이는 전신 염증과 관련이 있을 수 있다.손가락 끝의 변형인 몽둥이가 발생할 [19]수 있습니다.아밀로이드증은, 특히 심각하고 잘 통제되지 않는 질병과 함께 발생할 수 있는데, 이것은 보통 소변에 단백질이 포함되어 있고 신장염 [19]증후군을 나타냅니다.
원발성 경화성 담관염
궤양성 대장염은 크고 작은 담관의 진행성 염증 질환인 1차 경화 담관염(PSC)과 유의미한 관련이 있다.원발성 경화성 담관염을 가진 사람들의 70-90%가 궤양성 대장염을 [33]앓고 있다.궤양성 대장염을 가진 사람들의 5%가 원발성 경화성 [27][37]담관염으로 진행될 수 있다.PSC는 남성들에게서 더 흔하며,[27] 종종 30세에서 40세 사이에 발병한다.원발성 경화성 담관염은 궤양성 대장염의 장 증상이 [33]나타나기 몇 년 전에 발생하는 경우가 있다.PSC는 궤양성 [33]대장염에서 대장염의 시작, 범위, 지속시간 또는 활동을 병행하지 않는다.또한 결장절제술은 [33]UC환자의 1차 경화성 담관염 과정에 영향을 미치지 않는다.PSC는 대장암과 담관암(담관암)[33][27]의 위험 증가와 관련이 있다.PSC는 진행성 질환으로 [27]간경화를 일으킬 수 있습니다.PSC의 [27]장기 경과에 영향을 미치는 특별한 치료법은 아직 입증되지 않았다.
원인들
| 크론병 | 궤양성 대장염 | |
|---|---|---|
| 흡연석을 부탁해요. | 흡연자의 위험 증가 | 흡연자의 위험[20] 감소 |
| 나이 | 사이의 통상적인 개시 15년, 30년[38] | 사이의 피크 발생률 15년 및 25년 |
궤양성 대장염은 T세포가 [39]대장에 침투하는 것이 특징인 자가면역질환이다.UC의 직접적인 원인은 알려져 있지 않지만, 유전학, 환경, 그리고 과잉 활동적인 면역 체계와 같은 요소들이 [1]한 역할을 한다.UC는 소화계 밖의 [citation needed]신체 많은 부분에서 증상을 일으키는 동반 질환과 관련이 있다.
유전적 요인
UC의 원인에 대한 유전적 구성요소는 가족 내 UC의 집계, 다른 민족 간의 유병률 변화, 유전적 표지 및 [40]연결을 바탕으로 가설화할 수 있다.또한 동일한 쌍둥이 일치율은 10%인 반면, 결합자 쌍둥이 일치율은 3%[40][41]에 불과합니다.궤양성 대장염 환자의 8~14%가 염증성 [14]장질환 가족력이 있다.게다가, UC와 친척 관계가 1학위인 사람들은 그 [14]병에 걸릴 위험이 4배 증가한다.
게놈의 12개 부위가 UC에 연결되어 있을 수 있으며, 발견 순서로는 16, 12, 6, 14, 5, 19, 1, [42]3번 염색체를 포함하지만, 이러한 위치 중 단층인 것은 일관되게 나타나지 않고 있어 이 질환이 여러 유전자의 영향을 받고 있음을 시사한다.예를 들어 염색체 밴드 1p36은 염증성 [43]장질환과 관련이 있다고 생각되는 영역 중 하나이다.추정 영역 중 일부는 OCTN1 및 OCTN2와 같은 트랜스포터 단백질을 부호화한다.다른 잠재적 영역에는 MAGUK 패밀리와 같은 세포 발판 단백질이 포함됩니다.인간 백혈구 항원 연합이 작동할 수도 있다.사실, 6번 염색체에 대한 이러한 연결은 가장 설득력 있고 유전자 [42]후보들과 일치할 수 있다.
다발성 자가면역장애는 소아지방염,[44] 건선,[45] 홍반성 [46]낭창, 류마티스 [47]관절염, 상피염,[31] 강막염을 포함한 궤양성 대장염과 관련이 있다.궤양성 대장염은 또한 급성 간헐성 포르피린증과 [48]관련이 있다.
환경 요인
식이요법, 모유 수유, 약물 치료를 포함한 궤양성 대장염의 병인에 기여하는 환경적 요인에 대한 많은 가설이 제기되어 왔다.모유 수유는 궤양성 대장염의 [49][50]발생에 보호 효과가 있을 수 있다.이소트레티노인에 대한 한 연구는 [51]UC의 비율이 약간 증가했음을 발견했다.
대장은 염증을 촉진할 수 있는 많은 식이 물질에 노출되어 있기 때문에, 식이 요인들은 궤양성 대장염과 크론병의 병인에 모두 영향을 미친다는 가설이 있다.그러나, 현재의 연구는 식사와 궤양성 대장염의 발병 사이의 연관성을 보여주지 않는다.그러한 연관성을 조사한 [52]연구는 거의 없다; 한 연구는 궤양성 대장염에 걸린 사람들의 수에 정제당의 연관성을 보여주지 않았다.불포화지방과 비타민 B6의 높은 섭취는 궤양성 대장염에 [53]걸릴 위험을 높일 수 있다.질병의 발병 및/또는 재발에 영향을 미칠 수 있는 다른 확인된 식이 요인에는 육류 단백질 및 알코올 [54][55]음료가 포함된다.구체적으로 유황은 궤양성 대장염의 원인에 관여하고 있는 것으로 조사되고 있습니다만,[56] 이것은 논란이 되고 있습니다.유황 제한 식단은 UC와 그 질병의 동물 모델을 가진 사람들에게서 조사되었다.황의 병인설은 [57][58][59]식사와 더불어 내장 미생물 및 점막 황화물 해독과 관련이 있다.
대체 이론
황산염을 감소시키는 세균의 수치는 궤양성 대장염이 있는 사람에게 더 높은 경향이 있는데, 이것은 장에서 황화수소의 수치가 더 높을 수 있다.다른 이론은 이 질병의 증상이 [60]장내 세포에 있는 황화수소의 독성 작용에 의해 야기될 수 있다는 것을 암시한다.
궤양성 대장염과 크론병의 [61]궁극적인 원인으로는 아종인 파라결핵인 마이코박테륨아비움 감염이 제시되고 있다.
병태생리학
| 크론병 | 궤양성 대장염 | |
|---|---|---|
| 사이토카인 반응 | T17h[62] 관련 | T2와h 막연하게 관련지어짐 |
궤양성 대장염에 걸린 일부 사람들에게서 대장 황산염을 감소시키는 세균의 양이 증가하여 유독한 가스 황화수소의 농도가 높아졌습니다.인간의 대장 점막은 라미나 프로프리아에 있는 대장 상피 장벽과 면역 세포에 의해 유지된다.짧은 사슬 지방산인 N-부틸레이트는 베타 산화 경로를 통해 이산화탄소와 케톤체로 산화됩니다.N-낙산염은 이 상피 장벽에 영양소를 공급하는 것을 돕는 것으로 나타났다.연구에 따르면 황화수소는 짧은 사슬의 아세틸-CoA 탈수소효소를 방해함으로써 베타 산화 경로를 손상시키는 역할을 한다.또한 궤양성 대장염 흡연의 보호효과는 담배연기와 황화수소가 반응하여 무독성 이소티오시아네이트를 생성함으로써 황화물이 [63]경로를 방해하는 것을 억제하기 때문이라는 것이 제시되었다.관련 없는 연구는 [60]붉은 고기와 알코올에 함유된 황이 완화 중인 사람들에게 재발의 위험을 증가시킬 수 있다는 것을 시사했다.
진단.

궤양성 대장염의 초기 진단 작업은 완전한 병력과 신체 검사, 징후와 증상의 평가, 실험실 검사와 [64]내시경 검사로 구성됩니다.특정 테스트에는 다음이 포함됩니다.[20][65]
- 빈혈 여부를 확인하기 위해 전체 혈소판수치가 측정되며, 혈소판수치가 높은 혈소판수치가 가끔 관찰됩니다
- 만성 설사는 저칼륨혈증, 저자석혈증, 신장 손상과 관련이 있을 수 있으므로 전해질 연구와 신장 기능 검사를 실시합니다.
- 간 기능 검사는 담관 관련을 선별하기 위해 수행된다: 일차 경화성 담관염.
- 천공 또는 독성 메가콜론의 가능성을 평가하기 위한 X선 또는 CT 스캔 등의 이미징
- 감염성 대장염을[64] 배제하기 위한 변 배양 및 클로스트리디오이데스 디피실 변 분석
- 적혈구 침강속도 또는 C반응성 단백질과 같은 염증성 마커
- 직장 및 원위대장(Sigmoidoscopy) 또는 대장 전체 및 소장 말단(대장내시경)을 평가하기 위한 하부 내시경 검사
궤양성 대장염은 원인을 알 수 없는 질환이지만,[20] 이 질환을 유발하는 것으로 생각되는 특이한 요인에 대해 조사해야 한다.
단순임상대장염 활동지수는 1998년에 작성되었으며 [66][67]증상의 심각성을 평가하는 데 사용된다.
내시경
궤양성 대장염을 진단하기 위한 가장 좋은 검사는 플렉시블 카메라를 사용하여 장내 표면을 검사하는 내시경 검사입니다.처음에는 유연한 S자형 내시경을 완료하여 [68]진단을 확립할 수 있습니다.의사는 대장 천공 위험을 최소화하기 위해 심각한 대장염이 발생할 경우 초기 검사의 범위를 제한할 수 있습니다.그러나 크론병을 배제하고 질병의 [68]범위와 심각도를 평가하기 위해 회장 말기 진입과 함께 완전한 대장내시경 검사를 수행해야 한다.궤양성 대장염의 내시경 소견은 홍반(점막의 붉은색), 점막의 취약성, 표면 궤양, 그리고 대장의 혈관 외관 상실을 포함한다.궤양이 있을 경우 궤양이 합류할 수 있습니다.의사 폴립이 [69]관찰될 수 있습니다.
궤양성 대장염은 보통 직장부터 계속되며, 직장은 거의 보편적으로 관련된다.항문 주위 질환은 드물다.내시경적으로 관여하는 정도는 항문염(직장염)에서 좌뇌대장염(하행결장까지 확장) 및 광범위한 대장염(하행결장 근위부에서 [15]하행결장까지 확장)
조직학
점막의 생체검사는 내시경 검사에서 UC의 진단을 확인하고 임상적으로 다르게 관리되는 크론병과의 구별을 위해 실시합니다.궤양성 대장염의 조직학적 소견은 점막(림프구, 혈장세포 및 과립구)[27]의 크립트 구조, 크립트 농양 및 염증 세포의 왜곡을 포함한다.크론병에서 볼 수 있는 경막염과는 달리 궤양성 대장염의 염증은 [27]점막에 국한된다.
실험실 테스트
혈액과 대변 검사는 주로 질병의 심각성, 염증 정도를 평가하고 감염성 대장염의 원인을 배제하는 역할을 한다.궤양성 대장염이 의심되는 모든 사람들은 [14]감염을 배제하기 위해 대변 검사를 받아야 한다.
완전한 혈액 수치는 빈혈, 백혈구 증가 또는 혈소판 [14]증가증을 나타낼 수 있다.빈혈은 염증이나 출혈로 인해 발생할 수 있다.만성 출혈은 빈혈의 원인으로 철분 결핍을 초래할 수 있으며, 특히 혈청 페리틴, 철분, 총 철분 결합 능력 및 트랜스페린 포화로 평가할 수 있는 미세 적혈구 빈혈(소형 적혈구)을 유발할 수 있다.빈혈은 [70]아자티오플린이나 엽산 결핍을 일으킬 수 있는 술파살라딘에 의한 치료의 합병증 때문일 수 있다.티오푸린 대사물과 엽산 수치가 도움이 될 [71]수 있습니다.
UC는 CRP 및 ESR과 같은 혈청 염증 마커로 정량화할 수 있는 높은 수준의 염증을 몸 전체에 일으킬 수 있습니다.그러나 염증 마커는 UC에 특정되지 않으며 염증 마커는 감염을 포함한 다른 조건에서 흔히 볼 수 있습니다.또한 궤양성 대장염 환자에서는 염증 마커가 균일하게 상승하지 않는다.내시경 검사에서 염증이 확인된 사람의 25%는 정상적인 CRP [20]수치를 가지고 있다.혈청 알부민은 출혈과 대장염과 관련된 GI 관로의 단백질 손실 외에도 염증과 관련이 적을 수 있다.낮은 혈청 수준의 비타민 D는 UC와 관련이 있지만, 이 발견의 중요성은 [72]불분명합니다.
궤양성 대장염에서는 특이 항체 마커가 높아질 수 있다.구체적으로 [20]UC의 경우 70%에서 핵주위로 항중수소세포질항체(PANCA)가 발견된다.사카로미세스 세레비시아에 대한 항체가 존재할 수 있지만 궤양성 대장염에 비해 크론병에서 더 자주 양성입니다.그러나 이러한 혈청학적 테스트의 정확도가 낮기 때문에 가능한 염증성 대장 [20][27]질환의 진단 평가에 도움이 되지 않습니다.
몇몇 대변 검사는 결장과 직장에 존재하는 염증의 정도를 정량화하는 데 도움을 줄 수 있다.분변 칼프로텍틴은 대장에 영향을 미치는 염증 조건에서 증가하며, 염증성 대장 [20]질환에서 과민성 대장 증후군(비염증성)과 플레어를 구별하는 데 유용하다.분변 칼프로텍틴은 88% 민감하고 궤양성 대장염 진단에 79%[20] 특이적이다.분변 칼프로텍틴이 낮으면 염증성 장질환의 가능성은 1%[14] 미만이다.락토페린은 장염의 [73]추가적인 비특이적 지표이다.
이미징
X-ray 또는 CT 스캔과 같은 영상 검사는 천공이나 독성 메가콜론과 같은 궤양성 대장염의 합병증을 평가하는 데 도움이 될 수 있습니다.대장 초음파(US)는 UC를 포함한 염증성 장질환(IBD) 환자 관리를 위한 비용 효율적이고, 잘 경화되며, 비침습적이며,[74] 쉽게 사용할 수 있는 도구입니다.최근 일부 연구는 US가 [75][76]UC 환자의 질병 활동을 평가하는 정확한 도구라는 것을 증명했다.그 외에는 궤양성 대장염을 [14][27]진단하는 데 영상이 제한적으로 사용된다.자기공명영상(MRI)은 기본 PSC를 [27]진단하기 위해 필요합니다.
차동 진단
궤양성 대장염과 유사한 방법으로 여러 질환이 나타날 수 있으므로 제외해야 한다.이러한 조건은 다음과 같습니다.크론병, 감염성 대장염, 비스테로이드성 항염증제 장질환, 과민성 대장증후군.허혈성 대장염(대장으로의 혈류 부족), 방사선 대장염(방사선 치료 이전에 피폭된 경우) 또는 화학적 대장염과 같은 대장염의 대체 원인을 고려해야 한다.가성막성 대장염은 항생제 투여 후 클로스트리디오이데스 디피실 감염으로 인해 발생할 수 있다.엔타메바 조직 분해균은 장내 염증을 일으키는 원생동물 기생충이다.코르티코스테로이드의 사용으로 인해 결과가 좋지 않은 [77]UC로 오진된 사례도 있다.
궤양성 대장염의 증상을 모방하는 가장 흔한 질병은 크론병인데, 둘 다 비슷한 증상으로 대장에 영향을 미칠 수 있는 염증성 대장 질환이기 때문이다.이러한 질병들은 치료 과정과 치료법이 다를 수 있기 때문에 구별하는 것이 중요하다.그러나 어떤 경우에는 차이를 구별할 수 없을 수 있으며, 이 경우 이 질환은 부정대장염으로 [78]분류된다.
| 크론병 | 궤양성 대장염 | |
|---|---|---|
| 회장 말기 관련 | 일반적으로 | 드물게 |
| 결장병변 | 보통 | 항상 |
| 직장의 관여 | 드물게 | 통상(95%)[20] |
| 에 관한 관여 항문 | 공통[79] | 드물게 |
| 담관개입 | 원발성 경화성 담관염 증가 없음 | 더[80] 높은 비율 |
| 질병의 분포 | 염증이 있는 부분(스킵 병변) | 염증[20] 지속부위 |
| 내시경 검사 | 깊은 지리적 궤양과 뱀(뱀과 비슷한 뱀) 궤양 | 연속 궤양 |
| 염증의 깊이 | 경구적으로 조직[79][42] 깊숙이 침투할 수 있습니다. | 얕은 점막 |
| 협착 | 흔한 | 드물게 |
| 생검에 의한 육아종 | 비괴사성 비장암 육아종이[79][81][82] 있을 수 있다 | 비장주위암육아종은 보이지[83] 않습니다 |
관리
궤양성 대장염의 표준 치료는 관련 정도와 질병의 심각도에 따라 달라진다.목표는 처음에는 약물로 완화를 유도하고, 그 다음에는 재발을 방지하기 위한 유지 약물의 투여를 유도하는 것이다.완화의 유도와 완화의 유지의 개념은 매우 중요하다.완화를 유도하고 유지하기 위한 약물은 다소 중복되지만 치료법은 다르다.의사들은 우선 증상 완화와 대장 내막 점막 치유를 수반하는 완화를 유도한 후 완화를 유지하고 합병증을 예방하기 위해 장기적인 치료를 한다.급성 중증 궤양성 대장염은 입원, 감염 제외, 코르티코스테로이드가 [84]필요하다.
급성 질환의 경우 식이섬유가 적은 식단이 [85][86]권장될 수 있습니다.
약
궤양성 대장염은 술파살라진, 메살라진과 같은 5-ASA 약물을 포함한 많은 약물로 치료될 수 있다.프레드니손과 같은 코르티코스테로이드는 면역억제 및 단기 치유 특성 때문에 사용될 수 있지만, 그들의 위험이 그들의 이점보다 크기 때문에, 그들은 치료에 장기간 사용되지 않는다.아자티오프린과 같은 면역억제제와 인플릭시맵, 아달리미맵 같은 생물학적 약물은 5-ASA와 코르티코스테로이드로 완화를 이룰 수 없는 경우에만 투여된다.인플릭시맙, 우스테키누맙, 베돌리주맙은 중등도나 중증도 [87]질환자에게 권장된다.
2013년 [88][89]1월 미국 식품의약국(FDA)은 활성 궤양성 대장염 치료를 위해 부데소니드의 제제를 승인했다.2018년, 토파시티닙은 미국에서 중간 정도에서 심각한 활동성 궤양성 대장염의 치료를 위해 승인되었으며, 이 질환에서 [90]장기 사용이 확인된 최초의 경구 의약품이다.메토트렉세이트에 대한 증거는 궤양성 대장염을 [91]가진 사람들에게서 완화를 만들어내는데 이로운 점을 보여주지 않는다.시클로스포린은 심각한[87] UC에 효과적이며 타크로리무스 또한 [92][93][94][95]이로운 것으로 나타났다.
아미노살리실산염
술파살라진은 50년 이상 경도에서 중간 정도의 궤양성 대장염 치료에 주요 약제였다.1977년에는 5-아미노살리실산(5-ASA, 메살라진/[96]메살라민)이 술파살라진의 치료 활성 성분으로 나타났다.많은 5-ASA 약물은 치료 효과를 유지하기 위해 활성 화합물을 대장으로 전달하는 것을 목적으로 개발되었지만 술파살라딘의 술파피리딘 부분과 관련된 부작용을 감소시켰다.경구용 5-ASA 약물은 특히 가벼운 궤양성 대장염을 [97][98]유발하고 완화를 유지하는 데 효과적이다.5-ASA의 직장 좌약, 폼 또는 액상 관장 제제는 직장, Sigmoid 또는 하행 결장에 영향을 미치는 대장염에 사용되며, 특히 경구 [99]치료와 결합되었을 때 효과가 있는 것으로 나타났다.
바이오로지스
TNF 억제제 infliximab, Adalimumab, golimumab과 같은 생물학적 치료법은 더 이상 코르티코스테로이드에 반응하지 않는 UC를 가진 사람들을 치료하기 위해 일반적으로 사용됩니다.Topfacitinib와 vedolizumab은 [8]또한 UC에서 좋은 임상적 완화 및 응답률을 생산할 수 있습니다.생물은 치료 초기에 사용하거나(단계적 접근법), 또는 다른 치료법이 완화를 유도하지 못한 후에(단계적 접근법) 사용할 수 있다. 전략은 [100]개별화되어야 한다.
아미노살리실산염과 달리, 생물은 [101]장외암 발병 위험 증가, 심부전, 면역체계 약화 등의 심각한 부작용을 일으킬 수 있으며, 이로 인해 면역체계가 감염을 명확히 하고 결핵과 같은 잠복감염의 재활성화를 초래할 수 있다.이러한 이유로, 이러한 치료제를 복용하는 사람들은 면밀하게 관찰되고 매년 [102][103]간염과 결핵 검사를 받는다.
니코틴
크론병과는 달리 궤양성 대장염은 [104][105]비흡연자보다 흡연자에게 영향을 미칠 확률이 낮다.이전 담배 사용 전력이 있는 선별된 개인에서, 저용량 흡연을 재개하면 활동성 궤양성 [106]대장염의 징후와 증상이 개선될 수 있지만,[107] 담배가 건강에 미치는 영향이 압도적으로 크기 때문에 권장되지 않는다.경피 니코틴 패치를 사용한 연구는 임상적, 조직학적 [108]개선을 보여주었다.영국에서 실시된 한 이중맹검, 위약 대조군 연구에서 표준 치료와 함께 니코틴 패치를 사용한 UC 환자 중 48.6%가 증상이 완전히 해결된 것으로 나타났다.미국에서 실시된 또 다른 무작위 이중맹검, 위약 대조군의 단일 센터 임상시험에서는 패치를 사용한 사람들의 39%가 [109]위약을 투여한 사람들의 9%에 비해 상당한 개선을 보였다.그러나 니코틴 치료는 부작용과 일관성 없는 [110][111][112]결과 때문에 일반적으로 권장되지 않는다.
철분 보충
만성 염증뿐만 아니라 위장관으로부터의 점진적인 혈액 손실은 종종 빈혈로 이어지며, 전문 지침은 활동 중인 질병에서 3개월마다 그리고 정지 중인 [113]질병에서 매년 반복되는 혈액 검사를 통해 빈혈에 대한 일상적인 모니터링을 제안한다.적절한 질병 통제는 보통 만성 질환의 빈혈을 개선하지만 철분 결핍 빈혈은 철분 보충제로 치료해야 한다.치료가 투여되는 형태는 빈혈의 심각도와 그에 따르는 지침에 따라 달라집니다.어떤 사람들은 비경구 철분을 먼저 사용하라고 조언한다. 왜냐하면 사람들은 비경구 철분에 더 빨리 반응하고, 그것은 위장 부작용과 더 적은 관련이 있고, 그것은 준수 [114]문제와 관련이 없기 때문이다.다른 사람들은 결국 사람들이 반응하고 많은 사람들이 부작용을 [113][115]견딜 것이기 때문에 먼저 경구용 다리미를 사용할 것을 요구한다.
수술.
| 크론병 | 궤양성 대장염 | |
|---|---|---|
| 메살라진 | 유용성이[116] 낮다 | 보다[116] 편리함 |
| 항생제 | 장기간에[117] 걸쳐 효과적 | 일반적으로 유용하지[118] 않음 |
| 수술. | 반환되는 경우가 많다 환부의 제거 | 보통 제거로 치료됩니다. 결장의 |
크론병과는 달리 궤양성 대장염의 위장 측면은 절제된 증상이 지속될 수 있지만 일반적으로 대장의 외과적 제거로 치유될 수 있다.이 절차는 출혈, 프랭크 천공 또는 암으로 의심되거나 문서화된 경우 필요합니다.수술은 또한 심각한 대장염이나 독성 메가콜론을 가진 사람들에게도 지시된다.장애가 있고 약물에 반응하지 않는 증상을 가진 사람들은 수술이 [15]삶의 질을 향상시킬 수 있는지 고려하기를 원할 수 있다.
전결핵 절제술로 알려진 전체 대장의 제거는 영구 회장 절제술로 귀결됩니다. 여기서 복부를 통해 회장 말단을 당김으로써 스토마가 생성됩니다.내장 내용물을 [119]접착제를 사용하여 스토마 주위에 고정되는 탈착 가능한 오스트미 봉투에 비운다.
대부분의 대장에 영향을 미치는 궤양성 대장염의 또 다른 외과적 선택지는 회장 주머니 항문합(IPAA)이다.이것은 2단계 또는 3단계로 이루어진 절차입니다.3단계 시술에서 첫 번째 수술은 대장을 제거하되 직장은 제자리에 두고 임시 회장절제술을 하는 총결장절제술이다.두 번째 단계는 전절제술과 회장 주머니(일반적으로 "j-pouch"로 알려져 있음)의 형성입니다.이것은 남아 있는 직장 그루터기의 대부분을 제거하고 소장의 끝을 주머니로 만들어 항문에 붙이는 새로운 "직장"을 만드는 것을 포함한다.이 시술 후 새로운 유형의 회장절제술(루프 회장절제술)이 생성되어 문합이 치유됩니다.마지막 수술은 회장절제술이 뒤바뀌는 테이크다운 시술로 더 이상 대장절제술이 필요하지 않습니다.두 단계로 이루어진 경우, 결장과 직장을 모두 제거하는 전결장절제술이 주머니 형성 및 루프 회장절제술과 함께 수행됩니다.마지막 단계는 3단계 시술과 동일한 테이크다운 수술입니다.각 단계 사이에 걸리는 시간은 다양할 수 있지만, 일반적으로 처음 두 단계 사이에 6개월에서 12개월의 간격이 권장되며, 주머니의 형성과 회장절제술 [15]테이크다운 사이에 최소 2~3개월이 필요하다.
회장 주머니 시술은 오스트미 백의 필요성을 없애지만 정상적인 장 기능을 회복시키지는 못한다.최종 수술 후 몇 달 동안 환자들은 보통 하루에 8-15번의 배변을 경험합니다.시간이 지남에 따라 이 수치는 감소하여 많은 환자들이 수술 후 1년 후에 4-6번의 배변을 보고한다.많은 환자들이 이 시술에 성공했지만, 알려진 합병증들이 많이 있습니다.궤양성 대장염과 유사한 증상을 일으키는 회장 주머니의 염증인 주머니염은 비교적 흔하다.주머니염은 급성, 소실 또는 만성일 수 있지만 항생제, 스테로이드제 또는 생약품을 사용한 치료가 매우 효과적일 수 있습니다.다른 합병증으로는 누공, 농양, 주머니 부전이 있다.증상의 심각도에 따라 주머니 수정 수술을 수행해야 할 수도 있습니다.케이스에 따라서는 파우치를 기능 해제 또는 제거하여 회장 절제를 [120][121]다시 해야 할 수도 있습니다.
회장 주머니 항문 문합으로 인한 암 발생 위험은 낮다.[122]그러나 주머니 내시경 검사를 통한 연간 관찰은 이형성 또는 대장암, PSC, 난치성 주머니염 및 심각한 염증성 주머니 [122]점막과 같은 이형성 위험 인자를 가진 개인에게 고려될 수 있다.
세균재조합
많은 무작위 임상 시험에서, 생균제는 궤양성 대장염 치료에 도움이 될 수 있는 가능성을 입증했다.대장균 니슬레와 같은 특정 유형의 프로바이오틱스는 일부 사람들에게 최대 [123]1년 동안 완화를 유도하는 것으로 나타났다.VSL#3이라고 불리는 프로바이오틱스는 활동성 궤양성 대장염의 완화를 유도하는데 효과적일 수 있으며, 5-ASAs만큼 휴지 상태의 [124]UC의 재발을 예방하는데 효과적일 수 있다.
분변 마이크로바이오타 이식은 분변 관장을 통한 인간 생균제 주입을 포함한다.궤양성 대장염은 클로스트리듐 디피실 감염이 성공하기 위해서는 아마도 궤양성 상피를 치유하는 데 필요한 시간 때문에 더 오랜 시간 동안 세균 치료를 받아야 한다.궤양성 대장염의 반응은 잠재적으로 매우 호의적이어서 67.7%의 사람들이 [125]완치되었다고 보고되었다.다른 연구들은 분뇨 미생물 [126][127][128]이식을 사용하는 것의 이점을 발견했다.
대체의학
궤양성 대장염에는 다양한 대체 약물이 사용되었지만 결과가 일관되지 않았다.쿠르쿠민(강황) 치료는 메살라민 또는 술파살라딘의 복용과 함께, 대기성 궤양성 대장염을 가진 사람들의 [129][130]완화를 유지하는데 효과적이고 안전할 수 있다.커큐민 요법만으로는 대기성 궤양성 대장염에 미치는 영향은 [130]알려져 있지 않습니다.
대마초나 대마유를 사용한 치료는 불확실하다.지금까지, 연구들은 그것의 효과와 [131]안전성을 결정하지 못했다.
복통관리
FODMAPs 다이어트, 이완 훈련, 요가, 케피르 다이어트, 성상 신경절 차단 치료 등 궤양성 대장염 환자의 복통을 관리하기 위한 많은 개입이 고려되고 있다.이들 중 어떤 것이 통증을 개선하거나 불안과 [132]우울증을 줄이는데 안전하거나 효과적인지는 불분명하다.
예후
나쁜 예후 요인으로는 진단 후 40세 미만, 광범위한 대장염, 내시경 검사 시 중증 대장염, 사전 입원, CRP 상승 및 [20]혈청 알부민 저하 등이 있습니다.
진행 또는 경감
궤양성 대장염을 앓고 있는 사람들은 보통 간헐적인 과정을 거치는데, 질병이 활동하지 않는 기간과 질병의 "발광"이 번갈아 나타난다.항문염이나 좌뇌 대장염을 가진 사람들은 대개 더 양성적인 과정을 거친다: 단지 15%만이 그들의 질병이 근위부에서 진행되며, 20%는 어떠한 치료도 받지 않을 때 지속적인 완화를 가질 수 있다.일부 사람들은 병의 진행을 빠르게 경험한다.이러한 경우, 대개 약물에 반응하지 못하고 종종 질병 [133][134]발병 후 몇 년 이내에 수술이 수행됩니다.더 광범위한 질병을 가진 사람들은 완화를 지속할 가능성은 낮지만,[135] 완화의 속도는 질병의 심각성과는 무관하다.UC의 사전 입원, 광범위한 대장염, 전신 스테로이드제의 필요성, 진단 시 젊은 나이, 낮은 혈청 알부민, 높아진 염증 마커(CRP & ESR) 및 대장 [87][20]내시경 검사 중 나타나는 심각한 염증을 포함한 여러 위험 요인이 결장절제술의 궁극적 필요성과 관련되어 있다.경우에 [20]따라서는 대장의 외과적 제거가 필요하다.
대장암
10년 후 궤양성 대장염이 있는 사람들에게서 비장 굴곡을 벗어난다면 대장암의 위험은 상당히 증가한다.역류성 회장염이 있는 사람들은 대장암에 [136]걸릴 위험이 높아질 수 있다.항문염만 있는 사람들은 보통 위험이 [20]증가하지 않는다.8년 동안 질병 활동을 한 후 1, 2년 [137]간격으로 이형성 여부를 확인하기 위해 무작위로 생체 검진을 받는 것이 좋습니다.
사망률
궤양성 대장염을 앓고 있는 사람들은 [139]배경 인구에 비해 전체 사망 위험이 비슷하거나 약간 증가한다[138].그러나 사망 원인 분포는 일반 [138]모집단과 다릅니다.C. 디피실[20] 감염 및 사이토메갈로바이러스 감염(재활성화로 [140]인한)을 포함한 궤양성 대장염 환자에서 더 나쁜 결과와 높은 사망 위험을 예측할 수 있습니다.
역학
크론병과 함께,[10] 2015년[update] 현재 약 1,120만 명의 사람들이 영향을 받았다.궤양성 대장염은 매년 인구 10만명당 1~20명꼴로 새로 발생하며 10만명당 5~500명꼴로 발병한다.[7][9]2015년에는 전 세계적으로 47,400명이 염증성 장질환(UC와 크론병)[6]으로 사망했다.피크 발병은 [14]30세에서 40세 사이이며,[141] 두 번째 발병은 생후 6년차에 발생한다.궤양성 대장염은 남녀 [14][7]모두에게 똑같이 흔하다.적절한 치료를 받으면 사망 위험은 일반 인구의 [3]사망 위험과 유사하게 나타납니다.UC는 1950년대부터 [7][9]보급되어 왔습니다.
UC와 크론병의 지리적 분포는 전세계적으로 [142]비슷하며, 캐나다, 뉴질랜드, 영국에서 [143]UC의 연간 신규 사례가 가장 많이 발견됩니다.이 병은 다른 [9]지역보다 북미와 유럽에서 더 흔하다.일반적으로 유럽이나 [145]미국의 남부[144] 지역에 비해 북부 지역에서 더 높은 비율을 보인다.UC는 동유럽에 [146]비해 서유럽에서 더 흔하다.전 세계적으로 UC의 유병률은 [5]100,000명당 2 - 299명이다.궤양성 대장염과 크론병은 미국에서 [11]약 100만 명의 사람들에게 영향을 미친다.
크론병과 마찬가지로 UC의 발병률은 아슈케나지 유대인, 비유대계 백인, 아프리카인, 히스패닉계 및 [23]아시아인 사이에서 더 높고 점차적으로 감소한다.맹장염에[147] 대한 20세 이전의 맹장절제술과 현재의 담배 사용은[148] [14]UC의 발생을 막아준다.하지만, 이전의 담배 사용은 그 [148][14]질병에 걸릴 위험이 더 높다.
미국
2004년 현재[update] 미국에서 UC의 새로운 환자 수는 연간 [149]100,000명당 2.2~14.3명 사이입니다.2004년 미국에서 영향을 받은 사람들의 수는 10만 [149]명당 37명에서 246명 사이였다.
캐나다
캐나다에서는 1998년부터 2000년 사이에 인구 10만명당 연간 신규 발생 건수가 12.9건 또는 4,500건이었다.영향을 받은 사람들의 수는 10만명당 211명 또는 10만4천명으로 [150]추정되었다.
영국
영국에서는 인구 10만명당 10명꼴로 발병하는 반면, 영향을 받는 사람의 수는 10만명당 243명이다.영국에서 약 146,000명의 사람들이 [151]UC 진단을 받았다.
역사
궤양성 대장염에 대한 최초의 [9]설명은 1850년대에 발생했다.
조사.
회충 트리추리스 수이스를 이용한 헬민틱 요법은 궤양성 대장염을 [152]가진 사람들에게 유익함을 보여주기 위해 아이오와에서 무작위 대조 실험을 통해 나타났다.이 치료법은 선진국 사람들의 결장에 헬민스가 없으면 염증이 생길 수 있다고 주장하는 위생 가설을 테스트합니다.구충 치료와 분변 미생물 이식은 모두 질병 부위에서 특징적인 Th2 백혈구 반응을 유도하며, 이는 궤양성 대장염이 Th2 [152]과잉생산을 수반하는 것으로 생각되었기 때문에 예상하지 못했다.
Alicaforsen은 1세대 안티 센스 oligodeoxynucleotide 위해 ICAM-1.[153]ICAM-1의 표현을 진압하기 위해 특별히 웟슨 크릭 모형의. 기본 쌍의 상호 작용을 통해 인간의 ICAM-1 메신저 RNA로 묶도록 설계된 염증 반응형 백혈구들의 분출 및 활성화 inflam에(백혈구)을 전파합니다.ti IagoICAM-1의 [153]증식이 궤양성 대장염 환자의 염증 장 점막 내에서 관찰되었으며, 여기서 ICAM-1은 질병 활동과 [154]관련이 있다.이는 ICAM-1이 궤양성 대장염 [155]치료의 잠재적 치료 대상임을 시사한다.
내강에 존재하는 그램 양성 박테리아는 궤양성 대장염의 [156]재발 시간을 연장하는 것과 관련이 있을 수 있다.
개발 중인 일련의 약물은 Kca3.[157]1로 알려진 염증 시그널링 캐스케이드 내의 이온 채널을 선택적으로 목표로 하여 염증 과정을 방해할 것으로 보인다.쥐와 쥐를 대상으로 한 임상 전 연구에서 Kca3.1의 억제는 Th1 사이토카인 IL-2와 TNF-γ의 생성을 방해하고 [157]술파살라진만큼 효과적으로 대장 염증을 감소시켰다.
호중구 세포외[158] 트랩과 그로 인한 세포외[159] 기질의 저하가 임상적 완화 궤양성 대장염 환자의 대장 점막에서 보고되었으며,[158] 이는 선천적 면역체계가 병인에 관여함을 나타낸다.
알레르기 치료에 사용되는 항히스타민제인 펙소페나딘은 일부 [160][161]연구에서 병용 치료의 가능성을 보여주었다.펙소페나딘의 낮은 위장 흡수(또는 높은 흡수성 약물 위장 분비물)는 염증 부위의 높은 농도를 초래한다.따라서, 이 약은 관련된 위장 마스트 세포에 의해 국소적으로 히스타민 분비를 감소시키고 [161]염증을 완화시킬 수 있다.
에트로리주맙이 궤양성 대장염에 효과가 있다는 증거가 있으며 2016년 [8][162][163][164]현재 3단계 시험이 진행 중입니다.에트로리주맵은 인체화 모노클로널 항체로 인테그린 α4β7 및 αEβ7의 β7 서브유닛을 대상으로 한다.에트로리주맙은 베돌리주맙(또 다른 인테그린 길항제)과 유사하게 림프구 트래픽을 감소시킨다.
과립구 및 단구 흡착성 아페레시스라고 알려진 백혈구 아페레시스의 한 종류는 여전히 그것이 [165]효과적인지 여부를 판단하기 위해 대규모 실험이 필요하다.소규모 실험의 결과는 잠정적으로 [166]긍정적이었다.
주목할 만한 경우
레퍼런스
- ^ a b c d e f g h i j k l m n o p q r s t u v w x "Ulcerative Colitis". NIDDK. September 2014. Retrieved 3 August 2016.
- ^ "Ulcerative Colitis". Autoimmune Registry Inc. Retrieved 15 June 2022.
- ^ a b c d Wanderås MH, Moum BA, Høivik ML, Hovde Ø (May 2016). "Predictive factors for a severe clinical course in ulcerative colitis: Results from population-based studies". World Journal of Gastrointestinal Pharmacology and Therapeutics. 7 (2): 235–241. doi:10.4292/wjgpt.v7.i2.235. PMC 4848246. PMID 27158539.
- ^ Runge MS, Greganti MA (2008). Netter's Internal Medicine E-Book. Elsevier Health Sciences. p. 428. ISBN 9781437727722.
- ^ a b Molodecky NA, Soon IS, Rabi DM, Ghali WA, Ferris M, Chernoff G, et al. (January 2012). "Increasing incidence and prevalence of the inflammatory bowel diseases with time, based on systematic review". Gastroenterology. 142 (1): 46–54.e42, quiz e30. doi:10.1053/j.gastro.2011.10.001. PMID 22001864.
- ^ a b Wang, Haidong; et al. (GBD 2015 Mortality and Causes of Death Collaborators) (October 2016). "Global, regional, and national life expectancy, all-cause mortality, and cause-specific mortality for 249 causes of death, 1980-2015: a systematic analysis for the Global Burden of Disease Study 2015". Lancet. 388 (10053): 1459–1544. doi:10.1016/s0140-6736(16)31012-1. PMC 5388903. PMID 27733281.
- ^ a b c d e f g h Ford AC, Moayyedi P, Hanauer SB (February 2013). "Ulcerative colitis". BMJ. 346: f432. doi:10.1136/bmj.f432. PMID 23386404. S2CID 14778938.
- ^ a b c Akiho H, Yokoyama A, Abe S, Nakazono Y, Murakami M, Otsuka Y, et al. (November 2015). "Promising biological therapies for ulcerative colitis: A review of the literature". World Journal of Gastrointestinal Pathophysiology. 6 (4): 219–227. doi:10.4291/wjgp.v6.i4.219. PMC 4644886. PMID 26600980.
- ^ a b c d e f g h i j k Danese S, Fiocchi C (November 2011). "Ulcerative colitis". The New England Journal of Medicine. 365 (18): 1713–1725. doi:10.1056/NEJMra1102942. PMID 22047562.
- ^ a b Vos, Theo; et al. (GBD 2015 Disease and Injury Incidence and Prevalence Collaborators) (October 2016). "Global, regional, and national incidence, prevalence, and years lived with disability for 310 diseases and injuries, 1990-2015: a systematic analysis for the Global Burden of Disease Study 2015". Lancet. 388 (10053): 1545–1602. doi:10.1016/S0140-6736(16)31678-6. PMC 5055577. PMID 27733282.
- ^ a b Adams JG (2012). Emergency Medicine E-Book: Clinical Essentials (Expert Consult – Online). Elsevier Health Sciences. p. 304. ISBN 978-1455733941.
- ^ a b c d e f 인터넷 메디신se > Inspiratorisk tarmsjukdom, kronisk, IBD By Robert Löfberg.2010년 10월 번역 취득.
- ^ Hanauer SB, Sandborn W (March 2001). "Management of Crohn's disease in adults". The American Journal of Gastroenterology. 96 (3): 635–43. doi:10.1111/j.1572-0241.2001.3671_c.x (inactive 31 July 2022). PMID 11280528. S2CID 31219115.
{{cite journal}}: CS1 유지 : 2022년 7월 현재 DOI 비활성화 (링크) - ^ a b c d e f g h i j k l m n o p Ungaro R, Mehandru S, Allen PB, Peyrin-Biroulet L, Colombel JF (April 2017). "Ulcerative colitis". Lancet. 389 (10080): 1756–1770. doi:10.1016/S0140-6736(16)32126-2. PMC 6487890. PMID 27914657.
- ^ a b c d e Magro F, Gionchetti P, Eliakim R, Ardizzone S, Armuzzi A, Barreiro-de Acosta M, et al. (June 2017). "Third European Evidence-based Consensus on Diagnosis and Management of Ulcerative Colitis. Part 1: Definitions, Diagnosis, Extra-intestinal Manifestations, Pregnancy, Cancer Surveillance, Surgery, and Ileo-anal Pouch Disorders". Journal of Crohn's & Colitis. 11 (6): 649–670. doi:10.1093/ecco-jcc/jjx008. PMID 28158501.
- ^ Kaitha S, Bashir M, Ali T (August 2015). "Iron deficiency anemia in inflammatory bowel disease". World Journal of Gastrointestinal Pathophysiology. 6 (3): 62–72. doi:10.4291/wjgp.v6.i3.62. PMC 4540708. PMID 26301120.
- ^ Hanauer SB (March 1996). "Inflammatory bowel disease". The New England Journal of Medicine. 334 (13): 841–848. doi:10.1056/NEJM199603283341307. PMID 8596552.
- ^ Rosenberg L, Lawlor GO, Zenlea T, Goldsmith JD, Gifford A, Falchuk KR, et al. (2013). "Predictors of endoscopic inflammation in patients with ulcerative colitis in clinical remission". Inflammatory Bowel Diseases. 19 (4): 779–784. doi:10.1097/MIB.0b013e3182802b0e. PMC 3749843. PMID 23446338.
- ^ a b c d e f Colìa R, Corrado A, Cantatore FP (December 2016). "Rheumatologic and extraintestinal manifestations of inflammatory bowel diseases". Annals of Medicine. 48 (8): 577–585. doi:10.1080/07853890.2016.1195011. PMID 27310096. S2CID 1796160.
- ^ a b c d e f g h i j k l m n o p q r s t u v w x Rubin DT, Ananthakrishnan AN, Siegel CA, Sauer BG, Long MD (March 2019). "ACG Clinical Guideline: Ulcerative Colitis in Adults". The American Journal of Gastroenterology. 114 (3): 384–413. doi:10.14309/ajg.0000000000000152. PMID 30840605. S2CID 73473272.
- ^ Feuerstein JD, Cheifetz AS (July 2017). "Crohn Disease: Epidemiology, Diagnosis, and Management". Mayo Clinic Proceedings. 92 (7): 1088–1103. doi:10.1016/j.mayocp.2017.04.010. PMID 28601423. S2CID 20223406.
- ^ Haskell H, Andrews CW, Reddy SI, Dendrinos K, Farraye FA, Stucchi AF, et al. (November 2005). "Pathologic features and clinical significance of "backwash" ileitis in ulcerative colitis". The American Journal of Surgical Pathology. 29 (11): 1472–1481. doi:10.1097/01.pas.0000176435.19197.88. PMID 16224214. S2CID 42108108.
- ^ a b 파우치 등해리슨 내과 17학번입니다뉴욕: McGrow-Hill Medical, 2008.ISBN 978-0-07-15991-7
- ^ Greenstein AJ, Janowitz HD, Sachar DB (September 1976). "The extra-intestinal complications of Crohn's disease and ulcerative colitis: a study of 700 patients". Medicine. 55 (5): 401–12. doi:10.1097/00005792-197609000-00004. PMID 957999.
- ^ Bernstein CN, Blanchard JF, Rawsthorne P, Yu N (April 2001). "The prevalence of extraintestinal diseases in inflammatory bowel disease: a population-based study". The American Journal of Gastroenterology. 96 (4): 1116–22. doi:10.1111/j.1572-0241.2001.03756.x. PMID 11316157.
- ^ Harbord M, Annese V, Vavricka SR, Allez M, Barreiro-de Acosta M, Boberg KM, et al. (March 2016). "The First European Evidence-based Consensus on Extra-intestinal Manifestations in Inflammatory Bowel Disease". Journal of Crohn's & Colitis. 10 (3): 239–54. doi:10.1093/ecco-jcc/jjv213. PMID 26614685.
- ^ a b c d e f g h i j k l m n Feuerstein JD, Moss AC, Farraye FA (July 2019). "Ulcerative Colitis". Mayo Clinic Proceedings. 94 (7): 1357–1373. doi:10.1016/j.mayocp.2019.01.018. PMID 31272578.
- ^ Langan RC, Gotsch PB, Krafczyk MA, Skillinge DD (November 2007). "Ulcerative colitis: diagnosis and treatment". American Family Physician. 76 (9): 1323–1330. PMID 18019875.
- ^ Vavricka SR, Schoepfer A, Scharl M, Lakatos PL, Navarini A, Rogler G (August 2015). "Extraintestinal Manifestations of Inflammatory Bowel Disease". Inflammatory Bowel Diseases. 21 (8): 1982–1992. doi:10.1097/MIB.0000000000000392. PMC 4511685. PMID 26154136.
- ^ a b c d Muhvić-Urek M, Tomac-Stojmenović M, Mijandrušić-Sinčić B (July 2016). "Oral pathology in inflammatory bowel disease". World Journal of Gastroenterology. 22 (25): 5655–5667. doi:10.3748/wjg.v22.i25.5655. PMC 4932203. PMID 27433081.
- ^ a b c Troncoso LL, Biancardi AL, de Moraes HV, Zaltman C (August 2017). "Ophthalmic manifestations in patients with inflammatory bowel disease: A review". World Journal of Gastroenterology. 23 (32): 5836–5848. doi:10.3748/wjg.v23.i32.5836. PMC 5583569. PMID 28932076.
- ^ Schonberg, S.; Stokkermans, T. J. (January 2020). "Episcleritis". PMID 30521217.
{{cite journal}}:Cite 저널 요구 사항journal=(도움말) - ^ a b c d e f g h Langholz E (March 2010). "Current trends in inflammatory bowel disease: the natural history". Therapeutic Advances in Gastroenterology. 3 (2): 77–86. doi:10.1177/1756283X10361304. PMC 3002570. PMID 21180592.
- ^ a b c Cheng K, Faye AS (March 2020). "Venous thromboembolism in inflammatory bowel disease". World Journal of Gastroenterology. 26 (12): 1231–1241. doi:10.3748/wjg.v26.i12.1231. PMC 7109271. PMID 32256013. S2CID 214946656.
- ^ a b Nguyen GC, Bernstein CN, Bitton A, Chan AK, Griffiths AM, Leontiadis GI, et al. (March 2014). "Consensus statements on the risk, prevention, and treatment of venous thromboembolism in inflammatory bowel disease: Canadian Association of Gastroenterology". Gastroenterology. 146 (3): 835–848.e6. doi:10.1053/j.gastro.2014.01.042. PMID 24462530.
- ^ Andrade AR, Barros LL, Azevedo MF, Carlos AS, Damião AO, Sipahi AM, Leite AZ (April 2018). "Risk of thrombosis and mortality in inflammatory bowel disease". Clinical and Translational Gastroenterology. 9 (4): 142. doi:10.1038/s41424-018-0013-8. PMC 5886983. PMID 29618721.
- ^ Olsson R, Danielsson A, Järnerot G, Lindström E, Lööf L, Rolny P, et al. (May 1991). "Prevalence of primary sclerosing cholangitis in patients with ulcerative colitis". Gastroenterology. 100 (5 Pt 1): 1319–1323. doi:10.1016/0016-5085(91)90784-I. PMID 2013375.
- ^ Nachimuthu S. "Crohn's disease". eMedicineHealth. Archived from the original on 9 December 2019. Retrieved 8 December 2019.
- ^ Ko IK, Kim BG, Awadallah A, Mikulan J, Lin P, Letterio JJ, Dennis JE (July 2010). "Targeting improves MSC treatment of inflammatory bowel disease". Molecular Therapy. 18 (7): 1365–1372. doi:10.1038/mt.2010.54. PMC 2911249. PMID 20389289.
- ^ a b Orholm M, Binder V, Sørensen TI, Rasmussen LP, Kyvik KO (October 2000). "Concordance of inflammatory bowel disease among Danish twins. Results of a nationwide study". Scandinavian Journal of Gastroenterology. 35 (10): 1075–1081. doi:10.1080/003655200451207. PMID 11099061. S2CID 218907577.
- ^ Tysk C, Lindberg E, Järnerot G, Flodérus-Myrhed B (July 1988). "Ulcerative colitis and Crohn's disease in an unselected population of monozygotic and dizygotic twins. A study of heritability and the influence of smoking". Gut. 29 (7): 990–996. doi:10.1136/gut.29.7.990. PMC 1433769. PMID 3396969.
- ^ a b c Baumgart DC, Sandborn WJ (May 2007). "Inflammatory bowel disease: clinical aspects and established and evolving therapies". Lancet. 369 (9573): 1641–57. doi:10.1016/S0140-6736(07)60751-X. PMID 17499606. S2CID 35264387.
- ^ Cho JH, Nicolae DL, Ramos R, Fields CT, Rabenau K, Corradino S, et al. (May 2000). "Linkage and linkage disequilibrium in chromosome band 1p36 in American Chaldeans with inflammatory bowel disease". Human Molecular Genetics. 9 (9): 1425–1432. doi:10.1093/hmg/9.9.1425. PMID 10814724.
- ^ Shah A, Walker M, Burger D, Martin N, von Wulffen M, Koloski N, et al. (August 2019). "Link Between Celiac Disease and Inflammatory Bowel Disease". Journal of Clinical Gastroenterology. 53 (7): 514–522. doi:10.1097/MCG.0000000000001033. PMID 29762265. S2CID 44102071.
- ^ Fu Y, Lee CH, Chi CC (December 2018). "Association of Psoriasis With Inflammatory Bowel Disease: A Systematic Review and Meta-analysis". JAMA Dermatology. 154 (12): 1417–1423. doi:10.1001/jamadermatol.2018.3631. PMC 6583370. PMID 30422277.
- ^ Katsanos KH, Voulgari PV, Tsianos EV (August 2012). "Inflammatory bowel disease and lupus: a systematic review of the literature". Journal of Crohn's & Colitis. 6 (7): 735–742. doi:10.1016/j.crohns.2012.03.005. PMID 22504032.
- ^ Chen Y, Chen L, Xing C, Deng G, Zeng F, Xie T, et al. (June 2020). "The risk of rheumatoid arthritis among patients with inflammatory bowel disease: a systematic review and meta-analysis". BMC Gastroenterology. 20 (1): 192. doi:10.1186/s12876-020-01339-3. PMC 7301504. PMID 32552882.
- ^ Sieg I, Beckh K, Kersten U, Doss MO (November 1991). "Manifestation of acute intermittent porphyria in patients with chronic inflammatory bowel disease". Zeitschrift für Gastroenterologie. 29 (11): 602–605. PMID 1771936.
- ^ Xu L, Lochhead P, Ko Y, Claggett B, Leong RW, Ananthakrishnan AN (November 2017). "Systematic review with meta-analysis: breastfeeding and the risk of Crohn's disease and ulcerative colitis". Alimentary Pharmacology & Therapeutics. 46 (9): 780–789. doi:10.1111/apt.14291. PMC 5688338. PMID 28892171.
- ^ Corrao G, Tragnone A, Caprilli R, Trallori G, Papi C, Andreoli A, et al. (June 1998). "Risk of inflammatory bowel disease attributable to smoking, oral contraception and breastfeeding in Italy: a nationwide case-control study. Cooperative Investigators of the Italian Group for the Study of the Colon and the Rectum (GISC)". International Journal of Epidemiology. 27 (3): 397–404. doi:10.1093/ije/27.3.397. PMID 9698126.
- ^ Wolverton SE, Harper JC (April 2013). "Important controversies associated with isotretinoin therapy for acne". American Journal of Clinical Dermatology. 14 (2): 71–76. doi:10.1007/s40257-013-0014-z. PMID 23559397. S2CID 918753.
- ^ Järnerot G, Järnmark I, Nilsson K (November 1983). "Consumption of refined sugar by patients with Crohn's disease, ulcerative colitis, or irritable bowel syndrome". Scandinavian Journal of Gastroenterology. 18 (8): 999–1002. doi:10.3109/00365528309181832. PMID 6673083.
- ^ Geerling BJ, Dagnelie PC, Badart-Smook A, Russel MG, Stockbrügger RW, Brummer RJ (April 2000). "Diet as a risk factor for the development of ulcerative colitis". The American Journal of Gastroenterology. 95 (4): 1008–1013. doi:10.1111/j.1572-0241.2000.01942.x. PMID 10763951. S2CID 11295804.
- ^ Jowett SL, Seal CJ, Pearce MS, Phillips E, Gregory W, Barton JR, Welfare MR (October 2004). "Influence of dietary factors on the clinical course of ulcerative colitis: a prospective cohort study". Gut. 53 (10): 1479–1484. doi:10.1136/gut.2003.024828. PMC 1774231. PMID 15361498.
- ^ Andersen V, Olsen A, Carbonnel F, Tjønneland A, Vogel U (March 2012). "Diet and risk of inflammatory bowel disease". Digestive and Liver Disease. 44 (3): 185–194. doi:10.1016/j.dld.2011.10.001. PMID 22055893.
- ^ Tilg H, Kaser A (October 2004). "Diet and relapsing ulcerative colitis: take off the meat?". Gut. 53 (10): 1399–1401. doi:10.1136/gut.2003.035287. PMC 1774255. PMID 15361484.
- ^ Moore J, Babidge W, Millard S, Roediger W (January 1998). "Colonic luminal hydrogen sulfide is not elevated in ulcerative colitis". Digestive Diseases and Sciences. 43 (1): 162–165. doi:10.1023/A:1018848709769. PMID 9508519. S2CID 20919357.
- ^ Jørgensen J, Mortensen PB (August 2001). "Hydrogen sulfide and colonic epithelial metabolism: implications for ulcerative colitis". Digestive Diseases and Sciences. 46 (8): 1722–1732. doi:10.1023/A:1010661706385. PMID 11508674. S2CID 30373968.
- ^ Picton R, Eggo MC, Langman MJ, Singh S (February 2007). "Impaired detoxication of hydrogen sulfide in ulcerative colitis?". Digestive Diseases and Sciences. 52 (2): 373–378. doi:10.1007/s10620-006-9529-y. PMID 17216575. S2CID 22547709.
- ^ a b Roediger WE, Moore J, Babidge W (August 1997). "Colonic sulfide in pathogenesis and treatment of ulcerative colitis". Digestive Diseases and Sciences. 42 (8): 1571–1579. doi:10.1023/A:1018851723920. PMID 9286219. S2CID 25496705.
- ^ Pierce ES (2018). "Could Mycobacterium avium subspecies paratuberculosis cause Crohn's disease, ulcerative colitis…and colorectal cancer?". Infectious Agents and Cancer. 13: 1. doi:10.1186/s13027-017-0172-3. PMC 5753485. PMID 29308085.
- ^ Elson CO, Cong Y, Weaver CT, Schoeb TR, McClanahan TK, Fick RB, Kastelein RA (2007). "Monoclonal anti-interleukin 23 reverses active colitis in a T cell-mediated model in mice". Gastroenterology. 132 (7): 2359–70. doi:10.1053/j.gastro.2007.03.104. PMID 17570211.
- ^ Levine J, Ellis CJ, Furne JK, Springfield J, Levitt MD (January 1998). "Fecal hydrogen sulfide production in ulcerative colitis". The American Journal of Gastroenterology. 93 (1): 83–87. doi:10.1111/j.1572-0241.1998.083_c.x. PMID 9448181. S2CID 3141574.
- ^ a b Dassopoulos T, Cohen RD, Scherl EJ, Schwartz RM, Kosinski L, Regueiro MD (July 2015). "Ulcerative Colitis Care Pathway". Gastroenterology. 149 (1): 238–245. doi:10.1053/j.gastro.2015.05.036. PMID 26025078.
- ^ eMedicine 궤양성 대장염
- ^ Walmsley RS, Ayres RC, Pounder RE, Allan RN (July 1998). "A simple clinical colitis activity index". Gut. 43 (1): 29–32. doi:10.1136/gut.43.1.29. PMC 1727189. PMID 9771402.
- ^ Mardini HE, Grigorian AY (September 2014). "Probiotic mix VSL#3 is effective adjunctive therapy for mild to moderately active ulcerative colitis: a meta-analysis". Inflammatory Bowel Diseases. 20 (9): 1562–1567. doi:10.1097/MIB.0000000000000084. PMID 24918321. S2CID 36218602.
- ^ a b Lamb CA, Kennedy NA, Raine T, Hendy PA, Smith PJ, Limdi JK, et al. (December 2019). "British Society of Gastroenterology consensus guidelines on the management of inflammatory bowel disease in adults". Gut. 68 (Suppl 3): s1–s106. doi:10.1136/gutjnl-2019-318484. PMC 6872448. PMID 31562236.
- ^ Politis DS, Papamichael K, Katsanos KH, Koulouridis I, Mavromati D, Tsianos EV, Christodoulou DK (March 2019). "Presence of pseudopolyps in ulcerative colitis is associated with a higher risk for treatment escalation". Annals of Gastroenterology. 32 (2): 168–173. doi:10.20524/aog.2019.0357. PMC 6394261. PMID 30837789.
- ^ "Azathioprine Product Information" (PDF). Access FDA. Food and Drug Administration.
- ^ Dignass AU, Gasche C, Bettenworth D, Birgegård G, Danese S, Gisbert JP, et al. (March 2015). "European consensus on the diagnosis and management of iron deficiency and anaemia in inflammatory bowel diseases". Journal of Crohn's & Colitis. 9 (3): 211–222. doi:10.1093/ecco-jcc/jju009. PMID 25518052.
- ^ Del Pinto R, Pietropaoli D, Chandar AK, Ferri C, Cominelli F (November 2015). "Association Between Inflammatory Bowel Disease and Vitamin D Deficiency: A Systematic Review and Meta-analysis". Inflammatory Bowel Diseases. 21 (11): 2708–2717. doi:10.1097/MIB.0000000000000546. PMC 4615394. PMID 26348447.
- ^ Mosli MH, Zou G, Garg SK, Feagan SG, MacDonald JK, Chande N, et al. (June 2015). "C-Reactive Protein, Fecal Calprotectin, and Stool Lactoferrin for Detection of Endoscopic Activity in Symptomatic Inflammatory Bowel Disease Patients: A Systematic Review and Meta-Analysis". The American Journal of Gastroenterology. 110 (6): 802–19, quiz 820. doi:10.1038/ajg.2015.120. PMID 25964225. S2CID 26111716.
- ^ Bryant RV, Friedman AB, Wright EK, Taylor KM, Begun J, Maconi G, et al. (May 2018). "Gastrointestinal ultrasound in inflammatory bowel disease: an underused resource with potential paradigm-changing application". Gut. 67 (5): 973–985. doi:10.1136/gutjnl-2017-315655. PMID 29437914. S2CID 3344377.
- ^ Aloca M, Filippi E, Costantino A, Bonovas S, 피오리노 G, Furfaro F, Peirin-Biroulet L, Frakeli M, Caprioli F, Danese S.밀라노 초음파 기준은 궤양성 대장염의 질병 활동을 평가하는 데 정확하다: 외부 검증.United European Gasteenterol J. 2021년 5월;9(4):438-442.
- ^ 알로카 M, 피오리노 G, 보노바스 S 등궤양성 대장염의 질병 활동 및 심각도를 평가하는 Humanitas 초음파 기준의 정확성: 선행 연구.J 크론스 대장염2018; 12: 1385– 91.
- ^ Shirley DA, Moonah S (July 2016). "Fulminant Amebic Colitis after Corticosteroid Therapy: A Systematic Review". PLOS Neglected Tropical Diseases. 10 (7): e0004879. doi:10.1371/journal.pntd.0004879. PMC 4965027. PMID 27467600.
- ^ Tremaine WJ (April 2012). "Is indeterminate colitis determinable?". Current Gastroenterology Reports. 14 (2): 162–165. doi:10.1007/s11894-012-0244-x. PMID 22314810. S2CID 40346031.
- ^ a b c Hanauer SB, Sandborn W (March 2001). "Management of Crohn's disease in adults". The American Journal of Gastroenterology. 96 (3): 635–43. doi:10.1111/j.1572-0241.2001.3671_c.x (inactive 31 July 2022). PMID 11280528. S2CID 31219115.
{{cite journal}}: CS1 유지 : 2022년 7월 현재 DOI 비활성화 (링크) - ^ Broomé U, Bergquist A (February 2006). "Primary sclerosing cholangitis, inflammatory bowel disease, and colon cancer". Seminars in Liver Disease. 26 (1): 31–41. doi:10.1055/s-2006-933561. PMID 16496231.
- ^ Shepherd NA (August 2002). "Granulomas in the diagnosis of intestinal Crohn's disease: a myth exploded?". Histopathology. 41 (2): 166–8. doi:10.1046/j.1365-2559.2002.01441.x. PMID 12147095. S2CID 36907992.
- ^ Mahadeva U, Martin JP, Patel NK, Price AB (July 2002). "Granulomatous ulcerative colitis: a re-appraisal of the mucosal granuloma in the distinction of Crohn's disease from ulcerative colitis". Histopathology. 41 (1): 50–5. doi:10.1046/j.1365-2559.2002.01416.x. PMID 12121237. S2CID 29476514.
- ^ DeRoche TC, Xiao SY, Liu X (August 2014). "Histological evaluation in ulcerative colitis". Gastroenterology Report. 2 (3): 178–92. doi:10.1093/gastro/gou031. PMC 4124271. PMID 24942757.
- ^ Chen JH, Andrews JM, Kariyawasam V, Moran N, Gounder P, Collins G, et al. (July 2016). "Review article: acute severe ulcerative colitis - evidence-based consensus statements". Alimentary Pharmacology & Therapeutics. 44 (2): 127–144. doi:10.1111/apt.13670. PMID 27226344.
- ^ "Should You Try a Low-Residue Diet?". WebMD. WebMD. 25 October 2016. Retrieved 29 April 2017.
- ^ Manual of Clinical Nutrition Management (PDF). Compass Group. 2013.
- ^ a b c Feuerstein JD, Isaacs KL, Schneider Y, Siddique SM, Falck-Ytter Y, Singh S (April 2020). "AGA Clinical Practice Guidelines on the Management of Moderate to Severe Ulcerative Colitis". Gastroenterology. 158 (5): 1450–1461. doi:10.1053/j.gastro.2020.01.006. PMC 7175923. PMID 31945371.
- ^ "FDA approves Uceris as ulcerative colitis treatment". Healio Gastroenterology. 15 January 2013.
- ^ "UCERIS (budesonide) extended release tablets label" (PDF). FDA.
- ^ "FDA approves new treatment for moderately to severely active ulcerative colitis". U.S. Food and Drug Administration (FDA) (Press release). 30 May 2018. Retrieved 31 May 2018.
- ^ Chande N, Wang Y, MacDonald JK, McDonald JW (August 2014). "Methotrexate for induction of remission in ulcerative colitis". The Cochrane Database of Systematic Reviews. 8 (8): CD006618. doi:10.1002/14651858.CD006618.pub3. PMC 6486224. PMID 25162749.
- ^ Krishnamoorthy R, Abrams KR, Guthrie N, Samuel S, Thomas T (28 May 2012). "PWE-237 Ciclosporin in acute severe ulcerative colitis: a meta-analysis". Gut. 61 (Suppl 2): A394.2–A394. doi:10.1136/gutjnl-2012-302514d.237. S2CID 74798482.
- ^ Ogata H, Kato J, Hirai F, Hida N, Matsui T, Matsumoto T, et al. (May 2012). "Double-blind, placebo-controlled trial of oral tacrolimus (FK506) in the management of hospitalized patients with steroid-refractory ulcerative colitis". Inflammatory Bowel Diseases. 18 (5): 803–808. doi:10.1002/ibd.21853. PMID 21887732. S2CID 1294555.
- ^ Lichtiger S, Present DH, Kornbluth A, Gelernt I, Bauer J, Galler G, et al. (June 1994). "Cyclosporine in severe ulcerative colitis refractory to steroid therapy". The New England Journal of Medicine. 330 (26): 1841–1845. doi:10.1056/NEJM199406303302601. PMID 8196726.
- ^ Weisshof R, Ollech JE, El Jurdi K, Yvellez OV, Cohen RD, Sakuraba A, et al. (September 2019). "Ciclosporin Therapy After Infliximab Failure in Hospitalized Patients With Acute Severe Colitis is Effective and Safe". Journal of Crohn's & Colitis. 13 (9): 1105–1110. doi:10.1093/ecco-jcc/jjz032. PMC 7327272. PMID 30726894.
- ^ Azad Khan AK, Piris J, Truelove SC (October 1977). "An experiment to determine the active therapeutic moiety of sulphasalazine". Lancet. 2 (8044): 892–895. doi:10.1016/s0140-6736(77)90831-5. PMID 72239. S2CID 44785199.
- ^ Murray A, Nguyen TM, Parker CE, Feagan BG, MacDonald JK (August 2020). "Oral 5-aminosalicylic acid for induction of remission in ulcerative colitis". The Cochrane Database of Systematic Reviews. 2020 (8): CD000543. doi:10.1002/14651858.CD000543.pub5. PMC 8189994. PMID 32786164.
- ^ Murray A, Nguyen TM, Parker CE, Feagan BG, MacDonald JK (August 2020). "Oral 5-aminosalicylic acid for maintenance of remission in ulcerative colitis". The Cochrane Database of Systematic Reviews. 2020 (8): CD000544. doi:10.1002/14651858.CD000544.pub5. PMC 8094989. PMID 32856298.
- ^ Marshall JK, Thabane M, Steinhart AH, Newman JR, Anand A, Irvine EJ (November 2012). "Rectal 5-aminosalicylic acid for maintenance of remission in ulcerative colitis". The Cochrane Database of Systematic Reviews. 11: CD004118. doi:10.1002/14651858.CD004118.pub2. PMID 23152224.
- ^ Salahudeen MS (June 2019). "A review of current evidence allied to step-up and top-down medication therapy in inflammatory bowel disease". Drugs of Today. 55 (6): 385–405. doi:10.1358/dot.2019.55.6.2969816. PMID 31250843. S2CID 195763151.
- ^ Axelrad JE, Lichtiger S, Yajnik V (May 2016). "Inflammatory bowel disease and cancer: The role of inflammation, immunosuppression, and cancer treatment". World Journal of Gastroenterology (Review). 22 (20): 4794–4801. doi:10.3748/wjg.v22.i20.4794. PMC 4873872. PMID 27239106.
- ^ Stevens JP, Ballengee CR, Chandradevan R, Thompson AB, Schoen BT, Kugathasan S, Sauer CG (October 2019). "Performance of Interferon-Gamma Release Assays for Tuberculosis Screening in Pediatric Inflammatory Bowel Disease". Journal of Pediatric Gastroenterology and Nutrition. 69 (4): e111–e116. doi:10.1097/MPG.0000000000002428. PMID 31261245. S2CID 195771593.
- ^ Lee CK, Wong SH, Lui G, Tang W, Tam LS, Ip M, et al. (July 2018). "A Prospective Study to Monitor for Tuberculosis During Anti-tumour Necrosis Factor Therapy in Patients With Inflammatory Bowel Disease and Immune-mediated Inflammatory Diseases". Journal of Crohn's & Colitis. 12 (8): 954–962. doi:10.1093/ecco-jcc/jjy057. PMID 29757355. S2CID 21673794.
- ^ Calkins BM (December 1989). "A meta-analysis of the role of smoking in inflammatory bowel disease". Digestive Diseases and Sciences. 34 (12): 1841–1854. doi:10.1007/BF01536701. PMID 2598752. S2CID 5775169.
- ^ Lakatos PL, Szamosi T, Lakatos L (December 2007). "Smoking in inflammatory bowel diseases: good, bad or ugly?". World Journal of Gastroenterology. 13 (46): 6134–6139. doi:10.3748/wjg.13.6134. PMC 4171221. PMID 18069751.
- ^ Calabrese E, Yanai H, Shuster D, Rubin DT, Hanauer SB (August 2012). "Low-dose smoking resumption in ex-smokers with refractory ulcerative colitis". Journal of Crohn's & Colitis. 6 (7): 756–762. doi:10.1016/j.crohns.2011.12.010. PMID 22398093.
- ^ Cosnes J (June 2004). "Tobacco and IBD: relevance in the understanding of disease mechanisms and clinical practice". Best Practice & Research. Clinical Gastroenterology. 18 (3): 481–496. doi:10.1016/j.bpg.2003.12.003. PMID 15157822.
- ^ Guslandi M (October 1999). "Nicotine treatment for ulcerative colitis". British Journal of Clinical Pharmacology. 48 (4): 481–484. doi:10.1046/j.1365-2125.1999.00039.x. PMC 2014383. PMID 10583016.
- ^ Sandborn WJ, Tremaine WJ, Offord KP, Lawson GM, Petersen BT, Batts KP, et al. (March 1997). "Transdermal nicotine for mildly to moderately active ulcerative colitis. A randomized, double-blind, placebo-controlled trial". Annals of Internal Medicine. 126 (5): 364–371. doi:10.7326/0003-4819-126-5-199703010-00004. PMID 9054280. S2CID 25745900.
- ^ Bonapace CR, Mays DA (1997). "The effect of mesalamine and nicotine in the treatment of inflammatory bowel disease". The Annals of Pharmacotherapy. 31 (7–8): 907–913. doi:10.1177/106002809703100719. PMID 9220055. S2CID 24122049.
- ^ Kennedy LD (September 1996). "Nicotine therapy for ulcerative colitis". The Annals of Pharmacotherapy. 30 (9): 1022–1023. PMID 8876866.
- ^ Rubin DT, Hanauer SB (August 2000). "Smoking and inflammatory bowel disease". European Journal of Gastroenterology & Hepatology. 12 (8): 855–862. doi:10.1097/00042737-200012080-00004. PMID 10958212.
- ^ a b Goddard AF, James MW, McIntyre AS, Scott BB, et al. (British Society of Gastroenterology) (October 2011). "Guidelines for the management of iron deficiency anaemia". Gut. 60 (10): 1309–1316. doi:10.1136/gut.2010.228874. PMID 21561874.
- ^ Gasche C, Berstad A, Befrits R, Beglinger C, Dignass A, Erichsen K, et al. (December 2007). "Guidelines on the diagnosis and management of iron deficiency and anemia in inflammatory bowel diseases". Inflammatory Bowel Diseases. 13 (12): 1545–1553. doi:10.1002/ibd.20285. PMID 17985376.
- ^ Mowat C, Cole A, Windsor A, Ahmad T, Arnott I, Driscoll R, et al. (May 2011). "Guidelines for the management of inflammatory bowel disease in adults". Gut. 60 (5): 571–607. doi:10.1136/gut.2010.224154. PMID 21464096. S2CID 8269837.
- ^ a b Agabegi ED, Agabegi SS (2008). "Inflammatory bowel disease (IBD)". Step-Up to Medicine (Step-Up Series). Hagerstwon, MD: Lippincott Williams & Wilkins. pp. 152–156. ISBN 0-7817-7153-6.
- ^ Feller M, Huwiler K, Schoepfer A, Shang A, Furrer H, Egger M (February 2010). "Long-term antibiotic treatment for Crohn's disease: systematic review and meta-analysis of placebo-controlled trials". Clinical Infectious Diseases. 50 (4): 473–80. doi:10.1086/649923. PMID 20067425.
- ^ Prantera C, Scribano ML (July 2009). "Antibiotics and probiotics in inflammatory bowel disease: why, when, and how". Current Opinion in Gastroenterology. 25 (4): 329–33. doi:10.1097/MOG.0b013e32832b20bf. PMID 19444096.
- ^ "Living with a stoma". IBD Relief.
- ^ "Colectomy Not a Final Cure for Ulcerative Colitis, Data Show". www.mdedge.com. Retrieved 15 December 2019.
- ^ Pappou EP, Kiran RP (June 2016). "The Failed J Pouch". Clinics in Colon and Rectal Surgery. 29 (2): 123–129. doi:10.1055/s-0036-1580724. PMC 4882179. PMID 27247537.
- ^ a b Clarke WT, Feuerstein JD (August 2019). "Colorectal cancer surveillance in inflammatory bowel disease: Practice guidelines and recent developments". World Journal of Gastroenterology. 25 (30): 4148–4157. doi:10.3748/wjg.v25.i30.4148. PMC 6700690. PMID 31435169. S2CID 201114672.
- ^ Fedorak RN (November 2010). "Probiotics in the management of ulcerative colitis". Gastroenterology & Hepatology. 6 (11): 688–690. PMC 3033537. PMID 21437015.
- ^ Derwa Y, Gracie DJ, Hamlin PJ, Ford AC (August 2017). "Systematic review with meta-analysis: the efficacy of probiotics in inflammatory bowel disease". Alimentary Pharmacology & Therapeutics. 46 (4): 389–400. doi:10.1111/apt.14203. PMID 28653751.
- ^ Borody TJ, Brandt LJ, Paramsothy S (January 2014). "Therapeutic faecal microbiota transplantation: current status and future developments". Current Opinion in Gastroenterology. 30 (1): 97–105. doi:10.1097/MOG.0000000000000027. PMC 3868025. PMID 24257037.
- ^ Narula N, Kassam Z, Yuan Y, Colombel JF, Ponsioen C, Reinisch W, Moayyedi P (October 2017). "Systematic Review and Meta-analysis: Fecal Microbiota Transplantation for Treatment of Active Ulcerative Colitis". Inflammatory Bowel Diseases. 23 (10): 1702–1709. doi:10.1097/MIB.0000000000001228. PMID 28906291.
- ^ Shi Y, Dong Y, Huang W, Zhu D, Mao H, Su P (2016). "Fecal Microbiota Transplantation for Ulcerative Colitis: A Systematic Review and Meta-Analysis". PLOS ONE. 11 (6): e0157259. Bibcode:2016PLoSO..1157259S. doi:10.1371/journal.pone.0157259. PMC 4905678. PMID 27295210.
- ^ Costello SP, Hughes PA, Waters O, Bryant RV, Vincent AD, Blatchford P, et al. (January 2019). "Effect of Fecal Microbiota Transplantation on 8-Week Remission in Patients With Ulcerative Colitis: A Randomized Clinical Trial". JAMA. 321 (2): 156–164. doi:10.1001/jama.2018.20046. PMC 6439766. PMID 30644982.
- ^ Hanai H, Iida T, Takeuchi K, Watanabe F, Maruyama Y, Andoh A, et al. (December 2006). "Curcumin maintenance therapy for ulcerative colitis: randomized, multicenter, double-blind, placebo-controlled trial". Clinical Gastroenterology and Hepatology. 4 (12): 1502–1506. doi:10.1016/j.cgh.2006.08.008. PMID 17101300.
- ^ a b Kumar S, Ahuja V, Sankar MJ, Kumar A, Moss AC (October 2012). "Curcumin for maintenance of remission in ulcerative colitis". The Cochrane Database of Systematic Reviews. 10: CD008424. doi:10.1002/14651858.CD008424.pub2. PMC 4001731. PMID 23076948.
- ^ Kafil TS, Nguyen TM, MacDonald JK, Chande N (November 2018). "Cannabis for the treatment of ulcerative colitis". The Cochrane Database of Systematic Reviews. 11: CD012954. doi:10.1002/14651858.CD012954.pub2. PMC 6516819. PMID 30406638.
- ^ Sinopoulou V, Gordon M, Dovey TM, Akobeng AK, et al. (Cochrane Gut Group) (July 2021). "Interventions for the management of abdominal pain in ulcerative colitis". The Cochrane Database of Systematic Reviews. 2021 (7): CD013589. doi:10.1002/14651858.CD013589.pub2. PMC 8407332. PMID 34291816.
- ^ Kevans D, Murthy S, Mould DR, Silverberg MS (May 2018). "Accelerated Clearance of Infliximab is Associated With Treatment Failure in Patients With Corticosteroid-Refractory Acute Ulcerative Colitis". Journal of Crohn's & Colitis. 12 (6): 662–669. doi:10.1093/ecco-jcc/jjy028. PMID 29659758.
- ^ Horio Y, Uchino M, Bando T, Chohno T, Sasaki H, Hirata A, et al. (May 2017). "Rectal-sparing type of ulcerative colitis predicts lack of response to pharmacotherapies". BMC Surgery. 17 (1): 59. doi:10.1186/s12893-017-0255-5. PMC 5437574. PMID 28526076.
- ^ 마크 T. 오스터맨, 게리 R.리히텐슈타인궤양성 대장염, 116장, 페이지 2023–2061.인: Sleisenger and Fordtran's Sweator and Liver Disease, 제10판, 2016년.eds 마크 펠드먼, 로렌스 S프리드먼, 로렌스 J. 브랜트
- ^ Patil DT, Odze RD (August 2017). "Backwash Is Hogwash: The Clinical Significance of Ileitis in Ulcerative Colitis". The American Journal of Gastroenterology. 112 (8): 1211–1214. doi:10.1038/ajg.2017.182. PMID 28631729. S2CID 10801391.
- ^ Leighton JA, Shen B, Baron TH, Adler DG, Davila R, Egan JV, et al. (April 2006). "ASGE guideline: endoscopy in the diagnosis and treatment of inflammatory bowel disease". Gastrointestinal Endoscopy. 63 (4): 558–565. doi:10.1016/j.gie.2006.02.005. PMID 16564852.
- ^ a b Jess T, Gamborg M, Munkholm P, Sørensen TI (March 2007). "Overall and cause-specific mortality in ulcerative colitis: meta-analysis of population-based inception cohort studies". The American Journal of Gastroenterology. 102 (3): 609–617. doi:10.1111/j.1572-0241.2006.01000.x. PMID 17156150. S2CID 2086542.
- ^ da Silva BC, Lyra AC, Rocha R, Santana GO (July 2014). "Epidemiology, demographic characteristics and prognostic predictors of ulcerative colitis". World Journal of Gastroenterology. 20 (28): 9458–9467. doi:10.3748/wjg.v20.i28.9458. PMC 4110577. PMID 25071340.
- ^ Nguyen M, Bradford K, Zhang X, Shih DQ (January 2011). "Cytomegalovirus Reactivation in Ulcerative Colitis Patients". Ulcers. 2011: 1–7. doi:10.1155/2011/282507. PMC 3124815. PMID 21731826.
- ^ Karlinger K, Györke T, Makö E, Mester A, Tarján Z (September 2000). "The epidemiology and the pathogenesis of inflammatory bowel disease". European Journal of Radiology. 35 (3): 154–167. doi:10.1016/s0720-048x(00)00238-2. PMID 11000558.
- ^ Podolsky DK (August 2002). "Inflammatory bowel disease". The New England Journal of Medicine. 347 (6): 417–429. doi:10.1056/NEJMra020831. PMID 12167685.
- ^ Schmidt JA, Marshall J, Hayman MJ (December 1985). "Identification and characterization of the chicken transferrin receptor". The Biochemical Journal. 232 (3): 735–741. doi:10.1042/bj2320735. PMC 1152945. PMID 3004417.
- ^ Shivananda S, Lennard-Jones J, Logan R, Fear N, Price A, Carpenter L, van Blankenstein M (November 1996). "Incidence of inflammatory bowel disease across Europe: is there a difference between north and south? Results of the European Collaborative Study on Inflammatory Bowel Disease (EC-IBD)". Gut. 39 (5): 690–697. doi:10.1136/gut.39.5.690. PMC 1383393. PMID 9014768.
- ^ Sonnenberg A, McCarty DJ, Jacobsen SJ (January 1991). "Geographic variation of inflammatory bowel disease within the United States". Gastroenterology. 100 (1): 143–149. doi:10.1016/0016-5085(91)90594-B. PMID 1983816.
- ^ Burisch J, Pedersen N, Čuković-Čavka S, Brinar M, Kaimakliotis I, Duricova D, et al. (April 2014). "East-West gradient in the incidence of inflammatory bowel disease in Europe: the ECCO-EpiCom inception cohort". Gut. 63 (4): 588–597. doi:10.1136/gutjnl-2013-304636. hdl:2336/325171. PMID 23604131. S2CID 25069828.
- ^ Andersson RE, Olaison G, Tysk C, Ekbom A (March 2001). "Appendectomy and protection against ulcerative colitis". The New England Journal of Medicine. 344 (11): 808–814. doi:10.1056/NEJM200103153441104. PMID 11248156.
- ^ a b Boyko EJ, Koepsell TD, Perera DR, Inui TS (March 1987). "Risk of ulcerative colitis among former and current cigarette smokers". The New England Journal of Medicine. 316 (12): 707–710. doi:10.1056/NEJM198703193161202. PMID 3821808.
- ^ a b "Epidemiology of the IBD". Centers for Disease Control and Prevention (CDC). Archived from the original on 23 February 2017. Retrieved 23 February 2017.
- ^ Makhlouf GM, Zfass AM, Said SI, Schebalin M (April 1978). "Effects of synthetic vasoactive intestinal peptide (VIP), secretin and their partial sequences on gastric secretion". Proceedings of the Society for Experimental Biology and Medicine. 157 (4): 565–568. doi:10.3181/00379727-157-40097. PMID 349569. S2CID 40543366.
- ^ "Ulcerative colitis:management". National Institute for Health and Care Excellence, Ulcerative colitis: management Clinical guideline (PDF). 3 May 2019.
- ^ a b Summers RW, Elliott DE, Urban JF, Thompson RA, Weinstock JV (April 2005). "Trichuris suis therapy for active ulcerative colitis: a randomized controlled trial". Gastroenterology. 128 (4): 825–832. doi:10.1053/j.gastro.2005.01.005. PMID 15825065.
- ^ a b Bennett CF, Condon TC, Grimm S, Chan H, Chiang MY (1994). "Inhibition of endothelial cell-leukocyte adhesion molecule expression with antisense oligonucleotides". The Journal of Immunology. 152 (1): 3530–40.
- ^ Jones SC, Banks RE, Haidar A, Gearing AJ, Hemingway IK, Ibbotson SH, et al. (May 1995). "Adhesion molecules in inflammatory bowel disease". Gut. 36 (5): 724–730. doi:10.1136/gut.36.5.724. PMC 1382677. PMID 7541009.
- ^ van Deventer SJ, Wedel MK, Baker BF, Xia S, Chuang E, Miner PB (May 2006). "A phase II dose ranging, double-blind, placebo-controlled study of alicaforsen enema in subjects with acute exacerbation of mild to moderate left-sided ulcerative colitis". Alimentary Pharmacology & Therapeutics. 23 (10): 1415–1425. doi:10.1111/j.1365-2036.2006.02910.x. PMID 16669956. S2CID 31495688.
- ^ Ghouri YA, Richards DM, Rahimi EF, Krill JT, Jelinek KA, DuPont AW (9 December 2014). "Systematic review of randomized controlled trials of probiotics, prebiotics, and synbiotics in inflammatory bowel disease". Clinical and Experimental Gastroenterology. 7: 473–487. doi:10.2147/CEG.S27530. PMC 4266241. PMID 25525379.
- ^ a b Strøbæk D, Brown DT, Jenkins DP, Chen YJ, Coleman N, Ando Y, et al. (January 2013). "NS6180, a new K(Ca) 3.1 channel inhibitor prevents T-cell activation and inflammation in a rat model of inflammatory bowel disease". British Journal of Pharmacology. 168 (2): 432–444. doi:10.1111/j.1476-5381.2012.02143.x. PMC 3572569. PMID 22891655.
- ^ a b Bennike TB, Carlsen TG, Ellingsen T, Bonderup OK, Glerup H, Bøgsted M, et al. (September 2015). "Neutrophil Extracellular Traps in Ulcerative Colitis: A Proteome Analysis of Intestinal Biopsies". Inflammatory Bowel Diseases. 21 (9): 2052–2067. doi:10.1097/MIB.0000000000000460. PMC 4603666. PMID 25993694.
- ^ Kirov S, Sasson A, Zhang C, Chasalow S, Dongre A, Steen H, et al. (February 2019). "Degradation of the extracellular matrix is part of the pathology of ulcerative colitis". Molecular Omics. 15 (1): 67–76. doi:10.1039/C8MO00239H. PMID 30702115.
- ^ Raithel M, Winterkamp S, Weidenhiller M, Müller S, Hahn EG (July 2007). "Combination therapy using fexofenadine, disodium cromoglycate, and a hypoallergenic amino acid-based formula induced remission in a patient with steroid-dependent, chronically active ulcerative colitis". International Journal of Colorectal Disease. 22 (7): 833–839. doi:10.1007/s00384-006-0120-y. PMID 16944185. S2CID 2605447.
- ^ a b Dhaneshwar S, Gautam H (August 2012). "Exploring novel colon-targeting antihistaminic prodrug for colitis". Journal of Physiology and Pharmacology. 63 (4): 327–337. PMID 23070081.
- ^ Vermeire S, O'Byrne S, Keir M, Williams M, Lu TT, Mansfield JC, et al. (July 2014). "Etrolizumab as induction therapy for ulcerative colitis: a randomised, controlled, phase 2 trial". Lancet. 384 (9940): 309–318. doi:10.1016/S0140-6736(14)60661-9. PMID 24814090. S2CID 7369482.
- ^ Rosenfeld G, Parker CE, MacDonald JK, Bressler B (December 2015). "Etrolizumab for induction of remission in ulcerative colitis". The Cochrane Database of Systematic Reviews. 2015 (12): CD011661. doi:10.1002/14651858.CD011661.pub2. PMC 8612697. PMID 26630451.
- ^ Makker J, Hommes DW (2016). "Etrolizumab for ulcerative colitis: the new kid on the block?". Expert Opinion on Biological Therapy. 16 (4): 567–572. doi:10.1517/14712598.2016.1158807. PMID 26914639. S2CID 24706213.
- ^ Abreu MT, Plevy S, Sands BE, Weinstein R (2007). "Selective leukocyte apheresis for the treatment of inflammatory bowel disease". Journal of Clinical Gastroenterology. 41 (10): 874–888. doi:10.1097/MCG.0b013e3180479435. PMID 18090155. S2CID 36724094.
- ^ Vernia P, D'Ovidio V, Meo D (October 2010). "Leukocytapheresis in the treatment of inflammatory bowel disease: Current position and perspectives". Transfusion and Apheresis Science. 43 (2): 227–229. doi:10.1016/j.transci.2010.07.023. PMID 20817610.
추가 정보
- Rubin DT, Ananthakrishnan AN, Siegel CA, Sauer BG, Long MD (March 2019). "ACG Clinical Guideline: Ulcerative Colitis in Adults". The American Journal of Gastroenterology. 114 (3): 384–413. doi:10.14309/ajg.0000000000000152. PMID 30840605. S2CID 73473272.

- Torpy JM, Lynm C, Golub RM (January 2012). "JAMA patient page. Ulcerative colitis". JAMA. 307 (1): 104. doi:10.1001/jama.2011.1889. PMID 22215172.