알츠하이머병
Alzheimer's disease이 기사는 업데이트해야 합니다.한 이벤트나 하여 이 할 수 바랍니다. (2021년 3월) |
| 알츠하이머병 | |
|---|---|
 | |
| 알츠하이머 환자의 뇌와 비교한 정상 뇌의 도표 | |
| 발음 |
|
| 전문 | 신경학 |
| 증상 | 기억력 감퇴, 언어문제, 방향감각 상실, 기분변동[1][2] |
| 합병증 | 말기의[3] 탈수 및 폐렴 |
| 보통발병 | 65세이상[4] |
| 지속 | 장기[2] |
| 원인들 | 제대로[1] 이해되지 않음 |
| 위험요소 | 유전학, 머리 부상, 우울증, 고혈압[1] |
| 진단방법 | 다른 가능한 원인을[5] 배제한 후 증상 및 인지 검사를 기반으로 합니다. |
| 감별진단 | 정상적인 뇌노화,[1] Lewy body 치매, [6]Trisomy 21[7] |
| 약 | 아세틸콜린에스테라제 억제제, NMDA 수용체 길항제 (작은 이점)[medical citation needed] |
| 예후 | 기대수명 3~9년[needs update][8] |
| 빈도수. | 5천만 (2020)[9] |
| 이름은 다음과 같습니다. | 알로이스 알츠하이머 |
알츠하이머병(Alzheimer's disease, AD)은 일반적으로 천천히 시작하여 점차 악화되는 신경퇴행성 질환으로 [2]치매 발생의 60~70%를 차지하는 원인이 됩니다.[2][10] 가장 흔한 초기 증상은 최근 사건을 기억하기 어렵다는 것입니다.[1] 질병이 진행됨에 따라 증상에는 언어, 방향감각 상실(쉽게 길을 잃는 것을 포함), 기분 전환, 동기 상실, 자기 무시 및 행동 문제가 포함될 수 있습니다.[2] 한 사람의 상태가 나빠지면서, 그들은 종종 가족과 사회에서 물러납니다.[11] 점차 신체 기능이 상실되어 결국 사망에 이르게 됩니다. 진행 속도는 다를 수 있지만 진단 후 평균 수명은 3~9년입니다.[needs update][8][12]
알츠하이머병의 원인은 잘 알려져 있지 않습니다.[11] 개발과 관련된 많은 환경 및 유전적 위험 요소가 있습니다. 가장 강력한 유전적 위험 인자는 APOE의 대립유전자에서 기인합니다.[13][14] 다른 위험 요소에는 머리 부상 이력, 임상 우울증 및 고혈압이 포함됩니다.[1] 질병 과정은 주로 아밀로이드 플라크, 신경섬유 엉킴 및 뇌의 신경 연결 손실과 관련이 있습니다.[15] 가능한 진단은 다른 가능한 원인을 배제하기 위해 의료 영상 및 혈액 검사와 함께 질병 이력 및 인지 검사를 기반으로 합니다.[5][16] 초기 증상은 정상적인 뇌 노화로 오인되는 경우가 많습니다.[11] 확실한 진단을 위해서는 뇌 조직의 검사가 필요하지만, 이는 사후에만 이루어질 수 있습니다.[17] 좋은 영양, 신체 활동 및 사회적 참여는 일반적으로 노화에 도움이 되는 것으로 알려져 있으며 인지 기능 저하 및 알츠하이머 위험을 줄이는데 도움이 될 수 있습니다.[15]
어떤 치료법도 일시적으로 증상이 개선될 수 있지만, 어떤 치료법도 그 진행을 멈추거나 되돌릴 수 없습니다.[2] 피해를 입은 사람들은 도움을 받기 위해 다른 사람들에게 점점 더 의존하게 되고, 종종 간병인에게 부담을 줍니다.[18] 압력에는 사회적, 심리적, 신체적, 경제적 요소가 포함될 수 있습니다.[18] 운동 프로그램은 일상 생활의 활동과 관련하여 도움이 될 수 있으며 잠재적으로 결과를 향상시킬 수 있습니다.[19] 치매로 인한 행동 문제나 정신병은 항정신병약으로 치료하는 경우가 많은데, 이는 이득이 거의 없고 조기 사망 위험이 높아지기 때문에 보통 권장하지 않습니다.[20][21]
2020년 기준 전 세계 알츠하이머병 환자는 약 5천만 명입니다.[9] 가장 많은 경우 65세 이상에서 시작되지만 30대에서 60대 중반까지 초기 발병률이 10%에 이릅니다.[17][4] 65세 이상은 약 6%,[11] 남성보다는 여성이 더 자주 영향을 미칩니다.[22] 이 병의 이름은 1906년에 처음 기술한 독일의 정신과 의사이자 병리학자인 알로이스 알츠하이머(Alois Alzheimer)의 이름을 따서 지어졌습니다.[23] 알츠하이머가 사회에 미치는 경제적 부담은 크고, 전 세계적으로 연간 약 1조 달러가 소요될 것으로 추정됩니다.[9] 이것은 미국에서 사망 원인 7위에 올라있습니다.[15]
징후 및 증상
알츠하이머의 진행 과정은 일반적으로 인지 및 기능 장애의 점진적인 패턴과 함께 세 단계로 설명됩니다.[24][17] 세 단계는 초기 또는 경증, 중간 또는 중등도, 후기 또는 중증으로 설명됩니다.[24] 이 질병은 기억력과 관련된 해마를 표적으로 하는 것으로 알려져 있으며, 이것이 기억력 장애의 첫 번째 증상의 원인이 됩니다. 질병이 진행됨에 따라 기억력 손상의 정도도 증가합니다.[15]
첫 증상

첫 번째 증상은 노화나 스트레스 때문이라고 잘못 생각하는 경우가 많습니다.[25] 상세한 신경 심리 검사를 통해 알츠하이머병 진단 임상 기준을 충족하기까지 최대 8년 동안 가벼운 인지 장애를 드러낼 수 있습니다.[26] 이러한 초기 증상은 일상생활의 가장 복잡한 활동에 영향을 미칠 수 있습니다.[27] 가장 눈에 띄는 적자는 단기기억상실증으로 최근 학습한 사실을 기억하기 어렵고 새로운 정보를 습득하지 못하는 것으로 나타납니다.[26]
주의력, 계획, 유연성, 추상적 사고의 실행 기능에 대한 미묘한 문제나 의미 기억(의미의 기억, 개념 관계)의 장애도 알츠하이머병의 초기 단계의 증상일 수 있습니다.[26] 병증과 우울증은 이 단계에서 볼 수 있으며, 병이 진행되는 동안 병증은 가장 지속적인 증상으로 남아 있습니다.[28][29] 경도인지장애(MCI)는 종종 정상 노화와 치매 사이의 과도기 단계로 밝혀집니다. MCI는 다양한 증상을 보일 수 있으며, 기억력 감퇴가 주된 증상일 때는 기억력 감퇴 MCI라고 하며 알츠하이머병의 전구병기로 흔히 볼 수 있습니다.[30] 기억력 MCI는 알츠하이머와 연관될 가능성이 90% 이상입니다.[31]
초기단계
알츠하이머병을 앓고 있는 사람들의 경우, 학습과 기억력의 손상이 증가하면서 결국 확정적인 진단으로 이어집니다. 기억력 문제보다 언어, 실행 기능, 지각(아그노시아) 또는 동작 실행(아프락시아)에 대한 어려움이 더 두드러지는 경우는 적은 비율입니다.[32] 알츠하이머병은 모든 기억 용량에 똑같이 영향을 주지 않습니다. 사람의 삶에 대한 오래된 기억(에피소드 기억), 학습된 사실(의미적 기억), 암묵적 기억(포크를 사용하여 음식을 먹거나 잔에서 마시는 방법과 같은 일을 하는 방법에 대한 신체의 기억)은 새로운 사실이나 기억보다 덜 영향을 받습니다.[33][34]
언어 문제는 주로 어휘가 줄어들고 단어의 유창성이 감소하여 구어와 문자 언어의 전반적인 빈곤으로 이어지는 것이 특징입니다.[32][35] 이 단계에서 알츠하이머 환자는 일반적으로 기본적인 생각을 적절하게 전달할 수 있습니다.[32][35][36] 쓰기, 그리기, 옷 입히기와 같은 미세한 운동 작업을 수행하는 동안 특정한 움직임 조정 및 계획상의 어려움(apraxia)이 있을 수 있지만 일반적으로 눈에 띄지 않습니다.[32] 질병이 진행됨에 따라, 알츠하이머 병을 가진 사람들은 종종 독립적으로 많은 일을 계속 수행할 수 있지만, 인지적으로 가장 어려운 활동에 대한 도움이나 감독이 필요할 수 있습니다.[32]
중간단계
점진적인 악화는 결국 독립성을 저해하고, 피험자들은 일상 생활의 가장 일반적인 활동을 수행할 수 없습니다.[32] 어휘를 기억하지 못해 언어적 어려움이 뚜렷해지고, 이로 인해 잘못된 단어의 치환(parapasia)이 빈번하게 발생합니다. 읽기와 쓰기 능력도 점진적으로 떨어집니다.[32][36] 복잡한 운동 순서는 시간이 지날수록 조율이 덜 되고 알츠하이머병이 진행되면서 낙상 위험이 높아집니다.[32] 이 단계에서는 기억력 문제가 악화되어 가까운 친척을 인식하지 못할 수도 있습니다.[32] 이전에는 온전했던 장기 기억력이 손상됩니다.[32]
행동 및 신경 정신과적 변화가 더욱 널리 퍼집니다. 일반적인 증상은 방황, 짜증 및 감정적 불안정으로 인해 울거나 예정에 없는 공격성의 폭발 또는 돌봄에 대한 저항입니다.[32] 선다운도 나타날 수 있습니다.[37] 알츠하이머병 환자의 약 30%는 환상적인 오인 및 기타 망상 증상이 발생합니다.[32] 피험자들은 또한 자신의 질병 과정과 한계에 대한 통찰력을 잃습니다.[32] 요실금이 생길 수 있습니다.[32] 이러한 증상은 친척과 간병인에게 스트레스를 발생시키며, 이는 재가에서 다른 장기요양시설로 이동함으로써 감소될 수 있습니다.[32][38]
후기

말기 또는 중증 단계로 알려진 최종 단계에서는 간병인에게 전적으로 의존합니다.[15][24][32] 언어는 단순한 문구나 심지어 한 단어로 줄어들기 때문에 결국 말을 완전히 잃게 됩니다.[32][36] 언어 능력이 상실되었음에도 불구하고, 사람들은 종종 감정적인 신호를 이해하고 돌아올 수 있습니다. 공격성은 여전히 존재할 수 있지만, 극도의 무관심과 탈진은 훨씬 더 흔한 증상입니다. 알츠하이머병을 앓고 있는 사람들은 궁극적으로 가장 간단한 일도 혼자서 할 수 없게 될 것입니다. 근육량과 운동성은 병석에 누워 스스로 음식을 먹지 못할 정도로 악화됩니다. 사망 원인은 대개 욕창이나 폐렴에 감염되는 등 외부 요인이지 질병 자체가 아닙니다.[32] 죽음 직전의 역설적인 명쾌함이 있는 경우도 있는데, 예상치 못한 정신적 명료함의 회복이 있는 것입니다.[39]
원인들
알츠하이머병은 아밀로이드 플라크와 타우 단백질로 세포 내에 축적된 아밀로이드 베타(Aβ)가 비정상적으로 뇌에 형성되어 신경섬유결합으로 신경 기능과 연결성에 영향을 미쳐 뇌 기능이 점진적으로 소실될 때 발생하는 것으로 추정됩니다.[40][41] 이렇게 변화된 단백질 제거 능력은 나이와 관련이 있고, 뇌 콜레스테롤에 의해 조절되며,[42] 다른 신경퇴행성 질환과 관련이 있습니다.[43][44]
결정론적 유전적 차이가 확인된 경우의 1~2%를 [9]제외하고는 대부분의 알츠하이머 환자의 원인은 여전히 알려지지 않았습니다.[13] 그 근본적인 원인을 설명하려는 몇 가지 경쟁 가설이 있는데, 가장 지배적인 가설은 아밀로이드 베타 가설입니다.[9]
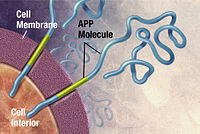
대부분의 약물 치료의 기초가 되는 가장 오래된 가설은 신경전달물질인 아세틸콜린의 합성 감소로 알츠하이머병이 발생한다는 콜린성 가설입니다.[9] 변연계와 대뇌피질에서 주목되는 콜린신경세포의 소실은 알츠하이머 진행의 핵심적인 특징입니다.[30] 1991년 아밀로이드 가설은 세포외 아밀로이드 베타(Aβ) 침전물이 질병의 근본적인 원인이라고 가정했습니다.[45][46] 이 가설을 뒷받침하는 것은 21번 염색체의 아밀로이드 전구체 단백질(APP)에 대한 유전자 위치에서 비롯되며, 추가 유전자 사본을 가진 21번 트리솜(Down Syndrome) 환자는 40세까지 최소한 알츠하이머병의 초기 증상을 거의 보편적으로 나타낸다는 사실입니다.[7] 아포지단백의 특정 동형인 APOE4는 알츠하이머병의 주요 유전적 위험 인자입니다.[10] 아포지단백은 베타 아밀로이드의 분해를 향상시키지만, 일부 이소형(APOE4와 같은)은 이 작업에서 그다지 효과적이지 않아 뇌에 과도한 아밀로이드 축적을 초래합니다.[47]
유전의
후기발병
후기 발병 알츠하이머는 약 70%가 유전 가능합니다.[48][49] 2020년 유전자 모델은 알츠하이머병을 90%의 정확도로 예측합니다.[50] 대부분의 알츠하이머병은 가족이 아니기 때문에 산발성 알츠하이머병이라고 합니다.[medical citation needed] 산발성 알츠하이머병은 대부분 발병이 늦어 65세 이후 발병합니다.[51]
산발성 알츠하이머병의 가장 강력한 유전적 위험인자는 APOE ε4입니다. APOE ε4는 아포지단백 E(APOE)의 4가지 대립유전자 중 하나입니다. APOE는 지단백질 입자에서 지질 결합 단백질에 중요한 역할을 하며 ε4 대립유전자는 이 기능을 방해합니다. 알츠하이머병 환자의 40~80%는 적어도 하나의 APOE ε4 대립유전자를 가지고 있습니다. APOE ε4 대립유전자는 이형 접합체에서 3배, 동형 접합체에서 15배 질병의 위험을 증가시킵니다. 많은 인간의 질병과 마찬가지로 환경 영향과 유전자 변형은 불완전한 침투를 초래합니다. 예를 들어, 나이지리아 요루바 사람들은 APOE ε4의 용량과 다른 인간 집단에서 볼 수 있는 알츠하이머병의 발병률 또는 발병 연령 사이의 관계를 보여주지 않습니다.
조기발병
상염색체 우성 효과로 인해 유전되는 경우는 1~2%에 불과하며, 알츠하이머는 다유전성이 매우 높습니다. 상염색체 우성 변이에 의해 발병하면 조기 발병 가족성 알츠하이머병으로 알려져 더 희귀하고 진행 속도가 빠릅니다.[13] 산발성 알츠하이머병 중 조기 발병률이 5% 미만이고,[13] 조기 발병 알츠하이머병은 유전성이 약 90%에 달합니다.[48][49] FAD는 일반적으로 한 세대 또는 여러 세대에서 영향을 받는 여러 사람을 의미합니다.[medical citation needed][57]
조기 발병 가족성 알츠하이머병은 아밀로이드 베타 전구체 단백질(APP)과 프레세닐린 PSEN1, PSEN2를 암호화하는 유전자 세 가지 중 하나의 돌연변이 때문입니다.[31] APP와 프레세닐린 유전자의 대부분의 돌연변이는 아밀로이드 플라크의 주성분인 아밀로이드 베타(Aβ)42라는 작은 단백질의 생성을 증가시킵니다.[58] 일부 돌연변이는 뇌에서 Aβ42 수준을 증가시키지 않고 Aβ42와 다른 주요 형태, 특히 Aβ40 사이의 비율을 변경할 뿐입니다.[59] 상염색체 우성 알츠하이머병과 관련된 다른 두 유전자는 ABCA7과 SORL1입니다.[60]
TREM2 유전자의 대립유전자는 알츠하이머병에 걸릴 위험이 3배에서 5배 더 높은 것과 관련이 있습니다.[61]
일본의 가족성 알츠하이머병 혈통은 APP의 코돈 693의 결손 돌연변이와 관련이 있는 것으로 밝혀졌습니다.[62] 이 돌연변이와 알츠하이머병과의 연관성은 2008년에 처음 보고되었고,[63] 오사카 돌연변이라고 알려져 있습니다. 이 돌연변이를 가진 동형 접합체만이 알츠하이머병에 걸릴 위험이 증가합니다. 이 돌연변이는 Aβ 올리고머화를 가속화하지만 단백질은 아밀로이드 플라크로 응집되는 아밀로이드 피브릴을 형성하지 않아 이 질병의 원인이 될 수 있는 것은 피브릴이 아니라 Aβ 올리고머화임을 시사합니다. 이 돌연변이를 발현하는 쥐는 알츠하이머병의 모든 일반적인 병리학을 가지고 있습니다.[64]
가설.
아밀로이드 베타 및 타우 단백질

타우 가설은 타우 단백질 이상이 질병 캐스케이드를 시작한다고 제안합니다.[46] 이 모델에서 과인산화된 타우는 쌍을 이루는 나선 필라멘트로서 타우의 다른 스레드와 쌍을 이루기 시작합니다. 결국, 그들은 신경 세포체 안에서 신경 섬유 엉킴을 형성합니다.[65] 이런 일이 일어나면 미세소관이 분해되어 세포의 세포골격 구조가 파괴되어 뉴런의 수송 체계가 붕괴됩니다.[66]
알츠하이머병의 병리학과 관련된 잘못 접힌 아밀로이드 베타와 타우 단백질을 연결하여 만성 염증을 유발하는 산화 스트레스를 유발하는 많은 연구가 있습니다.[67] 지속적인 염증(신경염증)은 파킨슨병, ALS를 포함한 다른 신경퇴행성 질환의 특징이기도 합니다.[68] 스피로헤타 감염은 치매와도 관련이 있습니다.[9] DNA 손상은 AD 뇌에 축적됩니다; 활성 산소 종들이 DNA 손상의 주요 원인이 될 수 있습니다.[69]
수면.
수면 장애는 알츠하이머병에서 염증의 가능한 위험 요소로 여겨집니다. 수면 문제는 알츠하이머병의 결과로 여겨져 왔지만, 연구들은 수면 문제가 대신 원인이 될 수 있다고 암시합니다. 수면 장애는 지속적인 염증과 관련이 있는 것으로 생각됩니다.[70]
금속 독성, 흡연, 신경염증 및 대기오염
이온성 구리, 철 및 아연과 같은 생체 금속의 세포 항상성은 알츠하이머병에서 방해를 받지만 이것이 단백질에 의해 생성되는지 또는 단백질의 변화를 유발하는지는 여전히 불분명합니다.[9][71] 흡연은 알츠하이머병의 중요한 위험 요소입니다.[1] 선천성 면역계의 전신 표지자는 후기 알츠하이머병의 위험인자입니다.[72] 대기 오염에 노출되는 것은 알츠하이머병 발병에 기여하는 요인이 될 수 있습니다.[9]
기타 가설
퇴행성은 태아가 신경 자극에서 시작하여 골수화로 끝나는 신경 발달 과정을 거치는 것처럼 의학적 가설입니다. 알츠하이머병을 앓고 있는 사람들의 뇌는 역신경변성 과정을 거치며, 탈수와 축삭(백질)의 죽음으로 시작하여, 회백질의 죽음으로 끝납니다.[73] 마찬가지로, 이 가설은 유아가 인지 발달 상태를 겪으면서 알츠하이머병에 걸린 사람들은 진행성 인지 장애의 역과정을 겪게 된다는 것입니다.[74]
셀리악병과의 연관성은 불분명하며, 2019년 연구에서는 CD를 가진 사람들에게서 치매의 전반적인 증가가 발견되지 않은 반면, 2018년 검토에서는 알츠하이머병을 포함한 여러 유형의 치매와 연관성이 발견되었습니다.[75][76]
한 이론에 따르면, 노화 동안 올리고덴드로세포와 그와 관련된 미엘린의 기능 장애는 축삭 손상에 기여하고, 이는 차례로 아밀로이드 생성과 타우 과인산화를 발생시킵니다.[77][78]
연구들은 특정 바이러스에 감염되는 것과 나중에 알츠하이머 병이 발병하는 것 사이의 잠재적인 연관성을 보여주었습니다.[79] 특히 6,245,282명의 환자를 대상으로 수행된 대규모 연구는 인지적으로 정상적인 65세 이상의 사람들에게서 코로나19 감염 후 알츠하이머병에 걸릴 위험이 증가하는 것을 보여주었습니다.[80]
병태생리학

신경병리학
알츠하이머병은 대뇌피질과 특정 피질하부에서 뉴런과 시냅스가 소실되는 것이 특징입니다. 이 손실은 측두엽과 두정엽의 퇴화를 포함한 영향을 받는 부위의 총체적인 위축을 초래하고 전두엽 피질과 경추의 일부를 포함합니다.[81] 퇴화는 뇌간 핵, 특히 음경의 유전자좌에도 존재합니다.[82] MRI와 PET를 사용한 연구는 가벼운 인지 장애에서 알츠하이머병으로 진행됨에 따라 알츠하이머병 환자의 특정 뇌 영역의 크기가 감소하고 건강한 노인의 유사한 이미지와 비교하여 기록되었습니다.[83][84]
Aβ 플라크와 신경섬유 엉킴은 모두 알츠하이머병을 앓고 있는 사람들의 뇌,[85] 특히 해마에서 현미경으로 뚜렷하게 보입니다.[86] 그러나 알츠하이머병은 신피질에 신경섬유 엉킴이 없이 발생할 수 있습니다.[87] 플라크는 밀도가 높고 대부분 용해되지 않는 베타 아밀로이드 펩티드와 세포 물질의 뉴런 외부와 주변에 침착됩니다. 엉킴 (신경섬유 엉킴)은 과인산화되어 세포 내부에 축적된 미세소관 관련 단백질 타우의 집합체입니다. 많은 노인들이 노화의 결과로 플라크와 엉킴이 생기지만, 알츠하이머병에 걸린 사람들의 뇌는 측두엽과 같은 특정 뇌 영역에 더 많은 수의 플라크를 가지고 있습니다.[88] 알츠하이머병을 앓고 있는 사람들의 뇌에서 루이체가 드물지 않습니다.[89]
생화학
알츠하이머병은 비정상적으로 접힌 아밀로이드 베타 단백질이 아밀로이드 플라크로, 타우 단백질이 뇌의 신경섬유 엉킴으로 축적돼 생기는 단백질 병증인 단백질 오접병으로 밝혀졌습니다.[90] 플라크는 아밀로이드 베타(Aβ)라고 불리는 길이 39~43개의 아미노산으로 이루어진 작은 펩티드로 이루어져 있습니다. 아밀로이드 베타는 더 큰 아밀로이드 베타 전구체 단백질(APP)에서 나온 조각으로, 뉴런의 막을 관통하는 막횡단 단백질입니다. APP는 뉴런 성장, 생존 및 부상 후 복구에 중요합니다.[91][92] 알츠하이머병에서 감마 세크레타제와 베타 세크레타제는 단백질 분해 과정에서 함께 작용하여 APP가 더 작은 조각으로 분해됩니다.[93] 이 조각들 중 하나는 아밀로이드 베타의 피브릴을 생성하고, 이 덩어리를 형성하여 외부 뉴런을 아밀로이드 플라크라고 하는 조밀한 형태로 침전시킵니다.[85][94]
알츠하이머병은 타우 단백질의 비정상적인 응집으로 인한 타우병증으로도 여겨집니다. 모든 뉴런은 부분적으로 미세소관이라고 불리는 구조로 구성된 내부 지지 구조인 세포골격을 가지고 있습니다. 이 미세소관은 세포의 몸에서 축삭의 끝과 뒤로 영양분과 분자를 안내하는 트랙과 같은 역할을 합니다. 타우라고 불리는 단백질은 인산화될 때 미세소관을 안정화시키므로 미세소관 관련 단백질이라고 불립니다. 알츠하이머병에서 타우는 화학적 변화를 겪으면서 과인산화되고, 그 후 다른 실과 짝을 이루어 신경섬유 엉킴을 일으키고 뉴런의 수송 체계를 붕괴시킵니다.[95] 병원성 타우는 전위 요소 조절 장애를 통해 신경세포 사멸을 일으킬 수도 있습니다.[96] 네크롭토시스는 타우 엉킴에 영향을 받은 뇌세포의 세포 사멸 메커니즘으로도 보고되었습니다.[97][98]
질병기전
베타 아밀로이드 펩타이드의 생성과 응집의 장애가 알츠하이머병의 병리학적 원인이 되는 정확한 방법은 알려져 있지 않습니다.[99][100] 아밀로이드 가설은 전통적으로 베타 아밀로이드 펩타이드의 축적을 뉴런 퇴화를 유발하는 중심 사건으로 지적합니다. 세포의 칼슘 이온 항상성을 방해하는 단백질의 독성 형태로 추정되는 응집된 아밀로이드 섬유의 축적은 프로그램된 세포 사멸(apoptosis)을 유도합니다.[101] 또한β A는 알츠하이머에 걸린 뇌의 세포에서 미토콘드리아에 선택적으로 축적되며, 특정 효소 기능과 뉴런에 의한 포도당 활용을 억제하는 것으로 알려져 있습니다.[102]
철 항상성은 질병 진행과 관련이 있으며 철 의존적인 형태의 ferroptosis라고 불리는 조절된 세포 사멸이 관련될 수 있습니다. 지질 과산화 생성물은 대조군에 비해 AD 뇌에서도 상승합니다.[103]
다양한 염증 과정과 사이토카인도 알츠하이머병의 병리학적 원인이 될 수 있습니다. 염증은 모든 질병에서 조직 손상의 일반적인 표지자이며, 알츠하이머병에서 조직 손상의 이차적인 것이거나 면역학적 반응의 표지자일 수 있습니다.[104] 뉴런과 뇌의 면역학적 메커니즘 사이에 강한 상호작용의 증거가 증가하고 있습니다. 비만과 전신 염증은 질병 진행을 촉진하는 면역학적 과정을 방해할 수 있습니다.[105]
알츠하이머병에서 다양한 신경영양인자의 분포와 뇌 유래 신경영양인자(BDNF)와 같은 수용체 발현의 변화가 설명되었습니다.[106][107]
진단.

알츠하이머병(AD)은 부검 소견으로만 확실하게 진단할 수 있습니다; 부검이 없는 경우, AD의 임상 진단은 다른 소견에 기초하여 "가능"하거나 "가능"합니다.[108][109][110] 임상적으로 AD로 진단된 사람의 최대 23%가 오진될 수 있으며 AD와 유사한 증상이 있는 다른 상태를 암시하는 병리학을 가질 수 있습니다.[109]
AD는 일반적으로 환자의 병력, 친척의 병력 및 행동 관찰을 기반으로 임상적으로 진단됩니다. 특징적인 신경 및 신경 심리학적 특징의 존재와 대체 조건의 부재가 진단을 뒷받침합니다.[needs update][111][112] 컴퓨터 단층 촬영(CT) 또는 자기 공명 영상(MRI)을 사용하고 단일 광자 방출 컴퓨터 단층 촬영(SPEC) 또는 양전자 방출 단층 촬영(PET)을 사용하는 첨단 의료 영상을 사용하여 다른 뇌병리학이나 치매의 하위 유형을 배제할 수 있습니다.[113] 더욱이, 그것은 전구 단계(경미한 인지 장애)에서 알츠하이머 병으로의 전환을 예측할 수 있습니다.[114] 알츠하이머병 PET에 사용되는 FDA 승인 방사선 의약품 진단제는 플로르베타피르(2012), 플루트메타몰(2013), 플로르베타벤(2014) 및 플로르토키피르(2020)입니다.[115] 미국의 많은 보험사들이 이 절차를 보장하지 않기 때문에 2018년[update] 현재 임상에서 사용하는 것은 대부분 임상시험으로 제한됩니다.[116]
기억력 검사를 포함한 지적 기능에 대한 평가는 질병의 상태를 더욱 특성화할 수 있습니다.[1] 의료 기관은 개업의의 진단 프로세스를 용이하게 하고 표준화하기 위해 진단 기준을 만들었습니다. 최종 진단은 뇌 물질이 이용 가능할 때에만 사후 평가로 확인할 수 있고 노인성 플라크와 신경섬유 엉킴에 대해 조직학적으로 검사할 수 있습니다.[116][117]
기준
알츠하이머병 스펙트럼의 임상 진단을 위한 세 가지 기준이 있습니다: 정신 장애 진단 및 통계 매뉴얼 (DSM-5) 2013년 5판, 2011년 개정된 미국 국립 노인-알츠하이머 협회 (NIA-AA) 정의, 그리고 에서 개정된 국제 작업 그룹 기준. 2010.[31][116] 수십 년에 걸쳐 진행될 수 있는 세 가지 광범위한 기간은 알츠하이머병이 전임상 단계에서 경도 인지 장애(MCI)로 진행되고 알츠하이머병 치매가 뒤따르는 것을 정의합니다.[118]
DSM(DSM-IV-TR)의 네 번째 텍스트 개정판에 나열된 바와 같이 기억, 언어, 지각 능력, 주의력, 운동 능력, 방향성, 문제 해결 및 실행 기능 능력 등 8개의 지적 영역이 AD에서 가장 일반적으로 손상됩니다.[119]
DSM-5는 주요 신경 인지 장애와 경증 신경 인지 장애 모두에 대한 알츠하이머 가능성 또는 가능성에 대한 기준을 정의합니다.[120][121][110] AD의 가능성 또는 가능성 진단을 위해서는 하나 이상의 인지적 결함과 함께 주요 또는 경미한 신경 인지 장애가 있어야 합니다.[120][122] 알츠하이머병으로 인한 주요 신경인지장애의 경우 알츠하이머의 유전적[123] 증거가 있거나 후천적으로 2개 이상의 인지결손과 다른 질환이 아닌 기능장애가 있는 경우 알츠하이머병 가능성을 진단할 수 있습니다.[124] 그렇지 않으면 진단이 비정형적인 경로를 따라 진행되기 때문에 알츠하이머 가능성을 진단할 수 있습니다.[125] 알츠하이머로 인한 가벼운 신경인지장애의 경우 유전적 증거가 있을 경우 알츠하이머병을 진단할 수 있는 반면, 알츠하이머병은 유전적 증거가 없을 경우, 학습과 기억력 모두의 저하, 2개 이상의 인지결손, 또 다른 장애가 아닌 기능적 장애입니다.[120][126]
NIA-AA 기준은 임상 평가보다는 연구에서 주로 사용됩니다.[127] 그들은 알츠하이머병을 전임상, 경도 인지 장애(MCI), 알츠하이머 치매의 세 가지 주요 단계로 정의합니다.[128][129] 전임상 단계의 진단은 복잡하고 증상이 없는 개인에게 초점이 맞추어져 있으며,[129][130] 후자의 두 단계는 증상을 경험하는 개인을 설명합니다.[129] MCI의 핵심 임상 기준은 주로 신경 손상(주로 타우 관련) 및 아밀로이드 베타 침착에 대한 [131]바이오마커의 식별과 함께 사용됩니다.[127][129] 핵심 임상 기준 자체는 동반 질환이 없는 인지 장애의[129] 존재에 달려 있습니다.[132][133] 세 번째 단계는 알츠하이머성 치매의 가능성과 가능성으로 구분됩니다.[133] 알츠하이머성 치매일 가능성이 있는 치매에는 시간이 지남에 따라 인지 기능의 지속적인 손상과 기억 관련 또는 비기억 관련 인지 기능 장애가 있습니다.[133] 알츠하이머성 치매 가능성에는 뇌혈관 질환과 같은 또 다른 원인 질환이 존재합니다.[133]
기술

미니-멘탈 상태 검사(MMSE), 몬트리올 인지 평가(MoCA) 및 미니-코그(Mini-Cog)와 같은 인지 검사를 포함한 신경 심리 검사는 AD의 인지 장애 진단을 돕기 위해 널리 사용됩니다.[134] 이러한 테스트는 가벼운 인지 장애에 대한 민감성이 부족하고 언어나 주의력 문제에 따라 편향될 수 있으므로 항상 정확하지는 않을 수 있습니다.[134] 특히 질병의 초기 단계에서 결과의 높은 신뢰성을 위해서는 보다 포괄적인 테스트 배열이 필요합니다.[135][136]
알츠하이머 및 기타 질병의 감별 진단에는 추가적인 신경학적 검사가 중요합니다.[25] 가족과의 인터뷰는 평가에 사용됩니다. 간병인은 일상 생활 능력과 개인의 정신 기능 저하에 대한 중요한 정보를 제공할 수 있습니다.[137] 알츠하이머병을 앓고 있는 사람은 일반적으로 자신의 결손을 인식하지 못하기 때문에 간병인의 관점이 특히 중요합니다.[138] 가족들이 치매 초기 증상을 발견하는 데 어려움을 겪고 의사에게 정확한 정보를 전달하지 못하는 경우가 많습니다.[139]
보충 테스트는 잠재적으로 치료 가능한 다른 진단을 배제하고 오진을 방지하는 데 도움이 될 수 있습니다.[140] 일반적인 보충 검사에는 혈액 검사, 갑상선 기능 검사뿐만 아니라 비타민 B12 수치를 평가하고 신경 매독을 배제하고 대사 문제(신장 기능, 전해질 수치 및 당뇨병 검사 포함)를 배제하기 위한 검사가 포함됩니다.[140] MRI 또는 CT 스캔을 사용하여 종양이나 뇌졸중을 포함한 다른 잠재적인 증상을 배제할 수도 있습니다.[134] 섬망과 우울증은 개인들 사이에서 흔히 발생할 수 있으며 배제해야 할 중요한 사항입니다.[141]
우울증은 알츠하이머병(알츠하이머병 우울증 참조), 인지 장애의 초기 징후 [142]또는 심지어 원인과 동시에 발생할 수 있기 때문에 우울증에 대한 심리 검사가 사용됩니다.[143][144]
정확도가 낮기 때문에 C-PIB-PET 스캔은 사람들이 가벼운 인지 장애(MCI)의 징후를 보일 때 조기 진단 도구나 알츠하이머 병의 발병을 예측하기 위해 권장되지 않습니다.[145] F-FDG PET 스캔을 단일 테스트로 사용하여 알츠하이머병에 걸릴 수 있는 사람을 식별하는 것은 증거에 의해 뒷받침되지 않습니다.[146]
예방

알츠하이머병을 치료할 수 있는 질병 수정 치료제는 없으며 이 때문에 AD 연구는 발병과 진행을 예방하기 위한 개입에 초점을 맞추고 있습니다.[147] 알츠하이머를 예방하는 데 있어 특별한 방법을 뒷받침하는 증거는 없으며,[1] 발병이나 진행을 예방하는 방법에 대한 연구는 일관되지 않은 결과를 도출했습니다. 역학 연구는 개인의 AD 발병 가능성과 약물, 생활 습관 및 식단과 같은 수정 가능한 요인 사이의 관계를 제안했습니다. 알츠하이머병에 대한 개입이 1차 예방법으로 작용하는지, 질병 자체를 예방하는지, 아니면 질병의 초기 단계를 파악하는 2차 예방법으로 작용하는지를 판단하는 데는 몇 가지 어려움이 있습니다.[148] 이러한 과제에는 개입 기간, 개입이 시작되는 질병의 다양한 단계, 알츠하이머병에 특정한 바이오마커에 관한 포함 기준의 표준화 부족 등이 포함됩니다.[148] 알츠하이머병을 예방하는 데 도움이 될 수 있는 요인을 결정하기 위해서는 추가적인 연구가 필요합니다.[148]
약
고콜레스테롤혈증, 고혈압, 당뇨병, 흡연과 같은 심혈관 위험 인자는 AD의 발병 위험이 높고 경과가 악화되는 것과 관련이 있습니다.[149][150] 콜레스테롤을 낮추기 위해 스타틴을 사용하는 것은 알츠하이머병에 도움이 될 수 있습니다.[151] 명백한 인지 장애가 없는 사람들에게 항고혈압제와 당뇨병 치료제는 뇌혈관 병리학에 영향을 주어 치매 위험을 감소시킬 수 있습니다.[1][152] 알츠하이머병과의 관계를 구체적으로 조사하기 위해서는 더 많은 연구가 필요합니다. 다른 동시적인 생활 습관 변화(식이, 운동, 흡연)에 대한 약물의 직접적인 역할에 대한 명확한 설명이 필요합니다.[1]
우울증은 알츠하이머병의 위험 증가와 관련이 있습니다; 항우울제를 사용한 관리는 예방책을 제공할 수 있습니다.[153]
역사적으로 비스테로이드성 항염증제(NSAIDs)의 장기간 사용은 염증을 감소시키기 때문에 알츠하이머병의 발병 가능성을 감소시키는 것과 관련이 있는 것으로 여겨졌지만, NSAIDs는 치료제로서 유용하지 않은 것으로 보입니다.[116] 또한 여성이 남성보다 알츠하이머병 발병률이 높기 때문에 폐경기 에스트로겐 결핍이 위험요인으로 생각된 적도 있습니다. 하지만 폐경기 호르몬 대체요법(HRT)이 인지기능 저하 위험을 감소시킨다는 증거는 부족합니다.[154]
식물로 만든 메탈로샤페론은 알츠하이머병 치료를 위한 새로운 접근법이 될 수 있습니다.[155]
라이프스타일
신체 및 인지 운동, 고등 교육 및 직업 성취도, 흡연, 스트레스, 수면 및 당뇨병 및 고혈압을 포함한 다른 동반 질환의 관리와 같은 특정 생활 방식 활동은 알츠하이머 발병 위험에 영향을 미칠 수 있습니다.[153]
신체 운동은 치매 발병률 감소와 관련이 있으며,[156] AD 환자의 증상 중증도 감소에 효과적입니다.[157] 주 3회 40분씩 활발한 걷기를 포함한 유산소 운동으로 기억력과 인지 기능을 향상시킬 수 있습니다.[158] 그것은 또한 뇌의 신경 가소성을 유발할 수 있습니다.[159] 독서, 십자말풀이, 체스와 같은 정신 운동에 참여하는 것은 예방 가능성을 보여주었습니다.[153] 신체 활동에 대한 WHO의 권고를 충족하는 것은 AD의 위험을 낮추는 것과 관련이 있습니다.[160]
더 높은 교육과 직업 성취, 그리고 여가 활동에 참여하는 것은 알츠하이머 발병의 위험을 [161]줄이거나 증상의 시작을 지연시키는 데 기여합니다. 이것은 인지적 예비 이론과 양립할 수 있는데, 이 이론은 일부 삶의 경험이 개인에게 치매 증상의 시작을 지연시키는 인지적 예비를 제공하는 더 효율적인 신경 기능을 제공한다는 것입니다.[161] 교육은 알츠하이머병 증후군의 발병을 질병의 지속 기간을 변경하지 않고 지연시킵니다.[162]
금연은 특히 APOE ɛ4 대립유전자를 가지고 있는 사람들의 알츠하이머병 발병 위험을 줄일 수 있습니다. 흡연으로 인한 증가된 산화 스트레스는 하류의 염증성 또는 신경퇴행성 과정을 초래하여 AD 발생 위험을 증가시킬 수 있습니다.[164] 금연을 위한 금연, 상담 및 약리치료 등을 이용하며 환경성 담배연기를 피하는 것이 좋습니다.[153]
알츠하이머병은 수면장애와 관련이 있지만 정확한 연관성은 불분명합니다.[165][166] 사람들이 나이가 들수록 수면장애와 AD가 독립적으로 발생할 위험이 높아진다고 한때 생각했지만, 수면장애가 AD의 유병률을 높일 수 있는지에 대해서는 연구가 진행되고 있습니다.[165] 한 가지 이론은 Aβ를 포함한 독성 물질의 제거를 증가시키는 메커니즘이 수면 중에 활성화된다는 것입니다.[165][167] 수면이 감소하면서 사람은 Aβ 생산을 증가시키고 Aβ 간극을 감소시켜 Aβ 축적을 초래하고 있습니다.[168][165][166] 매일 밤 충분한 수면(약 7-8시간)을 취하는 것은 AD의 발병을 예방하는 잠재적인 생활습관 중재가 되었습니다.[153]
스트레스는 알츠하이머 발병의 위험 요소입니다.[153] 스트레스가 알츠하이머 발병의 원인이 되는 메커니즘은 불분명하지만, 평생의 스트레스 요인이 사람의 후성유전체에 영향을 미쳐 특정 유전자의 과발현 또는 과소발현을 초래할 수 있다고 제안됩니다.[169] 스트레스와 알츠하이머의 관계는 불분명하지만, 스트레스를 줄이고 마음을 편안하게 하는 전략은 진행이나 알츠하이머병을 예방하는 데 도움이 되는 전략이 될 수 있습니다.[170] 예를 들어, 명상은 인지와 웰빙을 지원하기 위한 유용한 생활 방식 변화이지만, 장기적인 효과를 평가하기 위해서는 추가적인 연구가 필요합니다.[159]
관리
알츠하이머병에 대한 치료법은 없습니다.[171] 사용 가능한 치료법은 비교적 증상이 적은 이점을 제공하지만 자연적으로 완화된 상태를 유지합니다.[9][172] 치료는 제약, 심리사회, 돌봄으로 나눌 수 있습니다.
제약


알츠하이머병의 인지 증상을 치료하기 위해 사용되는 약물은 4가지 아세틸콜린에스테라제 억제제(타크린, 리바스티그민, 갈란타민, 도네페질)와 NMDA 수용체 길항제인 메만틴입니다. 아세틸콜린에스테라제 억제제는 경증에서 중증의 알츠하이머 환자를 대상으로 하는 반면, 메만틴은 중등도 또는 중증의 알츠하이머 환자를 대상으로 합니다.[116] 그들의 사용으로 인한 이점은 적습니다.[173][174][175][10]
콜린신경세포의 활동이 감소하는 것은 알츠하이머병의 잘 알려진 특징입니다.[176] 아세틸콜린에스테라아제 억제제를 사용하여 아세틸콜린(ACH)의 분해 속도를 감소시켜 뇌의 ACh 농도를 증가시키고 콜린신경세포의 사멸로 인한 ACh의 손실을 방지합니다.[177] 경증에서 중등도의 알츠하이머병에서 이러한 약물의 효능에 대한 증거와 [178][173]진행 단계에서의 사용에 대한 일부 증거가 있습니다.[173] 경도 인지 장애에서 이러한 약물의 사용은 알츠하이머병의 발병 지연에 어떠한 효과도 보여주지 않았습니다.[179] 가장 흔한 부작용은 메스꺼움과 구토이며, 둘 다 콜린 과잉과 관련이 있습니다. 이러한 부작용은 사용자의 약 10-20%에서 발생하며, 중증도가 경미하거나 중등도이며, 약물 용량을 천천히 조정하여 관리할 수 있습니다.[180] 덜 일반적인 2차 효과로는 근육 경련, 심박수 감소(대맥), 식욕과 체중 감소, 위산 생성 증가 등이 있습니다.[178]
글루타메이트는 신경계의 흥분성 신경전달물질이지만, 뇌의 과도한 양은 글루타메이트 수용체의 과도한 자극으로 구성된 흥분성 독성이라는 과정을 통해 세포 사멸로 이어질 수 있습니다. 흥분독성은 알츠하이머병뿐만 아니라 파킨슨병, 다발성 경화증 등 다른 신경계 질환에서도 발생합니다.[181] Memantine은 비경쟁적인 NMDA 수용체 길항제로 처음 항인플루엔자제로 사용됩니다. 그것은 NMDA 수용체를 차단하고 글루타메이트에 의한 과자극을 억제함으로써 글루타머틱 시스템에 작용합니다.[181][182] 메만틴은 중등도에서 중증의 알츠하이머병 치료에 작은 이점이 있는 것으로 나타났습니다.[183] 메만틴과 함께 보고된 부작용은 환각, 혼란, 어지러움, 두통 및 피로를 포함하여 드물게 발생하고 경미합니다.[184][185] 메만틴과 도네페질의[186] 조합은 "통계적으로 유의하지만 임상적으로 한계가 있는 효과"인 것으로 나타났습니다.[187]
EGB 761로 알려진 은행나무 추출물은 알츠하이머 및 기타 신경 정신 질환 치료에 사용되었습니다.[188] 그것의 사용은 유럽 전역에서 승인되었습니다.[189] 세계생물정신의학연맹 지침에는 아세틸콜린에스테라제 억제제와 메만틴에 동일한 무게의 증거(레벨 B)가 부여된 EGB 761이 나열되어 있습니다. 알츠하이머병과 혈관성 치매 모두에서 증상이 개선된 것은 EGB 761이 유일합니다. EGB 761은 단독으로 또는 다른 치료법이 효과가 없는 것으로 판명될 경우 추가적인 역할을 할 수 있습니다.[188] 2016년의 한 리뷰는 은행나무에 대한 임상 실험의 증거의 질이 알츠하이머병 치료에 사용될 것을 보증하기에 충분하지 않다고 결론지었습니다.[190]
비정형 항정신병 약물은 알츠하이머병 환자의 공격성과 정신병을 줄이는 데는 약간 유용하지만 뇌졸중, 운동 장애 또는 인지 기능 저하와 같은 심각한 부작용으로 인해 장점이 상쇄됩니다.[191] 장기적으로 사용할 경우 사망률 증가와 관련이 있는 것으로 나타났습니다.[192] 이 그룹의 사람들에게 항정신병 약물 사용을 중단하는 것은 안전한 것으로 보입니다.[193]
심리사회적
심리사회적 개입은 약물 치료의 부가물로 사용되며 행동, 감정, 인지 또는 자극 중심 접근법으로 분류할 수 있습니다.[needs update][194]
행동적 개입은 문제행동의 선행과 결과를 파악하고 감소시키기 위해 시도됩니다. 이 접근법은 전반적인 기능 개선에는 성공하지 [195]못했지만, 요실금과 같은 일부 특정 문제 행동을 줄이는 데 도움이 될 수 있습니다.[196] 방황과 같은 다른 행동 문제에서 이러한 기술의 효과에 대한 고품질 데이터가 부족합니다.[197][198] 음악 치료는 행동적, 심리적 증상을 줄이는 데 효과적입니다.[199]
감정 지향적 개입으로는 회상 요법, 타당화 요법, 지지 심리 요법, 감각 통합, 일명 스누젤렌, 모의 존재 요법 등이 있습니다. 코크란 리뷰에서는 이것이 효과적이라는 증거를 찾지 못했습니다.[200] 회상요법(RT)은 사진, 생활용품, 음악 및 음향 녹음 또는 기타 과거의 친숙한 물품의 도움으로 과거의 경험을 개인 또는 그룹으로 여러 번 논의하는 것을 포함합니다. RT의 효과에 대한 2018년 검토는 효과가 일관성이 없고 크기가 작으며 임상적 중요성이 의심스러우며 설정에 따라 다양하다는 것을 발견했습니다.[201] 모의 존재 요법(SPT)은 애착 이론에 기반을 두고 있으며 알츠하이머 병에 걸린 사람의 가장 가까운 친척의 목소리로 녹음을 재생하는 것을 포함합니다. SPT가 도전적인 행동을 줄일 수 있다는 부분적인 증거가 있습니다.[202]
현실 지향과 인지 재훈련을 포함하는 인지 지향 치료의 목적은 인지 결손의 감소입니다. 현실 지향성은 주변 환경과 그 안에 있는 사람의 위치에 대한 이해를 쉽게 하기 위해 시간, 장소 또는 사람에 대한 정보를 제시하는 것으로 구성됩니다. 반면, 인지 재훈련은 정신적 능력을 발휘하여 손상된 역량을 향상시키려 합니다. 둘 다 인지 능력을 향상시키는 효능을 보여주었습니다.[203]
자극 지향적인 치료에는 예술, 음악 및 애완 동물 치료, 운동 및 기타 모든 종류의 레크리에이션 활동이 포함됩니다. 자극은 행동, 기분, 그리고 더 적은 정도로 기능을 향상시키는 데 약간의 지원을 합니다. 그럼에도 불구하고, 이러한 효과들이 중요한 만큼, 자극 요법의 사용에 대한 주요 지지는 그 사람의 루틴의 변화입니다.[194]
케어기빙
알츠하이머는 치료법이 없고 점차 사람들이 그들의 필요를 돌볼 수 없게 만들기 때문에, 돌보는 것은 본질적으로 치료이며 질병이 진행되는 동안 신중하게 관리되어야 합니다.
초기와 중간 단계에서 생활 환경과 생활 방식의 변화는 안전성을 높이고 관리자 부담을 줄일 수 있습니다.[204][205] 그러한 변경의 예로는 단순화된 루틴 준수, 안전 잠금 장치 배치, 질병에 걸린 사람에게 신호를 보내기 위한 가정 용품의 라벨 표시 또는 수정된 일상 생활 용품의 사용 등이 있습니다.[194][206][207] 만약 먹는 것이 문제가 된다면, 음식은 더 작은 조각으로 준비되거나 심지어 퓨레로 준비되어야 할 것입니다.[208] 삼킴 곤란이 발생했을 때는 수유관의 사용이 필요할 수 있습니다. 이러한 경우 지속적인 수유의 의학적 효능과 윤리는 보호자와 가족 구성원의 중요한 고려 사항입니다.[209][210] 알츠하이머병을 앓고 있는 사람이나 보호자에게 해를 끼치는 것을 예방하기 위해 필요한 상황이 있기는 하지만, 신체적 제약의 사용은 질병의 어떤 단계에서도 거의 나타나지 않습니다.[194]
질병의 마지막 단계에서 치료는 종종 호스피스의 도움으로 사망할 때까지의 불편함을 완화하는 데 중점을 둡니다.[211]
다이어트
식단은 알츠하이머병 발병의 수정 가능한 위험 요소일 수 있습니다. 지중해식 식단과 DASH식 식단은 모두 인지 능력 저하와 관련이 있습니다. 다른 접근법은 이 두 가지 식단의 요소를 MIND 식단으로 알려진 것에 통합하는 것이었습니다.[212] 개별 식이 성분, 미네랄 및 보충제에 대한 연구는 AD 또는 인지 기능 저하를 예방하는지에 대해 상충됩니다.[212]
예후
알츠하이머병의 초기 단계는 진단이 어렵습니다. 일반적으로 인지 장애가 일상 생활 활동에 손상을 입히면 최종 진단이 내려지지만, 그 사람은 여전히 독립적으로 살고 있을 수 있습니다. 증상은 인지 및 비인지 장애의 증가 단계를 통해 기억 상실과 같은 가벼운 인지 문제에서 진행되어 특히 질병의 후기 단계에서 독립적인 생활의 가능성을 제거합니다.[32]
알츠하이머병에 걸린 사람들의 기대수명이 줄어듭니다.[213] 60세에서 70세의 평균 수명은 23세에서 15세이고, 90세의 경우 4.5세입니다.[214] 알츠하이머병 진단 후 60대와 70대 초반은 7년에서 10년(13년에서 8년), 90대는 3년 이하(1.5년)에 불과합니다.[213]
진단 후 14년 이상 사는 사람은 3% 미만입니다.[215] 생존율 감소와 상당히 관련된 질병 특징은 인지 장애의 중증도 증가, 기능 수준 감소, 낙상 이력 및 신경학적 검사의 장애입니다. 심장병, 당뇨병 또는 알코올 남용의 병력과 같은 다른 우연한 질병도 생존 기간 단축과 관련이 있습니다.[216][217][218] 시작 연령이 빠를수록 총 생존연수가 증가하지만, 젊은 사람들 사이의 건강한 인구에 비해 기대수명은 특히 줄어듭니다.[219] 남성은 여성에 비해 생존 예후가 좋지 않습니다.[needs update][215][3]
폐렴과 탈수는 알츠하이머병이 가져오는 가장 빈번한 즉각적인 사망원인인 반면, 암은 일반인에 비해 사망원인이 덜합니다.[needs update][3]
역학
역학 연구에서는 발병률과 유병률이라는 두 가지 주요 척도가 사용됩니다. 발병률은 위험에 처한 사람-시간 단위당 신규 환자 수(일반적으로 1,000명-년당 신규 환자 수)이며, 유병률은 특정 시간에 모집단에서 발생한 질병의 총 환자 수이다.
발병률과 관련하여 코호트 종단 연구(수년에 걸쳐 질병이 없는 인구를 추적하는 연구)는 모든 치매에 대해 1000명당 10~15명, 알츠하이머병에 대해 5~8명 사이의 비율을 제공하며, [220][221]이는 매년 새로운 치매 환자의 절반이 알츠하이머병이라는 것을 의미합니다. 고령화는 질병의 주요 위험 요소이며 발병률은 모든 연령에서 동일하지 않습니다. 65세 이후 5년마다 질병에 걸릴 위험이 약 두 배로 증가하여 1,000명당 3명에서 많게는 69명까지 증가합니다.[220][221] 여성 알츠하이머병 환자는 남성보다 더 흔하지만, 이러한 차이는 여성의 수명이 길기 때문일 가능성이 높습니다. 나이에 맞게 조정하면 남녀 모두 동일한 비율로 알츠하이머의 영향을 받습니다.[10] 미국에서는 2010년 알츠하이머병으로 사망할 위험이 비히스패닉계 흑인 인구보다 비히스패닉계 백인 인구에서 26% 높았고, 히스패닉계 인구는 비히스패닉계 백인 인구보다 30% 낮았습니다.[222] 하지만, 많은 알츠하이머 연구는 아프리카계 미국인, 동아시아인, 히스패닉계/라틴계 인구와 같은 소수 집단에서 행해져야 합니다.[223][224] 연구에 따르면 이 그룹들은 임상시험에서 잘 나타나지 않으며 백인 그룹에 비해 특정 유전적 위험인자(즉 APOE4)를 가지고 있을 때 알츠하이머 발병 위험이 동일하지 않습니다.[224][225][226]
인구에서 알츠하이머병의 유병률은 발병률과 생존율을 포함한 요인에 따라 다릅니다. 알츠하이머병의 발병률은 나이가 들수록 증가하기 때문에 유병률은 유병률이 주어진 인구의 평균 연령에 따라 달라집니다. 2020년 미국에서 알츠하이머 치매 유병률은 60-74세 그룹에서 5.3%로 추정되었으며, 74-84세 그룹에서는 13.8%, 85세 이상에서는 34.6%로 증가했습니다.[227] 전 세계적으로 일부 덜 개발된 지역의 유병률은 더 낮습니다.[228][229] 발병률과 유병률이 꾸준히 증가하고 있어 2050년에는 유병률 자체가 3배로 증가할 것으로 전망됩니다.[clarification needed][230] 2020년 현재 전 세계적으로 5천만 명의 사람들이 AD를 가지고 있으며, 이 숫자는 2050년까지 1억 5천 2백만 명으로 증가할 것으로 예상됩니다.[9]
역사

고대 그리스와 로마의 철학자와 의사들은 노령과 증가하는 치매를 연관시켰습니다.[23] 1901년이 되어서야 독일의 정신과 의사 알로이스 알츠하이머(Alois Alzheimer)는 오귀스트 D(Auguste D)라고 불리는 50세 여성에게서 자신의 이름을 딴 알츠하이머병으로 알려진 첫 번째 사례를 확인했습니다. 그는 그녀가 1906년에 사망할 때까지 그녀의 사건을 추적했고, 그는 그것에 대해 처음으로 공개적으로 보고했습니다.[231] 이후 5년 동안 의학 문헌에 11건의 유사한 사례가 보고되었으며, 그 중 일부는 이미 알츠하이머병이라는 용어를 사용하고 있습니다.[23] 이 질병은 에밀 크라펠린에 의해 Auguste D의 원래 보고서에 포함된 임상적(망상 및 환각) 및 병리학적 특징(동맥경화성 변화)의 일부를 억제한 후 특징적인 질병으로 처음 기술되었습니다.[232] 그는 1910년 7월 15일 발간된 그의 정신의학 교과서 제8판에서 Kraepelin에 의해 노인성 치매로 명명된 알츠하이머병을 노인성 치매의 하위 유형으로 포함시켰습니다.[233]
20세기 대부분의 기간 동안 알츠하이머병 진단은 치매 증상이 나타난 45세에서 65세 사이의 사람들을 위해 예약되었습니다. 1977년 알츠하이머병 학회에서 노인성 치매와 노인성 치매의 임상적, 병리학적 징후가 거의 동일하다는 결론이 나오면서 용어가 바뀌었지만, 저자들은 이것이 이들이 다른 원인을 가졌을 가능성을 배제하지는 못했다고 덧붙였습니다.[234] 이는 결국 나이와 무관하게 알츠하이머병 진단으로 이어졌습니다.[235] 알츠하이머 유형의 노인성 치매(SDAT)라는 용어는 65세 이상의 사람들의 상태를 설명하기 위해 한동안 사용되었으며 고전적인 알츠하이머병은 젊은 사람들을 설명하기 위해 사용되었습니다. 결국 알츠하이머병이라는 용어는 특징적인 공통 증상 패턴, 질병 경과 및 신경병리학을 가진 모든 연령대의 사람들을 설명하기 위해 의학 명명법에 공식적으로 채택되었습니다.[236]
National Institute of Neurological and Communication Disorders and Stroke (NINCDS)와 Alzheimer's Disease and Related Disorders Association (ADRDA, 현재 Alzheimer's Association으로 알려져 있음)는 1984년에 가장 일반적으로 사용되는 NINCDS-ADRDA Alzheimer's Criteria를 진단 기준으로 [237]제정하고 2007년에 광범위하게 업데이트했습니다.[238][140] 이러한 기준은 알츠하이머병의 가능성 또는 가능성이 있는 임상적 진단을 위해 신경심리학적 검사를 통해 인지 장애의 존재 및 치매 증후군 의심 여부를 확인할 것을 요구합니다. 최종 진단을 위해서는 뇌 조직의 현미경 검사를 포함한 조직병리학적 확진이 필요합니다. 진단 기준과 최종 조직병리학적 확진 사이에 좋은 통계적 신뢰성과 타당성이 나타났습니다.[239]
사회와 문화
사회적 비용
치매, 특히 알츠하이머병은 전 세계 사회에서 가장 비용이 많이 드는 질병 중 하나일 수 있습니다.[240] 인구가 고령화됨에 따라 이러한 비용은 아마도 증가하고 중요한 사회 문제 및 경제적 부담이 될 것입니다.[241] AD와 관련된 비용에는 직접 및 간접 의료 비용이 포함되며, 이 비용은 AD를 가진 사람에 대한 사회적 관리에 따라 국가 간에 다릅니다.[240][242][243] 직접 비용은 의사 방문, 병원 진료, 진료, 요양원 진료, 전문 장비, 생활비 등입니다.[240][241] 간접 비용에는 비공식 돌봄 비용과 비공식 돌봄자의 생산성 손실이 포함됩니다.[241]
2019년[update] 현재 미국에서 비공식적인 (가족) 돌봄은 연간 2,340억 달러의 비용과 약 185억 시간의 돌봄으로 AD를 가진 사람들의 돌봄의 거의 4분의 3을 구성하는 것으로 추정됩니다.[240] AD 환자를 돌보는 전 세계 사회의 비용은 거의 10배 증가하고 2050년에는 약 9조 1천억 달러에 이를 것으로 예상됩니다.[242]
치매나 행동 장애가 더 심한 사람들의 비용은 더 높고 신체적 돌봄을 제공하기 위한 추가 돌봄 시간과 관련이 있습니다.[243]
간병부담
이 섹션을 업데이트해야 합니다.한 이벤트나 하여 이 할 수 바랍니다. (2022년 2월) |
알츠하이머를 앓고 있는 사람들은 평생 동안 도움을 받아야 하며, 돌봄은 배우자나 가까운 친척이 맡는 역할인 상근 돌봄자의 형태로 이루어질 가능성이 높습니다. 돌봄은 신체적, 정서적 부담뿐만 아니라 때때로 원조를 관리하는 사람에게 시간적, 재정적 부담을 포함하는 경향이 있습니다.[244][245] 알츠하이머병은 사회적, 심리적, 신체적 또는 경제적 측면을 포함하는 간병인에게 큰 부담을 주는 것으로 알려져 있습니다.[18][246][247] 가정 의료는 일반적으로 알츠하이머병을 앓고 있는 사람들과 그들의 가족 모두에게 선호됩니다.[248] 또한 이 옵션을 사용하면 보다 전문적이고 비용이 많이 드는 수준의 관리가 필요하지 않습니다.[248][249] 그럼에도 요양원 입소자의 3분의 2는 치매를 앓고 있습니다.[194]
치매 간병인은 신체적, 정신적 장애 비율이 높습니다.[250] 주돌봄자의 더 큰 심리사회적 문제와 관련된 요인에는 가정에 영향을 받는 사람이 있는 경우, 돌봄자가 배우자인 경우, 우울증, 행동 장애, 환각, 수면 문제 또는 보행 장애 및 사회적 고립과 같은 돌봄자의 까다로운 행동이 포함됩니다.[251][252] 경제적인 문제와 관련하여, 가족 간병인들은 알츠하이머 병을 앓고 있는 사람과 주당 평균 47시간을 보내기 위해 퇴근 시간을 포기하는 경우가 많은 반면, 그들을 돌보는 비용은 높습니다. 연구에 따라 미국에서 알츠하이머 환자를 돌보는 데 드는 직간접적인 비용은 연평균 18,000달러에서 77,500달러 사이입니다.[253][245]
인지 행동 치료와 대처 전략의 교육은 개별적으로 또는 그룹으로 보호자의 심리적 건강을 향상시키는 데 효과가 있음을 입증했습니다.[18][254]
미디어
알츠하이머병은 존 베이리의 아내 아이리스 머독의 회고록을 바탕으로 한 아이리스(2001),[255] 니콜라스 스팍스의 1996년 동명 소설을 바탕으로 한 노트북(2004),[256] 기억할 순간(2004), Thanmathra (2005);[257] 오기와라 히로시의 동명 소설을 원작으로 한 내일의 추억 (아시타 노 키오쿠) (2006)[258] Alice Munro의 단편 소설 The Bear Come Over the Mountain;[259] Still Alice (2014)를 기반으로 한 Alice (2006)는 조기 알츠하이머 병에 걸린 컬럼비아 대학 교수에 대한 이야기로 Lisa Genova의 2007년 동명 소설을 기반으로 하고 Julianne Moore가 타이틀 롤로 등장합니다. 알츠하이머 병에 관한 다큐멘터리로는 말콤과 바바라: 러브 스토리(1999), 말콤과 바바라: 러브 굿바이(2007)가 있으며, 둘 다 말콤 포인턴이 출연합니다.[260][261][262]
알츠하이머병은 또한 영국의 음악가인 관리인에 의해 음악에서도 묘사되었는데, 이는 "구문의 지속적인 반복"(2008), "이 세상을 넘어선 공허한 블리스"(2011), 그리고 "시간의 끝의 모든 곳"(2016-2019)과 같은 발표들에서 그러했습니다.[263][264][265] 이 장애를 묘사한 그림들에는 1995년부터 2000년까지 자신의 병을 예술을 통해 보여주는 실험으로 자화상을 그린 미국 화가 윌리엄 우테르몰렌의 후기 작품들이 포함되어 있습니다.[266][267]
연구방향
라이프스타일 효과에 대한 추가 연구는 신경 영상 바이오마커에 대한 통찰력과 알츠하이머병과 조기 발병 AD를 유발하는 메커니즘에 대한 더 나은 이해를 제공할 수 있습니다.[268]
신흥 가설
알츠하이머병은 중추신경계의 상주 면역세포인 미세아교세포의 신경염증 및 기능 상실과 관련이 있습니다.[269] 미세아교세포는 아밀로이드 플라크에 노출된 후 점진적으로 기능 장애를 일으키며, 전염증성 사이토카인(예: TNFα, IL-1β, IL-12)에 노출되면 이러한 기능 장애가 지속되는 것으로 가정되었습니다. 미세아교세포증을 통한 비정상적인 시냅스 가지치기도 AD 병리에 기여할 수 있습니다.[270] 발달 동안 전형적인 미세아교세포 가지치기의 일부 형태에 관여하는 보체 시스템은 [271]아밀로이드 플라크에 근접한 시냅스에서 활성화(예: C1q; C3b) 및 말단(예: MAC) 경로의 조절 장애를 통해 AD의 동물 모델에 연루됩니다.[272]
탐지, 예방 및 치료
항체는 도나네맙, 아두카누맙, 레카네맙과 같은 면역치료제로 아밀로이드 베타를 표적으로 삼아 질병 경과를 바꿀 수 있습니다.[273][274][275] 아두카누맙은 2021년 미국 식품의약국(FDA)의 승인을 가속화했지만 승인 과정에서 논란이 일었고 투여와 안전성, 효과를 다루기 위해서는 더 많은 증거가 필요합니다.[276][277][278][279] 이미 심각한 알츠하이머 증상이 있었던 사람들에게는 효과가 적습니다.[280] Lecanemab도 FDA 가속 승인 절차를 거쳐 승인되었으며,[281][282][283] 아밀로이드 관련 영상 이상에 대한 블랙박스 경고와 함께 추가 테스트를 거쳐 2023년 7월 전통적인 승인으로 전환되었습니다.[284][285] 또한 항아밀로이드 약물은 뇌의 수축을 유발합니다.[286]
알츠하이머병의 위험이나 진행을 줄일 수 있는 특정 약물이 연구되었습니다.[287] 약물을 조사하는 연구 시험은 일반적으로 Aβ 플라크, 염증, APOE, 신경 전달 물질 수용체, 신경 발생, 성장 인자 또는 호르몬에 영향을 미칩니다.[287][288][289]
앞서 AD를 예측하는 방법으로 전자건강기록이 있는 기계학습 알고리즘이 연구되고 있습니다.[290]
참고문헌
- ^ a b c d e f g h i j k Knopman DS, Amieva H, Petersen RC, Chételat G, Holtzman DM, Hyman BT, et al. (May 2021). "Alzheimer disease". Nature Reviews Disease Primers. 7 (1): 33. doi:10.1038/s41572-021-00269-y. PMC 8574196. PMID 33986301.
- ^ a b c d e f "Dementia Fact sheet". World Health Organization. 15 March 2023. Retrieved 10 July 2023.
- ^ a b c Ganguli M, Dodge HH, Shen C, Pandav RS, DeKosky ST (May 2005). "Alzheimer disease and mortality: a 15-year epidemiological study". Archives of Neurology. 62 (5): 779–784. doi:10.1001/archneur.62.5.779. PMID 15883266.
- ^ a b Mendez MF (November 2012). "Early-onset Alzheimer's disease: nonamnestic subtypes and type 2 AD". Archives of Medical Research. 43 (8): 677–685. doi:10.1016/j.arcmed.2012.11.009. PMC 3532551. PMID 23178565.
- ^ a b "Dementia diagnosis and assessment" (PDF). National Institute for Health and Care Excellence (NICE). Archived from the original (PDF) on 5 December 2014. Retrieved 30 November 2014.
- ^ Gomperts SN (April 2016). "Lewy Body Dementias: Dementia With Lewy Bodies and Parkinson Disease Dementia". Continuum (Review). 22 (2 Dementia): 435–463. doi:10.1212/CON.0000000000000309. PMC 5390937. PMID 27042903.
- ^ a b Lott IT, Head E (March 2019). "Dementia in Down syndrome: unique insights for Alzheimer disease research". Nat Rev Neurol. 15 (3): 135–147. doi:10.1038/s41582-018-0132-6. PMC 8061428. PMID 30733618.
- ^ a b Querfurth HW, LaFerla FM (January 2010). "Alzheimer's disease". The New England Journal of Medicine. 362 (4): 329–344. doi:10.1056/NEJMra0909142. PMID 20107219. S2CID 205115756.
- ^ a b c d e f g h i j k Breijyeh Z, Karaman R (December 2020). "Comprehensive Review on Alzheimer's Disease: Causes and Treatment". Molecules (Review). 25 (24): 5789. doi:10.3390/molecules25245789. PMC 7764106. PMID 33302541.
- ^ a b c d Simon RP, Greenberg DA, Aminoff MJ (2018). Clinical neurology (Tenth ed.). [New York]: McGraw Hill. p. 111. ISBN 978-1-259-86173-4. OCLC 1012400314.
- ^ a b c d Burns A, Iliffe S (February 2009). "Alzheimer's disease". BMJ. 338: b158. doi:10.1136/bmj.b158. PMID 19196745. S2CID 8570146.
- ^ Todd S, Barr S, Roberts M, Passmore AP (November 2013). "Survival in dementia and predictors of mortality: a review". International Journal of Geriatric Psychiatry. 28 (11): 1109–1124. doi:10.1002/gps.3946. PMID 23526458. S2CID 25445595.
- ^ a b c d Long JM, Holtzman DM (October 2019). "Alzheimer Disease: An Update on Pathobiology and Treatment Strategies". Cell. 179 (2): 312–339. doi:10.1016/j.cell.2019.09.001. PMC 6778042. PMID 31564456.
- ^ a b "Study reveals how APOE4 gene may increase risk for dementia". National Institute on Aging. 16 March 2021. Archived from the original on 17 March 2021. Retrieved 17 March 2021.
- ^ a b c d e "Alzheimer's Disease Fact Sheet". National Institute on Aging. Archived from the original on 23 March 2022. Retrieved 23 March 2022.
- ^ Dementia: assessment, management and support for people living with dementia and their carers (Report). National Institute for Health and Care Excellence (NICE). 20 June 2018. NG97. Retrieved 8 July 2023.
- ^ a b c "Alzheimer's Disease Fact Sheet". National Institute on Aging. Archived from the original on 24 January 2021. Retrieved 25 January 2021.
- ^ a b c d Thompson CA, Spilsbury K, Hall J, Birks Y, Barnes C, Adamson J (July 2007). "Systematic review of information and support interventions for caregivers of people with dementia". BMC Geriatrics. 7: 18. doi:10.1186/1471-2318-7-18. PMC 1951962. PMID 17662119.
- ^ Forbes D, Forbes SC, Blake CM, Thiessen EJ, Forbes S (April 2015). "Exercise programs for people with dementia". The Cochrane Database of Systematic Reviews (Submitted manuscript). 132 (4): CD006489. doi:10.1002/14651858.CD006489.pub4. PMC 9426996. PMID 25874613.
- ^ "Low-dose antipsychotics in people with dementia". National Institute for Health and Care Excellence (NICE). Archived from the original on 5 December 2014. Retrieved 29 November 2014.
- ^ "Information for Healthcare Professionals: Conventional Antipsychotics". US Food and Drug Administration. 16 June 2008. Archived from the original on 29 November 2014. Retrieved 29 November 2014.
- ^ Zhu D, Montagne A, Zhao Z (June 2021). "Alzheimer's pathogenic mechanisms and underlying sex difference". Cell Mol Life Sci. 78 (11): 4907–4920. doi:10.1007/s00018-021-03830-w. PMC 8720296. PMID 33844047.
- ^ a b c Berchtold NC, Cotman CW (1998). "Evolution in the conceptualization of dementia and Alzheimer's disease: Greco-Roman period to the 1960s". Neurobiology of Aging. 19 (3): 173–189. doi:10.1016/S0197-4580(98)00052-9. PMID 9661992. S2CID 24808582.
- ^ a b c "Alzheimer's disease – Symptoms". National Health Service (NHS). 10 May 2018. Archived from the original on 30 January 2021. Retrieved 25 January 2021.
- ^ a b Waldemar G, Dubois B, Emre M, Georges J, McKeith IG, Rossor M, et al. (January 2007). "Recommendations for the diagnosis and management of Alzheimer's disease and other disorders associated with dementia: EFNS guideline". European Journal of Neurology. 14 (1): e1-26. doi:10.1111/j.1468-1331.2006.01605.x. PMID 17222085. S2CID 2725064.
- ^ a b c Bäckman L, Jones S, Berger AK, Laukka EJ, Small BJ (September 2004). "Multiple cognitive deficits during the transition to Alzheimer's disease". Journal of Internal Medicine. 256 (3): 195–204. doi:10.1111/j.1365-2796.2004.01386.x. PMID 15324363. S2CID 37005854.
- ^ Nygård L (2003). "Instrumental activities of daily living: a stepping-stone towards Alzheimer's disease diagnosis in subjects with mild cognitive impairment?". Acta Neurologica Scandinavica. Supplementum. 179 (s179): 42–46. doi:10.1034/j.1600-0404.107.s179.8.x. PMID 12603250. S2CID 25313065.
- ^ Deardorff WJ, Grossberg GT (2019). "Behavioral and psychological symptoms in Alzheimer's dementia and vascular dementia". Psychopharmacology of Neurologic Disease. Handbook of Clinical Neurology. Vol. 165. pp. 5–32. doi:10.1016/B978-0-444-64012-3.00002-2. ISBN 978-0444640123. PMID 31727229. S2CID 208037448.
- ^ Murray ED, Buttner N, Price BH (2012). "Depression and Psychosis in Neurological Practice". In Bradley WG, Daroff RB, Fenichel GM, Jankovic J (eds.). Bradley's neurology in clinical practice (6th ed.). Philadelphia, PA: Elsevier/Saunders. ISBN 978-1-4377-0434-1.
- ^ a b Petersen RC, Lopez O, Armstrong MJ, Getchius TS, Ganguli M, Gloss D, et al. (January 2018). "Practice guideline update summary: Mild cognitive impairment: Report of the Guideline Development, Dissemination, and Implementation Subcommittee of the American Academy of Neurology". Neurology. 90 (3): 126–135. doi:10.1212/WNL.0000000000004826. PMC 5772157. PMID 29282327.
- ^ a b c Atri A (March 2019). "The Alzheimer's Disease Clinical Spectrum: Diagnosis and Management". The Medical Clinics of North America (Review). 103 (2): 263–293. doi:10.1016/j.mcna.2018.10.009. PMID 30704681. S2CID 73432842.
- ^ a b c d e f g h i j k l m n o p q r s Förstl H, Kurz A (1999). "Clinical features of Alzheimer's disease". European Archives of Psychiatry and Clinical Neuroscience. 249 (6): 288–290. doi:10.1007/s004060050101. PMID 10653284. S2CID 26142779.
- ^ Carlesimo GA, Oscar-Berman M (June 1992). "Memory deficits in Alzheimer's patients: a comprehensive review". Neuropsychology Review. 3 (2): 119–169. doi:10.1007/BF01108841. PMID 1300219. S2CID 19548915.
- ^ Jelicic M, Bonebakker AE, Bonke B (1995). "Implicit memory performance of patients with Alzheimer's disease: a brief review". International Psychogeriatrics. 7 (3): 385–392. doi:10.1017/S1041610295002134. PMID 8821346. S2CID 9419442.
- ^ a b Taler V, Phillips NA (July 2008). "Language performance in Alzheimer's disease and mild cognitive impairment: a comparative review". Journal of Clinical and Experimental Neuropsychology. 30 (5): 501–556. doi:10.1080/13803390701550128. PMID 18569251. S2CID 37153159.
- ^ a b c Frank EM (September 1994). "Effect of Alzheimer's disease on communication function". Journal of the South Carolina Medical Association. 90 (9): 417–423. PMID 7967534.
- ^ Volicer L, Harper DG, Manning BC, Goldstein R, Satlin A (May 2001). "Sundowning and circadian rhythms in Alzheimer's disease". The American Journal of Psychiatry. 158 (5): 704–711. doi:10.1176/appi.ajp.158.5.704. PMID 11329390. S2CID 10492607.
- ^ Gold DP, Reis MF, Markiewicz D, Andres D (January 1995). "When home caregiving ends: a longitudinal study of outcomes for caregivers of relatives with dementia". Journal of the American Geriatrics Society. 43 (1): 10–16. doi:10.1111/j.1532-5415.1995.tb06235.x. PMID 7806732. S2CID 29847950.
- ^ Mashour GA, Frank L, Batthyany A, Kolanowski AM, Nahm M, Schulman-Green D, et al. (August 2019). "Paradoxical lucidity: A potential paradigm shift for the neurobiology and treatment of severe dementias". Alzheimer's & Dementia. 15 (8): 1107–1114. doi:10.1016/j.jalz.2019.04.002. hdl:2027.42/153062. PMID 31229433. S2CID 195063786.
- ^ "Alzheimer's disease – Causes". National Health Service (NHS). 24 April 2023. Archived from the original on 29 September 2020. Retrieved 10 July 2023.
- ^ Tackenberg C, Kulic L, Nitsch RM (2020). "Familial Alzheimer's disease mutations at position 22 of the amyloid β-peptide sequence differentially affect synaptic loss, tau phosphorylation and neuronal cell death in an ex vivo system". PLOS ONE. 15 (9): e0239584. Bibcode:2020PLoSO..1539584T. doi:10.1371/journal.pone.0239584. PMC 7510992. PMID 32966331.
- ^ Wang H, Kulas JA, Wang C, Holtzman DM, Ferris HA, Hansen SB (August 2021). "Regulation of beta-amyloid production in neurons by astrocyte-derived cholesterol". Proceedings of the National Academy of Sciences of the United States of America. 118 (33): e2102191118. Bibcode:2021PNAS..11802191W. doi:10.1073/pnas.2102191118. ISSN 0027-8424. PMC 8379952. PMID 34385305. S2CID 236998499.
- ^ Vilchez D, Saez I, Dillin A (December 2014). "The role of protein clearance mechanisms in organismal ageing and age-related diseases". Nature Communications. 5: 5659. Bibcode:2014NatCo...5.5659V. doi:10.1038/ncomms6659. PMID 25482515.
- ^ Jacobson M, McCarthy N (2002). Apoptosis. Oxford, OX: Oxford University Press. p. 290. ISBN 0199638497.
- ^ Hardy J, Allsop D (October 1991). "Amyloid deposition as the central event in the aetiology of Alzheimer's disease". Trends in Pharmacological Sciences. 12 (10): 383–388. doi:10.1016/0165-6147(91)90609-V. PMID 1763432.
- ^ a b Mudher A, Lovestone S (January 2002). "Alzheimer's disease-do tauists and baptists finally shake hands?". Trends in Neurosciences. 25 (1): 22–26. doi:10.1016/S0166-2236(00)02031-2. PMID 11801334. S2CID 37380445.
- ^ Polvikoski T, Sulkava R, Haltia M, Kainulainen K, Vuorio A, Verkkoniemi A, et al. (November 1995). "Apolipoprotein E, dementia, and cortical deposition of beta-amyloid protein". The New England Journal of Medicine. 333 (19): 1242–1247. doi:10.1056/NEJM199511093331902. PMID 7566000.
- ^ a b Andrews SJ, Renton AE, Fulton-Howard B, Podlesny-Drabiniok A, Marcora E, Goate AM (April 2023). "The complex genetic architecture of Alzheimer's disease: novel insights and future directions". eBioMedicine. 90: 104511. doi:10.1016/j.ebiom.2023.104511. PMC 10024184. PMID 36907103.
- ^ a b Scheltens P, De Strooper B, Kivipelto M, Holstege H, Chételat G, Teunissen CE, et al. (April 2021). "Alzheimer's disease". Lancet. 397 (10284): 1577–1590. doi:10.1016/S0140-6736(20)32205-4. PMC 8354300. PMID 33667416.
- ^ Sims R, Hill M, Williams J (March 2020). "The multiplex model of the genetics of Alzheimer's disease" (PDF). Nat Neurosci. 23 (3): 311–322. doi:10.1038/s41593-020-0599-5. PMID 32112059. S2CID 256839971.
- ^ Piaceri I, Nacmias B, Sorbi S (January 2013). "Genetics of familial and sporadic Alzheimer's disease". Front Biosci (Elite Ed). 5 (1): 167–177. doi:10.2741/e605. PMID 23276979.
- ^ Perea JR, Bolós M, Avila J (October 2020). "Microglia in Alzheimer's Disease in the Context of Tau Pathology". Biomolecules. 10 (10): 1439. doi:10.3390/biom10101439. PMC 7602223. PMID 33066368.
- ^ Mahley RW, Weisgraber KH, Huang Y (April 2006). "Apolipoprotein E4: a causative factor and therapeutic target in neuropathology, including Alzheimer's disease". Proceedings of the National Academy of Sciences of the United States of America. 103 (15): 5644–5651. Bibcode:2006PNAS..103.5644M. doi:10.1073/pnas.0600549103. PMC 1414631. PMID 16567625.
- ^ Blennow K, de Leon MJ, Zetterberg H (July 2006). "Alzheimer's disease". Lancet. 368 (9533): 387–403. doi:10.1016/S0140-6736(06)69113-7. PMID 16876668. S2CID 47544338.
- ^ Hall K, Murrell J, Ogunniyi A, Deeg M, Baiyewu O, Gao S, et al. (January 2006). "Cholesterol, APOE genotype, and Alzheimer disease: an epidemiologic study of Nigerian Yoruba". Neurology. 66 (2): 223–227. doi:10.1212/01.wnl.0000194507.39504.17. PMC 2860622. PMID 16434658.
- ^ Gureje O, Ogunniyi A, Baiyewu O, Price B, Unverzagt FW, Evans RM, et al. (January 2006). "APOE epsilon4 is not associated with Alzheimer's disease in elderly Nigerians". Annals of Neurology. 59 (1): 182–185. doi:10.1002/ana.20694. PMC 2855121. PMID 16278853.
- ^ Piaceri I (2013). "Genetics of familial and sporadic Alzheimer s disease". Frontiers in Bioscience. E5 (1): 167–177. doi:10.2741/E605. ISSN 1945-0494. PMID 23276979.
- ^ Selkoe DJ (June 1999). "Translating cell biology into therapeutic advances in Alzheimer's disease". Nature. 399 (6738 Suppl): A23–A31. doi:10.1038/19866. PMID 10392577. S2CID 42287088.
- ^ Borchelt DR, Thinakaran G, Eckman CB, Lee MK, Davenport F, Ratovitsky T, et al. (November 1996). "Familial Alzheimer's disease-linked presenilin 1 variants elevate Abeta1-42/1-40 ratio in vitro and in vivo". Neuron. 17 (5): 1005–1013. doi:10.1016/S0896-6273(00)80230-5. PMID 8938131. S2CID 18315650.
- ^ Kim JH (December 2018). "Genetics of Alzheimer's Disease". Dementia and Neurocognitive Disorders. 17 (4): 131–136. doi:10.12779/dnd.2018.17.4.131. PMC 6425887. PMID 30906402.
- ^ Carmona S, Zahs K, Wu E, Dakin K, Bras J, Guerreiro R (August 2018). "The role of TREM2 in Alzheimer's disease and other neurodegenerative disorders". Lancet Neurol. 17 (8): 721–730. doi:10.1016/S1474-4422(18)30232-1. PMID 30033062. S2CID 51706988. Archived from the original on 27 March 2022. Retrieved 21 February 2022.
- ^ Tomiyama T (July 2010). "[Involvement of beta-amyloid in the etiology of Alzheimer's disease]". Brain and Nerve = Shinkei Kenkyu No Shinpo. 62 (7): 691–699. PMID 20675873.
- ^ Tomiyama T, Nagata T, Shimada H, Teraoka R, Fukushima A, Kanemitsu H, et al. (March 2008). "A new amyloid beta variant favoring oligomerization in Alzheimer's-type dementia". Annals of Neurology. 63 (3): 377–387. doi:10.1002/ana.21321. PMID 18300294. S2CID 42311988.
- ^ Tomiyama T, Shimada H (February 2020). "APP Osaka Mutation in Familial Alzheimer's Disease-Its Discovery, Phenotypes, and Mechanism of Recessive Inheritance". International Journal of Molecular Sciences. 21 (4): 1413. doi:10.3390/ijms21041413. PMC 7073033. PMID 32093100.
- ^ Goedert M, Spillantini MG, Crowther RA (July 1991). "Tau proteins and neurofibrillary degeneration". Brain Pathology. 1 (4): 279–286. doi:10.1111/j.1750-3639.1991.tb00671.x. PMID 1669718. S2CID 33331924.
- ^ Iqbal K, Alonso A, Chen S, Chohan MO, El-Akkad E, Gong CX, et al. (January 2005). "Tau pathology in Alzheimer disease and other tauopathies". Biochimica et Biophysica Acta (BBA) - Molecular Basis of Disease. 1739 (2–3): 198–210. doi:10.1016/j.bbadis.2004.09.008. PMID 15615638.
- ^ Sinyor B, Mineo J, Ochner C (June 2020). "Alzheimer's Disease, Inflammation, and the Role of Antioxidants". Journal of Alzheimer's Disease Reports. 4 (1): 175–183. doi:10.3233/ADR-200171. PMC 7369138. PMID 32715278.
- ^ Kinney JW, Bemiller SM, Murtishaw AS, Leisgang AM, Salazar AM, Lamb BT (2018). "Inflammation as a central mechanism in Alzheimer's disease". Alzheimer's & Dementia. 4: 575–590. doi:10.1016/j.trci.2018.06.014. PMC 6214864. PMID 30406177.
- ^ Lin X, Kapoor A, Gu Y, Chow MJ, Peng J, Zhao K, et al. (February 2020). "Contributions of DNA Damage to Alzheimer's Disease". Int J Mol Sci. 21 (5): 1666. doi:10.3390/ijms21051666. PMC 7084447. PMID 32121304.
- ^ Irwin MR, Vitiello MV (March 2019). "Implications of sleep disturbance and inflammation for Alzheimer's disease dementia". The Lancet. Neurology. 18 (3): 296–306. doi:10.1016/S1474-4422(18)30450-2. PMID 30661858. S2CID 58546748.
- ^ Huat TJ, Camats-Perna J, Newcombe EA, Valmas N, Kitazawa M, Medeiros R (April 2019). "Metal Toxicity Links to Alzheimer's Disease and Neuroinflammation". J Mol Biol. 431 (9): 1843–1868. doi:10.1016/j.jmb.2019.01.018. PMC 6475603. PMID 30664867.
- ^ Eikelenboom P, van Exel E, Hoozemans JJ, Veerhuis R, Rozemuller AJ, van Gool WA (2010). "Neuroinflammation – an early event in both the history and pathogenesis of Alzheimer's disease". Neuro-Degenerative Diseases. 7 (1–3): 38–41. doi:10.1159/000283480. PMID 20160456. S2CID 40048333.
- ^ Alves GS, Oertel Knöchel V, Knöchel C, Carvalho AF, Pantel J, Engelhardt E, Laks J (2015). "Integrating retrogenesis theory to Alzheimer's disease pathology: insight from DTI-TBSS investigation of the white matter microstructural integrity". BioMed Research International. 2015: 291658. doi:10.1155/2015/291658. PMC 4320890. PMID 25685779.
- ^ Reisberg B, Franssen EH, Hasan SM, Monteiro I, Boksay I, Souren LE, et al. (1999). "Retrogenesis: clinical, physiologic, and pathologic mechanisms in brain aging, Alzheimer's and other dementing processes". European Archives of Psychiatry and Clinical Neuroscience. 249 (3): 28–36. doi:10.1007/pl00014170. PMID 10654097. S2CID 23410069.
- ^ Zis P, Hadjivassiliou M (February 2019). "Treatment of Neurological Manifestations of Gluten Sensitivity and Coeliac Disease". Current Treatment Options in Neurology. 21 (3): 10. doi:10.1007/s11940-019-0552-7. PMID 30806821. S2CID 73466457.
- ^ Makhlouf S, Messelmani M, Zaouali J, Mrissa R (March 2018). "Cognitive impairment in celiac disease and non-celiac gluten sensitivity: review of literature on the main cognitive impairments, the imaging and the effect of gluten free diet". Acta Neurologica Belgica (Review). 118 (1): 21–27. doi:10.1007/s13760-017-0870-z. PMID 29247390. S2CID 3943047.
- ^ Bartzokis G (August 2011). "Alzheimer's disease as homeostatic responses to age-related myelin breakdown". Neurobiology of Aging. 32 (8): 1341–1371. doi:10.1016/j.neurobiolaging.2009.08.007. PMC 3128664. PMID 19775776.
- ^ Cai Z, Xiao M (2016). "Oligodendrocytes and Alzheimer's disease". The International Journal of Neuroscience. 126 (2): 97–104. doi:10.3109/00207454.2015.1025778. PMID 26000818. S2CID 21448714.
- ^ Zhou, Li; Miranda-Saksena, Monica; Saksena, Nitin K. (31 May 2013). "Viruses and neurodegeneration". Virology Journal. 10 (1): 172. doi:10.1186/1743-422X-10-172. ISSN 1743-422X. PMC 3679988. PMID 23724961.
- ^ Gonzalez-Fernandez, Ezekiel; Huang, Juebin (1 September 2023). "Cognitive Aspects of COVID-19". Current Neurology and Neuroscience Reports. 23 (9): 531–538. doi:10.1007/s11910-023-01286-y. ISSN 1534-6293. PMID 37490194. S2CID 260132167.
- ^ Wenk GL (2003). "Neuropathologic changes in Alzheimer's disease". The Journal of Clinical Psychiatry. 64 (Suppl 9): 7–10. PMID 12934968.
- ^ Braak H, Del Tredici K (December 2012). "Where, when, and in what form does sporadic Alzheimer's disease begin?". Current Opinion in Neurology. 25 (6): 708–714. doi:10.1097/WCO.0b013e32835a3432. PMID 23160422.
- ^ Desikan RS, Cabral HJ, Hess CP, Dillon WP, Glastonbury CM, Weiner MW, et al. (August 2009). "Automated MRI measures identify individuals with mild cognitive impairment and Alzheimer's disease". Brain. 132 (Pt 8): 2048–2057. doi:10.1093/brain/awp123. PMC 2714061. PMID 19460794.
- ^ Moan R (July 2009). "MRI Software Accurately IDs Preclinical Alzheimer's Disease". Diagnostic Imaging. Archived from the original on 21 February 2022. Retrieved 21 February 2022.
- ^ a b Tiraboschi P, Hansen LA, Thal LJ, Corey-Bloom J (June 2004). "The importance of neuritic plaques and tangles to the development and evolution of AD". Neurology. 62 (11): 1984–1989. doi:10.1212/01.WNL.0000129697.01779.0A. PMID 15184601. S2CID 25017332.
- ^ DeTure MA, Dickson DW (August 2019). "The neuropathological diagnosis of Alzheimer's disease". Molecular Neurodegeneration. 14 (1): 32. doi:10.1186/s13024-019-0333-5. PMC 6679484. PMID 31375134.
- ^ Tiraboschi P, Sabbagh MN, Hansen LA, Salmon DP, Merdes A, Gamst A, et al. (April 2004). "Alzheimer disease without neocortical neurofibrillary tangles: "a second look"". Neurology. 62 (7): 1141–1147. doi:10.1212/01.wnl.0000118212.41542.e7. PMID 15079014. S2CID 22832110.
- ^ Bouras C, Hof PR, Giannakopoulos P, Michel JP, Morrison JH (1994). "Regional distribution of neurofibrillary tangles and senile plaques in the cerebral cortex of elderly patients: a quantitative evaluation of a one-year autopsy population from a geriatric hospital". Cerebral Cortex. 4 (2): 138–150. doi:10.1093/cercor/4.2.138. PMID 8038565.
- ^ Kotzbauer PT, Trojanowsk JQ, Lee VM (October 2001). "Lewy body pathology in Alzheimer's disease". Journal of Molecular Neuroscience. 17 (2): 225–232. doi:10.1385/JMN:17:2:225. PMID 11816795. S2CID 44407971.
- ^ Hashimoto M, Rockenstein E, Crews L, Masliah E (2003). "Role of protein aggregation in mitochondrial dysfunction and neurodegeneration in Alzheimer's and Parkinson's diseases". Neuromolecular Medicine. 4 (1–2): 21–36. doi:10.1385/NMM:4:1-2:21. PMID 14528050. S2CID 20760249.
- ^ Priller C, Bauer T, Mitteregger G, Krebs B, Kretzschmar HA, Herms J (July 2006). "Synapse formation and function is modulated by the amyloid precursor protein". The Journal of Neuroscience. 26 (27): 7212–7221. doi:10.1523/JNEUROSCI.1450-06.2006. PMC 6673945. PMID 16822978.
- ^ Turner PR, O'Connor K, Tate WP, Abraham WC (May 2003). "Roles of amyloid precursor protein and its fragments in regulating neural activity, plasticity and memory". Progress in Neurobiology. 70 (1): 1–32. doi:10.1016/S0301-0082(03)00089-3. PMID 12927332. S2CID 25376584.
- ^ Hooper NM (April 2005). "Roles of proteolysis and lipid rafts in the processing of the amyloid precursor protein and prion protein". Biochemical Society Transactions. 33 (Pt 2): 335–338. doi:10.1042/BST0330335. PMID 15787600. S2CID 14269634.
- ^ Ohnishi S, Takano K (March 2004). "Amyloid fibrils from the viewpoint of protein folding". Cellular and Molecular Life Sciences. 61 (5): 511–524. doi:10.1007/s00018-003-3264-8. PMID 15004691. S2CID 25739126.
- ^ Hernández F, Avila J (September 2007). "Tauopathies". Cellular and Molecular Life Sciences. 64 (17): 2219–2233. doi:10.1007/s00018-007-7220-x. PMID 17604998. S2CID 261121643.
- ^ Sun W, Samimi H, Gamez M, Zare H, Frost B (August 2018). "Pathogenic tau-induced piRNA depletion promotes neuronal death through transposable element dysregulation in neurodegenerative tauopathies". Nature Neuroscience. 21 (8): 1038–1048. doi:10.1038/s41593-018-0194-1. PMC 6095477. PMID 30038280.
- ^ Balusu S, Horré K, Thrupp N, Craesaerts K, Snellinx A, Sernels L, T'Syen D, Chrysidou I, Arranz AM, Sierksma A, Simrén J, Karikari TK, Zetterberg H, Chen WT, Thal DR, Salta E, Fiers M, De Strooper B. MEG3는 알츠하이머병을 모델링하는 인간 뉴런 이종이식에서 괴사를 활성화합니다. 과학. 2023 Sep 15;381(6663):1176-1182. doi:10.1126/science.abp9556 PMID 37708272
- ^ "Scientists discover how brain cells die in Alzheimer's". BBC News. 15 September 2023. Retrieved 27 September 2023.
- ^ Van Broeck B, Van Broeckhoven C, Kumar-Singh S (2007). "Current insights into molecular mechanisms of Alzheimer disease and their implications for therapeutic approaches". Neuro-Degenerative Diseases. 4 (5): 349–365. doi:10.1159/000105156. PMID 17622778. S2CID 7949658.
- ^ Huang Y, Mucke L (March 2012). "Alzheimer mechanisms and therapeutic strategies". Cell. 148 (6): 1204–1222. doi:10.1016/j.cell.2012.02.040. PMC 3319071. PMID 22424230.
- ^ Yankner BA, Duffy LK, Kirschner DA (October 1990). "Neurotrophic and neurotoxic effects of amyloid beta protein: reversal by tachykinin neuropeptides". Science. 250 (4978): 279–282. Bibcode:1990Sci...250..279Y. doi:10.1126/science.2218531. PMID 2218531.
- ^ Chen X, Yan SD (December 2006). "Mitochondrial Abeta: a potential cause of metabolic dysfunction in Alzheimer's disease". IUBMB Life. 58 (12): 686–694. doi:10.1080/15216540601047767. PMID 17424907. S2CID 85423830.
- ^ Ryan, Sean K.; Ugalde, Cathryn L.; Rolland, Anne-Sophie; Skidmore, John; Devos, David; Hammond, Timothy R. (2023). "Therapeutic inhibition of ferroptosis in neurodegenerative disease". Trends in Pharmacological Sciences. 44 (10): 674–688. doi:10.1016/j.tips.2023.07.007. PMID 37657967.
- ^ Greig NH, Mattson MP, Perry T, Chan SL, Giordano T, Sambamurti K, et al. (December 2004). "New therapeutic strategies and drug candidates for neurodegenerative diseases: p53 and TNF-alpha inhibitors, and GLP-1 receptor agonists". Annals of the New York Academy of Sciences. 1035: 290–315. doi:10.1196/annals.1332.018. PMID 15681814. S2CID 84659695. Archived from the original on 3 June 2020. Retrieved 19 July 2019.
- ^ Heneka MT, Carson MJ, El Khoury J, Landreth GE, Brosseron F, Feinstein DL, et al. (April 2015). "Neuroinflammation in Alzheimer's disease". The Lancet. Neurology. 14 (4): 388–405. doi:10.1016/S1474-4422(15)70016-5. PMC 5909703. PMID 25792098.
- ^ Tapia-Arancibia L, Aliaga E, Silhol M, Arancibia S (November 2008). "New insights into brain BDNF function in normal aging and Alzheimer disease". Brain Research Reviews. 59 (1): 201–220. doi:10.1016/j.brainresrev.2008.07.007. hdl:10533/142174. PMID 18708092. S2CID 6589846.
- ^ Schindowski K, Belarbi K, Buée L (February 2008). "Neurotrophic factors in Alzheimer's disease: role of axonal transport". Genes, Brain and Behavior. 7 (Suppl 1): 43–56. doi:10.1111/j.1601-183X.2007.00378.x. PMC 2228393. PMID 18184369.
- ^ Khan S, Barve KH, Kumar MS (2020). "Recent Advancements in Pathogenesis, Diagnostics and Treatment of Alzheimer's Disease". Curr Neuropharmacol. 18 (11): 1106–1125. doi:10.2174/1570159X18666200528142429. PMC 7709159. PMID 32484110.
- ^ a b Gauthreaux K, Bonnett TA, Besser LM, Brenowitz WD, Teylan M, Mock C, et al. (May 2020). "Concordance of Clinical Alzheimer Diagnosis and Neuropathological Features at Autopsy". Journal of Neuropathology and Experimental Neurology. 79 (5): 465–473. doi:10.1093/jnen/nlaa014. PMC 7160616. PMID 32186726.
- ^ a b Sachdev PS, Blacker D, Blazer DG, Ganguli M, Jeste DV, Paulsen JS, Petersen RC (November 2014). "Classifying neurocognitive disorders: the DSM-5 approach". Nature Reviews. Neurology. 10 (11): 634–642. doi:10.1038/nrneurol.2014.181. PMID 25266297. S2CID 20635070. Archived from the original on 20 March 2022. Retrieved 27 November 2021.
- ^ Mendez MF (2006). "The accurate diagnosis of early-onset dementia". International Journal of Psychiatry in Medicine. 36 (4): 401–412. doi:10.2190/Q6J4-R143-P630-KW41. PMID 17407994. S2CID 43715976. Archived from the original on 3 June 2020. Retrieved 25 May 2020.
- ^ Klafki HW, Staufenbiel M, Kornhuber J, Wiltfang J (November 2006). "Therapeutic approaches to Alzheimer's disease". Brain. 129 (Pt 11): 2840–2855. doi:10.1093/brain/awl280. PMID 17018549.
- ^ Dementia: Quick Reference Guide (PDF). London: (UK) National Institute for Health and Clinical Excellence. 2006. ISBN 978-1-84629-312-2. Archived from the original (PDF) on 27 February 2008. Retrieved 22 February 2008.
- ^ Schroeter ML, Stein T, Maslowski N, Neumann J (October 2009). "Neural correlates of Alzheimer's disease and mild cognitive impairment: a systematic and quantitative meta-analysis involving 1351 patients". NeuroImage. 47 (4): 1196–1206. doi:10.1016/j.neuroimage.2009.05.037. PMC 2730171. PMID 19463961.
- ^ Jie CV, Treyer V, Schibli R, Mu L (January 2021). "Tauvid: The First FDA-Approved PET Tracer for Imaging Tau Pathology in Alzheimer's Disease". Pharmaceuticals. 14 (2): 110. doi:10.3390/ph14020110. PMC 7911942. PMID 33573211.
- ^ a b c d e Weller J, Budson A (2018). "Current understanding of Alzheimer's disease diagnosis and treatment". F1000Research (Review). 7: 1161. doi:10.12688/f1000research.14506.1. PMC 6073093. PMID 30135715.
- ^ Silva MV, Loures CM, Alves LC, de Souza LC, Borges KB, Carvalho MD (May 2019). "Alzheimer's disease: risk factors and potentially protective measures". Journal of Biomedical Science. 26 (1): 33. doi:10.1186/s12929-019-0524-y. PMC 6507104. PMID 31072403.
- ^ Hane FT, Robinson M, Lee BY, Bai O, Leonenko Z, Albert MS (2017). "Recent Progress in Alzheimer's Disease Research, Part 3: Diagnosis and Treatment". Journal of Alzheimer's Disease (Review). 57 (3): 645–665. doi:10.3233/JAD-160907. PMC 5389048. PMID 28269772.
- ^ Diagnostic and statistical manual of mental disorders: DSM-IV-TR (4th Text Revision ed.). Washington, DC: American Psychiatric Association. 2000. ISBN 978-0-89042-025-6.
- ^ a b c Diagnostic and statistical manual of mental disorders: DSM-5. Washington, D.C: American Psychiatric Association. 2013. p. 611. ISBN 978-0890425558.
- ^ Sachs-Ericsson N, Blazer DG (January 2015). "The new DSM-5 diagnosis of mild neurocognitive disorder and its relation to research in mild cognitive impairment". Aging & Mental Health. 19 (1): 2–12. doi:10.1080/13607863.2014.920303. PMID 24914889. S2CID 46244321.
- ^ Stokin GB, Krell-Roesch J, Petersen RC, Geda YE (2015). "Mild Neurocognitive Disorder: An Old Wine in a New Bottle". Harvard Review of Psychiatry (Review). 23 (5): 368–376. doi:10.1097/HRP.0000000000000084. PMC 4894762. PMID 26332219.
- ^ Sperry L, Carlson J, Sauerheber J, Sperry J, eds. (2014). Psychopathology and Psychotherapy: DSM-5 Diagnosis, Case Conceptualization, and Treatment (3 ed.). New York: Routledge. pp. 342–343. doi:10.4324/9780203772287. ISBN 978-0-203-77228-7. Archived from the original on 16 November 2021. Retrieved 16 November 2021.
- ^ Fink HA, Hemmy LS, Linskens EJ, Silverman PC, MacDonald R, McCarten JR, et al. (2020). Diagnosis and Treatment of Clinical Alzheimer's-Type Dementia: A Systematic Review. AHRQ Comparative Effectiveness Reviews. Rockville (MD): Agency for Healthcare Research and Quality (US). PMID 32369312. Archived from the original on 7 July 2023. Retrieved 16 November 2021.
- ^ Stokin GB, Krell-Roesch J, Petersen RC, Geda YE (September 2015). "Mild Neurocognitive Disorder: An Old Wine in a New Bottle". Harvard Review of Psychiatry. Wolters Kluwer Health. 23 (5): 368–376. doi:10.1097/HRP.0000000000000084. PMC 4894762. PMID 26332219.
- ^ Bradfield NI, Ames D (April 2020). "Mild cognitive impairment: narrative review of taxonomies and systematic review of their prediction of incident Alzheimer's disease dementia". BJPsych Bulletin (Review). 44 (2): 67–74. doi:10.1192/bjb.2019.77. PMC 7283119. PMID 31724527.
- ^ a b Vega JN, Newhouse PA (October 2014). "Mild cognitive impairment: diagnosis, longitudinal course, and emerging treatments". Current Psychiatry Reports. SpringerLink. 16 (10): 490. doi:10.1007/s11920-014-0490-8. PMC 4169219. PMID 25160795.
- ^ Parnetti L, Chipi E, Salvadori N, D'Andrea K, Eusebi P (January 2019). "Prevalence and risk of progression of preclinical Alzheimer's disease stages: a systematic review and meta-analysis". Alzheimer's Research & Therapy. Springer Nature. 11 (1): 7. doi:10.1186/s13195-018-0459-7. PMC 6334406. PMID 30646955.
- ^ a b c d e Jack CR, Bennett DA, Blennow K, Carrillo MC, Dunn B, Haeberlein SB, et al. (April 2018). "NIA-AA Research Framework: Toward a biological definition of Alzheimer's disease". Alzheimer's & Dementia. Wiley Online Library. 14 (4): 535–562. doi:10.1016/j.jalz.2018.02.018. PMC 5958625. PMID 29653606.
- ^ Sperling RA, Aisen PS, Beckett LA, Bennett DA, Craft S, Fagan AM, et al. (May 2011). "Toward defining the preclinical stages of Alzheimer's disease: recommendations from the National Institute on Aging-Alzheimer's Association workgroups on diagnostic guidelines for Alzheimer's disease". Alzheimer's & Dementia. Wiley Online Library. 7 (3): 280–292. doi:10.1016/j.jalz.2011.03.003. PMC 3220946. PMID 21514248.
- ^ Cheng YW, Chen TF, Chiu MJ (16 February 2017). "From mild cognitive impairment to subjective cognitive decline: conceptual and methodological evolution". Neuropsychiatric Disease and Treatment. Dove Medical Press Limited. 13: 491–498. doi:10.2147/NDT.S123428. PMC 5317337. PMID 28243102.
- ^ Albert MS, DeKosky ST, Dickson D, Dubois B, Feldman HH, Fox NC, et al. (May 2011). "The diagnosis of mild cognitive impairment due to Alzheimer's disease: recommendations from the National Institute on Aging-Alzheimer's Association workgroups on diagnostic guidelines for Alzheimer's disease". Alzheimer's & Dementia. Wiley Online Library. 7 (3): 270–279. doi:10.1016/j.jalz.2011.03.008. PMC 3312027. PMID 21514249.
- ^ a b c d Chertkow H, Feldman HH, Jacova C, Massoud F (July 2013). "Definitions of dementia and predementia states in Alzheimer's disease and vascular cognitive impairment: consensus from the Canadian conference on diagnosis of dementia". Alzheimer's Research & Therapy. BMC. 5 (Suppl 1): S2. doi:10.1186/alzrt198. PMC 3981054. PMID 24565215.
- ^ a b c Papadakis MA, McPhee SJ, Rabow MW (2021). Current medical diagnosis & treatment (Sixtieth ed.). New York: McGraw Hill. p. 1760. ISBN 978-1-260-46986-8. OCLC 1195972209.
- ^ Tombaugh TN, McIntyre NJ (September 1992). "The mini-mental state examination: a comprehensive review". Journal of the American Geriatrics Society. 40 (9): 922–935. doi:10.1111/j.1532-5415.1992.tb01992.x. PMID 1512391. S2CID 25169596.
- ^ Pasquier F (January 1999). "Early diagnosis of dementia: neuropsychology". Journal of Neurology. 246 (1): 6–15. doi:10.1007/s004150050299. PMID 9987708. S2CID 2108587.
- ^ Harvey PD, Moriarty PJ, Kleinman L, Coyne K, Sadowsky CH, Chen M, Mirski DF (2005). "The validation of a caregiver assessment of dementia: the Dementia Severity Scale". Alzheimer Disease and Associated Disorders. 19 (4): 186–194. doi:10.1097/01.wad.0000189034.43203.60. PMID 16327345. S2CID 20238911.
- ^ Antoine C, Antoine P, Guermonprez P, Frigard B (2004). "[Awareness of deficits and anosognosia in Alzheimer's disease]". L'Encéphale (in French). 30 (6): 570–577. doi:10.1016/S0013-7006(04)95472-3. PMID 15738860.
- ^ Cruz VT, Pais J, Teixeira A, Nunes B (2004). "[The initial symptoms of Alzheimer disease: caregiver perception]". Acta Médica Portuguesa (in Portuguese). 17 (6): 435–444. PMID 16197855.
- ^ a b c Stern SD (2020). Symptom to diagnosis: an evidence-based guide. Adam S. Cifu, Diane Altkorn (4th ed.). [New York]. pp. 209–210. ISBN 978-1260121117. OCLC 1121597721.
{{cite book}}: CS1 maint: 위치 누락 게시자(링크) - ^ Jha A, Mukhopadhaya K (2021). Alzheimer's disease: diagnosis and treatment guide. Cham, Switzerland: Springer. p. 32. ISBN 978-3-030-56739-2. OCLC 1202472277.
- ^ Sun X, Steffens DC, Au R, Folstein M, Summergrad P, Yee J, et al. (May 2008). "Amyloid-associated depression: a prodromal depression of Alzheimer disease?". Archives of General Psychiatry. 65 (5): 542–550. doi:10.1001/archpsyc.65.5.542. PMC 3042807. PMID 18458206.
- ^ Geldmacher DS, Whitehouse PJ (May 1997). "Differential diagnosis of Alzheimer's disease". Neurology. 48 (5 Suppl 6): S2–S9. doi:10.1212/WNL.48.5_Suppl_6.2S. PMID 9153154. S2CID 30018544.
- ^ Potter GG, Steffens DC (May 2007). "Contribution of depression to cognitive impairment and dementia in older adults". The Neurologist. 13 (3): 105–117. doi:10.1097/01.nrl.0000252947.15389.a9. PMID 17495754. S2CID 24569198.
- ^ Zhang S, Smailagic N, Hyde C, Noel-Storr AH, Takwoingi Y, McShane R, Feng J (July 2014). "(11)C-PIB-PET for the early diagnosis of Alzheimer's disease dementia and other dementias in people with mild cognitive impairment (MCI)". The Cochrane Database of Systematic Reviews. 2014 (7): CD010386. doi:10.1002/14651858.CD010386.pub2. PMC 6464750. PMID 25052054.
- ^ Smailagic N, Vacante M, Hyde C, Martin S, Ukoumunne O, Sachpekidis C (January 2015). "18F-FDG PET for the early diagnosis of Alzheimer's disease dementia and other dementias in people with mild cognitive impairment (MCI)". The Cochrane Database of Systematic Reviews. 1 (1): CD010632. doi:10.1002/14651858.CD010632.pub2. PMC 7081123. PMID 25629415.
- ^ Viña J, Sanz-Ros J (October 2018). "Alzheimer's disease: Only prevention makes sense". European Journal of Clinical Investigation. 48 (10): e13005. doi:10.1111/eci.13005. PMID 30028503. S2CID 51703879.
- ^ a b c Hsu D, Marshall GA (2017). "Primary and secondary prevention trials in Alzheimer disease: looking back, moving forward". Curr Alzheimer Res. 14 (4): 426–440. doi:10.2174/1567205013666160930112125. PMC 5329133. PMID 27697063.
- ^ Patterson C, Feightner JW, Garcia A, Hsiung GY, MacKnight C, Sadovnick AD (February 2008). "Diagnosis and treatment of dementia: 1. Risk assessment and primary prevention of Alzheimer disease". CMAJ. 178 (5): 548–556. doi:10.1503/cmaj.070796. PMC 2244657. PMID 18299540.
- ^ Rosendorff C, Beeri MS, Silverman JM (2007). "Cardiovascular risk factors for Alzheimer's disease". The American Journal of Geriatric Cardiology. 16 (3): 143–149. doi:10.1111/j.1076-7460.2007.06696.x. PMID 17483665.
- ^ Chu CS, Tseng PT, Stubbs B, Chen TY, Tang CH, Li DJ, et al. (April 2018). "Use of statins and the risk of dementia and mild cognitive impairment: A systematic review and meta-analysis". Scientific Reports. 8 (1): 5804. Bibcode:2018NatSR...8.5804C. doi:10.1038/s41598-018-24248-8. PMC 5895617. PMID 29643479.
- ^ Ungvari Z, Toth P, Tarantini S, Prodan CI, Sorond F, Merkely B, et al. (October 2021). "Hypertension-induced cognitive impairment: from pathophysiology to public health". Nature Reviews Nephrology. 17 (10): 639–654. doi:10.1038/s41581-021-00430-6. PMC 8202227. PMID 34127835.
- ^ a b c d e f g Yu JT, Xu W, Tan CC, Andrieu S, Suckling J, Evangelou E, et al. (November 2020). "Evidence-based prevention of Alzheimer's disease: systematic review and meta-analysis of 243 observational prospective studies and 153 randomised controlled trials". Journal of Neurology, Neurosurgery, and Psychiatry. 91 (11): 1201–1209. doi:10.1136/jnnp-2019-321913. PMC 7569385. PMID 32690803.
- ^ Lethaby A, Hogervorst E, Richards M, Yesufu A, Yaffe K (January 2008). "Hormone replacement therapy for cognitive function in postmenopausal women". Cochrane Database Syst Rev. 2008 (1): CD003122. doi:10.1002/14651858.CD003122.pub2. PMC 6599876. PMID 18254016.
- ^ Kastenholz B, Garfin DE, Horst J, Nagel KA (2009). "Plant metal chaperones: A novel perspective in dementia therapy". Amyloid. 16 (2): 81–83. doi:10.1080/13506120902879392. PMID 20536399. S2CID 37490474.
- ^ Cheng ST (September 2016). "Cognitive Reserve and the Prevention of Dementia: the Role of Physical and Cognitive Activities". Current Psychiatry Reports (Review). 18 (9): 85. doi:10.1007/s11920-016-0721-2. PMC 4969323. PMID 27481112.
- ^ Farina N, Rusted J, Tabet N (January 2014). "The effect of exercise interventions on cognitive outcome in Alzheimer's disease: a systematic review". International Psychogeriatrics (Review). 26 (1): 9–18. doi:10.1017/S1041610213001385. PMID 23962667. S2CID 24936334.
- ^ Barnard ND, Bush AI, Ceccarelli A, Cooper J, de Jager CA, Erickson KI, et al. (September 2014). "Dietary and lifestyle guidelines for the prevention of Alzheimer's disease". Neurobiology of Aging. 35 (Suppl 2): S74–S78. doi:10.1016/j.neurobiolaging.2014.03.033. PMID 24913896. S2CID 8265377.
- ^ a b Bhatti GK, Reddy AP, Reddy PH, Bhatti JS (2019). "Lifestyle Modifications and Nutritional Interventions in Aging-Associated Cognitive Decline and Alzheimer's Disease". Frontiers in Aging Neuroscience (Review). 11: 369. doi:10.3389/fnagi.2019.00369. PMC 6966236. PMID 31998117.
- ^ López-Ortiz S, Lista S, Valenzuela PL, Pinto-Fraga J, Carmona R, Caraci F, et al. (November 2022). "Effects of physical activity and exercise interventions on Alzheimer's disease: an umbrella review of existing meta-analyses". Journal of Neurology. 270 (2): 711–725. doi:10.1007/s00415-022-11454-8. PMID 36342524. S2CID 253382289.
- ^ a b Viña J, Sanz-Ros J (October 2018). "Alzheimer's disease: Only prevention makes sense". European Journal of Clinical Investigation (Review). 48 (10): e13005. doi:10.1111/eci.13005. PMID 30028503. S2CID 51703879.
- ^ Imtiaz B, Tolppanen AM, Kivipelto M, Soininen H (April 2014). "Future directions in Alzheimer's disease from risk factors to prevention". Biochemical Pharmacology (Review). 88 (4): 661–670. doi:10.1016/j.bcp.2014.01.003. PMID 24418410.
- ^ Imtiaz B, Tolppanen AM, Kivipelto M, Soininen H (April 2014). "Future directions in Alzheimer's disease from risk factors to prevention". Biochem Pharmacol. 88 (4): 661–70. doi:10.1016/j.bcp.2014.01.003. PMID 24418410.
- ^ Kivipelto M, Mangialasche F, Ngandu T (November 2018). "Lifestyle interventions to prevent cognitive impairment, dementia and Alzheimer disease". Nat Rev Neurol. 14 (11): 653–666. doi:10.1038/s41582-018-0070-3. PMID 30291317. S2CID 52925352.
- ^ a b c d Borges CR, Poyares D, Piovezan R, Nitrini R, Brucki S (November 2019). "Alzheimer's disease and sleep disturbances: a review". Arq Neuropsiquiatr. 77 (11): 815–824. doi:10.1590/0004-282X20190149. PMID 31826138. S2CID 209327994.
- ^ a b Uddin MS, Tewari D, Mamun AA, Kabir MT, Niaz K, Wahed MI, et al. (July 2020). "Circadian and sleep dysfunction in Alzheimer's disease". Ageing Research Reviews. 60: 101046. doi:10.1016/j.arr.2020.101046. PMID 32171783. S2CID 212729131.
- ^ Rasmussen MK, Mestre H, Nedergaard M (November 2018). "The glymphatic pathway in neurological disorders". Lancet Neurol. 17 (11): 1016–1024. doi:10.1016/S1474-4422(18)30318-1. PMC 6261373. PMID 30353860.
- ^ Irwin MR, Vitiello MV (March 2019). "Implications of sleep disturbance and inflammation for Alzheimer's disease dementia". Lancet Neurol. 18 (3): 296–306. doi:10.1016/S1474-4422(18)30450-2. PMID 30661858. S2CID 58546748.
- ^ Hampel H, Vergallo A, Aguilar LF, Benda N, Broich K, Cuello AC, et al. (April 2018). "Precision pharmacology for Alzheimer's disease". Pharmacological Research. 130: 331–365. doi:10.1016/j.phrs.2018.02.014. PMC 8505114. PMID 29458203.
- ^ Chen Y, Zhang J, Zhang T, Cao L, You Y, Zhang C, et al. (March 2020). "Meditation treatment of Alzheimer disease and mild cognitive impairment: A protocol for systematic review". Medicine. 99 (10): e19313. doi:10.1097/MD.0000000000019313. PMC 7478420. PMID 32150066.
- ^ Winkelman, Michael James; Szabo, Attila; Frecska, Ede (1 November 2023). "The potential of psychedelics for the treatment of Alzheimer's disease and related dementias". European Neuropsychopharmacology. 76: 3–16. doi:10.1016/j.euroneuro.2023.07.003. ISSN 0924-977X.
- ^ Drislane F, Hovauimian A, Tarulli A, Boegle AK, McIiduff C, Caplan LR (2019). Blueprints neurology (Fifth ed.). Philadelphia: Wolters Kluwer. p. 146. ISBN 978-1-4963-8739-4. OCLC 1048659425.
- ^ a b c Birks JS, Harvey RJ (June 2018). "Donepezil for dementia due to Alzheimer's disease". The Cochrane Database of Systematic Reviews. 2018 (6): CD001190. doi:10.1002/14651858.CD001190.pub3. PMC 6513124. PMID 29923184.
- ^ Fink HA, Linskens EJ, MacDonald R, Silverman PC, McCarten JR, Talley KM, et al. (May 2020). "Benefits and Harms of Prescription Drugs and Supplements for Treatment of Clinical Alzheimer-Type Dementia". Annals of Internal Medicine. 172 (10): 656–668. doi:10.7326/M19-3887. PMID 32340037. S2CID 216595473.
- ^ Berkowitz A (2017). Clinical neurology and neuroanatomy: a localization-based approach. New York: McGraw Hill. p. 236. ISBN 978-1-259-83440-0. OCLC 948547621.
- ^ Geula C, Mesulam MM (1995). "Cholinesterases and the pathology of Alzheimer disease". Alzheimer Disease and Associated Disorders. 9 (Suppl 2): 23–28. doi:10.1097/00002093-199501002-00005. PMID 8534419.
- ^ Stahl SM (November 2000). "The new cholinesterase inhibitors for Alzheimer's disease, Part 2: illustrating their mechanisms of action". The Journal of Clinical Psychiatry. 61 (11): 813–814. doi:10.4088/JCP.v61n1101. PMID 11105732.
- ^ a b Birks J (January 2006). Birks J (ed.). "Cholinesterase inhibitors for Alzheimer's disease". The Cochrane Database of Systematic Reviews. 2016 (1): CD005593. doi:10.1002/14651858.CD005593. PMC 9006343. PMID 16437532.
- ^ Raschetti R, Albanese E, Vanacore N, Maggini M (November 2007). "Cholinesterase inhibitors in mild cognitive impairment: a systematic review of randomised trials". PLOS Medicine. 4 (11): e338. doi:10.1371/journal.pmed.0040338. PMC 2082649. PMID 18044984.
- ^ Alldredge BK, Corelli RL, Ernst ME, Guglielmo BJ, Jacobson PA, Kradjan WA, et al. (2013). Applied therapeutics : the clinical use of drugs (10th ed.). Baltimore: Wolters Kluwer Health/Lippincott Williams & Wilkins. p. 2385. ISBN 978-1-60913-713-7.
- ^ a b Lipton SA (February 2006). "Paradigm shift in neuroprotection by NMDA receptor blockade: memantine and beyond". Nature Reviews. Drug Discovery. 5 (2): 160–170. doi:10.1038/nrd1958. PMID 16424917. S2CID 21379258.
- ^ "Memantine". US National Library of Medicine (Medline). 4 January 2004. Archived from the original on 22 February 2010. Retrieved 3 February 2010.
- ^ McShane R, Westby MJ, Roberts E, Minakaran N, Schneider L, Farrimond LE, et al. (March 2019). "Memantine for dementia". The Cochrane Database of Systematic Reviews. 3 (3): CD003154. doi:10.1002/14651858.CD003154.pub6. PMC 6425228. PMID 30891742.
- ^ "Namenda- memantine hydrochloride tablet Namenda- memantine hydrochloride kit". DailyMed. 15 November 2018. Archived from the original on 27 January 2022. Retrieved 20 February 2022.
- ^ "Namenda XR- memantine hydrochloride capsule, extended release Namenda XR- memantine hydrochloride kit". DailyMed. 15 November 2019. Archived from the original on 21 February 2022. Retrieved 20 February 2022.
- ^ "Namzaric- memantine hydrochloride and donepezil hydrochloride capsule Namzaric- memantine hydrochloride and donepezil hydrochloride kit". DailyMed. 22 January 2019. Archived from the original on 20 January 2022. Retrieved 20 February 2022.
- ^ Raina P, Santaguida P, Ismaila A, Patterson C, Cowan D, Levine M, et al. (March 2008). "Effectiveness of cholinesterase inhibitors and memantine for treating dementia: evidence review for a clinical practice guideline". Annals of Internal Medicine. 148 (5): 379–397. doi:10.7326/0003-4819-148-5-200803040-00009. PMID 18316756. S2CID 22235353.
- ^ a b Kandiah N, Ong PA, Yuda T, Ng LL, Mamun K, Merchant RA, et al. (February 2019). "Treatment of dementia and mild cognitive impairment with or without cerebrovascular disease: Expert consensus on the use of Ginkgo biloba extract, EGb 761". CNS Neuroscience & Therapeutics. 25 (2): 288–298. doi:10.1111/cns.13095. PMC 6488894. PMID 30648358.
- ^ McKeage K, Lyseng-Williamson KA (2018). "Ginkgo biloba extract EGb 761 in the symptomatic treatment of mild-to-moderate dementia: a profile of its use". Drugs & Therapy Perspectives. 34 (8): 358–366. doi:10.1007/s40267-018-0537-8. PMC 6267544. PMID 30546253.
- ^ Yang G, Wang Y, Sun J, Zhang K, Liu J (22 October 2015). "Ginkgo Biloba for Mild Cognitive Impairment and Alzheimer's Disease: A Systematic Review and Meta-Analysis of Randomized Controlled Trials". Current Topics in Medicinal Chemistry. 16 (5): 520–528. doi:10.2174/1568026615666150813143520. PMID 26268332.
- ^ Ballard C, Waite J (January 2006). Ballard CG (ed.). "The effectiveness of atypical antipsychotics for the treatment of aggression and psychosis in Alzheimer's disease". The Cochrane Database of Systematic Reviews (1): CD003476. doi:10.1002/14651858.CD003476.pub2. PMID 16437455.
- ^ Ballard C, Hanney ML, Theodoulou M, Douglas S, McShane R, Kossakowski K, et al. (February 2009). "The dementia antipsychotic withdrawal trial (DART-AD): long-term follow-up of a randomised placebo-controlled trial". The Lancet. Neurology. 8 (2): 151–157. doi:10.1016/S1474-4422(08)70295-3. PMID 19138567. S2CID 23000439. 2009년 1월 요약을 참조하십시오.
- ^ Declercq T, Petrovic M, Azermai M, Vander Stichele R, De Sutter AI, van Driel ML, Christiaens T (March 2013). "Withdrawal versus continuation of chronic antipsychotic drugs for behavioural and psychological symptoms in older people with dementia". The Cochrane Database of Systematic Reviews. 3 (3): CD007726. doi:10.1002/14651858.CD007726.pub2. hdl:1854/LU-3109108. PMID 23543555.
- ^ a b c d e [needs 업데이트] Rabins PV, Blacker D, Rovner BW, Rummans T, Schneider LS, Tariot PN, et al. (Steering Committee on Practice Guidelines) (December 2007). "American Psychiatric Association practice guideline for the treatment of patients with Alzheimer's disease and other dementias. Second edition". The American Journal of Psychiatry. 164 (12 Suppl): 5–56. PMID 18340692.
- ^ Bottino CM, Carvalho IA, Alvarez AM, Avila R, Zukauskas PR, Bustamante SE, et al. (December 2005). "Cognitive rehabilitation combined with drug treatment in Alzheimer's disease patients: a pilot study". Clinical Rehabilitation. 19 (8): 861–869. doi:10.1191/0269215505cr911oa. PMID 16323385. S2CID 21290731.
- ^ Doody RS, Stevens JC, Beck C, Dubinsky RM, Kaye JA, Gwyther L, et al. (May 2001). "Practice parameter: management of dementia (an evidence-based review). Report of the Quality Standards Subcommittee of the American Academy of Neurology". Neurology. 56 (9): 1154–1166. doi:10.1212/WNL.56.9.1154. PMID 11342679. S2CID 10711725.
- ^ Hermans DG, Htay UH, McShane R (January 2007). "Non-pharmacological interventions for wandering of people with dementia in the domestic setting". The Cochrane Database of Systematic Reviews. 2010 (1): CD005994. doi:10.1002/14651858.CD005994.pub2. PMC 6669244. PMID 17253573.
- ^ Robinson L, Hutchings D, Dickinson HO, Corner L, Beyer F, Finch T, et al. (January 2007). "Effectiveness and acceptability of non-pharmacological interventions to reduce wandering in dementia: a systematic review". International Journal of Geriatric Psychiatry. 22 (1): 9–22. doi:10.1002/gps.1643. PMID 17096455. S2CID 45660235.
- ^ Abraha I, Rimland JM, Trotta FM, Dell'Aquila G, Cruz-Jentoft A, Petrovic M, et al. (March 2017). "Systematic review of systematic reviews of non-pharmacological interventions to treat behavioural disturbances in older patients with dementia. The SENATOR-OnTop series". BMJ Open. 7 (3): e012759. doi:10.1136/bmjopen-2016-012759. PMC 5372076. PMID 28302633.
- ^ Chung JC, Lai CK, Chung PM, French HP (2002). "Snoezelen for dementia". The Cochrane Database of Systematic Reviews. 2010 (4): CD003152. doi:10.1002/14651858.CD003152. PMC 9002239. PMID 12519587.
- ^ Woods B, O'Philbin L, Farrell EM, Spector AE, Orrell M (March 2018). "Reminiscence therapy for dementia". The Cochrane Database of Systematic Reviews. 2018 (3): CD001120. doi:10.1002/14651858.CD001120.pub3. PMC 6494367. PMID 29493789.
- ^ Zetteler J (November 2008). "Effectiveness of simulated presence therapy for individuals with dementia: a systematic review and meta-analysis". Aging & Mental Health. 12 (6): 779–785. doi:10.1080/13607860802380631. PMID 19023729. S2CID 39529938.
- ^ Spector A, Thorgrimsen L, Woods B, Royan L, Davies S, Butterworth M, Orrell M (September 2003). "Efficacy of an evidence-based cognitive stimulation therapy programme for people with dementia: randomised controlled trial". The British Journal of Psychiatry. 183 (3): 248–254. doi:10.1192/bjp.183.3.248. PMID 12948999.
- ^ Gitlin LN, Corcoran M, Winter L, Boyce A, Hauck WW (February 2001). "A randomized, controlled trial of a home environmental intervention: effect on efficacy and upset in caregivers and on daily function of persons with dementia". The Gerontologist. 41 (1): 4–14. doi:10.1093/geront/41.1.4. PMID 11220813.
- ^ Gitlin LN, Hauck WW, Dennis MP, Winter L (March 2005). "Maintenance of effects of the home environmental skill-building program for family caregivers and individuals with Alzheimer's disease and related disorders". The Journals of Gerontology. Series A, Biological Sciences and Medical Sciences. 60 (3): 368–374. doi:10.1093/gerona/60.3.368. PMID 15860476.
- ^ "Treating Behavioral and Psychiatric Symptoms". Alzheimer's Association. 2006. Archived from the original on 25 September 2006. Retrieved 25 September 2006.
- ^ Dunne TE, Neargarder SA, Cipolloni PB, Cronin-Golomb A (August 2004). "Visual contrast enhances food and liquid intake in advanced Alzheimer's disease". Clinical Nutrition. 23 (4): 533–538. doi:10.1016/j.clnu.2003.09.015. PMID 15297089.
- ^ Dudek SB (2007). Nutrition Essentials for Nursing Practice. Hagerstown, Maryland: Lippincott Williams & Wilkins. p. 360. ISBN 978-0-7817-6651-7. Retrieved 19 August 2008.
- ^ Dennehy C (2006). "Analysis of patients' rights: dementia and PEG insertion". British Journal of Nursing. 15 (1): 18–20. doi:10.12968/bjon.2006.15.1.20303. PMID 16415742.
- ^ Chernoff R (April 2006). "Tube feeding patients with dementia". Nutrition in Clinical Practice. 21 (2): 142–146. doi:10.1177/0115426506021002142. PMID 16556924. S2CID 20841502.
- ^ Shega JW, Levin A, Hougham GW, Cox-Hayley D, Luchins D, Hanrahan P, et al. (April 2003). "Palliative Excellence in Alzheimer Care Efforts (PEACE): a program description". Journal of Palliative Medicine. 6 (2): 315–320. doi:10.1089/109662103764978641. PMID 12854952. S2CID 6072807.
- ^ a b Dominguez LJ, Barbagallo M (June 2018). "Nutritional prevention of cognitive decline and dementia". Acta Bio-Medica. 89 (2): 276–290. doi:10.23750/abm.v89i2.7401. PMC 6179018. PMID 29957766.
- ^ a b Zanetti O, Solerte SB, Cantoni F (2009). "Life expectancy in Alzheimer's disease (AD)". Archives of Gerontology and Geriatrics. 49 (Suppl 1): 237–243. doi:10.1016/j.archger.2009.09.035. PMID 19836639.
- ^ "United States Life Tables, 2017" (PDF). National Vital Statistics Reports, CDC. Archived (PDF) from the original on 24 May 2021. Retrieved 10 June 2021.
- ^ a b Mölsä PK, Marttila RJ, Rinne UK (March 1995). "Long-term survival and predictors of mortality in Alzheimer's disease and multi-infarct dementia". Acta Neurologica Scandinavica. 91 (3): 159–164. doi:10.1111/j.1600-0404.1995.tb00426.x. PMID 7793228. S2CID 19724937.
- ^ Bowen JD, Malter AD, Sheppard L, Kukull WA, McCormick WC, Teri L, Larson EB (August 1996). "Predictors of mortality in patients diagnosed with probable Alzheimer's disease". Neurology. 47 (2): 433–439. doi:10.1212/wnl.47.2.433. PMID 8757016. S2CID 24961809.
- ^ Larson EB, Shadlen MF, Wang L, McCormick WC, Bowen JD, Teri L, Kukull WA (April 2004). "Survival after initial diagnosis of Alzheimer disease". Annals of Internal Medicine. 140 (7): 501–509. doi:10.7326/0003-4819-140-7-200404060-00008. PMID 15068977. S2CID 27410149.
- ^ Jagger C, Clarke M, Stone A (January 1995). "Predictors of survival with Alzheimer's disease: a community-based study". Psychological Medicine. 25 (1): 171–177. doi:10.1017/S0033291700028191. PMID 7792352. S2CID 34066330.
- ^ Dodge HH, Shen C, Pandav R, DeKosky ST, Ganguli M (February 2003). "Functional transitions and active life expectancy associated with Alzheimer disease". Archives of Neurology. 60 (2): 253–259. doi:10.1001/archneur.60.2.253. PMID 12580712.
- ^ a b Bermejo-Pareja F, Benito-León J, Vega S, Medrano MJ, Román GC (January 2008). "Incidence and subtypes of dementia in three elderly populations of central Spain". Journal of the Neurological Sciences. 264 (1–2): 63–72. doi:10.1016/j.jns.2007.07.021. PMID 17727890. S2CID 34341344.
- ^ a b Di Carlo A, Baldereschi M, Amaducci L, Lepore V, Bracco L, Maggi S, et al. (January 2002). "Incidence of dementia, Alzheimer's disease, and vascular dementia in Italy. The ILSA Study". Journal of the American Geriatrics Society. 50 (1): 41–48. doi:10.1046/j.1532-5415.2002.50006.x. PMID 12028245. S2CID 22576935.
- ^ Tejada-Vera B. (2013). 미국 알츠하이머병 사망률: 2000년과 2010년의 데이터. 하이츠빌, MD: 미국 보건복지부, 질병통제예방센터, 국립보건통계센터.
- ^ Reitz C, Rogaeva E, Beecham GW (October 2020). "Late-onset vs nonmendelian early-onset Alzheimer disease: A distinction without a difference?". Neurology. Genetics. 6 (5): e512. doi:10.1212/NXG.0000000000000512. PMC 7673282. PMID 33225065.
- ^ a b Liu CC, Liu CC, Kanekiyo T, Xu H, Bu G (February 2013). "Apolipoprotein E and Alzheimer disease: risk, mechanisms and therapy". Nature Reviews. Neurology. 9 (2): 106–118. doi:10.1038/nrneurol.2012.263. PMC 3726719. PMID 23296339.
- ^ Massett HA, Mitchell AK, Alley L, Simoneau E, Burke P, Han SH, et al. (29 June 2021). "Facilitators, Challenges, and Messaging Strategies for Hispanic/Latino Populations Participating in Alzheimer's Disease and Related Dementias Clinical Research: A Literature Review". Journal of Alzheimer's Disease. 82 (1): 107–127. doi:10.3233/JAD-201463. PMID 33998537. S2CID 234745473.
- ^ Huynh RA, Mohan C (2017). "Alzheimer's Disease: Biomarkers in the Genome, Blood, and Cerebrospinal Fluid". Frontiers in Neurology. 8: 102. doi:10.3389/fneur.2017.00102. PMC 5357660. PMID 28373857.
- ^ Rajan KB, Weuve J, Barnes LL, McAninch EA, Wilson RS, Evans DA (May 2021). "Population estimate of people with clinical Alzheimer's disease and mild cognitive impairment in the United States (2020-2060)". Alzheimer's & Dementia. 17 (12): 1966–1975. doi:10.1002/alz.12362. PMC 9013315. PMID 34043283. S2CID 235215290.
- ^ Rizzi L, Rosset I, Roriz-Cruz M (2014). "Global epidemiology of dementia: Alzheimer's and vascular types". Biomed Res Int. 2014: 908915. doi:10.1155/2014/908915. PMC 4095986. PMID 25089278.
- ^ Ferri CP, Prince M, Brayne C, Brodaty H, Fratiglioni L, Ganguli M, et al. (December 2005). "Global prevalence of dementia: a Delphi consensus study". Lancet. 366 (9503): 2112–2117. doi:10.1016/S0140-6736(05)67889-0. PMC 2850264. PMID 16360788.
- ^ Li F, Qin W, Zhu M, Jia J (1 January 2021). "Model-Based Projection of Dementia Prevalence in China and Worldwide: 2020-2050". Journal of Alzheimer's Disease. IOS Press. 82 (4): 1823–1831. doi:10.3233/JAD-210493. PMID 34219732. S2CID 235735045.
- ^ 오거스트 D.
- Alzheimer A (1907). "Über eine eigenartige Erkrankung der Hirnrinde" [About a peculiar disease of the cerebral cortex]. Allgemeine Zeitschrift für Psychiatrie und Psychisch-Gerichtlich Medizin (in German). 64 (1–2): 146–148.
- Translated by H. Greenson. "About a peculiar disease of the cerebral cortex. By Alois Alzheimer, 1907 (Translated by L. Jarvik and H. Greenson)". Alzheimer Disease and Associated Disorders. 1 (1): 3–8. 1987. PMID 3331112.
- Maurer U, Maurer K (2003). Alzheimer: The Life of a Physician and the Career of a Disease. New York: Columbia University Press. p. 270. ISBN 978-0-231-11896-5.
- ^ Berrios GE (1990). "Alzheimer's Disease: A Conceptual History". Int. J. Geriatr. Psychiatry. 5 (6): 355–365. doi:10.1002/gps.930050603. S2CID 145155424.
- ^ Kraepelin E (2007). Clinical Psychiatry: A Textbook For Students And Physicians (Reprint). Translated by Diefendorf AR. Kessinger Publishing. p. 568. ISBN 978-1-4325-0833-3.
- ^ Katzman R, Terry RD, Bick KL, eds. (1978). Alzheimer's Disease: Senile Dementia and Related Disorders. New York: Raven Press. p. 595. ISBN 978-0-89004-225-0.
- ^ Boller F, Forbes MM (June 1998). "History of dementia and dementia in history: an overview". Journal of the Neurological Sciences. 158 (2): 125–133. doi:10.1016/S0022-510X(98)00128-2. PMID 9702682. S2CID 42399340.
- ^ Amaducci LA, Rocca WA, Schoenberg BS (November 1986). "Origin of the distinction between Alzheimer's disease and senile dementia: how history can clarify nosology". Neurology. 36 (11): 1497–1499. doi:10.1212/wnl.36.11.1497. PMID 3531918. S2CID 7689479.
- ^ McKhann G, Drachman D, Folstein M, Katzman R, Price D, Stadlan EM (July 1984). "Clinical diagnosis of Alzheimer's disease: report of the NINCDS-ADRDA Work Group under the auspices of Department of Health and Human Services Task Force on Alzheimer's Disease". Neurology. 34 (7): 939–944. doi:10.1212/wnl.34.7.939. PMID 6610841. S2CID 11646075.
- ^ Dubois B, Feldman HH, Jacova C, Dekosky ST, Barberger-Gateau P, Cummings J, et al. (August 2007). "Research criteria for the diagnosis of Alzheimer's disease: revising the NINCDS-ADRDA criteria". The Lancet. Neurology. 6 (8): 734–746. doi:10.1016/S1474-4422(07)70178-3. PMID 17616482. S2CID 7356809.
- ^ Blacker D, Albert MS, Bassett SS, Go RC, Harrell LE, Folstein MF (December 1994). "Reliability and validity of NINCDS-ADRDA criteria for Alzheimer's disease. The National Institute of Mental Health Genetics Initiative". Archives of Neurology. 51 (12): 1198–1204. doi:10.1001/archneur.1994.00540240042014. PMID 7986174.
- ^ a b c d El-Hayek YH, Wiley RE, Khoury CP, Daya RP, Ballard C, Evans AR, et al. (2019). "Tip of the Iceberg: Assessing the Global Socioeconomic Costs of Alzheimer's Disease and Related Dementias and Strategic Implications for Stakeholders". Journal of Alzheimer's Disease. 70 (2): 323–341. doi:10.3233/JAD-190426. PMC 6700654. PMID 31256142.
- ^ a b c Wong W (August 2020). "Economic burden of Alzheimer disease and managed care considerations". Am J Manag Care. 26 (8 Suppl): S177–S183. doi:10.37765/ajmc.2020.88482. PMID 32840331. S2CID 221308149. Archived from the original on 25 February 2022. Retrieved 17 March 2022.
- ^ a b Tahami Monfared AA, Byrnes MJ, White LA, Zhang Q (February 2022). "The Humanistic and Economic Burden of Alzheimer's Disease". Neurol Ther. 11 (2): 525–551. doi:10.1007/s40120-022-00335-x. PMC 9095804. PMID 35192176. S2CID 247014076.
- ^ a b Kosaner Kließ M, Martins R, Connolly MP (2021). "Major Cost Drivers in Assessing the Economic Burden of Alzheimer's Disease: A Structured, Rapid Review". J Prev Alzheimers Dis. 8 (3): 362–370. doi:10.14283/jpad.2021.17. PMID 34101795. S2CID 233403683.
- ^ Demirbas M, Hahn-Pedersen JH, Jørgensen HL (August 2023). "Comparison Between Burden of Care Partners of Individuals with Alzheimer's Disease Versus Individuals with Other Chronic Diseases". Neurology and Therapy. 12 (4): 1051–1068. doi:10.1007/s40120-023-00493-6. PMC 10310688. PMID 37222859.
- ^ a b "The MetLife study of Alzheimer's disease: The caregiving experience" (PDF). MetLife Mature Market Institute. August 2006. Archived from the original (PDF) on 8 January 2011. Retrieved 5 February 2011.
- ^ Schneider J, Murray J, Banerjee S, Mann A (August 1999). "EUROCARE: a cross-national study of co-resident spouse carers for people with Alzheimer's disease: I—Factors associated with carer burden". International Journal of Geriatric Psychiatry. 14 (8): 651–661. doi:10.1002/(SICI)1099-1166(199908)14:8<651::AID-GPS992>3.0.CO;2-B. PMID 10489656. S2CID 27346798.
- ^ Murray J, Schneider J, Banerjee S, Mann A (August 1999). "EUROCARE: a cross-national study of co-resident spouse carers for people with Alzheimer's disease: II—A qualitative analysis of the experience of caregiving". International Journal of Geriatric Psychiatry. 14 (8): 662–667. doi:10.1002/(SICI)1099-1166(199908)14:8<662::AID-GPS993>3.0.CO;2-4. PMID 10489657. S2CID 41741923.
- ^ a b Zhu CW, Sano M (2006). "Economic considerations in the management of Alzheimer's disease". Clinical Interventions in Aging. 1 (2): 143–154. doi:10.2147/ciia.2006.1.2.143. PMC 2695165. PMID 18044111.
- ^ Gaugler JE, Kane RL, Kane RA, Newcomer R (April 2005). "Early community-based service utilization and its effects on institutionalization in dementia caregiving". The Gerontologist. 45 (2): 177–185. doi:10.1093/geront/45.2.177. PMID 15799982.
- ^ Ritchie K, Lovestone S (November 2002). "The dementias". Lancet. 360 (9347): 1759–1766. doi:10.1016/S0140-6736(02)11667-9. PMID 12480441. S2CID 21404062.
- ^ Brodaty H, Hadzi-Pavlovic D (September 1990). "Psychosocial effects on carers of living with persons with dementia". The Australian and New Zealand Journal of Psychiatry. 24 (3): 351–361. doi:10.3109/00048679009077702. PMID 2241719. S2CID 11788466.
- ^ Donaldson C, Tarrier N, Burns A (April 1998). "Determinants of carer stress in Alzheimer's disease". International Journal of Geriatric Psychiatry. 13 (4): 248–256. doi:10.1002/(SICI)1099-1166(199804)13:4<248::AID-GPS770>3.0.CO;2-0. PMID 9646153. S2CID 22187694.
- ^ Moore MJ, Zhu CW, Clipp EC (July 2001). "Informal costs of dementia care: estimates from the National Longitudinal Caregiver Study". The Journals of Gerontology. Series B, Psychological Sciences and Social Sciences. 56 (4): S219–S228. doi:10.1093/geronb/56.4.S219. PMID 11445614.
- ^ Pusey H, Richards D (May 2001). "A systematic review of the effectiveness of psychosocial interventions for carers of people with dementia". Aging & Mental Health. 5 (2): 107–119. doi:10.1080/13607860120038302. PMID 11511058. S2CID 32517015.
- ^ Bayley J (2000). Iris: A Memoir of Iris Murdoch. London: Abacus. ISBN 978-0-349-11215-2. OCLC 41960006.
- ^ Sparks N (1996). The notebook. Thorndike, Maine: Thorndike Press. p. 268. ISBN 978-0-7862-0821-0.
- ^ "Thanmathra". Webindia123.com. Archived from the original on 6 November 2007. Retrieved 24 January 2008.
- ^ Ogiwara H (2004). Ashita no Kioku (in Japanese). Tōkyō: Kōbunsha. ISBN 978-4-334-92446-1. OCLC 57352130.
- ^ Munro A (2001). Hateship, Friendship, Courtship, Loveship, Marriage: Stories. New York: A.A. Knopf. ISBN 978-0-375-41300-1. OCLC 46929223.
- ^ "Malcolm and Barbara: A love story". Dfgdocs. Archived from the original on 24 May 2008. Retrieved 24 January 2008.
- ^ "Malcolm and Barbara: A love story". BBC Cambridgeshire. Archived from the original on 10 November 2012. Retrieved 2 March 2008.
- ^ Plunkett J (7 August 2007). "Alzheimer's film-maker to face ITV lawyers". London: Guardian Media. Archived from the original on 15 January 2008. Retrieved 24 January 2008.
- ^ "The Caretaker: Persistent Repetition of Phrases". Fact. 26 August 2009. Archived from the original on 15 April 2021. Retrieved 9 April 2021.
- ^ Powell M (14 June 2011). "The Caretaker: An Empty Bliss Beyond This World Album Review". Pitchfork. Archived from the original on 18 June 2011. Retrieved 19 February 2021.
- ^ Ezra M (23 October 2020). "Why Are TikTok Teens Listening to an Album About Dementia?". The New York Times. Archived from the original on 23 October 2020. Retrieved 21 April 2021.
- ^ Gerrard N (19 July 2015). "Words fail us: dementia and the arts". The Guardian. Archived from the original on 19 July 2015. Retrieved 14 June 2021.
- ^ Grady D (24 October 2006). "Self-Portraits Chronicle a Descent Into Alzheimer's". The New York Times. Archived from the original on 24 October 2006. Retrieved 14 June 2021.
- ^ Arenaza-Urquijo EM, Wirth M, Chételat G (10 August 2015). "Cognitive reserve and lifestyle: moving towards preclinical Alzheimer's disease". Frontiers in Aging Neuroscience. 7: 134. doi:10.3389/fnagi.2015.00134. PMC 4530312. PMID 26321944.
- ^ Heppner FL, Ransohoff RM, Becher B (June 2015). "Immune attack: the role of inflammation in Alzheimer disease". Nature Reviews. Neuroscience. 16 (6): 358–372. doi:10.1038/nrn3880. PMID 25991443. S2CID 6116253.
- ^ Rajendran L, Paolicelli RC (March 2018). "Microglia-Mediated Synapse Loss in Alzheimer's Disease". The Journal of Neuroscience. 38 (12): 2911–2919. doi:10.1523/JNEUROSCI.1136-17.2017. PMC 6596066. PMID 29563239.
- ^ Schafer DP, Lehrman EK, Kautzman AG, Koyama R, Mardinly AR, Yamasaki R, et al. (May 2012). "Microglia sculpt postnatal neural circuits in an activity and complement-dependent manner". Neuron. 74 (4): 691–705. doi:10.1016/j.neuron.2012.03.026. PMC 3528177. PMID 22632727.
- ^ Carpanini SM, Torvell M, Bevan RJ, Byrne RA, Daskoulidou N, Saito T, et al. (July 2022). "Terminal complement pathway activation drives synaptic loss in Alzheimer's disease models". Acta Neuropathologica Communications. 10 (1): 99. doi:10.1186/s40478-022-01404-w. PMC 9258209. PMID 35794654.
- ^ Shi M, Chu F, Zhu F, Zhu J (2022). "Impact of Anti-amyloid-β Monoclonal Antibodies on the Pathology and Clinical Profile of Alzheimer's Disease: A Focus on Aducanumab and Lecanemab". Frontiers in Aging Neuroscience. 14: 870517. doi:10.3389/fnagi.2022.870517. PMC 9039457. PMID 35493943.
- ^ Cummings J, Zhou Y, Lee G, Zhong K, Fonseca J, Cheng F (2023). "Alzheimer's disease drug development pipeline: 2023". Alzheimer's & Dementia. 9 (2): e12385. doi:10.1002/trc2.12385. PMC 10210334. PMID 37251912.
- ^ "How Is Alzheimer's Disease Treated?". U.S. National Institute on Aging. 1 April 2023. Retrieved 10 July 2023.
- ^ Vaz M, Silva V, Monteiro C, Silvestre S (2022). "Role of Aducanumab in the Treatment of Alzheimer's Disease: Challenges and Opportunities". Clin Interv Aging. 17: 797–810. doi:10.2147/CIA.S325026. PMC 9124475. PMID 35611326.
- ^ Day GS, Scarmeas N, Dubinsky R, Coerver K, Mostacero A, West B, et al. (April 2022). "Aducanumab Use in Symptomatic Alzheimer Disease Evidence in Focus: A Report of the AAN Guidelines Subcommittee". Neurology. 98 (15): 619–631. doi:10.1212/wnl.0000000000200176. PMC 9012273. PMID 35197360.
- ^ Mahase E (June 2021). "Three FDA advisory panel members resign over approval of Alzheimer's drug". BMJ. 373: n1503. doi:10.1136/bmj.n1503. PMID 34117086. S2CID 235405355. Archived from the original on 8 July 2023. Retrieved 7 July 2023.
- ^ Belluck P, Robbins R (10 June 2021). "Three F.D.A. Advisers Resign Over Agency's Approval of Alzheimer's Drug". The New York Times. Archived from the original on 14 November 2021. Retrieved 7 July 2023.
- ^ Abyadeh M, Gupta V, Gupta V, Chitranshi N, Wu Y, Amirkhani A, et al. (December 2021). "Comparative Analysis of Aducanumab, Zagotenemab and Pioglitazone as Targeted Treatment Strategies for Alzheimer's Disease". Aging and Disease. 12 (8): 1964–1976. doi:10.14336/AD.2021.0719. PMC 8612603. PMID 34881080.
- ^ Marsool MDM, Prajjwal P, Reddy YB, Marsool ADM, Lam JR, Nandwana V (May 2023). "Newer modalities in the management of Alzheimer's dementia along with the role of aducanumab and lecanemab in the treatment of its refractory cases". Disease-a-Month. 69 (5): 101547. doi:10.1016/j.disamonth.2023.101547. PMID 36931947. S2CID 257568052.
- ^ "FDA Grants Accelerated Approval for Alzheimer's Disease Treatment" (Press release). U.S. Food and Drug Administration (FDA). 6 January 2023. Archived from the original on 7 January 2023. Retrieved 7 January 2023.
 이 문서는 공용 도메인에 있는 이 소스의 텍스트를 통합합니다.
이 문서는 공용 도메인에 있는 이 소스의 텍스트를 통합합니다. - ^ "Lecanemab Summary Review" (PDF). U.S. Food and Drug Administration (FDA). Archived (PDF) from the original on 7 January 2023. Retrieved 7 January 2023.
- ^ "FDA Converts Novel Alzheimer's Disease Treatment to Traditional Approval". U.S. Food and Drug Administration (FDA) (Press release). 6 July 2023. Retrieved 6 July 2023.
 이 문서는 공용 도메인에 있는 이 소스의 텍스트를 통합합니다.
이 문서는 공용 도메인에 있는 이 소스의 텍스트를 통합합니다. - ^ "FDA Makes Alzheimer's Drug Leqembi Widely Accessible". The New York Times. 6 July 2023. Archived from the original on 7 July 2023. Retrieved 8 July 2023.
- ^ Alves, Francesca; Kalinowski, Pawel; Ayton, Scott (16 May 2023). "Accelerated Brain Volume Loss Caused by Anti–β-Amyloid Drugs: A Systematic Review and Meta-analysis". Neurology. 100 (20): e2114–e2124. doi:10.1212/WNL.0000000000207156. ISSN 0028-3878. PMC 10186239. PMID 36973044.
- ^ a b McDade E, Llibre-Guerra JJ, Holtzman DM, Morris JC, Bateman RJ (July 2021). "The informed road map to prevention of Alzheimer Disease: A call to arms". Mol Neurodegener. 16 (1): 49. doi:10.1186/s13024-021-00467-y. PMC 8293489. PMID 34289882.
- ^ Lemche E (November 2018). "Early Life Stress and Epigenetics in Late-onset Alzheimer's Dementia: A Systematic Review". Curr Genomics. 19 (7): 522–602. doi:10.2174/1389202919666171229145156. PMC 6194433. PMID 30386171.
- ^ Galle SA, Geraedts IK, Deijen JB, Milders MV, Drent ML (2020). "The Interrelationship between Insulin-Like Growth Factor 1, Apolipoprotein E ε4, Lifestyle Factors, and the Aging Body and Brain". J Prev Alzheimers Dis. 7 (4): 265–273. doi:10.14283/jpad.2020.11. PMID 32920629. S2CID 214784366.
- ^ Li Q, Yang X, Xu J, Guo Y, He X, Hu H, et al. (February 2023). "Early prediction of Alzheimer's disease and related dementias using real-world electronic health records". Alzheimer's & Dementia. 19 (8): 3506–3518. doi:10.1002/alz.12967. PMID 36815661. S2CID 257101613.
더보기
- Van Acker ZP, Perdok A, Bretou M, Annaert W (November 2021). "The microglial lysosomal system in Alzheimer's disease: Guardian against proteinopathy". Ageing Research Reviews. 71: 101444. doi:10.1016/j.arr.2021.101444. PMID 34391945. S2CID 236994329.
- Xi Y, Chen Y, Jin Y, Han G, Song M, Song T, et al. (May 2022). "Versatile nanomaterials for Alzheimer's disease: Pathogenesis inspired disease-modifying therapy". Journal of Controlled Release. 345: 38–61. doi:10.1016/j.jconrel.2022.02.034. PMID 35257810. S2CID 247285338.
외부 링크
- "Alzheimer's Disease Research Timeline – Alzforum". www.alzforum.org.
- "Alzheimer's Disease Brain Cell Atlas- brain-map.org". portal.brain-map.org.