유전성 경련성 하반신 마비
Hereditary spastic paraplegia| 유전성 경련성 하반신 마비 | |
|---|---|
| 전문 | 신경학 |
유전성 경련성 하반신마비(HSP)는 진행성 보행장애가 주요 특징인 유전 질환 그룹이다.그 병은 진행성 경직(경련성)과 하반신 [1]수축이 동반된다.HSP는 유전성 경련성 하반신 마비, 가족성 경련성 하반신 마비, 프랑스 정착병, 스트럼펠병 또는 스트럼펠-로레인병으로도 알려져 있습니다.그 증상은 척수의 긴 축삭의 기능 장애의 결과이다.영향을 받는 세포는 일차 운동 뉴런이다. 따라서 그 질병은 상부 운동 뉴런 [2]질환이다.HSP는 비록 신체적으로 경련성 이중마비처럼 보이고 행동할 수 있지만 뇌성마비의 한 형태가 아니다.HSP의 기원은 뇌성마비와 다르다.그럼에도 불구하고, 경련성 뇌성마비에서 사용되는 것과 같은 항경련제 중 일부는 때때로 HSP 증상을 치료하기 위해 사용된다.
HSP는 세포를 통한 단백질, 구조 단백질, 세포 유지 단백질, 지질, 그리고 다른 물질들의 수송의 결함으로 인해 발생한다.긴 신경 섬유(축)는 긴 거리가 신경 세포를 이러한 메커니즘의 [3][4]결함에 특히 민감하게 만들기 때문에 영향을 받습니다.
이 병은 1880년 독일의 신경학자 아돌프 스트렘펠에 [5]의해 처음 기술되었다.그것은 1888년 프랑스 [6]의사 모리스 로레인에 의해 더 광범위하게 기술되었다.이 병을 기술하는 데 기여했기 때문에 프랑스어권 국가에서는 여전히 Strümpell-Lorrain 병으로 불린다.유전성 경련성 하반신 마비라는 용어는 1983년 [7]아니타 하딩에 의해 만들어졌다.
징후 및 증상
증상은 상속되는 HSP 유형에 따라 달라집니다.이 질환의 주요 특징은 피라미드형 관로 장애로 인한 하지의 진행성 경련이다.이것은 또한 활발한 반사, 신장 발바닥 반사, 근육 약화, 그리고 다양한 방광 장애를 초래한다.또한 HSP의 주요 증상으로는 보행 이상, 보행 곤란, 발목의 진동감각 저하, 감각 [8]마비 등이 있습니다.HSP를 가진 사람들은 중추신경계와 신경근 장애와 관련된 극심한 피로를 경험할 수 있는데,[9][10][11] 이것은 장애를 일으킬 수 있다.초기 증상은 일반적으로 균형을 잡는 데 어려움을 겪거나 발가락이 뭉개지거나 비틀거리는 것입니다.HSP의 증상은 유아기부터 60세 이상까지 모든 연령에서 시작될 수 있다.만약 증상이 10대 이후에 시작된다면, 경련성 보행 장애는 보통 몇 년에 걸쳐 진행됩니다.지팡이, 보행기, 휠체어가 결국 필요할 수 있지만, 어떤 사람들은 절대 보조 [12]장치가 필요하지 않습니다.장애는 성인의 발병 [13]형태에서 더 빠르게 진행되는 것으로 묘사되어 왔다.
보다 구체적으로, HSP의 상염색체 우성 순수 형태를 가진 환자들은 정상적인 얼굴 및 안구외 움직임을 보인다.나이 든 피험자는 턱이 거칠지만 언어 장애나 삼키는 데 어려움이 없다.상지근육의 긴장감과 힘은 정상입니다.하지에서는 햄스트링, 사두근 및 발목의 근육 긴장도가 높아집니다.약성은 장골, 정강이뼈 전방, 그리고 더 적은 정도로 햄스트링 [13]근육에서 가장 두드러진다.복잡한 형태의 장애에서는 추가적인 증상이 나타난다.여기에는 말초신경장애, 근위축증, 운동실조증, 지적장애, 어증, 간질, 시신경장애, 치매, 난청 또는 언어, 삼키기 또는 [14]호흡에 관한 문제가 포함된다. 뇌전증
아니타[7] 하딩은 HSP를 순수하고 복잡한 형태로 분류했다.순수 HSP는 하지에 경련성을 나타내며, 신경성 방광 장애뿐만 아니라 진동 민감도(완충각) 부족과 관련이 있다.한편, 하지 경련이 추가적인 신경학적 [citation needed]증상과 결합되면 HSP는 복합체로 분류된다.
이 분류는 주관적이며 복합 HSP를 가진 환자들은 때때로 경련성 소뇌실조증, 지적장애(경련성) 또는 백혈구영양증을 [7]가지고 있는 것으로 진단된다.아래 나열된 유전자 중 일부는 이전에 HSP 이외의 다른 질병에서 기술된 적이 있습니다.그러므로, 몇몇 주요 유전자들은 다른 질병 [citation needed]집단들과 겹친다.
발병 연령
과거에 HSP는 조기 소아기부터 시작하여 성인기에 늦게 발병하는 것으로 분류되어 왔다.온셋의 연령은 2세와 [15]40세 전후로 최대 2점이 됩니다.새로운 연구결과는 조기 발병 시 환경 손실이나 휠체어 [15]사용의 필요성 없이 질병 지속시간이 길어질 수 있음을 시사한다.이것은 또한 나중에 발병하는 형태가 더 [13]빠르게 진화한다는 것을 앞에서 기술했다.
원인
HSP는 유전 질환의 집단이다.일반 유전 규칙을 따르고 상염색체 우성, 상염색체 열성 또는 X-연결 열성 방식으로 유전될 수 있습니다.관련된 유전 방식은 그 장애를 유전할 가능성에 직접적인 영향을 미친다.70개 이상의 유전자형이 기술되었으며 50개 이상의 유전자 위치가 이 [16]질환과 연관되어 있다.10개의 유전자가 상염색체 우성 유전으로 확인되었다.이들 중 하나인 SPG4는 유전적으로 해결된 모든 사례의 50% 또는 모든 HSP [15]사례의 약 25%를 차지한다.12개의 유전자가 상염색체 열성 방식으로 유전되는 것으로 알려져 있다.이 후자 그룹은 총 [citation needed]3분의 1까지를 차지한다.
대부분의 변형된 유전자들은 기능을 알고 있지만, 일부 유전자들은 아직 그 기능이 확인되지 않았다.모든 유전자는 유전 형태를 포함하여 아래 유전자 목록에 나열되어 있습니다.예를 들어 SPG4와 파라플레긴(SPG7)은 모두 AAA ATPase입니다.[17]
유전자형
그 유전자들은 SPG라고 불린다.유전자 위치는 염색체 - 팔(짧은 또는 p: 긴 또는 q) - 밴드 번호의 형식이다.이 명칭들은 오직 인간 유전자만을 위한 것이다.위치는 다른 유기체에서도 다를 수 있습니다(아마도 다를 것입니다).이 질환에 관여하는 것으로 알려진 유전자의 수에도 불구하고, 환자의 40%는 아직 원인이 [18]밝혀지지 않았다.아래 표에서 SPG?는 HSP와 관련이 있지만 아직 공식적인 HSP 유전자 지정을 받지 않은 유전자를 나타내는 데 사용됩니다.
| 유전자형 | 옴 | 유전자 기호 | 유전자자리 | 상속 | 발병 연령 | 기타 이름 및 특징 |
|---|---|---|---|---|---|---|
| SPG1 | 303350 | L1CAM | Xq28 | X-연결 열성 | 빠른 | MASA 증후군 |
| SPG2 | 312920 | PLP1 | Xq22.2 | X-연결 열성 | 변수 | 펠리제우스메르즈바허병 |
| SPG3A | 182600 | ATL1 | 14분기 22.1 | 상염색체 우성 | 빠른 | Strumpell 질병(이 Wiki) |
| SPG4 | 182601 | 스페스트 | 2p22.3 | 상염색체 우성 | 변수 | |
| SPG5A | 270800 | CYP7B1 | 8분기 12.3 | 상염색체 열성 | 변수 | |
| SPG6 | 600363 | NIPA1 | 15분기 11.2 | 상염색체 우성 | 변수 | |
| SPG7 | 607259 | SPG7 | 16/24.3 | 상염색체 우성 | 변수 | |
| SPG8 | 603563 | KIAA0196 | 13년 8월 24일 | 상염색체 우성 | 어른 | |
| SPG9A | 601162 | ALDH18A1 | 10월 24일 1 | 상염색체 우성 | 10대 | 운동신경증, 단신, 골격 이상 백내장 |
| SPG9B | 616586 | ALDH18A1 | 10월 24일 1 | 상염색체 열성 | 빠른 | |
| SPG10 | 604187 | KIF5A | 12/13.3 | 상염색체 우성 | 빠른 | |
| SPG11 | 604360 | SPG11 | 15q21.1 | 상염색체 열성 | 변수 | |
| SPG12 | 604805 | RTN2 | 19분기 13.32 | 상염색체 우성 | 빠른 | |
| SPG13 | 605280 | HSP60 | 2q33.1 | 상염색체 우성 | 변수 | |
| SPG14 | 605229 | ? | 3q27–q28 | 상염색체 열성 | 어른 | |
| SPG15 | 270700 | ZFYVE26 | 14q24.1 | 상염색체 열성 | 빠른 | |
| SPG16 | 300266 | ? | Xq11.2 | 열성 X염색체에 연쇄된 | 빠른 | |
| SPG17 | 270685 | BSCL2 | 11q12.3 | 상염색체 우성 | 10대 | |
| SPG18 | 611225 | 에린2 | 8p11.23 | 상염색체 열성 | 빠른 | |
| SPG19 | 607152 | ? | 9분기 | 상염색체 우성 | 성인의 발병 | |
| SPG20 | 275900 | SPG20 | 13분기 13.3 | 상염색체 열성 | 조기 발병 | 트로이어 증후군 |
| SPG21 | 248900 | ACP33 | 15Q22.31 | 상염색체 열성 | 조기 발병 | MAST 증후군 |
| SPG22 | 300523 | SLC16A2 | XQ13.2 | X-연결 열성 | 조기 발병 | 앨런-헤른든-더들리 증후군 |
| SPG23 | 270750 | RIPK5 | 1q32.1 | 상염색체 열성 | 조기 발병 | 리슨 증후군 |
| SPG24 | 607584 | ? | 14년 1월 13일 | 상염색체 열성 | 조기 발병 | |
| SPG25 | 608220 | ? | 6q23~q24.1 | 상염색체 열성 | 어른 | |
| SPG26 | 609195 | B4GALNT1 | 12/13.3 | 상염색체 열성 | 조기 발병 | |
| SPG27 | 609041 | ? | 10q22.1~q24.1 | 상염색체 열성 | 변수 | |
| SPG28 | 609340 | DDHD1 | 14분기 22.1 | 상염색체 열성 | 조기 발병 | |
| SPG29 | 609727 | ? | 1p31.1~p21.1 | 상염색체 우성 | 10대 | |
| SPG30 | 610357 | KIF1A | 2분기 37.3 | 상염색체 열성 | 10대 | |
| SPG31 | 610250 | 리EP1 | 2p11.2 | 상염색체 우성 | 조기 발병 | |
| SPG32 | 611252 | ? | 14q12~q21 | 상염색체 열성 | 어린시절 | |
| SPG33 | 610244 | ZFYVE27 | 10/24.2 | 상염색체 우성 | 어른 | |
| SPG34 | 300750 | ? | Xq24~q25 | X-연결 열성 | 10대/어른 | |
| SPG35 | 612319 | FA2H | 16q23.1 | 상염색체 열성 | 어린시절 | |
| SPG36 | 613096 | ? | 12q23 ~q24 | 상염색체 우성 | 10대/어른 | |
| SPG37 | 611945 | ? | 8p21.1~q13.3 | 상염색체 우성 | 변수 | |
| SPG38 | 612335 | ? | 4p16~p15 | 상염색체 우성 | 10대/어른 | |
| SPG39 | 612020 | PNPLA6 | 19p13.2 | 상염색체 열성 | 어린시절 | |
| SPG41 | 613364 | ? | 11p14.1~p11.2 | 상염색체 우성 | 사춘기 | |
| SPG42 | 612539 | SLC33A1 | 3분기 25.31 | 상염색체 우성 | 변수 | |
| SPG43 | 615043 | C19orf12 | 19분기 12 | 상염색체 열성 | 어린시절 | |
| SPG44 | 613206 | GJC2 | 1Q42.13 | 상염색체 열성 | 어린 시절/10대 | |
| SPG45 | 613162 | NT5C2 | 10q24.32~q24.33 | 상염색체 열성 | 유아기 | |
| SPG46 | 614409 | GBA2 | 9p13.3 | 상염색체 열성 | 변수 | |
| SPG47 | 614066 | AP4B1 | 1p13.2 | 상염색체 열성 | 어린시절 | |
| SPG48 | 613647 | AP5Z1 | 7p22.1 | 상염색체 열성 | 제6십년 | |
| SPG49 | 615041 | TECPR2 | 14분기 32.31 | 상염색체 열성 | 유아기 | |
| SPG50 | 612936 | AP4M1 | 7분기 22.1 | 상염색체 열성 | 유아기 | |
| SPG51 | 613744 | AP4E1 | 15q21.2 | 상염색체 열성 | 유아기 | |
| SPG52 | 614067 | AP4S1 | 14분기 | 상염색체 열성 | 유아기 | |
| SPG53 | 614898 | VPS37A | 8p22 | 상염색체 열성 | 어린시절 | |
| SPG54 | 615033 | DDHD2 | 8p11.23 | 상염색체 열성 | 어린시절 | |
| SPG55 | 615035 | C12orf65 | 12월 24일 31일 | 상염색체 열성 | 어린시절 | |
| SPG56 | 615030 | CYP2U1 | 4분기 25일 | 상염색체 열성 | 어린시절 | |
| SPG57 | 615658 | TFG | 3분기 12.2 | 상염색체 열성 | 빠른 | |
| SPG58 | 611302 | KIF1C | 17p13.2 | 상염색체 열성 | 처음 20년 이내 | 경련성 실조증 2 |
| SPG59 | 603158 | USP8 | 15q21.2 | 자가 염색체 열성 | 어린시절 | |
| SPG60 | 612167 | WDR48 | 3p22.2 | 자가 염색체 열성 | 유아기 | |
| SPG61 | 615685 | ARL6IP1 | 16p12.3 | 상염색체 열성 | 유아기 | |
| SPG62 | 615681 | 에린1 | 10월 24일 31일 | 상염색체 열성 | 어린시절 | |
| SPG63 | 615686 | AMPD2 | 1p13.3 | 상염색체 열성 | 유아기 | |
| SPG64 | 615683 | ENTPD1 | 10월 24일 1 | 상염색체 열성 | 어린시절 | |
| SPG66 | 610009 | ARSI | 5분기 32분 | 자가염색체 우성 | 유아기 | |
| SPG67 | 615802 | PGAP1 | 2q33.1 | 상염색체 열성 | 유아기 | |
| SPG68 | 609541 | KLC2 | 11/13.1 | 상염색체 열성 | 어린시절 | SPOAN 증후군 |
| SPG69 | 609275 | RAB3GAP2 | 1q41 | 상염색체 열성 | 유아기 | 마르톨프 증후군, 워버그 마이크로 증후군 |
| SPG70 | 156560 | 마스 | 13년 12월 | 자가염색체 우성 | 유아기 | |
| SPG71 | 615635 | ZFR | 5p13.3 | 자가 염색체 열성 | 어린시절 | |
| SPG72 | 615625 | 리EP2 | 5분기 31일 | 상염색체 열성 상염색체 우성 | 유아기 | |
| SPG73 | 616282 | CPT1C | 19분기 13.33 | 상염색체 우성 | 어른 | |
| SPG74 | 616451 | IBA57 | 1Q42.13 | 상염색체 열성 | 어린시절 | |
| SPG75 | 616680 | MAG | 12년 4월 19일 | 상염색체 열성 | 어린시절 | |
| SPG76 | 616907 | 캡N1 | 13년 11월 | 상염색체 열성 | 어른 | |
| SPG77 | 617046 | FARS2 | 6p25 | 상염색체 열성 | 어린시절 | |
| SPG78 | 617225 | ATP13A2 | 1p36 | 상염색체 열성 | 어른 | 쿠포르-라케브 증후군 |
| SPG79 | 615491 | UCHL1 | 4p13 | 상염색체 열성 | 어린시절 | |
| HSNSP | 256840 | CCT5 | 5p15.2 | 상염색체 열성 | 어린시절 | 경련성 하반신 마비를 동반한 유전성 감각 장애 |
| SPG? | SERAC1 | 6분기 25.3 | 청소년 | MEGDEL 증후군 | ||
| SPG? | 605739 | KY | 3분기 22.2 | 상염색체 열성 | 유아기 | |
| SPG? | PLA2G6 | 22/13.1 | 상염색체 열성 | 어린시절 | ||
| SPG? | ATAD3A | 1p36.33 | 상염색체 우성 | 어린시절 | 하렐윤증후군 | |
| SPG? | KCNA2 | 1p13.3 | 상염색체 우성 | 어린시절 | ||
| SPG? | 그라눌린 | 17Q21.31 | ||||
| SPG? | 폴러3A | 10q22.3 | 상염색체 열성 |
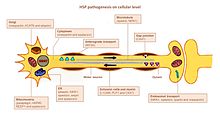
병태생리학
HSP의 주요 특징은 길이에 의존하는 [19]축삭변성입니다.이것들은 다리와 파시쿨루스 그라실리스에 교차된 피질척수관을 포함한다.척추신경관은 덜 관여한다.퇴화 축삭의 신경 세포체는 보존되어 있으며 일차 [16]탈수 증거는 없다.척수의 전방 뿔 세포의 손실이 관찰되는 경우도 있다.배근신경절, 후근, 말초신경은 직접적인 [citation needed]영향을 받지 않는다.
HSP는 운동 뉴런의 여러 경로에 영향을 미친다.많은 유전자들이 확인되었고 HSP와 관련이 있다.많은 유전자가 여러 기능을 가지고 있고 둘 이상의[citation needed] 경로에 관여하기 때문에 영향을 받는 각각의 경로에서 핵심 관계자를 정확하게 정의하는 것은 여전히 어려운 과제이다.
액손 패스파인딩
경로 찾기는 올바른 목적지로 축삭을 성장시키는 데 중요하다(예: 다른 신경 세포나 근육).이 메커니즘에 중요한 것은 면역글로불린 슈퍼패밀리의 세포 표면 당단백질인 L1CAM 유전자이다.L1CAM의 기능 상실을 초래하는 돌연변이는 다른 X-연결 증후군에서도 발견된다.이러한 모든 장애는 피질척수관 장애를 나타낸다.L1CAM은 다른 L1CAM 분자뿐만 아니라 세포외 접착 분자, 인테그린,[citation needed] 프로테오글리칸 또는 강키린과 같은 세포내 단백질과 결합하는 일련의 상호작용에 참여합니다.
패스파인딩 결함은 L1CAM과 neuroilin-1의 관련성을 통해 발생합니다.뉴로빌린-1은 플렉신-A 단백질과 상호작용하여 세마포린-3A 수용체 복합체를 형성한다.그리고 나서 세마포린-a3A가 복측척수에서 방출되어 중간선척수/수 접합부에서 피질척수 뉴런을 멀어지게 한다.돌연변이로 인해 L1CAM이 제대로 작동하지 않으면 피질척수신경세포가 올바른 위치로 향하지 않아 장애가 발생합니다.[3]
지질대사
중추신경계와 말초신경계의 축삭은 활동전위전파의 속도를 높이기 위해 미엘린층이라는 절연체로 코팅되어 있다.HSP의 [20]일부 형태에서 CNS의 비정상적인 미엘리네이션이 검출됩니다.PLP1, GFC2, FA2H [3]등 여러 유전자가 미엘린 기형과 연관됐다.돌연변이는 미엘린의 구성, 두께, [citation needed]무결성을 변화시킵니다.
소포체(ER)는 지질 합성을 위한 주요 세포소기관이다.ER 형태와 지질 대사를 형성하는 역할을 하는 단백질을 코드하는 유전자의 돌연변이는 HSP와 관련이 있었다.ATL1, BSCL2 및 ERLIN2의 돌연변이는 ER 구조, 특히 관상 네트워크 및 ER 세관에서 삼원 접합의 형성을 변화시킨다.많은 돌연변이 유전자들은 비정상적인 지질 대사와 관련이 있다.가장 일반적인 효과는 아라키돈산(CYP2U1)과 콜레스테롤(CYP7B1) 대사, 포스포리파아제 활성(DDHD1과 DDHD2), 간글리오시드 생성(B4GALNT-1) 및 탄수화물과 지방 대사(SLV33A1)[3][21][20] 간의 균형에 있다.
내염색체 밀매
신경세포는 내구증(endocytosis)에 의해 주변의 물질을 흡수한다.세포내 소포는 내용물을 방출하기 위해 엔도솜과 융합한다.엔도솜 밀매를 하는 세 개의 주요 구획이 있습니다: 엔도솜으로 가는 골지, 엔도솜으로 가는 혈장막 그리고 리소솜으로 가는 말기 엔도솜.HSP에서 보고된 바와 같이, 내염색체 밀매의 기능 장애는 긴 축삭을 가진 운동 신경 세포에 심각한 결과를 초래할 수 있다.AP4B1과 KIAA0415의 돌연변이는 소포 형성 장애 및 소포에 단백질의 선택적 흡수를 포함한 막트래픽과 관련이 있다.두 유전자 모두 다른 단백질과 상호작용하는 단백질을 암호화하고 분비 경로와 내구성 [20]경로를 방해합니다.
미토콘드리아 기능
미토콘드리아 기능 장애는 발달 및 퇴행성 신경 장애와 연관되어 있다.몇몇 HSP 유전자만이 미토콘드리아 단백질을 암호화한다.HSP에서는 파라플레긴과 샤페로닌 60의 2개의 미토콘드리아 상주 단백질이 돌연변이된다.파라플레긴은 미토콘드리아 내막의 m-AAA 금속단백질가수분해효소이다.그것은 리보솜 조립과 단백질 품질 관리에서 기능한다.손상된 샤페로닌 60 활성은 미토콘드리아 품질 관리 저하로 이어진다.DDHD1과 CYP2U1 두 유전자는 환자 섬유아세포에서 미토콘드리아 구조의 변화를 보였다.이 유전자들은 지방산 [citation needed]대사에 관여하는 효소를 암호화한다.
진단.
HSP의 초기 진단은 가족력, 추가 징후 유무 및 기타 비유전성 경련 원인의 제외에 의존하며, 후자는 산발적인 [7]경우에 특히 중요하다.
뇌 및 척추 MRI는 다발성 경화증과 같은 다른 빈번한 신경학적 상태를 배제하기 위해 수행되는 중요한 시술이지만, 소뇌 또는 뇌량 위축 및 백질 이상과 같은 관련 이상을 발견하기 위해 수행됩니다.HSP의 차이 진단은 또한 거의 동일한 일상적 효과를 나타내며 심지어 바클로펜과 정형외과 수술과 같은 유사한 약물로 치료 가능한 경련성 이중마비증을 제외해야 한다. 때때로 이 두 질환은 매우 비슷해 보이고 느낄 수 있기 때문에 유일한 인식된 차이는 HSP의 유전성 대 비만일 수 있다.경련성 이중마비의 비유전적 특성(단, 경련성 이중마비 및 다른 형태의 경련성 뇌성마비와 달리 HSP는 선택적 [citation needed]등근절개술로 확실하게 치료될 수 없다).
HSP 진단의 최종 확인은 알려진 유전자 [citation needed]돌연변이를 대상으로 한 유전자 검사를 수행해야만 제공됩니다.
분류
유전성 경련성 부전골은 증상, 유전 방식, 발병 시 환자의 나이, 영향을 받은 유전자, 관련된 [citation needed]생화학적 경로에 따라 분류될 수 있다.
치료
HSP를 방지, 지연 또는 역방향으로 하는 구체적인 치료법은 알려져 있지 않습니다.이용 가능한 치료법은 주로 대증적 의학적 관리와 신체적,[citation needed] 정서적 행복 증진으로 구성된다.HSP 환자에게 제공되는 치료제는 다음과 같습니다.
- 바클로펜 – 근육을 이완시키고 긴장감을 줄이기 위한 자발적인 근육 이완제.이는 경구 또는 뇌내 투여가 가능합니다.(HSP 연구)
- 티자니딘 – 야간 또는 간헐적 경련 치료(연구 이용 가능)
- 디아제팜 및 클로나제팜 – 경련[citation needed] 강도 감소
- 옥시부티닌 염화물 – 방광 조절[citation needed] 문제가 있는 환자의 방광의 경련을 줄이기 위해 사용되는 비자발적인 근육 이완제 및 경련제
- Tolterodine tartrate – 방광 조절[citation needed] 문제가 있는 환자의 방광 경련을 줄이기 위해 사용되는 무의식적인 근육 이완제 및 경련제
- Cro 시스템 – 근육의 과잉 활동을 줄입니다(경련성에 대한 기존 연구).
- 보툴리누스 독소 – 근육 과잉 활동 감소(HSP 환자를[30][31] 위한 기존 연구)
- 항우울제(선택적인 세로토닌 재흡입 억제제, 삼환계 항우울제, 모노아민 산화효소 억제제 등) – 임상 우울증을[citation needed] 겪는 환자용
- 물리치료 – 운동능력을 회복 및 유지; 근육긴장 감소; 운동범위와 이동성 유지 또는 개선; 힘과 조정력 증가; 동결관절, 수축 또는 [citation needed]욕창과 같은 합병증을 예방한다.
예후
HSP는 진행성 질환이지만 HSP를 가진 사람의 예후는 크게 다르다.이것은 주로 다리에 영향을 미치지만 일부 개인에게는 상반신이 관여할 수 있다.심각한 디세이블이 되는 경우도 있고 디세이블이 적고 생산적이고 완전한 라이프와 호환되는 경우도 있습니다.HSP를 가진 대부분의 사람들은 정상적인 [14]수명을 가지고 있다.
역학
전 세계적으로 모든 유전성 경련성 하반신 마비 유병률은 10만 [32]명 중 2에서 6명으로 추정된다.2009년 3월에 발표된 250만 명 이상의 인구를 대상으로 한 노르웨이 연구에 따르면 HSP 유병률은 인구의 7.4/100,000명으로, 이는 이전 연구와 동일한 비율이다.성별과 관련된 비율의 차이는 발견되지 않았으며, 발병 시 평균 연령은 [33]24세였다.미국에서는 미국 국립보건원 희귀병국(ORD)에 의해 유전성 경련성 하반신마비가 희귀병으로 등재되어 있으며 이는 미국 인구 [32]중 20만 명 미만에게 발병하는 질환이다.
레퍼런스
- ^ Fink, John K. (2003-08-01). "The hereditary spastic paraplegias: nine genes and counting". Archives of Neurology. 60 (8): 1045–1049. doi:10.1001/archneur.60.8.1045. ISSN 0003-9942. PMID 12925358.
- ^ Depienne, Christel; Stevanin, Giovanni; Brice, Alexis; Durr, Alexandra (2007-12-01). "Hereditary spastic paraplegias: an update". Current Opinion in Neurology. 20 (6): 674–680. doi:10.1097/WCO.0b013e3282f190ba. ISSN 1350-7540. PMID 17992088. S2CID 35343501.
- ^ a b c d Blackstone, Craig (21 July 2012). "Cellular Pathways of Hereditary Spastic Paraplegia". Annual Review of Neuroscience. 35 (1): 25–47. doi:10.1146/annurev-neuro-062111-150400. PMC 5584684. PMID 22540978.
- ^ De Matteis, Maria Antonietta; Luini, Alberto (2011-09-08). "Mendelian disorders of membrane trafficking". The New England Journal of Medicine. 365 (10): 927–938. doi:10.1056/NEJMra0910494. ISSN 1533-4406. PMID 21899453. S2CID 14772080.
- ^ Faber I, Pereira ER, Martinez AR, França M Jr, Teive HA (November 2013). "Hereditary spastic paraplegia from 1880 to 2017: an historical review". Arquivos de Neuro-Psiquiatria. Brazilian Academy of Neurology. 75 (11): 813–818. doi:10.1590/0004-282X20170160. PMID 29236826.
- ^ 로레인, 모리스기여 ution l'tude de la paraplegie spasmodique familiale : travail de la crinique des maladique du systéme neurvux à la Salpétriére.G. 스타인힐, 1898년
- ^ a b c d Harding, AE (1983). "Classification of the hereditary ataxias and paraplegias". Lancet. New York. 1 (8334): 1151–5. doi:10.1016/s0140-6736(83)92879-9. PMID 6133167. S2CID 6780732.
- ^ McAndrew CR, Harms P (2003). "Paraesthesias during needle-through-needle combined spinal epidural versus single-shot spinal for elective caesarean section". Anaesthesia and Intensive Care. 31 (5): 514–517. doi:10.1177/0310057X0303100504. PMID 14601273.
- ^ Fjermestad, Krister W.; Kanavin, Øivind J.; Næss, Eva E.; Hoxmark, Lise B.; Hummelvoll, Grete (2016-07-13). "Health survey of adults with hereditary spastic paraparesis compared to population study controls". Orphanet Journal of Rare Diseases. 11 (1): 98. doi:10.1186/s13023-016-0469-0. ISSN 1750-1172. PMC 4944497. PMID 27412159.
- ^ Chaudhuri, Abhijit; Behan, Peter O. (2004-03-20). "Fatigue in neurological disorders". Lancet. 363 (9413): 978–988. doi:10.1016/S0140-6736(04)15794-2. ISSN 1474-547X. PMID 15043967. S2CID 40500803.
- ^ "Hereditary spastic paraplegia". nhs.uk. 2017-10-18. Retrieved 2018-01-28.
- ^ Fink JK (2003). "The Hereditary Spastic Paraplegias". Archives of Neurology. 60 (8): 1045–1049. doi:10.1001/archneur.60.8.1045. PMID 12925358.
- ^ a b c Harding AE (1981). "Hereditary "pure" spastic paraplegia: a clinical and genetic study of 22 families". Journal of Neurology, Neurosurgery, and Psychiatry. 44 (10): 871–883. doi:10.1136/jnnp.44.10.871. PMC 491171. PMID 7310405.
- ^ a b Depienne C, Stevanin G, Brice A, Durr A (2007). "Hereditary Spastic Paraplegia: An Update". Current Opinion in Neurology. 20 (6): 674–680. doi:10.1097/WCO.0b013e3282f190ba. PMID 17992088. S2CID 35343501.
- ^ a b c Schüle, Rebecca; Wiethoff, Sarah; Martus, Peter; Karle, Kathrin N.; Otto, Susanne; Klebe, Stephan; Klimpe, Sven; Gallenmüller, Constanze; Kurzwelly, Delia (2016-04-01). "Hereditary spastic paraplegia: Clinicogenetic lessons from 608 patients". Annals of Neurology. 79 (4): 646–658. doi:10.1002/ana.24611. ISSN 1531-8249. PMID 26856398. S2CID 10558032.
- ^ a b Schüle R, Schöls L (2011) 유전성 경련성 부두전증.Semin Neurol 31(5): 484-493
- ^ Wang YG, Shen L(2009) AAA ATPase 및 유전성 경련성 하반신 마비.중화이학이학자지26(3):298-301
- ^ Helbig KL, Hedrich UB, Shinde DN, Krey I, Teichmann AC, 헨첼 J, 슈베르트 J, 챔벌린 AC, Huether R, Lu HM4, Alcaraz WA, 탕 S, 중블루스 C, 듀간, 바이언, Lépain액시아. 앤 뉴롤 80(4)
- ^ Wharton SB, McDermott CJ, Grierson AJ, Wood JD, Gelsthorpe C, Ince PG, Shaw PJ(2003) 스파스틴 유전자의 돌연변이에 의한 운동계의 세포 및 분자 병리학.J 뉴로아톨 Exp Neurol 62:1166–1177
- ^ a b c Noreau, A., Dion, P.A. & Rouleau, G.A., 2014.유전성 경련성 하반마비의 분자적 측면이죠실험 세포 연구, 325(1) 페이지 18-26
- ^ Lo Giudice, T. et al., 2014.유전성 경련성 하반신 마비:임상 유전학적 특성과 진화하는 분자 메커니즘.실험 신경학, 261, 페이지 518–539.
- ^ Margetis K, Korfias S, Boutos N, Gatzonis S, Temistocleous M, Siatouni A 등유전성 경련성 하반신마비의 증상 치료를 위한 자궁내 바클로펜 치료.임상 신경과 및 신경외과. 2014;123:142-5.
- ^ Heetla HW, Halbertsma JP, Dekker R, Stal MJ, van Laar T.유전성 경련성 하반신 마비 환자의 지속적 경련성 바클로펜 시험 주입 및 후속 펌프 이식 후 개선된 보행 성능: 사례 보고서물리 의학 및 재활 기록 보관소.2015;96(6):1166-9.
- ^ Klebe S, Stolze H, Kopper F, Lorenz D, Wenzelburger R, Deuscl G 등유전성 경련성 하반신 마비에서 경막 내 바클로펜 이후의 보행에 대한 객관적 평가.신경학 저널2005;252(8):991-3.
- ^ 크누트손 E, 모르텐손 A, 그란스베르크 L.경련성 파레시스 환자에게서 티자니딘에 의해 유발되는 항경련 및 항경련 효과.신경과학 저널1982;53(2):187-204.
- ^ Bes A, Eysette M, Pierro-Deseilligny E, Rohmer F, Warter JM.반신불수증과 관련된 경련성의 새로운 항경련제인 티자니딘의 다중심 이중맹검 시험.현재의 의학 연구 및 의견.1988;10(10):709-18.
- ^ 셀레티 C, 카메라타 F이탈리아 어린이의 작은 표본에서 뇌성마비로 인한 초점근육 진동이 경련에 영향을 미친다는 예비 증거.Clin Ter. 162(5): 2011년 125일
- ^ Caliandro P, Celetti C, Padua L, Minciotti I, Russo G, Granata G, La Torre G, Granieri E, Camerota F.상지 경련성 치료에서의 국소 근육 진동: 만성 뇌졸중 환자의 시험적 무작위 대조 시험.Arch Phys Med Reval. 93(9):1656-61. 2012.
- ^ . Casale R1, Damiani C, Maestri R, Fundar c C, Chimento P, Foti C.이중 블라인드 제어 스터디인 100Hz 진동에 의해 기능이 향상되고 상지의 경련이 감소합니다.Euro J Phys Real Med. 2014년 10월;50(5):495-504.
- ^ Hecht MJ, Stolze H, Auf Dem Brinke M, Giess R, Treig T, Winterholler M 등보툴리누스 뉴로톡신 타입 A 주사는 경미하거나 중간 정도의 유전성 경련성 하반마비에서 경련성을 감소시킨다— 19건의 사례 보고.운동 장애2008;23(2):228-33.
- ^ 드 니트 M, 드 봇 ST, 반 드 워렌버그 BP, 위르데스테인 V, 게르트 ACA형 보툴리누스 독소 치료와 그에 따른 종아리 근육 스트레칭의 기능적 영향:유전성 경련성 하반신 마비 환자의 연구.재활의학 저널.2015;47(2):147-53.
- ^ a b National Institute of Health (2008). "Hereditary Spastic Paraplegia Information Page". Archived from the original on 2014-02-21. Retrieved 2008-04-30.
- ^ Erichsen, AK; Koht, J; Stray-Pedersen, A; Abdelnoor, M; Tallaksen, CM (June 2009). "Prevalence of hereditary ataxia and spastic paraplegia in southeast Norway: a population-based study". Brain. 132 (Pt 6): 1577–88. doi:10.1093/brain/awp056. PMID 19339254.
추가 정보
- 경련성 하반신 마비 3A에서의 Gene Reviews/NCBI/NIH/UW 엔트리
- 유전성 경련성 하반신마비의 유전자 리뷰/NCBI/NIH/UW 엔트리 개요
- Warner, Tom (January–February 2007). "Hereditary Spastic Paraplegia" (PDF). Advances in Clinical Neuroscience and Rehabilitation. 6 (6): 16–17.