인피
Human skin| 인피 | |
|---|---|
 사람 손의 피부 | |
 | |
| 세부 사항 | |
| 시스템. | 외각계 |
| 식별자 | |
| 라틴어 | 큐티스 |
| TA98 | A16.0.00.002 |
| TA2 | 7041 |
| TH | H3.12.00.1.00001 |
| FMA | 7163 |
| 해부학 용어 [위키데이터 편집] | |
사람의 피부는 신체의 바깥쪽을 덮고 있는 기관으로 외피계의 가장 큰 기관입니다. 피부에는 근육, 뼈, 인대 및 내부 장기를 보호하는 최대 7층의 외배엽 조직이 있습니다. 사람의 피부는 대부분의 다른 포유류의 피부와 비슷하고, 돼지의 피부와 매우 비슷합니다. 거의 모든 사람의 피부가 모낭으로 덮여 있지만 털이 없어 보일 수 있습니다. 일반적인 피부에는 털이 많은 피부와 번들거리는 피부(털이 없는 피부) 두 가지 유형이 있습니다. 피부라는 형용사는 문자 그대로 (라틴어 cutis, skin) "피부의"를 의미합니다.
피부는 병원균과 과도한 수분 손실로부터 몸을 보호하는 중요한 면역 역할을 합니다. 다른 기능은 절연, 온도 조절, 감각, 비타민 D 합성, 비타민 B 엽산 보호입니다. 심하게 손상된 피부는 흉터 조직을 형성하여 치유하려고 노력할 것입니다. 변색되고 변색되는 경우가 많습니다.
인간의 경우, 피부 색소 침착(멜라닌에 의해 영향을 받는)은 인구에 따라 다르며, 피부 유형은 건조한 것부터 건조하지 않은 것까지 그리고 기름진 것부터 기름지지 않은 것까지 다양합니다. 이러한 피부 품종은 인간의 피부에 존재하는 19개의 문에서 약 1,000 종의 박테리아가 풍부하고 다양한 서식지를 제공합니다.
구조.
인간의 피부는 다른 포유류 계통, 특히 돼지 피부와 해부학적, 생리학적, 생화학적, 면역학적 특성을 공유합니다.[1][2] 돼지 피부는 인간 피부와 유사한 표피 및 진피 두께 비율을 공유하고,[1][2] 돼지 및 인간 피부는 유사한 모낭 및 혈관 패턴을 공유하며,[1][2] 생화학적으로 돼지 및 인간 피부에서 진피 콜라겐 및 엘라스틴 함량은 유사하며,[1][2] 돼지 피부 및 인간 피부는 다양한 성장 인자에 대해 유사한 물리적 반응을 갖는 것을 특징으로 하는 돼지 피부 및 인간 피부.[1][2]
피부에는 멜라닌 세포에 의해 제공되는 멜라닌과 같은 색소 침착과 같은 중배엽 세포가 있으며, 이는 잠재적으로 위험한 자외선(UV)의 일부를 햇빛에서 흡수합니다. 또한 자외선 손상을 되돌리는 데 도움이 되는 DNA 복구 효소가 포함되어 있어 이 효소의 유전자가 부족한 사람들은 피부암 발병률이 높습니다. 주로 자외선에 의해 생성되는 한 형태인 악성 흑색종은 특히 침습적이어서 빠르게 퍼지며 종종 치명적일 수 있습니다. 사람의 피부 색소 침착은 개체군마다 현저한 방식으로 다릅니다. 이것은 피부색에 기초하여 사람들을 분류하는 결과로 이어졌습니다.[3]
피부는 표면적으로 인체에서 두 번째로 큰 기관(소장 내부는 15~20배)입니다. 평균적인 성인 인간의 경우, 피부의 표면적은 1.5-2.0 제곱 미터 (16-22 평방 피트)입니다. 피부의 두께는 신체의 모든 부분에 걸쳐, 그리고 남녀, 젊은 층과 노년층 사이에 상당한 차이가 있습니다. 예를 들어, 수컷은 평균 1.3mm, 암컷은 평균 1.26mm인 팔뚝의 피부가 있습니다.[4] 평균 1제곱인치(6.5cm2)의 피부에는 650개의 땀샘, 20개의 혈관, 60,000개의 멜라닌 세포, 그리고 1,000개 이상의 신경 말단이 있습니다.[5][better source needed] 평균적인 인간 피부세포의 지름은 약 30마이크로미터(μm)이지만 변종도 있습니다. 피부 세포는 일반적으로 다양한 요인에 따라 25~40μm2 범위입니다.
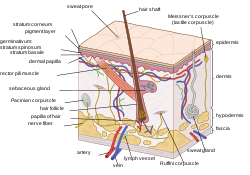
피부는 표피, 진피 및 피하의 세 가지 원초적 층으로 구성됩니다.[4]

표피
표피는 그리스어로 "넘다" 또는 "위로"를 의미하는 "에피"에서 온 것으로 피부의 가장 바깥층입니다. 그것은 몸의 표면에 방수 보호 랩을 형성하고 감염에 대한 장벽의 역할을 하며 기저 층을 가진 층화된 편평 상피로 구성됩니다.
표피는 혈관을 포함하지 않으며, 가장 깊은 층의 세포는 거의 독점적으로 주변 공기의[6] 확산된 산소에 의해 영양을 공급받고 진피의 외부 층으로 확장되는 혈액 모세혈관에 의해 훨씬 적은 정도로 영양을 공급받습니다. 표피를 구성하는 주요 세포 유형은 각질세포인 메르켈 세포이며, 멜라닌 세포와 랑게르한스 세포도 존재합니다. 표피는 더 세분화될 수 있습니다 (가장 바깥 층부터 시작하여): 각막, 루시덤(손바닥과 발바닥에만 있음), 과립막, 스피노섬 및 기저층. 세포는 기저층에서 유사분열을 통해 형성됩니다. 딸 세포(세포 분열 참조)는 혈액원으로부터 고립되어 사망함에 따라 지층의 변화하는 형태와 구성을 증가시킵니다. 세포질이 방출되고 단백질 케라틴이 삽입됩니다. 그들은 결국 각막에 도달하여 슬로우 오프(명예훼손)됩니다. 이 과정을 케라틴화(keratinization)라고 합니다. 이 각질화된 피부 층은 체내 수분을 유지하고 다른 유해한 화학 물질과 병원균을 차단하여 피부를 감염의 자연 장벽으로 만듭니다.[7]

표피에는 혈관이 없고 진피에서 확산되어 영양이 공급됩니다. 표피를 구성하는 주요 세포 종류는 케라틴 세포, 멜라닌 세포, 랑게르한스 세포, 메르켈 세포입니다. 표피는 피부가 체온을 조절하는 데 도움이 됩니다.
레이어
피부에는 최대 7층의 외배엽 조직이 있으며 기저 근육, 뼈, 인대 및 내부 장기를 보호합니다.[8] 표피는 여러 층으로 나뉘는데, 여기서 세포는 가장 안쪽 층에서 유사분열을 통해 형성됩니다. 그들은 분화하고 케라틴으로 채워지면서 형태와 구성을 변화시키는 지층을 이동시킵니다. 최상층의 각질층에 도달한 후, 그들은 결국 '슬라우징 오프'되거나, 또는 탈질됩니다. 이 과정을 케라틴화라고 하며 몇 주 안에 이루어집니다.
이전에는 각질층이 "죽은 케라틴의 섬유 격자를 포함하는 단순하고 생물학적으로 비활성인 외부 표피층"이라고 믿었습니다.[9] 이것은 사실이 아니며, 각질층은 살아있는 조직으로 간주되어야 한다는 것이 지금 이해되고 있습니다.[10] 각질층은 주로 핵을 가진 각질세포라고 불리는 말단 분화 각질세포로 구성되어 있는 것은 사실이지만, 이 세포들은 각질이 제거될 때까지 살아 있고 대사 기능을 유지합니다.[citation needed]
부계층
표피는 다음의 5개의 하부층 또는 지층으로 나뉩니다.
- 각질층
- 명지층
- 과립층
- 지층 스피노섬
- 지층(Stratum basale, "stratum germinativum"이라고도 함)
혈액 모세혈관은 표피 아래에서 발견되며 동맥과 정맥과 연결되어 있습니다. 동맥 션트 혈관은 귀, 코 및 손가락 끝에서 네트워크를 우회할 수 있습니다.
표피에서 발현되는 유전자와 단백질
인간의 모든 단백질 코딩 유전자의 약 70%가 피부에서 발현됩니다.[11][12] 거의 500개의 유전자가 피부에서 높은 발현 패턴을 가지고 있습니다. 피부에 특이적인 유전자는 100개 미만으로 표피에서 발현됩니다.[13] 해당 단백질을 분석한 결과, 이들은 주로 각질세포에서 발현되며 편평 분화 및 옥수수화와 관련된 기능을 가지고 있음을 알 수 있습니다.
진피
진피는 결합 조직으로 구성된 표피 아래의 피부 층으로, 스트레스와 스트레스로부터 몸을 완화시킵니다. 진피는 기저막에 의해 표피와 단단히 연결되어 있습니다. 또한 촉각과 열감을 제공하는 많은 신경 끝을 가지고 있습니다. 모낭, 땀샘, 피지선, 아포크린샘, 림프관 및 혈관이 포함되어 있습니다. 진피의 혈관은 표피의 기저층뿐만 아니라 자체 세포에서 영양분을 공급하고 노폐물을 제거합니다.
진피는 구조적으로 표피에 인접한 표면적인 영역인 유두 영역과 망상 영역으로 알려진 깊고 두꺼운 영역으로 구분됩니다.
유두부
유두 부위는 느슨한 막대형 결합 조직으로 구성되어 있습니다. 그것은 표피 쪽으로 뻗어 있는 유두라고 불리는 손가락 모양의 돌기 때문에 이름 지어졌습니다. 유두는 진피에 표피와 상호 소화되는 "엉덩이" 표면을 제공하여 두 층의 피부 연결을 강화합니다.
손바닥, 손가락, 발바닥, 발가락에는 표피로 돌출된 유두의 영향으로 피부 표면에 윤곽이 형성됩니다. 이러한 표피 융기는 유전적, 후성유전적으로 결정되는 패턴(예: 지문)에서 발생하며, 따라서 개인에게 고유하므로 지문이나 발자국을 식별 수단으로 사용하는 것이 가능합니다.
레티큘라 영역
망상 부위는 유두 부위에 깊게 위치하며 일반적으로 훨씬 두껍습니다. 촘촘한 불규칙한 결합조직으로 구성되어 있으며, 그 전체에 걸쳐 짜여진 콜라겐성, 탄력성, 망상섬유의 촘촘한 농도에서 그 이름을 따왔습니다. 이 단백질 섬유는 진피에 강도, 확장성 및 탄력의 특성을 제공합니다.
또한 망상 영역 내에는 털, 피지선, 땀샘, 수용체, 손톱, 혈관의 뿌리가 있습니다.
문신 잉크는 진피에 보관되어 있습니다. 종종 임신과 비만으로 인한 스트레치 마크도 진피에 위치합니다.
피하조직
피하 조직(피하 및 피하)은 피부의 일부가 아니라 피부의 진피 아래에 있습니다. 피부를 기저 뼈와 근육에 부착하고 혈관과 신경을 공급하는 것이 목적입니다. 느슨한 결합 조직, 지방 조직, 엘라스틴으로 구성되어 있습니다. 주요 세포 유형은 섬유아세포, 대식세포 및 지방세포(피하조직은 체지방의 50%를 포함합니다)입니다. 지방은 몸의 패딩과 절연 역할을 합니다.
횡단면
세포수 및 세포질량
피부세포표
아래 표는 70 kg의 성인 남성(ICRP-23; ICRP-89, ICRP-110)의 피부 세포 수 및 총 세포 질량 추정치를 식별합니다.[14][15][16]
조직 질량은 3.3kg(ICRP-89, ICRP110)으로 정의되며 피부의 표피, 진피, 모낭 및 선을 다룹니다. 세포 데이터는 지원 정보 SO1 데이터 세트(xlsx)의 Tissue-Table 탭인 '인간 세포 수 및 세포 크기 분포'[17][18]에서 추출됩니다. 1200 레코드 데이터 세트는 셀 수, 셀 크기 및 집계 셀 질량에 대한 광범위한 참조를 통해 지원됩니다.
아래의 세포 그룹에 대한 상세 데이터는 위의 섹션에 나열된 모든 세포 유형으로 더 세분화되며 데이터셋의 표피, 진피, 모낭 및 선 하위 범주와 데이터셋의 그래픽 웹 사이트 인터페이스에 따라 분류됩니다.[19] 피하 지방 조직의 지방 세포는 ICRP 조직 범주에서 별도로 처리되는 반면, 진피층에 존재하는 지방 함량(마이너스 세포-막-지질)은 진피층의 아래의 간질-지방 세포에 의해 처리됩니다(표-105, ICRP-23).
| 명명된 티슈와 연결된 셀 그룹 | 조직 질량(g) | 셀 카운트 | 집합 셀 질량(g) |
| 피부. | 3,300 | 6.1E+11 | 837 |
| ICRP-89, 110 (조직질량원) | |||
| 지방세포 | 3,300 | 7.3E+08 | 292 |
| 혈구, 핵, 조직.거주자. | 3,300 | 5.4E+10 | 87 |
| ___WBCs / 과립구(마스트 세포) | 3,300 | __2.2E+10 | __33 |
| ___WBCs / Lymphoid | 3,300 | __1.3E+10 | ___2 |
| ___WBCs / 단핵구-대식세포 | 3,300 | __1.9E+10 | __53 |
| 내피세포(EnC) | 3,300 | 1.5E+10 | 6.2 |
| 상피세포(EpC) | 3,300 | 4.1E+11 | 314 |
| 상피세포(EpC); 비핵세포 | 3,300 | 7.1E+10 | 28 |
| 섬유아세포 | 3,300 | 4.3E+10 | 95 |
| 근세포 | 3,300 | 2.6E+07 | 0.08 |
| 신경교 | 3,300 | 8.5E+09 | 13 |
| 혈관주위 세포/주위 세포/벽화 | 3,300 | 1.5E+09 | 0.6 |
| 줄기세포; 상피세포(EpSC) | 3,300 | 3.6E+09 | 1.5 |
발전
피부색
사람의 피부는 가장 어두운 갈색부터 가장 밝은 분홍색-흰색까지 다양한 피부색을 보여줍니다. 인간의 피부는 다른 어떤 단일 포유류 종보다 더 높은 색상 변화를 보이며 자연 선택의 결과입니다. 인간의 피부 색소 침착은 주로 피부에 침투하는 자외선(UVR)의 양을 조절하고 생화학적 효과를 조절하도록 진화했습니다.[20]
비록 인간의 피부색을 결정하는 가장 중요한 단일 물질은 색소 멜라닌이지만, 다양한 인간의 실제 피부색은 많은 물질에 의해 영향을 받습니다. 멜라닌은 멜라닌 세포라고 불리는 세포에서 피부 내에서 생성되며, 어두운 피부를 가진 사람들의 피부색을 결정하는 주요 요인입니다. 가벼운 피부를 가진 사람들의 피부색은 주로 진피 아래의 청백색의 결합 조직과 진피의 정맥에서 순환하는 헤모글로빈에 의해 결정됩니다. 특히 신체 운동이나 신경계의 자극(분노, 공포)으로 인해 동맥이 확장될 때, 피부 밑에 있는 붉은 색이 얼굴에서 더 잘 보입니다.[21]
피부의 색을 결정하는 최소 5가지의 다양한 색소가 있습니다.[22][23] 이 색소는 다양한 수준과 장소에 존재합니다.
- 멜라닌: 갈색을 띠며 표피의 기저층에 존재합니다.
- 멜라노이드: 멜라닌과 비슷하지만 표피 전체에 넓게 존재합니다.
- 카로틴: 이 색소의 색은 노란색에서 주황색입니다. 진피와 표재성 근막의 각질층과 지방 세포에 존재합니다.
- 헤모글로빈(헤모글로빈이라고도 함): 이것은 혈액에서 발견되며 피부의 색소가 아니라 보라색을 발합니다.
- 옥시헤모글로빈: 그것은 또한 혈액에서 발견되며 피부의 색소가 아닙니다. 붉은 색을 발합니다.
자외선(UVR)의 지리적 분포와 전 세계 토착 피부 색소 분포 사이에는 상관관계가 있습니다. 더 많은 양의 UVR을 강조하는 지역은 일반적으로 적도 쪽에 더 가까이 위치한 어두운 피부의 개체군을 반영합니다. 열대 지방에서 멀리 떨어져 있고 극지방에 가까운 지역은 피부가 밝은 인구에 반영되는 UVR 농도가 낮습니다.[24]
같은 개체군에서 성인 인간 여성이 남성보다 피부 색소 침착이 상당히 가벼운 것으로 관찰되었습니다. 여성은 임신과 수유 기간 동안 칼슘이 더 많이 필요하고, 햇빛으로부터 합성되는 비타민 D는 칼슘 흡수에 도움이 됩니다. 이러한 이유로 여성들은 몸이 더 많은 칼슘을 흡수하도록 돕기 위해 피부가 더 가벼워지도록 진화했을 것으로 생각됩니다.[25]
Fitzpatrick scale은[26][27] 자외선(UV) 빛에 대한 다양한 유형의 피부의 일반적인 반응을 분류하기 위한 방법으로 1975년에 개발된 인간 피부 색상에 대한 수치 분류 스키마입니다.
| I | 항상 타오르고, 절대로 태우지 않습니다. | 창백, 뽀얀, 주근깨 |
| II | 보통 화상을 입거나, 가끔은 탠을 하기도 합니다. | 공정한 |
| III | 태울 수 있음, 보통 탠스 | 라이트브라운 |
| Ⅳ | 거의 화상을 입지 않고, 항상 탠을 합니다. | 올리브브라운 |
| V | 중등도의 체질 색소 침착 | 갈색 |
| Ⅵ | 현저한 체질색소침착 | 블랙입니다. |
노화

피부가 노화되면 얇아지고 쉽게 손상됩니다. 이 효과를 강화하는 것은 사람이 나이가 들면서 스스로 치유되는 피부의 능력이 감소한다는 것입니다.
무엇보다도 피부 노화는 볼륨과 탄력의 감소로 주목됩니다. 피부 노화의 내부적, 외부적 원인이 많습니다. 예를 들어 노화된 피부는 혈류량이 적고 선 활동이 더 낮습니다.
검증된 종합 등급 척도는 피부 노화의 임상 결과를 느슨함(소름), 운모(주름) 및 광노화의 다양한 측면, 즉 홍반(적색) 및 텔랑지텍타시아, 색소 침착 장애(갈색 변색), 태양 탄성증(황색), 각화증(이상 성장) 및 불량한 질감으로 분류했습니다.[28]
코르티솔은 콜라겐의 분해를 [29]일으켜 피부 노화를 가속화합니다.[30]
노화 방지 보충제는 피부 노화를 치료하는 데 사용됩니다.[citation needed]
포토에이징
광노화는 피부암 위험 증가와 손상된 피부의 외관이라는 두 가지 주요 관심사를 가지고 있습니다. 젊은 피부에서는 표피의 세포가 회전율이 빨라지기 때문에 자외선 손상이 더 빨리 치유되는 반면, 고령 인구에서는 피부가 얇아지고 세포 수복을 위한 표피 회전율이 낮아 진피층이 손상될 수 있습니다.[31]
자외선에 의한 DNA 손상
인간 피부 세포의 UV 조사는 DNA의 동일한 가닥에 인접한 티민 또는 시토신 잔기에서 직접적인 광화학 반응을 통해 DNA에 손상을 발생시킵니다.[32] DNA에서 두 개의 인접한 티민 염기 또는 두 개의 인접한 시토신 염기에 의해 형성되는 시클로부탄 피리미딘 이량체는 UV에 의해 유도되는 가장 빈번한 DNA 손상 유형입니다. 인간은 물론이고 다른 생물들도 이러한 자외선에 의한 손상을 뉴클레오티드 절단 복구 과정을 통해 복구할 수 있습니다.[32] 인간의 경우 이 수리 과정이 피부암으로부터 보호합니다.[32]
종류들
대부분의 사람의 피부는 모낭으로 덮여 있지만, 어떤 부분은 털이 없을 수 있습니다. 일반적인 피부에는 털이 많은 피부와 번들거리는 피부(털이 없는 피부) 두 가지 유형이 있습니다.[33] cutaneous라는 형용사는 (라틴어 cutis, skin에서 유래) "피부의"를 의미합니다.[34]
기능들
피부는 다음과 같은 기능을 수행합니다.
- 보호: 병원균으로부터의 해부학적 장벽과 신체 방어의 내부 환경과 외부 환경 사이의 손상; 피부의 랑게르한스 세포는 적응 면역 체계의 일부입니다.[7][35] 땀에는 박테리아의 세포벽 내의 결합을 깨는 리소자임이 포함되어 있습니다.[36]
- 감각: 열과 추위, 촉각, 압력, 진동, 조직 손상에 반응하는 다양한 신경 말단을 포함합니다. 체성 감각 시스템과 햅틱을 참조하십시오.
- 열 조절: 피부는 방사선, 대류 및 전도에 의한 에너지 손실을 정밀하게 제어할 수 있는 요구량보다 훨씬 더 많은 혈액 공급을 포함하고 있습니다. 확장된 혈관은 관류와 열 손실을 증가시키는 반면, 수축된 혈관은 피부 혈류를 크게 감소시키고 열을 보존합니다.
- 증발 제어: 피부는 비교적 건조하고 반투과성의 유체 손실 장벽을 제공합니다.[35] 이 기능의 상실은 화상의 대량 유체 손실의 원인이 됩니다.
- 미학과 의사소통: 다른 사람들은 우리의 피부를 보고 우리의 기분, 신체 상태, 매력을 평가할 수 있습니다.
- 저장 및 합성: 지질과 물의 저장 중심지 역할을 할 뿐만 아니라 피부의 특정 부분에 UV의 작용으로 비타민 D를 합성하는 수단 역할을 합니다.
- 배설: 땀에는 요소가 포함되어 있지만 그 농도는 소변의 130분의 1이므로 땀에 의한 배설은 기껏해야 온도 조절의 부차적인 기능입니다.
- 흡수: 피부의 가장 바깥쪽 0.25–0.40 mm를 구성하는 세포는 "거의 독점적으로 외부 산소에 의해 공급되지만" "전체 호흡에 대한 기여는 무시할 수 있습니다.[6] 또한, 니코틴 패치 또는 이온영동과 같이 피부를 통해, 연고 또는 접착 패치를 통해 약을 투여할 수 있습니다. 피부는 다른 많은 유기체에서 중요한 수송 부위입니다.
- 내수성: 피부는 방수 장벽 역할을 하기 때문에 필수 영양소가 몸 밖으로 씻겨 나가지 않습니다.[35]
피부식물상
사람의 피부는 미생물이 풍부한 환경입니다.[37][38] 19개의 박테리아 문에서 약 1,000종의 박테리아가 발견되었습니다.[38][37] 대부분은 4개의 문에서만 나옵니다. Actinomycetota (51.8%), Bacillota (24.4%), Pseudomonadota (16.5%), Bacteroidota (6.3%). 피지 지역은 프로피오니박테리아와 포도상구균 종이 주종이었습니다. 주요 생태 영역은 습윤, 건조, 피지의 세 가지입니다. 몸의 습기가 많은 곳에서는 포도상구균과 함께 코리네박테리아가 우세합니다. 건조한 지역에는 종들이 섞여 있지만 베타프로테오박테리아와 플라보박테리아가 지배적입니다. 생태학적으로 피지 지역은 습하고 건조한 지역보다 종 존재비가 더 컸습니다. 종별 사람 간 유사성이 가장 적은 영역은 손가락 사이, 발가락 사이, 겨드랑이, 탯줄 그루터기였습니다. 가장 유사한 것은 콧구멍 옆, 콧구멍(콧구멍 안쪽), 그리고 등 쪽이었습니다.
인간 피부 마이크로바이옴에 대한 인간 피부의 다양성을 반영하면서, "털이 많고 습기가 많은 겨드랑이는 매끄러운 건조한 팔뚝에서 짧은 거리에 있지만, 이 두 틈새는 열대 우림이 사막과 마찬가지로 생태학적으로 다를 가능성이 있습니다."[37]
NIH는 인간 마이크로바이옴 프로젝트를 수행하여 피부에 미치는 미생물과 건강과 질병에 대한 마이크로바이옴의 역할을 포함하는 인간 마이크로바이옴을 특성화했습니다.[39]
표피포도구균과 같은 미생물이 피부 표면에 서식합니다. 피부 식물군의 밀도는 피부 부위에 따라 다릅니다. 소독된 피부 표면은 모낭, 내장 및 비뇨생식기 입구의 더 깊은 영역에 존재하는 박테리아로부터 다시 집락화됩니다.
임상적 의의
피부의 질병에는 피부 감염 및 피부 신생물(피부암 포함)이 포함됩니다. 피부과는 피부 상태를 다루는 의학의 한 분야입니다.[33]
경추 7개, 흉부 12개, 요추 5개, 천추 5개가 있습니다. 수두-대상포진 감염에 의해 발생하는 대상포진과 같은 특정 질병은 피부염 분포와 관련된 통증 감각과 발진성 발진을 가지고 있습니다. 더마톰은 척추 손상 수준 진단에 도움이 됩니다. 피부세포 외에도 표피세포는 종양성 변화에 민감하여 다양한 암 유형이 발생합니다.
많은 의학적 징후가 피부를 통해 보여주기 때문에 피부는 다른 상태를 진단하는 데에도 가치가 있습니다. 피부색은 이러한 징후의 가시성에 영향을 미치며, 이는 인지하지 못하는 의료인의 오진의 원인이 됩니다.[41][42]
사회와 문화
위생 및 피부관리
피부는 어떤 양의 세척으로도 제거할 수 없는 효모와 박테리아를 포함한 자체 미생물 생태계를 지원합니다. 이 수치는 인간 피부의 평균 1.9 평방 미터(20 평방 피트)에 비해 크게 다르지만, 인간 피부의 표면에 있는 개별 박테리아의 수는 5천만 개로 추정됩니다. 얼굴과 같은 기름진 표면에는 평방 센티미터 당 7천8백만 개 이상의 박테리아가 포함되어 있을 수 있습니다. 이러한 방대한 양에도 불구하고 피부 표면에서 발견되는 모든 박테리아는 완두콩 크기의 부피에 맞을 것입니다.[43] 일반적으로 미생물은 서로를 견제하고 건강한 피부의 일부입니다. 균형이 흐트러지면 항생제가 미생물을 죽이고 그 결과 효모가 과증식하는 등 과증식과 감염이 일어날 수 있습니다. 피부는 구멍에서 몸의 내부 상피 내벽과 연속적이며, 각각의 피부는 미생물의 보체를 지지합니다.
화장품은 알레르기 반응을 일으킬 수 있으므로 피부에 조심해서 사용해야 합니다. 계절마다 땀의 증발을 촉진하기 위해 적절한 옷이 필요합니다. 햇빛, 물, 공기는 피부를 건강하게 유지하는 데 중요한 역할을 합니다.
지성피부
지성 피부는 피지선이 과도하게 활성화되어 자연적으로 건강한 피부 윤활제인 피지라는 물질을 생성하기 때문에 발생합니다.[8][44] 혈당지수가 높은 식단과 유제품(치즈 제외) 섭취는 IGF-1 생성을 증가시키고, 이는 다시 피지 생성을 증가시킵니다.[44] 피부를 과식하면 피지가 과잉 생성되는 것이 아니라 건조함을 유발할 수 있습니다.[44]
피부가 과도한 피지를 생성하면 지성 피부로 알려진 질감이 무겁고 두꺼워집니다.[44] 지성 피부는 번들거림, 잡티 및 여드름으로 대표됩니다.[8] 기름기가 필요한 수분을 표피 (피부의 가장 바깥 층)에 가두는 것을 돕기 [8]때문에 그러한 피부는 주름이나 다른 노화의 징후가 덜하기 때문에 지성 피부 타입이 반드시 나쁜 것은 아닙니다. 지성 피부 타입의 부정적인 측면은 지성 안색이 특히 피부 표면의 모공, 블랙헤드, 각질 축적에 취약하다는 것입니다.[8] 지성 피부는 질감이 느리고 거칠 수 있으며 눈과 목 주변을 제외한 모든 곳에 크고 선명하게 보이는 모공이 있는 경향이 있습니다.[8]
투과성
사람의 피부는 낮은 투과성을 가지고 있습니다. 즉, 대부분의 이물질은 피부를 통해 침투 및 확산되지 못합니다. 피부의 가장 바깥층인 각질층은 대부분의 무기 나노 크기 입자에 대한 효과적인 장벽입니다.[45][46] 이는 독소와 같은 외부 입자로부터 내부 조직과 접촉하지 않도록 하여 신체를 보호합니다. 그러나 경우에 따라서는 피부를 통해 입자가 체내로 들어올 수 있도록 하는 것이 바람직합니다. 이러한 입자 전달의 잠재적인 의학적 응용은 피부 투과성을 증가시키기 위한 나노 의학 및 생물학의 발전을 촉발했습니다. 경피적 입자 전달의 한 가지 응용은 암을 찾아 치료하는 것일 수 있습니다. 나노 의학 연구자들은 나노 입자가 성장 조절 메커니즘(암 세포)을 잃은 세포와 직접 상호 작용할 수 있는 활성 세포 분열의 표피와 다른 층을 목표로 합니다. 이러한 직접적인 상호작용은 특정 종양의 특성을 보다 정확하게 진단하거나 세포 특이성을 가진 약물을 전달하여 치료하는 데 사용될 수 있습니다.
나노입자
직경 40nm 이하의 나노 입자가 피부 침투에 성공했습니다.[47][48][49] 연구 결과 40nm 이상의 나노 입자는 각질층을 지나 피부로 침투하지 않는 것으로 확인됐습니다.[47] 침투하는 대부분의 입자는 피부 세포를 통해 확산되지만 일부 입자는 모낭을 타고 내려가 진피층에 도달합니다.
다양한 모양의 나노 입자에 대한 피부의 투과성도 연구되었습니다. 연구에 따르면 구면은 3개의 공간 차원에서 모두 대칭이기 때문에 구면 입자가 장방형(타원형) 입자에 비해 피부 침투 능력이 우수한 것으로 나타났습니다.[49] 한 연구에서는 두 가지 모양을 비교하여 표피와 진피 깊숙이 위치한 구형 입자를 보여주는 데이터를 기록했지만 타원체 입자는 주로 각질층과 표피층에서 발견되었습니다.[50] 나노 로드는 특유의 형광 특성 때문에 실험에 사용되지만 침투 정도는 미미했습니다.
다양한 재료의 나노 입자는 피부의 투과성 한계를 보여주었습니다. 많은 실험에서 직경 40nm 이하의 금 나노입자가 사용되며 표피까지 침투하는 것으로 나타났습니다. 산화티타늄(TiO2), 산화아연(ZnO), 은 나노입자는 각질층을 지나 피부로 침투하는 데 효과가 없습니다.[46][51] 셀렌화 카드뮴(CdSe) 양자점은 특정 특성을 가질 때 매우 효과적으로 침투하는 것으로 입증되었습니다. CdSe는 살아있는 유기체에 독성이 있기 때문에 입자는 표면 그룹으로 덮여 있어야 합니다. 폴리에틸렌 글리콜(PEG), PEG-아민 및 카르복실산으로 코팅된 양자점의 투과성을 비교한 실험에서 PEG와 PEG-아민 표면 그룹이 입자의 가장 큰 침투를 허용한다는 결론을 내렸습니다. 카르복실산 코팅 입자는 각질층을 지나 침투하지 않았습니다.[50]
투과율 증가
과학자들은 이전에 그 피부가 무기 입자에 대한 효과적인 장벽이라고 믿었습니다. 기계적 스트레스 요인의 손상은 투과성을 증가시키는 유일한 방법이라고 믿었습니다.[52]
최근에는 보다 간단하고 효과적인 피부 투과율을 높이기 위한 방법들이 개발되고 있습니다. 자외선(UVR)은 피부 표면을 약간 손상시키고 나노 입자의 침투를 쉽게 하는 시간 의존적 결함을 유발합니다.[53] UVR의 높은 에너지는 세포의 재구조화를 일으켜 각질층과 표피층의 경계를 약화시킵니다.[53][52] 피부 손상은 일반적으로 경피 수분 손실(TEWL)로 측정되지만, TEWL이 최고치에 도달하는 데는 3-5일이 걸릴 수 있습니다. TEWL이 최고치에 도달하면 나노 입자의 최대 밀도가 피부에 스며들 수 있습니다. UVR 노출 후의 투과성 증가 효과는 피부에 침투하는 입자의 수 증가로 이어질 수 있지만, 크기 및 물질이 다른 입자에 비해 UVR 노출 후 피부의 구체적인 투과성은 결정되지 않았습니다.[53]
피부 손상에 의해 나노입자의 침투를 증가시키는 다른 방법들이 있습니다: 테이프 스트리핑은 테이프를 피부에 바른 후 들어 올려 피부의 최상층을 제거하는 과정이고, 피부 마모는 피부 표면의 상단 5~10 μm를 면도하여 이루어집니다. 화학적 강화는 폴리비닐피롤리돈(PVP)과 같은 화학물질을 적용하고, DMSO(dimethyl sulfoxide) 및 올레산(oleic acid)은 피부 표면에 침투성을 증가시키고,[54][55] 전기천공은 짧은 전기장 펄스를 적용하여 피부 투과성을 증가시킵니다. 펄스는 인가 시 밀리초 단위의 고전압입니다. 전하를 띤 분자는 피부가 전기장 펄스에 노출된 후 중성 분자보다 더 자주 피부에 침투합니다. 결과는 분자가 전기천공된 피부에 쉽게 스며들도록 100μm 정도로 나타났습니다.[55]
적용들
나노 의학에서 관심이 많은 분야는 매우 적은 부작용으로 치료제의 무통 적용 가능성 때문에 경피 패치입니다. 경피 패치는 피부의 투과성의 한계 때문에 니코틴과 같은 소수의 약물을 투여하는 데 제한되어 왔습니다. 피부 투과성을 높이는 기술의 발달로 경피 패치를 통해 적용할 수 있는 약물이 늘어나고 환자에게 더 많은 옵션이 제공되고 있습니다.[55]
피부의 투과성을 높이면 나노입자가 암세포에 침투하여 표적이 될 수 있습니다. 나노입자는 비침습적으로 암을 진단하는 방법으로 멀티모달 이미징 기술과 함께 사용되어 왔습니다. 투과성이 높은 피부를 통해 표면에 항체가 부착된 양자점이 쥐의 암 종양에 성공적으로 침투해 식별할 수 있게 했습니다. 종양 표적화는 형광 현미경을 사용하여 입자를 들뜨게 할 수 있고 암세포를 파괴할 빛 에너지와 열을 방출하기 때문에 유익합니다.[56]
자외선 차단제와 자외선 차단제
자외선 차단제와 자외선 차단제는 서로 다른 중요한 스킨케어 제품이지만 둘 다 태양으로부터 완벽한 보호를 제공합니다.[57]
선크림—썬블록은 자외선 차단제보다 불투명하고 강력하며, 자외선 차단제는 자외선 차단제와 태양으로부터의 방사선을 대부분 차단할 수 있고, 하루에 여러 번 덧칠할 필요가 없습니다. 이산화 티타늄과 산화 아연은 자외선 차단제의 중요한 성분 중 하나입니다.[58]
자외선 차단제—자외선 차단제의 성분이 햇빛에 노출되면 더 빠른 속도로 분해되고, 일부 방사선이 피부까지 침투할 수 있지만 자외선 차단제는 피부에 도포되면 더 투명해지고 자외선 차단제/자외선 차단 기능도 있습니다. 자외선 차단제가 더 효과적이기 위해서는 자외선 차단율이 높은 것을 꾸준히 덧발라 사용하는 것이 필요합니다.
다이어트
레티노이드라고도 불리는 비타민 A는 각질화를 정상화하고, 여드름의 원인이 되는 피지 생성을 억제하며, 광손상, 스트리에, 셀룰라이트를 역전시켜 치료함으로써 피부에 도움이 됩니다.
비타민 D와 유사체는 피부 면역 체계와 상피 증식을 하향 조절하는 동시에 분화를 촉진하는 데 사용됩니다.
비타민 C는 콜라겐 합성을 조절하고 장벽 지질을 형성하며 비타민 E를 재생시키고 광보호 기능을 제공하는 항산화 물질입니다.
비타민 E는 산화적 손상으로부터 보호하고 유해한 자외선으로부터도 보호하는 막 항산화제입니다.
여러 과학적 연구를 통해 기준선 영양 상태의 변화가 피부 상태에 영향을 미친다는 것을 확인했습니다.
메이요 클리닉에서는 과일과 채소, 통곡물, 짙은 잎이 무성한 녹색, 견과류, 씨앗 등 피부에 도움이 되는 식품을 소개합니다.[61]
참고 항목
- 산성 맨틀
- 아담과 이브.
- 인류피학 서지학
- 인조피부
- 굳은살, 두꺼운 피부 부위
- 피부질환 목록
- 피부구조 발달
- 지문, 손가락 끝 피부
- 인체
- 과도한 피부색에 대한 과색소침착
- 인터트리진스
- 마이스너의 말뭉치
- 누드비치
- 나체수영
- 나체
- 파키니아 말뭉치
- 폴리페놀 항산화제
- 피부암
- 피부병변
- 피부 수선
- 일광욕
참고문헌
- ^ a b c d e Herron AJ (5 December 2009). "Pigs as Dermatologic Models of Human Skin Disease" (PDF). ivis.org. DVM Center for Comparative Medicine and Department of Pathology Baylor College of Medicine Houston, Texas. Retrieved 27 January 2018.
pig skin has been shown to be the most similar to human skin. Pig skin is structurally similar to human epidermal thickness and dermal-epidermal thickness ratios. Pigs and humans have similar hair follicle and blood vessel patterns in the skin. Biochemically pigs contain dermal collagen and elastic content that is more similar to humans than other laboratory animals. Finally pigs have similar physical and molecular responses to various growth factors.
- ^ a b c d e Liu J, Kim D, Brown L, Madsen T, Bouchard GF. "Comparison of Human, Porcine and Rodent Wound Healing With New Miniature Swine Study Data" (PDF). sinclairresearch.com. Sinclair Research Centre, Auxvasse, MO, USA; Veterinary Medical Diagnostic Laboratory, Columbia, MO, USA. Archived from the original (PDF) on 27 January 2018. Retrieved 27 January 2018.
Pig skin is anatomically, physiologically, biochemically and immunologically similar to human skin
- ^ Maton A, Hopkins J, McLaughlin CW, Johnson S, Warner MQ, LaHart D, Wright JD (1893). Human Biology and Health. Englewood Cliffs, New Jersey, USA: Prentice Hall. ISBN 978-0-13-981176-0.
- ^ a b Wilkinson PF, Millington R (2009). Skin (Digitally printed version ed.). Cambridge: Cambridge University Press. pp. 49–50. ISBN 978-0-521-10681-8.
- ^ Bennett H (25 May 2014). "Ever wondered about your skin?". The Washington Post. Retrieved 27 October 2014.
- ^ a b Stücker M, Struk A, Altmeyer P, Herde M, Baumgärtl H, Lübbers DW (February 2002). "The cutaneous uptake of atmospheric oxygen contributes significantly to the oxygen supply of human dermis and epidermis". The Journal of Physiology. 538 (Pt 3): 985–994. doi:10.1113/jphysiol.2001.013067. PMC 2290093. PMID 11826181.
- ^ a b Proksch E, Brandner JM, Jensen JM (December 2008). "The skin: an indispensable barrier". Experimental Dermatology. 17 (12): 1063–1072. doi:10.1111/j.1600-0625.2008.00786.x. PMID 19043850. S2CID 31353914.
- ^ a b c d e f "Skin care" (분석), Health-Cares.net , 2007, 웹페이지: 2007년 12월 12일 Wayback Machine에서 HCare 아카이브 완료
- ^ Del Rosso JQ, Levin J (September 2011). "The clinical relevance of maintaining the functional integrity of the stratum corneum in both healthy and disease-affected skin". The Journal of Clinical and Aesthetic Dermatology. 4 (9): 22–42. doi:10.1111/j.1365-2133.1990.tb06268.x. PMC 3175800. PMID 21938268.
- ^ Kligman A (2006). "A brief history of how the dead stratum corneum became alive". Skin Barrier. New York: Taylor & Francis. pp. 35–44. ISBN 9780429163470.
- ^ "The human proteome in skin – The Human Protein Atlas". www.proteinatlas.org.
- ^ Uhlén M, Fagerberg L, Hallström BM, Lindskog C, Oksvold P, Mardinoglu A, et al. (January 2015). "Proteomics. Tissue-based map of the human proteome". Science. 347 (6220): 1260419. doi:10.1126/science.1260419. PMID 25613900. S2CID 802377.
- ^ Edqvist PH, Fagerberg L, Hallström BM, Danielsson A, Edlund K, Uhlén M, Pontén F (February 2015). "Expression of human skin-specific genes defined by transcriptomics and antibody-based profiling". The Journal of Histochemistry and Cytochemistry. 63 (2): 129–141. doi:10.1369/0022155414562646. PMC 4305515. PMID 25411189.
- ^ Snyder WS, Cook M, Nasset E, Karhausen L, Howells GP, Tipton IH (1975). "ICRP Publication 23: report of the task group on reference man". www.icrp.org. Elmsford, NY: International Commission on Radiological Protection. Retrieved 30 October 2023.
- ^ Valentin J (September 2002). "Basic anatomical and physiological data for use in radiological protection: reference values: ICRP Publication 89". Annals of the ICRP. 32 (3–4): 1–277. doi:10.1016/S0146-6453(03)00002-2. S2CID 222552. Retrieved 30 October 2023.
- ^ Zankl M (2010). "Adult male and female reference computational phantoms (ICRP Publication 110)". Japanese Journal of Health Physics. 45 (4): 357–369. doi:10.5453/jhps.45.357. Retrieved 30 October 2023.
- ^ Hatton IA, Galbraith ED, Merleau NS, Miettinen TP, Smith BM, Shander JA (September 2023). "The human cell count and size distribution". Proceedings of the National Academy of Sciences of the United States of America. 120 (39): e2303077120. Bibcode:2023PNAS..12003077H. doi:10.1073/pnas.2303077120. PMC 10523466. PMID 37722043.
- ^ Max Planck Society. "Cellular cartography: Charting the sizes and abundance of our body's cells reveals mathematical order underlying life". medicalxpress.com. Retrieved 30 October 2023.
- ^ "Human Cell data". humancelltreemap.mis.mpg.de. Retrieved 30 October 2023.
- ^ Muehlenbein M (2010). Human Evolutionary Biology. Cambridge University Press. pp. 192–213. ISBN 978-1139789004.
- ^ Jablonski NG (2006). Skin: a Natural History. Berkeley: University of California Press. ISBN 978-0520954816.
- ^ B. D. 의 일반 해부학 핸드북. 샤우라시아. ISBN 978-81-239-1654-5
- ^ "Pigmentation of Skin". Mananatomy.com. Archived from the original on 7 October 2012. Retrieved 3 June 2019.
- ^ Webb AR (September 2006). "Who, what, where and when-influences on cutaneous vitamin D synthesis". Progress in Biophysics and Molecular Biology. 92 (1): 17–25. doi:10.1016/j.pbiomolbio.2006.02.004. PMID 16766240.
- ^ Jablonski NG, Chaplin G (July 2000). "The evolution of human skin coloration". Journal of Human Evolution. 39 (1): 57–106. doi:10.1006/jhev.2000.0403. PMID 10896812.
- ^ "The Fitzpatrick Skin Type Classification Scale". Skin Inc. (November 2007). 28 May 2009. Retrieved 7 January 2014.
- ^ "Fitzpatrick Skin Type" (PDF). Australian Radiation Protection and Nuclear Safety Agency. Archived from the original (PDF) on 31 March 2016. Retrieved 7 January 2014.
- ^ Alexiades-Armenakas MR, Dover JS, Arndt KA (May 2008). "The spectrum of laser skin resurfacing: nonablative, fractional, and ablative laser resurfacing". Journal of the American Academy of Dermatology. 58 (5): 719–737. doi:10.1016/j.jaad.2008.01.003. PMID 18423256.
- ^ Cutroneo KR, Sterling KM (May 2004). "How do glucocorticoids compare to oligo decoys as inhibitors of collagen synthesis and potential toxicity of these therapeutics?". Journal of Cellular Biochemistry. 92 (1): 6–15. doi:10.1002/jcb.20030. PMID 15095399. S2CID 24160757.(구독 필수)
- ^ Oikarinen A (2004). "Connective tissue and aging". International Journal of Cosmetic Science. 26 (2): 107. doi:10.1111/j.1467-2494.2004.213_6.x. ISSN 0142-5463.(구독 필수)
- ^ Gilchrest BA (April 1990). "Skin aging and photoaging". Dermatology Nursing. 2 (2): 79–82. PMID 2141531.
- ^ a b c Lee JW, Ratnakumar K, Hung KF, Rokunohe D, Kawasumi M (May 2020). "Deciphering UV-induced DNA Damage Responses to Prevent and Treat Skin Cancer". Photochemistry and Photobiology. 96 (3): 478–499. doi:10.1111/php.13245. PMC 7651136. PMID 32119110.
- ^ a b Marks, James G; Miller, Jeffery (2006). 피부과의 미용실과 마크스 원리입니다. (4화). 엘스비어 주식회사 ISBN 1-4160-3185-5.
- ^ "Definition of CUTANEOUS". www.merriam-webster.com. Retrieved 4 March 2022.
- ^ a b c Madison KC (August 2003). "Barrier function of the skin: "la raison d'être" of the epidermis". The Journal of Investigative Dermatology. 121 (2): 231–241. doi:10.1046/j.1523-1747.2003.12359.x. PMID 12880413.
- ^ Todar K. "Immune Defense against Bacterial Pathogens: Innate Immunity". textbookofbacteriology.net. Retrieved 19 April 2017.
- ^ a b c Grice EA, Kong HH, Conlan S, Deming CB, Davis J, Young AC, et al. (May 2009). "Topographical and temporal diversity of the human skin microbiome". Science. 324 (5931): 1190–1192. Bibcode:2009Sci...324.1190G. doi:10.1126/science.1171700. PMC 2805064. PMID 19478181.
- ^ a b 파파스 S. (2009) 당신의 몸은... 박테리아의 이상한 나라입니다. 과학2009년 6월 2일 Wayback Machine에서 보관된 NOW Daily News
- ^ "NIH Human Microbiome Project". Hmpdacc.org. Retrieved 3 June 2019.
- ^ Yousef H, Alhajj M, Sharma S (2023). "Anatomy, Skin (Integument), Epidermis". StatPearls. Treasure Island (FL): StatPearls Publishing. PMID 29262154. Retrieved 28 September 2023.
- ^ "Color awareness: A must for patient assessment". American Nurse. 11 January 2011.
- ^ McCue D (21 July 2020). "Medical student creates handbook for diagnosing conditions in Black and brown skin". As It Happens. CBC Radio. Retrieved 15 December 2020.
- ^ 테오도르 로즈베리. 라이프 온 맨: Seker & Warburg, 1969 ISBN 0-670-42793-4
- ^ a b c d Sakuma TH, Maibach HI (2012). "Oily skin: an overview". Skin Pharmacology and Physiology. 25 (5): 227–235. doi:10.1159/000338978. PMID 22722766. S2CID 2446947.
- ^ Baroli B (January 2010). "Penetration of nanoparticles and nanomaterials in the skin: fiction or reality?". Journal of Pharmaceutical Sciences. 99 (1): 21–50. doi:10.1002/jps.21817. PMID 19670463.
- ^ a b Filipe P, Silva JN, Silva R, Cirne de Castro JL, Marques Gomes M, Alves LC, et al. (2009). "Stratum corneum is an effective barrier to TiO2 and ZnO nanoparticle percutaneous absorption". Skin Pharmacology and Physiology. 22 (5): 266–275. doi:10.1159/000235554. PMID 19690452. S2CID 25769287.
- ^ a b Vogt A, Combadiere B, Hadam S, Stieler KM, Lademann J, Schaefer H, et al. (June 2006). "40 nm, but not 750 or 1,500 nm, nanoparticles enter epidermal CD1a+ cells after transcutaneous application on human skin". The Journal of Investigative Dermatology. 126 (6): 1316–1322. doi:10.1038/sj.jid.5700226. PMID 16614727.
- ^ a b Ryman-Rasmussen JP, Riviere JE, Monteiro-Riviere NA (May 2006). "Penetration of intact skin by quantum dots with diverse physicochemical properties". Toxicological Sciences. 91 (1): 159–165. doi:10.1093/toxsci/kfj122. PMID 16443688.
- ^ a b Ryman-Rasmussen JP, Riviere JE, Monteiro-Riviere NA (May 2006). "Penetration of intact skin by quantum dots with diverse physicochemical properties". Toxicological Sciences. 91 (1): 159–165. doi:10.1093/toxsci/kfj122. PMID 16443688.
- ^ Larese FF, D'Agostin F, Crosera M, Adami G, Renzi N, Bovenzi M, Maina G (January 2009). "Human skin penetration of silver nanoparticles through intact and damaged skin". Toxicology. 255 (1–2): 33–37. doi:10.1016/j.tox.2008.09.025. PMID 18973786.
- ^ a b Mortensen LJ, Oberdörster G, Pentland AP, Delouise LA (September 2008). "In vivo skin penetration of quantum dot nanoparticles in the murine model: the effect of UVR". Nano Letters. 8 (9): 2779–2787. Bibcode:2008NanoL...8.2779M. doi:10.1021/nl801323y. PMC 4111258. PMID 18687009.
- ^ a b c Mortensen L, Zheng H, Faulknor R, De Benedetto A, Beck L, DeLouise LA (2009). Osinski M, Jovin TM, Yamamoto K (eds.). "Increased in vivo skin penetration of quantum dots with UVR and in vitro quantum dot cytotoxicity". Colloidal Quantum Dots for Biomedical Applications IV. 7189: 718919–718919–12. Bibcode:2009SPIE.7189E..19M. doi:10.1117/12.809215. ISSN 0277-786X. S2CID 137060184.
- ^ Sokolov K, Follen M, Aaron J, Pavlova I, Malpica A, Lotan R, Richards-Kortum R (May 2003). "Real-time vital optical imaging of precancer using anti-epidermal growth factor receptor antibodies conjugated to gold nanoparticles". Cancer Research. 63 (9): 1999–2004. PMID 12727808.
- ^ a b c Prausnitz MR, Mitragotri S, Langer R (February 2004). "Current status and future potential of transdermal drug delivery". Nature Reviews. Drug Discovery. 3 (2): 115–124. doi:10.1038/nrd1304. PMID 15040576. S2CID 28888964.
- ^ Gao X, Cui Y, Levenson RM, Chung LW, Nie S (August 2004). "In vivo cancer targeting and imaging with semiconductor quantum dots". Nature Biotechnology. 22 (8): 969–976. doi:10.1038/nbt994. PMID 15258594. S2CID 41561027.
- ^ "Sunblock vs. sunscreen: Which one should you use?". Baylor Scott & White Health. 17 March 2022.
- ^ "Nanotechnology Information Center: Properties, Applications, Research, and Safety Guidelines". American Elements.
- ^ Shapiro SS, Saliou C (October 2001). "Role of vitamins in skin care". Nutrition. 17 (10): 839–844. doi:10.1016/S0899-9007(01)00660-8. PMID 11684391.
- ^ Boelsma E, van de Vijver LP, Goldbohm RA, Klöpping-Ketelaars IA, Hendriks HF, Roza L (February 2003). "Human skin condition and its associations with nutrient concentrations in serum and diet". The American Journal of Clinical Nutrition. 77 (2): 348–355. doi:10.1093/ajcn/77.2.348. PMID 12540393.
- ^ "Foods for healthy skin". Mayo Clinic.
외부 링크
 Wikimedia Commons의 인간 피부 관련 미디어
Wikimedia Commons의 인간 피부 관련 미디어- "Skin Conditions". MedlinePlus. U.S. National Library of Medicine. Retrieved 12 November 2013.



