도파민 베타-하이드록실라아제
Dopamine beta-hydroxylase| DBH | |||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| 식별자 | |||||||||||||||||||||||||
| 별칭 | DBH, DBM, 도파민 베타-모노옥시제네제, 도파민 베타-하이드록시제네제, 도파민 β-하이드록시아제, ORTYP1 | ||||||||||||||||||||||||
| 외부 ID | OMIM: 609312 MGI: 94864 HomoloGene: 615 GeneCard: DBH | ||||||||||||||||||||||||
| EC 번호 | 1.14.17.1 | ||||||||||||||||||||||||
| |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| 직교체 | |||||||||||||||||||||||||
| 종 | 인간 | 마우스 | |||||||||||||||||||||||
| 엔트레스 | |||||||||||||||||||||||||
| 앙상블 | |||||||||||||||||||||||||
| 유니프로트 | |||||||||||||||||||||||||
| RefSeq(mRNA) | |||||||||||||||||||||||||
| RefSeq(단백질) | |||||||||||||||||||||||||
| 위치(UCSC) | Chr 9: 133.64 – 133.66Mb | n/a | |||||||||||||||||||||||
| PubMed 검색 | [2] | [3] | |||||||||||||||||||||||
| 위키다타 | |||||||||||||||||||||||||
| |||||||||||||||||||||||||
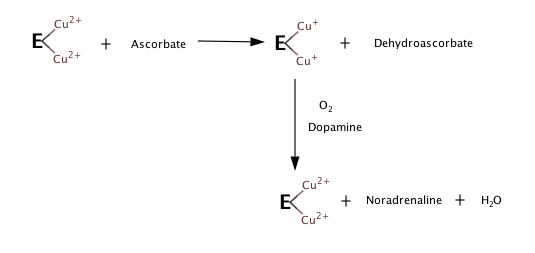
도파민 베타-하이드록실라아제(DBH)는 도파민 베타-모노옥시게나제(DBH)로 알려진 효소(EC 1.14.17.1)로 인간에서 DBH 유전자에 의해 암호화된 것이다. 도파민 베타-하이드록실라아제는 도파민의 노레피네프린으로의 전환을 촉진한다.
효소의 세 기질은 도파민, 비타민C(아스코르베이트), O이다2. 그 제품들은 노레피네프린, 탈수증, 그리고 HO이다2.
DBH는 동일 서브유닛 4개로 구성된 290kDa 구리 함유 산소효소로, 그 활성도에는 공동 인자로서 아스코르베이트가 필요하다.[4]
그것은 막에 묶여 있는 소분자 신경전달물질의 합성에 관여하는 유일한 효소로서, 노레피네프린이 베실체 안에서 합성된 것으로 알려진 유일한 송신기가 되게 한다. 중추신경계(즉, locus coeruleus)와 말초신경계(즉, 교감신경계)의 노라드레날린 신경세포(noradrenergic nerrones)뿐만 아니라 부신중뇌의 크로마핀세포에서도 발현된다.
카탈루션
| 도파민 베타-모노옥시제네제 | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| 식별자 | |||||||||
| EC 번호 | 1.14.17.1 | ||||||||
| CAS 번호. | 9013-38-1 | ||||||||
| 데이터베이스 | |||||||||
| 인텐츠 | IntEnz 뷰 | ||||||||
| 브렌다 | 브렌다 입력 | ||||||||
| 엑스퍼시 | 나이스자이메 뷰 | ||||||||
| 케그 | KEG 입력 | ||||||||
| 메타사이크 | 대사통로 | ||||||||
| 프리암 | 프로필 | ||||||||
| PDB 구조 | RCSB PDB PDBe PDBsum | ||||||||
| 진 온톨로지 | 아미고 / 퀵고 | ||||||||
| |||||||||
기질, 즉 산소가 없을 때 일어나는 일을 관찰한 결과, 다음의 단계는 히드록실화 반응을 구성하는 것으로 보인다.[5][6]
DBH 메커니즘의 자세한 내용은 아직 확인되지 않았지만 DBH는 또 다른 효소인 펩티딜글리신 α-히드록시드화 모노옥시제나제(PHM)와 동질성이 있다.DBH와 PHM은 유사한 구조를 공유하기 때문에 PHM 메커니즘에 대해 알려진 것을 기반으로 DBH 메커니즘을 모델링하는 것이 가능하다.[7]
기질특성
도파민 베타-하이드록실라제는 도파민뿐만 아니라 다른 페닐시아민 유도체의 히드록실화를 촉진한다. 최소 요건은 페닐틸아민 골격인 것 같다: 아미노 그룹에서 끝나는 2탄소 사이드 체인을 가진 벤젠 링이다.[5]
인간 혈청 및 뇌척수액의 DBH 활성도 분석
인간 혈청에서의 DBH 활성도는 분광학적 방법 또는 광다이오드 배열 검출기(UHPLC-PDA)를 사용한 초고성능 액체 크로마토그래피(Chromatography)의 도움으로 추정할 수 있다.[12] 전기화학검출기(HPLC-ECD)를 이용한 고성능 액체 크로마토그래피를 이용한 뇌척수액의 DBH 활성 감지를 위한 민감한 측정도 앞에서 설명하였다.[13]
DBH loci의 표현 정량적 특성 loci(eQTL)
DBH loci의 단일 뉴클레오티드 다형성(SNPs)[14][15]과 같은 유전적 변형이 DBH 활동과 관련이 있는 것으로 밝혀졌으며 잘 알려진 표현 양적 특성 loci이다. 두 가지 규제 SNP(rs16111115 및 rs1989787)에서 알레르 변형이 이 유전자의 전사에도 영향을 미치는 것으로 나타났다. 도파민 베타 히드록실라아제 결핍증에서[18] 확인된 돌연변이와 이 유전자의 rs6271과 같은 비동기식 SNP는 소포체성 망막에서 단백질의 분비를 일으키는 것으로 밝혀졌다.[19]
임상적 유의성
DBH는 주로 카테콜아민과 미량 아민 생합성에 기여한다. 또한 이러한 물질과 관련된 제노바이오틱스의 대사에도 참여하는데, 예를 들어 인간 DBH 효소는 암페타민과 파라-하이드록시암페타민의 베타-하이드록시암페타민을 촉매하여 각각 노레페드린과 파라-하이드록시노레페드린을 생산한다.[20][21][22]
DBH는 알코올 중독과[23] 흡연,[24] 주의력 결핍 과잉행동 장애,[25] 정신분열증,[26] 알츠하이머병과 같은 의사결정 및 중독성 약물과 관련된 조건의 상관관계 요인으로 연루되어 왔다.[27] 부적절한 DBH는 도파민 베타 수산화효소 결핍증이라고 불린다.
근위촉진자 SNPs rs1989787 및 rs16111115는 조현병 환자에서 인식과 관련이 있는 것으로 밝혀졌다.[28] 또한 이러한 SNP(rs1989787;rs16111115)와 원위촉진 변종 19bp Ins/Del(rs141116007)은 Tadive diskinesia 양성 정신분열증 환자에서 비정상적 비자발적 이동 척도와 관련이 있었다.[28] 세 가지 변종 중 근위부 추진자 SNP(rs16111115)[28]는 타디브 이질병 양성 정신분열증 환자에서 양성 및 음성 증후군 척도(PANS) 점수와 연관되었다.
구조
도파민 베타-하이드록실라아제의 안정적인 크리스탈을 얻기란 어려웠다. 따라서 PHM과의 비교와 일차 순서에 기초한 호몰로지 모델을 이용할 수 있다.[29]
하지만 2016년에도 수정구조가 나왔다.[30]
규제 및 억제
이 단백질은 알로스테릭 조절의 모르핀 모델을 사용할 수 있다.[31]
억제제
| 하이드[a] | HP[b] | QCA[c] | IQCA[d] | BI[e] | IAA[f] | |
|---|---|---|---|---|---|---|
| , 경쟁력 | 아스코르베이트 | 아스코르베이트 | 아스코르베이트 | 아스코르베이트 | 아스코르베이트 | 아스코르베이트 |
| 경쟁력 없음 | 티라미네 | 티라미네 | ||||
| 혼합 | 티라미네 | 티라미네 | 티라미네 | 티라미네 | ||
| 아스코르베이트는 공동 인자, 티라민은 DBH의 명명 기질인 도파민을 대체한다. | ||||||
DBH는 이설피람,[32] 트로폴론,[33] 그리고 가장 선택적으로 네피카스타트에 의해 억제된다.[34]
DBH is reversibly inhibited by l-2H-Phthalazine hydrazone (hydralazine; HYD), 2-1H-pyridinone hydrazone (2-hydrazinopyridine; HP), 2-quinoline-carboxylic acid (QCA), l-isoquinolinecarboxylic acid (IQCA), 2,2'-bi-lH-imidazole (2,2'-biimidazole; BI), and IH-imidazole-4-acetic acid (imidazole-4-acetic acid; IAA). HID,[35] QCA, IAA는 불가사의한 경쟁이다.
명명법
이 효소 등급의 체계적 명칭은 3,4-디하이드록시페네틸아민, 아스코르베이트:옥시겐산화효소(베타하이드록시릴레이팅)이다.
일반적으로 사용되는 다른 이름에는 다음이 포함된다.
- 도파민 베타-모노옥시제네제
- 도파민 베타산화효소
- 막 관련 도파민 베타-모노옥시제네제(MDBH)
- 가용성 도파민 베타-모노옥시제네제(SDBH)
- 도파민-B-하이드록실라아제
- 3,4-디하이드록시페네틸아민 베타-제아제
- 4-(2-142-메틸) 피로카테콜 베타-제아제
- 도파 베타 아산화효소
- 도파민 베타-화효소
- 도파민 수산화효소
- 페닐라민 베타-벡실라아제
- (3,4-dihydroxyphenethylamine) 베타-화합-화합효소
참조
- ^ a b c GRCh38: 앙상블 릴리스 89: ENSG00000123454 - 앙상블, 2017년 5월
- ^ "Human PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ "Mouse PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ Rush RA, Geffen LB (1980). "Dopamine beta-hydroxylase in health and disease". Critical Reviews in Clinical Laboratory Sciences. 12 (3): 241–77. doi:10.3109/10408368009108731. PMID 6998654.
- ^ a b Kaufman S, Bridgers WF, Baron J (1968). "The Mechanism of Action of Dopamine beta-Hydroxylase". Advances in Chemistry. 77, chapter 73: 172–176. doi:10.1021/ba-1968-0077.ch073. ISBN 0-8412-0078-5.
- ^ Friedman S, Kaufman S (May 1966). "An electron paramagnetic resonance study of 3,4-dihydroxyphenylethylamine beta-hydroxylase". The Journal of Biological Chemistry. 241 (10): 2256–9. doi:10.1016/S0021-9258(18)96614-7. PMID 4287853.
- ^ Prigge ST, Mains RE, Eipper BA, Amzel LM (August 2000). "New insights into copper monooxygenases and peptide amidation: structure, mechanism and function". Cellular and Molecular Life Sciences. 57 (8–9): 1236–59. doi:10.1007/pl00000763. PMID 11028916. S2CID 12738480.
- ^ Broadley KJ (March 2010). "The vascular effects of trace amines and amphetamines". Pharmacology & Therapeutics. 125 (3): 363–375. doi:10.1016/j.pharmthera.2009.11.005. PMID 19948186.
- ^ Lindemann L, Hoener MC (May 2005). "A renaissance in trace amines inspired by a novel GPCR family". Trends in Pharmacological Sciences. 26 (5): 274–281. doi:10.1016/j.tips.2005.03.007. PMID 15860375.
- ^ Wang X, Li J, Dong G, Yue J (February 2014). "The endogenous substrates of brain CYP2D". European Journal of Pharmacology. 724: 211–218. doi:10.1016/j.ejphar.2013.12.025. PMID 24374199.
- ^ Nagatsu T, Udenfriend S (1972). "Photometric Assay of Dopamine-β-Hydroxylase Activity in Human Blood". Clinical Chemistry. 18 (9): 980–983. doi:10.1093/clinchem/18.9.980. PMID 5052101.
- ^ Punchaichira TJ, Deshpande SN, Thelma BK (2018). "Determination of Dopamine-β-hydroxylase Activity in Human Serum Using UHPLC-PDA Detection". Neurochemical Research. 43 (12): 2324–2332. doi:10.1007/s11064-018-2653-1. PMID 30357655. S2CID 53024826.
- ^ Matsui H, Kato T, Yamamoto C, Fujita K, Nagatsu T (1981). "Highly sensitive assay for dopamine-beta-hydroxylase activity in human cerebrospinal fluid by high performance liquid chromatography-electrochemical detection: properties of the enzyme". Journal of Neurochemistry. 37 (2): 289–296. doi:10.1111/j.1471-4159.1981.tb00454.x. PMID 7264660. S2CID 42736106.
- ^ Zabetian CP, Anderson GM, Buxbaum SG, Elston RC, Ichinose H, Nagatsu T, Kim KS, Kim CH, Malison RT, Gelernter J, Cubells JF (2001). "A quantitative-trait analysis of human plasma-dopamine beta-hydroxylase activity: evidence for a major functional polymorphism at the DBH locus". American Journal of Human Genetics. 68 (2): 515–22. doi:10.1086/318198. PMC 1235285. PMID 11170900.
- ^ Punchaichira TJ, Prasad S, Deshpande SN, Thelma BK (2016). "Deep sequencing identifies novel regulatory variants in the distal promoter region of the dopamine-beta-hydroxylase gene". Pharmacogenetics and Genomics. 26 (7): 311–23. doi:10.1097/FPC.0000000000000214. PMID 26959714. S2CID 205601803.
- ^ Chen Y, Wen G, Rao F, Zhang K, Wang L, Rodriguez-Flores JL, Sanchez, AP, Mahata M, Taupenot L, Sun P, Mahata SK, Tayo B, Schork NJ, Ziegler MG, Hamilton BA, O'Connor DT (2010). "Human dopamine beta-hydroxylase (DBH) regulatory polymorphism that influences enzymatic activity, autonomic function, and blood pressure". Journal of Hypertension. 28 (1): 76–86. doi:10.1097/HJH.0b013e328332bc87. PMC 2860271. PMID 20009769.
- ^ Chen Y, Zhang K, Wen G, Rao F, Sanchez AP, Wang L, Rodriguez-Flores JL, Mahata M, Mahata SK, Waalen J, Ziegler MG, Hamilton BA, O'Connor DT (2011). "Human dopamine beta-hydroxylase promoter variant alters transcription in chromaffin cells, enzyme secretion, and blood pressure". American Journal of Hypertension. 24 (1): 24–32. doi:10.1038/ajh.2010.186. PMC 4906639. PMID 20814407.
- ^ Kim CH, Leung A, Huh YH, Yang E, Kim DJ, Leblanc P, Ryu H, Kim K, Kim DW, Garland EM, Raj SR, Biaggioni I, Robertson D, Kim KS (2011). "Norepinephrine deficiency is caused by combined abnormal mRNA processing and defective protein trafficking of dopamine beta-hydroxylase". Journal of Biological Chemistry. 286 (11): 9196–204. doi:10.1074/jbc.M110.192351. PMC 3059068. PMID 21209083.
- ^ Punchaichira TJ, Dey SK, Mukhopadhyay A, Kundu S, Thelma BK (2017). "Characterization of SNPs in the dopamine-beta-hydroxylase gene providing new insights into its structure-function relationship". Neurogenetics. 18 (3): 155–168. doi:10.1007/s10048-017-0519-3. PMID 28707163. S2CID 5259134.
- ^ Glennon RA (2013). "Phenylisopropylamine stimulants: amphetamine-related agents". In Lemke TL, Williams DA, Roche VF, Zito W (eds.). Foye's principles of medicinal chemistry (7th ed.). Philadelphia, USA: Wolters Kluwer Health/Lippincott Williams & Wilkins. pp. 646–648. ISBN 9781609133450. Retrieved 11 September 2015.
The phase 1 metabolism of amphetamine analogs is catalyzed by two systems: cytochrome P450 and flavin monooxygenase. ... Amphetamine can also undergo aromatic hydroxylation to p-hydroxyamphetamine. ... Subsequent oxidation at the benzylic position by DA β-hydroxylase affords p-hydroxynorephedrine. Alternatively, direct oxidation of amphetamine by DA β-hydroxylase can afford norephedrine.
- ^ Taylor KB (January 1974). "Dopamine-beta-hydroxylase. Stereochemical course of the reaction" (PDF). J. Biol. Chem. 249 (2): 454–458. doi:10.1016/S0021-9258(19)43051-2. PMID 4809526. Retrieved 6 November 2014.
Dopamine-β-hydroxylase catalyzed the removal of the pro-R hydrogen atom and the production of 1-norephedrine, (2S,1R)-2-amino-1-hydroxyl-1-phenylpropane, from d-amphetamine.
- ^ Horwitz D, Alexander RW, Lovenberg W, Keiser HR (May 1973). "Human serum dopamine-β-hydroxylase. Relationship to hypertension and sympathetic activity". Circ. Res. 32 (5): 594–599. doi:10.1161/01.RES.32.5.594. PMID 4713201.
Subjects with exceptionally low levels of serum dopamine-β-hydroxylase activity showed normal cardiovascular function and normal β-hydroxylation of an administered synthetic substrate, hydroxyamphetamine.
- ^ Mutschler J, Abbruzzese E, Witt SH, Dirican G, Nieratschker V, Frank J, Grosshans M, Rietschel M, Kiefer F (August 2012). "Functional polymorphism of the dopamine β-hydroxylase gene is associated with increased risk of disulfiram-induced adverse effects in alcohol-dependent patients". Journal of Clinical Psychopharmacology. 32 (4): 578–80. doi:10.1097/jcp.0b013e31825ddbe6. PMID 22760354.
- ^ Ella E, Sato N, Nishizawa D, Kageyama S, Yamada H, Kurabe N, Ishino K, Tao H, Tanioka F, Nozawa A, Renyin C, Shinmura K, Ikeda K, Sugimura H (June 2012). "Association between dopamine beta hydroxylase rs5320 polymorphism and smoking behaviour in elderly Japanese". Journal of Human Genetics. 57 (6): 385–90. doi:10.1038/jhg.2012.40. PMID 22513716.
- ^ Bhaduri N, Sinha S, Chattopadhyay A, Gangopadhyay PK, Singh M, Mukhopadhyay KK (February 2005). "Analysis of polymorphisms in the dopamine beta hydroxylase gene: association with attention deficit hyperactivity disorder in Indian children". Indian Pediatrics. 42 (2): 123–9. PMID 15767706.
- ^ Cubells JF, Sun X, Li W, Bonsall RW, McGrath JA, Avramopoulos D, Lasseter VK, Wolyniec PS, Tang YL, Mercer K, Pulver AE, Elston RC (November 2011). "Linkage analysis of plasma dopamine β-hydroxylase activity in families of patients with schizophrenia". Human Genetics. 130 (5): 635–43. doi:10.1007/s00439-011-0989-6. PMC 3193571. PMID 21509519.
- ^ Combarros O, Warden DR, Hammond N, Cortina-Borja M, Belbin O, Lehmann MG, Wilcock GK, Brown K, Kehoe PG, Barber R, Coto E, Alvarez V, Deloukas P, Gwilliam R, Heun R, Kölsch H, Mateo I, Oulhaj A, Arias-Vásquez A, Schuur M, Aulchenko YS, Ikram MA, Breteler MM, van Duijn CM, Morgan K, Smith AD, Lehmann DJ (2010). "The dopamine β-hydroxylase -1021C/T polymorphism is associated with the risk of Alzheimer's disease in the Epistasis Project". BMC Medical Genetics. 11 (161): 162. doi:10.1186/1471-2350-11-162. PMC 2994840. PMID 21070631.
- ^ a b c Punchaichira TJ, Mukhopadhyay A, Kukshal P, Bhatia T, Deshpande SN, Thelma BK (2020). "Association of regulatory variants of dopamine β-hydroxylase with cognition and tardive dyskinesia in schizophrenia subjects". Journal of Psychopharmacology. 34 (3): 358–369. doi:10.1177/0269881119895539. PMC 7150076. PMID 31913053.
- ^ a b Kapoor A, Shandilya M, Kundu S (2011). "Structural insight of dopamine β-hydroxylase, a drug target for complex traits, and functional significance of exonic single nucleotide polymorphisms". PLOS ONE. 6 (10): e26509. Bibcode:2011PLoSO...626509K. doi:10.1371/journal.pone.0026509. PMC 3197665. PMID 22028891.
- ^ Vendelboe TV, Harris P, Zhao Y, Walter TS, Harlos K, Omari KE, Christensen HM (2016). "The crystal structure of human dopamine β-hydroxylase at 2.9 Å resolution". Science Advances. 2 (4): e1500980. Bibcode:2016SciA....2E0980V. doi:10.1126/sciadv.1500980. PMC 4846438. PMID 27152332.
- ^ Selwood T, Jaffe EK (March 2012). "Dynamic dissociating homo-oligomers and the control of protein function". Archives of Biochemistry and Biophysics. 519 (2): 131–43. doi:10.1016/j.abb.2011.11.020. PMC 3298769. PMID 22182754.
- ^ Goldstein M, Anagnoste B, Lauber E, Mckeregham MR (July 1964). "Inhibition of dopamine- β -hydroxylase by disulfiram". Life Sciences. 3 (7): 763–7. doi:10.1016/0024-3205(64)90031-1. PMID 14203977.
- ^ Goldstein M, Lauber E, Mckereghan MR (July 1964). "The inhibitionof dopamine-β-hydroxylase by tropolone and other chelating agents". Biochemical Pharmacology. 13 (7): 1103–6. doi:10.1016/0006-2952(64)90109-1. PMID 14201135.
- ^ Stanley WC, Li B, Bonhaus DW, Johnson LG, Lee K, Porter S, Walker K, Martinez G, Eglen RM, Whiting RL, Hegde SS (August 1997). "Catecholamine modulatory effects of nepicastat (RS-25560-197), a novel, potent and selective inhibitor of dopamine-beta-hydroxylase". British Journal of Pharmacology. 121 (8): 1803–9. doi:10.1038/sj.bjp.0701315. PMC 1564872. PMID 9283721.
- ^ Townes S, Titone C, Rosenberg RC (February 1990). "Inhibition of dopamine beta-hydroxylase by bidentate chelating agents". Biochimica et Biophysica Acta (BBA) - Protein Structure and Molecular Enzymology. 1037 (2): 240–7. doi:10.1016/0167-4838(90)90174-E. PMID 2306475.
추가 읽기
- Friedman S, Kaufman S (December 1965). "3,4-dihydroxyphenylethylamine beta-hydroxylase. Physical properties, copper content, and role of copper in the catalytic activity". The Journal of Biological Chemistry. 240 (12): 4763–73. doi:10.1016/S0021-9258(18)97021-3. PMID 5846992.
- Levin EY, Levenberg B, Kaufman S (1960). "The enzymatic conversion of 3,4-dihydroxyphenylethylamine to norepinephrine". J. Biol. Chem. 235 (7): 2080–2086. doi:10.1016/S0021-9258(18)69366-4. PMID 14416204.