산소 독성
Oxygen toxicity| 산소 독성 | |
|---|---|
| 기타 이름 | 산소 독성 증후군, 산소 중독, 산소 중독 |
 | |
| 1942-43년 영국 정부는 다이버들의 산소 독성에 대한 광범위한 테스트를 실시했다.챔버를 3.7bar까지 공기로 가압한다.중심부의 피사체는 마스크로부터 100% 산소를 호흡하는 것이다.[1] | |
| 전문 | 응급의학 |
산소 독성은 분자 산소(O
2)를 증가된 부분 압력으로 호흡하는 유해한 영향에서 비롯되는 질환이다.심한 경우는 세포 손상과 사망을 초래할 수 있으며, 그 영향은 중추신경계, 폐, 눈에서 가장 많이 나타난다.역사적으로 중추신경계 질환은 19세기 말 발견과 설명을 개척한 연구자들의 이름을 따서 폴 버트 효과, 그리고 폐질환인 로레인 스미스 효과라고 불렸다.산소 독성은 수중 다이버, 고농도 보조 산소(특히 미숙아), 고압 산소 치료를 받고 있는 다이버들의 관심사다.
호흡으로 산소의 부분 압력이 증가된 결과는 신체 조직에서 산소의 과잉인 과산화지질이다.신체는 노출 유형에 따라 다른 방식으로 영향을 받는다.중추신경계 독성은 대기압보다 높은 산소의 높은 부분압에 짧은 노출에 의해 발생한다.폐와 안구 독성은 정상 압력에서 증가된 산소 레벨에 장기간 노출되어 발생한다.증상에는 방향 감각 상실, 호흡 문제, 근시와 같은 시력 변화가 포함될 수 있다.정상 이상의 산소 부분 압력에 장기간 노출되거나 매우 높은 부분 압력에 대한 짧은 노출은 세포막의 산화적 손상, 폐에 있는 폐포 붕괴, 망막 박리, 발작을 일으킬 수 있다.산소 독성은 증가된 산소 농도에 대한 노출을 줄임으로써 관리된다.장기적으로는 대부분의 유형의 산소 독성으로부터 강력한 회복이 가능하다는 연구결과가 나왔다.
고압산소의 영향을 피하기 위한 프로토콜은 압축 호흡 가스를 이용한 수중 다이빙, 고압 약, 신생아 치료, 인간 우주 비행 등 정상보다 높은 부분 압력으로 산소를 호흡하는 분야에서 존재한다.이러한 프로토콜들은 산소 독성으로 인한 발작의 희귀성을 증가시키는 결과를 가져왔는데, 폐와 안구 손상은 주로 미숙아 관리 문제에 국한되어 있다.
최근 몇 년 동안, 산소는 산소 바에서 레크리에이션용으로 사용 가능하게 되었다.미국 식품의약국은 심장이나 폐 질환과 같은 문제를 겪고 있는 사람들에게 산소 바를 사용하지 말라고 경고했다.스쿠버 다이버들은 최대 100% 산소가 함유된 호흡 가스를 사용하며, 그러한 가스를 사용하는 데 있어 특별한 훈련을 받아야 한다.
분류
산소 독성의 영향은 영향을 받는 장기에 의해 분류될 수 있으며,[2][3][4] 다음과 같은 세 가지 주요 형태를 생성할 수 있다.
- 경련으로 특징지어지는 중추신경계, 의식불명 상태에서 발생한다.
- 호흡 곤란과 가슴 내 통증으로 특징지어지는 폐(폐)는 장기간 산소 압력이 증가했을 때 발생한다.
- 눈의 개조에 의해 특징지어지는 안구(반병성 질환)는 장기간 산소 압력이 증가했을 때 발생한다.
중추신경계 산소 독성은 발작, 경련, 무의식 등의 짧은 기간 동안 경련을 일으킬 수 있으며, 대기압보다 더 큰 압력에 부딪치는 다이버들에게 우려의 대상이다.폐산소 독성은 폐에 손상을 입혀 고통과 호흡곤란을 일으킨다.눈에 대한 산화 손상은 근시나 망막의 부분 분리로 이어질 수 있다.폐와 안구 손상은 특히 신생아를 대상으로 한 치료의 일환으로 보조산소를 투여할 때 발생할 가능성이 가장 높지만 고압산소 치료 시에도 우려된다.
산화 손상은 신체의 어떤 세포에서도 발생할 수 있지만 가장 취약한 세 개의 장기에 대한 영향이 주된 관심사가 될 것이다.또한 적혈구 손상([5][6]해몰리시스), 간,[7] 심장,[8] 내분비선(아드레날린, 생식선, 갑상선)[9][10][11] 또는 신장에 대한 손상,[12] 그리고 세포의 일반적인 손상에 관여할 수도 있다.[2][13]
비정상적인 상황에서 다른 조직에 대한 영향을 관찰할 수 있다. 우주 비행 중에 높은 산소 농도가 뼈 손상의 원인이 될 수 있다고 의심된다.[14]또한 과산화지질은 만성폐쇄성폐질환과 같은 폐질환이나 중추호흡기 우울증과 같은 폐질환 환자에게 이산화탄소 중독을 간접적으로 유발할 수 있다.[14]대기압에서 대기 중 공기의 과호흡은 산소 독성을 유발하지 않는데, 해수면 공기는 산소 압력이 0.21bar(21kPa)인 반면 독성은 0.3bar(30kPa) 이하로 발생하지 않기 때문이다.[15]
징후 및 증상
| 노출(분) | 과목수 | 증상 |
|---|---|---|
| 96 | 1 | 장기간의 눈부심, 심한 경련성 구토 |
| 60–69 | 3 | 심한 입술 트위치, 행복감, 메스꺼움과 현기증, 팔 비틀림 |
| 50–55 | 4 | 심한 입술 트임, 눈부심, 입술 블러블링, 잠들었다, 멍해졌다. |
| 31–35 | 4 | 메스꺼움, 현기증, 입술 트위치, 경련 |
| 21–30 | 6 | 경련, 졸림, 심한 입술 트임, 경련, 경련, 경련, L팔, 기억상실증 |
| 16–20 | 8 | 경련, 현기증과 심한 입술 경련, 경련성 아우라, 경련성 호흡, |
| 11–15 | 4 | 자극적 우위, 입술 트위치 및 싱코프, 메스꺼움과 혼란 |
| 6–10 | 6 | 멍하고 입술이 트이는 소리, 현기증, "직립경련", 심한 구역질 |
중추신경계
중추신경계 산소 독성은 시각 변화(특히 터널 시력), 귀에서 울리는 소리(명상), 구역질, 경련(특히 얼굴의 경우), 행동 변화(불가침, 불안, 혼란), 현기증 등의 증상으로 나타난다.이것은 두 단계로 구성된 강장성-클론 발작이 뒤따를 수 있다: 강도 높은 근육 수축은 몇 초 동안 일어난다(토닉 페이즈), 그 다음으로는 경련성 저킹을 생성하는 대체 근육 이완과 수축의 빠른 경련이 뒤따른다.발작은 무의식(사후 상태)의 기간으로 끝난다.[16][17]발작의 시작은 호흡 가스의 산소 부분 압력과 노출 지속시간에 달려 있다.그러나 검사에서 개인과 동일 개인에서 모두 큰 변동을 보였기 때문에 발병 전 노출 시간은 예측할 수 없다.[16][18][19]또 수중몰입, 추위 노출, 운동 등 많은 외부 요인들이 중추신경계 증상의 시작 시간을 줄여줄 것이다.[1]공차 감소는 이산화탄소 보유와 밀접하게 연관되어 있다.[20][21][22]어둠과 카페인과 같은 다른 요소들은 시험 동물들의 내성을 증가시키지만, 이러한 영향은 인간에게 증명되지 않았다.[23][24]
폐
폐독성 증상은 폐로 이어지는 기도에서 시작해 폐(기관지엽수)로 퍼지는 염증에서 비롯된다.그 증상은 위쪽 가슴 부위(하부 및 하부 부위)에서 나타난다.[25][26][27]이것은 흡입 시 가벼운 간지럼으로 시작하여 잦은 기침으로 진행된다.[25]호흡이 빨라진 부분적인 산소 압력이 계속되면 환자는 흡입 시 통제할 수 없는 기침과 함께 가벼운 연소, 간헐적인 호흡곤란(질식호흡)을 경험하게 된다.[25]폐독성 관련 신체 소견으로는 청진기를 통해 들리는 거품소리(거품성 발톱), 발열, 코 안쪽으로 가는 혈류량 증가(비강 점막의 고혈증) 등이 있다.[27]폐의 X-ray는 단기적으로 거의 변화가 없지만, 장시간 노출은 양쪽 폐에 걸쳐 확산 그림자를 증가시킨다.[25]폐 기능 측정은 폐가 수용할 수 있는 공기의 양 감소(활용량)와 폐 기능 및 폐 탄력성의 변화에서 지적한 바와 같이 감소한다.[27][28]동물 실험에서는 종들 간의 유의미한 변화뿐만 아니라 중추신경계 독성에서 발견되는 것과 유사한 내성 변화를 보여 왔다.0.5bar(50kPa) 이상의 산소에 간헐적으로 노출되면 폐가 회복되고 독성 발병이 지연된다.[29]
눈
미숙아의 경우, 신생아의 망막의 혈관화 부위와 비혈관화 부위 사이의 경계로서 안과경을 통해 눈의 손상 징후(미숙증, ROP)가 관찰된다.이 경계의 정도는 4단계를 지정하는데 사용된다. (I) 경계가 선이다. (II) 경계가 능선이 된다. (III) 능선 주위에서 새로운 혈관의 성장이 일어난다. (IV) 망막은 눈의 내벽(초로이드)에서 분리되기 시작한다.[30]
원인들
산소 독성은 신체가 정상적으로 노출되는 것보다 더 큰 부분 압력으로 산소에 노출되어 발생한다.이것은 수중 다이빙, 고압 산소 치료, 그리고 특히 미숙아에게 보조 산소 공급의 세 가지 주요한 환경에서 발생한다.각각의 경우에 위험요인은 현저하게 다르다.
중추신경계 독성
몇 분에서 몇 시간 동안 1.6bar(160kPa) 이상의 산소 부분 압력에 대한 노출은 보통 정상 대기 부분 압력의 약 8배인 중앙 신경계 산소 독성과 관련이 있으며 고압 산소 치료를 받는 환자와 다이버 사이에서 가장 많이 발생할 가능성이 높다.해수면 대기압이 약 1bar(100kPa)이기 때문에 중추신경계 독성은 주변 압력이 정상보다 높은 고압 조건에서만 발생할 수 있다.[31][32]60m(200ft) 이상의 깊이에서 공기를 호흡하는 다이버들은 산소 독성 "히트"의 위험 증가에 직면한다.니트로스와 같이 산소가 농축된 가스 혼합물을 호흡하는 다이버들도 혼합물에 허용된 최대 작동 깊이 이하로 내려갈 경우 마찬가지로 얕은 깊이에서 발작을 겪을 수 있다.[33]
폐독성
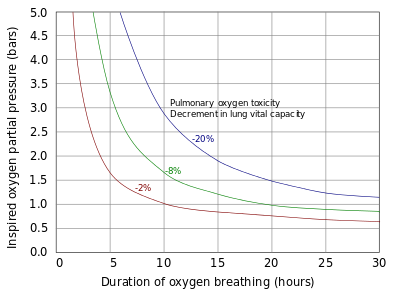
폐와 나머지 호흡기는 인체 내에서 가장 높은 농도의 산소에 노출되어 있기 때문에 독성을 보이는 최초의 기관이다.폐 독성은 정상 대기압에서 산소 분율이 50%에 해당하는 0.5bar(50kPa) 이상의 산소의 부분 압력에 노출될 때만 발생한다.폐독성의 초기 증상은 95% 이상의 산소에서 4시간에서 22시간 사이의 무증상 기간 후 기관절개염 또는 상부 기도에 염증이 있다는 증거로부터 시작되며,[34] 어떤 연구는 증상이 보통 이 산소 수준에서 약 14시간 후에 시작된다는 것을 시사한다.[35]
대기압의 2배에서 3배에서 100% 산소인 2~3bar(200~300kPa)의 산소 부분압에서 이러한 증상은 산소에 노출된 후 빠르면 3시간 후에 시작될 수 있다.[34]1~3bar(100~300kPa) 사이의 압력에서 산소를 호흡하는 쥐에 대한 실험에서는 산소 독성의 폐 징후가 고압 조건과 마찬가지로 노르모바르의 조건에서는 같지 않을 수 있음을 시사한다.[36]폐 기능 검사로 측정한 폐 기능 저하 증거는 100% 산소에 24시간 연속 노출되는 만큼 빠르게 발생할 수 있으며,[35] 확산성 치경 손상 및 급성 호흡곤란 증후군은 보통 100% 산소에 48시간 후에 발생한다.[34]또한 100% 산소를 호흡하면 결국 폐포(열전증)가 붕괴되는 반면, 동일한 부분적인 산소 압력에서 불활성 기체(일반적으로 질소)의 상당한 부분 압력이 이러한 영향을 막을 것이다.[37]
임신 전 신생아는 고농도 산소에 장시간 노출되면 기관지폐 기능장애 위험이 높은 것으로 알려져 있다.[38]산소 독성의 위험이 높은 다른 그룹은 산소 레벨이 50% 이상인 기계적 인공호흡기 환자와 화학 요법제 블로마이신 같은 산소 독성의 위험을 증가시키는 화학물질에 노출된 환자들이다.[35]따라서 중환자실에서 기계적 인공호흡에 관한 현행 지침은 산소농도를 [34]60% 이하로 유지할 것을 권고하고 있다.마찬가지로 감압 질환 치료를 받는 잠수부들은 잠수 중 산소 노출 외에도 고압 조건에서 장기간 산소 호흡에 노출되기 때문에 산소 독성의 위험이 증가한다.[31]
안구 독성
산소 분수에 장기간 노출되면 망막이 손상된다.[39][40][41]정상 압력에서 높은 산소 분율에 노출된 유아의 발육 안구 손상은 고압 조건에서 성인 잠수부가 경험하는 눈 손상과 다른 메커니즘과 효과를 가진다.[42][43]과산화지질은 유아에서 재생산 섬유증 또는 미성숙(ROP)의 망막병증이라고 불리는 장애의 원인이 될 수 있다.[42][44]유아의 경우 망막이 완전히 혈관화되어 있지 않은 경우가 많다.미성숙의 망막증은 망막정맥의 발달이 정지된 후 비정상적으로 진행될 때 발생한다.이러한 새로운 혈관의 성장과 연관되어 망막 분리를 일으킬 수 있는 섬유 조직(스카르 조직)이 있다.위험인자일 때 보조 산소 노출은 이 질병의 발병의 주요 위험인자가 아니다.보조 산소 사용을 제한한다고 해서 반드시 미성숙의 망막병증 발생률이 감소되는 것은 아니며 저산소증 관련 전신 합병증의 위험이 높아질 수 있다.[42]
고산화 근시는 장기간 노출되는 폐쇄회로 산소 재호흡기 다이버들에게 발생했다.[43][45][46]반복적인 고압산소요법을 받는 사람들에게도 자주 발생한다.[40][47]이는 축방향 길이와 각진 측정값으로는 근시적 이동에 대한 각막 또는 길이 기준이 나타나지 않기 때문에 렌즈의 굴절력이 증가하기 때문이다.[47][48]그것은 보통 시간이 지나면 되돌릴 수 있다.[40][47]
메커니즘
산소의 독성에 대한 생화학적 근거는 활성산소 종을 형성하기 위해 1~2개의 전자가 산소를 부분적으로 감소시키는 것으로 [49]산소의 정상적인 신진대사의 자연 부산물이며 세포 신호 전달에 중요한 역할을 한다.[50]인체에 의해 생성되는 한 종인 과산화 음이온([51]O−
2)은 철 획득에 관여할 가능성이 있다.[52]정상 산소 농도보다 높으면 활성 산소 종의 수치가 증가한다.[53]산소는 세포대사에 필요하며, 혈액은 그것을 신체의 모든 부분에 공급한다.높은 부분압력으로 산소를 들이마실 때, 가장 혈관화된 조직이 가장 취약한 고산소 상태가 빠르게 확산될 것이다.환경 스트레스 기간에는 반응성 산소 종의 수치가 급격히 증가하여 세포 구조를 손상시키고 산화 스트레스를 발생시킬 수 있다.[19][54]
체내 이러한 종들의 모든 반응 메커니즘이 아직 완전히 이해되지는 않았지만,[55] 산화 스트레스의 가장 반응적인 산물 중 하나는 히드록실 래디컬(·OH)인데, 이것은 세포막 내 불포화 지질에서 지질 과산화물의 해로운 연쇄 반응을 일으킬 수 있다.[56]고농도의 산소는 또한 질산화물, 과산화질소, 트리오시딘과 같은 다른 활성산소의 형성을 증가시켜 DNA와 다른 생체 분자를 해친다.[19][57]비록 신체는 산화 스트레스를 막아주는 글루타티온과 같은 항산화 시스템을 많이 가지고 있지만, 이러한 시스템은 결국 매우 고농도의 자유산소에서 압도되고, 세포 손상률이 그것을 방지하거나 수리하는 시스템의 용량을 초과한다.[58][59][60]세포손상과 세포사망은 그 후에 발생한다.[61]
진단
발작 전 잠수부들의 중추신경계 산소독성 진단은 시각장애, 귀 문제, 현기증, 혼잡, 메스꺼움 등의 증상이 수면환경에 공통적으로 나타나는 요인이 많아 진단이 어렵다.그러나 이러한 증상은 고압산소요법을 받는 환자의 산소 독성의 첫 단계를 진단하는 데 도움이 될 수 있다.어느 경우든 간질의 이전 이력이 없거나 검사에서 저혈당혈증이 나타나지 않는 한, 부분압력 1.4bar(140kPa) 이상의 호흡산소 설정에서 발생하는 발작은 산소 독성의 진단을 시사한다.[62]
호흡곤란이 있는 신생아의 기관지폐이형성증 진단은 처음 몇 주 동안은 어렵다.다만 이 기간 동안 영아의 호흡이 나아지지 않으면 혈액검사와 엑스레이를 통해 기관지폐이형성증을 확인할 수 있다.또한 심초음파 검사는 선천성 심장 결함이나 폐동맥 고혈압과 같은 다른 가능한 원인들을 제거하는 데 도움을 줄 수 있다.[63]
유아에서 미성숙의 망막병증의 진단은 일반적으로 임상 환경에 의해 제안된다.미성숙, 저출생 체중, 산소 노출 이력이 주요 지표인 반면, 유전적 요인이 패턴을 낳는 것으로 밝혀진 것은 없다.[64]
예방
산소 독성의 방지는 전적으로 설정에 달려 있다.수중과 우주 둘 다, 적절한 예방조치는 가장 치명적인 영향을 제거할 수 있다.미숙아는 보통 임신 전 합병증을 치료하기 위해 보충 산소를 필요로 한다.이 경우 기관지 심폐이형성증 예방과 미성숙 망막증은 신생아의 생명을 보존하기에 충분한 산소 공급을 손상시키지 않고 수행해야 한다.
수중
산소 독성은 스쿠버 다이빙에서 치명적인 위험으로, 발작 시 익사에 의한 사망에 가까운 결과를 낳기 때문이다.[33]발작이 갑자기 일어나 경고 증상이 없을 수도 있다.[17]그 영향은 갑작스러운 경련과 무의식인데, 그 동안 피해자들은 조절기를 잃고 익사할 수 있다.[65][66]풀페이스 다이빙 마스크의 장점 중 하나는 발작 시 조절기 손실 방지다.산소가 풍부한 호흡 가스를 사용하는 깊은 잠수, 긴 잠수, 잠수에서 중추신경계 산소 독성의 위험이 증가하므로 다이버들은 산소가 풍부한 호흡 가스의 최대 작동 깊이를 계산하도록 가르치며, 그러한 혼합물이 들어 있는 실린더는 그 깊이로 명확하게 표시해야 한다.[22][67]
이러한 유형의 다이빙을 위한 일부 다이버 훈련 과정에서는 다이버들이 다이빙의 '산소 시계'라고 불리는 것을 계획하고 감시하는 것을 가르친다.[67]이는 산소 압력 증가 시 보다 빠르게 체크하며 국립해양대기청 잠수 매뉴얼에서 권장하는 최대 단일 노출 한계치에서 작동하도록 설정된 개념적 알람 시계다.[22][67]산소의 다음과 같은 부분압력의 경우 한계는 1.6bar에서 45분(160kPa),[68][69] 1.5bar에서 120분(150kPa), 1.4bar에서 150분(140kPa), 1.3bar에서 180분(130kPa) 및 1.2bar(120kPa)에서 210분이지만 독성 증상의 발생 여부나 시기를 신뢰성 있게 예측할 수는 없다.많은 니트록스 가능 다이브 컴퓨터는 산소 부하를 계산하여 여러 다이브에 걸쳐 추적할 수 있다.그 목적은 호흡 가스의 산소 부분 압력을 줄이거나 산소 부분 압력이 더 큰 호흡 가스를 사용하는 시간을 줄임으로써 경보의 활성화를 피하는 것이다.호흡 가스의 산소 분율과 잠수 깊이에 따라 산소의 부분 압력이 증가함에 따라, 잠수부는 얕은 깊이에서 다이빙하거나 산소가 풍부한 가스를 덜 들이마시거나 산소가 풍부한 가스에 대한 노출 기간을 단축함으로써 산소 시계에 더 많은 시간을 얻는다.[70][71]
공기 중 56m(184ft) 미만으로 잠수하면 산소의 부분 압력이 1.4bar(140kPa)를 초과함에 따라 다이버가 산소 독성의 증가 위험에 노출되므로, 21% 미만의 산소를 함유한 가스 혼합물(저산소 혼합물)을 사용해야 한다.질소의 비율을 높이는 것은 강력한 마약 혼합물을 생산하기 때문에 가능하지 않다.그러나 헬륨은 마약성분이 아니며, 질소를 헬륨으로 완전히 대체하거나(결과 혼합물을 헬륨이라고 함) 질소의 일부를 헬륨으로 대체하여 트리믹스를 생성함으로써 사용 가능한 혼합물을 혼합할 수 있다.[72]
폐산소 독성은 다이빙하는 동안 완전히 피할 수 있는 사건이다.대부분의 다이빙의 제한된 지속시간과 자연적으로 간헐적인 성질은 다이버들에게 상대적으로 드물게(그리고 그 때조차도, 되돌릴 수 있는) 복잡성을 만든다.[73]확립된 가이드라인은 다이버들이 언제 폐독성의 위험에 처해있는지 계산할 수 있게 해준다.[74][75][76]포화 다이빙에서는 생활 구역에서 가스의 산소 함량을 0.4bar 이하로 제한함으로써 피할 수 있다.
고압적 설정
발열이나 발작의 이력이 있는 것은 고압산소치료에 대한 상대적인 억제작용이다.[77]감압질환 치료에 사용되는 일정표를 보면 100% 산소(산소파열)가 아닌 호흡공기 기간을 허용해 발작이나 폐손상 가능성을 줄일 수 있다.미 해군은 100% 산소와 공기로 교대하는 기간을 기준으로 처리표를 사용한다.예를 들어 USN 표 6은 18m(60ft)의 깊이에 해당하는 2.8 표준 대기(280kPa)의 주변 압력에서 75분(20분 산소/5분 공기 3주기)이 필요하다.이후 산소 30분 이상 1.9 atm(190 kPa)으로 서서히 압력이 감소한다.그러면 환자는 산소 30분 이상 대기압으로 감소하기 전에 15분 공기/60분 산소의 두 기간으로 구성된 150분 더 그 압력을 유지한다.[78]
비타민 E와 셀레늄이 제안되었고 후에 폐산소 독성에 대한 잠재적 보호 방법으로 거부되었다.[79][80][81]그러나 쥐에게는 비타민E와 셀레늄이 생체내 지질 과산화방지 및 급격한 손상을 방지하고 따라서 반복적인 고압산소 노출에 따른 망막변화를 방지한다는 실험적인 증거가 있다.[82]
노르모바르 설정
기관지심폐이형성증은 산소의 낮은 압력에 휴식기를 사용함으로써 초기에 가역할 수 있지만, 심각한 손상으로 진행되도록 허용하면 결국 돌이킬 수 없는 폐 손상을 초래할 수 있다.이런 피해를 일으키려면 산소파단 없이 하루 이틀 노출이 필요하다.[14]
미성숙의 망막증은 대부분 선별을 통해 예방할 수 있다.현행 지침은 임신 32주 미만 또는 출산 중량이 1.5kg(3.3lb) 미만인 모든 아기에게 최소한 2주에 한 번씩 미성숙 망막증을 검사하도록 요구하고 있다.[83]1954년 국가협동연구는 보조산소와 미성숙 망막병증 사이의 인과관계를 보여주었지만, 그 후 보조산소의 축소가 유아 사망률을 증가시켰다.저산소증과 미숙아의 망막병증의 위험의 균형을 맞추기 위해, 현대의 프로토콜은 산소를 공급받는 미숙아의 혈액 산소 농도의 모니터링을 필요로 한다.[84]
하이포바르 설정
저압 환경에서는 단순히 높은 산소 분율이 아니라 높은 산소의 부분 압력에 의해 독성이 발생하기 때문에 산소 독성을 피할 수 있다.이는 저압에서 작동해야 하는 우주복에 현대적인 순수 산소 사용에 의해 설명된다(또한 역사적으로 매우 높은 비율의 산소와 보통 대기압보다 낮은 압력도 초기 우주선, 예를 들어 제미니와 아폴로 우주선에 사용되었다).[85]차량 외 활동과 같은 경우 산소 부분 압력이 만성적으로 0.3bar(4.4psi)를 초과할 수 없기 때문에 호흡 혼합물 분율이 100%에 근접하더라도 고-프랙션 산소는 독성이 없다.[85]
관리

고압 산소 치료 중 환자는 공기로 가압된 고압 챔버 내부에서 약 2.8bar(280kPa)로 가압된 상태에서 마스크로부터 100% 산소를 호흡한다.치료 중 발작은 환자로부터 마스크를 제거하여 영상의 산소 부분압을 0.6bar(60kPa) 이하로 떨어뜨려 관리한다.[17]
수중 발작은 가능한 한 빨리 잠수부를 수면 위로 끌어올려야 한다.비록 여러 해 동안 발작 그 자체 동안 잠수부를 기르지 말라는 권고가 있었지만, 동맥 가스 색전증(AGE)의 위험 때문에 글로티스가 기도를 완전히 방해하지 않는다는 증거가 있다.[86][87]이로 인해 현재 해저 및 고압의학회의 다이빙 위원회가 잠수부의 입 안에 조절기가 없을 경우(이 때 익사 위험이 AGE보다 크므로) 발작의 클론(경동) 단계 동안 잠수부를 올려야 한다고 권고하고 있으나 상승은 끝까지 연기해야 한다.그렇지 않으면 [65]상투적인 국면구조대원들은 경련 단계 동안 그들 자신의 안전이 훼손되지 않도록 한다.그런 다음, 희생자의 공기 공급이 설정된 곳에서 공기 공급이 유지되는지 확인하고, 제어된 부력 리프트를 수행한다.의식 없는 몸을 들어올리는 것은 대부분의 레크리에이션 다이버 훈련 기관에서 고급 기술로 가르치고 있으며, 전문 다이버들에게는 그것은 대기 다이버의 주요 기능 중 하나이기 때문에 기본적인 기술이다.수면에 도달하면 추가적으로 의료적 치료가 필요한 합병증이 발생할 가능성이 있기 때문에 항상 응급서비스에 연락을 취한다.[88]미 해군은 재압축실을 즉시 사용할 수 없는 감압정지를 완료하는 절차가 있다.[89]
기관지심폐이형성증후군이나 급성호흡곤란증후군의 증상은 정상공기가 공급되는 휴식기간의 감소와 함께 투여되는 산소분율을 낮춰 치료한다.다른 질병(특히 유아에서)의 치료를 위해 보충 산소가 필요한 경우, 폐 조직이 팽창된 상태를 유지하도록 하기 위해 인공호흡기가 필요할 수 있다.압력과 노출의 감소는 점진적으로 이루어질 것이며, 기관지확장제, 폐계면활성제 등의 약물을 사용할 수 있다.[90]
다이버들은 특정 부분 압력의 노출 시간에 기초한 누적 산소 독성 유닛 시스템을 사용하여 실험 증거에 의해 일반적으로 허용되는 수준으로 노출을 제한함으로써 폐 손상 위험을 관리한다.감압질환에 대한 응급처치가 있을 경우 보다 심각한 증상을 관리하기 위해 정상적인 노출 제한을 초과해야 할 수 있다.[91]
미성숙의 망막증은 자연적으로 퇴행할 수 있지만, 질병이 문턱을 넘어서 진행되면(미숙의 연속 5시간 또는 3단계 망막증의 누적 8시간으로 정의), 극저온수술과 레이저 수술 모두 결과적으로 실명의 위험을 줄이는 것으로 나타났다.질병이 더 진행된 경우, 경골 좌굴과 자궁 절제 수술과 같은 기술은 망막을 다시 붙이는 데 도움을 줄 수 있다.[92]
예후
중추신경계 산소 독성에 의한 경련이 피해자에게 부수적인 상해를 입힐 수도 있지만, 발작에 따른 신경계 손상이 발생할 수 있을지는 수년 동안 불확실했고 여러 연구에서 그러한 손상의 증거를 찾아냈다.2004년 Witterman의 이러한 연구의 개요는 높은 산소를 함유한 호흡 가스를 제거한 후에도 발작에 의한 장기적 신경학적 손상은 남아 있지 않다는 결론을 내렸다.[19][93]
기관지폐소생술 발생 후 생존한 영아의 대다수는 초기 5~7년 동안 폐가 계속 성장하며 기관지폐소생술로 인한 손상은 어느 정도 되돌릴 수 있기 때문에(성인에서도) 결국 거의 정상적인 폐 기능을 회복할 것이다.그러나, 그들은 남은 평생 동안 호흡기 감염에 더 취약할 가능성이 높고, 나중에 감염되는 것의 심각도는 종종 그들의 또래들보다 더 크다.[94][95]
유아에서 종종 간섭 없이 퇴행하는 미성숙증(ROP)의 망막증은 나중엔 정상일 수 있다.수술이 필요한 단계까지 병이 진행된 경우, 결과는 일반적으로 3단계 ROP 치료에 좋으나 이후 단계에서는 훨씬 더 나쁘다.수술은 대개 눈의 해부학적 구조를 회복하는 데 성공하지만, 병의 진행에 의한 신경계통의 손상은 시력 회복에 상대적으로 더 나쁜 결과를 초래한다.다른 복잡한 질병의 존재는 또한 바람직한 결과의 가능성을 감소시킨다.[96]
역학
잠수부들의 중추신경계 독성 발생률은 2차 세계대전 이후 감소했는데, 이는 감산된 산소의 노출과 부분 압력을 제한하는 프로토콜이 발달했기 때문이다.도날드는 1947년 순수한 산소를 호흡할 수 있는 깊이를 1.8bar(180kPa)의 산소 부분압에 해당하는 7.6m(25ft)로 제한할 것을 권고했다.[98]시간이 지남에 따라 이 한계는 감소되었으며, 오늘날까지 레크리에이션 다이빙 중에는 1.4bar(140kPa), 얕은 감압 스톱에서는 1.6bar(160kPa)의 한도가 권장된다.[99]이제 산소 독성은 장비 오작동과 사람의 실수로 인한 경우를 제외하고 드문 현상이 되었다.역사적으로 미 해군은 산소 독성 사고를 줄이기 위해 네이비 다이빙 매뉴얼 테이블을 정비했다.1995년과 1999년 사이에 보고서에는 헬륨-산소 표를 사용하여 405개의 표면 지원 다이브가 나타났으며, 이 중 6개의 다이브(1.5%)에서 산소 독성 증상이 관찰되었다.그 결과 2000년 미 해군은 일정을 수정하고 150개의 다이빙에 대한 현장 테스트를 실시했는데, 이 중 산소 독성 증상은 전혀 발생하지 않았다.개정된 표는 2001년에 출판되었다.[100]
허용오차 및 작업량과 같은 다른 가변 요인의 변동성으로 인해 미 해군은 산소 허용오차 검사를 포기하게 되었다.1976년과 1997년 사이에 실시된 6,250회의 산소 내성 시험 중 산소 독성이 관측된 것은 6회(0.1%)[101][102]에 불과했다.
고압 산소 치료를 받는 환자들 사이의 중추신경계 산소 독성은 드물며, 개인 감도와 치료 프로토콜, 그리고 아마도 치료 표시와 사용되는 장비와 같은 많은 요인에 의해 영향을 받는다.1996년 웰슬라우의 연구에서는 환자 10만7264명 중 16명(0.015%)이 발생했고, 2003년 햄프슨과 아틱은 0.03%[103][104]의 발병률을 보였다.일디즈, 아이, 큐레디 등은 1996년부터 2003년까지 3만6500건의 환자 치료 결과를 요약한 결과 산소 독성 질환이 3건에 불과해 0.008%[103]의 비율을 보였다.나중에 8만 개 이상의 환자 치료법을 검토한 결과 0.0024%로 훨씬 낮은 비율을 보였다.발생률 감소는 부분적으로 산소를 공급하기 위한 마스크(후드 대신 마스크)의 사용 때문일 수 있다.[105]
기관지폐성형성증은 조산아들의 가장 흔한 합병증 중 하나이며, 극도로 조산아들의 생존이 증가함에 따라 발병률이 증가했다.그럼에도 불구하고, 보충 산소의 더 나은 관리가 현재 고산소 이외의 요인에 주로 관련되는 질병으로 귀결됨에 따라 그 심각성은 줄어들었다.[38]
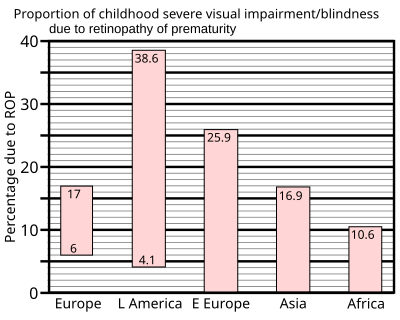
1997년 산업화된 국가의 신생아 중환자실에 대한 연구 요약에 따르면 저체중아기의 60%까지가 미성숙 망막증을 가지고 있으며, 이는 출생 시 1kg(2.2lb) 미만으로 정의되는 초저체중아에서 72%까지 증가한 것으로 나타났다.그러나 심각한 결과는 훨씬 덜 빈번하다. 즉, 태어날 때 1.5kg(3.3lb) 미만인 매우 저체중 아기들의 경우, 실명 발생률은 8%[97] 이하인 것으로 나타났다.
역사
중추신경계 독성은 1878년 폴 버트에 의해 처음 설명되었다.[106][107]그는 산소가 곤충, 거미류, 무수한 동물, 연체동물, 지렁이, 곰팡이, 발아 씨앗, 새, 그리고 다른 동물들에게 독성이 있다는 것을 보여주었다.중추신경계 독성을 "폴 버트 효과"[14]라고 할 수 있다.
폐산소 독성은 1899년 J. Lorrain Smith에 의해 처음 설명되었는데, 그는 중추신경계 독성에 주목했고 쥐와 새의 실험에서 0.43bar(43kPa)의 산소는 효과가 없지만 0.75bar(75kPa)의 산소는 폐 자극제라는 것을 발견했다.[29]폐 독성은 "로레인 스미스 효과"[14]라고 할 수 있다.인간 노출이 처음 기록된 것은 1910년 본슈타인이 2.8바(280kPa)에서 두 남자가 30분 동안 산소를 들이마신 후 아무런 증상 없이 48분 동안 계속됐다.1912년 본슈타인은 51분간 2.8바(280kPa)에서 산소를 호흡하면서 손과 다리에 경련이 생겼다.[3]그리고 나서 스미스는 산소가 적은 호흡 가스에 간헐적으로 노출되면 폐가 회복될 수 있고 폐 독성의 시작을 지연시킬 수 있다는 것을 보여주었다.[29]
앨버트 R. 1935년 Behnke 외 연구진은 1.0bar(100kPa)에서 4.1bar(410kPa) 사이의 다이빙에서 가장 먼저 시야 수축(터널 비전)을 관찰했다.[108][109]제2차 세계 대전 동안, 도날드와 야브로 외 연구진은 폐쇄 회로 산소 재호흡기의 초기 사용을 지원하기 위해 산소 독성에 대한 2,000개 이상의 실험을 수행했다.[39][110]산소 재호흡기 다이빙 초기의 해군 잠수부들이 '산소 피트(Oxygen Pete)'라는 괴물에 대한 신화를 개발했는데, 이들은 해군 실험 잠수부대의 '습기 냄비'(물이 가득 찬 고압실) 바닥에 잠복해 불청객 잠수부들을 잡으려 했다.그들은 산소 독성 공격을 "피트를 얻기"라고 불렀다.[111][112]
제2차 세계대전이 끝난 10년 동안 램버트슨 외 연구진은 압박과 예방법에 따른 호흡 산소의 효과에 대한 추가 발견을 했다.[113][114]산소 내구성 확장을 위한 간헐적 노출과 폐 기능에 기초한 폐산소 독성 예측 모델에 대한 그들의 연구는 산소의 증가된 압력을 호흡할 때 표준 작동 절차를 개발하는 데 있어 중요한 문서들이다.[115]중추신경계 증상의 시작 시간 단축에 있어 이산화탄소의 영향을 보여주는 램버트슨의 연구는 현재 노출 지침에서 향후 호흡기 설계에 이르는 작업에 영향을 미쳤다.[21][22][116]
제2차 세계 대전 전에는 미성숙의 망막증이 관찰되지 않았지만, 그 후 10년 동안 보충 산소가 사용 가능해지면서, 그것은 선진국에서 유아 실명의 주요 원인 중 하나가 되었다.1960년까지 산소의 사용은 위험요인으로 확인되었고 그것의 투여는 제한되었다.그 결과 미성숙의 망막병증 감소는 유아 사망률과 저산소 관련 합병증의 증가를 동반했다.그 이후로, 보다 정교한 모니터링과 진단은 저산소 조건과 미성숙의 망막병증 문제 사이의 균형을 맞추는 것을 목표로 하는 산소 사용에 대한 프로토콜을 확립했다.[97]
기관지폐소생술은 1967년 노스웨이가 처음 설명한 것으로, 노스웨이는 진단으로 이어질 조건을 개략적으로 설명했다.[117]이것은 나중에 Bancalari에 의해 확장되었고 1988년에 Shennan에 의해 확장되었는데, Sennan은 36주의 보조 산소의 필요성을 제안하여 장기적인 결과를 예측할 수 있었다.[118]그럼에도 불구하고 1998년 Palta 등은 방사선 증거가 장기적 효과에 대한 가장 정확한 예측 변수라고 결론지었다.[119]
1986년과 1995년의 비터맨 외 연구진은 어둠과 카페인이 쥐의 뇌 전기 활동에 대한 변화의 시작을 지연시킬 것이라는 것을 보여주었다.[23][24]그 후 몇 년 동안 중추신경계 독성에 대한 연구는 예방과 내성의 안전한 확장 방법에 초점을 맞추었다.[120]중추신경계 산소 독성에 대한 민감도는 순환 리듬, 약물, 나이, 성별 등의 요인에 의해 영향을 받는 것으로 나타났다.[121][122][123][124]1988년 해밀턴 등은 국립해양대기청이 서식지 운영을 위한 산소 노출 한계를 설정하는 절차를 작성했다.[74][75][76]오늘날에도 폐산소 독성 예측 모델은 높은 산소의 부분압에 노출되는 모든 결과를 설명하지는 않는다.[125]
사회와 문화
레크리에이션 스쿠버 다이버들은 보통 최대 40%의 산소를 함유한 니트로x를 호흡하는 반면, 기술 다이버들은 최대 80%의 산소를 함유한 순수 산소나 니트로x를 사용한다.공기(21%)보다 산소 분율을 크게 호흡하는 다이버들은 산소 독성의 위험과 예방 방법에 대해 교육받을 필요가 있다.[67]니트로스를 구입하기 위해서는 다이버가 그러한 자격의 증거를 보여야 한다.[126]
1990년대 후반부터 산소의 레크리에이션 사용은 고객들이 비강 캐뉼라를 통해 산소를 호흡하는 산소봉에 의해 촉진되었다.이를 뒷받침할 과학적 근거가 부족함에도 불구하고 스트레스를 줄이고 에너지를 증가시키며 숙취와 두통의 영향을 줄인다는 주장이 제기됐다.[127]체내 독소를 제거하고 체지방을 줄인다는 주장과 함께 '산소 마사지'와 '산소 해독'을 제공하는 장치도 판매 중이다.[128]미국폐협회(American Lung Association)는 "바에서 사용되는 낮은 유량 산소가 정상인의 건강에 위험할 수 있다는 증거는 없다"고 밝혔지만, 미국 약물평가연구센터는 심장이나 폐질환이 있는 사람들은 보조 산소를 세심하게 조절할 필요가 있으며 산소봉을 사용하지 말아야 한다고 경고하고 있다.[127]
빅토리아 사회는 급속히 팽창하는 과학 분야에 매료되었다.1872년 쥘 베른이 쓴 단편 '소박사의 실험'에서 이 심복 의사는 물의 전기분해를 이용해 산소와 수소를 분리한다.그리고 나서 그는 키켄도네 마을 전체에 순수한 산소를 펌프질하여 평상시에 평온한 주민들과 그들의 동물들이 공격적으로 변하고 식물이 빠르게 자라게 한다.옥스 박사의 공장에서 수소와 산소의 폭발이 그의 실험을 끝내게 한다.베르네는 이 이야기에서 묘사된 산소의 영향이 자신의 발명품이라고 설명함으로써 그의 이야기를 요약했다.[129]그의 "지구에서 달까지"에는 산소 중독의 짧은 에피소드도 있다.[130]
참고 항목
- 만성폐쇄성폐질환에 대한 산소의 영향
- 질소 마취 – 상승된 부분 압력에서 호흡기 질소의 가역성 마취 효과
참조
- ^ a b c 1947년 1부 도날드
- ^ a b 클라크 & 톰 2003, 페이지 358–60.
- ^ a b Acott, Chris (1999). "Oxygen toxicity: A brief history of oxygen in diving". South Pacific Underwater Medicine Society Journal. 29 (3): 150–55. ISSN 0813-1988. OCLC 16986801. Retrieved 29 April 2008.
- ^ Beehler, CC (1964). "Oxygen and the eye". Survey of Ophthalmology. 9: 549–60. PMID 14232720.
- ^ Goldstein, JR; Mengel, CE (1969). "Hemolysis in mice exposed to varying levels of hyperoxia". Aerospace Medicine. 40 (1): 12–13. PMID 5782651.
- ^ Larkin, EC; Adams, JD; Williams, WT; Duncan, DM (1972). "Hematologic responses to hypobaric hyperoxia". American Journal of Physiology. 223 (2): 431–37. doi:10.1152/ajplegacy.1972.223.2.431. PMID 4403030.
- ^ Schaffner, Fenton; Felig, Philip (1965). "Changes in Hepatic Structure in Rats Produced by Breathing Pure Oxygen". Journal of Cell Biology. 27 (3): 505–17. doi:10.1083/jcb.27.3.505. PMC 2106769. PMID 5885427.
- ^ Caulfield, JB; Shelton, RW; Burke, JF (1972). "Cytotoxic effects of oxygen on striated muscle". Archives of Pathology. 94 (2): 127–32. PMID 5046798.
- ^ Bean, JW; Johnson, PC (1954). "Adrenocortical response to single and repeated exposure to oxygen at high pressure". American Journal of Physiology. 179 (3): 410–44. doi:10.1152/ajplegacy.1954.179.3.410. PMID 13228600.
- ^ Edstrom, JE; Rockert, H (1962). "The effect of oxygen at high pressure on the histology of the central nervous system and sympathetic and endocrine cells". Acta Physiologica Scandinavica. 55 (2–3): 255–63. doi:10.1111/j.1748-1716.1962.tb02438.x. PMID 13889254.
- ^ Gersh, I; Wagner, CE (1945). "Metabolic factors in oxygen poisoning". American Journal of Physiology. 144 (2): 270–77. doi:10.1152/ajplegacy.1945.144.2.270.
- ^ Hess, RT; Menzel, DB (1971). "Effect of dietary antioxidant level and oxygen exposure on the fine structure of the proximal convoluted tubules". Aerospace Medicine. 42 (6): 646–49. PMID 5155150.
- ^ Clark, John M (1974). "The toxicity of oxygen". American Review of Respiratory Disease. 110 (6 Pt 2): 40–50. doi:10.1164/arrd.1974.110.6P2.40 (inactive 28 February 2022). PMID 4613232.
{{cite journal}}: CS1 maint : 2022년 2월 현재 DOI 비활성화(링크) (가입 필요) - ^ a b c d e Patel, Dharmeshkumar N; Goel, Ashish; Agarwal, SB; Garg, Praveenkumar; Lakhani, Krishna K (2003). "Oxygen toxicity" (PDF). Journal, Indian Academy of Clinical Medicine. 4 (3): 234–37. Retrieved 28 September 2008.
- ^ Clark & Lambertsen 1970, 페이지 159.
- ^ a b 클라크 & 톰 2003, 페이지 376.
- ^ a b c d Bitterman, N (2004). "CNS oxygen toxicity". Undersea and Hyperbaric Medicine. 31 (1): 63–72. PMID 15233161. Retrieved 29 April 2008.
- ^ Lang 2001, 페이지 82.
- ^ a b Richardson, Drew; Menduno, Michael; Shreeves, Karl, eds. (1996). "Proceedings of rebreather forum 2.0". Diving Science and Technology Workshop: 286. Retrieved 20 September 2008.
- ^ a b c d Richardson, Drew; Shreeves, Karl (1996). "The PADI enriched air diver course and DSAT oxygen exposure limits". South Pacific Underwater Medicine Society Journal. 26 (3). ISSN 0813-1988. OCLC 16986801. Retrieved 2 May 2008.
- ^ a b Bitterman, N; Melamed, Y; Perlman, I (1986). "CNS oxygen toxicity in the rat: role of ambient illumination". Undersea Biomedical Research. 13 (1): 19–25. PMID 3705247. Retrieved 20 September 2008.
- ^ a b Bitterman, N; Schaal, S (1995). "Caffeine attenuates CNS oxygen toxicity in rats". Brain Research. 696 (1–2): 250–53. doi:10.1016/0006-8993(95)00820-G. PMID 8574677. S2CID 9020944.
- ^ a b c d 클라크 & 톰 2003, 페이지 383.
- ^ Clark, John M; Lambertsen, Christian J (1971). "Pulmonary oxygen toxicity: a review". Pharmacological Reviews. 23 (2): 37–133. PMID 4948324.
- ^ a b c Clark, John M; Lambertsen, Christian J (1971). "Rate of development of pulmonary O2 toxicity in man during O2 breathing at 2.0 Ata". Journal of Applied Physiology. 30 (5): 739–52. doi:10.1152/jappl.1971.30.5.739. PMID 4929472.
- ^ 클라크 & 톰 2003 페이지 386–87.
- ^ a b c Smith, J Lorrain (1899). "The pathological effects due to increase of oxygen tension in the air breathed". Journal of Physiology. London: The Physiological Society and Blackwell Publishing. 24 (1): 19–35. doi:10.1113/jphysiol.1899.sp000746. PMC 1516623. PMID 16992479. 참고: 1대기(atm)는 1.013bar이다.
- ^ Fielder, Alistair R (1993). Fielder, Alistair R; Best, Anthony; Bax, Martin C O (eds.). The Management of Visual Impairment in Childhood. London: Mac Keith Press : Distributed by Cambridge University Press. p. 33. ISBN 0-521-45150-7.
- ^ a b Smerz, RW (2004). "Incidence of oxygen toxicity during the treatment of dysbarism". Undersea and Hyperbaric Medicine. 31 (2): 199–202. PMID 15485081. Retrieved 30 April 2008.
- ^ Hampson, Neal B; Simonson, Steven G; Kramer, CC; Piantadosi, Claude A (1996). "Central nervous system oxygen toxicity during hyperbaric treatment of patients with carbon monoxide poisoning". Undersea and Hyperbaric Medicine. 23 (4): 215–19. PMID 8989851. Retrieved 29 April 2008.
- ^ a b Lang 2001, 페이지 7.
- ^ a b c d Bitterman, H (2009). "Bench-to-bedside review: Oxygen as a drug". Critical Care. 13 (1): 205. doi:10.1186/cc7151. PMC 2688103. PMID 19291278.
- ^ a b c Jackson, RM (1985). "Pulmonary oxygen toxicity". Chest. 88 (6): 900–05. doi:10.1378/chest.88.6.900. PMID 3905287.
- ^ Demchenko, Ivan T; Welty-Wolf, Karen E; Allen, Barry W; Piantadosi, Claude A (2007). "Similar but not the same: normobaric and hyperbaric pulmonary oxygen toxicity, the role of nitric oxide". American Journal of Physiology. Lung Cellular and Molecular Physiology. 293 (1): L229–38. doi:10.1152/ajplung.00450.2006. PMID 17416738.
- ^ Wittner, M; Rosenbaum, RM (1966). Pathophysiology of pulmonary oxygen toxicity. Proceedings of the Third International Conference on Hyperbaric Medicine. NAS/NRC, 1404, Washington DC. pp. 179–88. – 및 Clark & Lambertsen 1970, 페이지 256–60에서 논의한 기타 사항
- ^ a b Bancalari, Eduardo; Claure, Nelson; Sosenko, Ilene RS (2003). "Bronchopulmonary dysplasia: changes in pathogenesis, epidemiology and definition". Seminars in Neonatology. London: Elsevier Science. 8 (1): 63–71. doi:10.1016/S1084-2756(02)00192-6. PMID 12667831.
- ^ a b Yarbrough, OD; Welham, W; Brinton, ES; Behnke, Alfred R (1947). "Symptoms of Oxygen Poisoning and Limits of Tolerance at Rest and at Work". Navy Experimental Diving Unit Technical Report 47-01. United States Navy Experimental Diving Unit Technical Report. Retrieved 29 April 2008.
- ^ a b c Anderson, B; Farmer, Joseph C (1978). "Hyperoxic myopia". Transactions of the American Ophthalmological Society. 76: 116–24. PMC 1311617. PMID 754368.
- ^ Ricci, B; Lepore, D; Iossa, M; Santo, A; D'Urso, M; Maggiano, N (1990). "Effect of light on oxygen-induced retinopathy in the rat model. Light and OIR in the rat". Documenta Ophthalmologica. 74 (4): 287–301. doi:10.1007/BF00145813. PMID 1701697. S2CID 688116.
- ^ a b c Drack, AV (1998). "Preventing blindness in premature infants". New England Journal of Medicine. 338 (22): 1620–21. doi:10.1056/NEJM199805283382210. PMID 9603802.
- ^ a b Butler, Frank K; White, E; Twa, M (1999). "Hyperoxic myopia in a closed-circuit mixed-gas scuba diver". Undersea and Hyperbaric Medicine. 26 (1): 41–45. PMID 10353183. Retrieved 29 April 2009.
- ^ Nichols, CW; Lambertsen, Christian (1969). "Effects of high oxygen pressures on the eye". New England Journal of Medicine. 281 (1): 25–30. doi:10.1056/NEJM196907032810106. PMID 4891642.
- ^ Shykoff, Barbara E (2005). "Repeated Six-Hour Dives 1.35 ATM Oxygen Partial Pressure". Nedu-Tr-05-20. Panama City, FL: US Navy Experimental Diving Unit Technical Report. Retrieved 19 September 2008.
- ^ Shykoff, Barbara E (2008). "Pulmonary effects of submerged oxygen breathing in resting divers: repeated exposures to 140 kPa". Undersea and Hyperbaric Medicine. 35 (2): 131–43. PMID 18500077.
- ^ a b c Anderson Jr, B; Shelton, DL (1987). "Axial length in hyperoxic myopia". In: Bove, Alfred A; Bachrach, Arthur J; Greenbaum, Leon (Eds.) Ninth International Symposium of the UHMS. Undersea and Hyperbaric Medical Society: 607–11.
- ^ Schaal, S; Beiran, I; Rubinstein, I; Miller, B; Dovrat, A (2005). "Oxygen effect on ocular lens". Harefuah (in Hebrew). 144 (11): 777–80, 822. PMID 16358652.
- ^ 클라크 & 톰 2003, 페이지 360.
- ^ Rhee, SG (2006). "Cell signaling. H2O2, a necessary evil for cell signaling". Science. 312 (5782): 1882–83. doi:10.1126/science.1130481. PMID 16809515. S2CID 83598498.
- ^ Thom, Steven R (1992). "Inert gas enhancement of superoxide radical production". Archives of Biochemistry and Biophysics. 295 (2): 391–96. doi:10.1016/0003-9861(92)90532-2. PMID 1316738.
- ^ Ghio, Andrew J; Nozik-Grayck, Eva; Turi, Jennifer; Jaspers, Ilona; Mercatante, Danielle R; Kole, Ryszard; Piantadosi, Claude A (2003). "Superoxide-dependent iron uptake: a new role for anion exchange protein 2". American Journal of Respiratory Cell and Molecular Biology. 29 (6): 653–60. doi:10.1165/rcmb.2003-0070OC. PMID 12791678.
- ^ Fridovich, I (1998). "Oxygen toxicity: a radical explanation" (PDF). Journal of Experimental Biology. 201 (8): 1203–09. doi:10.1242/jeb.201.8.1203. PMID 9510531.
- ^ Piantadosi, Claude A (2008). "Carbon Monoxide, Reactive Oxygen Signaling, and Oxidative Stress". Free Radical Biology & Medicine. 45 (5): 562–69. doi:10.1016/j.freeradbiomed.2008.05.013. PMC 2570053. PMID 18549826.
- ^ Imlay, JA (2003). "Pathways of oxidative damage". Annual Review of Microbiology. 57: 395–418. doi:10.1146/annurev.micro.57.030502.090938. PMID 14527285.
- ^ Bowen, R. "Free Radicals and Reactive Oxygen". Colorado State University. Archived from the original on 12 May 2008. Retrieved 26 September 2008.
- ^ Oury, TD; Ho, YS; Piantadosi, Claude A; Crapo, JD (1992). "Extracellular superoxide dismutase, nitric oxide, and central nervous system O2 toxicity". Proceedings of the National Academy of Sciences of the United States of America. 89 (20): 9715–19. Bibcode:1992PNAS...89.9715O. doi:10.1073/pnas.89.20.9715. PMC 50203. PMID 1329105.
- ^ Thom, Steven R; Marquis, RE (1987). "Free radical reactions and the inhibitory and lethal actions of high-pressure gases". Undersea Biomedical Research. 14 (6): 485–501. PMID 2825395. Retrieved 26 September 2008.
- ^ Djurhuus, R; Svardal, AM; Thorsen, E (1999). "Glutathione in the cellular defense of human lung cells exposed to hyperoxia and high pressure". Undersea and Hyperbaric Medicine. 26 (2): 75–85. PMID 10372426. Retrieved 26 September 2008.
- ^ Freiberger, John J; Coulombe, Kathy; Suliman, Hagir; Carraway, Martha-sue; Piantadosi, Claude A (2004). "Superoxide dismutase responds to hyperoxia in rat hippocampus". Undersea and Hyperbaric Medicine. 31 (2): 227–32. PMID 15485085. Retrieved 26 September 2008.
- ^ Kim, YS; Kim, SU (1991). "Oligodendroglial cell death induced by oxygen radicals and its protection by catalase". Journal of Neuroscience Research. 29 (1): 100–06. doi:10.1002/jnr.490290111. PMID 1886163. S2CID 19165217.
- ^ NBDHMT (4 February 2009). "Recommended Guidelines for Clinical Internship in Hyperbaric Technology (V: C.D)". Harvey, LA: National Board of Diving and Hyperbaric Medical Technology. Archived from the original on 20 September 2007. Retrieved 26 March 2009.
- ^ "How is bronchopulmonary dysplasia diagnosed?". U.S. Department of Health & Human Services. Retrieved 28 September 2008.
- ^ Regillo, Brown & Flyn 1998, 페이지 178.
- ^ a b Mitchell, Simon J; Bennett, Michael H; Bird, Nick; Doolette, David J; Hobbs, Gene W; Kay, Edward; Moon, Richard E; Neuman, Tom S; Vann, Richard D; Walker, Richard; Wyatt, HA (2012). "Recommendations for rescue of a submerged unresponsive compressed-gas diver". Undersea & Hyperbaric Medicine. 39 (6): 1099–108. PMID 23342767. Retrieved 13 March 2013.
- ^ 클라크 & 톰 2003, 페이지 375.
- ^ a b c d Lang 2001, 페이지 195.
- ^ Butler, Frank K; Thalmann; Edward D (1986). "Central nervous system oxygen toxicity in closed circuit scuba divers II". Undersea Biomedical Research. 13 (2): 193–223. PMID 3727183. Retrieved 29 April 2008.
- ^ Butler, Frank K (2004). "Closed-circuit oxygen diving in the U.S. Navy". Undersea and Hyperbaric Medicine. 31 (1): 3–20. PMID 15233156. Retrieved 29 April 2008.
- ^ Clark & Lambertsen 1970, 페이지 157–62.
- ^ Baker, Erik C (2000). "Oxygen toxicity calculations" (PDF). Retrieved 29 June 2009.
- ^ 해밀턴 & 탈만 2003, 페이지 475, 479.
- ^ Clark & Lambertsen 1970, 페이지 270.
- ^ a b Hamilton, RW; Kenyon, David J; Peterson, RE; Butler, GJ; Beers, DM (1988). "Repex habitat diving procedures: Repetitive vertical excursions, oxygen limits, and surfacing techniques". Technical Report 88-1A. Rockville, MD: NOAA Office of Undersea Research. Retrieved 29 April 2008.
- ^ a b Hamilton, Robert W; Kenyon, David J; Peterson, RE (1988). "Repex habitat diving procedures: Repetitive vertical excursions, oxygen limits, and surfacing techniques". Technical Report 88-1B. Rockville, MD: NOAA Office of Undersea Research. Retrieved 29 April 2008.
- ^ a b Hamilton, Robert W (1997). "Tolerating oxygen exposure". South Pacific Underwater Medicine Society Journal. 27 (1). ISSN 0813-1988. OCLC 16986801. Retrieved 29 April 2008.
- ^ Latham, Emi (7 November 2008). "Hyperbaric Oxygen Therapy: Contraindications". Medscape. Retrieved 25 September 2008.
- ^ Schatte, CL (1977). "Dietary selenium and vitamin E as a possible prophylactic to pulmonary oxygen poisoning". Proceedings of the Sixth International Congress on Hyperbaric Medicine, University of Aberdeen, Aberdeen, Scotland. Aberdeen: Aberdeen University Press: 84–91. ISBN 0-08-024918-3. OCLC 16428246.
- ^ Boadi, WY; Thaire, L; Kerem, D; Yannai, S (1991). "Effects of dietary supplementation with vitamin E, riboflavin and selenium on central nervous system oxygen toxicity". Pharmacology & Toxicology. 68 (2): 77–82. doi:10.1111/j.1600-0773.1991.tb02039.x. PMID 1852722.
- ^ Piantadosi, Claude A (2006). In: The Mysterious Malady: Toward an understanding of decompression injuries (DVD). Global Underwater Explorers. Retrieved 2 April 2012.
- ^ Stone, WL; Henderson, RA; Howard, GH; Hollis, AL; Payne, PH; Scott, RL (1989). "The role of antioxidant nutrients in preventing hyperbaric oxygen damage to the retina". Free Radical Biology & Medicine. 6 (5): 505–12. doi:10.1016/0891-5849(89)90043-9. PMID 2744583.
- ^ "UK Retinopathy of Prematurity Guideline" (PDF). Royal College of Paediatrics and Child Health, Royal College of Ophthalmologists & British Association of Perinatal Medicine. 2007. p. i. Archived from the original (PDF) on 18 February 2012. Retrieved 2 April 2009.
- ^ Silverman, William (1980). Retrolental Fibroplasia: A Modern Parable. Grune & Stratton. pp. 39, 41, 143. ISBN 978-0-8089-1264-4.
- ^ a b Webb, James T; Olson, RM; Krutz, RW; Dixon, G; Barnicott, PT (1989). "Human tolerance to 100% oxygen at 9.5 psia during five daily simulated 8-hour EVA exposures". Aviation, Space, and Environmental Medicine. 60 (5): 415–21. doi:10.4271/881071. PMID 2730484.
- ^ Mitchell, Simon J (20 January 2008). "Standardizing CCR rescue skills". RebreatherWorld. Archived from the original on 3 March 2012. Retrieved 26 May 2009. 이 포럼 포스트의 저자는 해저와 고압의학회의 다이빙 위원장을 맡고 있다.
- ^ Thalmann, Edward D (2 December 2003). "OXTOX: If You Dive Nitrox You Should Know About OXTOX". Divers Alert Network. Retrieved 11 October 2015. – 섹션 "산소 독성 또는 경련이 발생하면 어떻게 하는가?"
- ^ "NIH MedlinePlus: Bronchopulmonary dysplasia". U.S. National Library of Medicine. Retrieved 2 October 2008.
- ^ NOAA Diving Program (U.S.) (2001). Joiner, James T. (ed.). NOAA Diving Manual, Diving for Science and Technology (4th ed.). Silver Spring, Maryland: National Oceanic and Atmospheric Administration, Office of Oceanic and Atmospheric Research, National Undersea Research Program. ISBN 978-0-941332-70-5.
- ^ 레길로, 브라운 & 플린 1998, 페이지 184.
- ^ Lambertsen, Christian J (1965). Fenn, WO; Rahn, H (eds.). "Effects of oxygen at high partial pressure". Handbook of Physiology: Respiration. American Physiological Society. Sec 3 Vol 2: 1027–46.
- ^ "National Institutes of Health: What is bronchopulmonary dysplasia?". U.S. Department of Health & Human Services. Retrieved 2 October 2008.
- ^ Spear, Michael L – reviewer (June 2008). "Bronchopulmonary dysplasia (BPD)". Nemours Foundation. Retrieved 3 October 2008.
- ^ 레길로, 브라운 & 플린 1998, 페이지 190.
- ^ a b c Gilbert, Clare (1997). "Retinopathy of prematurity: epidemiology". Journal of Community Eye Health. London: International Centre for Eye Health. 10 (22): 22–24.
- ^ 도날드, 2부 1947.
- ^ Lang 2001, 페이지 183.
- ^ Gerth, Wayne A (2006). "Decompression sickness and oxygen toxicity in U.S. Navy surface-supplied He-O2 diving". Proceedings of Advanced Scientific Diving Workshop. Smithsonian Institution. Retrieved 2 October 2008.
- ^ Walters, KC; Gould, MT; Bachrach, EA; Butler, Frank K (2000). "Screening for oxygen sensitivity in U.S. Navy combat swimmers". Undersea and Hyperbaric Medicine. 27 (1): 21–26. PMID 10813436. Retrieved 2 October 2008.
- ^ Butler, Frank K; Knafelc, ME (1986). "Screening for oxygen intolerance in U.S. Navy divers". Undersea Biomedical Research. 13 (1): 91–98. PMID 3705251. Retrieved 2 October 2008.
- ^ a b Yildiz, S; Ay, H; Qyrdedi, T (2004). "Central nervous system oxygen toxicity during routine hyperbaric oxygen therapy". Undersea and Hyperbaric Medicine. Undersea and Hyperbaric Medical Society, Inc. 31 (2): 189–90. PMID 15485078. Retrieved 3 October 2008.
- ^ Hampson, Neal; Atik, D (2003). "Central nervous system oxygen toxicity during routine hyperbaric oxygen therapy". Undersea and Hyperbaric Medicine. Undersea and Hyperbaric Medical Society, Inc. 30 (2): 147–53. PMID 12964858. Retrieved 20 October 2008.
- ^ Yildiz, S; Aktas, S; Cimsit, M; Ay, H; Togrol, E (2004). "Seizure incidence in 80,000 patient treatments with hyperbaric oxygen". Aviation, Space, and Environmental Medicine. 75 (11): 992–94. PMID 15559001. Retrieved 1 July 2009.
- ^ Bert, Paul (1943) [First published in French in 1878]. Barometric pressure: Researches in Experimental Physiology. Columbus, OH: College Book Company. 번역자: 히치콕, 메리 앨리스, 히치콕, 프레드 A
- ^ British Sub-aqua Club (1985). Sport diving : the British Sub-Aqua Club diving manual. London: Stanley Paul. p. 110. ISBN 0-09-163831-3. OCLC 12807848.
- ^ Behnke, Alfred R; Johnson, FS; Poppen, JR; Motley, EP (1935). "The effect of oxygen on man at pressures from 1 to 4 atmospheres". American Journal of Physiology. 110 (3): 565–72. doi:10.1152/ajplegacy.1934.110.3.565. 참고: 1대기(atm)는 1.013bar이다.
- ^ Behnke, Alfred R; Forbes, HS; Motley, EP (1935). "Circulatory and visual effects of oxygen at 3 atmospheres pressure". American Journal of Physiology. 114 (2): 436–42. doi:10.1152/ajplegacy.1935.114.2.436. 참고: 1대기(atm)는 1.013bar이다.
- ^ 도날드 1992.
- ^ Taylor, Larry "Harris" (1993). "Oxygen Enriched Air: A New Breathing Mix?". IANTD Journal. Retrieved 29 May 2008.
- ^ Davis, Robert H (1955). Deep Diving and Submarine Operations (6th ed.). Tolworth, Surbiton, Surrey: Siebe Gorman & Company Ltd. p. 291.
- ^ Lambertsen, Christian J; Clark, John M; Gelfand, R (2000). "The Oxygen research program, University of Pennsylvania: Physiologic interactions of oxygen and carbon dioxide effects and relations to hyperoxic toxicity, therapy, and decompression. Summation: 1940 to 1999". EBSDC-IFEM Report No. 3-1-2000. Philadelphia, PA: Environmental Biomedical Stress Data Center, Institute for Environmental Medicine, University of Pennsylvania Medical Center.
- ^ Vann, Richard D (2004). "Lambertsen and O2: Beginnings of operational physiology". Undersea and Hyperbaric Medicine. 31 (1): 21–31. PMID 15233157. Retrieved 29 April 2008.
- ^ Clark & Lambertsen 1970.
- ^ Lang 2001, 페이지 81-86.
- ^ Northway, WH; Rosan, RC; Porter, DY (1967). "Pulmonary disease following respirator therapy of hyaline-membrane disease. Bronchopulmonary dysplasia". New England Journal of Medicine. 276 (7): 357–68. doi:10.1056/NEJM196702162760701. PMID 5334613.
- ^ Shennan, AT; Dunn, MS; Ohlsson, A; Lennox, K; Hoskins, EM (1988). "Abnormal pulmonary outcomes in premature infants: prediction from oxygen requirement in the neonatal period". Pediatrics. 82 (4): 527–32. doi:10.1542/peds.82.4.527. PMID 3174313. S2CID 2398582.
- ^ Palta, Mari; Sadek, Mona; Barnet, Jodi H; et al. (January 1998). "Evaluation of criteria for chronic lung disease in surviving very low birth weight infants. Newborn Lung Project". Journal of Pediatrics. 132 (1): 57–63. doi:10.1016/S0022-3476(98)70485-8. PMID 9470001.
- ^ Natoli, MJ; Vann, Richard D (1996). "Factors Affecting CNS Oxygen Toxicity in Humans". Report to the U.S. Office of Naval Research. Durham, NC: Duke University. Retrieved 29 April 2008.
- ^ Hof, DG; Dexter, JD; Mengel, CE (1971). "Effect of circadian rhythm on CNS oxygen toxicity". Aerospace Medicine. 42 (12): 1293–96. PMID 5130131.
- ^ Torley, LW; Weiss, HS (1975). "Effects of age and magnesium ions on oxygen toxicity in the neonate chicken". Undersea Biomedical Research. 2 (3): 223–27. PMID 15622741. Retrieved 20 September 2008.
- ^ Troy, SS; Ford, DH (1972). "Hormonal protection of rats breathing oxygen at high pressure". Acta Neurologica Scandinavica. 48 (2): 231–42. doi:10.1111/j.1600-0404.1972.tb07544.x. PMID 5061633. S2CID 28618515.
- ^ Hart, George B; Strauss, Michael B (2007). "Gender differences in human skeletal muscle and subcutaneous tissue gases under ambient and hyperbaric oxygen conditions". Undersea and Hyperbaric Medicine. 34 (3): 147–61. PMID 17672171. Retrieved 20 September 2008.
- ^ Shykoff, Barbara E (2007). "Performance of various models in predicting vital capacity changes caused by breathing high oxygen partial pressures". Nedu-Tr-07-13. Panama City, FL: U.S. Naval Experimental Diving Unit Technical Report. Retrieved 6 June 2008.
- ^ British Sub-Aqua Club (2006). "The Ocean Diver Nitrox Workshop" (PDF). British Sub-Aqua Club. p. 6. Archived from the original (PDF) on 16 July 2011. Retrieved 15 September 2010.
- ^ a b Bren, Linda (November–December 2002). "Oxygen Bars: Is a Breath of Fresh Air Worth It?". FDA Consumer. Vol. 36, no. 6. pp. 9–11. PMID 12523293. Retrieved 25 March 2020.
- ^ "O2 Planet – Exercise and Fitness Equipment". O2Planet LLC. 2006. Archived from the original on 15 April 2006. Retrieved 21 October 2008.
- ^ Verne, Jules (2004) [1872]. A Fantasy of Dr Ox. Hesperus Press. ISBN 978-1-84391-067-1. Retrieved 8 May 2009. 프랑스어에서 번역됨
- ^ Verne, Jules (1877) [1870]. "VIII" [At seventy-eight thousand one hundred and fourteen leagues]. Autour de la Lune [Round the Moon]. London: Ward Lock. ISBN 2-253-00587-8. Retrieved 2 September 2009. 프랑스어에서 번역됨
원천
- Clark, James M; Thom, Stephen R (2003). "Oxygen under pressure". In Brubakk, Alf O; Neuman, Tom S (eds.). Bennett and Elliott's physiology and medicine of diving (5th ed.). United States: Saunders. pp. 358–418. ISBN 978-0-7020-2571-6. OCLC 51607923.
- Clark, John M; Lambertsen, Christian J (1970). "Pulmonary oxygen tolerance in man and derivation of pulmonary oxygen tolerance curves". IFEM Report No. 1-70. Philadelphia, PA: Environmental Biomedical Stress Data Center, Institute for Environmental Medicine, University of Pennsylvania Medical Center. Archived from the original on 7 October 2008. Retrieved 29 April 2008.
- Donald, Kenneth W (1947). "Oxygen Poisoning in Man: Part I". British Medical Journal. 1 (4506): 667–72. doi:10.1136/bmj.1.4506.667. PMC 2053251. PMID 20248086.
- Donald, Kenneth W (1947). "Oxygen Poisoning in Man: Part II". British Medical Journal. 1 (4507): 712–17. doi:10.1136/bmj.1.4507.712. PMC 2053400. PMID 20248096.
- 도날드 기사 개정판도 다음과 같이 이용할 수 있다.
- Donald, Kenneth W (1992). Oxygen and the diver. UK: Harley Swan, 237 pages. ISBN 1-85421-176-5. OCLC 26894235.
- Hamilton, Robert W; Thalmann, Edward D (2003). "Decompression practice". In Brubakk, Alf O; Neuman, Tom S (eds.). Bennett and Elliott's physiology and medicine of diving (5th ed.). United States: Saunders. pp. 475–79. ISBN 978-0-7020-2571-6. OCLC 51607923.
- Lang, Michael A, ed. (2001). DAN nitrox workshop proceedings. Durham, NC: Divers Alert Network, 197 pages. Archived from the original on 16 September 2011. Retrieved 20 September 2008.
- Regillo, Carl D; Brown, Gary C; Flynn, Harry W (1998). Vitreoretinal Disease: The Essentials. New York: Thieme, 693 pages. ISBN 978-0-86577-761-3. OCLC 39170393.
- U.S. Navy Supervisor of Diving (2011). U.S. Navy Diving Manual (PDF). SS521-AG-PRO-010 0910-LP-106-0957, revision 6 with Change A entered. U.S. Naval Sea Systems Command. Archived from the original (PDF) on 10 December 2014. Retrieved 29 January 2015.
추가 읽기
- Lamb, John S. (1999). The Practice of Oxygen Measurement for Divers. Flagstaff: Best Publishing, 120 pages. ISBN 0-941332-68-3. OCLC 44018369.
- Lippmann, John; Bugg, Stan (1993). The Diving Emergency Handbook. Teddington, UK: Underwater World Publications. ISBN 0-946020-18-3. OCLC 52056845.
- Lippmann, John; Mitchell, Simon (2005). "Oxygen". Deeper into Diving (2nd ed.). Victoria, Australia: J.L. Publications. pp. 121–24. ISBN 0-9752290-1-X. OCLC 66524750.
외부 링크
일반
다음의 외부 사이트는 자원의 종합이다.
- Rubicon Research Repository – 산소 독성 연구 온라인 모음
전문화
다음 외부 사이트에는 특정 주제에 해당하는 리소스가 포함되어 있다.
- 2008년 다이버 경보 네트워크 기술 다이빙 컨퍼런스 – Richard Vann 박사의 "산소 독성" 강의 비디오(무료 다운로드, mp4, 86MB)
- Nosek, Thomas M. "Section 4/4ch7/s4ch7_7". Essentials of Human Physiology. Archived from the original on 24 March 2016. – 호흡 산소가 호흡기에 미치는 영향에 대한 논의
- Rajiah, Prabhakar (11 March 2009). "Bronchopulmonary Dysplasia". eMedicine. WebMD. Retrieved 29 June 2009. – 참조를 포함한 임상 개요