유전자 조작 식품
Genetically modified food| 시리즈의 일부 |
| 유전공학 |
|---|
 |
| 유전자 조작 생물 |
| 역사와 규정 |
| 과정 |
| 적용들 |
| 논쟁 |
유전자 조작 식품 또는 유전자 조작 식품으로 알려진 유전자 조작 식품은 유전자 공학의 방법을 사용하여 DNA에 변화를 도입한 유기체로부터 생산된 식품이다.유전자 공학 기술은 선택적 사육과 돌연변이 [1]사육과 같은 이전의 방법에 비해 새로운 형질을 도입할 수 있을 뿐만 아니라 형질을 더 잘 제어할 수 있게 해준다.
20세기 DNA의 발견과 유전자 기술의 발전은 유전자 변형 [2]기술의 발전에 결정적인 역할을 했다.1988년 유전자 변형 미생물 효소가 식품 제조에 사용되도록 처음으로 승인되었다.재조합 레넷은 1990년대에 [3]소수의 국가에서 사용되었다.유전자 변형 식품의 상업적인 판매는 1994년 칼겐이 실패한 플라브 사브르의 지연 숙성 [4][5]토마토를 처음 판매했을 때 시작되었다.대부분의 식품 변형은 주로 콩, 옥수수/옥수수, 유채, 목화와 같은 농부들의 수요가 많은 현금 작물에 초점을 맞추고 있다.유전자 조작 작물은 병원균과 제초제에 대한 저항성과 더 나은 영양분 프로파일을 위해 개발되었습니다.2000년의 황금 쌀 생산량은 유전자 변형 [6]식품의 영양가 면에서 더 큰 향상을 보였다.GM 가축은 개발되었지만, 2015년 현재[update] [7]시판되고 있는 가축은 없습니다.2015년 현재,[8][9] AquAdvantage 연어는 FDA에 의해 상업적 생산, 판매 및 소비가 승인된 유일한 동물이었다.그것은 인간의 소비를 위해 승인된 최초의 유전자 변형 동물이다.
바람직한 특징, 예를 들어 개선된 영양소 수준, 농약 및 제초제 내성, 치료 물질의 보유를 위해 코드화된 유전자는 종종 추출되어 대상 생물에게 전달되어 우수한 생존 및 생산 [10][11][12][13][14][15][16]능력을 제공한다.이용가치의 향상은 일반적으로 소비자에게 특정 [10][11][15]측면에서 혜택을 주었다.
유전자 변형 식품의 적용은 또한 변형된 유전자의 인간에 대한 부정적인 영향과 주변 [10][11][15][16][17][18]환경에 대한 오염을 포함한 몇 가지 잠재적 위험을 수반한다.이러한 우려는 유전자 변형 식품에 [10][16][19]대한 사람들의 다른 태도로 이어진다.현재 유전자 조작 작물에서 유래한 식품은 기존의 [25][26][27][28][29][30][31]식품보다 인간의 건강에 더 큰 위험을 초래하지 않지만,[32][33][34] 각 유전자 조작 식품은 도입 전에 케이스 바이 케이스(case by case)로 테스트해야 한다는 과학적 합의가[20][21][22][23][24] 있다.그럼에도 불구하고, 일반 대중들은 유전자 조작 식품이 [35][36][37][38]안전하다고 인식할 가능성이 과학자들보다 훨씬 적다.유전자 변형 식품의 법적, 규제적 지위는 국가마다 다르며, 일부 국가는 금지 또는 제한하고 있고, 다른 국가들은 지리적, 종교적, 사회적, 그리고 다른 [10][43][44][45][46]요인들로 인해 크게 다른 [39][40][41][42]규제 정도를 허용하고 있다.
그러나 식품 안전, 규제, 라벨 부착, 환경 영향, 연구 방법, 그리고 일부 유전자 조작 씨앗과 모든 새로운 식물 품종이 [47]기업이 소유한 식물 사육자의 권리에 따라 결정된다는 사실과 관련된 대중의 우려가 계속되고 있다.
정의.
유전자 변형 식품은 기존의 이종 [48][49]교배와 달리 유전자 공학적 방법을 사용하여 DNA에 변화를 가져온 유기체로부터 생산되는 식품이다.미국에서는 미국 농무부(USDA)와 식품의약국(FDA)이 유전자 변형보다 유전 공학이라는 용어를 사용하는 것을 선호한다. USDA는 "유전자 공학 또는 다른 전통적인 방법"[50][51]을 포함하도록 유전자 변형을 정의한다.
세계보건기구에 따르면, "유전자 유기체에서 생산되거나 유전자 변형 유기체를 사용하여 생산된 식품은 종종 유전자 변형 [48]식품이라고 불린다."
유전자 변형 유기체(GMO)를 구성하는 것은 명확하지 않고 국가, 국제기구 및 기타 지역사회에 따라 크게 달라졌으며, EU의 정의에서 [52]돌연변이 번식을 제외하는 등 "관습"에 기초한 수많은 예외를 적용받았다.
식품 마케팅의 다양한 "비 GMO" 또는 "GMO-free" 라벨링 체계와 더 큰 불일치와 혼란이 관련되어 있으며, 물이나 소금과 같은 제품도 유기 물질과 유전 물질을 포함하지 않고(따라서 정의에 따라 유전적으로 변형될 수 없음) 라벨링을 통해 "더 많은 유전자 변형"의 인상을 만들어 내고 있다.건강합니다.[53][54]
역사
식품에 대한 인간 주도의 유전자 조작은 기원전 [55]: 1 10,500년에서 10,100년 사이에 인위적인 선택을 통해 식물과 동물의 가축화와 함께 시작되었다.유전자 변형(GM)[55]의 현대적인 개념:1[56]:1DNA의 1900년대 초기 발견과 그는에서 다양한 발전하고 있는 선택적 사육의 원하는 특색을 지닌 유기체(그리고 이처럼을 원하는 유전자)다음 세대와 유기체는 특성이 번식하기 위해 사용되는 과정이 아니다 교육이 된 것.netic 기술1970년대까지[2] 음식 안의 DNA와 유전자를 직접 바꾸는 것이 가능해졌다.
유전자 조작 미생물 효소는 식품 생산에 유전자 조작 생물을 최초로 적용한 것으로 1988년 미국 식품의약국에 [3]의해 승인되었다.1990년대 초, 재조합 키모신은 여러 [3][57]국가에서 사용이 승인되었다.치즈는 전형적으로 소의 위벽에서 추출한 복합 레넷 효소를 사용하여 만들어졌다.과학자들은 키모신을 생성하기 위해 박테리아를 변형시켰는데, 키모신은 우유를 응고시켜 치즈 [58]응고를 만들었다.
최초로 [4]유전자 조작 식품이 출시가 승인된 것은 1994년 플라브르 사브르 토마토였습니다.칼젠이 개발한 이 제품은 숙성을 지연시키는 [59]안티센스 유전자를 삽입해 유통기한이 길어지도록 설계됐다.중국은 1993년 바이러스 내성 [60]담배를 도입하면서 유전자 변형 작물을 상용화한 첫 번째 국가였다.1995년에는 바실루스 튀링겐시스(Bt) 감자의 재배가 승인되어 미국에서 [61]최초로 농약 생산 작물이 승인되었다.1995년에 시판 허가를 받은 다른 유전자 변형 작물로는 유채꽃, BT 옥수수/옥수수, 제초제 브로목실닐에 강한 면화, BT 면화, 글리포세이트 내성 콩, 바이러스 내성 호박, 그리고 다른 지연 숙성 [4]토마토가 있었다.
2000년 황금 쌀이 만들어지면서 과학자들은 처음으로 [6]영양가치를 높이기 위해 유전자 조작 식품을 개발했다.
2010년까지 29개국이 상품화된 생명공학 작물을 심었고, 추가로 31개국이 유전자 변형 작물의 [62]수입에 대한 규제 승인을 승인했다.미국은 2011년 GM 식품 생산에서 25개의 [63]GM 작물이 규제 승인을 받은 선두 국가였다.2015년에는 미국에서 생산된 옥수수의 92%, 콩의 94%, 면화의 94%가 유전자 변형 [64]품종이었다.
2015년 [65]최초로 식품 사용이 승인된 유전자 변형 동물은 AquAdvantage 연어였다.이 연어는 태평양 치누크 연어의 성장호르몬 조절 유전자와 바다 주둥이의 프로모터로 봄과 [66]여름뿐만 아니라 일년 내내 자랄 수 있도록 변형되었다.
유전자 조작 흰버튼 버섯(Agaricus bisporus)은 2016년부터 미국에서 승인되었습니다.아래 § Mushroom을 참조하십시오.
가장 널리 심어진 유전자변형농산물은 제초제를 견딜 수 있도록 고안되었다.제초제의 사용은 제초제에 대한 내성을 얻기 위해 처리된 잡초에 강한 선택 압력을 가한다.글리포세이트에 내성이 있는 유전자 변형 작물의 광범위한 재배는 잡초와 팔머 아마란스와 같은 많은 잡초 종들을 제어하기 위해 글리포세이트를 사용하는 것으로 이어져 제초제에 [67][68][69]대한 내성을 갖게 되었다.
2021년, 최초의 CRISPR 편집 식품이 일본에서 공매에 들어갔습니다.토마토는 GABA를 [71]진정시킬 수 있는 정상[70] 양의 약 5배 정도로 유전자 조작되었다.CRISPR은 [72]2014년에 토마토에 처음 적용되었다.그 후, 식욕을 억제하는 렙틴의 교란으로 1종이 자연 표본의 2배로 성장해, 다른 1종이 자연 표본의 1.2배로 성장해, 1종이 식욕을 억제하는 제1세트의 해양 동물·해산물·해산물·해산물·해산물·2세트가 일본에서 공매에 들어갔다.근육 [73][74][75]성장을 억제하는 미오스타틴 장애로 인해 발생한다.
과정
유전자 변형 식품을 만드는 것은 다단계 과정이다.첫 번째 단계는 당신이 추가하고 싶은 다른 유기체의 유용한 유전자를 확인하는 것이다.이 유전자는 세포에서[76] 추출되거나 인공적으로 [77]합성될 수 있으며, 프로모터 및 터미네이터 영역과 선택 가능한 [78]마커를 포함한 다른 유전 요소와 결합될 수 있습니다.그런 다음 유전자 요소가 표적 게놈에 삽입됩니다.DNA는 일반적으로 미세 주입을 사용하여 동물 세포에 삽입되는데, 여기서 세포 핵 외피를 통해 직접 주입되거나 바이러스 [79]벡터를 사용하여 주입될 수 있습니다.식물에서 DNA는 종종 아그로박테륨 매개 재조합,[80][81] 생물학[82] 또는 전기학으로 삽입된다.오직 하나의 세포만이 유전 물질로 변형되기 때문에, 유기체는 그 단일 세포에서 재생되어야 한다.식물에서 이것은 조직 [83][84]배양에 의해 달성된다.동물에서는 삽입된 DNA가 배아줄기세포에 [80]존재하는지 확인하는 것이 필요하다.PCR, Southern Hybridation 및 DNA Sequencing을 사용하여 유기체가 새로운 [85]유전자를 가지고 있는지 확인하기 위한 추가 시험을 실시한다.
전통적으로 새로운 유전 물질은 숙주의 게놈 안에 무작위로 삽입되었다.이중가닥 절단을 만들어 세포 자연적 상동 재조합 복구 시스템을 활용하는 유전자 표적화 기술은 정확한 위치에 삽입하는 것을 목표로 개발되었습니다.게놈 편집은 인공적으로 조작된 핵산가수분해효소를 사용하여 특정 지점에서 파괴를 일으킨다.공학적 핵산가수분해효소에는 메가핵산가수분해효소,[86][87] 아연 핑거 핵산가수분해효소,[88][89] 전사활성화제 유사 이펙터 핵산가수분해효소(TALENs)[90][91] 및 Cas9-가이드의 네 가지 종류가 있다.RNA 시스템(CRISPR에서 [92][93]채택됨).TALEN과 CRISPR은 가장 일반적으로 사용되는 두 가지이며 각각 고유한 [94]장점이 있습니다.TALEN은 타겟의 특수성이 높은 반면 CRISPR은 설계하기 쉽고 [94]효율적입니다.
유기체별
농작물.
유전자 조작 작물(GM 작물)은 농업에 사용되는 유전자 조작 식물이다.처음 개발된 작물은 동물이나 인간의 먹이로 사용되었으며 특정 해충, 질병, 환경 조건, 부패 또는 화학적 처리(예: 제초제에 대한 내성)에 대한 저항성을 제공하였다.제2세대의 작물은 종종 영양소 프로파일을 변경함으로써 품질을 향상시키는 것을 목표로 했다.3세대 유전자 변형 작물은 의약품, 바이오 연료 및 기타 산업적으로 유용한 상품의 생산뿐만 아니라 생물적 [95]매개에도 사용될 수 있다.유전자 변형 작물은 곤충의 압력을 줄이고 영양가를 높이며 다양한 비생물적 스트레스를 견뎌냄으로써 수확량을 개선하기 위해 생산되었다.2018년 현재 상용화된 작물은 대부분 면화, 콩, 옥수수/옥수수 및 유채나무와 같은 현금 작물로 제한되며, 도입된 특성의 대부분은 제초제 내성 또는 [95]내충성을 제공한다.
GM 작물의 대부분은 보통 글리포세이트 또는 글루포세이트 기반 제초제인 엄선된 제초제에 내성이 있도록 수정되었습니다.제초제에 내성을 갖도록 설계된 유전자 변형 작물은 이제 기존의 내성 [96]품종보다 더 많이 구할 수 있다.현재 곤충의 내성을 개발하는 데 사용되는 대부분의 유전자는 바실러스 튜링기엔시스(Bt) 박테리아와 델타 엔도톡신 코드로부터 나온다.몇몇은 식물성 살충 [97]단백질을 암호화하는 유전자를 사용한다.B. 튜링겐시스에서 유래하지 않은 곤충 보호를 위해 상업적으로 사용되는 유일한 유전자는 Cowpea 트립신 억제제입니다.CpTI는 1999년 처음 면화 사용이 승인돼 현재 [98][99]쌀 시험 중이다.유전자 조작 작물의 1% 미만이 바이러스 내성 제공, 노화 지연, 식물 [100]조성 변경 등 다른 특성을 포함하고 있다.
1996년부터 2013년 사이에 GM 작물로 경작된 토지의 총 표면적이 [101]100배 증가했다.지리적으로 볼 때 미주 및 아시아 일부 지역에서는 강력한 성장이 이루어졌고 2013년 유럽과 아프리카에서는[95] 거의 성장하지 않은 가운데 GM은 세계 경작지의 10%에 불과했으며, 미국, 캐나다, 브라질 및 아르헨티나는 이 [24]중 90%를 차지했습니다.2013년 전 세계 GM 작물의 약 54%[101]가 개발도상국에서 재배되면서 사회경제적 확산은 더욱 균등해졌다.비록 의문이 [102]제기되었지만, 대부분의 연구는 GM 작물을 재배하는 것이 농약 사용 감소와 농작물 생산량 및 농업 [103][104][105]이익 증가를 통해 농부들에게 유익하다는 것을 발견했다.
과일과 야채
인간이 유전자변형을 사용하기 훨씬 전인 8000년 전 고구마는 박테리아 유전자를 내장해 당도를 높임으로써 자연스럽게 생겨났다.Kyndt et al 2015는 이 자연적인 유전자 변형 사건으로부터 [106][107]: 141 [108][109]아그로박테리움 투메파시엔스 DNA를 오늘날에도 여전히 이 작물의 게놈에서 발견한다.
파파야는 링스팟 바이러스(PSRV)에 저항하기 위해 유전자가 변형됐다. "SunUp"은 외피 단백질 유전자 PRSV와 동질인 트랜스제닉 선셋 파파야 품종이다. "Rainbow"는 "SunUp"와 "ntransic"을 교배하여 개발된 노란 살의 F1 잡종이다.GM 품종은 1998년에[111] 승인되었고 2010년까지 하와이산 파파야의 80%가 [112]유전공학으로 만들어졌다.뉴욕타임스는 "그것이 없었다면, 그 주의 파파야 산업은 [112]붕괴되었을 것이다"라고 말했다.중국에서 트랜스제닉 PRSV 내성 파파야는 남중국농업대학에 의해 개발되어 2006년에 상업용 식재 허가를 받았습니다.2012년 현재 광둥성에서 재배되는 파파야의 95%, 하이난성에서 재배되는 파파야의 40%가 유전자 [113]변형되었습니다.유전자 변형 파파야의 재배와 방출이 면제되는 홍콩에서는 재배와 수입 파파야의 80% 이상이 [114][115]트랜스제닉이었다.
바실러스 튜링기엔시스(Bt)를 이용해 개발된 유전자 조작 식품인 뉴 리프 포테이토는 생산량을 줄이는 콜로라도 [116]감자풍뎅이로부터 식물 내 보호를 제공하기 위해 만들어졌다.1990년대 후반 몬산토가 시장에 내놓은 뉴리프 포테이토는 패스트푸드 시장용으로 개발됐다.2001년 소매업자들이 이를 거부했고 식품 가공업자들이 수출 문제에 부딪히자 철수했다.2011년 BASF는 유럽 식품안전국에 사료 및 식품으로 포춘 감자의 재배 및 시판 승인을 요청했다.이 감자는 멕시코산 야생감자 솔라넘 [117][118]구근가스타눔에서 유래한 내성 유전자 blb1, blb2를 첨가해 늦깎이에 저항력을 갖게 했다.2013년 2월 BASF는 [119][120]신청을 철회했다.2014년, USDA는 J.R. Simplot Company가 개발한 유전자 변형 감자를 승인했습니다. 이 감자는 타박상을 방지하고 튀겼을 때 아크릴아미드를 덜 생성하는 10가지 유전자 변형입니다.수정은 새로운 [121][122]단백질을 도입하는 대신 RNA 간섭을 통해 감자에서 특정 단백질을 제거한다.
2005년 현재 미국에서 재배된 애호박의 약 13%는 세 가지 바이러스에 저항하기 위해 유전자 조작되었습니다.[123][124]그 종류는 캐나다에서도 재배되고 있습니다.
USDA는 2013년 핑크색 GM 파인애플의 수입을 승인하고 귤에서 유래한 유전자를 과다 발현시켜 다른 유전자를 억제해 리코펜 생산을 늘렸다.그 식물의 개화 주기는 보다 균일한 성장과 품질을 제공하기 위해 바뀌었다.USDA APHIS에 따르면, 이 과일은 "일단 수확된 후에는 환경에서 번식하고 지속할 능력이 없다"고 한다.델몬테의 제출에 따르면, 파인애플은 씨앗 생산을 막는 "단일 재배" 방식으로 상업적으로 재배되고 있는데, 이는 이 식물의 꽃들이 조화로운 꽃가루 공급원에 노출되지 않기 때문이다.하와이로의 수입은 "식물 위생"[125]상의 이유로 금지되어 있습니다.델몬테는 2020년 10월에 핑크 파인애플의 판매를 개시해, 「핑크글로우」[126]라고 하는 이름으로 마케팅을 개시했다.
2015년 2월 북극 사과는 USDA에 [127]의해 승인되어 미국에서 [128]판매 승인된 최초의 유전자 변형 사과가 되었습니다.유전자 사일런싱은 폴리페놀산화효소(PPO)의 발현을 감소시켜 과일이 [129]갈변하는 것을 방지하기 위해 사용된다.
옥수수/옥수수
식품과 에탄올에 사용되는 옥수수/옥수수는 다양한 제초제를 견디고 특정 [130]곤충을 죽이는 바실러스 튜링겐시스(Bt)의 단백질을 발현시키기 위해 유전자 변형되었습니다.미국에서 재배되는 옥수수의 약 90%가 [131]2010년에 유전자 조작되었습니다.2015년 미국에서는 옥수수 면적의 81%가 BT 특성을, 옥수수 면적의 89%가 글리포산염 내성 특성을 [64]포함했습니다.옥수수는 팬케이크, 머핀, 도넛, 빵, 튀김뿐만 아니라 유아용 식품, 육류 제품, 시리얼 및 일부 발효 제품의 재료로서 그레이트, 식사 및 밀가루로 가공될 수 있습니다.옥수수 기반의 마사 밀가루와 마사 반죽은 타코 껍질, 옥수수 칩, 토르티야 [132]생산에 사용된다.
콩
콩은 2014년 [100]재배된 전체 유전자 변형 작물의 절반을 차지했다.유전자 변형 콩은 제초제를 견디고 건강한 [133]기름을 생산하도록 변형되었다.2015년 미국 콩 경작지의 94%가 글리포세이트 [64]내성이 있도록 유전자 변형되었습니다.
밥
황금쌀은 영양가 상승을 목적으로 하는 가장 잘 알려진 유전자 조작 작물이다.쌀의 식용 부분에 비타민 A의 전구물질인 [134]베타카로틴을 생합성하는 3가지 유전자로 제작됐다.비타민 [135]A가 부족한 지역에서 재배되고 소비되는 강화 식품을 생산하기 위한 것이다.이 결핍은 매년 67만 명의 5세 미만의 어린이를[136] 죽이고 50만 명의 소아 [137]실명 사례를 추가로 발생시키는 것으로 추정된다.원래의 황금쌀은 1.6μg/g의 카로티노이드를 생성하였고, 그 이상의 개발은 23배 [138]증가하였다.2018년에 처음으로 [139]식품 사용 승인을 받았습니다.
밀
2017년 12월 현재 유전자 변형 밀은 현장시험에서 평가되고 있으나 상업적으로 [140][141][142]출시되지는 않았다.
버섯
2016년 4월, 크리스퍼(CRISPR) 기술을 사용하여 변형된 흰버튼버섯(Agaricus bisporus)은 USDA의 규제절차를 거치지 않아도 된다고 밝혀 미국에서 사실상의 승인을 받았다.이 기관은 편집 과정이 외래 DNA 도입과 관련이 없기 때문에 버섯이 면제된 것으로 간주하고 있으며, 오히려 여러 염기쌍이 중복 유전자에서 삭제되어 갈변을 일으키는 효소가 검출되어 해당 [143]효소의 수치가 30% 감소하였다.
가축.
유전자 조작 가축은 인간의 소비를 위해 사육되는 소, 양, 돼지, 염소, 새, 말, 물고기의 집단에서 유래한 유기체로, 이들의 유전 물질(DNA)은 유전자 공학적 기술을 사용하여 변형되었다.경우에 따라서는, 종에서 자연적으로 발생하지 않는 새로운 특성, 즉 유전자 변형(transgenis)을 동물에게 도입하는 것이 목적이다.
호주 뉴질랜드 식품표준(Food Standards Australia New Zealand)을 대표하여 발행된 2003년 리뷰에서는 육지 가축 종과 어패류 등의 수생 종에 대한 유전자 변환 실험을 조사했다.검토는 실험에 사용된 분자 기술뿐만 아니라 동물과 제품의 트랜스유전자를 추적하는 기술, 트랜스유전자의 [144]안정성에 관한 문제를 조사했다.
일반적으로 식량 생산에 사용되는 일부 포유류는 비식용품을 생산하기 위해 변형되었는데, 이러한 관행은 때때로 파밍이라고 불린다.
연어
1997년부터 [147]규제 승인을[145][146][8] 기다리고 있는 GM 연어는 2015년 11월 미국 FDA에 의해 인간 소비를 승인받아 캐나다와 [148]파나마의 특정 육지 부화장에서 사육되고 있다.
미생물
박테리오파지는 치즈 생산에서 배양 실패의 경제적으로 중요한 원인이다.다양한 배양 미생물, 특히 락토코커스 락티스와 스트렙토코커스 서모필러스는 내파지성을 개선하기 위해 유전자 분석과 수정을 위해 연구되어 왔다.이것은 특히 플라스미드와 재조합 염색체 [149][150]변형에 초점을 맞추고 있다.
파생상품
레시틴
레시틴은 자연적으로 발생하는 지질이다.그것은 계란 노른자와 기름을 생산하는 식물에서 발견될 수 있다.그것은 유화제이기 때문에 많은 음식에 사용된다.옥수수, 콩, 홍화기름은 레시틴의 공급원이지만 상업적으로 이용 가능한 레시틴의 대부분은 [151][152][153][page needed]콩에서 유래한다.충분히 처리된 레시틴은 표준 [154][failed verification]검사 방식으로는 종종 검출되지 않는다.FDA에 따르면 레시틴이 일반 수준에서 사용될 경우 일반인에게 위험을 나타내거나 시사하는 증거는 없다.식품에 첨가되는 레시틴은 하루에 [151][152]섭취되는 포스포글리세리드 1~5g의 2~10%에 불과합니다.그럼에도 불구하고, 유전자 조작 식품에 대한 소비자의 우려는 그러한 [155][better source needed]제품들로까지 확대된다.이러한 우려는 2000년 유럽에서 정책 및 규제 변화로 이어졌으며,[citation needed] 규정([citation needed]EC) 50/2000이 통과되면서[156] 레시틴을 포함한 GMO에서 파생된 첨가물을 함유한 식품의 라벨 표시가 요구되었다.현재의 테스트 관행에서는 레시틴과 같은 파생상품의 출처를 검출하는 것이 어렵기 때문에 유럽 규제는 유럽에서 레시틴을 판매하려는 사람들에게 포괄적인 신원 보존 시스템(IP)[157][verification needed][158][page needed]을 사용하도록 요구한다.
설탕
미국은 설탕의 10%를 수입하고 나머지 90%는 사탕무와 사탕수수에서 추출한다.2005년 규제완화 이후 미국에서는 글리포세이트 내성 사탕무가 광범위하게 채택되었다.미국 [159]비트 에이커의 95%는 2011년에 글리포세이트 내성 씨앗을 심었습니다.GM 사탕무는 미국, 캐나다 및 일본에서 재배가 승인되어 있으며, 대부분은 미국에서 재배되고 있습니다.GM 사탕무는 호주, 캐나다, 콜롬비아, EU, 일본, 한국, 멕시코, 뉴질랜드, 필리핀, 러시아 연방 [160]및 싱가포르에서 수입 및 소비가 승인되어 있습니다.정제 공정에서 나온 펄프를 동물 사료에 사용한다.유전자 조작 사탕무에서 생산된 설탕은 DNA나 단백질을 포함하지 않는다 – 그것은 단지 화학적으로 유전자 조작 사탕무에서 [154][161]생성된 설탕과 구별할 수 없는 수크로스이다.국제적으로 인정받는 연구소가 실시한 독자적인 분석에 따르면, Roundup Ready 설탕 비트의 설탕은 비교적 성장한 기존의 (Non-Roundup Ready) 설탕 [162]비트의 설탕과 동일한 것으로 나타났습니다.
식물성 기름
미국에서 사용되는 대부분의 식물성 기름은 GM 작물 유채나무,[163] 옥수수[166]/옥수수,[164][165] 면화 및 [167]콩에서 생산됩니다.식물성 기름은 식용유, 쇼트닝, 마가린으로[168] 소비자에게 직접 판매되며 조리된 식품에 사용된다.식물성 [154][169]기름에는 원래 작물의 단백질이나 DNA가 아주 소량 들어 있습니다.식물성 기름은 식물이나 씨앗에서 추출한 트리글리세리드로부터 만들어지고 정제되며, 액체 오일을 고체로 바꾸기 위해 수소화를 통해 추가로 처리될 수 있다.정제 공정은 모든 또는 거의 모든 비트리글리세리드 [170]성분을 제거합니다.
기타 용도
동물 사료
가축과 가금류는 동물성 사료로 사육되는데, 그 대부분은 유전자 조작 작물을 포함한 가공 작물의 잔여물로 구성되어 있다.예를 들어, 유채 씨앗의 약 43%가 기름입니다.기름 추출 후 남는 것은 동물 사료의 원료가 되어 유채단백질이 [171]함유된 식사입니다.마찬가지로, 콩의 대부분은 기름과 식사를 위해 재배된다.고단백질의 탈지, 구운 콩밥은 가축 사료와 개 사료입니다.미국 콩 수확량의 98%가 가축 [172][173]사료에 쓰인다.2011년 미국 옥수수/옥수수 수확량의 49%가 가축 사료에 사용되었습니다(증류기 [174]곡물의 폐기물 비율 포함)."점점 민감해지고 있는 방법들에도 불구하고, 실험에서는 먹이는 사료의 종류에 따라 동물들의 고기, 우유, 달걀의 차이를 아직 밝혀내지 못했습니다.그 결과 나온 고기, 유제품, 계란 제품만 보고 동물이 유전자 변형 콩을 먹었는지 구별하는 것은 불가능하다.동물 사료에 GMO가 있는지 확인하는 유일한 방법은 사료 자체의 [175]원산지를 분석하는 것입니다.
2012년 GM 사료의 동물 건강에 미치는 영향을 평가하는 연구의 문헌 검토에서는 작은 생물학적 차이가 가끔 발견되긴 했지만 동물이 부정적인 영향을 받았다는 증거는 발견되지 않았다.검토에 포함된 연구는 90일에서 2년 사이였으며, 긴 연구 중 일부는 생식 [176]및 세대 간 영향을 고려했다.
유전자 변형 미생물에 의해 생성된 효소는 영양소의 가용성과 전반적인 소화를 향상시키기 위해 동물 사료에 통합된다.이러한 효소들은 사료의 [177]가수분해 항영양인자뿐만 아니라 동물의 내장 미생물체에도 이점을 제공할 수 있다.
단백질
유전공학의 기초는 단백질 생산을 지시하는 DNA다.단백질은 또한 인간 알레르겐의 흔한 공급원이다.[178]새로운 단백질이 도입되면 잠재적 알레르기 [179]유발성을 평가해야 한다.
레넷은 우유를 치즈로 응고시키는 데 사용되는 효소의 혼합물이다.원래 송아지의 네 번째 위에서만 구할 수 있었고, 희귀하고 비쌌거나, 종종 불쾌한 맛을 내는 미생물 공급원에서 구할 수 있었다.유전자 공학을 통해 동물의 위에서 레넷을 생성하는 유전자를 추출하여 박테리아, 곰팡이, [180][181]효모에 삽입하여 키모신을 생성하는 것이 가능해졌다.변형된 미생물은 발효 후에 죽는다.발효육수로부터 키모신을 분리하여 치즈 제조자가 사용하는 발효생산 키모신(FPC)은 소 레넷과 [182]동일한 아미노산 배열을 가진다.도포된 키모신의 대부분은 유장에 저장됩니다.치즈에는 [182]미량의 키모신이 남아있을 수 있다.
FPC는 미국 식품의약국에 [3][57]의해 승인된 최초의 인공 생산 효소였다.FPC 제품은 1990년부터 출시되어 2015년 현재 상업 시장에서 [183]추월당하지 못하고 있다.1999년에는 미국 하드 치즈의 약 60%가 [184]FPC로 만들어졌습니다.세계 시장 점유율은 80%[185]에 육박했다.2008년까지 미국과 영국에서 상업적으로 만들어진 치즈의 약 80~90%가 [182]FPC를 사용하여 만들어졌다.
일부 국가에서는 우유 생산을 증가시키기 위해 재조합(GM) 소머토트로핀(rBST, 소 성장호르몬 또는 BGH라고도 함) 투여가 승인되었습니다.rBST는 rBST 처리된 소의 우유에 존재할 수 있지만 소화 시스템에서 파괴되어 사람의 혈류에 직접 주입되어도 관찰할 수 없습니다.FDA,[186][187][188] 세계보건기구, 미국 의학협회, 미국 영양학협회, 국립보건원은 독립적으로 rBST 처리된 소의 유제품과 고기가 인간의 소비에 [189]안전하다고 밝혔다.2010년 9월 30일, 미국 항소법원 제6순회법원은 제출된 증거를 분석한 결과, rBGH 처리된 소의 우유와 처리되지 않은 [190][191]소의 우유의 "성분 차이"를 발견했다.법원은 rBGH 처리된 젖소의 우유가 증가했다고 밝혔다: 인슐린 유사 성장인자 1(IGF-1) 호르몬의 증가, 젖소의 수유 주기 중 특정 지점에서 생산될 때 더 높은 지방 함량과 낮은 단백질 함량, 그리고 더 많은 체세포 수치가 [191]"우유를 더 빨리 상하게 만들 수 있다".
혜택들
유전자 조작 식품은 보통 극한 환경에서의 생존을 위한 특정한 이점, 강화된 영양 수준, 치료 물질의 접근, 그리고 살충제와 제초제에 대한 내성 유전자를 포함하여 원하는 특성을 가지도록 편집된다.이러한 특징들은 특정한 방법으로 인간과 환경에 유익할 수 있다.
극한의 날씨에 대비하다
유전자 변형을 거친 식물은 극한의 [10]날씨에도 살아남을 수 있다.유전자 변형(GM) 식품 작물은 때때로 [11]기후 조건이 좋지 않은 곳에서 재배될 수 있다.유전자 변형 식품의 품질과 생산량은 종종 [10]개선된다.이러한 식품들은 기존에 재배된 것보다 더 빨리 자라는 경향이 있다.게다가, 유전자 변형 식품의 적용은 가뭄과 척박한 [11]토양에 저항하는데 유익할 수 있다.
영양 강화
식품 작물의 특정 영양소의 증가 수준은 유전자 공학을 통해 달성될 수 있다.때때로 영양 개선으로 알려진 이 기술에 대한 연구는 이미 상당히 [10]진전되어 있다.식품은 다양한 [19]식단의 바람직한 구성 요소인 농축된 영양 수준과 건강 증진 화학물질과 같은 실용적인 특성을 얻기 위해 잘 감시된다.유전자 변형의 주목할 만한 발견 중 하나는 골든 라이스인데, 골든 라이스는 수선화 식물 조절 프로비타민 A [10][19]생산에서 비타민 A 유전자를 주입함으로써 게놈이 변화한다.이것은 피토엔 합성효소의 활성을 증가시키고, 따라서 더 많은 양의 베타카로틴을 합성하며, 철분 및 생물학적 [13][15]가용성의 수정과 개선이 뒤따른다.이것은 쌀의 색깔과 비타민 함량에 영향을 미치는데, 이것은 비타민 A가 [10]많이 부족한 곳에 이롭다.또한 미네랄, 비타민 A, 단백질 함량의 증가는 소아 실명과 철분 결핍 [13]빈혈 예방에 중요한 역할을 했다.
지질 조성 또한 바람직한 특징과 필수 [15]영양소를 생산하기 위해 조작될 수 있다.과학적 증거는 오메가-3 다불포화 지방산의 부적절한 섭취가 일반적으로 만성 질환의 발병과 발달 [12][14]이상과 관련이 있다는 것을 보여주었다.소화지질을 수식하여 감소된 다포화지방산 성분과 함께 증가된 포화지방산을 얻을 수 있다.따라서 불포화지방산의 합성을 위해 코드화된 유전자가 식물 세포에 도입되어 다불포화 오메가-3산의 [15]합성을 증가시킨다.이 오메가3 다불포화 지방산은 심혈관 [12][14][15]질환의 발병률뿐만 아니라 LDL 콜레스테롤과 트리글리세리드 수치를 낮추는 데 기여합니다.
치료 물질의 제조
감자, 토마토, 시금치를 포함한 유전자 변형 유기체는 면역 체계를 자극하여 특정 [15]병원균에 반응하는 물질을 생산하는데 사용된다.재조합 DNA 기술의 도움으로, 바이러스 또는 박테리아 항원을 위해 암호화된 유전자는 유전적으로 전사되고 식물 [15][16]세포로 변환될 수 있다.항체는 종종 항원의 도입에 반응하여 만들어지는데, 병리학적 미세 꽃은 특정 항원에 대한 면역 반응을 얻습니다.트랜스제닉 유기체는 보통 점막 면역 반응을 자극하는 소화관을 목표로 활성 물질이 인간의 소화기 계통에 들어갈 수 있도록 하는 경구 백신으로 사용된다.이 기술은 쌀, 옥수수, [15]콩을 포함한 백신 생산에 널리 사용되어 왔다.또한 트랜스제닉 식물은 백신, 호르몬, 인간혈청알부민(HSA) 등을 포함한 의약품단백질 및 펩타이드의 제조에 생물반응제로서 널리 이용된다.트랜스제닉 식물의 적합성은 치료용 [14]항체의 빠른 성장에 대한 수요를 충족시키는 데 도움을 줄 수 있다.이 모든 것이 [14][15][16]의학 발전에 새로운 자극을 주었다.
건강과 안전
현재 유전자 조작 작물에서 유래한 식품은 기존의 [25][26][27][28][29]식품보다 인간의 건강에 더 큰 위험을 초래하지 않지만,[32][33][34] 각 유전자 조작 식품은 도입 전에 케이스 바이 케이스(case by case)로 테스트해야 한다는 과학적 합의가[20][21][22][23] 있다.그럼에도 불구하고, 일반 대중들은 유전자 조작 식품이 [35][36][37][38]안전하다고 인식할 가능성이 과학자들보다 훨씬 적다.유전자 변형 식품의 법적, 규제적 지위는 국가에 따라 다르며, 일부 국가는 금지하거나 제한하고 있고,[39][40][41][42] 다른 국가는 규제 수준이 크게 다른 음식을 허용하고 있다.
반대론자들은 장기적인 건강 위험이 적절하게 평가되지 않았다고 주장하며 추가 검사, 라벨[192] 부착 또는 [193][194][195][196]시장에서의 제거의 다양한 조합을 제안합니다.
유전자 조작 식품(특히 잘 이해되고 안전하며 환경 친화적인 방식으로)과 다른 유기농(즉, 화학 살충제를 사용하지 않고 생산됨)에 대해 미국과 아마도 소비자들에게 2진법 선택을 제공하는 것으로 확인된 식품에 대한 인증은 없다.f 유전자 변형 식품 또는 유기농 [197][198][199]식품 중 하나.
테스트
유전자 변형 식품의 법적, 규제적 지위는 국가에 따라 다르며, 일부 국가는 금지하거나 제한하고 있고,[39][40][41][42] 다른 국가는 규제 수준이 크게 다른 음식을 허용하고 있다.미국, 캐나다, 레바논, 이집트와 같은 국가들은 추가적인 테스트가 필요한지 여부를 결정하기 위해 상당한 동등성을 사용하는 반면, 유럽연합, 브라질, 중국과 같은 많은 국가들은 사례별로만 GMO 재배를 허가한다.미국에서 FDA는 GMO가 "Generally Recognized as Safe"(GRAS)이므로 GMO 제품이 수정되지 않은 [200]제품과 실질적으로 동등한 경우 추가 테스트가 필요하지 않다고 판단했습니다.새로운 물질이 발견되면 잠재적인 독성, 알레르기 유발성, 인간으로의 유전자 이동 가능성 또는 다른 [48]유기체로의 유전자 교배에 대한 우려를 충족시키기 위해 추가 검사가 필요할 수 있습니다.
해를 끼친다고 주장하는 일부 연구는 신뢰를 잃었고, 어떤 경우에는 푸즈타이 사건이나 세랄리니 [24]사건 같은 연구자들에 대한 학계의 비난으로 이어졌다.
규정
GMO의 개발과 출시에 대한 정부의 규제는 국가마다 매우 다르다.현저한 차이는 미국의 GMO 규제와 유럽연합의 [42]GMO 규제를 분리한다.규정도 제품의 용도에 따라 달라집니다.예를 들어, 식품 사용을 의도하지 않은 작물은 일반적으로 식품 [201]안전을 책임지는 당국에 의해 검토되지 않는다.유럽 및 EU의 규제는 세계 어느 곳보다 훨씬 엄격하다.2013년에는 옥수수/옥수수 1개 품종과 감자 1개 품종만이 승인되었으며, 8개 EU 회원국은 [24]이마저도 허용하지 않았다.
미국의 규제
미국에서는 세 개의 정부 기관이 유전자변형농산물을 규제한다.FDA는 잠재적인 알레르겐이 있는지 유기체의 화학조성을 검사한다.미국 농무부(USDA)는 현장 테스트를 감독하고 GM 시드의 분포를 감시합니다.미국 환경보호국(EPA)은 곤충에 독성 있는 단백질을 포함하도록 변형된 식물을 포함한 농약 사용을 감시할 책임이 있다.EPA는 USDA와 마찬가지로 환경안전을 [202][better source needed]확보하기 위해 농약과 접촉한 작물의 현장시험과 유통을 감독하고 있다.2015년에 오바마 행정부는 정부가 GM [203]작물을 규제하는 방법을 갱신할 것이라고 발표했다.
1992년 FDA는 "Statement of Policy:신식물 품종에서 유래한 식품.이는 FDA가 재조합 디옥시리보핵산(rDNA) 기술을 이용해 개발한 신식물 품종에서 생산한 식품에 대해 식품, 의약품, 화장품법에 대한 해석을 명확히 한 것이다.FDA는 개발자들에게 개발 중인 생물 공학 식품에 대해 FDA와 상의할 것을 권장했다.FDA는 개발자들이 일상적으로 상담을 요청한다고 말한다.1996년 FDA는 협의 [204][205]절차를 업데이트했다.
StarLink 옥수수 리콜은 2000년 가을 300개 이상의 식품에서 인간의 [206]소비로 승인되지 않은 유전자 변형 옥수수/옥수수가 검출된 시점이었다.유전자 조작 식품에 대한 최초의 리콜이었다.
유럽 규정
유럽연합(EU)의 유전자 조작 생물에 대한 통제는 초국가적 [45]규제의 틀로서의 토론의 약속과 한계 이미지의 특정 부분이다.문제는 EU의 GMO규제에 의해 제기된 농업, 정치, 사회, 지위, 그리고 다른 분야에서 큰 문제를 일으켰다.EU법 다른 당국 공공 및 민간, 공공 정보의 한정 승인, 협의, 그리고 취향이 까다로운. 때에 책임을 배분하여 유전자 변형 농산물의 개발과 이용을 규제하[44][45]12.IPation [45]권한유럽인권협약(ECHR)은 EU 내 GM 생명공학에 일정한 권리와 보호를 제공했다.그러나 유럽의 기본권 헌장에서 강조된 바와 같이 인간의 존엄성, 자유, 평등, 연대의 가치와 민주주의와 법의 지위는 과학기술 연구개발의 [44]고용을 지배하는 윤리적 틀로 여겨진다.
EU 국가들의 정치적, 종교적, 사회적 차이로 인해 GM에 대한 EU의 입장은 100개 이상의 "GM이 없는" 지역을 포함하여 지리적으로 나뉘어져 왔다.유전자 조작 식품에 대한 지역별 태도가 다르기 때문에 유전자 [45]조작 식품에 대한 공통된 합의에 도달하는 것은 거의 불가능하다.그러나 최근 몇 년 사이 유럽연합(EU)에 대한 위기감은 더 크고 강력한 회원국들 중 몇 [46]개로 확대되고 있다.독일, 프랑스, 오스트리아, 이탈리아, 룩셈부르크를 포함한 일부 회원국은 GM [45][46]식품에 대한 대중의 반발에 대응하여 자국 내 특정 GM 식품의 재배를 금지하기도 했다.이 모든 것은 GM 식품이 환경과 인간의 건강에 해롭다는 태도를 가진 소비자들이 반(反)바이오텍 [43]연합에서 GM 식품에 반기를 들고 있는 것을 배경으로 하고 있다.GM 식품에 대한 현재의 정치적 교착상태는 또한 금지의 결과이며 과학적 방법과 [46]과정으로 아직 해결되지 않았다.여론은 [45]EU 협정의 주요 걸림돌인 GM 문제를 정치화하는 경향이 있다.
라벨링
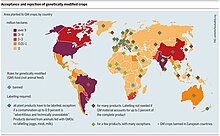
2015년 현재 64개국이 GMO 제품에 라벨을 부착해야 한다.
미국과 캐나다의 국가 정책은 일부 개별 미국 주(버몬트, 코네티컷 및 메인 주)가 이러한 사항을 [207][208][209][210]요구하는 법률을 제정했지만, 상당한 구성 차이 또는 문서화된 건강 영향만을 제공하는 라벨을 요구합니다.2016년 7월에는 GMO 식품에 대한 표시를 국가적으로 규제하기 위한 공법 114-214가 제정되었다.
일부 국가에서는 라벨링 요건이 제품 내 GMO의 상대적 양에 따라 달라진다.남아프리카공화국의 자발적 라벨링을 조사한 연구에 따르면 GMO 프리 라벨이 부착된 제품의 31%가 GM 함량이 1.0%[211]를 넘는 것으로 나타났습니다.
유럽연합에서는 0.9% 이상의 GMO를 함유한 모든 식품(가공식품 포함) 또는 사료를 라벨로 [212]표시해야 한다.
동시에 GMO의 단일하고 명확한 정의가 없기 때문에 유전자 공학 기술(예: 돌연변이 사육)을 사용하여 만들어진 많은 식품은 "관습"과 전통적인 [52]용법에 기초한 라벨링과 규제에서 제외된다.
Non-GMO Project는 검증 가능한 테스트를 실시하고 제품 내 GMO 존재 라벨에 스티커를 부착하는 유일한 미국 기관입니다.'Non-GMO Project Seal'에는 EU의 [213]라벨 표시 기준인 GMO 성분이 0.9% 이하인 것으로 나와 있습니다.
식품에 GMO를 제한하고 라벨을 붙이는 것을 돕기 위한 전 세계의 노력은 항원 공학 캠페인을 포함하고 있고 미국에서는 "Just Label It" 운동이 의무적인 라벨을 [213]붙이기 위해 단체들과 함께 하고 있다.
검출
식품과 사료에서 GMO에 대한 테스트는 PCR과 생물정보학 [214]같은 분자 기술을 사용하여 일상적으로 수행됩니다.
2010년 1월 논문에 따르면 완전한 공업용 콩유 처리망을 따라 DNA를 추출하고 검출하여 RR(Roundup Ready) 콩의 존재를 감시했다: "엔드포인트 중합효소 연쇄반응(PCR)에 의한 콩 렉틴 유전자의 증폭은 추출 및 정제 과정의 모든 단계에서 성공적으로 달성되었다.세스, 완전히 정제된 콩기름이 될 때까지.시료 불안정성으로 인한 정제 중간 단계(중화, 세척 및 표백)를 제외한 모든 추출 및 정제 단계에서 사건별 프라이머를 사용한 PCR 분석에 의한 RR 콩의 증폭도 달성되었다.특정 프로브를 사용한 실시간 PCR 어세이에서는 모든 결과가 확인되었으며 완전히 정제된 콩기름에서 유전자 변형 유기체를 검출하고 정량화할 수 있다는 것이 입증되었습니다.우리가 아는 바로는, 이것은 지금까지 보고된 적이 없고,[215] 정제유에서 유전자 조작 생물의 추적 가능성에 관한 중요한 업적입니다."
토마스 레딕에 따르면, 이종 수분의 검출과 방지는 농무청(FSA)과 천연자원보존청(NRCS)의 제안을 통해 가능하다.제안사항에는 농민들에게 공존의 중요성에 대한 교육, 공존을 촉진하기 위한 도구와 인센티브 제공, 유전자 흐름을 이해하고 감시하기 위한 연구 실시, 작물의 품질과 다양성의 보장 제공, [216]농민들에게 실제 경제적 손실에 대한 보상을 제공하는 것이 포함된다.
논쟁
유전자 조작 식품 논란은 유전자 조작 작물로 만든 식품의 사용에 대한 일련의 논쟁으로 구성되어 있다.이 분쟁에는 소비자, 농민, 생명공학 회사, 정부 규제 기관, 비정부 기구, 환경 및 정치 활동가, 과학자가 참여하고 있다.주요 불일치 사항에는 유전자 조작 식품을 안전하게 소비할 수 있는지, 인체와 환경을 해칠 수 있는지, 그리고/또는 적절하게 테스트하고 [194][217]규제할 수 있는지 등이 포함된다.과학 연구 및 출판물의 객관성에 [193]의문이 제기되어 왔다.농업 관련 분쟁에는 살충제의 사용과 영향, 종자 생산과 사용, 비 유전자변형농산물/[218]농장에 대한 부작용, 종자회사의 [193]유전자변형식품 공급에 대한 잠재적 통제 등이 포함된다.
GM 식품이 발명된 이래로 이러한 갈등은 계속되어 왔다.그들은 언론, 법원,[219] 지방, 지역, 국가 정부 및 국제 [citation needed]기구를 점령했다.
"GMO가 없는" 라벨 체계는 명확한 정의의 결여, 적용의 불일치 및 "기만적"[220][221]으로 묘사되어 농업계에서 논란을 일으키고 있다.
알레르기 유발성
과학자들, 지역사회 단체들, 그리고 [10]음식의 유전적 변이에 대해 우려하는 대중들의 말에 따르면, 새로운 알레르기가 부주의하게 도입될 수 있다고 한다.한 예로 메티오닌이 풍부한 콩을 생산한다.[15]메티오닌은 브라질 견과류에서 유래한 물질을 합성해 얻은 아미노산으로 [15][222]알레르겐일 가능성이 있다.브라질 견과류의 유전자가 [11][222]실험 중에 콩에 삽입되었다.브라질 견과류에 알레르기가 있는 사람도 유전자 변형 콩에 알레르기가 있을 수 있다는 사실이 밝혀져 실험을 중단했다.[10][223]원래 작물에 알레르기가 있는 사람들의 RAST나 혈청 같은 시험관내 어세이([10]in vitro assay)는 유전자의 알려진 소스를 가진 GM 상품의 알레르기 유발성을 증명하기 위해 적용될 수 있다.이는 브라질 견과류 2S 단백질을 발현한 GM 콩과 대구 [11]단백질 유전자를 발현한 GM 감자에서 확립됐다.이전에는 부모 세포에서 이용할 수 없었던 새로운 단백질의 발현과 합성은 한 유기체의 세포에서 다른 유기체의 핵으로의 유전자 이동에 의해 이루어졌다.트랜스제닉 음식을 섭취하면서 발생할 수 있는 알레르기의 잠재적 위험은 단백질 [19]형성의 아미노산 배열에서 비롯된다.그러나 현재 승인된 유전자 조작 식품에 대한 알레르기 반응 보고는 없으며, 실험 결과 유전자 조작 [10][19][224][225]콩과 유전자 조작 콩 이외의 콩 사이의 알레르기 유발성에 있어 측정 가능한 차이가 없는 것으로 나타났다.
저항 유전자
과학자들은 소비자들이 살충제 및 제초제에 강한 식물의 [11]이용과 관련된 건강 문제에도 주의를 기울여야 한다고 제안한다.'Bt' 유전자는 오늘날의 유전자 조작 작물에 곤충 내성을 일으킨다. 하지만 곤충 내성을 부여하는 다른 방법들이 연구 [18]중에 있다.BT 유전자는 보통 토양 박테리아인 바실루스 튜링기엔시스로부터 얻어지는데, 그것들은 곤충의 장에서 분해되는 단백질을 생성해 마비와 죽음을 [46]야기하는 델타 엔도톡신이라는 독소를 방출할 수 있다.BT독소를 발현하는 작물의 저항성과 목표외 효과, 제초제 사용에 의한 유전자 변형 내성 식물의 영향, 유전자 변형 작물로부터의 유전자 발현에 대한 우려는 모두 유전자 변형 [44]물질의 발현과 관련이 있다.
환경에 미치는 영향
생태학자들이 제기하는 또 다른 우려는 해충 내성 유전자가 야생 [10][46]동물로 확산될 수 있다는 것이다.이것은 종종 생물 다양성의 감소, 증식 저항성 잡초, 그리고 새로운 병충해와 [17][18]병원체의 형성과 관련된 유전자 오염의 한 예이다.
유전자 변형 유채씨로 인한 제초제 내성 꽃가루가 최대 3km까지 퍼질 수 있는 반면 유전자 변형 작물의 평균 유전자 확산은 2km이고 심지어 최대 [17]21km까지 퍼질 수 있다는 연구 결과가 나왔다.이러한 유전자 변형 작물의 높은 공격성은 물, 빛, 그리고 [222]영양분을 위해 전통적인 작물과 경쟁함으로써 특정한 재앙을 야기할 수 있다.주변 유기체와 꽃가루를 확산시키는 교배는 변형 저항성 [11]유전자의 도입으로 이어졌다.원치 않는 씨앗에 대한 유전자 오염을 증명하는 국제 데이터베이스는 현장 [17][222]실험의 확대와 상업적으로 실행 가능한 GM 작물의 재배로 인해 큰 문제가 되어왔다.해충 내성 잡초의 영향을 받아 한 해충의 수가 감소하더라도 [11]해충과 경쟁하는 다른 해충의 개체수가 증가할 수 있다.농작물 해충을 잡아먹기 때문에 그렇게 이름 붙여진 유익한 곤충들도 위험한 양의 [10]BT에 노출되었다.
기타 우려 사항
현지 적응 품종 대신 GM 작물의 도입은 농업 [16]시스템 전체에 장기적인 악영향을 미칠 수 있다.GM 기술에 대한 우려의 대부분은 생화학물질을 증가시키거나 감소시키는 유전자를 암호화하는 것과 관련이 있다.또는 새롭게 프로그램된 효소는 기질을 소비하여 [10]생성물을 형성하고 축적할 수 있다.또한 2차 생화학 경로 간의 대사물 전환으로 인해 대사 장애가 예측 불가능한 방법으로 교란되고 독소 [10][226]농도가 증가할 수 있다.독소 평가는 보통 동물에서 이루어지지만, 동물들 간의 차이는 동물의 유전자 변형 식품 섭취에 의한 유전자 변형 식품 효과에 따라 사람에게 미치는 영향을 평가하는 것을 어렵게 만든다.삽입형 돌연변이 유발은 일련의 결과와 관련되어 있다.예를 들어 돌연변이는 숙주 식물의 기존 유전자가 다시 쓰여질 때 발생하고 [10]내인성 유전자는 비활성화된다.
사회경제학의 관점에서, GM 작물은 보통 높은 수준의 외부 생산물, 예를 들어, 농약과 제초제에 의존하며, 이것은 GM 작물을 고투입 농업으로 제한한다.이는 GM 작물에 대한 광범위한 특허와 결합되어 로열티를 지불하지 않고 수확한 종자에 대한 농부들의 거래권을 제한했다.일부 반대론자들이 주장하는 GM 작물에 반대하는 다른 주장들은 GM 작물이 아닌 작물에 [16]대해 GM 작물을 격리하고 분배하는 데 드는 높은 비용에 바탕을 두고 있다.
소비자들은 유전자 변형 [43]식품에 대한 그들의 태도에 따라 분류될 수 있다.미국 소비자의 '태도적' 부문은 부분적으로 항상 관찰할 수 있는 것은 아닌 인지적 특성에 의해 설명될 수 있다.예를 들어, 개인의 특성과 가치는 생명공학에 대한 소비자의 인식을 형성하는 데 역할을 할 수 있다.동물의 DNA를 식물에 이식한다는 개념은 많은 [11]사람들을 불안하게 한다.연구에 따르면 GM 기술에 대한 소비자의 태도는 GM 기술에 [227]대한 그들의 지식과 긍정적인 상관관계가 있는 것으로 나타났습니다.유전자 변형 수용성의 증가는 대개 높은 교육 수준과 협력하는 반면, 인지된 위험의 높은 수준은 그 [43][227]반대와 관련이 있는 것으로 밝혀졌다.사람들은 부정적인 [227]영향을 예측하거나 피할 수 있는 충분한 지식이 없기 때문에 예측할 수 없는 위험에 대해 걱정하는 경향이 있다.
유전자 변형 식품에 대한 소비자 태도 변화의 또 다른 중요한 연결고리는 나이, 민족성, 거주지, 소비 [43][222]수준과 같은 사회경제적 및 인구통계학적 특징과의 상호작용과 밀접한 관련이 있는 것으로 나타났다.유전자 변형 식품에 대한 반대론에는 종교 및 문화 단체도 포함될 수 있는데, 유전자 변형 식품은 그들이 [11][222][228]자연산이라고 믿는 것에 반하는 것이기 때문이다.한편, 대부분의 유럽 국가, 특히 북유럽, 영국, 독일의 소비자들은 GM 식품의 혜택이 잠재적 위험을 초과하지 않는다고 믿고 있는 것으로 밝혀졌다.반면, 미국과 다른 유럽 국가들의 소비자들은 일반적으로 GM 식품의 위험이 그것이 [19]가져온 이익보다 훨씬 적을 수 있다는 견해를 갖고 있다.유전자 조작 식품은 보다 적절한 정책과 명확한 [222]규제에 의해 지지를 받을 것으로 예상된다.
「 」를 참조해 주세요.
- 유전자 조작 작물 목록
- 유전자 조작 작물
- 유전자 조작 식품 논란
- 유전자 조작 생물
- 캘리포니아 제안 37(2012) - 거부된 라벨링 이니셔티브
- 파밍(유전자학) – 의약품 생산을 위해 유전자 변형 포유동물 사용
- 유전자 변형 생물 방출 조절
- 2000년 StarLink 옥수수 리콜
레퍼런스
- ^ 2013년 10월 16일 영국 GM Science Review 패널에 의해 준비된 웨이백 머신에 보관된 GM Science Review 첫 보고서(2003년 7월).회장 David King 경, 영국 정부 최고 과학 고문, P 9
- ^ a b Jackson, DA; Symons, RH; Berg, P (1 October 1972). "Biochemical Method for Inserting New Genetic Information into DNA of Simian Virus 40: Circular SV40 DNA Molecules Containing Lambda Phage Genes and the Galactose Operon of Escherichia coli". Proceedings of the National Academy of Sciences of the United States of America. 69 (10): 2904–09. Bibcode:1972PNAS...69.2904J. doi:10.1073/pnas.69.10.2904. PMC 389671. PMID 4342968.
- ^ a b c d "FDA Approves 1st Genetically Engineered Product for Food". Los Angeles Times. 24 March 1990. Retrieved 1 May 2014.
- ^ a b c James, Clive (1996). "Global Review of the Field Testing and Commercialization of Transgenic Plants: 1986 to 1995" (PDF). The International Service for the Acquisition of Agri-biotech Applications. Retrieved 17 July 2010.
- ^ 족제비, 리사 H. 2009.음식 프라이.Amacom 퍼블리
- ^ a b Ye, Xudong; Al-Babili, Salim; Klöti, Andreas; Zhang, Jing; Lucca, Paola; Beyer, Peter; Potrykus, Ingo (2000-01-14). "Engineering the Provitamin A (β-Carotene) Biosynthetic Pathway into (Carotenoid-Free) Rice Endosperm". Science. 287 (5451): 303–05. Bibcode:2000Sci...287..303Y. doi:10.1126/science.287.5451.303. PMID 10634784.
- ^ "Consumer Q&A". FDA. 2009-03-06. Retrieved 2012-12-29.
- ^ a b Staff (December 26, 2012). "Draft Environmental Assessment and Preliminary Finding of No Significant Impact Concerning a Genetically Engineered Atlantic Salmon" (PDF). Federal Register. Retrieved January 2, 2013.
- ^ "Press Announcements - FDA takes several actions involving genetically engineered plants and animals for food". www.fda.gov. Office of the Commissioner of the U.S. Food and Drug Administration. Retrieved 2015-12-03.
- ^ a b c d e f g h i j k l m n o p q r s Bawa, A. S.; Anilakumar, K. R. (2012-12-19). "Genetically modified foods: safety, risks and public concerns—a review". Journal of Food Science and Technology. 50 (6): 1035–1046. doi:10.1007/s13197-012-0899-1. ISSN 0022-1155. PMC 3791249. PMID 24426015.
- ^ a b c d e f g h i j k l Healey, Justin. Organic and genetically modified food. ISBN 978-1-925339-11-6. OCLC 946314501.
- ^ a b c Mahgoub, Sala E. O. (2018). Testing and analysis of GMO-containing foods and feed. ISBN 978-1-315-17859-2. OCLC 1100467822.
- ^ a b c Dizon, Francis; Costa, Sarah; Rock, Cheryl; Harris, Amanda; Husk, Cierra; Mei, Jenny (2015-12-28). "Genetically Modified (GM) Foods and Ethical Eating". Journal of Food Science. 81 (2): R287–R291. doi:10.1111/1750-3841.13191. ISSN 0022-1147. PMID 26709962.
- ^ a b c d e Huang, Kunlun (2017). Safety Assessment of Genetically Modified Foods. doi:10.1007/978-981-10-3488-6. ISBN 978-981-10-3487-9.
- ^ a b c d e f g h i j k l m Kramkowska, Marta (2013). Benefits and risks associated with genetically modified food products. OCLC 922412861.
- ^ a b c d e f g Spreng, S; Viret, J (2005-03-18). "Plasmid maintenance systems suitable for GMO-based bacterial vaccines". Vaccine. 23 (17–18): 2060–2065. doi:10.1016/j.vaccine.2005.01.009. ISSN 0264-410X. PMID 15755571.
- ^ a b c d Walters, Reece (2010-10-04). Eco Crime and Genetically Modified Food. Routledge-Cavendish. doi:10.4324/9780203844151. ISBN 978-1-136-91813-1.
- ^ a b c Watson, Ronald R. (2016). Genetically modified organisms in food production, safety, regulation and public health. Elsevier Science. ISBN 978-0-12-802530-7. OCLC 1281814112.
- ^ a b c d e f Costa-Font, Montserrat; Gil, José M.; Traill, W. Bruce (April 2008). "Consumer acceptance, valuation of and attitudes towards genetically modified food: Review and implications for food policy". Food Policy. 33 (2): 99–111. doi:10.1016/j.foodpol.2007.07.002. ISSN 0306-9192.
- ^ a b Nicolia, Alessandro; Manzo, Alberto; Veronesi, Fabio; Rosellini, Daniele (2013). "An overview of the last 10 years of genetically engineered crop safety research" (PDF). Critical Reviews in Biotechnology. 34 (1): 77–88. doi:10.3109/07388551.2013.823595. PMID 24041244. S2CID 9836802.
We have reviewed the scientific literature on GE crop safety for the last 10 years that catches the scientific consensus matured since GE plants became widely cultivated worldwide, and we can conclude that the scientific research conducted so far has not detected any significant hazard directly connected with the use of GM crops.
The literature about Biodiversity and the GE food/feed consumption has sometimes resulted in animated debate regarding the suitability of the experimental designs, the choice of the statistical methods or the public accessibility of data. Such debate, even if positive and part of the natural process of review by the scientific community, has frequently been distorted by the media and often used politically and inappropriately in anti-GE crops campaigns. - ^ a b "State of Food and Agriculture 2003–2004. Agricultural Biotechnology: Meeting the Needs of the Poor. Health and environmental impacts of transgenic crops". Food and Agriculture Organization of the United Nations. Retrieved August 30, 2019.
Currently available transgenic crops and foods derived from them have been judged safe to eat and the methods used to test their safety have been deemed appropriate. These conclusions represent the consensus of the scientific evidence surveyed by the ICSU (2003) and they are consistent with the views of the World Health Organization (WHO, 2002). These foods have been assessed for increased risks to human health by several national regulatory authorities (inter alia, Argentina, Brazil, Canada, China, the United Kingdom and the United States) using their national food safety procedures (ICSU). To date no verifiable untoward toxic or nutritionally deleterious effects resulting from the consumption of foods derived from genetically modified crops have been discovered anywhere in the world (GM Science Review Panel). Many millions of people have consumed foods derived from GM plants - mainly maize, soybean and oilseed rape - without any observed adverse effects (ICSU).
- ^ a b Ronald, Pamela (May 1, 2011). "Plant Genetics, Sustainable Agriculture and Global Food Security". Genetics. 188 (1): 11–20. doi:10.1534/genetics.111.128553. PMC 3120150. PMID 21546547.
There is broad scientific consensus that genetically engineered crops currently on the market are safe to eat. After 14 years of cultivation and a cumulative total of 2 billion acres planted, no adverse health or environmental effects have resulted from commercialization of genetically engineered crops (Board on Agriculture and Natural Resources, Committee on Environmental Impacts Associated with Commercialization of Transgenic Plants, National Research Council and Division on Earth and Life Studies 2002). Both the U.S. National Research Council and the Joint Research Centre (the European Union's scientific and technical research laboratory and an integral part of the European Commission) have concluded that there is a comprehensive body of knowledge that adequately addresses the food safety issue of genetically engineered crops (Committee on Identifying and Assessing Unintended Effects of Genetically Engineered Foods on Human Health and National Research Council 2004; European Commission Joint Research Centre 2008). These and other recent reports conclude that the processes of genetic engineering and conventional breeding are no different in terms of unintended consequences to human health and the environment (European Commission Directorate-General for Research and Innovation 2010).
- ^ a b
단, 다음 항목도 참조하십시오.
Domingo, José L.; Bordonaba, Jordi Giné (2011). "A literature review on the safety assessment of genetically modified plants" (PDF). Environment International. 37 (4): 734–742. doi:10.1016/j.envint.2011.01.003. PMID 21296423.
In spite of this, the number of studies specifically focused on safety assessment of GM plants is still limited. However, it is important to remark that for the first time, a certain equilibrium in the number of research groups suggesting, on the basis of their studies, that a number of varieties of GM products (mainly maize and soybeans) are as safe and nutritious as the respective conventional non-GM plant, and those raising still serious concerns, was observed. Moreover, it is worth mentioning that most of the studies demonstrating that GM foods are as nutritional and safe as those obtained by conventional breeding, have been performed by biotechnology companies or associates, which are also responsible of commercializing these GM plants. Anyhow, this represents a notable advance in comparison with the lack of studies published in recent years in scientific journals by those companies.
Krimsky, Sheldon (2015). "An Illusory Consensus behind GMO Health Assessment". Science, Technology, & Human Values. 40 (6): 883–914. doi:10.1177/0162243915598381. S2CID 40855100.
I began this article with the testimonials from respected scientists that there is literally no scientific controversy over the health effects of GMOs. My investigation into the scientific literature tells another story.
대비:
Panchin, Alexander Y.; Tuzhikov, Alexander I. (January 14, 2016). "Published GMO studies find no evidence of harm when corrected for multiple comparisons". Critical Reviews in Biotechnology. 37 (2): 213–217. doi:10.3109/07388551.2015.1130684. ISSN 0738-8551. PMID 26767435. S2CID 11786594.
Here, we show that a number of articles some of which have strongly and negatively influenced the public opinion on GM crops and even provoked political actions, such as GMO embargo, share common flaws in the statistical evaluation of the data. Having accounted for these flaws, we conclude that the data presented in these articles does not provide any substantial evidence of GMO harm.
The presented articles suggesting possible harm of GMOs received high public attention. However, despite their claims, they actually weaken the evidence for the harm and lack of substantial equivalency of studied GMOs. We emphasize that with over 1783 published articles on GMOs over the last 10 years it is expected that some of them should have reported undesired differences between GMOs and conventional crops even if no such differences exist in reality.그리고.
Yang, Y.T.; Chen, B. (2016). "Governing GMOs in the USA: science, law and public health". Journal of the Science of Food and Agriculture. 96 (4): 1851–1855. doi:10.1002/jsfa.7523. PMID 26536836.It is therefore not surprising that efforts to require labeling and to ban GMOs have been a growing political issue in the USA (citing Domingo and Bordonaba, 2011). Overall, a broad scientific consensus holds that currently marketed GM food poses no greater risk than conventional food... Major national and international science and medical associations have stated that no adverse human health effects related to GMO food have been reported or substantiated in peer-reviewed literature to date.
Despite various concerns, today, the American Association for the Advancement of Science, the World Health Organization, and many independent international science organizations agree that GMOs are just as safe as other foods. Compared with conventional breeding techniques, genetic engineering is far more precise and, in most cases, less likely to create an unexpected outcome. - ^ a b c d Freedman, David H. (2013-08-20). "are engineered foods evil?". Scientific American. Springer Nature. 309 (3): 80–85. Bibcode:2013SciAm.309c..80F. doi:10.1038/scientificamerican0913-80. ISSN 0036-8733. JSTOR 26017991. PMID 24003560. S2CID 32994342.
- ^ a b "Statement by the AAAS Board of Directors On Labeling of Genetically Modified Foods" (PDF). American Association for the Advancement of Science. October 20, 2012. Retrieved August 30, 2019.
The EU, for example, has invested more than €300 million in research on the biosafety of GMOs. Its recent report states: "The main conclusion to be drawn from the efforts of more than 130 research projects, covering a period of more than 25 years of research and involving more than 500 independent research groups, is that biotechnology, and in particular GMOs, are not per se more risky than e.g. conventional plant breeding technologies." The World Health Organization, the American Medical Association, the U.S. National Academy of Sciences, the British Royal Society, and every other respected organization that has examined the evidence has come to the same conclusion: consuming foods containing ingredients derived from GM crops is no riskier than consuming the same foods containing ingredients from crop plants modified by conventional plant improvement techniques.
Pinholster, Ginger (October 25, 2012). "AAAS Board of Directors: Legally Mandating GM Food Labels Could "Mislead and Falsely Alarm Consumers"" (PDF). American Association for the Advancement of Science. Retrieved August 30, 2019. - ^ a b European Commission. Directorate-General for Research (2010). A decade of EU-funded GMO research (2001–2010) (PDF). Directorate-General for Research and Innovation. Biotechnologies, Agriculture, Food. European Commission, European Union. doi:10.2777/97784. ISBN 978-92-79-16344-9. Retrieved August 30, 2019.
- ^ a b "ISAAA Summary of AMA Report on Genetically Modified Crops and Foods". ISAAA. January 2001. Retrieved August 30, 2019.
A report issued by the scientific council of the American Medical Association (AMA) says that no long-term health effects have been detected from the use of transgenic crops and genetically modified foods, and that these foods are substantially equivalent to their conventional counterparts.
- ^ a b "Featured CSA Report: Genetically Modified Crops and Foods (I-00) Full Text". American Medical Association. Archived from the original on 10 June 2001.
Crops and foods produced using recombinant DNA techniques have been available for fewer than 10 years and no long-term effects have been detected to date. These foods are substantially equivalent to their conventional counterparts.
- ^ a b "Report 2 of the Council on Science and Public Health (A-12): Labeling of Bioengineered Foods" (PDF). American Medical Association. 2012. Archived from the original (PDF) on 2012-09-07. Retrieved August 30, 2019.
"Bioengineered foods have been consumed for close to 20 years, and during that time, no overt consequences on human health have been reported and/or substantiated in the peer-reviewed literature".
- ^ a b "Restrictions on Genetically Modified Organisms: United States. Public and Scholarly Opinion". Library of Congress. June 30, 2015. Retrieved August 30, 2019.
Several scientific organizations in the US have issued studies or statements regarding the safety of GMOs indicating that there is no evidence that GMOs present unique safety risks compared to conventionally bred products. These include the National Research Council, the American Association for the Advancement of Science, and the American Medical Association. Groups in the US opposed to GMOs include some environmental organizations, organic farming organizations, and consumer organizations. A substantial number of legal academics have criticized the US's approach to regulating GMOs.
- ^ a b National Academies Of Sciences, Engineering; Division on Earth Life Studies; Board on Agriculture Natural Resources; Committee on Genetically Engineered Crops: Past Experience Future Prospects (2016). Genetically Engineered Crops: Experiences and Prospects. The National Academies of Sciences, Engineering, and Medicine (US). p. 149. doi:10.17226/23395. ISBN 978-0-309-43738-7. PMID 28230933. Retrieved August 30, 2019.
Overall finding on purported adverse effects on human health of foods derived from GE crops: On the basis of detailed examination of comparisons of currently commercialized GE with non-GE foods in compositional analysis, acute and chronic animal toxicity tests, long-term data on health of livestock fed GE foods, and human epidemiological data, the committee found no differences that implicate a higher risk to human health from GE foods than from their non-GE counterparts.
- ^ a b "Frequently asked questions on genetically modified foods". World Health Organization. Retrieved August 30, 2019.
Different GM organisms include different genes inserted in different ways. This means that individual GM foods and their safety should be assessed on a case-by-case basis and that it is not possible to make general statements on the safety of all GM foods.
GM foods currently available on the international market have passed safety assessments and are not likely to present risks for human health. In addition, no effects on human health have been shown as a result of the consumption of such foods by the general population in the countries where they have been approved. Continuous application of safety assessments based on the Codex Alimentarius principles and, where appropriate, adequate post market monitoring, should form the basis for ensuring the safety of GM foods. - ^ a b Haslberger, Alexander G. (2003). "Codex guidelines for GM foods include the analysis of unintended effects". Nature Biotechnology. 21 (7): 739–741. doi:10.1038/nbt0703-739. PMID 12833088. S2CID 2533628.
These principles dictate a case-by-case premarket assessment that includes an evaluation of both direct and unintended effects.
- ^ a b 영국 의사협회를 포함한 일부 의료단체는 예방원칙에 기초한 추가 주의를 주장한다.
"Genetically modified foods and health: a second interim statement" (PDF). British Medical Association. March 2004. Retrieved August 30, 2019.In our view, the potential for GM foods to cause harmful health effects is very small and many of the concerns expressed apply with equal vigour to conventionally derived foods. However, safety concerns cannot, as yet, be dismissed completely on the basis of information currently available.
When seeking to optimise the balance between benefits and risks, it is prudent to err on the side of caution and, above all, learn from accumulating knowledge and experience. Any new technology such as genetic modification must be examined for possible benefits and risks to human health and the environment. As with all novel foods, safety assessments in relation to GM foods must be made on a case-by-case basis.
Members of the GM jury project were briefed on various aspects of genetic modification by a diverse group of acknowledged experts in the relevant subjects. The GM jury reached the conclusion that the sale of GM foods currently available should be halted and the moratorium on commercial growth of GM crops should be continued. These conclusions were based on the precautionary principle and lack of evidence of any benefit. The Jury expressed concern over the impact of GM crops on farming, the environment, food safety and other potential health effects.
The Royal Society review (2002) concluded that the risks to human health associated with the use of specific viral DNA sequences in GM plants are negligible, and while calling for caution in the introduction of potential allergens into food crops, stressed the absence of evidence that commercially available GM foods cause clinical allergic manifestations. The BMA shares the view that there is no robust evidence to prove that GM foods are unsafe but we endorse the call for further research and surveillance to provide convincing evidence of safety and benefit. - ^ a b Funk, Cary; Rainie, Lee (January 29, 2015). "Public and Scientists' Views on Science and Society". Pew Research Center. Retrieved August 30, 2019.
The largest differences between the public and the AAAS scientists are found in beliefs about the safety of eating genetically modified (GM) foods. Nearly nine-in-ten (88%) scientists say it is generally safe to eat GM foods compared with 37% of the general public, a difference of 51 percentage points.
- ^ a b Marris, Claire (2001). "Public views on GMOs: deconstructing the myths". EMBO Reports. 2 (7): 545–548. doi:10.1093/embo-reports/kve142. PMC 1083956. PMID 11463731.
- ^ a b Final Report of the PABE research project (December 2001). "Public Perceptions of Agricultural Biotechnologies in Europe". Commission of European Communities. Archived from the original on 2017-05-25. Retrieved August 30, 2019.
- ^ a b Scott, Sydney E.; Inbar, Yoel; Rozin, Paul (2016). "Evidence for Absolute Moral Opposition to Genetically Modified Food in the United States" (PDF). Perspectives on Psychological Science. 11 (3): 315–324. doi:10.1177/1745691615621275. PMID 27217243. S2CID 261060.
- ^ a b c "Restrictions on Genetically Modified Organisms". Library of Congress. June 9, 2015. Retrieved August 30, 2019.
- ^ a b c Bashshur, Ramona (February 2013). "FDA and Regulation of GMOs". American Bar Association. Archived from the original on June 21, 2018. Retrieved August 30, 2019.
- ^ a b c Sifferlin, Alexandra (October 3, 2015). "Over Half of E.U. Countries Are Opting Out of GMOs". Time. Retrieved August 30, 2019.
- ^ a b c d Lynch, Diahanna; Vogel, David (April 5, 2001). "The Regulation of GMOs in Europe and the United States: A Case-Study of Contemporary European Regulatory Politics". Council on Foreign Relations. Archived from the original on September 29, 2016. Retrieved August 30, 2019.
- ^ a b c d e Skogstad, Grace (2011-01-13). "Contested Accountability Claims and GMO Regulation in the European Union". JCMS: Journal of Common Market Studies. 49 (4): 895–915. doi:10.1111/j.1468-5965.2010.02166.x. ISSN 0021-9886. S2CID 154570139.
- ^ a b c d Thayyil, Naveen (2014). Biotechnology regulation and GMOs law, technology and public contestations in Europe. Edward Elgar Pub. Ltd. ISBN 978-1-84844-564-2. OCLC 891882521.
- ^ a b c d e f g Weimer, Maria (2015-05-24). "Risk Regulation and Deliberation in EU Administrative Governance-GMO Regulation and Its Reform". European Law Journal. 21 (5): 622–640. doi:10.1111/eulj.12140. ISSN 1351-5993. S2CID 154666745.
- ^ a b c d e f Wickson, Fern (December 2014). "Environmental protection goals, policy & publics in the European regulation of GMOs". Ecological Economics. 108: 269–273. doi:10.1016/j.ecolecon.2014.09.025. ISSN 0921-8009.
- ^ Cowan, Tadlock (18 Jun 2011). "Agricultural Biotechnology: Background and Recent Issues" (PDF). Congressional Research Service (Library of Congress). pp. 33–38. Retrieved 27 September 2015.
- ^ a b c World Health Organization. "Frequently asked questions on genetically modified foods". Retrieved 29 March 2016.
- ^ "Genetically engineered foods". University of Maryland Medical Center. Archived from the original on 2016-02-14. Retrieved 14 Feb 2016.
- ^ "Glossary of Agricultural Biotechnology Terms". United States Department of Agriculture. 27 February 2013. Retrieved 29 September 2015.
- ^ "Questions & Answers on Food from Genetically Engineered Plants". US Food and Drug Administration. 22 Jun 2015. Archived from the original on June 23, 2015. Retrieved 29 September 2015.
- ^ a b "Organisms obtained by mutagenesis are GMOs and are, in principle, subject to the obligations laid down by the GMO Directive" (PDF). curia.europa.eu. Retrieved 2019-01-05.
- ^ Knutson, Jonathan (May 28, 2018). "A sad day for our society when salt is labeled non-GMO". Agweek. Retrieved 2021-07-09.
- ^ "Non GMO salt? Water? Food companies exploit GMO free labels, misleading customers, promoting misinformation". Genetic Literacy Project. 2015-08-24. Retrieved 2021-07-09.
- ^ a b Daniel Zohary; Maria Hopf; Ehud Weiss (2012). Domestication of Plants in the Old World: The Origin and Spread of Plants in the Old World. Oxford University Press.
- ^ Clive Root (2007). Domestication. Greenwood Publishing Groups.
- ^ a b Staff, National Centre for Biotechnology Education (2006). "Chymosin". Archived from the original on May 22, 2016.
- ^ Campbell-Platt, Geoffrey (26 August 2011). Food Science and Technology. Ames, Iowa: John Wiley & Sons. ISBN 978-1-4443-5782-0.
- ^ Bruening, G.; Lyons, J. M. (2000). "The case of the FLAVR SAVR tomato". California Agriculture. 54 (4): 6–7. doi:10.3733/ca.v054n04p6.
- ^ James, Clive (2010). "Global Review of the Field Testing and Commercialization of Transgenic Plants: 1986 to 1995: The First Decade of Crop Biotechnology". ISAAA Briefs No. 1: 31.
- ^ 유전자 변형 감자 Ok'd for Crops Lawrence Journal-World - 1995년 5월 6일
- ^ 상용화된 생명공학/GM 작물의 글로벌 현황: 2011 ISAAA 개요 ISAAA 개요 43-2011.2012년 10월 14일 취득
- ^ James, C (2011). "ISAAA Brief 43, Global Status of Commercialized Biotech/GM Crops: 2011". ISAAA Briefs. Ithaca, New York: International Service for the Acquisition of Agri-biotech Applications (ISAAA). Retrieved 2012-06-02.
- ^ a b c "Adoption of Genetically Engineered Crops in the U.S." Economic Research Service, USDA. Retrieved 26 August 2015.
- ^ "Aquabounty Cleared to Sell Salmon in the USA for Commercial Purposes". FDA. 2019-06-19.
- ^ Bodnar, Anastasia (October 2010). "Risk Assessment and Mitigation of AquAdvantage Salmon" (PDF). ISB News Report. Archived from the original (PDF) on 2021-03-08. Retrieved 2016-01-22.
- ^ Culpepper, Stanley A; et al. (2006). "Glyphosate-resistant Palmer amaranth (Amaranthus palmeri) confirmed in Georgia". Weed Science. 54 (4): 620–26. doi:10.1614/ws-06-001r.1. S2CID 56236569.
- ^ Gallant, Andre. "Pigweed in the Cotton: A superweed invades Georgia". Modern Farmer.
- ^ Webster, TM; Grey, TL (2015). "Glyphosate-Resistant Palmer Amaranth (Amaranthus palmeri) Morphology, Growth, and Seed Production in Georgia". Weed Science. 63 (1): 264–72. doi:10.1614/ws-d-14-00051.1. S2CID 86300650.
- ^ Boonstra, Evert; de Kleijn, Roy; Colzato, Lorenza S.; Alkemade, Anneke; Forstmann, Birte U.; Nieuwenhuis, Sander (6 October 2015). "Neurotransmitters as food supplements: the effects of GABA on brain and behavior". Frontiers in Psychology. 6: 1520. doi:10.3389/fpsyg.2015.01520. PMC 4594160. PMID 26500584.
- ^ "Tomato In Japan Is First CRISPR-Edited Food In The World To Go On Sale". IFLScience. Retrieved 18 October 2021.
- ^ Wang, Tian; Zhang, Hongyan; Zhu, Hongliang (15 June 2019). "CRISPR technology is revolutionizing the improvement of tomato and other fruit crops". Horticulture Research. 6 (1): 77. doi:10.1038/s41438-019-0159-x. ISSN 2052-7276. PMC 6570646. PMID 31240102.
- ^ "Japan embraces CRISPR-edited fish". Nature Biotechnology. 40 (1): 10. 1 January 2022. doi:10.1038/s41587-021-01197-8. PMID 34969964. S2CID 245593283. Retrieved 17 January 2022.
- ^ "Startup hopes genome-edited pufferfish will be a hit in 2022". The Japan Times. 5 January 2022. Retrieved 17 January 2022.
- ^ "Gene-edited sea bream set for sale in Japan". thefishsite.com.
- ^ Nicholl DS (2008-05-29). An Introduction to Genetic Engineering. Cambridge University Press. p. 34. ISBN 9781139471787.
- ^ Liang J, Luo Y, Zhao H (2011). "Synthetic biology: putting synthesis into biology". Wiley Interdisciplinary Reviews: Systems Biology and Medicine. 3 (1): 7–20. doi:10.1002/wsbm.104. PMC 3057768. PMID 21064036.
- ^ Berg P, Mertz JE (January 2010). "Personal reflections on the origins and emergence of recombinant DNA technology". Genetics. 184 (1): 9–17. doi:10.1534/genetics.109.112144. PMC 2815933. PMID 20061565.
- ^ Chen I, Dubnau D (March 2004). "DNA uptake during bacterial transformation". Nature Reviews. Microbiology. 2 (3): 241–9. doi:10.1038/nrmicro844. PMID 15083159. S2CID 205499369.
- ^ a b National Research Council (US) Committee on Identifying and Assessing Unintended Effects of Genetically Engineered Foods on Human Health (2004-01-01). Methods and Mechanisms for Genetic Manipulation of Plants, Animals, and Microorganisms. National Academies Press (US).
- ^ Gelvin SB (March 2003). "Agrobacterium-mediated plant transformation: the biology behind the "gene-jockeying" tool". Microbiology and Molecular Biology Reviews. 67 (1): 16–37, table of contents. doi:10.1128/MMBR.67.1.16-37.2003. PMC 150518. PMID 12626681.
- ^ Head G, Hull RH, Tzotzos GT (2009). Genetically Modified Plants: Assessing Safety and Managing Risk. London: Academic Pr. p. 244. ISBN 978-0-12-374106-6.
- ^ Tuomela M, Stanescu I, Krohn K (October 2005). "Validation overview of bio-analytical methods". Gene Therapy. 12 Suppl 1 (S1): S131-8. doi:10.1038/sj.gt.3302627. PMID 16231045.
- ^ Narayanaswamy S (1994). Plant Cell and Tissue Culture. Tata McGraw-Hill Education. pp. vi. ISBN 9780074602775.
- ^ Setlow JK (2002-10-31). Genetic Engineering: Principles and Methods. Springer Science & Business Media. p. 109. ISBN 9780306472800.
- ^ Grizot S, Smith J, Daboussi F, Prieto J, Redondo P, Merino N, Villate M, Thomas S, Lemaire L, Montoya G, Blanco FJ, Pâques F, Duchateau P (September 2009). "Efficient targeting of a SCID gene by an engineered single-chain homing endonuclease". Nucleic Acids Research. 37 (16): 5405–19. doi:10.1093/nar/gkp548. PMC 2760784. PMID 19584299.
- ^ Gao H, Smith J, Yang M, Jones S, Djukanovic V, Nicholson MG, West A, Bidney D, Falco SC, Jantz D, Lyznik LA (January 2010). "Heritable targeted mutagenesis in maize using a designed endonuclease". The Plant Journal. 61 (1): 176–87. doi:10.1111/j.1365-313X.2009.04041.x. PMID 19811621.
- ^ Townsend JA, Wright DA, Winfrey RJ, Fu F, Maeder ML, Joung JK, Voytas DF (May 2009). "High-frequency modification of plant genes using engineered zinc-finger nucleases". Nature. 459 (7245): 442–5. Bibcode:2009Natur.459..442T. doi:10.1038/nature07845. PMC 2743854. PMID 19404258.
- ^ Shukla VK, Doyon Y, Miller JC, DeKelver RC, Moehle EA, Worden SE, Mitchell JC, Arnold NL, Gopalan S, Meng X, Choi VM, Rock JM, Wu YY, Katibah GE, Zhifang G, McCaskill D, Simpson MA, Blakeslee B, Greenwalt SA, Butler HJ, Hinkley SJ, Zhang L, Rebar EJ, Gregory PD, Urnov FD (May 2009). "Precise genome modification in the crop species Zea mays using zinc-finger nucleases". Nature. 459 (7245): 437–41. Bibcode:2009Natur.459..437S. doi:10.1038/nature07992. PMID 19404259. S2CID 4323298.
- ^ Christian M, Cermak T, Doyle EL, Schmidt C, Zhang F, Hummel A, Bogdanove AJ, Voytas DF (October 2010). "Targeting DNA double-strand breaks with TAL effector nucleases". Genetics. 186 (2): 757–61. doi:10.1534/genetics.110.120717. PMC 2942870. PMID 20660643.
- ^ Li T, Huang S, Jiang WZ, Wright D, Spalding MH, Weeks DP, Yang B (January 2011). "TAL nucleases (TALNs): hybrid proteins composed of TAL effectors and FokI DNA-cleavage domain". Nucleic Acids Research. 39 (1): 359–72. doi:10.1093/nar/gkq704. PMC 3017587. PMID 20699274.
- ^ Esvelt KM, Wang HH (2013). "Genome-scale engineering for systems and synthetic biology". Molecular Systems Biology. 9: 641. doi:10.1038/msb.2012.66. PMC 3564264. PMID 23340847.
- ^ Tan WS, Carlson DF, Walton MW, Fahrenkrug SC, Hackett PB (2012). "Precision editing of large animal genomes". Advances in Genetics Volume 80. Advances in Genetics. Vol. 80. pp. 37–97. doi:10.1016/B978-0-12-404742-6.00002-8. ISBN 9780124047426. PMC 3683964. PMID 23084873.
- ^ a b Malzahn A, Lowder L, Qi Y (2017-04-24). "Plant genome editing with TALEN and CRISPR". Cell & Bioscience. 7: 21. doi:10.1186/s13578-017-0148-4. PMC 5404292. PMID 28451378.
- ^ a b c Qaim M (2016-04-29). "Introduction". Genetically Modified Crops and Agricultural Development. Springer. pp. 1–10. ISBN 9781137405722.
- ^ Darmency H (August 2013). "Pleiotropic effects of herbicide-resistance genes on crop yield: a review". Pest Management Science. 69 (8): 897–904. doi:10.1002/ps.3522. PMID 23457026.
- ^ Fleischer SJ, Hutchison WD, Naranjo SE (2014). "Sustainable Management of Insect-Resistant Crops". Plant Biotechnology. pp. 115–127. doi:10.1007/978-3-319-06892-3_10. ISBN 978-3-319-06891-6.
- ^ "SGK321". GM Approval Database. ISAAA.org. Retrieved 2017-04-27.
- ^ Qiu J (October 2008). "Is China ready for GM rice?". Nature. 455 (7215): 850–2. doi:10.1038/455850a. PMID 18923484.
- ^ a b "Global Status of Commercialized Biotech/GM Crops: 2014 - ISAAA Brief 49-2014". ISAAA.org. Retrieved 2016-09-15.
- ^ a b ISAAA 2013 연차보고서 이그제큐티브 요약, 상용화 바이오/GM 작물의 글로벌 현황: 2013 ISAAA Brief 46-2013, 2014년 8월 6일 취득
- ^ Hakim, Danny (2016-10-29). "Doubts About the Promised Bounty of Genetically Modified Crops". The New York Times. ISSN 0362-4331. Retrieved 2017-05-05.
- ^ Areal FJ, Riesgo L, Rodríguez-Cerezo E (February 2013). "Economic and agronomic impact of commercialized GM crops: a meta-analysis". The Journal of Agricultural Science. 151 (1): 7–33. doi:10.1017/S0021859612000111. ISSN 0021-8596. S2CID 85891950.
- ^ Finger R, El Benni N, Kaphengst T, Evans C, Herbert S, Lehmann B, Morse S, Stupak N (2011-05-10). "A Meta Analysis on Farm-Level Costs and Benefits of GM Crops". Sustainability. 3 (5): 743–62. doi:10.3390/su3050743.
- ^ Klümper W, Qaim M (2014-11-03). "A meta-analysis of the impacts of genetically modified crops". PLOS ONE. 9 (11): e111629. Bibcode:2014PLoSO...9k1629K. doi:10.1371/journal.pone.0111629. PMC 4218791. PMID 25365303.
- ^ Doucleff, Michaeleen (2015-05-05). "Natural GMO? Sweet Potato Genetically Modified 8,000 Years Ago". NPR. Retrieved 2022-01-15.
- ^ Lebot, Vincent (2020). Tropical Root and Tuber Crops : Cassava, Sweet Potato, Yams And Aroids. Wallingford, Oxfordshire, UK Boston, MA, USA: CABI (Centre for Agriculture and Bioscience International). p. 541. ISBN 978-1-78924-336-9. OCLC 1110672215.
- ^ Soucy, Shannon M.; Huang, Jinling; Gogarten, Johann Peter (2015-07-17). "Horizontal gene transfer: building the web of life". Nature Reviews Genetics. Nature Portfolio. 16 (8): 472–482. doi:10.1038/nrg3962. ISSN 1471-0056. PMID 26184597. S2CID 6794788.
- ^ Andersen, Martin Marchman; Landes, Xavier; Xiang, Wen; Anyshchenko, Artem; Falhof, Janus; Østerberg, Jeppe Thulin; Olsen, Lene Irene; Edenbrandt, Anna Kristina; Vedel, Suzanne Elizabeth; Thorsen, Bo Jellesmark; Sandøe, Peter; Gamborg, Christian; Kappel, Klemens; Palmgren, Michael G. (2015). "Feasibility of new breeding techniques for organic farming". Trends in Plant Science. Cell Press. 20 (7): 426–434. doi:10.1016/j.tplants.2015.04.011. ISSN 1360-1385. PMID 26027462.
- ^ a b Gonsalves, D. (2004). "Transgenic papaya in Hawaii and beyond". AgBioForum. 7 (1&2): 36–40. Archived from the original on 2010-07-06. Retrieved 2013-01-20.
- ^ "The Rainbow Papaya Story". Hawaii Papaya Industry Association. Archived from the original on 2015-01-07. Retrieved April 17, 2015.
- ^ a b Ronald, Pamela; McWilliams, James (May 14, 2010). "Genetically Engineered Distortions". The New York Times. Retrieved July 26, 2010.
- ^ Li, Y; et al. (April 2014). "Biosafety management and commercial use of genetically modified crops in China". Plant Cell Reports. 33 (4): 565–73. doi:10.1007/s00299-014-1567-x. PMID 24493253. S2CID 16570688.
- ^ Loo, Jacky Fong-Chuen; But, Grace Wing-Chiu; Kwok, Ho-Chin; Lau, Pui-Man; Kong, Siu-Kai; Ho, Ho-Pui; Shaw, Pang-Chui (2019). "A rapid sample-to-answer analytical detection of genetically modified papaya using loop-mediated isothermal amplification assay on lab-on-a-disc for field use". Food Chemistry. 274: 822–830. doi:10.1016/j.foodchem.2018.09.049. ISSN 0308-8146. PMID 30373016. S2CID 53115420.
- ^ "Genetically Modified Organisms (Control of Release) Ordinance Cap. 607: Review of the Exemption of Genetically Modified Papayas in Hong Kong" (PDF).
- ^ Bawa, A. S.; Anilakumar, K. R. (2016-12-04). "Genetically modified foods: safety, risks and public concerns – a review". Journal of Food Science and Technology. 50 (6): 1035–46. doi:10.1007/s13197-012-0899-1. ISSN 0022-1155. PMC 3791249. PMID 24426015.
- ^ "Business BASF applies for approval for another biotech potato". Research in Germany. November 17, 2011. Archived from the original on June 2, 2013. Retrieved October 18, 2012.
- ^ Burger, Ludwig (October 31, 2011). "BASF applies for EU approval for Fortuna GM potato". Reuters. Frankfurt. Retrieved December 29, 2011.
- ^ Turley, Andrew (February 7, 2013). "BASF drops GM potato projects". Royal Society of Chemistry News.
- ^ "The History and Future of GM Potatoes". Potatopro.com. 2010-03-10. Retrieved 2012-12-29.
- ^ Pollack, Andrew (November 7, 2014). "U.S.D.A. Approves Modified Potato. Next Up: French Fry Fans". The New York Times.
- ^ "Availability of Petition for Determination of Nonregulated Status of Potato Genetically Engineered for Low Acrylamide Potential and Reduced Black Spot Bruise". Federal Register. May 3, 2013.
- ^ Johnson, Stanley R. (February 2008). "Quantification of the Impacts on US Agriculture of Biotechnology-Derived Crops Planted in 2006" (PDF). Washington, D.C.: National Center for Food and Agricultural Policy. Retrieved August 12, 2010.
- ^ "GMO Database: Zucchini (courgette)". GMO Compass. November 7, 2007. Archived from the original on February 25, 2017. Retrieved February 28, 2015.
- ^ Perkowski, Mateisz (April 16, 2013). "Del Monte Gets Approval to Import GMO Pineapple". Food Democracy Now.
- ^ Bradley, Diana (27 October 2020). "Inside the sweet and successful launch of the world's first pink pineapple". PRWeek. Retrieved 10 July 2021.
- ^ Pollack, A. (February 13, 2015). "Gene-Altered Apples Get U.S. Approval". The New York Times.
- ^ Tennille, Tracy (February 13, 2015). "First Genetically Modified Apple Approved for Sale in U.S." The Wall Street Journal. Retrieved February 13, 2015.
- ^ "How'd we 'make' a nonbrowning apple?". Okanagan Specialty Fruits. 2011-12-07. Retrieved September 19, 2016.
- ^ "Know Before You Grow". National Corn Growers Association. Archived from the original on October 23, 2011.
- ^ "Acreage NASS" (PDF). National Agricultural Statistics Board annual report. June 2010. Retrieved July 23, 2010.
- ^ "Corn-Based Food Production in South Dakota: A Preliminary Feasibility Study" (PDF). South Dakota State University, College of Agriculture and Biological Sciences, Agricultural Experiment Station. June 2004. Archived from the original (PDF) on 2016-03-03. Retrieved 2013-01-19.
- ^ Padgette SR, et al(1995) 글리포세이트 내성 콩 라인의 개발, 식별 및 특성화.크롭사이 35:1451-1461.
- ^ Ye X, Al-Babili S, Klöti A, Zhang J, Lucca P, Beyer P, Potrykus I (January 2000). "Engineering the provitamin A (beta-carotene) biosynthetic pathway into (carotenoid-free) rice endosperm". Science. 287 (5451): 303–5. Bibcode:2000Sci...287..303Y. doi:10.1126/science.287.5451.303. PMID 10634784.
- ^ Frist B (21 November 2006). "'Green revolution' hero". Washington Times.
One existing crop, genetically engineered "golden rice" that produces vitamin A, already holds enormous promise for reducing blindness and dwarfism that result from a vitamin-A deficient diet.
- ^ Black RE, Allen LH, Bhutta ZA, Caulfield LE, de Onis M, Ezzati M, Mathers C, Rivera J (January 2008). "Maternal and child undernutrition: global and regional exposures and health consequences". Lancet. 371 (9608): 243–60. doi:10.1016/S0140-6736(07)61690-0. PMID 18207566. S2CID 3910132.
- ^ Humphrey JH, West KP, Sommer A (1992). "Vitamin A deficiency and attributable mortality among under-5-year-olds". Bulletin of the World Health Organization. 70 (2): 225–32. PMC 2393289. PMID 1600583.
- ^ Paine JA, Shipton CA, Chaggar S, Howells RM, Kennedy MJ, Vernon G, Wright SY, Hinchliffe E, Adams JL, Silverstone AL, Drake R (April 2005). "Improving the nutritional value of Golden Rice through increased pro-vitamin A content". Nature Biotechnology. 23 (4): 482–7. doi:10.1038/nbt1082. PMID 15793573. S2CID 632005.
- ^ "US FDA approves GMO Golden Rice as safe to eat". Genetic Literacy Project. 2018-05-29. Retrieved 2018-05-30.
- ^ USDA 경제조사국 직원입니다.최종 갱신일 : 2013년 1월 24일 밀 배경
- ^ "Petitions for Determination of Nonregulated Status". USDA. Retrieved 9 March 2018.
- ^ Regalado, Antonio. "These are not your father's GMOs". MIT Technology Review. Retrieved 9 March 2018.
- ^ Waltz, Emily (2016). "Gene-edited CRISPR mushroom escapes US regulation". Nature. Nature Portfolio. 532 (7599): 293. Bibcode:2016Natur.532..293W. doi:10.1038/nature.2016.19754. PMID 27111611.
- ^ Harper, G.S.; Brownlee, A.; Hall, T.E.; Seymour, R.; Lyons, R.; Ledwith, P. (2003). "Global progress toward transgenic food animals: A survey of publicly available information" (PDF). Food Standards Australia and New Zealand. Retrieved August 27, 2015.
- ^ Rick MacInnes-Rae, Rick (November 27, 2013). "GMO salmon firm clears one hurdle but still waits for key OKs AquaBounty began seeking American approval in 1995". CBC News.
- ^ Pollack, Andrew (May 21, 2012). "An Entrepreneur Bankrolls a Genetically Engineered Salmon". The New York Times. Retrieved September 3, 2012.
- ^ Naik, Gautam (September 21, 2010). "Gene-Altered Fish Closer to Approval". The Wall Street Journal.
- ^ "FDA takes several actions involving genetically engineered plants and animals for food" (Press release). Office of the Commissioner of the U.S. Food and Drug Administration. Retrieved 2015-12-03.
- ^ Coffey, Aidan; Ross, R. Paul (2002). "Bacteriophage-resistance systems in dairy starter strains: molecular analysis to application". Antonie van Leeuwenhoek. Springer. 82 (1/4): 303–321. doi:10.1023/a:1020639717181. ISSN 0003-6072. PMID 12369198. S2CID 7217985.
- ^ O'Sullivan, Lisa; Bolton, Declan; McAuliffe, Olivia; Coffey, Aidan (2019-03-25). "Bacteriophages in Food Applications: From Foe to Friend". Annual Review of Food Science and Technology. Annual Reviews. 10 (1): 151–172. doi:10.1146/annurev-food-032818-121747. ISSN 1941-1413. PMID 30633564. S2CID 58620015.
- ^ a b "Lecithin". October 2015. Archived from the original on 1 November 2015. Retrieved 18 October 2015.
- ^ a b "Select Committee on GRAS Substances (SCOGS) Opinion: Lecithin". Food and Drug Administration. August 10, 2015. Retrieved 18 October 2015.
- ^ "Corn Oil, 5th Edition" (PDF). Corn Refiners Association. 2006.
- ^ a b c Jaffe, Greg (Director of Biotechnology at the Center for Science in the Public Interest) (February 7, 2013). "What You Need to Know About Genetically Engineered Food". Atlantic.
- ^ "Regulation (EC) 50/2000". Eur-lex.europa.eu.
- ^ Marx, Gertruida M. (December 2010). "Dissertation submitted in fulfilment of requirements for the degree Doctor of Philosophy in the Faculty of Health Sciences" (PDF). Monitoring of Genetically Modified Food Products in South Africa]. South Africa: University of the Free State. Archived from the original (PDF) on 2015-01-09.
- ^ Davison, John; Bertheau, Yves Bertheau (2007). "EU regulations on the traceability and detection of GMOs: difficulties in interpretation, implementation and compliance". CAB Reviews: Perspectives in Agriculture, Veterinary Science, Nutrition and Natural Resources. 2 (77). doi:10.1079/pavsnnr20072077.
- ^ "ISAAA Brief 43-2011. Executive Summary: Global Status of Commercialized Biotech/GM Crops: 2011". Isaaa.org. Retrieved 2012-12-29.
- ^ "Sugar beet". Archived from the original on 2016-03-01. Retrieved 2016-02-19.
- ^ Food and Agriculture Organization of the United Nations (2009). Sugar Beet: White Sugar (PDF). p. 9. Archived from the original (PDF) on 2015-09-05. Retrieved 2012-09-17.
- ^ Klein, Joachim; Altenbuchner, Josef; Mattes, Ralf (1998-02-26). "Nucleic acid and protein elimination during the sugar manufacturing process of conventional and transgenic sugar beets". Journal of Biotechnology. 60 (3): 145–53. doi:10.1016/S0168-1656(98)00006-6. PMID 9608751.
- ^ "Soyatech.com". Soyatech.com. Archived from the original on 2012-10-25. Retrieved 2012-12-29.
- ^ "Poster of corn products" (PDF). Archived from the original (PDF) on 2020-02-14. Retrieved 2012-12-29.
- ^ "Food Fats and Oils" (PDF). Institute of Shortening and Edible Oils. 2006. Archived from the original (PDF) on 2007-02-14. Retrieved 2011-11-19.
- ^ "Twenty Facts about Cottonseed Oil". National Cottonseed Producers Association. Archived from the original on October 17, 2015.
- ^ Simon, Michelle (August 24, 2011). "ConAgra Sued Over GMO '100% Natural' Cooking Oils". Food Safety News.
- ^ "ingredients of margarine". Imace.org. Archived from the original on February 25, 2012. Retrieved 2012-12-29.
- ^ "USDA Protein(g) in Fats and Oils". Archived from the original on 2018-10-05. Retrieved 2015-05-31.
- ^ Crevel, R.W.R.; Kerkhoff, M.A.T.; Koning, M.M.G (2000). "Allergenicity of refined vegetable oils". Food and Chemical Toxicology. 38 (4): 385–93. doi:10.1016/S0278-6915(99)00158-1. PMID 10722892.
- ^ "What is Canola Oil?". CanolaInfo. Retrieved 2012-12-29.
- ^ David Bennett, 사우스웨스트 팜 프레스, 2003년 2월 5일 세계 콩 소비 촉진 2006-06-05년 Wayback Machine 아카이브
- ^ "Soybean". Encyclopædia Britannica Online. Retrieved February 18, 2012.
- ^ "2012 World of Corn, National Corn Growers Association" (PDF). Archived from the original (PDF) on 2020-02-07. Retrieved 2012-12-29.
- ^ 직원, GMO 나침반입니다2006년 12월 7일유전자 공학: 2017년 1월 12일 웨이백 머신에서 보관된 EU 가축 사료 공급
- ^ Snell, C; Bernheim, A; Berge, JB; Kuntz, M; Pascal, G; Paris, A; Ricroch, AE (2012). "Assessment of the health impact of GM plant diets in long-term and multigenerational animal feeding trials: A literature review". Food and Chemical Toxicology. 50 (3–4): 1134–48. doi:10.1016/j.fct.2011.11.048. PMID 22155268.
- ^ Fellows, P.J. (2009). Food Processing Technology: Principles and Practice. Woodhead Publishing Limited. p. 236. ISBN 978-1845692162.
- ^ Gerdes, Louise. Genetic Engineering Opposing Viewpoints (2004 ed.). Greenhaven Press. p. 132.
- ^ Taylor, Steve; Hefle, Susan (May 2001). "Will genetically modified foods be allergenic?". Journal of Allergy and Clinical Immunology. 107 (5): 765–771. doi:10.1067/mai.2001.114241. PMID 11344340.
- ^ Emtage, JS; Angal, S; Doel, MT; Harris, TJ; Jenkins, B; Lilley, G; Lowe, PA (1983). "Synthesis of calf prochymosin (prorennin) in Escherichia coli". Proceedings of the National Academy of Sciences of the United States of America. 80 (12): 3671–75. Bibcode:1983PNAS...80.3671E. doi:10.1073/pnas.80.12.3671. PMC 394112. PMID 6304731.
- ^ Harris TJ, Lowe PA, Lyons A, Thomas PG, Eaton MA, Millican TA, Patel TP, Bose CC, Carey NH, Doel MT (April 1982). "Molecular cloning and nucleotide sequence of cDNA coding for calf preprochymosin". Nucleic Acids Research. 10 (7): 2177–87. doi:10.1093/nar/10.7.2177. PMC 320601. PMID 6283469.
- ^ a b c "Chymosin". GMO Compass. Archived from the original on 2015-03-26. Retrieved 2016-11-03.
- ^ Law, Barry A. (2010). Technology of Cheesemaking. UK: Wiley-Blackwell. pp. 100–101. ISBN 978-1-4051-8298-0.
- ^ "Food Biotechnology in the United States: Science, Regulation, and Issues". U.S. Department of State. Retrieved 2006-08-14.
- ^ Johnson, M.E.; Lucey, J.A. (2006). "Major Technological Advances and Trends in Cheese". Journal of Dairy Science. 89 (4): 1174–78. doi:10.3168/jds.S0022-0302(06)72186-5. PMID 16537950.
- ^ Baumana, Dale E.; Collier, Robert J. (September 15, 2010). "Use of Bovine Somatotropin in Dairy Production" (PDF). Archived from the original (PDF) on May 13, 2013. Retrieved February 23, 2013.
- ^ Staff (2011-02-18). Last Medical Review. American Cancer Society.
{{cite web}}: 누락되었거나 비어 있습니다(도움말).누락 또는 비어 있음(도움말)[full citation needed] - ^ "Recombinant Bovine Growth Hormone". www.cancer.org.
- ^ Brennand, Charlotte P. "Bovine Somatotropin in Milk" (PDF). Retrieved 2011-03-06.
- ^ Cima, Greg (November 18, 2010). "Appellate court gives mixed ruling on Ohio rBST labeling rules". JAVMA News.
- ^ a b leafcom. "International Dairy Foods Ass'n v. Boggs – Argued: June 10, 2010". Leagle.com.
- ^ "Genetically modified foods" (PDF). Public Health Association of Australia. 2007. Archived from the original (PDF) on January 20, 2014.
- ^ a b c "CAPE's Position Statement on GMOs". Canadian Association of Physicians for the Environment. November 11, 2013. Archived from the original on March 26, 2014. Retrieved March 26, 2014.
- ^ a b "IDEA Position on Genetically Modified Foods". Irish Doctors' Environmental Association. Archived from the original on 2014-03-26. Retrieved 2014-03-25.
- ^ "American Academy of Environmental Medicine Calls for Immediate Moratorium on Genetically Modified Foods, position paper". American Academy of Environmental Medicine. Archived from the original on 1 March 2019. Retrieved 3 August 2017.
- ^ "Press Advisory". American Academy of Environmental Medicine. Archived from the original on 28 April 2015. Retrieved 18 October 2015.
- ^ "Heterogeneity in consumer preferences for organic and genetically modified food products in Ghana" (PDF). African Journal of Agricultural and Resource Economics.
- ^ "Can GMOs Be Used in Organic Products? Agricultural Marketing Service". www.ams.usda.gov. Retrieved 28 October 2021.
- ^ Ashaolu, Tolulope J.; Ashaolu, Joseph O. (1 December 2020). "Perspectives on the trends, challenges and benefits of green, smart and organic (GSO) foods". International Journal of Gastronomy and Food Science. 22: 100273. doi:10.1016/j.ijgfs.2020.100273. ISSN 1878-450X. PMC 7574864. PMID 33101552.
- ^ Emily Marden, 위험과 규제: 유전자 조작 식품과 농업에 관한 미국 규제 정책 44 B.C.L. 개정판 733(2003)
- ^ "The History and Future of GM Potatoes". PotatoPro.com. 2013-12-11.
- ^ APPDMZ\ccvivr. "Commonly Asked Questions about the Food Safety of GMOs". monsanto.com.
- ^ Pollack, Andrew (2015-07-02). "White House Orders Review of Rules for Genetically Modified Crops". The New York Times. Retrieved 2015-07-03.
- ^ "Food from Genetically Engineered Plants". FDA. Retrieved 18 October 2015.
- ^ "Statement of Policy – Foods Derived from New Plant Varieties". Food and Drug Administration. Retrieved 18 October 2015.
- ^ 뉴욕타임스의 앤드류 폴락입니다.2000년 9월 23일 "크래프트, 바이오 엔지니어링 옥수수로 타코 껍질 회수"
- ^ Chokshi, Niraj (9 May 2014). "Vermont just passed the nation's first GMO food labeling law. Now it prepares to get sued". The Washington Post. Retrieved 19 January 2016.
- ^ "The Regulation of Genetically Modified Food". Archived from the original on 2017-06-10. Retrieved 2013-11-22.
- ^ Van Eenennaam, Alison; Chassy, Bruce; Kalaitzandonakes, Nicholas; Redick, Thomas (2014). "The Potential Impacts of Mandatory Labeling for Genetically Engineered Food in the United States" (PDF). Council for Agricultural Science and Technology (CAST). 54 (April 2014). ISSN 1070-0021. Archived from the original (PDF) on 2014-05-29. Retrieved 2014-05-28.
To date, no material differences in composition or safety of commercialized GE crops have been identified that would justify a label based on the GE nature of the product.
- ^ Hallenbeck, Terri (2014-04-27). "How GMO labeling came to pass in Vermont". Burlington Free Press. Retrieved 2014-05-28.
- ^ Botha, Gerda M.; Viljoen, Christopher D. (2009). "South Africa: A case study for voluntary GM labelling". Food Chemistry. 112 (4): 1060–64. doi:10.1016/j.foodchem.2008.06.050.
- ^ Davison, John (2010). "GM plants: Science, politics and EC regulations". Plant Science. 178 (2): 94–98. doi:10.1016/j.plantsci.2009.12.005.
- ^ a b Wunderlich, Shahla; Kelsey A. Gatto (November 2015). "Consumer Perception of Genetically Modified Organisms and Sources of Information". Advances in Nutrition. 6 (6): 842–851. doi:10.3945/an.115.008870. PMC 4642419. PMID 26567205.
- ^ "EU GMO testing homepage". European Commission Join Research Centre. 2012-11-20. Retrieved May 31, 2015.
- ^ Costa, Joana; Mafra, Isabel; Amaral, Joana S.; Oliveira, M.B.P.P. (2010). "Monitoring genetically modified soybean along the industrial soybean oil extraction and refining processes by polymerase chain reaction techniques". Food Research International. 43: 301–06. doi:10.1016/j.foodres.2009.10.003.
- ^ "Redirecting..." heinonline.org.
{{cite web}}:Cite는 일반 제목(도움말)을 사용합니다. - ^ 미국 의사 협회(2012).과학 및 공중 보건 위원회 보고서 2: 생물 공학 식품의 라벨링."생명공학 식품의 잠재적 위해성을 더 잘 감지하기 위해, 위원회는 사전 시장 안전성 평가가 자발적 통보 프로세스에서 필수 요건으로 전환되어야 한다고 생각합니다." 페이지 7
- ^ 환경위생부(2006) GM, 재래식, 유기농의 공존을 관리하기 위한 제안 환경식품부 자문서에 대한 대응.2006년 10월
- ^ Paul, John (2013) "유전자 변형 생물(GMO)이 유기 농업에 미치는 위협: 도입 사례의 갱신」을 참조.농업 및 식량, 3:56-63
- ^ "About". Peel Back The Label. Retrieved 2021-07-09.
- ^ Knutson, Jonathan (May 22, 2018). "Dairy farmers fight back against deceptive advertising". Agweek. Retrieved 2021-07-09.
- ^ a b c d e f g Paparini, Andrea; Romano-Spica, Vincenzo (2004), Public health issues related with the consumption of food obtained from genetically modified organisms, Biotechnology Annual Review, vol. 10, Elsevier, pp. 85–122, doi:10.1016/s1387-2656(04)10004-5, ISBN 9780444517494, PMID 15504704, retrieved 2022-05-24
- ^ Prescott, Vanessa E.; Hogan, Simon P. (August 2006). "Genetically modified plants and food hypersensitivity diseases: Usage and implications of experimental models for risk assessment". Pharmacology & Therapeutics. 111 (2): 374–383. doi:10.1016/j.pharmthera.2005.10.005. ISSN 0163-7258. PMID 16364445.
- ^ Ahmed, Farid E. (November 2003). "Genetically modified probiotics in foods". Trends in Biotechnology. 21 (11): 491–497. doi:10.1016/j.tibtech.2003.09.006. ISSN 0167-7799. PMID 14573362.
- ^ D'Agnolo, G. (August 2005). "GMO: Human Health Risk Assessment". Veterinary Research Communications. 29 (S2): 7–11. doi:10.1007/s11259-005-0003-7. ISSN 0165-7380. PMID 16244917. S2CID 12709929.
- ^ Dona, Artemis; Arvanitoyannis, Ioannis S. (2009-02-02). "Health Risks of Genetically Modified Foods". Critical Reviews in Food Science and Nutrition. 49 (2): 164–175. doi:10.1080/10408390701855993. ISSN 1040-8398. PMID 18989835. S2CID 6861474.
- ^ a b c Hwang, Hyesun; Nam, Su-Jung (2020-11-02). "The influence of consumers' knowledge on their responses to genetically modified foods". GM Crops & Food. 12 (1): 146–157. doi:10.1080/21645698.2020.1840911. ISSN 2164-5698. PMC 7644159. PMID 33138666.
- ^ Lucht, Jan (2015-07-30). "Public Acceptance of Plant Biotechnology and GM Crops". Viruses. 7 (8): 4254–4281. doi:10.3390/v7082819. ISSN 1999-4915. PMC 4576180. PMID 26264020.