로타바이러스
Rotavirus| 로타바이러스 | |
|---|---|
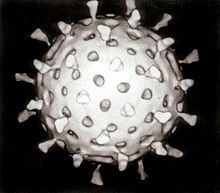 | |
| 여러 전자현미경 사진을 이용한 로타바이러스의 컴퓨터 보조 재구성 | |
| 바이러스 분류 | |
| (무순위): | 바이러스 |
| 영역: | 리보비리아 |
| 왕국: | 오르토르나비래 |
| 문: | Duplornaviricota |
| 클래스: | 레지노바이러스테스 |
| 주문: | 레오비랄레스 |
| 가족: | 세도로바이러스과 |
| 하위 그룹: | 세도로비리과 |
| 속: | 로타바이러스 |
| 종. | |
| |
로타바이러스는 영유아 설사병의 가장 흔한 원인입니다.[1] 세계의 거의 모든 아이들이 5세까지 최소한 한 번은 로타바이러스에 감염됩니다.[2] 감염될 때마다 면역이 생기므로 이후의 감염은 덜 심각합니다. 어른들은 거의 영향을 받지 않습니다.[3] 로타바이러스(Rotavirus)는 레오바이러스과에 속하는 이중가닥 RNA 바이러스의 한 속입니다. 가장 흔한 종인 A, B, C, D, F, G, H, I 및 J 로타바이러스 A는 인간에게 로타바이러스 감염의 90% 이상을 유발하는 9종의 속이 있습니다.[4]
이 바이러스는 분변-구강 경로를 통해 전염됩니다. 소장을 구성하는 세포를 감염시켜 손상시키고, 위장염(인플루엔자와 아무런 관련이 없음에도 불구하고 흔히 '위 독감'이라고 함)을 일으킵니다. 로타바이러스는 1973년 루스 비숍(Ruth Bishop)과 그녀의 동료들에 의해 전자현미경 사진으로[5] 발견되었으며 영유아의 심각한 설사로 입원하는 경우의 약 3분의 1을 차지하지만,[6] 역사적으로 공중 보건 커뮤니티, 특히 개발도상국에서 로타바이러스의 중요성은 과소평가되어 왔습니다.[7] 로타바이러스는 인간의 건강에 미치는 영향 외에도 다른 동물에게도 감염되며 가축의 병원체입니다.[8]
로타바이러스 장염은 보통 소아기에 쉽게 관리되는 질병이지만 5세 미만 어린이 중 로타바이러스로 인해 2019년 설사로 인한 사망자는 151,714명으로 추정됩니다.[9] 미국에서는 2000년대에 로타바이러스 예방접종 프로그램이 시작되기 전에 로타바이러스가 어린이에게 약 270만 건의 중증 위장염을 유발하고 거의 60,000명이 입원했으며 매년 약 37명이 사망했습니다.[10] 미국에서 로타바이러스 백신이 도입된 후 입원율이 크게 떨어졌습니다.[11][12] 로타바이러스 퇴치를 위한 공중보건 캠페인은 감염된 어린이들에게 경구 수분 보충 요법을 제공하고 질병 예방을 위한 예방접종에 초점을 맞추고 있습니다.[13] 로타바이러스 감염의 발병률과 중증도는 일상적인 소아 면역 정책에 로타바이러스 백신을 추가한 국가에서 크게 감소했습니다.[14][15][16]
바이러스학
로타바이러스의 종류
로타바이러스에는 9종이 있는데, A, B, C, D, F, G, H, I, J라고 합니다.[17][18] 인간은 주로 로타바이러스 A종에 감염됩니다. A–I 종은 다른 동물,[19] 돼지는 H, 조류는 D, F, G, 고양이는 I, 박쥐는 J에서 질병을 일으킵니다.[20][21][22][23]
로타바이러스 A종 내에는 혈청형이라고 불리는 다양한 균주가 있습니다.[24] 인플루엔자 바이러스와 마찬가지로 바이러스 표면에 있는 두 개의 단백질을 기준으로 이중 분류 시스템을 사용합니다. 당단백질 VP7은 G 혈청형을 정의하고 단백질분해효소 민감성 단백질 VP4는 P 혈청형을 정의합니다.[25] G형과 P형을 결정하는 두 유전자가 따로 자손 바이러스에 전달될 수 있기 때문에 서로 다른 조합이 발견됩니다.[25] 비정형 균주의 기원을 결정하는 데 사용된 A형 로타바이러스에 대해 전체 유전체 유전자형 시스템이 구축되었습니다.[26] 개별 G형과 P형의 유병률은 국가와 연도에 따라 다양합니다.[27] 최소 36개의 G형과 51개의 P형이[28] 있지만 사람의 감염에서는 G형과 P형의 몇 가지 조합만이 우세합니다. They are G1P[8], G2P[4], G3P[8], G4P[8], G9P[8] and G12P[8].[29]
구조.
로타바이러스의 게놈은 총 18,555개의 뉴클레오티드인 RNA(dsRNA)의 독특한 이중나선 분자 11개로 구성되어 있습니다. 각각의 나선, 즉 분절은 크기를 줄여 1에서 11로 번호가 매겨지는 유전자입니다. 각 유전자는 하나의 단백질을 암호화하고, 2개를 암호화하는 9번 유전자는 제외합니다.[30] RNA는 3겹의 20면체 단백질 캡시드로 둘러싸여 있습니다. 바이러스 입자는 직경이[31][32] 최대 76.5nm로 둘러싸여 있지 않습니다.[33]
단백질
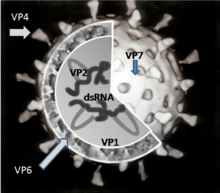
바이러스 입자(virion)를 형성하는 바이러스 단백질(VP)은 6개입니다. 이러한 구조 단백질을 VP1, VP2, VP3, VP4, VP6 및 VP7이라고 합니다. VP 외에도 로타바이러스에 감염된 세포에서만 생성되는 6개의 비구조 단백질(NSP)이 있습니다. These are called NSP1, NSP2, NSP3, NSP4, NSP5 and NSP6.[19]
로타바이러스 유전체에 의해 암호화된 12개의 단백질 중 적어도 6개는 RNA에 결합합니다.[35] 로타바이러스 복제에서 이러한 단백질의 역할은 완전히 이해되지 않았습니다. 그들의 기능은 비리온의 RNA 합성 및 포장, 유전체 복제 부위로의 mRNA 수송, mRNA 번역 및 유전자 발현 조절과 관련이 있는 것으로 생각됩니다.[36]
구조단백질
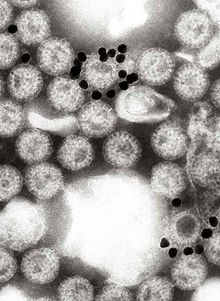
VP1은 바이러스 입자의 핵심에 위치하며 RNA 의존성 RNA 중합효소 효소입니다.[37] 감염된 세포에서 이 효소는 바이러스 단백질의 합성을 위한 mRNA 전사체를 생성하고 새로 생성된 바이러스 입자에 대한 로타바이러스 유전체 RNA 세그먼트의 사본을 생성합니다.[38]
VP2는 비리온의 핵심층을 형성하고 RNA 유전체에 결합합니다.[39]
VP3는 비리온의 내부 코어의 일부이며, 구아닐트랜스퍼라제라는 효소입니다. 이것은 mRNA의 전사 후 변형에서 5' 캡의 형성을 촉매하는 캡핑 효소입니다.[40] 이 캡은 뉴클레아제라고 불리는 핵산 분해 효소로부터 바이러스 mRNA를 보호하여 바이러스 mRNA를 안정화시킵니다.[41]
VP4는 스파이크로 돌출된 비리온 표면에 있습니다.[42] 수용체라는 세포 표면의 분자와 결합해 바이러스가 세포 안으로 들어오게 합니다.[43] VP4는 장에서 발견되는 단백질분해효소 효소 트립신에 의해 바이러스가 감염되기 전에 VP5*와 VP8*로 변형되어야 합니다.[44] VP4는 바이러스가 얼마나 독성이 있는지를 결정하고 바이러스의 P 유형을 결정합니다.[45] 사람의 경우 혈액형(루이스 항원 시스템, ABO 혈액형 시스템 및 분비 상태)과 감염에 대한 민감성 사이에 연관성이 있습니다. 비분비체는 P[4] 및 P[8] 유형에 의한 감염에 내성이 있는 것으로 보이며, 이는 혈액형 항원이 이러한 유전자형의 수용체임을 나타냅니다.[46] 이 내성은 로타바이러스 유전자형에 따라 달라집니다.[47]
VP6는 캡시드의 대부분을 형성합니다. 항원성이 높아 로타바이러스 종을 식별하는 데 사용할 수 있습니다.[48] 이 단백질은 로타바이러스 감염에 대한 실험실 테스트에 사용됩니다.[49]
VP7은 비리온의 외부 표면을 형성하는 당단백질입니다. 구조적 기능 외에도 균주의 G형을 결정하고 VP4와 함께 감염에 대한 면역에 관여합니다.[31]
비구조 바이러스 단백질
5번 유전자의 산물인 NSP1은 비구조적 RNA 결합 단백질입니다.[50] NSP1은 또한 바이러스 감염으로부터 세포를 보호하는 선천성 면역 체계의 부분인 인터페론 반응을 차단합니다. NSP1은 프로테오좀이 감염된 세포에서 인터페론의 생성을 자극하고 인접한 세포에서 분비되는 인터페론에 반응하는 데 필요한 주요 신호 구성 요소를 분해하도록 합니다.
분해 대상에는 인터페론 유전자 전사에 필요한 여러 IRF 전사 인자가 포함됩니다.[51]
NSP2는 RNA 결합 단백질로, 세포질 포함물(바이로플라스마)에 축적되어 유전체 복제에 필요합니다.[52][39]
NSP3는 감염된 세포에서 바이러스 mRNA와 결합하여 세포 단백질 합성을 중단시키는 역할을 합니다.[53] NSP3는 숙주 mRNA로부터 단백질 합성에 필수적인 두 개의 번역 개시 인자를 비활성화합니다.
먼저 NSP3는 번역 개시 인자 eIF4F로부터 폴리(A) 결합 단백질(PABP)을 배출합니다. PABP는 대부분의 숙주 세포 전사체에서 발견되는 3' 폴리(A) 꼬리를 가진 전사체의 효율적인 번역에 필요합니다. 둘째, NSP3는 eIF2의 인산화를 자극하여 eIF2를 비활성화합니다.[54] 3' poly(A) 꼬리가 없는 로타바이러스 mRNA의 효율적인 번역에는 이러한 요소 중 어느 것도 필요하지 않습니다.[55]
NSP4는 설사를 유발하는 바이러스성 장독소로 최초로 발견된 바이러스성 장독소입니다.[56] 포유류 세포에서 세포질 Ca를2+ 높이는 바이로포린입니다.[57]
NSP5는 로타바이러스 A의 유전체 세그먼트 11에 의해 암호화됩니다. 바이러스에 감염된 세포에서 NSP5는 바이러스질에 축적됩니다.[58]
NSP6는 핵산 결합 단백질이며[59], 역위상 개방 판독 프레임에서 유전자 11에 의해 암호화됩니다.[60]
| RNA 세그먼트(유전자) | 사이즈(베이스쌍) | 단백질 | 유니프로트 | 분자량 kDa | 위치 | 파티클당 복사본 수 | 기능. |
|---|---|---|---|---|---|---|---|
| 1 | 3302 | VP1 | P22678 | 125 | 코어의 꼭지점에서 | 12 | RNA 의존성 RNA 중합효소 |
| 2 | 2690 | VP2 | A2T3R5 | 102 | 코어의 내부 쉘을 형성합니다. | 120 | RNA결합 |
| 3 | 2591 | VP3 | A2T3S5 | 88 | 코어의 꼭지점에서 | 12 | 메틸트랜스퍼라제 mRNA 캡핑 효소 |
| 4 | 2362 | VP4 | A2T3T2 | 87 | 표면 스파이크 | 180 | 세포 부착, 독성 |
| 5 | 1611 | NSP1 | Q99FX5 | 59 | 비구조적 | 0 | 5'RNA 결합, 인터페론 길항제 |
| 6 | 1356 | VP6 | Q6LE89 | 45 | 내부 캡시드 | 780 | 구조 및 종 특이 항원 |
| 7 | 1104 | NSP3 | P03536 | 37 | 비구조적 | 0 | 바이러스 mRNA 활성을 향상시키고 세포 단백질 합성을 차단합니다. |
| 8 | 1059 | NSP2 | A2T3P0 | 35 | 비구조적 | 0 | RNA 포장에 관여하는 NTPase |
| 9 | 1062 | VP71 VP72 | P03533 | 38과 34 | 표면 | 780 | 구조 및 중화항원 |
| 10 | 751 | NSP4 | P04512 | 20 | 비구조적 | 0 | 비로포린 (장독소) |
| 11 | 667 | NSP5 NSP6 | A2T3Q9 P11203 | 22 | 비구조적 | 0 | NSP2의 ssRNA 및 dsRNA 결합 조절제, 인단백질 |
이 표는 simian rotavirus 균주 SA11을 기반으로 합니다. RNA-단백질 코딩 할당은 일부 균주에서 다릅니다.
복제

- VP4 및 VP7에 의해 매개되는 숙주 세포에 대한 바이러스 부착
- 바이러스에 의한 세포 침투 및 바이러스 캡시드의 코팅 해제
- VP1, VP3 및 VP2에 의해 매개되는 가닥 ssRNA 합성(이는 mRNA 역할을 함)
- 바이로플라스마 형성, 바이러스 RNA 패키징 및 마이너스 가닥 RNA 합성 및 이중층 바이러스 입자 형성
- 바이러스 입자 성숙 및 자손 비리온 방출
바이러스가 숙주 세포에 부착되는 것은 VP4에 의해 시작되는데, VP4는 세포 표면의 글리칸이라고 불리는 분자에 부착됩니다.[33] 바이러스는 수용체 매개 엔도사이토시스에 의해 세포 안으로 들어가 엔도솜으로 알려진 소포체를 형성합니다. 세 번째 층(VP7 및 VP4 스파이크)의 단백질은 엔도솜의 막을 파괴하여 칼슘 농도의 차이를 만듭니다. 이로 인해 VP7 삼량체가 단일 단백질 소단위로 분해되어 바이러스 dsRNA 주위에 VP2 및 VP6 단백질이 코팅되어 이중층 입자(DLP)를 형성합니다.[62]
11개의 dsRNA 가닥은 2개의 단백질 껍질의 보호 내에 남아 있고 바이러스 RNA 의존성 RNA 중합효소는 이중 가닥 바이러스 유전체의 mRNA 전사체를 생성합니다. 바이러스 RNA는 핵에 남아 이중 가닥 RNA의 존재에 의해 유발되는 RNA 간섭을 포함한 선천적인 숙주 면역 반응을 회피합니다.[63]
감염 과정에서 로타바이러스는 단백질 생합성과 유전자 복제를 위한 mRNA를 생성합니다. 로타바이러스 단백질의 대부분은 RNA가 복제되고 DLP가 조립되는 바이로플라스마에 축적됩니다. 바이로플라스마에서 바이러스 유전체 dsRNA 합성을 위한 템플릿으로 사용되는 포지티브 센스 바이러스 RNA는 siRNA에 의한 RNase 분해로부터 보호됩니다.[64] 바이러스질은 바이러스 감염 후 빠르면 2시간 후에 세포핵 주위에 형성되며, NSP5와 NSP2라는 두 가지 바이러스 비구조 단백질에 의해 만들어지는 것으로 생각되는 바이러스 공장으로 구성됩니다. 시험관 내 RNA 간섭에 의한 NSP5의 억제는 로타바이러스 복제의 급격한 감소를 초래합니다. DLP는 세 번째 외층(VP7 및 VP4에 의해 형성됨)을 얻는 소포체로 이동합니다. 자손 바이러스는 용해에 의해 세포에서 방출됩니다.[44][65][66]
변속기

로타바이러스는 분변-구강 경로를 통해, 오염된 손, 표면 및 물체와의 접촉을 통해,[67] 그리고 아마도 호흡기 경로를 통해 전염됩니다.[68] 바이러스성 설사는 전염성이 강합니다. 감염된 사람의 대변에는 1g당 10조 개 이상의 감염 입자가 포함될 수 있습니다.[48] 이 중 100개 미만이 다른 사람에게 감염을 전염시키는 데 필요합니다.[3]
로타바이러스는 환경에서 안정적이며 미국 갤런당 최대 1-5개의 감염 입자 수준으로 하구 샘플에서 발견되었습니다. 바이러스는 9일에서 19일 사이에 생존합니다.[69] 건강 수준이 높은 국가와 낮은 국가의 로타바이러스 감염 발생률이 비슷하기 때문에 박테리아와 기생충을 제거하는 데 적합한 위생 조치는 로타바이러스 통제에 효과가 없는 것으로 보입니다.[68]
징후 및 증상
로타바이러스 장염은 메스꺼움, 구토, 물 설사, 저등급 발열을 특징으로 하는 경증에서 중증의 질환입니다. 일단 어린이가 바이러스에 감염되면 증상이 나타나기까지 약 2일간의 잠복기가 있습니다.[70] 병기가 급합니다. 증상은 구토로 시작하여 4-8일 동안 설사를 많이 합니다. 탈수는 세균성 병원체에 의한 것보다 로타바이러스 감염에서 더 흔히 발생하며, 로타바이러스 감염과 관련된 가장 흔한 사망 원인입니다.[71]
로타바이러스 감염은 평생에 걸쳐 발생할 수 있습니다: 첫 번째는 일반적으로 증상을 일으키지만,[72][48] 이후의 감염은 면역 체계가 어느 정도 보호를 제공하기 때문에 일반적으로 경미하거나 무증상입니다.[73] 따라서 유증상 감염률은 2세 미만의 소아에서 가장 높고 45세로 갈수록 점진적으로 감소합니다.[74] 가장 심한 증상은 생후 6개월에서 2세 사이의 소아, 노인, 면역결핍 환자에서 발생하는 경향이 있습니다. 대부분의 성인은 어린 시절에 획득한 면역으로 인해 로타바이러스에 취약하지 않으며, 성인의 위장염은 대개 로타바이러스 이외의 다른 원인이 발생하지만, 성인의 무증상 감염은 지역사회 내 감염 전파를 유지할 수 있습니다.[75] 혈액형이 로타바이러스에 의한 감염에 대한 민감성에 영향을 미칠 수 있음을 시사하는 몇 가지 증거가 있습니다.[76]
질병 메커니즘

로타바이러스는 주로 장에서 복제되고 [77]소장 융모의 장세포를 감염시켜 상피의 구조적, 기능적 변화를 유도합니다.[78] 인간, 특히 동물 모델에서 감염성 바이러스가 다른 장기와 대식세포에 장외 전파된다는 증거가 있습니다.[79]
설사는 바이러스의 여러 활동으로 인해 발생합니다.[80] 장세포라는 장세포의 파괴로 인해 흡수 장애가 발생합니다. 독성 로타바이러스 단백질 NSP4는 연령 및 칼슘 이온 의존성 염화물 분비를 유도하고, SGLT1(나트륨/포도당 공동수송체 2) 수송체 매개 물 재흡수를 방해하며, 브러시 경계 막 이당화효소의 활성을 분명히 감소시키고, 장 신경계의 칼슘 이온 의존성 분비 반사를 활성화합니다.[56] NSP4가 바이로포린 역할을 함으로써 세포질의 칼슘 이온 농도가 높아집니다. 이러한 칼슘 이온의 증가는 감염된 장세포의 자가포식(자기 파괴)을 초래합니다.[81]
NSP4도 분비됩니다. 장에서 단백질분해효소 효소에 의해 변형되는 이 세포외 형태는 인테그린 수용체를 통해 미감염 세포에 작용하는 장독소이며, 이는 차례로 세포 내 칼슘 이온 농도, 분비성 설사 및 자가포식을 유발하고 증가시킵니다.[82]
로타바이러스 장염의 특징인 구토는 바이러스가 소화관 내막의 장크롬아핀 세포를 감염시켜 발생합니다. 이 감염은 5' 하이드록시트립타민(세로토닌)의 생성을 자극합니다. 이것은 질 구심성 신경을 활성화시키고, 이것은 차례로 구토 반사를 조절하는 뇌간의 세포를 활성화시킵니다.[83]
건강한 장세포는 소장으로 락타아제를 분비하는데, 락타아제 결핍으로 인한 우유 불내증은 로타바이러스 감염증으로 [84]몇 주간 지속될 수 있는 증상입니다.[85] 가벼운 설사의 재발은 종종 장내 이당류 유당의 박테리아 발효로 인해 어린이 식단에 우유를 다시 도입한 후에 발생합니다.[86]
면역반응
구체적인 응답
로타바이러스는 B 및 T 세포 면역 반응을 모두 유도합니다. 로타바이러스 VP4 및 VP7 단백질에 대한 항체는 시험관 내 및 생체 내에서 바이러스 감염성을 중화시킵니다.[87] IgM, IgA 및 IgG 그룹의 특정 항체가 생성되며, 이는 다른 동물에서 항체의 수동적인 전달에 의해 로타바이러스 감염으로부터 보호하는 것으로 나타났습니다.[88] 산모의 태반횡단 IgG는 신생아를 로타바이러스 감염으로부터 보호하는 역할을 할 수 있지만, 반대로 백신 효능을 감소시킬 수 있습니다.[89]
선천적 반응
로타바이러스에 의한 감염 후 바이러스의 복제를 억제하고 대식세포와 자연살해세포를 로타바이러스에 감염된 세포로 모집하는 I형 및 III형 인터페론 및 기타 사이토카인(특히 Th1 및 Th2)[90]을 포함하는 빠른 선천성 면역 반응이 있습니다.[91] 로타바이러스 dsRNA는 인터페론의 생성을 자극하는 톨 유사 수용체와 같은 패턴 인식 수용체를 활성화합니다.[92] 로타바이러스 단백질 NSP1은 인터페론 조절 단백질 IRF3, IRF5 및 IRF7의 활성을 억제하여 제1형 인터페론의 효과에 대응합니다.[92]
보호 표지
혈액 내 IgG 및 IgA와 장 내 IgA의 수준은 감염으로부터의 보호와 상관관계가 있습니다.[93] 높은 역가(예: >1:200)에서 로타바이러스 특이 혈청 IgG 및 IgA는 보호 효과가 있다고 주장되었으며 IgA 역가와 로타바이러스 백신 효능 사이에는 상당한 상관관계가 있습니다.[94]
진단 및 탐지
로타바이러스 감염 진단은 일반적으로 위장관염 진단에 이어 중증 설사의 원인이 됩니다. 위장염으로 병원에 입원한 아이들은 대부분 로타바이러스 검사를 받습니다.[95][96]
로타바이러스 감염에 대한 구체적인 진단은 효소면역측정법으로 아이의 대변에서 바이러스를 찾아냅니다. 시중에는 민감하고 특이하며 모든 혈청형의 로타바이러스를 검출하는 여러 허가된 테스트 키트가 있습니다.[97] 전자현미경과 PCR(중합효소 연쇄반응)과 같은 다른 방법은 연구실에서 사용됩니다.[98] 역전사-중합효소 연쇄반응(RT-PCR)은 인간 로타바이러스의 모든 종과 혈청형을 검출하고 식별할 수 있습니다.[99]
치료 및 예후
급성 로타바이러스 감염의 치료는 비특이적이며 증상의 관리와 가장 중요한 것은 탈수의 관리를 포함합니다.[13] 치료하지 않으면 어린이는 심각한 탈수로 사망할 수 있습니다.[100] 설사의 심각성에 따라 치료는 경구 수분 보충 요법으로 구성되며, 이 기간 동안 아이에게 특정 양의 소금과 설탕이 포함된 음료를 마실 수 있는 여분의 물이 제공됩니다.[101] 2004년 세계보건기구(WHO)와 유니세프는 급성 설사의 두 가지 치료법으로 저삼투압 경구 수분 보충 용액과 아연 보충제의 사용을 권장했습니다.[102] 일부 감염은 정맥 요법 또는 비위관 삽관으로 수액을 투여하고 아이의 전해질과 혈당을 모니터링하는 입원을 보장할 정도로 심각합니다.[95] 로타바이러스 감염증은 다른 합병증을 거의 일으키지 않으며 잘 관리되는 어린이의 예후는 우수합니다.[103] 프로바이오틱스는 로타바이러스 설사 기간을 줄이는 것으로 나타났으며,[104] 유럽 소아 소화기 학회에 따르면 "효과적인 개입에는 락트산간균 람노수스 또는 사카로미세스 불라디, 디오스멕타이트 또는 라세카도트릴과 같은 특정 프로바이오틱스의 투여가 포함됩니다."[105]
예방
로타바이러스는 전염성이 강해 항생제나 다른 약물로 치료할 수 없습니다. 위생 개선이 로타바이러스 질병의 유병률을 감소시키지 않고 경구 수분 보충제를 사용함에도 불구하고 입원율이 여전히 높기 때문에 공중 보건의 주요 개입은 백신 접종입니다.[2] 1998년 로타바이러스 백신이 미국에서 사용 허가를 받았습니다. 미국, 핀란드, 베네수엘라의 임상시험에서 로타바이러스 A에 의한 중증 설사 예방에 80-100%의 효과가 있는 것으로 밝혀졌으며, 연구자들은 통계적으로 유의미한 심각한 부작용을 발견하지 못했습니다.[106][107] 그러나 이 백신이 예방접종을 받은 유아 1만 2천 명당 1명꼴로 장폐색의 일종인 장중첩증의 위험을 높이는 데 기여했을 가능성이 있다는 사실이 밝혀지자 제조사는 1999년 이 백신을 시장에서 철수시켰습니다.[108] 이 경험은 로타바이러스 백신의 상대적 위험과 이점에 대한 치열한 논쟁을 촉발했습니다.[109]
2006년에는 로타바이러스 A형 감염에 대한 새로운 백신 2종이 어린이들에게 안전하고 효과적인 것으로 나타났으며,[110] 2009년 WHO는 모든 국가 예방접종 프로그램에 로타바이러스 백신을 포함할 것을 권고했습니다.[111]
이 권고에 따라 조치를 취한 국가에서 로타바이러스 감염의 발병률과 중증도가 크게 감소했습니다.[14][15][16] 국가 예방접종 프로그램에서 로타바이러스 백신을 일상적으로 사용하는 국가의 사용 가능한 임상 시험 데이터를 2014년 검토한 결과 로타바이러스 백신은 로타바이러스 입원을 49-92% 감소시켰고 모든 것이 설사 입원을 17-55%[112] 유발하는 것으로 나타났습니다. 2006년 세계 최초로 로타바이러스 백신을 도입한 멕시코에서는 2009년 로타바이러스 시즌 동안 2세 이하 어린이의 설사병 사망률이 65% 이상 떨어졌습니다.[113] 2006년 개발도상국 최초로 로타바이러스 백신을 도입한 니카라과에서는 중증 로타바이러스 감염이 40%, 응급실 방문이 절반으로 줄었습니다.[114] 미국에서는 2006년 이후 로타바이러스 백신 접종으로 로타바이러스 관련 입원이 86%나 감소했습니다.[115] 백신은 또한 순환 감염의 수를 제한함으로써 백신을 접종하지 않은 어린이의 질병을 예방했을 수 있습니다.[115][116] 로타바이러스 사망자의 대다수가 발생하는 아프리카와 아시아 개발도상국에서는 안전성 및 효능 시험을 대거 실시한 것은 물론 최근 로타릭스와 로타텍의 도입 후 영향 및 효과 연구에서도 백신이 유아들의 중증 질환을 극적으로 감소시키는 것으로 나타났습니다.[16][117][118][119] 2013년 9월, 영국에서 생후 2~3개월 사이의 모든 어린이들에게 백신을 제공했는데, 중증 감염 사례를 절반으로 줄이고, 감염으로 인해 병원에 입원하는 어린이의 수를 70%까지 줄일 수 있을 것으로 기대됩니다.[120] 유럽에서는 로타바이러스 감염에 따른 입원율이 백신 도입 후 65%에서 84%로 감소했습니다.[121] 전 세계적으로 백신 접종으로 병원 입원과 응급실 방문이 평균 67%[122] 감소했습니다.
로타바이러스 백신은 100개 이상의 국가에서 허가를 받고 있으며, 80개 이상의 국가에서 일상적인 로타바이러스 백신 접종을 도입했으며, 거의 절반이 GAVI 백신 동맹의 지원을 받고 있습니다.[123] 모든 국가, 특히 로타바이러스 사망자의 대부분이 발생하는 아프리카와 아시아의 저소득 및 중간 소득 국가, PATH(구 보건 적정 기술 프로그램), WHO, 미국 질병통제예방센터, 그리고 GAVI는 연구 기관 및 정부와 협력하여 증거를 생성 및 보급하고 가격을 낮추며 도입을 가속화했습니다.[124]
백신은 제1형 당뇨병을 예방할 수 있습니다.[125][126]
역학
사람에게서 로타바이러스 위장염의 90% 이상을 차지하는 로타바이러스 A는 전 세계적으로 풍토병입니다.[4] 매년 로타바이러스는 개발도상국에서 수백만 건의 설사를 유발하며, 이 중 거의 200만 건이 입원으로 이어집니다.[7] 2019년에는 5세 미만 어린이 약 151,714명이 로타바이러스 감염으로 사망했으며, 이 중 90%가 개발도상국에서 사망했습니다.[9] 거의 모든 어린이가 5세까지 로타바이러스에 감염되었습니다.[2][127] 로타바이러스는 영유아의 심각한 설사의 주요 단일 원인이며 입원이 필요한 경우의 약 3분의 1을 차지하며 [11]설사로 인한 사망의 37%와 5세 미만 어린이의 전체 사망의 5%를 유발합니다.[128] 남자 아이들이 로타바이러스 감염으로 병원에 입원할 확률이 여자 아이들보다 두 배나 높습니다.[129][130] 백신 접종 전 시대에 로타바이러스 감염은 주로 서늘하고 건조한 계절에 발생했습니다.[131][132] 식품 오염으로 인한 수는 알 수 없습니다.[133]
로타바이러스 A 설사의 발병은 입원한 유아, 탁아소에 다니는 어린 아이, 요양원의 노인들 사이에서 흔합니다.[75][134] 1981년 콜로라도에서 오염된 도시 물로 인한 발병이 발생했습니다.[135] 2005년 동안 니카라과에서 가장 큰 설사 전염병이 발생했습니다. 이 비정상적으로 크고 심각한 발병은 로타바이러스 A 유전체의 돌연변이와 관련이 있으며, 아마도 바이러스가 집단 내 만연한 면역에서 벗어나는 데 도움이 되었을 것입니다.[136] 1977년 브라질에서도 비슷한 규모의 대규모 발병이 발생했습니다.[137]
성인 설사 로타바이러스 또는 ADRV라고도 불리는 로타바이러스 B는 중국의 모든 연령대의 수천 명에게 심각한 설사를 일으키는 주요 전염병을 일으켰습니다. 이러한 전염병은 식수의 하수 오염으로 인해 발생했습니다.[138][139] 1998년 인도에서도 로타바이러스 B형 감염자가 발생하였으며, 원인 균주는 CAL로 명명되었습니다. ADRV와 달리 CAL 균주는 풍토병입니다.[140][141] 현재까지 로타바이러스 B에 의한 전염병은 중국 본토에 국한되어 있으며, 조사에 따르면 미국에서는 이 종에 대한 면역력이 부족한 것으로 나타났습니다.[142] Rotavirus C는 소아에서 드물고 산발적인 설사 사례와 관련이 있으며, 가정에서 작은 발병이 발생했습니다.[143]
- 영국의 로타바이러스 A 감염의 계절적 변화: 겨울 동안 감염률은 최고조에 달합니다.[144]
- 로타바이러스 예방접종으로 인한 예방 가능한 어린이 사망, 2016. 로타바이러스 백신의 완전한 적용이 달성된 경우 로타바이러스로 인한 5세 미만 어린이의 연간 예방 가능한 사망자 수.[145]
다른 동물들
로타바이러스는 많은 종의 동물들의 어린아이들을 감염시키며 전 세계적으로 야생 및 사육 동물들의 설사의 주요 원인입니다.[8] 가축의 병원체로서, 특히 어린 송아지와 자돈에서 로타바이러스는 높은 이환율 및 사망률과 관련된 치료 비용으로 인해 농부에게 경제적 손실을 초래합니다.[146] 이러한 로타바이러스는 인간 로타바이러스와의 유전적 교환을 위한 잠재적인 저장소입니다.[146] 동물 로타바이러스가 바이러스의 직접적인 전염 또는 인간 균주를 가진 재배열체에 하나 또는 여러 개의 RNA 세그먼트를 기여함으로써 인간을 감염시킬 수 있다는 증거가 있습니다.[147][148][149]
역사

1943년, 제이콥 라이트와 호레이스 호데스는 감염성 설사를 가진 아이들의 대변에서 여과 가능한 물질이 소에게 상처(축사 설사)를 유발한다는 것을 증명했습니다.[150] 30년 후, 이 병원체의 보존된 샘플은 로타바이러스인 것으로 나타났습니다.[151] 지난 몇 년 동안 쥐의[152] 바이러스는 바이러스가 흉터를 일으키는 것과 관련이 있는 것으로 나타났습니다.[153] 1973년 루스 비숍(Ruth Bishop)과 동료들은 위장염 어린이에게서 발견되는 관련 바이러스에 대해 설명했습니다.[5]
1974년 토마스 헨리 플라이엇(Thomas Henry Flyett)은 전자현미경으로 관찰했을 때 로타바이러스 입자가 바퀴(라틴어 로타)처럼 보이는 [154][155]것을 보고 로타바이러스라는 이름을 제안했습니다. 이 이름은 4년 후 국제바이러스분류위원회(International Committee on Taxonomy of Virus)로부터 공식적으로 인정받았습니다.[156] 1976년, 몇몇 다른 종의 동물에서 관련 바이러스가 기술되었습니다.[153] 급성 위장염을 일으키는 이 바이러스들은 전 세계적으로 인간을 비롯한 동물들에게 영향을 미치는 집단 병원체로 인식되었습니다.[154] 로타바이러스 혈청형은 1980년에 처음 기술되었고,[157] 이듬해에는 원숭이 신장에서 유래한 세포 배양에서 인간의 로타바이러스를 배양 배지에 트립신(포유류의 십이지장에서 발견되고 현재 로타바이러스가 복제하는 데 필수적인 것으로 알려진 효소)을 첨가하여 처음으로 성장시켰습니다.[158] 배양에서 로타바이러스를 성장시키는 능력은 연구 속도를 가속화시켰고 1980년대 중반까지 첫 번째 후보 백신이 평가되고 있었습니다.[159]
참고문헌
- ^ Dennehy PH (September 2015). "Rotavirus Infection: A Disease of the Past?". Infectious Disease Clinics of North America. 29 (4): 617–635. doi:10.1016/j.idc.2015.07.002. PMID 26337738.
- ^ a b c Bernstein DI (2009). "Rotavirus overview". The Pediatric Infectious Disease Journal. 28 (Suppl 3): S50–S53. doi:10.1097/INF.0b013e3181967bee. PMID 19252423. S2CID 30544613.
- ^ a b Grimwood K, Lambert SB (2009). "Rotavirus vaccines: opportunities and challenges". Human Vaccines. 5 (2): 57–69. doi:10.4161/hv.5.2.6924. PMID 18838873. S2CID 31164630.
- ^ a b Leung AK, Kellner JD, Davies HD (2005). "Rotavirus gastroenteritis". Advances in Therapy. 22 (5): 476–487. doi:10.1007/BF02849868. PMID 16418157. S2CID 39847059.
- ^ a b Bishop R (2009). "Discovery of rotavirus: Implications for child health". Journal of Gastroenterology and Hepatology. 24 (Suppl 3): S81–S85. doi:10.1111/j.1440-1746.2009.06076.x. PMID 19799704.
- ^ Hallowell BD, Chavers T, Parashar U, Tate JE (April 2022). "Global Estimates of Rotavirus Hospitalizations Among Children Below 5 Years in 2019 and Current and Projected Impacts of Rotavirus Vaccination". Journal of the Pediatric Infectious Diseases Society. 11 (4): 149–158. doi:10.1093/jpids/piab114. PMID 34904636.
- ^ a b Simpson E, Wittet S, Bonilla J, Gamazina K, Cooley L, Winkler JL (2007). "Use of formative research in developing a knowledge translation approach to rotavirus vaccine introduction in developing countries". BMC Public Health. 7: 281. doi:10.1186/1471-2458-7-281. PMC 2173895. PMID 17919334. S2CID 424503.
- ^ a b Dubovi EJ, MacLachlan NJ (2010). Fenner's Veterinary Virology (4th ed.). Boston: Academic Press. p. 288. ISBN 978-0-12-375158-4.
- ^ a b Janko MM, Joffe J, Michael D, Earl L, Rosettie KL, Sparks GW, Albertson SB, Compton K, Pedroza Velandia P, Stafford L, Zheng P, Aravkin A, Kyu HH, Murray CJ, Weaver MR (June 2022). "Cost-effectiveness of rotavirus vaccination in children under five years of age in 195 countries: A meta-regression analysis". Vaccine. 40 (28): 3903–3917. doi:10.1016/j.vaccine.2022.05.042. PMC 9208428. PMID 35643565. S2CID 249072461.
- ^ Fischer TK, Viboud C, Parashar U, Malek M, Steiner C, Glass R, Simonsen L (April 2007). "Hospitalizations and deaths from diarrhea and rotavirus among children <5 years of age in the United States, 1993–2003". The Journal of Infectious Diseases. 195 (8): 1117–1125. doi:10.1086/512863. PMID 17357047.
- ^ a b Leshem E, Moritz RE, Curns AT, Zhou F, Tate JE, Lopman BA, Parashar UD (July 2014). "Rotavirus vaccines and health care utilization for diarrhea in the United States (2007–2011)". Pediatrics. 134 (1): 15–23. doi:10.1542/peds.2013-3849. PMC 7975848. PMID 24913793.
- ^ Tate JE, Cortese MM, Payne DC, Curns AT, Yen C, Esposito DH, et al. (January 2011). "Uptake, impact, and effectiveness of rotavirus vaccination in the United States: review of the first 3 years of postlicensure data". The Pediatric Infectious Disease Journal. 30 (1 Suppl): S56–60. doi:10.1097/INF.0b013e3181fefdc0. PMID 21183842. S2CID 20940659.
- ^ a b Diggle L (2007). "Rotavirus diarrhea and future prospects for prevention". British Journal of Nursing. 16 (16): 970–974. doi:10.12968/bjon.2007.16.16.27074. PMID 18026034.
- ^ a b Giaquinto C, Dominiak-Felden G, Van Damme P, Myint TT, Maldonado YA, Spoulou V, Mast TC, Staat MA (2011). "Summary of effectiveness and impact of rotavirus vaccination with the oral pentavalent rotavirus vaccine: a systematic review of the experience in industrialized countries". Human Vaccines. 7 (7): 734–748. doi:10.4161/hv.7.7.15511. PMID 21734466. S2CID 23996836.
- ^ a b Jiang V, Jiang B, Tate J, Parashar UD, Patel MM (July 2010). "Performance of rotavirus vaccines in developed and developing countries". Human Vaccines. 6 (7): 532–42. doi:10.4161/hv.6.7.11278. PMC 3322519. PMID 20622508.
- ^ a b c Parashar UD, Johnson H, Steele AD, Tate JE (May 2016). Parashar UD, Tate JE (eds.). "Health Impact of Rotavirus Vaccination in Developing Countries: Progress and Way Forward". Clinical Infectious Diseases. 62 (Suppl 2): S91–95. doi:10.1093/cid/civ1015. PMID 27059361.
- ^ "Virus Taxonomy: 2021 Release". International Committee on Taxonomy of Viruses (ICTV). Retrieved 19 May 2022.
- ^ Suzuki H (August 2019). "Rotavirus Replication: Gaps of Knowledge on Virus Entry and Morphogenesis". The Tohoku Journal of Experimental Medicine. 248 (4): 285–296. doi:10.1620/tjem.248.285. PMID 31447474.
- ^ a b Kirkwood CD (September 2010). "Genetic and antigenic diversity of human rotaviruses: potential impact on vaccination programs". The Journal of Infectious Diseases. 202 Suppl (Suppl 1): S43–48. doi:10.1086/653548. PMID 20684716.
- ^ Wakuda M, Ide T, Sasaki J, Komoto S, Ishii J, Sanekata T, Taniguchi K (August 2011). "Porcine rotavirus closely related to novel group of human rotaviruses". Emerging Infectious Diseases. 17 (8): 1491–1493. doi:10.3201/eid1708.101466. PMC 3381553. PMID 21801631.
- ^ Marthaler D, Rossow K, Culhane M, Goyal S, Collins J, Matthijnssens J, Nelson M, Ciarlet M (July 2014). "Widespread rotavirus H in commercially raised pigs, United States". Emerging Infectious Diseases. 20 (7): 1195–1198. doi:10.3201/eid2007.140034. PMC 4073875. PMID 24960190.
- ^ Phan TG, Leutenegger CM, Chan R, Delwart E (June 2017). "Rotavirus I in feces of a cat with diarrhea". Virus Genes. 53 (3): 487–490. doi:10.1007/s11262-017-1440-4. PMC 7089198. PMID 28255929.
- ^ Bányai K, Kemenesi G, Budinski I, Földes F, Zana B, Marton S, Varga-Kugler R, Oldal M, Kurucz K, Jakab F (March 2017). "Candidate new rotavirus species in Schreiber's bats, Serbia". Infection, Genetics and Evolution. 48: 19–26. doi:10.1016/j.meegid.2016.12.002. PMC 7106153. PMID 27932285.
- ^ O'Ryan M (March 2009). "The ever-changing landscape of rotavirus serotypes". The Pediatric Infectious Disease Journal. 28 (3 Suppl): S60–62. doi:10.1097/INF.0b013e3181967c29. PMID 19252426. S2CID 22421988.
- ^ a b Patton JT (January 2012). "Rotavirus diversity and evolution in the post-vaccine world". Discovery Medicine. 13 (68): 85–97. PMC 3738915. PMID 22284787.
- ^ Phan MV, Anh PH, Cuong NV, Munnink BB, van der Hoek L, My PT, Tri TN, Bryant JE, Baker S, Thwaites G, Woolhouse M, Kellam P, Rabaa MA, Cotten M (July 2016). "Unbiased whole-genome deep sequencing of human and porcine stool samples reveals circulation of multiple groups of rotaviruses and a putative zoonotic infection". Virus Evolution. 2 (2): vew027. doi:10.1093/ve/vew027. PMC 5522372. PMID 28748110.
- ^ Beards GM, Desselberger U, Flewett TH (December 1989). "Temporal and geographical distributions of human rotavirus serotypes, 1983 to 1988". Journal of Clinical Microbiology. 27 (12): 2827–2833. doi:10.1128/JCM.27.12.2827-2833.1989. PMC 267135. PMID 2556435.
- ^ Rakau KG, Nyaga MM, Gededzha MP, Mwenda JM, Mphahlele MJ, Seheri LM, Steele AD (January 2021). "Genetic characterization of G12P[6] and G12P[8] rotavirus strains collected in six African countries between 2010 and 2014". BMC Infectious Diseases. 21 (1): 107. doi:10.1186/s12879-020-05745-6. PMC 7821174. PMID 33482744.
- ^ Antoni S, Nakamura T, Cohen AL, Mwenda JM, Weldegebriel G, Biey JN, Shaba K, Rey-Benito G, de Oliveira LH, Oliveira MT, Ortiz C, Ghoniem A, Fahmy K, Ashmony HA, Videbaek D, Daniels D, Pastore R, Singh S, Tondo E, Liyanage JB, Sharifuzzaman M, Grabovac V, Batmunkh N, Logronio J, Armah G, Dennis FE, Seheri M, Magagula N, Mphahlele J, Leite JP, Araujo IT, Fumian TM, El Mohammady H, Semeiko G, Samoilovich E, Giri S, Kang G, Thomas S, Bines J, Kirkwood CD, Liu N, Lee DY, Iturriza-Gomara M, Page NA, Esona MD, Ward ML, Wright CN, Mijatovic-Rustempasic S, Tate JE, Parashar UD, Gentsch J, Bowen MD, Serhan F (2023). "Rotavirus genotypes in children under five years hospitalized with diarrhea in low and middle-income countries: Results from the WHO-coordinated Global Rotavirus Surveillance Network". PLOS Global Public Health. 3 (11): e0001358. doi:10.1371/journal.pgph.0001358. PMC 10683987. PMID 38015834.
- ^ Estes MK, Cohen J (1989). "Rotavirus gene structure and function". Microbiological Reviews. 53 (4): 410–449. doi:10.1128/MMBR.53.4.410-449.1989. PMC 372748. PMID 2556635.
- ^ a b Pesavento JB, Crawford SE, Estes MK, Prasad BV (2006). "Rotavirus proteins: structure and assembly". In Roy P (ed.). Reoviruses: Entry, Assembly and Morphogenesis. Current Topics in Microbiology and Immunology. Vol. 309. New York: Springer. pp. 189–219. doi:10.1007/3-540-30773-7_7. ISBN 978-3-540-30772-3. PMID 16913048. S2CID 11290382.
- ^ Prasad BV, Chiu W (1994). "Structure of Rotavirus". In Ramig RF (ed.). Rotaviruses. Current Topics in Microbiology and Immunology. Vol. 185. New York: Springer. pp. 9–29. doi:10.1007/978-3-642-78256-5_2 (inactive 22 March 2024). ISBN 978-3-540-56761-5. PMID 8050286.
{{cite book}}: CS1 메인트: DOI 2024년 3월 기준 비활성화 (링크) - ^ a b Rodríguez JM, Luque D (2019). "Structural Insights into Rotavirus Entry". Physical Virology. Advances in Experimental Medicine and Biology. Vol. 1215. pp. 45–68. doi:10.1007/978-3-030-14741-9_3. hdl:20.500.12105/10344. ISBN 978-3-030-14740-2. PMID 31317495. S2CID 197541267.
- ^ Gray J, Desselberger U (2000). Rotaviruses : methods and protocols. Totowa, N.J.: Humana Press. p. 15. ISBN 978-1-59259-078-0. OCLC 55684328.
- ^ Patton JT (1995). "Structure and function of the rotavirus RNA-binding proteins". The Journal of General Virology. 76 (11): 2633–2644. doi:10.1099/0022-1317-76-11-2633. PMID 7595370.
- ^ Patton JT (2001). "Rotavirus RNA Replication and Gene Expression". Gastroenteritis Viruses. Novartis Foundation Symposia. Vol. 238. pp. 64–77, discussion 77–81. doi:10.1002/0470846534.ch5. ISBN 978-0-470-84653-7. PMID 11444036.
- ^ Vásquez-del Carpió R, Morales JL, Barro M, Ricardo A, Spencer E (2006). "Bioinformatic prediction of polymerase elements in the rotavirus VP1 protein". Biological Research. 39 (4): 649–659. doi:10.4067/S0716-97602006000500008. PMID 17657346.
- ^ Trask SD, Ogden KM, Patton JT (2012). "Interactions among capsid proteins orchestrate rotavirus particle functions". Current Opinion in Virology. 2 (4): 373–379. doi:10.1016/j.coviro.2012.04.005. PMC 3422376. PMID 22595300.
- ^ a b Taraporewala ZF, Patton JT (2004). "Nonstructural proteins involved in genome packaging and replication of rotaviruses and other members of the Reoviridae". Virus Research. 101 (1): 57–66. doi:10.1016/j.virusres.2003.12.006. PMID 15010217.
- ^ Angel J, Franco MA, Greenberg HB (2009). Mahy BW, Van Regenmortel MH (eds.). Desk Encyclopedia of Human and Medical Virology. Boston: Academic Press. p. 277. ISBN 978-0-12-375147-8.
- ^ Cowling VH (2009). "Regulation of mRNA cap methylation". The Biochemical Journal. 425 (2): 295–302. doi:10.1042/BJ20091352. PMC 2825737. PMID 20025612.
- ^ Gardet A, Breton M, Fontanges P, Trugnan G, Chwetzoff S (2006). "Rotavirus spike protein VP4 binds to and remodels actin bundles of the epithelial brush border into actin bodies". Journal of Virology. 80 (8): 3947–3456. doi:10.1128/JVI.80.8.3947-3956.2006. PMC 1440440. PMID 16571811.
- ^ Arias CF, Isa P, Guerrero CA, Méndez E, Zárate S, López T, Espinosa R, Romero P, López S (2002). "Molecular biology of rotavirus cell entry". Archives of Medical Research. 33 (4): 356–361. doi:10.1016/S0188-4409(02)00374-0. PMID 12234525.
- ^ a b Jayaram H, Estes MK, Prasad BV (2004). "Emerging themes in rotavirus cell entry, genome organization, transcription and replication". Virus Research. 101 (1): 67–81. doi:10.1016/j.virusres.2003.12.007. PMID 15010218.
- ^ Hoshino Y, Jones RW, Kapikian AZ (2002). "Characterization of neutralization specificities of outer capsid spike protein VP4 of selected murine, lapine, and human rotavirus strains". Virology. 299 (1): 64–71. doi:10.1006/viro.2002.1474. PMID 12167342.
- ^ Van Trang N, Vu HT, Le NT, Huang P, Jiang X, Anh DD (2014). "Association between norovirus and rotavirus infection and histo-blood group antigen types in Vietnamese children". Journal of Clinical Microbiology. 52 (5): 1366–1374. doi:10.1128/JCM.02927-13. PMC 3993640. PMID 24523471.
- ^ Sharma S, Hagbom M, Svensson L, Nordgren J (March 2020). "The Impact of Human Genetic Polymorphisms on Rotavirus Susceptibility, Epidemiology, and Vaccine Take". Viruses. 12 (3): 324. doi:10.3390/v12030324. PMC 7150750. PMID 32192193.
- ^ a b c Bishop RF (1996). "Natural history of human rotavirus infection". Archives of Virology. Supplementum. 12: 119–28. doi:10.1007/978-3-7091-6553-9_14. ISBN 978-3-211-82875-5. PMID 9015109.
- ^ Beards GM, Campbell AD, Cottrell NR, Peiris JS, Rees N, Sanders RC, Shirley JA, Wood HC, Flewett TH (1984). "Enzyme-linked immunosorbent assays based on polyclonal and monoclonal antibodies for rotavirus detection" (PDF). Journal of Clinical Microbiology. 19 (2): 248–54. doi:10.1128/JCM.19.2.248-254.1984. PMC 271031. PMID 6321549.
- ^ Hua J, Mansell EA, Patton JT (1993). "Comparative analysis of the rotavirus NS53 gene: conservation of basic and cysteine-rich regions in the protein and possible stem-loop structures in the RNA". Virology. 196 (1): 372–378. doi:10.1006/viro.1993.1492. PMID 8395125.
- ^ Arnold MM (2016). "The Rotavirus Interferon Antagonist NSP1: Many Targets, Many Questions". Journal of Virology. 90 (11): 5212–5215. doi:10.1128/JVI.03068-15. PMC 4934742. PMID 27009959.
- ^ Kattoura MD, Chen X, Patton JT (1994). "The rotavirus RNA-binding protein NS35 (NSP2) forms 10S multimers and interacts with the viral RNA polymerase". Virology. 202 (2): 803–13. doi:10.1006/viro.1994.1402. PMID 8030243.
- ^ Poncet D, Aponte C, Cohen J (1993). "Rotavirus protein NSP3 (NS34) is bound to the 3' end consensus sequence of viral mRNAs in infected cells" (PDF). Journal of Virology. 67 (6): 3159–3165. doi:10.1128/JVI.67.6.3159-3165.1993. PMC 237654. PMID 8388495.
- ^ Gratia M, Vende P, Charpilienne A, Baron HC, Laroche C, Sarot E, Pyronnet S, Duarte M, Poncet D (2016). "Challenging the Roles of NSP3 and Untranslated Regions in Rotavirus mRNA Translation". PLOS ONE. 11 (1): e0145998. Bibcode:2016PLoSO..1145998G. doi:10.1371/journal.pone.0145998. PMC 4699793. PMID 26727111.
- ^ López S, Arias CF (2012). "Rotavirus-host cell interactions: an arms race". Current Opinion in Virology. 2 (4): 389–398. doi:10.1016/j.coviro.2012.05.001. PMID 22658208.
- ^ a b Hyser JM, Estes MK (2009). "Rotavirus vaccines and pathogenesis: 2008". Current Opinion in Gastroenterology. 25 (1): 36–43. doi:10.1097/MOG.0b013e328317c897. PMC 2673536. PMID 19114772.
- ^ Pham T, Perry JL, Dosey TL, Delcour AH, Hyser JM (March 2017). "The Rotavirus NSP4 Viroporin Domain is a Calcium-conducting Ion Channel". Scientific Reports. 7: 43487. Bibcode:2017NatSR...743487P. doi:10.1038/srep43487. PMC 5335360. PMID 28256607.
- ^ Afrikanova I, Miozzo MC, Giambiagi S, Burrone O (1996). "Phosphorylation generates different forms of rotavirus NSP5". Journal of General Virology. 77 (9): 2059–2065. doi:10.1099/0022-1317-77-9-2059. PMID 8811003.
- ^ Rainsford EW, McCrae MA (2007). "Characterization of the NSP6 protein product of rotavirus gene 11". Virus Research. 130 (1–2): 193–201. doi:10.1016/j.virusres.2007.06.011. PMID 17658646.
- ^ Mohan KV, Atreya CD (2001). "Nucleotide sequence analysis of rotavirus gene 11 from two tissue culture-adapted ATCC strains, RRV and Wa". Virus Genes. 23 (3): 321–329. doi:10.1023/A:1012577407824. PMID 11778700. S2CID 21538632.
- ^ Gray J, Desselberger U (2000). Rotaviruses : methods and protocols. Totowa, N.J.: Humana Press. p. 5. ISBN 978-1-59259-078-0. OCLC 55684328.
- ^ Baker M, Prasad BV (2010). "Rotavirus cell entry". In Johnson J (ed.). Cell Entry by Non-Enveloped Viruses. Current Topics in Microbiology and Immunology. Vol. 343. pp. 121–148. doi:10.1007/82_2010_34. ISBN 978-3-642-13331-2. PMID 20397068.
- ^ Arnold MM (2016). "The Rotavirus Interferon Antagonist NSP1: Many Targets, Many Questions". Journal of Virology. 90 (11): 5212–5215. doi:10.1128/JVI.03068-15. PMC 4934742. PMID 27009959.
- ^ Silvestri LS, Taraporewala ZF, Patton JT (2004). "Rotavirus replication: plus-sense templates for double-stranded RNA synthesis are made in viroplasms". Journal of Virology. 78 (14): 7763–7774. doi:10.1128/JVI.78.14.7763-7774.2004. PMC 434085. PMID 15220450.
- ^ Patton JT, Vasquez-Del Carpio R, Spencer E (2004). "Replication and transcription of the rotavirus genome". Current Pharmaceutical Design. 10 (30): 3769–3777. doi:10.2174/1381612043382620. PMID 15579070.
- ^ Ruiz MC, Leon T, Diaz Y, Michelangeli F (2009). "Molecular biology of rotavirus entry and replication". The Scientific World Journal. 9: 1476–1497. doi:10.1100/tsw.2009.158. PMC 5823125. PMID 20024520.
- ^ Butz AM, Fosarelli P, Dick J, Cusack T, Yolken R (1993). "Prevalence of rotavirus on high-risk fomites in day-care facilities". Pediatrics. 92 (2): 202–205. doi:10.1542/peds.92.2.202. PMID 8393172. S2CID 20327842.
- ^ a b Dennehy PH (2000). "Transmission of rotavirus and other enteric pathogens in the home". Pediatric Infectious Disease Journal. 19 (Suppl 10): S103–105. doi:10.1097/00006454-200010001-00003. PMID 11052397. S2CID 28625697.
- ^ Rao VC, Seidel KM, Goyal SM, Metcalf TG, Melnick JL (1984). "Isolation of enteroviruses from water, suspended solids, and sediments from Galveston Bay: survival of poliovirus and rotavirus adsorbed to sediments" (PDF). Applied and Environmental Microbiology. 48 (2): 404–409. Bibcode:1984ApEnM..48..404R. doi:10.1128/AEM.48.2.404-409.1984. PMC 241526. PMID 6091548.
- ^ Hochwald C, Kivela L (1999). "Rotavirus vaccine, live, oral, tetravalent (RotaShield)". Pediatric Nursing. 25 (2): 203–204, 207. PMID 10532018.
- ^ Maldonado YA, Yolken RH (1990). "Rotavirus". Baillière's Clinical Gastroenterology. 4 (3): 609–625. doi:10.1016/0950-3528(90)90052-I. PMID 1962726.
- ^ Glass RI, Parashar UD, Bresee JS, Turcios R, Fischer TK, Widdowson MA, Jiang B, Gentsch JR (2006). "Rotavirus vaccines: current prospects and future challenges". The Lancet. 368 (9532): 323–332. doi:10.1016/S0140-6736(06)68815-6. PMID 16860702. S2CID 34569166.
- ^ Offit PA (2001). Gastroenteritis viruses. New York: Wiley. pp. 106–124. ISBN 978-0-471-49663-2.
- ^ Ramsay M, Brown D (2000). "Epidemiology of Group A Rotaviruses: Surveillance and Burden of Disease Studies". In Desselberger U, Gray J (eds.). Rotaviruses: Methods and Protocols. Methods in Molecular Medicine. Vol. 34. Totowa, NJ: Humana Press. pp. 217–238. doi:10.1385/1-59259-078-0:217. ISBN 978-0-89603-736-6. PMID 21318862.
- ^ a b Anderson EJ, Weber SG (2004). "Rotavirus infection in adults". The Lancet Infectious Diseases. 4 (2): 91–99. doi:10.1016/S1473-3099(04)00928-4. PMC 7106507. PMID 14871633.
- ^ Elhabyan A, Elyaacoub S, Sanad E, Abukhadra A, Elhabyan A, Dinu V (November 2020). "The role of host genetics in susceptibility to severe viral infections in humans and insights into host genetics of severe COVID-19: A systematic review". Virus Research. 289: 198163. doi:10.1016/j.virusres.2020.198163. PMC 7480444. PMID 32918943.
- ^ Greenberg HB, Estes MK (2009). "Rotaviruses: from pathogenesis to vaccination". Gastroenterology. 136 (6): 1939–1951. doi:10.1053/j.gastro.2009.02.076. PMC 3690811. PMID 19457420.
- ^ Greenberg HB, Clark HF, Offit PA (1994). "Rotavirus Pathology and Pathophysiology". In Ramig RF (ed.). Rotaviruses. Current Topics in Microbiology and Immunology. Vol. 185. New York: Springer. pp. 255–283. doi:10.1007/978-3-642-78256-5_9 (inactive 22 March 2024). ISBN 978-3-540-56761-5. PMID 8050281.
{{cite book}}: CS1 메인트: DOI 2024년 3월 기준 비활성화 (링크) - ^ Crawford SE, Patel DG, Cheng E, Berkova Z, Hyser JM, Ciarlet M, Finegold MJ, Conner ME, Estes MK (2006). "Rotavirus viremia and extraintestinal viral infection in the neonatal rat model". Journal of Virology. 80 (10): 4820–4832. doi:10.1128/JVI.80.10.4820-4832.2006. PMC 1472071. PMID 16641274.
- ^ Ramig RF (2004). "Pathogenesis of intestinal and systemic rotavirus infection". Journal of Virology. 78 (19): 10213–10220. doi:10.1128/JVI.78.19.10213-10220.2004. PMC 516399. PMID 15367586.
- ^ Hyser JM, Collinson-Pautz MR, Utama B, Estes MK (2010). "Rotavirus disrupts calcium homeostasis by NSP4 viroporin activity". mBio. 1 (5). doi:10.1128/mBio.00265-10. PMC 2999940. PMID 21151776.
- ^ Berkova Z, Crawford SE, Trugnan G, Yoshimori T, Morris AP, Estes MK (2006). "Rotavirus NSP4 induces a novel vesicular compartment regulated by calcium and associated with viroplasms". Journal of Virology. 80 (12): 6061–6071. doi:10.1128/JVI.02167-05. PMC 1472611. PMID 16731945.
- ^ Hagbom M, Sharma S, Lundgren O, Svensson L (2012). "Towards a human rotavirus disease model". Current Opinion in Virology. 2 (4): 408–418. doi:10.1016/j.coviro.2012.05.006. PMID 22722079.
- ^ Farnworth ER (2008). "The evidence to support health claims for probiotics". The Journal of Nutrition. 138 (6): 1250S–1254S. doi:10.1093/jn/138.6.1250S. PMID 18492865.
- ^ Ouwehand A, Vesterlund S (2003). "Health aspects of probiotics". IDrugs: The Investigational Drugs Journal. 6 (6): 573–580. PMID 12811680.
- ^ Arya SC (1984). "Rotaviral infection and intestinal lactase level". Journal of Infectious Diseases. 150 (5): 791. doi:10.1093/infdis/150.5.791. PMID 6436397.
- ^ Ward R (2009). "Mechanisms of protection against rotavirus infection and disease". The Pediatric Infectious Disease Journal. 28 (Suppl 3): S57–S59. doi:10.1097/INF.0b013e3181967c16. PMID 19252425.
- ^ Vega CG, Bok M, Vlasova AN, Chattha KS, Fernández FM, Wigdorovitz A, Parreño VG, Saif LJ (2012). "IgY antibodies protect against human Rotavirus induced diarrhea in the neonatal gnotobiotic piglet disease model". PLOS ONE. 7 (8): e42788. Bibcode:2012PLoSO...742788V. doi:10.1371/journal.pone.0042788. PMC 3411843. PMID 22880110.
- ^ Mwila K, Chilengi R, Simuyandi M, Permar SR, Becker-Dreps S (2017). "Contribution of Maternal Immunity to Decreased Rotavirus Vaccine Performance in Low- and Middle-Income Countries". Clinical and Vaccine Immunology. 24 (1). doi:10.1128/CVI.00405-16. PMC 5216432. PMID 27847365.
- ^ Gandhi GR, Santos VS, Denadai M, da Silva Calisto VK, de Souza Siqueira Quintans J, de Oliveira e Silva AM, de Souza Araújo AA, Narain N, Cuevas LE, Júnior LJ, Gurgel RQ (2017). "Cytokines in the management of rotavirus infection: A systematic review of in vivo studies". Cytokine. 96: 152–160. doi:10.1016/j.cyto.2017.04.013. PMID 28414969. S2CID 3568330.
- ^ Holloway G, Coulson BS (2013). "Innate cellular responses to rotavirus infection". The Journal of General Virology. 94 (6): 1151–1160. doi:10.1099/vir.0.051276-0. PMID 23486667.
- ^ a b Villena J, Vizoso-Pinto MG, Kitazawa H (2016). "Intestinal Innate Antiviral Immunity and Immunobiotics: Beneficial Effects against Rotavirus Infection". Frontiers in Immunology. 7: 563. doi:10.3389/fimmu.2016.00563. PMC 5136547. PMID 27994593.
- ^ Offit PA (1994). "Rotaviruses: immunological determinants of protection against infection and disease". Advances in Virus Research. 44: 161–202. doi:10.1016/s0065-3527(08)60329-2. ISBN 978-0-12-039844-7. PMC 7130874. PMID 7817873.
- ^ Patel M, Glass RI, Jiang B, Santosham M, Lopman B, Parashar U (2013). "A systematic review of anti-rotavirus serum IgA antibody titer as a potential correlate of rotavirus vaccine efficacy". The Journal of Infectious Diseases. 208 (2): 284–294. doi:10.1093/infdis/jit166. PMID 23596320.
- ^ a b Patel MM, Tate JE, Selvarangan R, Daskalaki I, Jackson MA, Curns AT, Coffin S, Watson B, Hodinka R, Glass RI, Parashar UD (2007). "Routine laboratory testing data for surveillance of rotavirus hospitalizations to evaluate the impact of vaccination". The Pediatric Infectious Disease Journal. 26 (10): 914–919. doi:10.1097/INF.0b013e31812e52fd. PMID 17901797. S2CID 10992309.
- ^ The Pediatric ROTavirus European CommitTee (PROTECT) (2006). "The paediatric burden of rotavirus disease in Europe". Epidemiology and Infection. 134 (5): 908–916. doi:10.1017/S0950268806006091. PMC 2870494. PMID 16650331.
- ^ Angel J, Franco MA, Greenberg HB (2009). Mahy WJ, Van Regenmortel MH (eds.). Desk Encyclopedia of Human and Medical Virology. Boston: Academic Press. p. 278. ISBN 978-0-12-375147-8.
- ^ Goode J, Chadwick D (2001). Gastroenteritis viruses. New York: Wiley. p. 14. ISBN 978-0-471-49663-2.
- ^ Fischer TK, Gentsch JR (2004). "Rotavirus typing methods and algorithms". Reviews in Medical Virology. 14 (2): 71–82. doi:10.1002/rmv.411. PMC 7169166. PMID 15027000.
- ^ Alam NH, Ashraf H (2003). "Treatment of infectious diarrhea in children". Paediatric Drugs. 5 (3): 151–165. doi:10.2165/00128072-200305030-00002. PMID 12608880. S2CID 26076784.
- ^ Sachdev HP (1996). "Oral rehydration therapy". Journal of the Indian Medical Association. 94 (8): 298–305. PMID 8855579.
- ^ World Health Organization, UNICEF. "Joint Statement: Clinical Management of Acute Diarrhoea" (PDF). Retrieved 3 May 2012.
- ^ Ramig RF (2007). "Systemic rotavirus infection". Expert Review of Anti-infective Therapy. 5 (4): 591–612. doi:10.1586/14787210.5.4.591. PMID 17678424. S2CID 27763488.
- ^ Ahmadi E, Alizadeh-Navaei R, Rezai MS (2015). "Efficacy of probiotic use in acute rotavirus diarrhea in children: A systematic review and meta-analysis". Caspian Journal of Internal Medicine. 6 (4): 187–195. PMC 4649266. PMID 26644891.
- ^ Guarino A, Ashkenazi S, Gendrel D, Lo Vecchio A, Shamir R, Szajewska H (2014). "European Society for Pediatric Gastroenterology, Hepatology, and Nutrition/European Society for Pediatric Infectious Diseases evidence-based guidelines for the management of acute gastroenteritis in children in Europe: update 2014". Journal of Pediatric Gastroenterology and Nutrition. 59 (1): 132–152. doi:10.1097/MPG.0000000000000375. PMID 24739189. S2CID 4845135.
- ^ "Rotavirus vaccine for the prevention of rotavirus gastroenteritis among children. Recommendations of the Advisory Committee on Immunization Practices (ACIP)". MMWR. Recommendations and Reports. 48 (RR-2): 1–20. 1999. PMID 10219046.
- ^ Kapikian AZ (2001). "A rotavirus vaccine for prevention of severe diarrhoea of infants and young children: development, utilization and withdrawal". Gastroenteritis Viruses. Novartis Foundation Symposia. Vol. 238. pp. 153–171, discussion 171–179. doi:10.1002/0470846534.ch10. ISBN 978-0-470-84653-7. PMID 11444025.
- ^ Bines JE (2005). "Rotavirus vaccines and intussusception risk". Current Opinion in Gastroenterology. 21 (1): 20–25. PMID 15687880. Archived from the original on 11 May 2013. Retrieved 21 January 2008.
- ^ Bines J (2006). "Intussusception and rotavirus vaccines". Vaccine. 24 (18): 3772–3776. doi:10.1016/j.vaccine.2005.07.031. PMID 16099078.
- ^ Dennehy PH (2008). "Rotavirus vaccines: an overview". Clinical Microbiology Reviews. 21 (1): 198–208. doi:10.1128/CMR.00029-07. PMC 2223838. PMID 18202442.
- ^ Tate JE, Patel MM, Steele AD, Gentsch JR, Payne DC, Cortese MM, Nakagomi O, Cunliffe NA, Jiang B, Neuzil KM, de Oliveira LH, Glass RI, Parashar UD (2010). "Global impact of rotavirus vaccines". Expert Review of Vaccines. 9 (4): 395–407. doi:10.1586/erv.10.17. PMID 20370550. S2CID 28963507.
- ^ Tate JE, Parashar UD (2014). "Rotavirus Vaccines in Routine Use". Clinical Infectious Diseases. 59 (9): 1291–1301. doi:10.1093/cid/ciu564. PMID 25048849.
- ^ Richardson V, Hernandez-Pichardo J, et al. (2010). "Effect of Rotavirus Vaccination on Death From Childhood Diarrhea in Mexico". The New England Journal of Medicine. 362 (4): 299–305. doi:10.1056/NEJMoa0905211. PMID 20107215. S2CID 27287753.
- ^ Patel M, Pedreira C, De Oliveira LH, Umaña J, Tate J, Lopman B, Sanchez E, Reyes M, Mercado J, Gonzalez A, Perez MC, Balmaceda A, Andrus J, Parashar U (2012). "Duration of protection of pentavalent rotavirus vaccination in Nicaragua". Pediatrics. 130 (2): e365–e372. doi:10.1542/peds.2011-3478. PMID 22753550. S2CID 7723807.
- ^ a b Omatola CA, Olaniran AO (April 2022). "Rotaviruses: From Pathogenesis to Disease Control-A Critical Review". Viruses. 14 (5): 875. doi:10.3390/v14050875. PMC 9143449. PMID 35632617.
- ^ Patel MM, Parashar UD, et al. (2011). "Real World Impact of Rotavirus Vaccination". Pediatric Infectious Disease Journal. 30 (1): S1–S5. doi:10.1097/INF.0b013e3181fefa1f. PMID 21183833. S2CID 1893099.
- ^ Neuzil KM, Armah GE, Parashar UD, Steele AD (2010). Steele AD, Armah GE, Page NA, Cunliffe NA (eds.). "Rotavirus Infection in Africa: Epidemiology, Burden of Disease, and Strain Diversity". Journal of Infectious Diseases. 202 (Suppl 1): S1–S265. doi:10.1086/653545. PMID 20684687.
- ^ Nelson EA, Widdowson MA, Kilgore PE, Steele D, Parashar UD, eds. (2009). "Rotavirus in Asia: Updates on Disease Burden, Genotypes and Vaccine Introduction". Vaccine. 27 (Suppl 5): F1–F138.
- ^ World Health Organization (2009). "Rotavirus vaccines: an update" (PDF). Weekly Epidemiological Record. 51–52 (84): 533–540. Retrieved 8 May 2012.
- ^ "New vaccine to help protect babies against rotavirus". UK Department of Health. 10 November 2012. Retrieved 10 November 2012.
- ^ Karafillakis E, Hassounah S, Atchison C (2015). "Effectiveness and impact of rotavirus vaccines in Europe, 2006–2014". Vaccine. 33 (18): 2097–2107. doi:10.1016/j.vaccine.2015.03.016. PMID 25795258.
- ^ Burnett E, Jonesteller CL, Tate JE, Yen C, Parashar UD (2017). "Global Impact of Rotavirus Vaccination on Childhood Hospitalizations and Mortality from Diarrhea". The Journal of Infectious Diseases. 215 (11): 1666–1672. doi:10.1093/infdis/jix186. PMC 5543929. PMID 28430997.
- ^ "Rotavirus Deaths & Rotavirus Vaccine Introduction Maps – ROTA Council". rotacouncil.org. Archived from the original on 12 July 2016. Retrieved 29 July 2016.
- ^ Moszynski P (2011). "GAVI rolls out vaccines against child killers to more countries". BMJ. 343: d6217. doi:10.1136/bmj.d6217. PMID 21957215. S2CID 7567316.
- ^ "Rotavirus vaccination tied to lower rates of type 1 diabetes". Reuters. 22 January 2019. Retrieved 10 February 2019.
- ^ Bakalar N (30 January 2019). "Rotavirus Vaccine May Protect Against Type 1 Diabetes". The New York Times. ISSN 0362-4331. Retrieved 10 February 2019.
- ^ Parashar UD, Gibson CJ, Bresse JS, Glass RI (2006). "Rotavirus and severe childhood diarrhea". Emerging Infectious Diseases. 12 (2): 304–306. doi:10.3201/eid1202.050006. PMC 3373114. PMID 16494759.
- ^ Tate JE, Burton AH, Boschi-Pinto C, Steele AD, Duque J, Parashar UD (2012). "2008 estimate of worldwide rotavirus-associated mortality in children younger than 5 years before the introduction of universal rotavirus vaccination programmes: a systematic review and meta-analysis". The Lancet Infectious Diseases. 12 (2): 136–141. doi:10.1016/S1473-3099(11)70253-5. PMID 22030330.
- ^ Rheingans RD, Heylen J, Giaquinto C (2006). "Economics of rotavirus gastroenteritis and vaccination in Europe: what makes sense?". Pediatric Infectious Disease Journal. 25 (Suppl 1): S48–S55. doi:10.1097/01.inf.0000197566.47750.3d. PMID 16397429. S2CID 3272810.
- ^ Ryan MJ, Ramsay M, Brown D, Gay NJ, Farrington CP, Wall PG (1996). "Hospital admissions attributable to rotavirus infection in England and Wales". Journal of Infectious Diseases. 174 (Suppl 1): S12–S18. doi:10.1093/infdis/174.Supplement_1.S12. PMID 8752285.
- ^ Atchison CJ, Tam CC, Hajat S, van Pelt W, Cowden JM, Lopman BA (2010). "Temperature-dependent transmission of rotavirus in Great Britain and The Netherlands". Proceedings of the Royal Society B: Biological Sciences. 277 (1683): 933–942. doi:10.1098/rspb.2009.1755. PMC 2842727. PMID 19939844.
- ^ Levy K, Hubbard AE, Eisenberg JN (2009). "Seasonality of rotavirus disease in the tropics: a systematic review and meta-analysis". International Journal of Epidemiology. 38 (6): 1487–1496. doi:10.1093/ije/dyn260. PMC 2800782. PMID 19056806.
- ^ Koopmans M, Brown D (1999). "Seasonality and diversity of Group A rotaviruses in Europe". Acta Paediatrica. 88 (Suppl 426): 14–19. doi:10.1111/j.1651-2227.1999.tb14320.x. PMID 10088906. S2CID 10969637.
- ^ Sassi HP, Sifuentes LY, Koenig DW, Nichols E, Clark-Greuel J, Wong LF, McGrath K, Gerba CP, Reynolds KA (2015). "Control of the spread of viruses in a long-term care facility using hygiene protocols". American Journal of Infection Control. 43 (7): 702–706. doi:10.1016/j.ajic.2015.03.012. PMID 25944726.
- ^ Hopkins RS, Gaspard GB, Williams FP, Karlin RJ, Cukor G, Blacklow NR (1984). "A community waterborne gastroenteritis outbreak: evidence for rotavirus as the agent". American Journal of Public Health. 74 (3): 263–265. doi:10.2105/AJPH.74.3.263. PMC 1651463. PMID 6320684.
- ^ Bucardo F, Karlsson B, Nordgren J, Paniagua M, González A, Amador JJ, Espinoza F, Svensson L (2007). "Mutated G4P[8] rotavirus associated with a nationwide outbreak of gastroenteritis in Nicaragua in 2005". Journal of Clinical Microbiology. 45 (3): 990–997. doi:10.1128/JCM.01992-06. PMC 1829148. PMID 17229854.
- ^ Linhares AC, Pinheiro FP, Freitas RB, Gabbay YB, Shirley JA, Beards GM (1981). "An outbreak of rotavirus diarrhea among a non-immune, isolated South American Indian community". American Journal of Epidemiology. 113 (6): 703–710. doi:10.1093/oxfordjournals.aje.a113151. PMID 6263087.
- ^ Hung T, Wang C, Fang Z, Chou Z, Chang X, Liong X, Chen G, Yao H, Chao T, Ye W, Den S, Chang W (1984). "Waterborne outbreak of rotavirus diarrhea in adults in China caused by a novel rotavirus". The Lancet. 323 (8387): 1139–1142. doi:10.1016/S0140-6736(84)91391-6. PMID 6144874. S2CID 54346351.
- ^ Fang ZY, Ye Q, Ho MS, Dong H, Qing S, Penaranda ME, Hung T, Wen L, Glass RI (1989). "Investigation of an outbreak of adult diarrhea rotavirus in China". Journal of Infectious Diseases. 160 (6): 948–953. doi:10.1093/infdis/160.6.948. PMID 2555422.
- ^ Kelkar SD, Zade JK (2004). "Group B rotaviruses similar to strain CAL-1, have been circulating in Western India since 1993". Epidemiology and Infection. 132 (4): 745–749. doi:10.1017/S0950268804002171. PMC 2870156. PMID 15310177.
- ^ Ahmed MU, Kobayashi N, Wakuda M, Sanekata T, Taniguchi K, Kader A, Naik TN, Ishino M, Alam MM, Kojima K, Mise K, Sumi A (2004). "Genetic analysis of group B human rotaviruses detected in Bangladesh in 2000 and 2001". Journal of Medical Virology. 72 (1): 149–155. doi:10.1002/jmv.10546. PMID 14635024. S2CID 21258083.
- ^ Penaranda ME, Ho MS, Fang ZY, Dong H, Bai XS, Duan SC, Ye WW, Estes MK, Echeverria P, Hung T (1989). "Seroepidemiology of adult diarrhea rotavirus in China, 1977 to 1987". Journal of Clinical Microbiology. 27 (10): 2180–2183. doi:10.1128/JCM.27.10.2180-2183.1989. PMC 266989. PMID 2479654.
- ^ Moon S, Humphrey CD, Kim JS, Baek LJ, Song JW, Song KJ, Jiang B (2011). "First detection of group C rotavirus in children with acute gastroenteritis in South Korea". Clinical Microbiology and Infection. 17 (2): 244–247. doi:10.1111/j.1469-0691.2010.03270.x. PMID 20491826.
- ^ "Rotavirus vaccination programme for infants". www.gov.uk. Public Health England. 26 July 2013.
- ^ Dadonaite B, Ritchie H (2019). "Rotavirus vaccine – an effective tool that prevents children dying from diarrhea". Our World in Data.
- ^ a b Martella V, Bányai K, Matthijnssens J, Buonavoglia C, Ciarlet M (2010). "Zoonotic aspects of rotaviruses". Veterinary Microbiology. 140 (3–4): 246–255. doi:10.1016/j.vetmic.2009.08.028. PMID 19781872.
- ^ Müller H, Johne R (2007). "Rotaviruses: diversity and zoonotic potential—a brief review". Berliner und Munchener Tierarztliche Wochenschrift. 120 (3–4): 108–112. PMID 17416132.
- ^ Cook N, Bridger J, Kendall K, Gomara MI, El-Attar L, Gray J (2004). "The zoonotic potential of rotavirus". The Journal of Infection. 48 (4): 289–302. doi:10.1016/j.jinf.2004.01.018. PMID 15066329.
- ^ Dóró R, Farkas SL, Martella V, Bányai K (2015). "Zoonotic transmission of rotavirus: surveillance and control". Expert Review of Anti-infective Therapy. 13 (11): 1337–1350. doi:10.1586/14787210.2015.1089171. PMID 26428261. S2CID 42693014.
- ^ Light JS, Hodes HL (1943). "Studies on Epidemic Diarrhea of the New-born: Isolation of a Filtrable Agent Causing Diarrhea in Calves". American Journal of Public Health and the Nation's Health. 33 (12): 1451–1454. doi:10.2105/AJPH.33.12.1451. PMC 1527675. PMID 18015921.
- ^ Mebus CA, Wyatt RG, Sharpee RL, Sereno MM, Kalica AR, Kapikian AZ, Twiehaus MJ (1976). "Diarrhea in gnotobiotic calves caused by the reovirus-like agent of human infantile gastroenteritis" (PDF). Infection and Immunity. 14 (2): 471–474. doi:10.1128/IAI.14.2.471-474.1976. PMC 420908. PMID 184047.
- ^ Rubenstein D, Milne RG, Buckland R, Tyrrell DA (1971). "The growth of the virus of epidemic diarrhoea of infant mice (EDIM) in organ cultures of intestinal epithelium". British Journal of Experimental Pathology. 52 (4): 442–445. PMC 2072337. PMID 4998842.
- ^ a b Woode GN, Bridger JC, Jones JM, Flewett TH, Davies HA, Davis HA, White GB (1976). "Morphological and antigenic relationships between viruses (rotaviruses) from acute gastroenteritis in children, calves, piglets, mice, and foals" (PDF). Infection and Immunity. 14 (3): 804–810. doi:10.1128/IAI.14.3.804-810.1976. PMC 420956. PMID 965097.
- ^ a b Flewett TH, Woode GN (1978). "The rotaviruses". Archives of Virology. 57 (1): 1–23. doi:10.1007/BF01315633. PMC 7087197. PMID 77663.
- ^ Flewett TH, Bryden AS, Davies H, Woode GN, Bridger JC, Derrick JM (1974). "Relation between viruses from acute gastroenteritis of children and newborn calves". The Lancet. 304 (7872): 61–63. doi:10.1016/S0140-6736(74)91631-6. PMID 4137164.
- ^ Matthews RE (1979). "Third report of the International Committee on Taxonomy of Viruses. Classification and nomenclature of viruses". Intervirology. 12 (3–5): 129–296. doi:10.1159/000149081. PMID 43850.
- ^ Beards GM, Brown DW (1988). "The antigenic diversity of rotaviruses: significance to epidemiology and vaccine strategies". European Journal of Epidemiology. 4 (1): 1–11. doi:10.1007/BF00152685. PMID 2833405. S2CID 11547573.
- ^ Urasawa T, Urasawa S, Taniguchi K (1981). "Sequential passages of human rotavirus in MA-104 cells". Microbiology and Immunology. 25 (10): 1025–1035. doi:10.1111/j.1348-0421.1981.tb00109.x. PMID 6273696. S2CID 25276891.
- ^ Ward RL, Bernstein DI (2009). "Rotarix: a rotavirus vaccine for the world". Clinical Infectious Diseases. 48 (2): 222–228. doi:10.1086/595702. PMID 19072246.
![The seasonal variation of rotavirus A infections in England: rates of infection peak during the winter months.[144]](http://upload.wikimedia.org/wikipedia/commons/thumb/4/4e/Rotavirus_seasonal_distribution.png/650px-Rotavirus_seasonal_distribution.png)
![Preventable child deaths from rotavirus vaccination, 2016. Annual number of preventable deaths in children under five years old from rotavirus if full coverage of the rotavirus vaccine was achieved.[145]](http://upload.wikimedia.org/wikipedia/commons/thumb/8/81/Avertable-deaths-from-rotavirus-with-full-vaccine-coverage.png/650px-Avertable-deaths-from-rotavirus-with-full-vaccine-coverage.png)


