자르디아시스
Giardiasis| 자르디아시스 | |
|---|---|
| 기타 이름 | 비버열, 지아디아 |
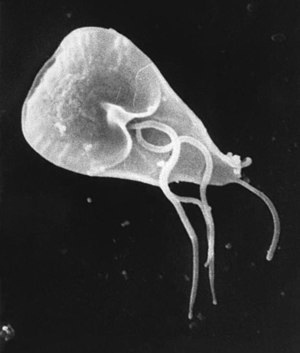 | |
| 주사 전자 현미경으로 본 지아디아 세포 | |
| 전문 | 감염성 질환, 소화기내과 |
| 증상 | 설사, 복통, 체중 감소, 메스꺼움[1] |
| 통상적인 개시 | 노출 후[2] 1~3주 후 |
| 원인들 | 주로 오염된 음식이나 물을[1] 통해 전파되는 십이지장균 |
| 위험요소 | 저감마글로불린혈증 |
| 진단 방법 | 대변[1] 검사 |
| 차동 진단 | 과민성 대장 증후군[1] |
| 예방 | 위생[1] 개선 |
| 치료 | 항원충제 |
| 약 | 티니다졸, 메트로니다졸[1] |
| 빈도수. | 최대 7%(선진국), 최대 30%(개도국)[1] |
Giardiasis는 G. lamblia와 [3]G. internalis로 알려져 있는 Giardia 십이지장에 의해 발생하는 기생충 질환이다.증상을 경험하는 감염된 사람들은 설사, 복통, 체중 [1]감소를 겪을 수 있다.덜 흔한 증상으로는 [1]구토와 대변의 피가 있다.증상은 보통 노출 후 1주에서 3주 후에 시작되며 치료하지 않으면 2주에서 [4]6주 이상 지속될 수 있습니다.
지아디아증은 보통 대변 속의 십이지장 낭종이 음식이나 물을 오염시켜 나중에 [1]입으로 섭취할 때 퍼진다.그 질병은 사람들 사이와 다른 동물들을 [1]통해서도 퍼질 수 있다.낭종은 차가운 [1]물에서 거의 3개월 동안 생존할 수 있다.Giardias는 대변 [1]검사를 통해 진단됩니다.
적절한 위생 [1]관행을 통해 예방을 개선할 수 있습니다.무증상 환자는 [1]치료가 필요하지 않은 경우가 많다.증상이 나타나면 일반적으로 티니다졸 또는 메트로니다졸로 [1]치료한다.감염되면 유당불내증이 생길 수 있으므로 감염 [1]후 일시적으로 유당을 피하는 것이 좋습니다.일부 [1]환자에게는 치료에 대한 거부감이 나타날 수 있습니다.
Giardias는 전세계적으로 [5]발생한다.그것은 가장 흔한 기생충성 인간 [3]질환 중 하나이다.선진국에서는 감염률이 7%, 개발도상국에서는 30%[1]에 이른다.2013년에는 전 세계적으로 약 2억 8천만 명의 사람들이 지아다증 [3]증세를 보였습니다.세계보건기구는 지아다증을 방치된 질병으로 [1]분류하고 있다.그것은 북미에서 비버[6] 열풍으로 널리 알려져 있다.
징후 및 증상
증상은 영양소의 [5]흡수가 잘 되지 않는 상태에서 심한 설사까지 다양하다.이 광범위한 증상의 원인은 충분히 알려져 있지 않지만 감염된 숙주의 장내 세균이 [7][8]한 역할을 할 수 있다.설사는 개발도상국에서 [7]온 사람들에게서 발생할 가능성이 적다.
증상은 일반적으로 노출 [9]후 9~15일 후에 발생하지만 빠르면 하루 [5]안에 발생할 수 있습니다.가장 흔하고 두드러진 증상은 치료하지 [10][11]않으면 몇 주 또는 몇 달 동안 발생할 수 있는 만성 설사이다.설사는 종종 기름지고 악취가 나며 [10][4]떠다니는 경향이 있다.이러한 특징적인 설사는 종종 가스, 복부 경련, 메스꺼움이나 [10][4]구토를 포함한 많은 다른 증상들을 동반합니다.어떤 사람들은 비록 덜 [4]흔하지만, 피부 가려움, 두드러기, 눈과 관절의 붓기와 같은 위장관 밖에서 증상을 경험하기도 한다.'[12]비버열'[6]이라는 별명에도 불구하고 발열은 15% 정도만 발생한다.
장기 질환은 종종 [10]장내 영양소 흡수 장애와 함께 설사로 특징지어진다.이러한 흡수 불량은 지방 대변, 상당한 체중 감소, 그리고 [10]피로를 초래한다.게다가, 지아다증 환자들은 종종 유당, 비타민 A, 엽산, 비타민12 [11][4]B를 흡수하는데 어려움을 겪는다.어린이에게 장기간에 걸친 지아다증은 성장을 저해하고 정신발달을 [10][11]저해할 수 있다.증상성 감염은 [13]유당불내증을 일으키는 것으로 잘 알려져 있으며, 이것은 보통 일시적이기는 하지만 [14][15]영구적일 수 있다.
원인
Giardiasis는 원생동물 Giardia [16]십이지장에 의해 발생한다.감염은 비버, 다른 설치류, 소, 그리고 [16]양을 포함한 많은 동물에서 발생한다.동물들은 [16]환경에 존재하는 감염을 유지하는 역할을 한다고 믿어진다.
G. 십이지장증은 8개의 유전자 집합체(지정 A–[17]H)로 하위 분류되었다.다양한 숙주로부터 분리된 십이지장의 유전자형은 집합체 A와 B가 가장 광범위한 숙주를 감염시키는 것으로 나타났으며,[17][18] 인간을 감염시키는 주요 십이지장 집합체이자 아마도 유일한 G. 십이지장 집합체인 것으로 보인다.
위험요소
미국 질병통제예방센터(CDC)에 따르면 감염 위험이 가장 높은 사람은 다음과 같습니다.
- 육아 환경에 있는 사람
- 질병이 있는 사람과 밀접하게 접촉하는 사람들은
- 위생상태가 좋지 않은 지역 내 여행자
- 성행위 중 대변과 접촉하는 사람
- 온천, 호수 또는 강에서 처리되지 않은 물을 마시는 배낭여행자 또는 캠핑객
- 수영장, 온수조, 쌍방향 분수 또는 처리되지 않은 온천, 호수 또는 강의 물을 마시는 수영객
- 얕은 우물에서 생활용수를 얻는 사람
- 면역력이 약한 사람
- 감염된 동물 또는 대변에 오염된[19] 동물 환경과 접촉한 사람
선진국 사람들의 감염 위험을 증가시키는 요인으로는 기저귀 갈기, 날 음식 섭취, 개 키우기, 개발도상국 [1]여행 등이 있다.그러나 영국 내 감염의 75%는 다른 [1]여행을 통해 감염되는 것이 아니라 영국에서 감염된다.미국에서, 자두증은 여름에 더 자주 발생하는데, 이것은 야외 활동과 [16]황야를 여행하는 데 더 많은 시간을 소비하기 때문이라고 여겨진다.
전송
Giardiasis는 낭종 [9]섭취와 함께 분변-구강 경로를 통해 전염된다.주요 경로는 개인적인 접촉과 오염된 물과 [9]음식이다.낭종은 차가운 [16]물에서 3개월까지 전염성을 유지할 수 있다.
Giardia 감염을 가진 많은 사람들은 [20]증상이 없거나 거의 없다.그러나 그들은 여전히 그 [20]병을 퍼뜨릴지도 모른다.
병태생리학
Giardia의 라이프 사이클은 낭종 형태와 영양소 [8]형태로 구성되어 있다.낭포는 전염성이 있으며 숙주를 발견하면 트로포조이트 [8]형태로 변한다.이 영양소는 장벽에 부착되어 [8]장내에서 복제된다.영양소가 위장관을 따라 계속되면서, 그들은 다시 낭종 형태로 바뀌어 [1]대변과 함께 배설된다.다른 [21]숙주에서 감염을 일으키기 위해서는 이러한 낭종들 중 일부만 섭취하면 된다.
Giardia에 감염되면 브러시 테두리 효소의 발현 감소, 미세 세균에 대한 형태학적 변화, 장 투과성 증가, 소장 상피 [22]세포의 프로그램된 세포 사멸이 초래됩니다.영양소와 낭종 모두 소화관 안에 포함되어 있어 그 [23]너머로 침입하지 않는다.
영양조석의 부착은 [7][22]장에서 이당류를 분해하는 효소의 융모 평탄화와 억제를 일으킨다.궁극적으로, 장에 사는 미생물 집단은 과잉 성장할 수 있고, 비록 이 생각이 충분히 조사되지 않았지만, 추가적인 증상의 원인이 될 수 있다.융모의 변화는 장에서 영양소와 수분을 흡수할 수 없게 되어 주요 [22]증상 중 하나인 설사를 일으킨다.무증상성 지아다증인 경우 소장에 조직학적 변화가 있든 없든 흡수불량이 있을 수 있다.증상과 무증상의 경우 흡수 불량이 발생하는 정도는 매우 다양하다.[citation needed]
Giardia internalis 종은 브러시 테두리의 융모를 공격하기 위해 단백질을 분해하는 효소를 사용하며 융모 양쪽에 존재하는 암세포 증식과 암세포 길이를 증가시키는 것으로 보입니다.면역학적 차원에서 활성화된 숙주 T림프구는 [7]세포를 제거하기 위해 손상된 내피세포를 공격한다.이것은 브러시 테두리 내피세포를 [22]서로 연결하는 단백질이 파괴된 후에 발생합니다.그 결과 장 투과성이 [22]높아집니다.
Giardia internalis에 의한 프로그램된 장구세포의 죽음은 더욱 증가하는 것으로 보이며, 이는 장 장벽을 더욱 손상시키고 [22]투과성을 증가시킨다.기생충에 의한 프로그램된 세포사망 캐스케이드의 유의한 상향조절, 나아가 항아포토시스 단백질 Bcl-2의 대폭 하향조절 및 프로아포토시스 단백질 [7]Bax의 상향조절이 있다.이러한 연결은 자두증의 [7]병원형성에서의 카스파아제 의존성 아포토시스의 역할을 암시한다.
Giardia는 [7]일산화질소를 만드는 데 필요한 아미노산인 모든 국소 아르기닌을 섭취함으로써 일산화질소의 형성을 감소시킴으로써 자신의 성장을 보호한다.아르기닌 결핍은 프로그램된 세포사의 원인으로 알려져 있으며 국소 제거는 강력한 아포토시스제이다.[24]
호스트 디펜스
Giardia에 대한 숙주 방어는 자연 장벽, 일산화질소의 생산, 그리고 선천적이고 적응적인 면역 시스템의 활성화로 구성됩니다.
천연 장벽
자연 장벽은 기생충이 숙주의 몸에 침입하는 것을 막아준다.자연 장벽은 점액층, 담즙염, 단백질 분해효소, 그리고 리파아제 등으로 구성되어 있습니다.또한 연동과 장세포의 재생은 [25][26]기생충에 대한 추가적인 보호를 제공한다.
산화질소 생산
일산화질소는 기생충을 죽이지는 않지만 영양소뿐만 아니라 엑시스테이션과 [27][28]엔시스테이션의 성장을 억제한다.
선천성 면역 체계
보체의 렉틴 경로
보체의 렉틴 경로는 N-아세틸글루코사민과 결합하는 만노스 결합 렉틴(MBL)에 의해 활성화된다.N-아세틸글루코사민은 MBL의 리간드로 Giardia [29]표면에 존재한다.
보체의 고전적 경로
보체의 고전적 경로는 Giardia에 특이적인 항체에 의해 활성화된다.
적응 면역 체계
항체
항체는 기생충의 복제를 억제하고 또한 [citation needed]보체의 고전적인 경로를 통해 기생충의 죽음을 유도한다.
Giardia 감염은 전형적으로 기생충에 대한 강한 항체 반응을 일으킨다.IgG는 상당한 양이 만들어지지만, IgA는 기생충 방제에 더 중요한 것으로 여겨진다.IgA는 장 분비물에 가장 풍부한 아이소형이며 모유에서 지배적인 아이소형이기도 합니다.모유의 항체는 아동의 자두증([30]수동면역)을 예방한다.
T세포
적응 면역 반응의 중요한 면은 T세포 반응이다.지아 디아는 세포 밖의 병원체입니다.따라서 CD4+ 도우미 T세포 주로 이런 예방 효과에 책임이 있다.[31일]
도우미 T세포의 역할 중 하나는 항체 생산과 아이소타입 전환을 촉진하는 것이다.다른 역할에는 [31][32]면역 반응의 다른 이펙터 세포를 모집하는 것을 돕는 사이토카인 생산(Il-4,IL-9)이 포함됩니다.
진단.
- CDC에 따르면 대변 검체 내 생물 표면에서 항원을 검출하는 것은 현재 지아다증 진단을 위한 선택 사항으로 보다 일반적인 현미경 [34]검사 기술에 비해 높은 민감도를 제공한다.
- 보존 변의 트리크롬 얼룩도 [35]지아디아를 검출하기 위해 사용되는 방법입니다.
- 진단을 [1]위해 대변의 현미경 검사를 수행할 수 있습니다.그러나 감염된 [1]호스트에서 영양소와 낭종이 일관되지 않기 때문에 이 방법은 권장되지 않습니다.일정 기간(일반적으로 1주일) 동안 여러 샘플을 [1]검사해야 합니다.
- 장내 테스트는 실이 부착된 젤라틴 캡슐을 사용합니다.한쪽 끝이 숙주의 뺨 안쪽에 부착되어 캡슐을 삼킵니다.그 후, 실을 식염수로 빼내 흔들면, 현미경으로 검출할 수 있는 영양소가 방출된다.그러나 이 테스트의 민감도는 낮으며 [36]진단에 일상적으로 사용되지 않습니다.
- 진단에는 [37]면역효소연계면역흡수검사(ELISA)를 사용할 수 있다.이러한 테스트에서는,[37] 검출율이 90%이상이 됩니다.
수소 호흡 검사에서 점근적으로 감염된 사람들의 탄수화물 흡수율이 낮은 것으로 나타났지만,[38] 그러한 검사들은 감염을 진단하지 않는다.혈청 검사는 [1]진단에 도움이 되지 않는다.
예방
CDC는 손 씻기를 권장하며 잠재적으로 오염된 식품과 처리되지 않은 [39]물을 피할 것을 권장합니다.
지아디아에 오염된 끓는 물은 감염성 [40]낭종을 효과적으로 죽인다.화학 소독제 또는 필터를 사용할 [41][42]수 있습니다.염소는 [43][44]낭종 파괴에 효과가 없기 때문에 염화보다는 요오드계 살균제가 선호된다.
비록 북미의 황야에서 물을 마시는 것과 지아디아증을 연관짓는 증거가 의문시되고 있지만,[45] 많은 연구들이 우려를 제기하고 있다.CDC에서 확인된 오지 지아다증 발병은 대부분 물에 기인한다.감시 데이터(2013년과 2014년)에 따르면 강, 하천 또는[46] 샘에서 6건의 수인성 지아다증 발병(96건)이 보고되었으며 보고된 지아다증 발병 건수의 1% 미만이 [47]발병과 관련이 있다.
개인 대 개인 전염은 Giardia 감염의 대부분을 차지하며, 보통 위생 및 위생 상태가 좋지 않습니다.지아디아는 땅 표면, 흙, 덜 익은 음식, 물, 그리고 감염된 [48]대변을 처리한 후 제대로 세척하지 않은 손에 자주 발견된다.수인성 전염은 오염된 물의 섭취와 관련이 있다.미국에서는 일반적으로 처리되지 않은 지표수를 사용하는 소규모 물 시스템에서 발병한다.성병은 분변-구강 오염을 통해 발생한다.또한 기저귀 교환과 부적절한 손 씻기는 감염된 어린이로부터 전염되는 위험 요소이다.마지막으로, Giardia의 음식 매개 전염병은 감염된 음식 [49]취급자들에 의한 음식 오염으로 발전했다.
백신
아직 인간을 위한 백신은 없지만, 개발 중인 백신 후보가 몇 개 있다.그들은 재조합 단백질, DNA 백신, 변이체 특이 표면 단백질, 낭포벽 단백질, 지아딘, [50]효소 등을 목표로 하고 있다.
현재 시판되고 있는 백신은 G. 람블리아 전트로포조이트 용해물로 제조된 GiardiaVax입니다.개와 고양이에게만 사용하는 수의용 백신입니다.GiardiaVax는 특정 [51]항체의 생산을 촉진해야 한다.
치료
감염은 대개 [7]저절로 해결되기 때문에 치료가 항상 필요한 것은 아니다.단, 급성 질환이거나 증상이 지속되어 치료를 위해 약물이 필요한 경우에는 메트로니다졸, 티니다졸, 세크니다졸 또는 오르니다졸 [9]등의 니트로이미다졸 약물을 사용한다.
세계보건기구와 미국감염병학회는 메트로니다졸을 1차 [52][53]치료제로 추천한다.미국 CDC효과적인 일선의 치료법으로서, 이 세[54], 오직 숲과 tinidazolenitazoxanide 편모충증의 미국 FDA.[55][56][57]에 의한 메타 분석이 Cochrane은 공동 작업에 의해 행해진은 메트로니다졸의 표준으로, 비교 albendazole equivale 것으로 치료를 위해 승인된다 메트로니다졸, tinidazole, nitazoxanide을 나열합니다.nt 효능 whi위장관이나 신경학적 [58]문제와 같은 부작용이 적은 le.다른 메타분석들도 비슷한 [59]결론에 도달했다.두 약 모두 5일에서 10일의 긴 과정이 필요하다; 알벤다졸은 하루에 한 번 복용하는 반면 메트로니다졸은 하루에 세 번 복용해야 한다.메트로니다졸을 메벤다졸, 티니다졸 또는 니타조옥사니드와 같은 다른 대안과 비교한 증거는 매우 낮은 [58]품질로 느껴졌다.티니다졸은 메트로니다졸과 유사한 부작용과 효능이 있지만, 1회 [20]투여로 투여된다.
니트로이미다졸과 알벤다졸에 대한 내성은 임상적으로 관찰되었지만 [21][60]니타조옥사니드는 관찰되지 않았다.이 모든 약물에 대한 내성의 정확한 메커니즘은 [60]잘 알려져 있지 않다.지아디아 내니트로이미다졸 균주의 경우 키나크린, 니타목산화물, 바시트라신 아연, 후라졸리돈, 파로모마이신 [20]등 치료에 효과가 있는 다른 약물을 이용할 수 있다.메파크린은 내화물 [21]케이스에도 사용될 수 있다.
프로바이오틱스는 표준 치료제와 함께 투여될 때 Giardia의 [61]청결을 돕는 것으로 나타났다.
임신 중에는 장내 흡수가 잘 되지 않아 [62]태아에 대한 노출이 적기 때문에 파로마이신이 선호되는 치료약이다.또는 임신 [20][63]중 트리코모나스에 대한 사용 경험이 풍부하기 때문에 임신 후 메트로니다졸을 사용할 수 있다.
예후
면역체계가 제대로 기능하는 사람들에게서, 감염은 [7]약물 없이도 해결될 수 있다.그러나 일부만 만성 [7]감염이 발생한다.면역체계가 손상된 사람들은 만성 [7]감염의 위험이 더 높다.약물 내성이 증가하고 있지만,[1][64][21] 약은 거의 모든 사람들에게 효과적인 치료법이다.
만성 지아다증을 앓고 있는 아이들은 성장 [65]장애와 같은 더 오래 지속되는 후유증을 겪을 위험이 있다.감염자의 절반까지 만성 [1]감염을 모방할 수 있는 일시적인 유당불내증이 나타난다.감염이 진정된 후에 [7]감염 후 과민성 대장 증후군을 경험하는 사람도 있다.Giardiasis는 또한 음식 [7]알레르기의 발병과 관련이 있다.이것은 장 [7]투과성에 대한 영향 때문인 것으로 생각된다.
역학
일부 개발도상국에서는 [16]Giardia가 인구의 30%에 존재합니다.미국에서는 인구의 3~[16]7%에 존재하는 것으로 추정된다.
2018년 미국에서 보고된 환자 수는 15,[66]584명이다.Giardias를 알림 질환으로 분류하는 모든 주에서 Giardias가 [66]발생했습니다.일리노이주, 켄터키주, 미시시피주, 노스캐롤라이나주, 오클라호마주, 테네시주, 텍사스주, 버몬트주는 2018년 [66]질병통제센터에 통보하지 않았다.2018년에 가장 많은 환자가 발생한 주는 캘리포니아, 뉴욕, 플로리다, [66]위스콘신이었다.지아다증과 [67]관련된 계절적 유행이 있다.7월, 8월, 9월은 미국에서 [68]지아다증 발생률이 가장 높은 달이다.
2014년 데이터를 포함하는 ECDC(European Center for Disease Prevention Control) 연례 역학 보고서에서 EU/EEA [69]회원국인 31개국 중 23개국이 확인된 지아다증 환자를 17,278명 보고했다.독일이 [69]4011건으로 가장 많았다.독일에 이어 영국에서도 3,628명의 지아다증 환자가 발생했다고 보고했습니다.전체 신고 건수의 [69]44%를 차지합니다.
조사.
일부 장내 기생충 감염은 과민성 대장[70] 증후군과 만성 피로 [71][72]증후군과 같은 다른 장기 후유증에 영향을 미칠 수 있다.낭종에서 영양소로 전환되는 메커니즘은 특성화되지[8] 않았지만 치료 내성이 있는 Giardia에 대한 약물 표적 개발에 도움이 될 수 있다.Giardia와 숙주 면역, 내부 식물군 및 기타 병원체 사이의 상호작용은 [7]잘 알려져 있지 않다.
Giardias에 대한 주요 회의는 "국제 Giardia and Cryptosporidium 회의"이다.최신판(2019, 프랑스 루앙)에 제시된 결과의 요약을 이용할 [73]수 있다.
기타 동물
개와 고양이 둘 다에서, 지아디아스는 보통 메트로니다졸과 펜벤다졸에 반응합니다.임신한 고양이의 메트로니다졸은 발육 [74]기형을 일으킬 수 있다.많은 고양이들은 페벤다졸의 [74]맛을 싫어한다.자르디아증은 가축의 [7]체중을 감소시키는 것으로 나타났다.
레퍼런스
- ^ a b c d e f g h i j k l m n o p q r s t u v w x y z aa ab ac Minetti C, Chalmers RM, Beeching NJ, Probert C, Lamden K (October 2016). "Giardiasis" (PDF). BMJ. 355: i5369. doi:10.1136/bmj.i5369. PMID 27789441. S2CID 220092781.
- ^ "Giardia. General information". CDC. 21 July 2015. Archived from the original on 17 November 2016. Retrieved 17 November 2016.
- ^ a b c Esch KJ, Petersen CA (January 2013). "Transmission and epidemiology of zoonotic protozoal diseases of companion animals". Clinical Microbiology Reviews. 26 (1): 58–85. doi:10.1128/CMR.00067-12. PMC 3553666. PMID 23297259.
- ^ a b c d e "Giardia. Illness and symptoms". CDC. 26 February 2021. Retrieved 27 March 2022.
- ^ a b c "Giardiasis". cdc.gov. December 9, 2017. Archived from the original on April 14, 2021. Retrieved 27 March 2022.
- ^ a b "Giardiasis (beaver fever)". New York State Department of Health. January 2022. Archived from the original on 20 January 2022. Retrieved 27 March 2022.
- ^ a b c d e f g h i j k l m n o p Cotton JA, Beatty JK, Buret AG (August 2011). "Host parasite interactions and pathophysiology in Giardia infections". International Journal for Parasitology. 41 (9): 925–33. doi:10.1016/j.ijpara.2011.05.002. PMID 21683702.
- ^ a b c d e Einarsson E, Ma'ayeh S, Svärd SG (December 2016). "An up-date on Giardia and giardiasis". Current Opinion in Microbiology. 34: 47–52. doi:10.1016/j.mib.2016.07.019. PMID 27501461.
- ^ a b c d Barry MA, Weatherhead JE, Hotez PJ, Woc-Colburn L (April 2013). "Childhood parasitic infections endemic to the United States". Pediatric Clinics of North America. 60 (2): 471–85. doi:10.1016/j.pcl.2012.12.011. PMID 23481112.
- ^ a b c d e f Despommier DD, Griffin DO, Gwadz RW, Hotez PJ, Knirsch CA. "III. Eukaryotic Parasites". Parasitic Diseases (6 ed.). NY: Parasites Without Borders. pp. 11–17. Archived from the original on 7 March 2020. Retrieved 11 July 2018.
- ^ a b c Robertson LJ, Hanevik K, Escobedo AA, Mørch K, Langeland N (February 2010). "Giardiasis--why do the symptoms sometimes never stop?". Trends in Parasitology. 26 (2): 75–82. doi:10.1016/j.pt.2009.11.010. PMID 20056486.
- ^ Guerrant, Richard L.; Walker, David H.; Weller, Peter F. (2011). Tropical infectious diseases : principles, pathogens and practice (3rd ed.). Edinburgh: Saunders/Elsevier. pp. 623. ISBN 9781437737776. OCLC 722800379.
- ^ Pettoello Mantovani M, Guandalini S, Ecuba P, Corvino C, di Martino L (October 1989). "Lactose malabsorption in children with symptomatic Giardia lamblia infection: feasibility of yogurt supplementation". Journal of Pediatric Gastroenterology and Nutrition. 9 (3): 295–300. doi:10.1097/00005176-198910000-00006. PMID 2614615. S2CID 32254397.
- ^ Wolfe MS (September 1975). "Giardiasis". JAMA. 233 (13): 1362–5. doi:10.1001/jama.233.13.1362. PMID 1174208.
- ^ Vega-Franco L, Meza C, Romero JL, Alanis SE, Meijerink J (1987). "Breath hydrogen test in children with giardiasis". Journal of Pediatric Gastroenterology and Nutrition. 6 (3): 365–8. doi:10.1097/00005176-198705000-00010. PMID 3430245. S2CID 20733304.
- ^ a b c d e f g Auerbach, Paul S. (2012). Wilderness medicine (6th ed.). Philadelphia, PA: Elsevier/Mosby. pp. Chapter 68. ISBN 9781437716788.
- ^ a b Heyworth MF (2016). "Giardia duodenalis genetic assemblages and hosts". Parasite. 23: 13. doi:10.1051/parasite/2016013. PMC 4794627. PMID 26984116. Archived from the original on 2017-09-10.

- ^ Lalle M, Hanevik K (2018-10-24). "Treatment-refractory giardiasis: challenges and solutions". Infection and Drug Resistance. 11: 1921–1933. doi:10.2147/idr.s141468. PMC 6207226. PMID 30498364.
- ^ CDC (July 15, 2015). "Sources of Infection & Risk Factors". Parasites – Giardia. Archived from the original on September 7, 2017.
- ^ a b c d e Gardner TB, Hill DR (January 2001). "Treatment of giardiasis". Clinical Microbiology Reviews. 14 (1): 114–28. doi:10.1128/CMR.14.1.114-128.2001. PMC 88965. PMID 11148005.
- ^ a b c d Carter ER, Nabarro LE, Hedley L, Chiodini PL (January 2018). "Nitroimidazole-refractory giardiasis: a growing problem requiring rational solutions". Clinical Microbiology and Infection. 24 (1): 37–42. doi:10.1016/j.cmi.2017.05.028. PMID 28624613.
- ^ a b c d e f Buret AG (September 2008). "Pathophysiology of enteric infections with Giardia duodenalius". Parasite. 15 (3): 261–5. doi:10.1051/parasite/2008153261. PMID 18814692.
- ^ Bartelt LA, Sartor RB (2015-05-26). "Advances in understanding Giardia: determinants and mechanisms of chronic sequelae". F1000Prime Reports. 7 (62): 62. doi:10.12703/P7-62. PMC 4447054. PMID 26097735.
- ^ Muhkerjee, Sandeep. "Giardiasis". Medscape Reference. Archived from the original on 17 November 2012. Retrieved 21 November 2012.
- ^ Eckmann, Lars (May 2003). "Mucosal defences against Giardia". Parasite Immunology. 25 (5): 259–270. doi:10.1046/j.1365-3024.2003.00634.x. ISSN 0141-9838. PMID 12969444. S2CID 7155680.
- ^ Thompson, R. C. Andrew (July 2011). "Giardia infections". Oxford Medicine Online. doi:10.1093/med/9780198570028.003.0052. ISBN 978-0-19-969782-3.
- ^ Eckmann, Lars; Laurent, Fabrice; Langford, T. Dianne; Hetsko, Michael L.; Smith, Jennifer R.; Kagnoff, Martin F.; Gillin, Frances D. (2000-02-01). "Nitric Oxide Production by Human Intestinal Epithelial Cells and Competition for Arginine as Potential Determinants of Host Defense Against the Lumen-Dwelling PathogenGiardia lamblia". The Journal of Immunology. 164 (3): 1478–1487. doi:10.4049/jimmunol.164.3.1478. ISSN 0022-1767. PMID 10640765.
- ^ Li, Erqiu; Zhou, Ping; Singer, Steven M. (2005-12-19). "Neuronal Nitric Oxide Synthase Is Necessary for Elimination of Giardia lamblia Infections in Mice". The Journal of Immunology. 176 (1): 516–521. doi:10.4049/jimmunol.176.1.516. ISSN 0022-1767. PMC 2585514. PMID 16365445.
- ^ Evans-Osses, Ingrid; Ansa-Addo, Ephraim A.; Inal, Jameel M.; Ramirez, Marcel I. (May 2010). "Involvement of lectin pathway activation in the complement killing of Giardia intestinalis". Biochemical and Biophysical Research Communications. 395 (3): 382–386. doi:10.1016/j.bbrc.2010.04.025. ISSN 0006-291X. PMID 20382117.
- ^ Tellez, Aleyda; Winiecka-krusnell, Jadwiga; Paniagua, Margarita; Linder, Ewert (May 2003). "Antibodies in Mother's Milk Protect Children Against Giardiasis". Scandinavian Journal of Infectious Diseases. 35 (5): 322–325. doi:10.1080/00365540310008041. ISSN 0036-5548. PMID 12875519. S2CID 12621232.
- ^ a b Singer, Steven M.; Nash, Theodore E. (2000-01-01). "T-Cell-Dependent Control of Acute Giardia lamblia Infections in Mice". Infection and Immunity. 68 (1): 170–175. doi:10.1128/iai.68.1.170-175.2000. ISSN 1098-5522. PMC 97117. PMID 10603384.
- ^ Scott, Kevin G.-E.; Yu, Linda C. H.; Buret, André G. (June 2004). "Role of CD8+ and CD4+ T Lymphocytes in Jejunal Mucosal Injury during Murine Giardiasis". Infection and Immunity. 72 (6): 3536–3542. doi:10.1128/iai.72.6.3536-3542.2004. ISSN 0019-9567. PMC 415705. PMID 15155662.
- ^ Kalas MA, Alduaij A, Alkhatib AA (2021). "Incidental Diagnosis of Duodenal Giardiasis". Cureus. 13 (6): e15499. doi:10.7759/cureus.15499. PMC 8262110. PMID 34268030.
{{cite journal}}: CS1 maint: 여러 이름: 작성자 목록(링크)
- "Creative Commons Attribution License CC-BY 4.0 조건에 따라 배포되는 오픈 액세스 기사입니다." - ^ "Stool Specimens - Detection of Parasite Antigens". CDC. Archived from the original on 2017-06-17. Retrieved 2017-09-09.
- ^ "Ova and Parasite Exam, Fecal (Immunocompromised or Travel History)". Archived from the original on 2014-10-29. Retrieved 2014-10-29.
- ^ Hooshyar H, Rostamkhani P, Arbabi M, Delavari M (2019). "Giardia lamblia infection: review of current diagnostic strategies". Gastroenterology and Hepatology from Bed to Bench. 12 (1): 3–12. PMC 6441489. PMID 30949313.
- ^ a b Rosenblatt JE, Sloan LM, Schneider SK (May–June 1993). "Evaluation of an enzyme-linked immunosorbent assay for the detection of Giardia lamblia in stool specimens". Diagnostic Microbiology and Infectious Disease. 16 (4): 337–41. doi:10.1016/0732-8893(93)90086-M. PMID 8495591.
- ^ Moya-Camarena SY, Sotelo N, Valencia ME (March 2002). "Effects of asymptomatic Giardia intestinalis infection on carbohydrate absorption in well-nourished Mexican children". The American Journal of Tropical Medicine and Hygiene. 66 (3): 255–9. doi:10.4269/ajtmh.2002.66.255. PMID 12139217.
- ^ "Parasites - Giardia, Prevention & Control". Centers for Disease Control and Prevention. CDC. Archived from the original on 30 April 2015. Retrieved 26 April 2015.
- ^ "Emergency Disinfection of Drinking Water". United States Environment Protection Agency. 2013-02-20. Archived from the original on 23 June 2015. Retrieved 21 June 2015. 2011년 2월 24일 취득
- ^ Betancourt WQ, Rose JB (December 2004). "Drinking water treatment processes for removal of Cryptosporidium and Giardia". Veterinary Parasitology. 126 (1–2): 219–34. doi:10.1016/j.vetpar.2004.09.002. PMID 15567586.
- ^ Exner M, Gornik V (July 2004). "[Parasitic zoonoses transmitted by drinking water. Giardiasis and cryptosporidiosis]". Bundesgesundheitsblatt, Gesundheitsforschung, Gesundheitsschutz. 47 (7): 698–704. doi:10.1007/s00103-004-0863-y. PMID 15254826.
- ^ Dunn, Noel; Juergens, Andrew L. (2019), "Giardiasis", StatPearls, StatPearls Publishing, PMID 30020611, retrieved 2019-10-31
- ^ Ongerth JE, Johnson RL, Macdonald SC, Frost F, Stibbs HH (December 1989). "Back-country water treatment to prevent giardiasis". American Journal of Public Health. 79 (12): 1633–7. doi:10.2105/ajph.79.12.1633. PMC 1349767. PMID 2817191.
- ^ Julia E. Painter, PhD; Julia W. Gargano, PhD; Sarah A. Collier, MPH; Jonathan S. Yoder, MPH (2015). "Giardiasis Surveillance—United States, 2011–2012". MMWR Supplements. 64 (Suppl 3): 15–25. PMID 25928582. Retrieved 31 March 2018.
- ^ McClung RP, Roth DM, Vigar M, Roberts VA, Kahler AM, Cooley LA, et al. (November 2017). "Waterborne Disease Outbreaks Associated With Environmental and Undetermined Exposures to Water - United States, 2013-2014". MMWR. Morbidity and Mortality Weekly Report. 66 (44): 1222–1225. doi:10.15585/mmwr.mm6644a4. PMC 5679586. PMID 29120997.
- ^ "Giardiasis Surveillance — United States, 2009–2010". www.cdc.gov.
- ^ CDC Giardia 2011
- ^ eMedicine의 Giardiasis
- ^ Davids, Barbara J.; Liu, Ching M.; Hanson, Elaine M.; Le, Christine H. Y.; Ang, Jonathan; Hanevik, Kurt; Fischer, Marvin; Radunovic, Matej; Langeland, Nina; Ferella, Marcela; Svärd, Staffan G. (2019-04-08). "Identification of Conserved Candidate Vaccine Antigens in the Surface Proteome of Giardia lamblia". Infection and Immunity. 87 (6). doi:10.1128/iai.00219-19. ISSN 0019-9567. PMC 6529650. PMID 30962402.
- ^ Palatnik-de-Sousa, CB; Nico, D (2020). "The Delay in the Licensing of Protozoal Vaccines: A Comparative History". Frontiers in Immunology. 11: 204. doi:10.3389/fimmu.2020.00204. PMC 7068796. PMID 32210953.
- ^ Guerrant RL, Van Gilder T, Steiner TS, Thielman NM, Slutsker L, Tauxe RV, et al. (February 2001). "Practice guidelines for the management of infectious diarrhea" (PDF). Clinical Infectious Diseases. 32 (3): 331–51. doi:10.1086/318514. PMID 11170940. Archived (PDF) from the original on February 10, 2016.
- ^ "Chapter 7.5.4 Continuing Diarrhoea ICHRC". www.ichrc.org. Archived from the original on 2016-01-29. Retrieved 2016-01-09.
- ^ "Giardia: Treatment". United States Centers for Disease Control and Prevention. 21 July 2015. Archived from the original on 24 December 2015. Retrieved 10 January 2016.
Several drugs can be used to treat Giardia infection. Effective treatments include metronidazole, tinidazole, and nitazoxanide1. Alternatives to these medications include paromomycin, quinacrine, and furazolidone1,2.
- ^ "Nitazoxanide Prescribing Information" (PDF). Romark Pharmaceuticals. August 2013. pp. 1–5. Archived from the original (PDF) on 16 January 2016. Retrieved 3 January 2016.
- ^ "Metronidazole Prescribing Information" (PDF). United States Food and Drug Administration. Pfizer. June 2015. pp. 6–7. Archived (PDF) from the original on 4 March 2016. Retrieved 10 January 2016.
- ^ "Tinidazole Prescribing Informatiuon" (PDF). United States Food and Drug Administration. Mission Pharma. May 2007. p. 1. Archived (PDF) from the original on 4 March 2016. Retrieved 10 January 2016.
- ^ a b Granados CE, Reveiz L, Uribe LG, Criollo CP (December 2012). "Drugs for treating giardiasis". The Cochrane Database of Systematic Reviews. 12: CD007787. doi:10.1002/14651858.cd007787.pub2. PMC 6532677. PMID 23235648.
- ^ Solaymani-Mohammadi S, Genkinger JM, Loffredo CA, Singer SM (May 2010). Keiser J (ed.). "A meta-analysis of the effectiveness of albendazole compared with metronidazole as treatments for infections with Giardia duodenalis". PLOS Neglected Tropical Diseases. 4 (5): e682. doi:10.1371/journal.pntd.0000682. PMC 2867942. PMID 20485492.
- ^ a b Leitsch D (2015-07-07). "Giardia lamblia". Current Tropical Medicine Reports. 2 (3): 128–135. doi:10.1007/s40475-015-0051-1. PMC 4523694. PMID 26258002.
- ^ Lalle, Marco; Hanevik, Kurt (2018-10-24). "Treatment-refractory giardiasis: challenges and solutions". Infection and Drug Resistance. 11: 1921–1933. doi:10.2147/IDR.S141468. ISSN 1178-6973. PMC 6207226. PMID 30498364.
- ^ Farthing MJ (August 2006). "Treatment options for the eradication of intestinal protozoa". Nature Clinical Practice. Gastroenterology & Hepatology. 3 (8): 436–45. doi:10.1038/ncpgasthep0557. PMID 16883348. S2CID 19657328.
- ^ Workowski KA, Bolan GA (June 2015). "Sexually transmitted diseases treatment guidelines, 2015". MMWR. Recommendations and Reports. 64 (RR-03): 1–137. PMC 5885289. PMID 26042815.
- ^ Kasper, Dennis L.; Larry Jameson, J.; Hauser, Stephen L.; Loscalzo, Joseph; Fauci, Anthony S.; Longo, Dan L. (2015-04-08). Harrison's principles of internal medicine. Kasper, Dennis L.,, Fauci, Anthony S., 1940-, Hauser, Stephen L.,, Longo, Dan L. (Dan Louis), 1949-, Jameson, J. Larry,, Loscalzo, Joseph (19th ed.). New York. ISBN 9780071802154. OCLC 893557976.
- ^ Donowitz JR, Alam M, Kabir M, Ma JZ, Nazib F, Platts-Mills JA, et al. (September 2016). "A Prospective Longitudinal Cohort to Investigate the Effects of Early Life Giardiasis on Growth and All Cause Diarrhea". Clinical Infectious Diseases. 63 (6): 792–7. doi:10.1093/cid/ciw391. PMC 4996141. PMID 27313261.
- ^ a b c d "TABLE 2f. Annual reported cases of notifiable diseases, by region and reporting area - - United States and U.S. Territories, 2018". wonder.cdc.gov. Retrieved 2019-11-13.
- ^ Painter, Julia E.; Gargano, Julia W.; Collier, Sarah A.; Yoder, Jonathan S. (2015-05-01). "Giardiasis surveillance -- United States, 2011-2012". MMWR Supplements. 64 (3): 15–25. ISSN 2380-8942. PMID 25928582.
- ^ Jonathan S. Yoder, MPH; Julia W. Gargano, PhD; Ryan M. Wallace, DVM; Michael J. Beach, PhD (2012). "Giardiasis Surveillance-United States, 2009-2010". Morbidity and Mortality Weekly Report. Surveillance Summaries. Centers of Disease Control and Prevention. 61 (5): 13–23. PMID 22951494. Retrieved 30 November 2017.
- ^ a b c "Giardiasis- Annual Epidemiological Report 2016". European Centre for Disease Prevention and Control. European Centre for Disease Prevention and Control. 2017-01-30. Retrieved 30 November 2017.
- ^ Stark D, van Hal S, Marriott D, Ellis J, Harkness J (January 2007). "Irritable bowel syndrome: a review on the role of intestinal protozoa and the importance of their detection and diagnosis". International Journal for Parasitology. 37 (1): 11–20. doi:10.1016/j.ijpara.2006.09.009. PMID 17070814.
- ^ Hanevik K, Wensaas KA, Rortveit G, Eide GE, Mørch K, Langeland N (November 2014). "Irritable bowel syndrome and chronic fatigue 6 years after giardia infection: a controlled prospective cohort study". Clinical Infectious Diseases. 59 (10): 1394–400. doi:10.1093/cid/ciu629. PMC 4207419. PMID 25115874.
- ^ 인용: "불명한 이유로, 감염 후 과민성 대장 증후군, 만성 피로[..], 영양실조, 인지장애[..] 및 장외 증상(음식 알레르기, 두드러기, 반응성 관절염, 염증성 안구 증상 등)을 포함한 만성 후유증이 발생할 수 있으며, 발견 가능한 범위를 넘어 지속될 수 있다.아라사이트 배출"을 참조하십시오.인용처:
- ^ Buret, André G.; Cacciò, Simone M.; Favennec, Loïc; Svärd, Staffan (2020). "Update on Giardia: Highlights from the seventh International Giardia and Cryptosporidium Conference". Parasite. 27: 49. doi:10.1051/parasite/2020047. ISSN 1776-1042. PMC 7425178. PMID 32788035.

- ^ a b Eldredge, Debra M. (2008). Cat Owner's Home Veterinary Handbook. Howell Book House. p. 67.





