RTI-55
RTI-55 | |
| 임상자료 | |
|---|---|
| 기타 이름 | (–--2β-카르보메트호익시-3β-(4-iodophyl)트로판, β-CIT, 이오메토판 I 123(USAN), 이오메토판 I(INN), 이오메토판 I 125(USAN), 이오메탄 I(IN) |
| 법적현황 | |
| 법적현황 |
|
| 식별자 | |
| |
| CAS 번호 | |
| 펍켐 CID | |
| 유니 | |
| 화학 및 물리적 데이터 | |
| 공식 | C16H20INO2 |
| 어금질량 | 385.1987 g·190−1 |
| 3D 모델(JSmol) | |
| |
| (iii) | |
RTI(-4229)-55는 RTI-55 또는 아이오메토판이라고도 하며, 과학 연구와 일부 의학적 용도에 사용되는 페닐트로판 기반의 정신안정제다. 이 약은 1991년에 처음 인용되었다.[1] RTI-55는 메틸레코니딘에서 파생된 비선택적 도파민 재흡수 억제제다. 그러나, 예를 들어, 보다 선택적인 아날로그는 "피롤리디노아미도" RTI-229로 변환함으로써 도출된다. 약하게 전자가 이오도 할로겐 원자를 빼내는 큰 전구 특성 때문에 RTI-55는 단순 파라 대체 대류탄 기반 아날로그 중 세로토닌성이 가장 강하다.[2] 설치류에서 RTI-55는 실제로 100mg/kg 용량에서 사망을 유발한 반면, RTI-51과 RTI-31은 그렇지 않았다.[2] 또 다른 주목할 만한 관찰은 RTI-55가 기관차 활동 개선을 유발하는 강한 성향이라는 것이다.[2] 비록 이전 연구에서 RTI-51은 사실 기준 LMA 이동에서 RTI-55보다 더 강했다.[3] 이 관찰은 연구 사이에 발생할 수 있는 불균형을 부각시키는 역할을 한다.
RTI-55는 엄격하게 통제되는 의료 환경 밖에서 사용할 경우 상당한 남용 가능성을 가질 수 있기 때문에 상업적으로 이용 가능한 가장 강력한 페닐트로판 자극제 중 하나이다.[4] 그러나, 트로파릴에 부착된 할로겐 원자의 크기를 증가시키는 것은 연구에서 이러한 아날로그를 비교했을 때 세션에서 레버 반응의 수를 감소시키는 역할을 한다는 것은 분명히 언급할 가치가 있다.[5] RTI-55가 본 연구에서 구체적으로 조사되지는 않았지만, 주어진 세션에서 레버 응답의 수는 코카인 > WIN35428 > RTI-31 > RTI-51의 순서였다.
주로 도파민성인 RTI-31과 대조적으로, 공동 결합 할로겐의 크기를 염소에서 요오드로 증가시키면 SERT에 대한 친화력이 현저하게 증가하는 반면, 대부분의 DAT 차단 활동은 유지된다.
요오드 원자가 방사성 요오드인 RTI-55의 방사선 의약품 형태는 단광방사선 방출 컴퓨터 단층촬영에 약물을 사용할 수 있도록 하는 것으로, iometopane I 123(USAN) 또는 iometopane I(INN)과 iometopane I 125(USAN) 또는 iometopane I(INN)이라고 한다. I와 I 동위원소는 매우 높은 에너지 γ선 방출체이기 때문에 선호된다.
"WIN" 화합물에 비해 극히 낮은 Ki 값을 달성할 수 있다.
사용하다
RTI-55는 주로 도파민 재흡수 전달체에 대한 과학적 연구에 사용된다. RTI-55의 다양한 방사성 동위원소 형태(응용도에 따라 사용되는 요오드의 방사성 동위원소가 서로 다른 것)는 사람과 동물 모두에서 도파민 전달체와 세로토닌 전달체의 뇌 분포를 지도화하는 데 사용된다.[6][7] I파생물은 아이오메토판이라고 알려져 있다.
의학에서 이 약의 주된 실용적 적용은 파킨슨병 환자의 뇌의 도파민 뉴런 저하율과 [8][9]진행성 핵성마비 같은 다른 조건들을 평가하는 것이다.[10]
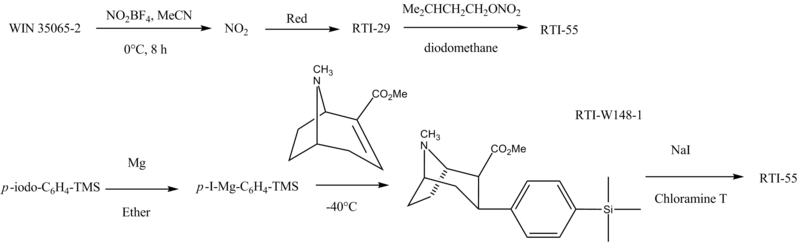
화학
RTI-55는 다음과 같이 제작된다.[11][12][13]
참고 항목
참조
- ^ Boja JW, Patel A, Carroll FI, Rahman MA, Philip A, Lewin AH, et al. (February 1991). "[125I]RTI-55: a potent ligand for dopamine transporters". European Journal of Pharmacology. 194 (1): 133–4. doi:10.1016/0014-2999(91)90137-F. PMID 2060590.
- ^ a b c Carroll FI, Runyon SP, Abraham P, Navarro H, Kuhar MJ, Pollard GT, Howard JL (December 2004). "Monoamine transporter binding, locomotor activity, and drug discrimination properties of 3-(4-substituted-phenyl)tropane-2-carboxylic acid methyl ester isomers". Journal of Medicinal Chemistry. 47 (25): 6401–9. doi:10.1021/jm0401311. PMID 15566309.
- ^ Kimmel HL, Carroll FI, Kuhar MJ (December 2001). "Locomotor stimulant effects of novel phenyltropanes in the mouse". Drug and Alcohol Dependence. 65 (1): 25–36. doi:10.1016/S0376-8716(01)00144-2. PMID 11714587.
- ^ Weed MR, Mackevicius AS, Kebabian J, Woolverton WL (August 1995). "Reinforcing and discriminative stimulus effects of beta-CIT in rhesus monkeys". Pharmacology, Biochemistry, and Behavior. 51 (4): 953–6. doi:10.1016/0091-3057(95)00032-r. PMID 7675883. S2CID 53215171.
- ^ Wee S, Carroll FI, Woolverton WL (February 2006). "A reduced rate of in vivo dopamine transporter binding is associated with lower relative reinforcing efficacy of stimulants". Neuropsychopharmacology. 31 (2): 351–62. doi:10.1038/sj.npp.1300795. PMID 15957006.
- ^ Shaya EK, Scheffel U, Dannals RF, Ricaurte GA, Carroll FI, Wagner HN, et al. (February 1992). "In vivo imaging of dopamine reuptake sites in the primate brain using single photon emission computed tomography (SPECT) and iodine-123 labeled RTI-55". Synapse. 10 (2): 169–72. doi:10.1002/syn.890100210. PMID 1585258. S2CID 38478862.
- ^ Shang Y, Gibbs MA, Marek GJ, Stiger T, Burstein AH, Marek K, et al. (February 2007). "Displacement of serotonin and dopamine transporters by venlafaxine extended release capsule at steady state: a [123I]2beta-carbomethoxy-3beta-(4-iodophenyl)-tropane single photon emission computed tomography imaging study". Journal of Clinical Psychopharmacology. 27 (1): 71–5. doi:10.1097/JCP.0b013e31802e0017. PMID 17224717. S2CID 25239273.
- ^ Staffen W, Mair A, Unterrainer J, Trinka E, Bsteh C, Ladurner G (May 2000). "[123I] beta-CIT binding and SPET compared with clinical diagnosis in parkinsonism". Nuclear Medicine Communications. 21 (5): 417–24. doi:10.1097/00006231-200005000-00002. PMID 10874697.
- ^ Zubal IG, Early M, Yuan O, Jennings D, Marek K, Seibyl JP (June 2007). "Optimized, automated striatal uptake analysis applied to SPECT brain scans of Parkinson's disease patients". Journal of Nuclear Medicine. 48 (6): 857–64. doi:10.2967/jnumed.106.037432. PMID 17504864.
- ^ Seppi K, Scherfler C, Donnemiller E, Virgolini I, Schocke MF, Goebel G, et al. (August 2006). "Topography of dopamine transporter availability in progressive supranuclear palsy: a voxelwise [123I]beta-CIT SPECT analysis". Archives of Neurology. 63 (8): 1154–60. doi:10.1001/archneur.63.8.1154. PMID 16908744.
- ^ 미국 특허 5,128,118
- ^ 미국 특허 6,123,917
- ^ Musachio JL, Keverline KI, Carroll FI, Dannals RF (January 1996). "3 Beta-(p-trimethylsilylphenyl)tropane-2 beta-carboxylic acid methyl ester: a new precursor for the preparation of [123I]RTI-55". Applied Radiation and Isotopes. 47 (1): 79–81. doi:10.1016/0969-8043(95)00259-6. PMID 8589674.