낭포성 섬유증
Cystic fibrosis| 낭포성 섬유증 | |
|---|---|
| 기타 이름 | 뮤코비스시도스 |
 | |
| 전문 | 의학유전학, 맥박학 |
| 증상 | 호흡곤란, 점액기침, 성장불량, 지방변[1] |
| 통상적인 개시 | 증상을 인식할 수 있는 기간은 최대 6개월[2] |
| 지속 | 장수[3] |
| 원인들 | 유전자(자염색체 열성)[1] |
| 위험요소 | 유전의 |
| 진단 방법 | 땀 검사, 유전자[1] 검사 |
| 치료 | 항생제, 췌장효소 대체, 폐 이식[1] |
| 예후 | 평균수명 42~50세(선진국)[4] |
| 빈도수. | 3,000분의 1(북유럽)[1] |
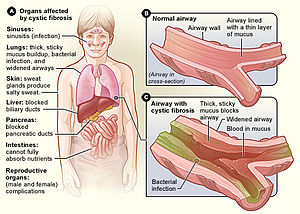
낭포성 섬유증은 대부분 폐뿐만 아니라 췌장, 간, 신장, [1][7]장에도 영향을 미치는 희귀한[5][6] 유전 질환이다.장기적인 문제로는 호흡곤란과 잦은 폐 [1]감염의 결과로 점액이 올라오는 것을 포함한다.다른 징후와 증상으로는 축농증, 성장 불량, 지방 대변, 손가락과 발가락의 몽둥이, 그리고 대부분의 [1]남성에서 불임이 있을 수 있습니다.사람마다 [1]증상의 정도가 다를 수 있습니다.
낭포성 섬유증은 상염색체 열성적으로 [1]유전된다.낭포성 섬유화 트랜스막 컨덕턴스 레귤레이터([1]CFTR) 단백질에 대한 유전자의 양쪽 복사본에 돌연변이가 존재하기 때문에 발생합니다.1개의 작업 복사본을 가지고 있는 것은 캐리어이며, 그 외에는 대부분 [3]정상입니다.CFTR은 땀, 소화액, [8]점액 생산에 관여한다.CFTR이 기능하지 않으면 보통 얇은 분비물이 [9]대신 두꺼워집니다.땀 검사와 유전자 [1]검사를 통해 상태를 진단합니다.출생 시 영유아 검진은 [1]세계 일부 지역에서 시행된다.
낭포성 섬유증의 [3]치료법은 알려져 있지 않다.폐 감염은 항생제로 치료되는데, 항생제는 정맥주사, 흡입주사 또는 [1]구강주사를 통해 투여될 수 있다.때로는 항생제인 아지트로마이신을 [1]장기간 사용하기도 한다.흡입된 하이퍼토닉 식염수와 살부타몰 또한 [1]유용할 수 있다.폐기능이 [1]계속 악화된다면 폐이식은 선택사항이 될 수 있다.췌장 효소 대체와 지용성 비타민 보충은 특히 [1]젊은이들에게 중요하다.흉부 물리치료와 같은 기도 청소 기술은 단기적인 이점이 있지만 장기적인 효과는 [10]불분명하다.선진국의 [4][11]평균 수명은 42세에서 50세 사이이다.낭포성 섬유증 [1]환자의 80%가 폐질환으로 사망에 책임이 있다.
CF는 북유럽계 사람들 사이에서 가장 흔하며 [1]신생아 3,000명 중 1명꼴로 발병한다.약 25명 중 1명이 [3]캐리어입니다.그것은 아프리카인들과 [1]아시아인들에게 가장 흔하지 않다.1938년 도로시 안데르센에 의해 특정 질병으로 처음 인정되었고, 적어도 1595년 [7]이전까지 그 조건에 맞는 기술이 있었다."낭포성 섬유증"이라는 이름은 [7][12]췌장 내에 형성되는 특징적인 섬유증과 낭종을 말합니다.
징후 및 증상
낭포성 섬유증은 일반적으로 젊었을 때 나타난다.낭포성 섬유증을 가진 신생아와 영아는 빈번하고 크고 기름진 변(흡수 불량으로 인한 결과)을 보이는 경향이 있으며 나이에 [13]비해 저체중이다. 신생아의 15~20%는 소장을 메코늄으로 막아서 종종 [13]교정을 위한 수술이 필요하다.신생아는 담관이 [13]막혀서 신생아 황달이 생기는 경우가 있다.낭포성 섬유증이 있는 아이는 땀으로 염분이 과다하게 손실되고, 부모가 아이에게 [13]키스할 때 피부에 염분이 결정화되거나 짠맛을 느끼는 경우가 많다.
낭포성 섬유증 환자의 질병과 사망의 주요 원인은 진행성 폐질환으로,[14] 결국 호흡부전으로 이어진다.이것은 일반적으로 항생제로 [14]치료될 때까지 계속되는 장기 호흡기 감염으로 시작된다.만성 호흡기 감염은 낭포성 섬유증 환자에게서 거의 보편적이며, Pseudomonas aeruginosa, 곰팡이, 마이코박테리아 모두 시간이 [15]지남에 따라 점점 더 흔해지고 있다.상기도에 염증이 생기면 콧물이 자주 나고 코막힘이 생긴다.코 용종은 특히 어린이와 [14]청소년들에게 흔하다.병이 진행되면서 숨이 가빠지고 [14]가래가 나오는 만성 기침이 생기기 쉽다.호흡 장애는 운동하는 것을 점점 더 어렵게 만들고, 장기간의 질병은 영향을 받는 사람들의 [14]나이에 비해 저체중을 야기한다.사춘기 후반이나 성인기에 사람들은 폐질환의 심각한 징후를 보이기 시작합니다: 헐떡임, 디지털 클럽, 청색증, 혈액 기침, 폐 심장병, 그리고 폐 붕괴.[14]
드물게 낭포성 섬유증은 응고 장애로 나타날 수 있다.비타민 K는 보통 모유, 조제분유, 그리고 나중에는 고형식품에서 흡수된다.이 흡수는 일부 CF 환자들에게서 손상되었다.어린 아이들은 매우 적은 양의 비타민 K만이 태반을 통과하기 때문에 특히 비타민 K 흡수 장애에 민감하며, 출생 후 식단에서 비타민 K를 흡수할 수 있는 매우 낮은 저장량과 제한적인 능력이 남아 있습니다.응고인자 II, VII, IX 및 X는 비타민 K에 의존하기 때문에 낮은 수준의 비타민 K는 응고 문제를 일으킬 수 있다.따라서 아이가 원인 불명의 멍이 있는 경우, 기초 질환이 존재하는지 여부를 판단하기 위한 응고 평가를 보증할 수 있다.[16]
폐와 부비강
폐질환은 점액 축적으로 인한 기도의 막힘, 점액담도 청소의 저하, 그리고 그에 따른 [17][18]염증으로 인해 발생한다.이후 단계에서 주요 기도의 병리(기관지 확장증)와 같은 폐 구조의 변화는 호흡 곤란을 더욱 악화시킨다.다른 징후로는 폐에 있는 고혈압, 심부전, 몸에 충분한 산소를 공급하기 어려운 것, 그리고 담즙 양기도압 기계나 [19]인공호흡기와 같은 호흡 마스크가 필요한 호흡 부전이 있다.황색포도상구균, 인플루엔자균, 황색포도상구균은 CF 환자의 [18]: 1254 폐 감염을 일으키는 가장 흔한 세 가지 유기체이다.또한 Burkholderia cepacia complex에 의한 기회성 감염, 특히 환자 간 전염이 발생할 수 있습니다.[20]
전형적인 박테리아 감염 외에도, CF를 가진 사람들은 다른 종류의 폐 질환에 더 많이 걸린다.이 중 대표적인 것이 알레르기성 기관지 폐 아스퍼길루스증인데, 아스퍼길루스 후미가투스에 대한 몸의 반응이 호흡곤란을 악화시킨다.다른 하나는 폐 손상을 일으킬 수 있고 일반적인 항생제에 [21]반응하지 않는 결핵과 관련된 박테리아 그룹인 마이코박테리움 아비움 콤플렉스 감염이다.
부비강 내 점액은 똑같이 두꺼우며 부비강 통로가 막혀 감염을 일으킬 수 있다.이것은 얼굴의 통증, 발열, 코의 배출, 그리고 두통을 일으킬 수 있다.CF를 가진 사람은 만성 부비강 [22]감염으로 인한 염증으로 인해 비강 조직(비강 용종)이 과도하게 성장할 수 있다.재발성 시노나살 용종은 CF환자의 [18]: 1254 10~25%에서 발생할 수 있다.이 용종은 비강을 막고 호흡 [23][24]곤란을 증가시킨다.
미국 [18]: 1254 대부분의 CF 센터에서 심폐 합병증이 환자의 가장 일반적인 사망 원인(약 80%)이다.
위장
또한 CF가 [18]있는 어린이의 10%에서 발생하는 내부 직장막의 돌출(직장탈출)은 더 흔하며,[25] 이는 기침으로 인한 분뇨량 증가, 영양실조, 복강내 압력 상승에 의해 발생한다.
폐에서 보이는 두꺼운 점액은 음식을 분해하는 데 도움을 주는 소화액을 공급하는 기관인 췌장에서 나오는 진화된 분비물에 대응합니다.이러한 분비물은 소화 효소의 십이지장으로의 외분비 운동을 차단하고 종종 고통스러운 염증을 [26]동반하는 췌장에 돌이킬 수 없는 손상을 초래합니다.췌관은 보통 더 나이가 많은 어린이나 [18]청소년들에게서 나타나는 더 발전된 케이스에 완전히 연결되어 있다.이것은 외분비선의 위축과 진행성 섬유화를 [18]일으킨다.
CF를 가진 사람들은 또한 지용성 비타민 A, D, E, [27]K를 흡수하는 데 어려움을 겪는다.
췌장 질환 외에도 CF가 있는 사람들은 속쓰림,[27] 장폐색, 변비 [28]등을 더 많이 경험한다.CF를 가진 나이든 사람들은 변이 점액으로 두꺼워질 때 발생하는 원위성 장폐색 증후군을 일으킬 수 있고, 붓기, 통증, 불완전하거나 완전한 [29][27]장폐색을 일으킬 수 있다.
외분비성 [18]: 1253 췌장부전증은 CF환자의 대다수(85~90%)에서 발생한다.이는 주로 양쪽 대립 유전자가 완전히 기능하지 않는 "심각한" CFTR 돌연변이와 관련이 있다(예: δF508/δF508).[18]: 1253 CFTR 활동이 거의 발생하지 않거나 두 개의 CFTR 돌연변이가 [18]: 1253 존재하는 경우 1개의 "심각한" CFTR 돌연변이와 1개의 "온화한" CFTR 돌연변이를 가진 환자의 10%에서 15%에서 발생한다.이러한 경도의 경우, 충분한 췌장 외분비 기능이 존재하기 때문에 효소 [18]: 1253 보충이 필요하지 않습니다.보통 췌장이 충분한 표현형에서는 다른 GI 합병증이 발생하지 않으며, 일반적으로 이러한 개인은 성장과 [18]: 1254 발육이 뛰어나다.그럼에도 불구하고 특발성 만성 췌장염은 CF를 가진 췌장충분한 사람들의 일부에서 발생할 수 있으며, 재발하는 복통 및 생명을 위협하는 [18]합병증과 관련이 있다.
진화된 분비물은 또한 CF 환자들에게 간 문제를 일으킬 수 있다.소화를 돕기 위해 간에서 분비되는 담즙은 담관을 막아 간 손상을 초래할 수 있다.소화불량이나 지질흡수는 지방질화를 초래할 수 있다.시간이 지남에 따라, 이것은 흉터와 결절(순환)으로 이어질 수 있다.간은 혈액의 독소를 제거하지 못하고 혈액 [30][31]응고에 책임이 있는 단백질과 같은 중요한 단백질을 만들지 못한다.간 질환은 [18]CF와 관련된 세 번째로 흔한 사망 원인이다.
약 5~7%의 사람들이 증상을 일으킬 정도로 심각한 간 손상을 경험한다: 전형적으로 담도통증의 [32]원인이 되는 담석이다.
내분비
췌장은 혈당 조절을 돕는 호르몬인 인슐린을 만드는 역할을 하는 랑게르한스 섬을 포함하고 있다.췌장의 손상은 췌도세포의 상실로 이어질 수 있으며, 이는 [33]췌장질환자 특유의 당뇨병을 유발할 수 있다.낭포성 섬유증 관련 당뇨병은 [34]제1형 당뇨병과 제2형 당뇨병의 특징을 공유하며 CF의 주요 비폐 합병증 중 하나이다.
비타민 D는 칼슘과 인산염 조절에 관여한다.흡수 불량으로 인해 식단에서 비타민 D를 제대로 섭취하지 못하면 약해진 뼈가 [35]골절되기 쉬운 골다공증으로 이어질 수 있다.
불임
불임은 남녀 모두에게 영향을 미친다.낭포성 섬유증을 가진 남성의 적어도 97%가 불임이지만 불임은 아니며, 보조 생식 [36]기술을 가진 아이를 가질 수 있다.CF를 가진 남성에서 불임의 주된 원인은 선천적으로 정자가 없는 것이지만, 또한 잠재적으로 정자가 없거나 비정상적으로 생긴 정자가 거의 없는 것과 같은 다른 메커니즘에 의해서도 가능하다.[37]불임 평가 중 선천적으로 혈관 배변이 없는 것으로 밝혀진 많은 남성들은 경미하고 이전에 진단되지 않은 형태의 [38]CF를 가지고 있다.자궁경부 점액이 두꺼워지거나 영양실조로 인해 CF를 가진 여성의 약 20%가 임신에 어려움을 겪고 있다.심각한 경우, 영양실조는 배란을 방해하고 [39]생리를 하지 못하게 한다.
원인들
CF는 유전자 낭포성 섬유증 트랜스막 컨덕턴스 레귤레이터(CFTR)의 돌연변이에 의해 발생한다.가장 일반적인 돌연변이인 δF508은 단백질의 [40][41]508번째 위치에서 아미노산 페닐알라닌(F)의 손실을 초래하는 3개의 뉴클레오티드의 결실(결실을 나타내는 δ)이다.이 돌연변이는 전 세계 CF 증례의 3분의 2(66-70%)[18]와 미국 증례의 90%를 차지한다. 그러나 1500개 이상의 다른 돌연변이가 [42]CF를 생성할 수 있다.대부분의 사람들이 CFTR 유전자의 두 개의 작업 복사본(알레르)을 가지고 있지만 낭포성 섬유증을 예방하기 위해서는 하나만 필요하다.CF는 어느 대립 유전자도 기능성 CFTR 단백질을 생성할 수 없을 때 발생한다.따라서 CF는 상염색체 열성 [43]질환으로 간주된다.
7번 염색체의 q31.2 궤적에서 발견된 CFTR 유전자는 23만 쌍의 염기쌍으로 1480개의 아미노산 길이의 단백질을 생성한다.보다 구체적으로, 위치는 7q31.2로 표현되는 7, 영역 3, 밴드 1, 서브밴드 2의 긴 팔의 염기쌍 117,120,016과 117,308,718 사이에 있다.구조적으로 CFTR은 ABC 유전자로 알려진 유전자의 한 종류이다.이 유전자의 산물은 땀, 소화액, 그리고 점액을 만드는 데 중요한 염화물 이온 채널이다.이 단백질은 두 개의 ATP 가수 분해 도메인을 가지고 있는데, 이것은 단백질이 ATP의 형태로 에너지를 사용할 수 있게 해줍니다.또한 단백질이 세포막을 통과할 수 있도록 각각 6개의 알파 나선으로 구성된 두 개의 도메인을 포함합니다.단백질의 조절결합부위는 주로 cAMP의존성 단백질인산화효소인 [19]인산화에 의한 활성화를 가능하게 한다.단백질의 카르복실 말단은 PDZ 도메인 [44]상호작용에 의해 세포골격에 고정된다.폐의 통로에 있는 CFTR의 대부분은 점액 [45]특성을 조절하는 희귀한 이온 수송 세포에 의해 생성됩니다.
또한 CFTR 외에 유전적 수식어가 질병의 빈도와 심각도를 조절한다는 증거가 증가하고 있다.한 가지 예는 미생물의 식세포화를 촉진함으로써 선천적인 면역에 관여하는 만나 결합 렉틴이다.단백질의 낮은 순환수준을 초래하는 마난결합 렉틴 대립 유전자 중 하나 또는 양쪽의 다형성은 만성세균 [18]감염의 부담 증가뿐만 아니라 말기 폐질환의 위험이 3배 더 높은 것과 관련이 있다.
캐리어
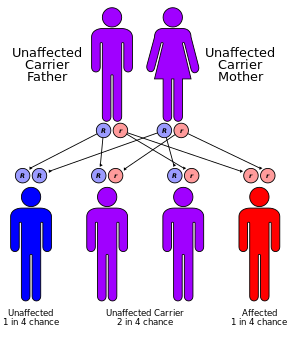
북유럽 조상의 25명 중 1명은 유전적 매개체로 여겨진다.이 질병은 이들 보균자 중 두 명이 아이를 가질 때만 나타나는데, 그들 사이의 각 임신은 이 질병으로 아이를 낳을 확률이 25%이기 때문이다.비록 영향을 받은 조상의 신생아 3,000명 중 한 명만이 CF를 가지고 있지만, CF를 일으키는 유전자의 돌연변이는 900개 이상 알려져 있다.현재 검사에서는 가장 [46]흔한 돌연변이를 찾습니다.
테스트에 의해 선별된 돌연변이는 개인의 인종 집단이나 가족 내 이미 CF의 발생에 따라 다르다.백인 미국인 25명 중 1명을 포함한 천만 명 이상의 미국인들이 CF 유전자의 한 변이를 가지고 있습니다.CF는 다른 인종에도 존재하지만 백인만큼 자주 나타나지는 않는다.히스패닉계 미국인 46명 중 1명, 흑인 65명 중 1명, 아시아계 미국인 90명 중 1명이 CF 유전자 [46]변이를 갖고 있다.
병태생리학
CFTR 유전자의 여러 돌연변이가 발생할 수 있으며, 다른 돌연변이는 CFTR 단백질의 다른 결함을 야기하며, 때로는 더 가볍거나 더 심각한 질병을 야기한다.이러한 단백질 결함은 때때로 그들의 기능을 회복시킬 수 있는 약물의 표적이 되기도 한다.δF508-CFTR 유전자 돌연변이는 미국 환자의 90% 이상에서 발생하며, 정상적으로 접히지 않고 세포막으로 적절하게 운반되지 않는 단백질을 생성하여 [47]분해된다.
다른 돌연변이는 생산이 조기에 종료되기 때문에 단백질이 너무 짧다(절단).다른 돌연변이는 정상적으로 에너지를 사용하지 않고 염화물, 요오드화물, 티오시안산염이 적절하게 [48]막을 통과하지 못하고 정상보다 빠른 속도로 분해되는 단백질을 생성한다.돌연변이는 또한 [19]생산되는 CFTR 단백질의 더 적은 복사본으로 이어질 수 있다.
이 유전자에 의해 만들어진 단백질은 땀샘, 폐, 췌장, 그리고 체내에 남아있는 모든 외분비샘의 세포 외막에 고정된다.단백질은 이 막을 덮고 세포 내부(세포질)와 주변 액체를 연결하는 통로 역할을 합니다.이 채널은 주로 할로겐화 음이온의 세포 내부로부터 외부로의 이동을 제어합니다. 그러나 땀 덕트에서는 염화물이 땀 덕트에서 세포질로 이동하도록 도와줍니다.CFTR 단백질이 땀샘에서 이온을 흡수하지 않으면 땀샘에서 방출되는 염화물과 티오시아네이트가[49] 땀샘 안에 갇혀 피부로 펌프된다.
추가적으로, OSCN은 면역 방어 [50][51]체계에 의해 생성될 수 없습니다.염화물이 음전하를 띠기 때문에, 이것은 일반적으로 양이온을 세포로 교차시키는 세포 내부와 외부의 전위를 변화시킵니다.나트륨은 세포외 공간에서 가장 흔한 양이온이다.땀 덕트 내의 과도한 염화물은 상피 나트륨 채널에 의한 나트륨 흡수를 방지하고 나트륨과 염화물의 결합으로 염분이 생성되어 CF에 걸린 사람의 땀에서 많은 양이 손실됩니다.이 잃어버린 소금은 땀 [19]테스트의 기초가 된다.
CF 손상의 대부분은 진화된 분비물과 함께 영향을 받는 장기의 좁은 통로가 막혀 있기 때문입니다.이러한 막힘은 폐의 리모델링과 감염, 췌장에 축적된 소화효소에 의한 손상, 두꺼운 대변에 의한 장폐색 등으로 이어진다.단백질과 세포 기능의 결함이 임상 효과를 어떻게 일으키는지에 대한 여러 이론들이 제시되어 왔다.가장 최근의 이론은 이온 수송의 결함이 기도 상피에서 탈수를 일으켜 [52]점액을 두꺼워지게 한다는 것을 암시한다.기도 상피 세포에서 섬모는 세포의 꼭대기 표면과 기도 표면 액체라고 알려진 층의 점액 사이에 존재합니다.세포에서 이 층으로 이온의 흐름은 CFTR과 같은 이온 채널에 의해 결정됩니다. CFTR은 염화 이온이 세포에서 ASL로 빨려들어가도록 할 뿐만 아니라 ENAC라고 불리는 또 다른 채널을 조절합니다. 이 채널은 나트륨 이온이 ASL을 떠나 호흡기 상피로 들어갈 수 있도록 합니다.CFTR은 보통 이 채널을 억제하지만 CFTR에 결함이 있는 경우 나트륨은 ASL에서 [citation needed]셀로 자유롭게 흐릅니다.
물이 나트륨을 따라가면 ASL의 깊이가 고갈되고 섬모가 점액층에 [53]남게 됩니다.섬모는 두껍고 끈적끈적한 환경에서는 효과적으로 움직일 수 없기 때문에 점액성 클리어런스가 부족하고 점액이 축적되어 작은 [54]기도가 막힌다.폐에 점성이 더 높고 영양분이 풍부한 점액이 축적되면 박테리아가 몸의 면역 체계로부터 숨어서 반복적인 호흡기 감염을 일으킨다.췌관과 피부의 땀샘에 동일한 CFTR 단백질이 존재하는 것 또한 이러한 시스템에서 [citation needed]증상을 일으킨다.
만성 감염
낭포성 섬유증 환자의 폐는 어릴 때부터 세균에 감염되어 식민지화된다.CF가 있는 사람들 사이에서 종종 퍼지는 이 박테리아는 변화된 점액에서 번성하며, 이것은 폐의 작은 기도에 모인다.이 점액은 면역 세포와 항생제가 침투하기 어려운 생물막으로 알려진 박테리아 미세 환경의 형성을 이끈다.점액 분비물과 지속적인 호흡기 감염은 기도를 점차적으로 개조하여 폐를 손상시키는 것을 반복하며, 이는 감염을 [55]근절하는 것을 더욱 어렵게 만든다.CF 폐 감염과 기도 리모델링의 자연사는 CF [56]환자의 마이크로바이옴 내 및 마이크로바이옴 사이의 엄청난 공간적, 시간적 이질성 때문에 잘 알려져 있지 않다.
시간이 지남에 따라 CF에 걸린 사람마다 박테리아의 종류와 개개인의 특성이 모두 변한다.초기 단계에서는 황색포도상구균, 인플루엔자균과 같은 일반적인 박테리아가 정착하여 [18]폐를 감염시킨다.결국, Pseudomonas aeruginosa (그리고 때로는 Burkholderia cepacia)가 지배합니다.18세까지 고전 CF 환자의 80%, B.[18] 두화증 환자의 3.5%가 포진한다.일단 폐에 들어가면, 이 박테리아들은 환경에 적응하고 일반적으로 사용되는 항생제에 대한 내성을 키웁니다.슈도모나스는 "무코이드" 슈도모나스로 알려진 큰 군락을 형성할 수 있는 특별한 특성을 발달시킬 수 있는데,[55] 이것은 CF가 없는 사람들에게서 거의 나타나지 않습니다.과학적 증거는 인터류킨 17 경로가 CF에서 P.[57] Aeruginosa 감염 중 염증 반응의 저항과 조절에 중요한 역할을 한다는 것을 시사한다.특히 인터류킨17 매개면역은 만성 기도감염 시 양면성을 발휘하며 한쪽에서는 P. Aeruginosa 부담 조절에 기여하는 반면 다른 한쪽에서는 악화되는 폐호중구증 및 조직개조를 [57]전파한다.
감염은 [58]CF에 걸린 다른 사람들 사이를 통과함으로써 확산될 수 있다.과거에는 CF를 가진 사람들이 여름 "CF 캠프"나 다른 레크리에이션 [59][60]모임에 자주 참여했습니다.병원에서는 CF를 가진 환자를 공통 영역으로 그룹화하고 일반 장비(예: 분무기)[61]를 개별 [62]환자 간에 멸균하지 않았습니다.이것은 환자 집단들 사이에서 더 위험한 종류의 박테리아가 전염되는 결과를 가져왔다.그 결과 CF를 가진 개인은 현재 의료 환경에서 일상적으로 서로 격리되어 있으며, 의료 제공자는 CF를 가진 환자를 검사할 때 치명적인 박테리아 균주의 확산을 제한하기 위해 [63]가운과 장갑을 착용하도록 권장됩니다.
CF 환자는 또한 필라멘트 균(Aspergillus fumigatus, Scedosporium apiospermum, Aspergillus tereus 등) 및/또는 효모균(Candida albicans 등)에 의해 만성적으로 기도가 형성될 수 있습니다. 또한 일반적으로 분리되지 않은 다른 필라멘트 균류에는 Aspergillus flavus flavus와 Aspirus nidulans(Cratus, Aspiratory cratus nidulans)가 포함되어 있습니다.) 및 Exophiala dermitidis 및 Scedosporium derpicans(만성 기도 착색제), Penicillium Emersoni 및 Acrophialophora fusispora와 같은 일부 필라멘트 균류는 [64]CF의 맥락에서만 환자에게서 발견됩니다.CF를 특징짓는 결손 점막 클리어런스는 국소 면역학적 장애와 관련되어 있다.또한 항생제에 의한 장기 치료와 코르티코스테로이드 치료제의 사용도 곰팡이의 성장을 촉진할 수 있다.곰팡이 기도 콜로니제이션의 임상적 관련성은 여전히 논쟁의 대상이지만 필라멘트 균류는 국소 염증 반응에 기여할 수 있고 따라서 폐 기능의 점진적 악화를 일으킬 수 있다. 알레르기성 기관지 폐 아스페르길루스증 - CF의 맥락에서 가장 흔한 곰팡이 질환인아스페르길루스 [64][65]종에 대한 Th2 유도 면역 반응을 수반한다.
진단.
많은 지역에서 모든 신생아는 생후 며칠 이내에 낭포성 섬유증 검사를 받습니다. 일반적으로 높은 수준의 면역 반응성 트립시노겐에 [66]대한 혈액 검사를 통해 검사됩니다.양성으로 판정된 신생아나 증상이나 가족력으로 낭포성 섬유증 의심자는 땀 검사를 받는다.전류가 필로카르핀을 피부에 주입하여 땀을 자극하기 위해 사용됩니다.땀을 채취하여 염분 농도를 분석합니다.땀에 비정상적으로 염화물 수치가 높다는 것은 CFTR이 기능하지 못한다는 것을 의미한다; 그 사람은 낭포성 섬유증으로 [67][note 1]진단된다.낭포성 섬유증과 전형적으로 관련된 CFTR 돌연변이를 식별하기 위해 유전자 검사도 이용할 수 있다.많은 실험실에서 낭포성 섬유증 환자의 90% 이상을 식별할 수 있는 가장 흔한 30-96개의 CFTR [67]돌연변이를 테스트할 수 있다.
CF를 가진 사람들은 침과[69] 점액에 티오시안산염과 하이포티오시안산염을 적게 가지고 있다.경미한 형태의 CF의 경우 경피 전위차 측정이 도움이 될 수 있습니다.CF는 CFTR [70]유전자의 돌연변이를 확인함으로써 진단할 수도 있다.
많은 경우, 아기의 맛이 [18]짜기 때문에 부모가 진단을 내린다.면역반응성 트립시노겐 수치는 CFTR 유전자(캐리어)의 단일 변이 복사를 가진 개인 또는 드물게 CFTR 유전자의 두 개의 정상 복사를 가진 개인에서 증가할 수 있다.이러한 잘못된 양성으로 인해 신생아의 CF 검사는 논란이 [71][72]될 수 있다.
2010년까지 미국의 모든 주(州)가 신생아 선별 프로그램을 도입했으며, 2016년 현재[update] 21개 유럽 국가가 [74]최소 일부 지역에 프로그램을 보유하고 있다.
태내
임신 중인 여성이나 임신을 계획하고 있는 커플은 CFTR 유전자 돌연변이를 검사하여 아이가 CF로 태어날 위험을 결정할 수 있습니다.검사는 일반적으로 한쪽 또는 양쪽 부모에게 먼저 수행되며 CF 위험이 높은 경우 태아에 대한 검사가 수행됩니다.미국 산부인과 학회는 임신을 생각하고 있는 모든 사람들에게 [75]보균자인지 여부를 검사해 볼 것을 권고하고 있다.
태아의 CF 발달을 위해서는 각 부모가 CFTR 유전자의 돌연변이 사본을 전달해야 하고 CF 테스트는 비용이 많이 들기 때문에 종종 한 부모에 대해 초기에 테스트를 수행합니다.테스트 결과 부모가 CFTR 유전자 돌연변이 운반체임이 판명되면 다른 부모는 자녀가 CF에 걸릴 위험을 계산하기 위해 테스트됩니다.CF는 천 가지 이상의 다른 [43]돌연변이로 인해 발생할 수 있습니다.2016년 현재[update] δF508과[43] 같이 가장 일반적인 돌연변이만 검사됩니다. 시판되는 대부분의 검사는 32개 이하의 다른 돌연변이를 찾습니다.가족이 알려진 특이한 돌연변이를 가지고 있는 경우, 그 돌연변이에 대한 특정 스크리닝을 수행할 수 있다.현재 테스트에서 알려진 모든 돌연변이가 발견되는 것은 아니기 때문에 음성 화면이 아이에게 [76]CF가 생기지 않도록 보장하지는 않습니다.
임신 중에는 태반(콜리온 융모 채취) 또는 태아 주위의 유체(암니오센시스)에 대해 검사를 수행할 수 있습니다.그러나 융모막 샘플링은 태아 사망 100명 중 1명,[77] 양막 천자 200명 중 1명의 위험을 가지고 있다; 최근의 연구는 이것이 약 [78]1,600명 중 1명으로 훨씬 더 낮을 수 있다는 것을 보여준다.
경제적으로 낭포성 섬유증 보균자 커플의 경우, 이식 전 유전자 진단(PGD)과 자연 임신(NC)을 비교한 후, 산전 검사와 영향을 받은 임신을 낙태할 때, PGD는 산모 연령까지 순경제적 이익을 제공하며, 이후 NC, 산전 검사, 낙태는 경제적 이익이 더 높다.잘 어울립니다.[79]
관리
CF에 대한 치료법은 알려져 있지 않지만, 몇 가지 치료 방법이 사용됩니다.CF의 관리는 지난 70년간 크게 개선되었습니다.70년 전에 그것을 가지고 태어난 영아들은 그들의 첫해를 넘기지 못할 것 같지만, 오늘날의 영아들은 성인기까지 잘 살 것 같다.낭포성 섬유증 치료의 최근 발전은 낭포성 섬유증을 가진 사람들이 그들의 상태에 덜 지장을 받는 삶을 살 수 있다는 것을 의미한다.관리의 초석은 기도 감염의 적극적인 치료와 좋은 영양 섭취와 적극적인 생활습관의 장려입니다.CF의 관리로서의 폐 재활은 사람의 일생 동안 지속되며, 장기 기능, 즉 삶의 질을 극대화하는 것을 목적으로 한다.작업 치료사들은 낭포성 섬유증 [80]환자를 위한 재활 과정에 에너지 보존 기술(ECT)을 사용합니다.에너지 절약 기술의 예로는 인체공학적 원리, 오므린 입술 호흡, 횡격막 [81]호흡 등이 있습니다.CF 환자는 만성 폐감염으로 피로와 발작장애가 나타나기 쉬우므로 활동 중 소비되는 에너지의 양을 줄이면 환자의 기분이 좋아지고 [80]자립심을 높일 수 있다.기껏해야 현재의 치료법은 장기 기능의 저하를 지연시킨다.질병 증상의 편차가 크기 때문에 치료는 일반적으로 다원적 전문 센터에서 이루어지며 개인에 맞게 조정된다.치료 대상은 폐, 위장관(췌장효소 보충제 포함), 생식기관(보조 생식기술 포함), 심리적 [82]지원이다.
CF 치료의 가장 일관된 측면은 삶의 질을 유지하기 위해 두꺼운 점액과 감염으로 인한 폐 손상을 제한하고 치료하는 것입니다.정맥주사, 흡입, 경구 항생제는 만성 및 급성 감염을 치료하기 위해 사용된다.점액 농도를 변화시키고 제거하기 위해 기계 장치와 흡입 약물을 사용한다.이러한 치료법은 효과적이기는 하지만 시간이 많이 걸릴 수 있다.산소 [83]수치가 상당히 낮은 사람들에게는 집에서 산소 치료를 받는 것이 좋습니다.CF를 가진 많은 사람들은 장내 이상과 염증을 교정할 수 있다고 생각되는 프로바이오틱스를 사용하지만 CF를 가진 사람들의 폐 악화를 줄이기 위한 프로바이오틱스의 효과에 대한 임상 실험 증거는 [84]불확실하다.
항생제
CF에 걸린 많은 사람들은 감염을 예방적으로 억제하기 위해 심지어 건강할 때에도 항상 하나 이상의 항생제를 복용한다.항생제는 폐렴이 의심되거나 폐 기능의 현저한 저하가 나타날 때마다 절대적으로 필요하며, 보통 가래 분석 결과와 그 사람의 과거 반응을 바탕으로 선택됩니다.이 장기 치료는 종종 입원 및 말초 삽입된 중앙 카테터 또는 Port-a-Cath와 같은 보다 영구적인 링거를 삽입해야 합니다.토브라마이신, 콜리스틴, 아즈트레오남과 같은 항생제를 사용한 흡입 요법은 종종 [85][86][87]한 번에 몇 달 동안 식민지화된 세균의 성장을 방해하여 폐 기능을 향상시키기 위해 주어진다.흡입 항생제 치료는 감염과 싸우면서 폐 기능에 도움을 주지만 항생제 내성 발달, 이명, 목소리 [88]변화 등 큰 단점도 있다.흡입된 레보플록사신은 [89]낭포성 섬유증이 있는 사람들에게서 Pseudomonas aeruginosa 치료에 사용될 수 있다.Pseudomonas Aeruginosa 감염의 조기 관리는 쉽고 더 낫습니다. 경구 항생제를 포함하거나 사용하지 않고 분무 항생제를 사용하면 2년까지 [90]근절될 수 있습니다.낭포성 섬유증 환자의 폐감염 CF환자를 치료하기 위해 항생제를 선택할 때 항생제 선택은 항생제를 따로(한 번에 하나씩) 검사한 결과를 기준으로 해야 할지 서로 [91]조합해야 할지 여전히 불분명하다.
시프로플록사신이나 아지트로마이신과 같은 항생제는 감염을 예방하거나 진행 중인 [92]감염을 통제하기 위해 구강 내 투여된다.사용된 아미노글리코시드 항생제(예: 토브라마이신)는 장기 [93]사용 시 청력 손실, 내이의 균형 체계 손상 또는 신부전을 일으킬 수 있습니다.이러한 부작용을 예방하기 위해 혈액 내 항생제의 양을 정기적으로 측정하고 그에 [94]따라 조절합니다.
항생제 사용, 질병의 만성성, 그리고 내성 박테리아의 출현과 관련된 이 모든 요소들은 항생제 보조 [95]요법과 같은 다른 전략들을 위한 더 많은 연구를 필요로 한다.현재, 낭포성 섬유증 및 버크홀데리아 세파시아[96] 복합체 환자의 폐 악화에 대한 항생제의 효과와 [97]CF가 있는 사람의 비결핵 마이코박테리아 치료에 대한 항생제의 효과를 보여주는 신뢰할 수 있는 임상 실험 증거는 없다.
기타 의약품
분비물을 완화시키는 데 도움이 되는 에어로졸화 약물은 도나아제 알파와 고토닉 [98]식염수를 포함한다.도나아제는 인간 디옥시리보핵산가수분해효소이며, 가래에서 DNA를 분해하여 [99]점도를 감소시킨다.도나아제 알파는 폐 기능을 향상시키고 아마도 악화 위험을 감소시키지만, 다른 유사한 [100]약물보다 효과가 더 있는지 덜한지 알 수 있는 충분한 증거가 없다.도나아제 알파는 폐 기능을 향상시킬 수 있지만, 다른 고삼투압 [100]치료법보다 낫다는 강력한 증거는 없습니다.
조사약인 데누포솔은 대체 염화물 채널을 열어 [101]점액을 액화시키는 데 도움을 준다.흡입 코르티코스테로이드가 유용한지는 확실하지 않지만 흡입 코르티코스테로이드 치료를 중단하는 것은 [102]안전합니다.코르티코스테로이드 치료가 [102]성장을 방해함으로써 해를 끼칠 수 있다는 증거가 약하다.폐렴구균 예방접종은 2014년 [103]현재[update] 연구되지 않았다.2014년 현재[update], 인플루엔자 백신이 낭포성 [104]섬유증 환자에게 유익하다는 확실한 증거는 없다.
이바카프토르는 이바카프토르 유도 CFTR 단백질 [105][106]강화에 반응하는 여러 특정 돌연변이로 인해 CF 치료를 위해 경구 복용하는 약물이다.폐 기능을 약 10% 향상시키지만 2014년 현재[update] 가격이 [105]비싸다.시판된 첫 해에 미국에서는 [105][needs update]정가가 연간 30만 달러가 넘었습니다.2015년 7월 미국 식품의약국은 루마카프트/ivacaftor를 승인했다.[107]2018년에 FDA는 ivacaftor/tezacaftor 조합을 승인했습니다. 제조사는 연간 [108]292,000달러의 정가를 발표했습니다.Tezacaftor는 CFTR 단백질을 세포 표면의 올바른 위치로 이동시키는 데 도움을 주며 F508del [109]돌연변이를 가진 사람을 치료하도록 설계되었습니다.
2019년에는 미국에서 Trikafta로 판매되는 복합 약물 elexacaftor/ivacaftor/tezacaftor가 [110][111]12세 이상 CF 환자에 대해 승인되었다.2021년에는 [112]6세 이상의 환자를 포함하도록 확대되었다.유럽에서는 이 약이 2020년에 승인되어 카프트리오로 [113]시판되었다.낭포성 섬유증 [110][114]환자의 약 90%에서 발생하는 f508del 돌연변이를 가진 사람에게 사용된다.그 포낭성 섬유증 재단에 따르면 임상 실험에서는 combina을 투여했다 참가자들"이 약 CF의 역사상증, 결국 CF을 가진 사람들 중 90%로 변조기 치료를 가져올 수 있는 근본 원인을 위한 치료를 제공하는 것은 유일무이한 치료 발전을 나타냅니다."[115].tion약물은 폐 악화를 63% 감소시키고 염화 땀 [116]농도를 41.8mmol/L 감소시켰다.낭포성 섬유증과 관련된 증상의 레퍼토리를 완화함으로써, 복합 약물은 또한 이 [116][115]질환 환자들 사이의 삶의 질 메트릭을 유의하게 개선했다.이 조합 약물은 또한 조울증 치료에 사용되는 카바마제핀과 같은 CYP3A 유도제와 상호작용하여 감소된 농도로 체내 순환을 일으키는 것으로 알려져 있다.따라서 병용하지 않는 것이 좋습니다.[117]미국에서의 정가는 [118]연간 31만1천 달러가 될 것이다. 그러나 보험은 [119]약값의 대부분을 충당할 수 있다.
담즙염인 우르소데옥시콜산이 사용됐지만 효과가 있는지 [120]여부를 입증할 자료가 부족하다.
영양 보충
비타민 A나 베타카로틴 보충제가 비타민 A [121]결핍으로 인한 눈과 피부 질환에 어떤 영향을 미치는지 확실하지 않다.
낭포성 섬유증이 있는 사람들이 비타민 [122]D의 섭취를 늘림으로써 골다공증을 예방할 수 있다는 강력한 증거는 없다.
비타민 E 결핍과 낭포성 섬유증을 가진 사람들의 경우, 비타민 E 보충제가 비타민 E specific 특이적 결핍 장애나 폐 [123]기능에 어떤 영향을 미치는지 아직 불확실하지만 비타민 E 보충제가 비타민 E 수치를 향상시킬 수 있다는 증거가 있다.
낭포성 섬유증 환자의 비타민 K 보충 효과에 관한 확실한 증거는 2020년 [124]현재 부족하다.
낭포성 섬유증 환자에게 오메가3 지방산 보충제의 효과를 다양한 연구들이 연구해 왔지만, 그것이 어떤 유익성이 있는지 혹은 [125]역효과가 있는지에 대한 증거는 불확실하다.
절차들
가래를 제거하고 가래의 예상을 촉진하기 위해 몇 가지 기계 기술이 사용된다.단기 기도 청소에 좋은 기술 중 하나는 호흡기 치료사가 하루에 여러 번 손으로 사람의 가슴을 두드려서 분비물을 풀어주는 흉부 물리치료이다.이 "충돌 효과"는 흉벽 진동 또는 폐내충돌식 인공호흡기를 사용하는 특정 장치를 통해서도 투여될 수 있습니다.이러한 장치에서 사용할 수 있는 바이패스 퀴라스 환기 및 관련 클리어런스 모드와 같은 다른 방법은 기침 보조 단계와 분비물을 제거하기 위한 진동 단계를 통합합니다.휴대성이 뛰어나 가정용입니다.[10]
또 다른 기술은 호기 중에 기도에 배압을 공급하는 양의 호기압 물리치료입니다.이 효과는 마스크 또는 마우스피스로 구성된 장치에서 제공되며, 이때 저항은 호기 [126]단계에만 적용됩니다.이 기술의 작동 원리는 인공호흡을 통한 점액 이면의 가스 압력 증가와 함께 호기 [127][128]중 작은 기도의 조기 붕괴를 막는 기능적 잔류 용량이 일시적으로 증가하는 것으로 보인다.
폐질환이 악화되면 기계적 호흡 보조가 필요할 수 있습니다.CF를 가진 사람들은 밤에 공기를 폐로 밀어 넣기 위해 특수 마스크를 써야 할 수도 있다.BiPAP 인공호흡기로 알려진 이 기계는 수면 중 저혈중 산소수치를 예방하는데 도움을 준다.물리치료 중에 가래를 [129]제거하기 위해 비침습 인공호흡기를 사용할 수 있습니다.이런 종류의 치료가 폐의 악화나 질병의 [129]진행에 영향을 미치는지는 알려지지 않았다.낭포성 섬유증 [129]환자의 운동 능력을 향상시키기 위해 비침습적 인공호흡 요법이 어떤 역할을 하는지는 알려지지 않았다.그러나 저자들은 "비침습적 인공호흡은 특히 [130]가래를 예상하는 데 어려움을 겪는 낭포성 섬유증을 가진 사람들에게 다른 기도 클리어런스 기법의 유용한 부가물이 될 수 있다"고 지적했다.심각한 질병 중에는 인공호흡기로 [131][132]지탱되는 호흡을 가능하게 하기 위해 목구멍에 튜브를 삽입할 수 있다.
아이들의 경우, 예비 연구는 마사지 요법이 사람들과 그들의 가족의 삶의 [133]질에 도움을 줄 수 있다는 것을 보여준다.
일부 폐 감염은 폐의 감염된 부분을 외과적으로 제거해야 한다.이것이 여러 번 필요할 경우 폐 기능이 심각하게 [134]저하됩니다.자발적 또는 재발적 기흉을 가진 CF를 가진 사람들에게 가장 효과적인 치료 방법은 [135]명확하지 않다.
이식
폐기능과 운동내성이 저하됨에 따라 CF가 있는 사람에게는 폐이식이 필요할 수 있다.비록 단일 폐 이식이 다른 질병에서도 가능하지만, CF가 있는 사람들은 이식된 폐를 감염시킬 수 있는 박테리아를 가지고 있을 수 있기 때문에 양쪽 폐가 모두 교체되어야 한다.간질환 및/[136]또는 당뇨병을 완화하기 위해 췌장 또는 간이식을 동시에 실시할 수 있다.폐 이식은 폐 기능이 기계 장치의 도움이 필요할 정도로 저하되거나 누군가의 생존이 [137]위협받을 때 고려된다.Merck Manual에 따르면, "심각한 폐 질환에 대한 양측 폐 이식은 경험과 향상된 기술로 점점 더 일상화되고 있고 더 성공적이다.CF가 있는 성인의 경우 이식 후 중간 생존 기간은 약 9년입니다.[138]
기타 측면
장폐색을 가진 신생아는 일반적으로 수술이 필요한 반면, 원위성 장폐색 증후군을 가진 성인은 일반적으로 수술이 필요하지 않다.부족한 소화 효소의 대체에 의한 췌장 기능 부전의 치료는 십이지장이 대변에서 손실되었을 영양소와 비타민을 적절히 흡수할 수 있도록 합니다.그러나 췌장 효소 대체의 최선의 용량과 형태는 이 [139]치료의 위험성과 장기적인 효과와 마찬가지로 불분명하다.
지금까지 낭포성 섬유증 성인의 아테롬성 동맥경화증이나 관상동맥질환 발병과 관련된 대규모 연구는 이루어지지 않았다.이것은 낭포성 섬유증을 가진 대부분의 사람들이 임상적으로 유의한 아테롬성 동맥경화증이나 관상동맥 심장 [140]질환에 걸릴 만큼 충분히 오래 살지 못하기 때문일 가능성이 높다.
당뇨병은 CF의 가장 흔한 비폐 합병증이다.제1형 당뇨병과 제2형 당뇨병의 특징을 혼합하여 낭포성 섬유증 관련 [34][141]당뇨병으로 인식되고 있습니다.경구용 항당뇨제를 사용하는 경우도 있지만 인슐린 주사나 인슐린 [142]펌프를 사용하는 것이 권장되며, 1, 2형 당뇨병과 달리 식사 제한은 [34]권장되지 않습니다.스테노트로포모나스 말토필리아는 낭포성 섬유증을 가진 사람들에게서 비교적 흔하지만, S. 말토필리아에 대한 항생제의 효과에 대한 증거는 [143]불확실하다.
비스포네이트는 구강이나 정맥주사로 복용하면 낭포성 섬유증 [144]환자의 골밀도를 향상시키기 위해 사용될 수 있다.비스포스포네이트를 정맥에 주사할 때 통증이나 독감 같은 부작용들이 문제가 [144]될 수 있다.비스포스포네이트를 입으로 섭취하는 것이 위장관에 미치는 악영향은 [144]알려져 있지 않다.
영양 보충 사료를 통해 식품 에너지를 증가시키기 위한 공급 튜브를 삽입하거나 성장 호르몬 [145]주입을 통해 성장 저하를 방지할 수 있다.
부비강 감염은 항생제의 장기 투여로 치료된다.코 용종의 발달이나 코 안의 다른 만성적인 변화는 코를 통한 공기 흐름을 심각하게 제한할 수 있고 시간이 지남에 따라 사람의 후각을 감소시킨다.코막힘을 완화하고 더 이상의 감염을 제한하기 위해 부비강 수술이 종종 사용된다.플루티카손 프로피온산염과 같은 비강 스테로이드제가 코염을 [146]줄이기 위해 사용된다.
여성의 불임은 보조 생식 기술, 특히 배아 이식 기술로 극복할 수 있다.정자의 부재로 인한 남성 불임은 고환에서 직접 정자 세포를 채취하는 고환 정자 적출로 극복할 수 있다.채취한 샘플이 너무 적은 수의 정자 세포를 포함하고 있어 자연 수정 가능성이 높은 경우에는 세포질 내 정자 주입을 [147]실시할 수 있다.CF를 가진 여성에게는 제3자 재생산이 가능하기도 하다.항산화제를 복용하는 것이 결과에 영향을 미치는지는 [148]불분명하다.
신체 운동은 보통 낭포성 섬유증이 [149]있는 사람들을 위한 외래 치료의 일부이다.유산소 운동은 유산소 운동 능력, 폐 기능, 그리고 건강과 관련된 삶의 질에 이로운 것으로 보이지만, 증거의 질은 [149]낮았다.
아미노글리코시드 항생제의 사용으로 인해 이독성이 일반적이다.증상으로는 "이명, 난청, 과산, 청각 충만, 현기증, 현기증"[150]이 있을 수 있다.
위장
낭포성 섬유증 [29]환자에게는 변비와 원위 장폐색 증후군을 포함한 위장관의 폐색 등 위장 계통의 문제가 빈번한 합병증이다.완전한 폐색을 막고, 다른 CF 증상을 줄이고,[29] 삶의 질을 향상시키기 위해서는 위장 질환의 치료가 필요하다.변 연화제, 설사약 및 프로키네틱스(GI 중심 치료법)가 종종 제안되지만, 어떤 방법이 최선이고 위험이 [29]가장 적은지에 대한 전문가들의 명확한 합의가 없다.CFTR의 기능장애를 목적으로 하는 점액분해제나 전신치료제 [151]또한 증상을 개선하기 위해 때때로 제안된다.
예후
낭포성 섬유증의 예후는 검진을 통한 조기 진단과 더 나은 치료 및 의료 접근으로 인해 개선되었다.1959년 미국에서 CF를 가진 아이들의 평균 생존 연령은 6개월이었다.[152]2010년에는 여성이 37세,[153] 남성이 40세로 추정되고 있다.캐나다에서 중앙 생존율은 1982년 [154]24세에서 2007년 47.7세로 증가했다.미국에서는 2016년에 CF로 태어난 사람의 예상 수명은 [155]전문 클리닉에서 치료했을 때 47.7세입니다.
미국에서는 2009년 현재 18세 이상 CF 보유자의 92%가 고등학교를 졸업했으며 67%는 대학 교육을 일부 받은 상태, 15%는 장애인, 9%는 무직, 56%는 미혼, 39%는 [156]결혼 또는 파트너와 함께 살고 있다.
삶의 질
만성 질환은 관리하기 어려울 수 있다.CF는 "일반적인 영양실조와 만성 호흡기 [157]감염을 일으키는 소화 및 호흡기에 영향을 미치는 만성 질환"이다.두꺼운 분비물은 종종 염증과 심각한 폐 [158][159]감염을 일으키는 폐의 기도를 막는다.만약 그것이 손상된다면, 그것은 CF를 가진 사람의 삶의 질과 일상적인 [citation needed]일과 같은 일을 완수하는 능력에 영향을 미친다.
Schmitz와 Goldbeck(2006)에 따르면 CF는 개인과 가족 모두에게 정서적 스트레스를 크게 증가시키고, "필요한 시간이 걸리는 매일의 치료 [160]일상이 삶의 질에 더 부정적인 영향을 미칠 수 있다.그러나 Havermans와 동료들(2006)은 낭포성 섬유증 질문-개정에 참여한 젊은 CF 외래환자들이 "부모보다 삶의 [161]질 영역을 더 높게 평가했다"고 밝혔다.그 결과 CF 외래환자는 자신에 대해 보다 긍정적인 견해를 가지고 있다.Merck Manual에서 언급했듯이, "적절한 지원을 받으면 대부분의 환자는 가정과 학교에서 나이에 맞는 조정을 할 수 있습니다.수많은 문제에도 불구하고 환자의 교육적, 직업적, 결혼생활적 성공은 [138]인상적입니다.
게다가, CF 환자들의 삶의 질을 높일 수 있는 많은 방법들이 있다.운동은 폐 기능을 높이기 위해 촉진된다.운동요법을 CF환자의 일상에 통합하면 삶의 [162]질이 크게 향상될 수 있다.CF에 대한 확실한 치료법은 알려져 있지 않지만 [163]점액 이완, 기도 확장, 염증 감소, 폐 감염 퇴치를 목적으로 하는 점액 용해제, 기관지 확장제, 스테로이드제, 항생제 등 다양한 약물이 사용되고 있다.
역학
| 돌연변이 | 빈도수. 세계적[164] |
|---|---|
| δF508 | 66%~70%[18] |
| G542X | 2.4% |
| G551D | 1.6% |
| N1303K | 1.3% |
| W1282X | 1.2% |
| 기타 모든 것 | 27.5% |
낭포성 섬유증은 유럽 [165]유산 사람들 사이에서 생명을 제한하는 가장 흔한 상염색체 열성 질환이다.미국에서는 약 30,000명의 사람들이 CF를 가지고 있으며 대부분은 생후 6개월에 의해 진단된다.캐나다에서는 약 4,000명의 사람들이 [166]CF를 가지고 있다.유럽계 25명 중 1명꼴로 백인 미국인 [167]30명 중 1명은 CF 돌연변이의 매개체입니다.CF는 이들 집단에서 덜 흔하지만, 대략 46명 중 1명, 65명 중 1명, 그리고 90명 중 1명은 최소한 하나의 비정상적인 CFTR [168][169]유전자를 가지고 있다.아일랜드는 1353년에 [170]한 번꼴로 세계에서 가장 높은 CF 유병률을 보이고 있다.
엄밀히 말하면 희귀병이지만 CF는 가장 널리 퍼진 수명 단축 유전병 중 하나로 꼽히고 있다.그것은 서양의 국가들 사이에서 가장 흔하다.예외적으로 80명 중 1명만이 CF [171]변이를 가지고 있는 핀란드는 예외이다.세계보건기구(WHO)는 "유럽연합에서 2000~3000명 중 한 명의 신생아가 CF의 영향을 받는 것으로 나타났다"[172]고 밝히고 있다.미국에서는 3,500명 중 1명의 어린이가 [173]CF를 가지고 태어난다.1997년, 미국의 3,300명 중 한 명의 백인 아이들이 CF를 가지고 태어났다.반면 흑인 어린이 1만5000명 중 1명꼴로 발병률이 낮았다.아시아계속 아시아계 미국인은 32000명 [174]중 1명꼴로 발병률이 더 낮았다.
낭포성 섬유증은 남성과 여성 모두 동일하게 진단된다.최근 연구에 따르면 의료시설의 [177][178]개선으로 인해 이러한 성별 격차가 더 이상 존재하지 않을 수 있지만, 여전히 불분명한 이유로 인해 데이터는 남성이 [175][176]여성보다 기대수명이 더 긴 경향이 있는 것으로 나타났다.아일랜드의 최근 연구는 여성 호르몬인 에스트로겐과 [179]CF의 더 나쁜 결과 사이의 연관성을 확인했다.
CF 대립 유전자의 분포는 모집단마다 다르다.δF508 반송파의 주파수는 스웨덴 북부에서는 200명 중 1명, 리투아니아에서는 143명 중 1명, 덴마크에서는 38명 중 1명으로 추정된다.171명의 핀란드인과 151명의 Saami인 [180]중에서 δF508 캐리어는 발견되지 않았다.δF508은 핀란드에서 발생하지만 핀란드에서는 소수 대립 유전자이다.핀란드에서 [181]CF는 20개 과에서만 발생하는 것으로 알려져 있다.
진화
δF508 돌연변이는 최대 52,000년 [182]된 것으로 추정된다.왜 그러한 치명적인 돌연변이가 지속되고 인간들에게 퍼지는지에 대한 수많은 가설들이 발전되어 왔다.겸상적혈구 빈혈과 같은 다른 흔한 상염색체 열성 질환은 헤테로 접합체 장점으로 알려진 진화적 트레이드오프인 다른 질병으로부터 보균자를 보호하는 것으로 밝혀졌다.헤테로 접합체 장점의 가능한 원천으로 다음 모두에 대한 내성이 제안되었습니다.
- 콜레라:콜레라 독소가 정상 숙주 CFTR 단백질을 필요로 한다는 사실이 밝혀지면서 돌연변이 CFTR 유전자의 보균자가 콜레라 내성 등 [183][184]설사의 원인이라는 가설을 세웠다.그 이후의 연구들은 이 [185][186]가설을 입증하지 못했다.
- 장티푸스:CFTR 단백질은 또한 살모넬라 티피균이 [187]세포에 들어오기 위해 필수적이며, CFTR 유전자의 돌연변이 운반체가 장티푸스에 내성이 있을 수 있다는 것을 암시합니다.생체내 연구는 아직 이것을 확인하지 않았다.두 경우 모두 콜레라와 장티푸스가 유행하는 유럽 이외의 낭포성 섬유증의 낮은 수준은 즉시 설명되지 않는다.
- 설사:유럽에서의 CF의 유행은 소 사육의 발달과 관련이 있을지도 모른다.이 가설에서, 단일 돌연변이 CFTR의 보균자는 유당 내성을 만드는 돌연변이가 [188]나타나기 전에 유당 불내증으로 인한 설사로부터 어느 정도 보호를 받았다.
- 결핵:또 다른 가능한 설명은 유전자의 운반체가 [189][190]결핵에 대해 어느 정도 내성을 가질 수 있다는 것이다.이 가설은 CFTR 유전자 돌연변이 운반체가 마이코박테륨 결핵의 독성에 필요한 효소 중 하나인 아릴술파타아제에서 불충분한 작용을 한다는 논지에 기초하고 있다.M. 결핵은 숙주의 원천을 사용하여 개인에게 영향을 미치며, 효소의 부족으로 인해 독성을 나타낼 수 없기 때문에 CFTR 돌연변이의 매개체가 되는 것은 [191]결핵에 대한 내성을 제공할 수 있다.
역사

CF는 사람들의 이동, 유전자 돌연변이, 그리고 [192]영양의 새로운 조건 때문에 기원전 3,000년경에 나타났다고 여겨진다.CF의 전체 임상 스펙트럼은 1930년대까지 인식되지 않았지만 CF의 특정 측면이 훨씬 일찍 확인되었다.실제로 18세기 독일과 스위스의 문학은 CF염과 [192]염분 손실 사이의 연관성을 인식하면서 "Wehe dem Kind, das beim Kuf auf die Stirn salzig schmeckt, es verhext und mus bald sterben" (이마에 입을 맞추고 짠맛을 본 아이는 저주받으며 곧 죽어야 한다.)라고 경고했다.
19세기에 칼 폰 로키탄스키는 CF와 관련된 메코늄 회백염 합병증인 메코늄 복막염으로 인한 태아 사망 사례를 묘사했다.메코늄 일레우스는 1905년 Karl Landsteiner에 [192]의해 처음 기술되었다.1936년 귀도 판코니는 소아지방병, 췌장의 낭포성 섬유증,[193] 기관지 확장증 사이의 연관성을 설명했다.
1938년 도로시 한신 안데르센은 "췌장의 낭포성 섬유증과 셀리악 질환과의 관계: 임상적이고 병적인 연구"라는 논문을 미국 아동 질병 저널에 발표했다.그녀는 최초로 췌장의 특징적인 낭포성 섬유화를 설명하고 [12]CF에서 두드러지는 폐 및 장 질환과 연관지었습니다.그녀는 또한 먼저 CF가 열성 질환이라는 가설을 세우고 췌장 효소 대체제를 사용하여 감염된 아이들을 치료했습니다.1952년, Paul di Sant'Agnese는 땀 전해질에서 이상을 발견했다; 땀 테스트가 개발되었고 다음 [194]10년 동안 개선되었다.
CF와 다른 마커(Paroxonase) 사이의 첫 번째 연결은 1985년 Hans Eiberg에 의해 발견되었으며, CF에 대한 궤적이 하나만 있음을 나타냅니다.1988년 CF의 첫 번째 돌연변이인 δF508이 Francis Collins, Lap-Chee Tui 및 John R에 의해 발견되었다. 7번째 염색체에 리오단이 있어요후속 연구는 [citation needed]CF를 일으키는 1,000개 이상의 다른 돌연변이를 발견했다.
CFTR 유전자의 돌연변이는 전형적으로 작기 때문에, 고전적인 유전 기술은 돌연변이 [195]유전자를 정확하게 특정할 수 없었다.단백질 마커를 사용하여 유전자 연계 연구는 돌연변이를 7번 염색체에 매핑할 수 있었다.그 [196]후 염색체 보행과 염색체 점프 기술을 사용하여 유전자를 식별하고 배열했다.1989년, Lap-Chee Tui는 토론토에 있는 아픈 아이들을 위한 병원의 연구팀을 이끌고 CF의 원인이 되는 유전자를 발견했다.CF는 인간의 유전 질환이 유전학의 [citation needed]발달 과정에 의해 어떻게 엄격하게 설명되었는지를 보여주는 고전적인 예이다.
조사.
CF를 가진 사람들은 연구원과 의사들이 건강 결과를 추적하고 임상시험의 [197]후보자를 식별할 수 있도록 하는 질병 등록부에 등재될 수 있다.
유전자 치료
유전자 치료는 CF의 잠재적 치료법으로 연구되어 왔다.임상시험 결과는[update] 2016년 현재 제한적인 성공을 보이고 있으며 유전자 치료를 일상적인 치료로 사용하는 것은 [198]권장되지 않는다.2015년에 발표된 소규모 연구에서 작은 이점을 [199]발견했습니다.
CF 유전자 치료 연구의 초점은 CFTR 유전자의 정상적인 복사를 영향을 받는 세포에 배치하는 것을 목표로 한다.정상 CFTR 유전자를 영향을 받은 상피 세포로 이동시키면 부작용이나 염증 반응 없이 모든 표적 세포에서 기능성 CFTR 단백질이 생성된다.CF의 폐발현을 방지하기 위해 CFTR 유전자 발현은 정상량의 5~10%만 필요하다.[200]동물모델과 임상시험에서 리포좀과 바이러스 벡터와 같은 유전자 전달을 위한 여러 접근법이 테스트되었다.그러나 두 방법 모두 매우 적은 수의 세포가 벡터를 차지하고 유전자를 발현하기 때문에 치료 효과가 거의 없기 때문에 상대적으로 비효율적인 치료 [201]방법인 것으로 밝혀졌다.또한 cDNA 재조합에 문제가 있어 치료에 의해 도입된 유전자를 사용할 [202]수 없게 되었다.낭포성 섬유증 [203]환자의 장줄기세포 유기체에서 CRISPR/Cas9에 의한 CFTR 배양에 대한 기능적 복구가 있었다.
파지 요법
파지 요법은 [204][205]CF를 가진 사람들의 다제내성 박테리아에 대해 연구되고 있다.
유전자 변조기
CFTR 유전자의 다양한 돌연변이를 보상하는 것을 목표로 하는 많은 작은 분자들이 개발되고 있다.CFTR 변조 요법은 다른 유형의 유전자 치료법 대신 사용되어 왔다.이 치료법은 돌연변이 유전자 자체보다는 유전자 돌연변이의 발현에 초점을 맞추고 있다.변조기는 전위차 및 수정기의 두 가지 클래스로 나뉩니다.전위차제는 세포막에 내장된 CFTR 이온 채널에 작용하며, 이러한 종류의 약물은 막 통과 흐름을 허용하기 위해 채널을 개방하는 데 도움을 줍니다.수정기는 세포막에 [206]구현될 세포 표면으로의 리보솜에 의해 형성되는 단백질인 초기 단백질의 운반을 돕기 위한 것이다.
대부분은 유전자 발현의 전사 단계를 목표로 한다.한 가지 접근법은 리보솜이 정지 코돈을 극복하고 전체 길이의 CFTR 단백질을 생산하도록 하는 약물을 개발하고 시도하는 것이었다.CF의 약 10%는 DNA의 조기 정지 코돈에서 발생하며, 단백질 합성과 잘린 단백질의 조기 종료를 초래한다.이러한 약물은 위치 542의 아미노산 글리신으로 구성된 G542X와 같은 말도 안 되는 돌연변이를 중지 코돈으로 대체한다.아미노글리코시드 항생제는 단백질 합성과 오류 교정을 방해한다.경우에 따라서는 랜덤 아미노산을 삽입함으로써 세포가 조기 정지 코돈을 극복함으로써 전장 단백질의 발현을 가능하게 할 수 있다.이 조절기들에 대한 미래 연구는 유전자 발현 변화에 의해 영향을 받을 수 있는 세포 표적에 초점을 맞추고 있다.그렇지 않으면 낭포성 섬유증 환자의 10%가 이 [207]약물의 영향을 받지 않는다는 점을 감안해 조절기 요법이 효과가 없을 때 유전자 치료를 치료제로 활용하게 된다.
Elexacaftor/ivacaftor/tezacaftor는 2019년 미국에서 낭포성 섬유증으로 승인되었다.[208]이전에 개발된 이 약들의 조합은 낭포성 섬유증을 [206][208]가진 사람들의 90%까지 치료할 수 있다.이 약물은 CFTR 단백질의 효과를 회복시켜 [209]세포 표면에서 이온 채널 역할을 할 수 있도록 합니다.
생태 치료
종간 상호작용이 CF 폐감염의 병리학에 중요한 영향을 미치는 것으로 이전에 밝혀졌다.예를 들어, β-락타마아제 등의 항생제 분해 효소의 생산과 혐기성 종에 의한 짧은 사슬 지방산(SCFAs) 등의 대사 부산물의 생산은 Pseudomonas aeruginosa와 [210]같은 전통적인 병원체의 병원성을 높일 수 있다.이에 따라 CF 미생물 군집 구성과 대사 기능을 직접 변화시키는 것이 전통적인 항생제 [56]치료의 대안을 제공할 수 있을 것으로 제안되어 왔다.
사회와 문화
- 식스: 슈퍼마조히스트 밥 플래너건의 삶과 죽음, 1997년 다큐멘터리 영화
- 65 레드로스, 2009년 다큐멘터리 영화
- Laura Rodenberg의 회고록 Breathing for a Living
- Claire Wineland의 저서, Every Breaking I Treaked, Surviving and Blooming with Cystic Fibrosis
- 콜 스프라우스와 헤일리 루 리처드슨이 주연한 2019년 로맨틱 드라마 영화 파이브 피트 아파트
- 올라 틴슬리: CF캠페이터 올라 틴슬리에 관한 2018년 다큐멘터리 영화 '워리어'
- 마틴 오브라이언의 퍼포먼스 아트
- 컨티넨트 체이저, 여행자 및 CF 환자, 여행 및 CF 블로그 기록, continentchasers.com
메모들
레퍼런스
- ^ a b c d e f g h i j k l m n o p q r s t u O'Sullivan BP, Freedman SD (May 2009). "Cystic fibrosis". Lancet. 373 (9678): 1891–904. doi:10.1016/s0140-6736(09)60327-5. PMID 19403164. S2CID 46011502.
- ^ Allen JL, Panitch HB, Rubenstein RC (2016). Cystic Fibrosis. CRC Press. p. 92. ISBN 9781439801826. Archived from the original on 8 September 2017.
- ^ a b c d Massie J, Delatycki MB (December 2013). "Cystic fibrosis carrier screening". Paediatric Respiratory Reviews. 14 (4): 270–5. doi:10.1016/j.prrv.2012.12.002. PMID 23466339.
- ^ a b Ong T, Ramsey BW (September 2015). "Update in Cystic Fibrosis 2014". American Journal of Respiratory and Critical Care Medicine. 192 (6): 669–75. doi:10.1164/rccm.201504-0656UP. PMID 26371812.
- ^ Sencen, Lisa. "Cystic Fibrosis". NORD (National Organization for Rare Disorders). Retrieved 29 July 2022.
- ^ RESERVED, INSERM US14-- ALL RIGHTS. "Orphanet: Cystic fibrosis". www.orpha.net. Retrieved 29 July 2022.
- ^ a b c Hodson M, Geddes D, Bush A, eds. (2012). Cystic Fibrosis (3rd ed.). London: Hodder Arnold. p. 3. ISBN 978-1-4441-1369-3. Archived from the original on 8 September 2017.
- ^ Buckingham L (2012). Molecular Diagnostics: Fundamentals, Methods and Clinical Applications (2nd ed.). Philadelphia: F.A. Davis Co. p. 351. ISBN 978-0-8036-2975-2. Archived from the original on 8 September 2017.
- ^ Yankaskas JR, Marshall BC, Sufian B, Simon RH, Rodman D (January 2004). "Cystic fibrosis adult care: consensus conference report". Chest. 125 (1 Suppl): 1S–39S. CiteSeerX 10.1.1.562.1904. doi:10.1378/chest.125.1_suppl.1S. PMID 14734689.
- ^ a b Warnock L, Gates A (December 2015). "Chest physiotherapy compared to no chest physiotherapy for cystic fibrosis". The Cochrane Database of Systematic Reviews. 2015 (12): CD001401. doi:10.1002/14651858.CD001401.pub3. PMC 6768986. PMID 26688006.
- ^ Nazareth D, Walshaw M (October 2013). "Coming of age in cystic fibrosis - transition from paediatric to adult care". Clinical Medicine. 13 (5): 482–6. doi:10.7861/clinmedicine.13-5-482. PMC 4953800. PMID 24115706.
- ^ a b Andersen DH (1938). "Cystic fibrosis of the pancreas and its relation to celiac disease: a clinical and pathological study". Am. J. Dis. Child. 56 (2): 344–99. doi:10.1001/archpedi.1938.01980140114013.
- ^ a b c d Egan, Schechter & Voynow 2020, "임상 징후"
- ^ a b c d e f Egan, Schechter & Voynow 2020, "호흡로"
- ^ Shteinberg M, Haq IJ, Polineni D, Davies JC (June 2021). "Cystic fibrosis". Lancet. 397 (10290): 2195–2211. doi:10.1016/S0140-6736(20)32542-3. PMID 34090606. S2CID 235327978.
- ^ Reaves J, Wallace G (2010). "Unexplained bruising: weighing the pros and cons of possible causes". Consultant for Pediatricians. 9: 201–2. Archived from the original on 22 February 2020. Retrieved 22 February 2020.
- ^ Flume PA, Mogayzel PJ, Robinson KA, Rosenblatt RL, Quittell L, Marshall BC (August 2010). "Cystic fibrosis pulmonary guidelines: pulmonary complications: hemoptysis and pneumothorax". American Journal of Respiratory and Critical Care Medicine. 182 (3): 298–306. doi:10.1164/rccm.201002-0157OC. PMID 20675678.
- ^ a b c d e f g h i j k l m n o p q r s t Mitchell RS, Kumar V, Robbins SL, et al. (2007). Robbins Basic Pathology. Saunders/Elsevier. p. 1253, 1254. ISBN 978-1-4160-2973-1.
- ^ a b c d Rowe SM, Miller S, Sorscher EJ (May 2005). "Cystic fibrosis". The New England Journal of Medicine. 352 (19): 1992–2001. doi:10.1056/NEJMra043184. PMID 15888700.
- ^ Saiman L, Siegel J (January 2004). "Infection control in cystic fibrosis". Clinical Microbiology Reviews. 17 (1): 57–71. doi:10.1128/CMR.17.1.57-71.2004. PMC 321464. PMID 14726455.
- ^ Girón RM, Domingo D, Buendía B, Antón E, Ruiz-Velasco LM, Ancochea J (October 2005). "[Nontuberculous mycobacteria in patients with cystic fibrosis]". Archivos de Bronconeumologia (in Spanish). 41 (10): 560–5. doi:10.1016/S1579-2129(06)60283-8. PMID 16266669.
- ^ Franco LP, Camargos PA, Becker HM, Guimarães RE (2009). "Nasal endoscopic evaluation of children and adolescents with cystic fibrosis". Brazilian Journal of Otorhinolaryngology. 75 (6): 806–13. doi:10.1590/S1808-86942009000600006. PMID 20209279.
- ^ Maldonado M, Martínez A, Alobid I, Mullol J (December 2004). "The antrochoanal polyp". Rhinology. 42 (4): 178–82. PMID 15626248.
- ^ Ramsey B, Richardson MA (September 1992). "Impact of sinusitis in cystic fibrosis". The Journal of Allergy and Clinical Immunology. 90 (3 Pt 2): 547–52. doi:10.1016/0091-6749(92)90183-3. PMID 1527348.
- ^ Kulczycki LL, Shwachman H (August 1958). "Studies in cystic fibrosis of the pancreas; occurrence of rectal prolapse". The New England Journal of Medicine. 259 (9): 409–12. doi:10.1056/NEJM195808282590901. PMID 13578072.
- ^ Cohn JA, Friedman KJ, Noone PG, Knowles MR, Silverman LM, Jowell PS (September 1998). "Relation between mutations of the cystic fibrosis gene and idiopathic pancreatitis". The New England Journal of Medicine. 339 (10): 653–8. doi:10.1056/NEJM199809033391002. PMID 9725922.
- ^ a b c Assis DN, Freedman SD (March 2016). "Gastrointestinal Disorders in Cystic Fibrosis". Clinics in Chest Medicine (Review). 37 (1): 109–118. doi:10.1016/j.ccm.2015.11.004. PMID 26857772.
- ^ Malfroot A, Dab I (November 1991). "New insights on gastro-oesophageal reflux in cystic fibrosis by longitudinal follow up". Archives of Disease in Childhood. 66 (11): 1339–1345. doi:10.1136/adc.66.11.1339. PMC 1793275. PMID 1755649.
- ^ a b c d Carroll, Will; Green, Jessica; Gilchrist, Francis J. (22 December 2021). "Interventions for preventing distal intestinal obstruction syndrome (DIOS) in cystic fibrosis". The Cochrane Database of Systematic Reviews. 2021 (12): CD012619. doi:10.1002/14651858.CD012619.pub3. ISSN 1469-493X. PMC 8693853. PMID 34936085.
- ^ Williams SG, Westaby D, Tanner MS, Mowat AP (October 1992). "Liver and biliary problems in cystic fibrosis". British Medical Bulletin. 48 (4): 877–92. doi:10.1093/oxfordjournals.bmb.a072583. PMID 1458306.
- ^ Colombo C, Russo MC, Zazzeron L, Romano G (July 2006). "Liver disease in cystic fibrosis". Journal of Pediatric Gastroenterology and Nutrition. 43 (Suppl 1): S49-55. doi:10.1097/01.mpg.0000226390.02355.52. PMID 16819402. S2CID 27836468.
- ^ Egan, Schechter & Voynow 2020, "담관"
- ^ Moran A, Pyzdrowski KL, Weinreb J, Kahn BB, Smith SA, Adams KS, Seaquist ER (August 1994). "Insulin sensitivity in cystic fibrosis". Diabetes. 43 (8): 1020–6. doi:10.2337/diabetes.43.8.1020. PMID 8039595.
- ^ a b c de Aragão Dantas Alves C, Aguiar RA, Alves AC, Santana MA (2007). "Diabetes mellitus in patients with cystic fibrosis". Jornal Brasileiro de Pneumologia. 33 (2): 213–21. doi:10.1590/S1806-37132007000200017. PMID 17724542.
- ^ Haworth CS, Selby PL, Webb AK, Dodd ME, Musson H, McL Niven R, et al. (November 1999). "Low bone mineral density in adults with cystic fibrosis". Thorax. 54 (11): 961–7. doi:10.1136/thx.54.11.961. PMC 1745400. PMID 10525552.
- ^ McCallum TJ, Milunsky JM, Cunningham DL, Harris DH, Maher TA, Oates RD (October 2000). "Fertility in men with cystic fibrosis: an update on current surgical practices and outcomes". Chest. 118 (4): 1059–62. doi:10.1378/chest.118.4.1059. PMID 11035677.
- ^ Chen H, Ruan YC, Xu WM, Chen J, Chan HC (2012). "Regulation of male fertility by CFTR and implications in male infertility". Human Reproduction Update. 18 (6): 703–13. doi:10.1093/humupd/dms027. PMID 22709980.
- ^ Augarten A, Yahav Y, Kerem BS, Halle D, Laufer J, Szeinberg A, et al. (November 1994). "Congenital bilateral absence of vas deferens in the absence of cystic fibrosis". Lancet. 344 (8935): 1473–4. doi:10.1016/S0140-6736(94)90292-5. PMID 7968122. S2CID 28860665.
- ^ Gilljam M, Antoniou M, Shin J, Dupuis A, Corey M, Tullis DE (July 2000). "Pregnancy in cystic fibrosis. Fetal and maternal outcome". Chest. 118 (1): 85–91. doi:10.1378/chest.118.1.85. PMID 10893364. S2CID 32289370.
- ^ Guimbellot J, Sharma J, Rowe SM (November 2017). "Toward inclusive therapy with CFTR modulators: Progress and challenges". Pediatric Pulmonology. 52 (S48): S4–S14. doi:10.1002/ppul.23773. PMC 6208153. PMID 28881097.
- ^ Sharma J, Keeling KM, Rowe SM (August 2020). "Pharmacological approaches for targeting cystic fibrosis nonsense mutations". European Journal of Medicinal Chemistry. 200: 112436. doi:10.1016/j.ejmech.2020.112436. PMC 7384597. PMID 32512483.
- ^ Bobadilla JL, Macek M, Fine JP, Farrell PM (June 2002). "Cystic fibrosis: a worldwide analysis of CFTR mutations--correlation with incidence data and application to screening". Human Mutation. 19 (6): 575–606. doi:10.1002/humu.10041. PMID 12007216. S2CID 35428054.
- ^ a b c Elborn JS (November 2016). "Cystic fibrosis". Lancet. 388 (10059): 2519–2531. doi:10.1016/S0140-6736(16)00576-6. PMID 27140670. S2CID 20948144.
- ^ Short DB, Trotter KW, Reczek D, Kreda SM, Bretscher A, Boucher RC, et al. (July 1998). "An apical PDZ protein anchors the cystic fibrosis transmembrane conductance regulator to the cytoskeleton". The Journal of Biological Chemistry. 273 (31): 19797–801. doi:10.1074/jbc.273.31.19797. PMID 9677412.
- ^ Travaglini KJ, Krasnow MA (August 2018). "Profile of an unknown airway cell". Nature. 560 (7718): 313–314. Bibcode:2018Natur.560..313T. doi:10.1038/d41586-018-05813-7. PMID 30097657.
- ^ a b Edwards QT, Seibert D, Macri C, Covington C, Tilghman J (November 2004). "Assessing ethnicity in preconception counseling: genetics--what nurse practitioners need to know". Journal of the American Academy of Nurse Practitioners. 16 (11): 472–80. doi:10.1111/j.1745-7599.2004.tb00426.x. PMID 15617360. S2CID 7644129.
- ^ Wang, Xiaodong Robert; Li, Chenglong (6 May 2014). "Decoding F508del Misfolding in Cystic Fibrosis". Biomolecules. 4 (2): 498–509. doi:10.3390/biom4020498. ISSN 2218-273X. PMC 4101494. PMID 24970227.
- ^ Childers M, Eckel G, Himmel A, Caldwell J (2007). "A new model of cystic fibrosis pathology: lack of transport of glutathione and its thiocyanate conjugates". Medical Hypotheses. 68 (1): 101–12. doi:10.1016/j.mehy.2006.06.020. PMID 16934416.
- ^ Xu Y, Szép S, Lu Z (December 2009). "The antioxidant role of thiocyanate in the pathogenesis of cystic fibrosis and other inflammation-related diseases". Proceedings of the National Academy of Sciences of the United States of America. 106 (48): 20515–9. Bibcode:2009PNAS..10620515X. doi:10.1073/pnas.0911412106. PMC 2777967. PMID 19918082.
- ^ Moskwa P, Lorentzen D, Excoffon KJ, Zabner J, McCray PB, Nauseef WM, et al. (January 2007). "A novel host defense system of airways is defective in cystic fibrosis". American Journal of Respiratory and Critical Care Medicine. 175 (2): 174–83. doi:10.1164/rccm.200607-1029OC. PMC 2720149. PMID 17082494.
- ^ Conner GE, Wijkstrom-Frei C, Randell SH, Fernandez VE, Salathe M (January 2007). "The lactoperoxidase system links anion transport to host defense in cystic fibrosis". FEBS Letters. 581 (2): 271–8. doi:10.1016/j.febslet.2006.12.025. PMC 1851694. PMID 17204267.
- ^ Haq IJ, Gray MA, Garnett JP, Ward C, Brodlie M (March 2016). "Airway surface liquid homeostasis in cystic fibrosis: pathophysiology and therapeutic targets". Thorax. 71 (3): 284–287. doi:10.1136/thoraxjnl-2015-207588. PMID 26719229.
- ^ Verkman AS, Song Y, Thiagarajah JR (January 2003). "Role of airway surface liquid and submucosal glands in cystic fibrosis lung disease". American Journal of Physiology. Cell Physiology. 284 (1): C2-15. doi:10.1152/ajpcell.00417.2002. PMID 12475759. S2CID 11790119.
- ^ Marieb EN, Hoehn K, Hutchinson M (2014). "22: The Respiratory System". Human Anatomy and Physiology. Pearson Education. p. 906. ISBN 978-0805361179.
- ^ a b Saiman L (2004). "Microbiology of early CF lung disease". Paediatric Respiratory Reviews. 5 (Suppl A): S367-9. doi:10.1016/S1526-0542(04)90065-6. PMID 14980298.
- ^ a b Khanolkar RA, Clark ST, Wang PW, et al. (2020). "Ecological Succession of Polymicrobial Communities in the Cystic Fibrosis Airways". mSystems. 5 (6): e00809-20. doi:10.1128/mSystems.00809-20. PMC 7716390. PMID 33262240.
- ^ a b Lorè NI, Cigana C, Riva C, De Fino I, Nonis A, Spagnuolo L, et al. (May 2016). "IL-17A impairs host tolerance during airway chronic infection by Pseudomonas aeruginosa". Scientific Reports. 6: 25937. Bibcode:2016NatSR...625937L. doi:10.1038/srep25937. PMC 4870500. PMID 27189736.
- ^ Tümmler B, Koopmann U, Grothues D, Weissbrodt H, Steinkamp G, von der Hardt H (June 1991). "Nosocomial acquisition of Pseudomonas aeruginosa by cystic fibrosis patients". Journal of Clinical Microbiology. 29 (6): 1265–7. Bibcode:1991JPoSA..29.1265A. doi:10.1002/pola.1991.080290905. PMC 271975. PMID 1907611.
- ^ Centers for Disease Control Prevention (CDC) (June 1993). "Pseudomonas cepacia at summer camps for persons with cystic fibrosis". MMWR. Morbidity and Mortality Weekly Report. 42 (23): 456–9. PMID 7684813.
- ^ Pegues DA, Carson LA, Tablan OC, FitzSimmons SC, Roman SB, Miller JM, Jarvis WR (May 1994). "Acquisition of Pseudomonas cepacia at summer camps for patients with cystic fibrosis. Summer Camp Study Group". The Journal of Pediatrics. 124 (5 Pt 1): 694–702. doi:10.1016/S0022-3476(05)81357-5. PMID 7513755.
- ^ Pankhurst CL, Philpott-Howard J (April 1996). "The environmental risk factors associated with medical and dental equipment in the transmission of Burkholderia (Pseudomonas) cepacia in cystic fibrosis patients". The Journal of Hospital Infection. 32 (4): 249–55. doi:10.1016/S0195-6701(96)90035-3. PMID 8744509.
- ^ Jones AM, Govan JR, Doherty CJ, Dodd ME, Isalska BJ, Stanbridge TN, Webb AK (June 2003). "Identification of airborne dissemination of epidemic multiresistant strains of Pseudomonas aeruginosa at a CF centre during a cross infection outbreak". Thorax. 58 (6): 525–7. doi:10.1136/thorax.58.6.525. PMC 1746694. PMID 12775867.
- ^ Høiby N (June 1995). "Isolation and treatment of cystic fibrosis patients with lung infections caused by Pseudomonas (Burkholderia) cepacia and multiresistant Pseudomonas aeruginosa". The Netherlands Journal of Medicine. 46 (6): 280–7. doi:10.1016/0300-2977(95)00020-N. PMID 7643943.
- ^ a b Pihet M, Carrere J, Cimon B, Chabasse D, Delhaes L, Symoens F, Bouchara JP (June 2009). "Occurrence and relevance of filamentous fungi in respiratory secretions of patients with cystic fibrosis--a review". Medical Mycology. 47 (4): 387–97. doi:10.1080/13693780802609604. PMID 19107638.
- ^ Rapaka RR, Kolls JK (2009). "Pathogenesis of allergic bronchopulmonary aspergillosis in cystic fibrosis: current understanding and future directions". Medical Mycology. 47 (Suppl 1): S331-7. doi:10.1080/13693780802266777. PMID 18668399.
- ^ "Newborn Screening for CF". Cystic Fibrosis Foundation. Retrieved 25 January 2022.
- ^ a b Egan, Schechter 및 Voynow 2020, "진단 및 평가"
- ^ Farrell PM, White TB, Ren CL, Hempstead SE, Accurso F, Derichs N, Howenstine M, McColley SA, Rock M, Rosenfeld M, Sermet-Gaudelus I, Southern KW, Marshall BC, Sosnay PR (February 2017). "Diagnosis of Cystic Fibrosis: Consensus Guidelines from the Cystic Fibrosis Foundation". J Pediatr. 181S: S4–S15.e1. doi:10.1016/j.jpeds.2016.09.064. PMID 28129811. S2CID 206410545.
- ^ Minarowski Ł, Sands D, Minarowska A, Karwowska A, Sulewska A, Gacko M, Chyczewska E (2008). "Thiocyanate concentration in saliva of cystic fibrosis patients". Folia Histochemica et Cytobiologica. 46 (2): 245–6. doi:10.2478/v10042-008-0037-0. PMID 18519245.
- ^ Stern RC (February 1997). "The diagnosis of cystic fibrosis". The New England Journal of Medicine. 336 (7): 487–91. doi:10.1056/NEJM199702133360707. PMID 9017943.
- ^ Ross LF (September 2008). "Newborn screening for cystic fibrosis: a lesson in public health disparities". The Journal of Pediatrics. 153 (3): 308–13. doi:10.1016/j.jpeds.2008.04.061. PMC 2569148. PMID 18718257.
- ^ Assael BM, Castellani C, Ocampo MB, Iansa P, Callegaro A, Valsecchi MG (September 2002). "Epidemiology and survival analysis of cystic fibrosis in an area of intense neonatal screening over 30 years". American Journal of Epidemiology. 156 (5): 397–401. doi:10.1093/aje/kwf064. PMID 12196308.
- ^ Hoch H, Sontag MK, Scarbro S, Juarez-Colunga E, McLean C, Kempe A, Sagel SD (November 2018). "Clinical outcomes in U.S. infants with cystic fibrosis from 2001 to 2012". Pediatric Pulmonology. 53 (11): 1492–1497. doi:10.1002/ppul.24165. PMID 30259702. S2CID 52845580.
- ^ Barben, Jürg, et al. (2017). "The expansion and performance of national newborn screening programmes for cystic fibrosis in Europe". Journal of Cystic Fibrosis. 16 (2): 207–13. doi:10.1016/j.jcf.2016.12.012. PMID 28043799.
- ^ "Carrier Screening in the Age of Genomic Medicine". American College of Obstetricians and Gynecologists. 2017. Archived from the original on 25 February 2017. Retrieved 22 February 2020.
- ^ Elias S, Annas GJ, Simpson JL (April 1991). "Carrier screening for cystic fibrosis: implications for obstetric and gynecologic practice". American Journal of Obstetrics and Gynecology. 164 (4): 1077–83. doi:10.1016/0002-9378(91)90589-j. PMID 2014829.
- ^ Tabor A, Philip J, Madsen M, Bang J, Obel EB, Nørgaard-Pedersen B (June 1986). "Randomised controlled trial of genetic amniocentesis in 4606 low-risk women". Lancet. 1 (8493): 1287–93. doi:10.1016/S0140-6736(86)91218-3. PMID 2423826. S2CID 31237495.
- ^ Eddleman KA, Malone FD, Sullivan L, Dukes K, Berkowitz RL, Kharbutli Y, et al. (November 2006). "Pregnancy loss rates after midtrimester amniocentesis". Obstetrics and Gynecology. 108 (5): 1067–72. doi:10.1097/01.AOG.0000240135.13594.07. PMID 17077226. S2CID 19081825.
- ^ Davis LB, Champion SJ, Fair SO, Baker VL, Garber AM (April 2010). "A cost-benefit analysis of preimplantation genetic diagnosis for carrier couples of cystic fibrosis". Fertility and Sterility. 93 (6): 1793–804. doi:10.1016/j.fertnstert.2008.12.053. PMID 19439290.
- ^ a b "Abstracts from the 25th Italian Congress of Cystic Fibrosis and the 15th National Congress of Cystic Fibrosis Italian Society : Assago, Milan. 10 - 12 October 2019". Italian Journal of Pediatrics. 46 (Suppl 1): 32. April 2020. doi:10.1186/s13052-020-0790-z. PMC 7110616. PMID 32234058.
- ^ Wingårdh AS, Göransson C, Larsson S, Slinde F, Vanfleteren LE (2020). "Effectiveness of Energy Conservation Techniques in Patients with COPD". Respiration; International Review of Thoracic Diseases. 99 (5): 409–416. doi:10.1159/000506816. PMC 7265758. PMID 32272478.
- ^ Davies JC, Alton EW, Bush A (December 2007). "Cystic fibrosis". BMJ. 335 (7632): 1255–9. doi:10.1136/bmj.39391.713229.AD. PMC 2137053. PMID 18079549.
- ^ Hayes D, Wilson KC, Krivchenia K, Hawkins SM, Balfour-Lynn IM, Gozal D, et al. (February 2019). "Home Oxygen Therapy for Children. An Official American Thoracic Society Clinical Practice Guideline". American Journal of Respiratory and Critical Care Medicine. 199 (3): e5–e23. doi:10.1164/rccm.201812-2276ST. PMC 6802853. PMID 30707039.
- ^ Coffey MJ, Garg M, Homaira N, Jaffe A, Ooi CY (January 2020). "Probiotics for people with cystic fibrosis". The Cochrane Database of Systematic Reviews. 1: CD012949. doi:10.1002/14651858.CD012949.pub2. PMC 6984633. PMID 31962375.
- ^ Pai VB, Nahata MC (October 2001). "Efficacy and safety of aerosolized tobramycin in cystic fibrosis". Pediatric Pulmonology. 32 (4): 314–27. doi:10.1002/ppul.1125. PMID 11568993. S2CID 30108514.
- ^ Westerman EM, Le Brun PP, Touw DJ, Frijlink HW, Heijerman HG (March 2004). "Effect of nebulized colistin sulphate and colistin sulphomethate on lung function in patients with cystic fibrosis: a pilot study". Journal of Cystic Fibrosis. 3 (1): 23–8. doi:10.1016/j.jcf.2003.12.005. PMID 15463883.
- ^ McCoy KS, Quittner AL, Oermann CM, Gibson RL, Retsch-Bogart GZ, Montgomery AB (November 2008). "Inhaled aztreonam lysine for chronic airway Pseudomonas aeruginosa in cystic fibrosis". American Journal of Respiratory and Critical Care Medicine. 178 (9): 921–8. doi:10.1164/rccm.200712-1804OC. PMC 2577727. PMID 18658109.
- ^ Ryan G, Singh M, Dwan K (March 2011). "Inhaled antibiotics for long-term therapy in cystic fibrosis". The Cochrane Database of Systematic Reviews (3): CD001021. doi:10.1002/14651858.CD001021.pub2. PMID 21412868.
- ^ "Quinsair (levofloxacin)". European Medicines Agency. Archived from the original on 26 December 2016. Retrieved 26 December 2016.
- ^ Langton Hewer SC, Smyth AR (April 2017). "Antibiotic strategies for eradicating Pseudomonas aeruginosa in people with cystic fibrosis" (PDF). The Cochrane Database of Systematic Reviews. 4 (4): CD004197. doi:10.1002/14651858.CD004197.pub5. PMC 6478104. PMID 28440853. Archived from the original (PDF) on 24 February 2019. Retrieved 22 January 2019.
- ^ Smith S, Ratjen F, Remmington T, Waters V (May 2020). "Combination antimicrobial susceptibility testing for acute exacerbations in chronic infection of Pseudomonas aeruginosa in cystic fibrosis". The Cochrane Database of Systematic Reviews. 5 (4): CD006961. doi:10.1002/14651858.CD006961.pub5. PMC 7387858. PMID 32412092.
- ^ Hansen CR, Pressler T, Koch C, Høiby N (March 2005). "Long-term azitromycin treatment of cystic fibrosis patients with chronic Pseudomonas aeruginosa infection; an observational cohort study". Journal of Cystic Fibrosis. 4 (1): 35–40. doi:10.1016/j.jcf.2004.09.001. PMID 15752679.
- ^ Tan KH, Mulheran M, Knox AJ, Smyth AR (March 2003). "Aminoglycoside prescribing and surveillance in cystic fibrosis". American Journal of Respiratory and Critical Care Medicine. 167 (6): 819–23. doi:10.1164/rccm.200109-012CC. PMID 12623858.
- ^ "Antibiotic resistance". Fact Sheet. World Health Organization. 31 July 2020. Retrieved 24 June 2022.
- ^ Hurley MN, Smith S, Forrester DL, Smyth AR (July 2020). "Antibiotic adjuvant therapy for pulmonary infection in cystic fibrosis". The Cochrane Database of Systematic Reviews. 7 (9): CD008037. doi:10.1002/14651858.CD008037.pub4. PMC 8407502. PMID 32671834.
- ^ Lord R, Jones AM, Horsley A (April 2020). "Antibiotic treatment for Burkholderia cepacia complex in people with cystic fibrosis experiencing a pulmonary exacerbation". The Cochrane Database of Systematic Reviews. 2020 (4): CD009529. doi:10.1002/14651858.CD009529.pub4. PMC 7117566. PMID 32239690.
- ^ Waters V, Ratjen F (June 2020). "Antibiotic treatment for nontuberculous mycobacteria lung infection in people with cystic fibrosis". The Cochrane Database of Systematic Reviews. 6: CD010004. doi:10.1002/14651858.CD010004.pub5. PMC 7389742. PMID 32521055.
- ^ Kuver R, Lee SP (April 2006). "Hypertonic saline for cystic fibrosis". The New England Journal of Medicine. 354 (17): 1848–51, author reply 1848–51. doi:10.1056/NEJMc060351. PMID 16642591.
- ^ Lieberman J (July 1968). "Dornase aerosol effect on sputum viscosity in cases of cystic fibrosis". JAMA. 205 (5): 312–3. doi:10.1001/jama.205.5.312. PMID 5694947.
- ^ a b Yang C, Montgomery M, et al. (Cochrane Cystic Fibrosis and Genetic Disorders Group) (March 2021). "Dornase alfa for cystic fibrosis". The Cochrane Database of Systematic Reviews. 2021 (3): CD001127. doi:10.1002/14651858.CD001127.pub5. PMC 8094421. PMID 33735508.
- ^ Kellerman D, Rossi Mospan A, Engels J, Schaberg A, Gorden J, Smiley L (August 2008). "Denufosol: a review of studies with inhaled P2Y(2) agonists that led to Phase 3". Pulmonary Pharmacology & Therapeutics. 21 (4): 600–7. doi:10.1016/j.pupt.2007.12.003. PMID 18276176.
- ^ a b Balfour-Lynn IM, Welch K, Smith S (July 2019). "Inhaled corticosteroids for cystic fibrosis". The Cochrane Database of Systematic Reviews. 7 (4): CD001915. doi:10.1002/14651858.CD001915.pub6. PMC 6609325. PMID 31271656.
- ^ Burgess L, Southern KW (August 2014). Burgess L (ed.). "Pneumococcal vaccines for cystic fibrosis". The Cochrane Database of Systematic Reviews. 8 (8): CD008865. doi:10.1002/14651858.CD008865.pub3. PMID 25093421.
- ^ Dharmaraj P, Smyth RL (March 2014). "Vaccines for preventing influenza in people with cystic fibrosis". The Cochrane Database of Systematic Reviews. 2021 (3): CD001753. doi:10.1002/14651858.CD001753.pub3. PMC 7066935. PMID 24604671.
- ^ a b c Whiting P, Al M, Burgers L, Westwood M, Ryder S, Hoogendoorn M, et al. (March 2014). "Ivacaftor for the treatment of patients with cystic fibrosis and the G551D mutation: a systematic review and cost-effectiveness analysis". Health Technology Assessment. 18 (18): 1–106. doi:10.3310/hta18180. PMC 4780965. PMID 24656117.
- ^ Wainwright CE (October 2014). "Ivacaftor for patients with cystic fibrosis". Expert Review of Respiratory Medicine. 8 (5): 533–8. doi:10.1586/17476348.2014.951333. PMID 25148205. S2CID 39537446.
- ^ Office of the Commissioner. "Press Announcements - FDA approves new treatment for cystic fibrosis". www.fda.gov. Archived from the original on 18 January 2017. Retrieved 16 January 2017.
- ^ "FDA approves another Vertex drug for treatment of cystic fibrosis - The Boston Globe". The Boston Globe.
- ^ "Tezacaftor (VX-661) for Cystic Fibrosis - Cystic Fibrosis News Today". Archived from the original on 29 September 2018. Retrieved 23 December 2018.
- ^ a b "Trikafta (elexacaftor, ivacaftor and tezacaftor) FDA Approval History". Drugs.com.
- ^ Commissioner, Office of the (24 March 2020). "FDA approves new breakthrough therapy for cystic fibrosis". FDA. Retrieved 28 April 2022.
- ^ "FDA Accepts Vertex Application for Expansion of Trikafta to Include Children ages 6-11 Cystic Fibrosis Foundation". www.cff.org. Retrieved 28 April 2022.
- ^ "NHS England » Landmark NHS deal to open up access to life-changing cystic fibrosis drug". www.england.nhs.uk. Retrieved 8 August 2021.
- ^ Office of the Commissioner (24 March 2020). "FDA approves new breakthrough therapy for cystic fibrosis". FDA. Retrieved 12 August 2020.
- ^ a b "Cystic Fibrosis Foundation statement on FDA approval of Trikafta™, the first triple-combination therapy for the most common CF mutation". www.cff.org. Bethesda, Md.: Cystic Fibrosis Foundation. Retrieved 12 August 2020.
- ^ a b Middleton PG, Mall MA, Dřevínek P, Lands LC, McKone EF, Polineni D, et al. (November 2019). "Elexacaftor-Tezacaftor-Ivacaftor for Cystic Fibrosis with a Single Phe508del Allele". The New England Journal of Medicine. 381 (19): 1809–1819. doi:10.1056/NEJMoa1908639. PMC 7282384. PMID 31697873.
- ^ Ridley K, Condren M (1 April 2020). "Elexacaftor-Tezacaftor-Ivacaftor: The First Triple-Combination Cystic Fibrosis Transmembrane Conductance Regulator Modulating Therapy". The Journal of Pediatric Pharmacology and Therapeutics. 25 (3): 192–197. doi:10.5863/1551-6776-25.3.192. PMC 7134581. PMID 32265602.
- ^ "Vertex prices cystic fibrosis combo treatment at $311,000-per-year". Reuters. 21 October 2019. Retrieved 23 October 2019.
- ^ Good News Network (3 November 2019). "FDA Approves the First New Cystic Fibrosis Treatment in Decades". Good News Network. Retrieved 12 August 2020.
- ^ Cheng K, Ashby D, Smyth RL (September 2017). "Ursodeoxycholic acid for cystic fibrosis-related liver disease". The Cochrane Database of Systematic Reviews. 9 (4): CD000222. doi:10.1002/14651858.CD000222.pub4. PMC 6483662. PMID 28891588.
- ^ de Vries JJ, Chang AB, Bonifant CM, Shevill E, Marchant JM (August 2018). "Vitamin A and beta (β)-carotene supplementation for cystic fibrosis". The Cochrane Database of Systematic Reviews. 8: CD006751. doi:10.1002/14651858.CD006751.pub5. PMC 6513379. PMID 30091146.
- ^ Ferguson JH, Chang AB (May 2014). "Vitamin D supplementation for cystic fibrosis". The Cochrane Database of Systematic Reviews (5): CD007298. doi:10.1002/14651858.CD007298.pub4. PMID 24823922.
- ^ Okebukola PO, Kansra S, Barrett J (September 2020). "Vitamin E supplementation in people with cystic fibrosis". The Cochrane Database of Systematic Reviews. 2020 (9): CD009422. doi:10.1002/14651858.CD009422.pub4. PMC 8406985. PMID 32892350.
- ^ Jagannath VA, Thaker V, Chang AB, Price AI (June 2020). "Vitamin K supplementation for cystic fibrosis". The Cochrane Database of Systematic Reviews. John Wiley & sons, Ltd. 6 (6): CD008482. doi:10.1002/14651858.CD008482.pub6. PMC 7272115. PMID 32497260.
- ^ Watson H, Stackhouse C (April 2020). "Omega-3 fatty acid supplementation for cystic fibrosis". The Cochrane Database of Systematic Reviews. 4: CD002201. doi:10.1002/14651858.CD002201.pub6. PMC 7147930. PMID 32275788.
- ^ McIlwaine M, Button B, Nevitt SJ (November 2019). "Positive expiratory pressure physiotherapy for airway clearance in people with cystic fibrosis". The Cochrane Database of Systematic Reviews. 2019 (11). doi:10.1002/14651858.CD003147.pub5. PMC 6953327. PMID 31774149.
- ^ Andersen JB, Qvist J, Kann T (October 1979). "Recruiting collapsed lung through collateral channels with positive end-expiratory pressure". Scandinavian Journal of Respiratory Diseases. 60 (5): 260–6. PMID 392747.
- ^ Groth S, Stafanger G, Dirksen H, Andersen JB, Falk M, Kelstrup M (July 1985). "Positive expiratory pressure (PEP-mask) physiotherapy improves ventilation and reduces volume of trapped gas in cystic fibrosis". Bulletin Européen de Physiopathologie Respiratoire. 21 (4): 339–43. PMID 3899222.
- ^ a b c Moran F, Bradley JM, Piper AJ (February 2017). "Non-invasive ventilation for cystic fibrosis". The Cochrane Database of Systematic Reviews. 2: CD002769. doi:10.1002/14651858.CD002769.pub5. PMC 6464053. PMID 28218802.
- ^ Moran F, Bradley JM, Piper AJ (February 2017). "Non-invasive ventilation for cystic fibrosis". The Cochrane Database of Systematic Reviews. 2 (2): CD002769. doi:10.1002/14651858.CD002769.pub5. PMC 6464053. PMID 28218802.
- ^ "Tracheostomy Why it's used". NHS. 3 October 2018. Retrieved 10 May 2020.
- ^ Molnar H. "Types of Tracheostomy Tubes".
- ^ Huth MM, Zink KA, Van Horn NR (2005). "The effects of massage therapy in improving outcomes for youth with cystic fibrosis: an evidence review". Pediatric Nursing. 31 (4): 328–32. PMID 16229132.
- ^ Leinwand MJ (28 December 2019). Windle ML, Odim J (eds.). "Surgical Treatment of Infections of the Lung, Pleura, and Mediastinum". Medscape. Archived from the original on 5 October 2016.
- ^ Amin R, Noone PG, Ratjen F (December 2012). "Chemical pleurodesis versus surgical intervention for persistent and recurrent pneumothoraces in cystic fibrosis". The Cochrane Database of Systematic Reviews. 12: CD007481. doi:10.1002/14651858.CD007481.pub3. PMC 7208277. PMID 23235645.
- ^ Fridell JA, Vianna R, Kwo PY, Howenstine M, Sannuti A, Molleston JP, et al. (October 2005). "Simultaneous liver and pancreas transplantation in patients with cystic fibrosis". Transplantation Proceedings. 37 (8): 3567–9. doi:10.1016/j.transproceed.2005.09.091. PMID 16298663.
- ^ Belkin RA, Henig NR, Singer LG, Chaparro C, Rubenstein RC, Xie SX, et al. (March 2006). "Risk factors for death of patients with cystic fibrosis awaiting lung transplantation". American Journal of Respiratory and Critical Care Medicine. 173 (6): 659–66. doi:10.1164/rccm.200410-1369OC. PMC 2662949. PMID 16387803.
- ^ a b "Cystic Fibrosis - Pediatrics". Merck Manuals Professional Edition. Retrieved 12 August 2020.
- ^ Somaraju UR, Solis-Moya A (August 2020). "Pancreatic enzyme replacement therapy for people with cystic fibrosis". The Cochrane Database of Systematic Reviews. 8 (9): CD008227. doi:10.1002/14651858.CD008227.pub4. PMC 8094413. PMID 32761612.
- ^ Skolnik K, Levy RD, Wilcox PG, Quon BS (November 2016). "Coronary artery disease in cystic fibrosis: An emerging concern?". Journal of Cystic Fibrosis. 15 (6): e70–e71. doi:10.1016/j.jcf.2016.09.010. PMID 27751792.
- ^ Zirbes J, Milla CE (September 2009). "Cystic fibrosis related diabetes". Paediatric Respiratory Reviews. 10 (3): 118–23, quiz 123. doi:10.1016/j.prrv.2009.04.004. PMID 19651382.
- ^ Onady GM, Stolfi A (October 2020). "Drug treatments for managing cystic fibrosis-related diabetes". The Cochrane Database of Systematic Reviews. 2020 (10): CD004730. doi:10.1002/14651858.CD004730.pub5. PMC 8094754. PMID 33075159.
- ^ Amin R, Jahnke N, Waters V (March 2020). "Antibiotic treatment for Stenotrophomonas maltophilia in people with cystic fibrosis". The Cochrane Database of Systematic Reviews. 3: CD009249. doi:10.1002/14651858.CD009249.pub5. PMC 7080526. PMID 32189337.
- ^ a b c Conwell LS, Chang AB (March 2014). "Bisphosphonates for osteoporosis in people with cystic fibrosis". The Cochrane Database of Systematic Reviews (3): CD002010. doi:10.1002/14651858.CD002010.pub4. PMC 6718208. PMID 24627308.
- ^ Hardin DS, Rice J, Ahn C, Ferkol T, Howenstine M, Spears S, et al. (March 2005). "Growth hormone treatment enhances nutrition and growth in children with cystic fibrosis receiving enteral nutrition". The Journal of Pediatrics. 146 (3): 324–8. doi:10.1016/j.jpeds.2004.10.037. PMID 15756212.
- ^ Marks SC, Kissner DG (1997). "Management of sinusitis in adult cystic fibrosis". American Journal of Rhinology. 11 (1): 11–4. doi:10.2500/105065897781446810. PMID 9065342. S2CID 5606258.
- ^ Phillipson GT, Petrucco OM, Matthews CD (February 2000). "Congenital bilateral absence of the vas deferens, cystic fibrosis mutation analysis and intracytoplasmic sperm injection". Human Reproduction. 15 (2): 431–5. doi:10.1093/humrep/15.2.431. PMID 10655317.
- ^ Ciofu O, Lykkesfeldt J (August 2014). "Antioxidant supplementation for lung disease in cystic fibrosis". The Cochrane Database of Systematic Reviews. 8 (8): CD007020. doi:10.1002/14651858.CD007020.pub3. PMC 6777741. PMID 25102015.
- ^ a b Radtke T, Nevitt SJ, Hebestreit H, Kriemler S (November 2017). "Physical exercise training for cystic fibrosis". The Cochrane Database of Systematic Reviews. 2017 (11): CD002768. doi:10.1002/14651858.CD002768.pub4. PMC 6485991. PMID 29090734.
- ^ Ganesan P, Schmiedge J, Manchaiah V, Swapna S, Dhandayutham S, Kothandaraman PP (April 2018). "Ototoxicity: A Challenge in Diagnosis and Treatment". Journal of Audiology & Otology. 22 (2): 59–68. doi:10.7874/jao.2017.00360. PMC 5894487. PMID 29471610.
- ^ Green J, Gilchrist FJ, Carroll W (June 2018). "Interventions for preventing distal intestinal obstruction syndrome (DIOS) in cystic fibrosis". The Cochrane Database of Systematic Reviews. 6: CD012619. doi:10.1002/14651858.cd012619. PMC 6478257. PMID 29894558.
- ^ Davis PB (March 2006). "Cystic fibrosis since 1938". American Journal of Respiratory and Critical Care Medicine. 173 (5): 475–82. doi:10.1164/rccm.200505-840OE. PMID 16126935. S2CID 1770759.
- ^ MacKenzie T, Gifford AH, Sabadosa KA, Quinton HB, Knapp EA, Goss CH, Marshall BC (August 2014). "Longevity of patients with cystic fibrosis in 2000 to 2010 and beyond: survival analysis of the Cystic Fibrosis Foundation patient registry". Annals of Internal Medicine. 161 (4): 233–41. doi:10.7326/m13-0636. PMC 4687404. PMID 25133359.
- ^ "Canadian Cystic Fibrosis Patient Data Registry Report" (PDF). Canadian Cystic Fibrosis Foundation. 2007. Archived from the original (PDF) on 15 July 2010. Retrieved 14 March 2010.
- ^ "Annual Data Report 2016 Cystic Fibrosis Foundation Patient Registry" (PDF). p. 4. Archived from the original (PDF) on 19 June 2018. Retrieved 19 June 2018.
- ^ "Cystic Fibrosis Patient Registry Annual Data Report 2009" (PDF). Cystic Fibrosis Foundation. 2009. Archived from the original (PDF) on 5 January 2012.
- ^ Yu H, Nasr SZ, Deretic V (April 2000). "Innate lung defenses and compromised Pseudomonas aeruginosa clearance in the malnourished mouse model of respiratory infections in cystic fibrosis". Infection and Immunity. 68 (4): 2142–7. doi:10.1128/IAI.68.4.2142-2147.2000. PMC 97396. PMID 10722612.
- ^ Ratjen F, Döring G (February 2003). "Cystic fibrosis". Lancet. 361 (9358): 681–9. doi:10.1016/S0140-6736(03)12567-6. PMID 12606185. S2CID 24879334.
- ^ Rosenstein BJ, Zeitlin PL (January 1998). "Cystic fibrosis". Lancet. 351 (9098): 277–82. doi:10.1016/S0140-6736(97)09174-5. PMID 9457113. S2CID 44627706.
- ^ Schmitz TG, Goldbeck L (February 2006). "The effect of inpatient rehabilitation programmes on quality of life in patients with cystic fibrosis: a multi-center study". Health and Quality of Life Outcomes. 4: 8. doi:10.1186/1477-7525-4-8. PMC 1373610. PMID 16457728.
- ^ Hegarty M, Macdonald J, Watter P, Wilson C (July 2009). "Quality of life in young people with cystic fibrosis: effects of hospitalization, age and gender, and differences in parent/child perceptions". Child. 35 (4): 462–8. doi:10.1111/j.1365-2214.2008.00900.x. PMID 18991968.
Havermans T, Vreys M, Proesmans M, De Boeck C (January 2006). "Assessment of agreement between parents and children on health-related quality of life in children with cystic fibrosis". Child. 32 (1): 1–7. doi:10.1111/j.1365-2214.2006.00564.x. PMID 16398786. - ^ Moorcroft AJ, Dodd ME, Webb AK (1998). "Exercise limitations and training for patients with cystic fibrosis". Disability and Rehabilitation. 20 (6–7): 247–53. doi:10.3109/09638289809166735. PMID 9637933.
- ^ "Medications". Cystic Fibrosis Canada. 2011. No. 10684-5100 RR0001. Archived from the original on 4 September 2011.
- ^ Araújo FG, Novaes FC, Santos NP, Martins VC, Souza SM, Santos SE, Ribeiro-dos-Santos AK (January 2005). "Prevalence of deltaF508, G551D, G542X, and R553X mutations among cystic fibrosis patients in the North of Brazil". Brazilian Journal of Medical and Biological Research. 38 (1): 11–5. doi:10.1590/S0100-879X2005000100003. PMID 15665983.
- ^ Tobias E (2011). Essential Medical Genetics. John Wiley & Sons. p. 312. ISBN 978-1-118-29370-6. Archived from the original on 17 April 2016.
- ^ "The Canadian Facts & Figures on Cystic Fibrosis". cysticfibrosis.ca. Archived from the original on 16 June 2013.
- ^ "Genetic Carrier Testing". Cystic Fibrosis Foundation. 2007. Archived from the original on 23 March 2010.
- ^ Rosenstein BJ, Cutting GR (April 1998). "The diagnosis of cystic fibrosis: a consensus statement. Cystic Fibrosis Foundation Consensus Panel". The Journal of Pediatrics. 132 (4): 589–95. doi:10.1016/S0022-3476(98)70344-0. PMID 9580754.
- ^ Hamosh A, FitzSimmons SC, Macek M, Knowles MR, Rosenstein BJ, Cutting GR (February 1998). "Comparison of the clinical manifestations of cystic fibrosis in black and white patients". The Journal of Pediatrics. 132 (2): 255–9. doi:10.1016/S0022-3476(98)70441-X. PMID 9506637.
- ^ Farrell P, Joffe S, Foley L, Canny GJ, Mayne P, Rosenberg M (September 2007). "Diagnosis of cystic fibrosis in the Republic of Ireland: epidemiology and costs". Irish Medical Journal. 100 (8): 557–60. PMID 17955689. Archived from the original on 3 December 2013.
- ^ Hytönen M, Patjas M, Vento SI, Kauppi P, Malmberg H, Ylikoski J, Kere J (December 2001). "Cystic fibrosis gene mutations deltaF508 and 394delTT in patients with chronic sinusitis in Finland". Acta Oto-Laryngologica. 121 (8): 945–7. doi:10.1080/000164801317166835. PMID 11813900.
- ^ "WHO Genes and human disease". Who.int. 7 December 2010. Archived from the original on 20 October 2012. Retrieved 23 January 2013.
- ^ Russell P (2011). Biology: the dynamic science (2nd ed.). Belmont, CA: Brooks/Cole, Cengage Learning. p. 304. ISBN 978-0-538-49372-7. Archived from the original on 17 April 2016.
- ^ "Genetic testing for cystic fibrosis Genetic Testing for Cystic Fibrosis". Consensus Development Conference Statement. National Institutes of Health. 14–16 April 1997. Archived from the original on 27 March 2009.
- ^ Rosenfeld M, Davis R, FitzSimmons S, Pepe M, Ramsey B (May 1997). "Gender gap in cystic fibrosis mortality". American Journal of Epidemiology. 145 (9): 794–803. doi:10.1093/oxfordjournals.aje.a009172. PMID 9143209.
- ^ Coakley RD, Sun H, Clunes LA, Rasmussen JE, Stackhouse JR, Okada SF, et al. (December 2008). "17beta-Estradiol inhibits Ca2+-dependent homeostasis of airway surface liquid volume in human cystic fibrosis airway epithelia". The Journal of Clinical Investigation. 118 (12): 4025–35. doi:10.1172/JCI33893. PMC 2582929. PMID 19033671.
- ^ Verma N, Bush A, Buchdahl R (October 2005). "Is there still a gender gap in cystic fibrosis?". Chest. 128 (4): 2824–34. doi:10.1378/chest.128.4.2824. PMID 16236961.
- ^ Moran A, Dunitz J, Nathan B, Saeed A, Holme B, Thomas W (September 2009). "Cystic fibrosis-related diabetes: current trends in prevalence, incidence, and mortality". Diabetes Care. 32 (9): 1626–31. doi:10.2337/dc09-0586. PMC 2732133. PMID 19542209.
- ^ "CF worse for women 'due to effect of estrogen'". The Irish Times. 8 August 2010. Archived from the original on 11 August 2010.
- ^ Wennberg C, Kucinskas V (1994). "Low frequency of the delta F508 mutation in Finno-Ugrian and Baltic populations". Human Heredity. 44 (3): 169–71. doi:10.1159/000154210. PMID 8039801.
- ^ Kere J, Savilahti E, Norio R, Estivill X, de la Chapelle A (September 1990). "Cystic fibrosis mutation delta F508 in Finland: other mutations predominate". Human Genetics. 85 (4): 413–5. doi:10.1007/BF02428286. PMID 2210753. S2CID 38364780.
- ^ Wiuf C (August 2001). "Do delta F508 heterozygotes have a selective advantage?". Genetical Research. 78 (1): 41–7. CiteSeerX 10.1.1.174.7283. doi:10.1017/S0016672301005195. PMID 11556136.
- ^ Gabriel SE, Brigman KN, Koller BH, Boucher RC, Stutts MJ (October 1994). "Cystic fibrosis heterozygote resistance to cholera toxin in the cystic fibrosis mouse model". Science. 266 (5182): 107–9. Bibcode:1994Sci...266..107G. doi:10.1126/science.7524148. PMID 7524148.
- ^ Alfonso-Sánchez MA, Pérez-Miranda AM, García-Obregón S, Peña JA (June 2010). "An evolutionary approach to the high frequency of the Delta F508 CFTR mutation in European populations". Medical Hypotheses. 74 (6): 989–92. doi:10.1016/j.mehy.2009.12.018. PMID 20110149.
- ^ Cuthbert AW, Halstead J, Ratcliff R, Colledge WH, Evans MJ (January 1995). "The genetic advantage hypothesis in cystic fibrosis heterozygotes: a murine study". The Journal of Physiology. 482 (Pt 2): 449–54. doi:10.1113/jphysiol.1995.sp020531. PMC 1157742. PMID 7714835.
- ^ Högenauer C, Santa Ana CA, Porter JL, Millard M, Gelfand A, Rosenblatt RL, et al. (December 2000). "Active intestinal chloride secretion in human carriers of cystic fibrosis mutations: an evaluation of the hypothesis that heterozygotes have subnormal active intestinal chloride secretion". American Journal of Human Genetics. 67 (6): 1422–7. doi:10.1086/316911. PMC 1287919. PMID 11055897.
- ^ Pier GB, Grout M, Zaidi T, Meluleni G, Mueschenborn SS, Banting G, et al. (May 1998). "Salmonella typhi uses CFTR to enter intestinal epithelial cells". Nature. 393 (6680): 79–82. Bibcode:1998Natur.393...79P. doi:10.1038/30006. PMID 9590693. S2CID 5894247.
- ^ Modiano G, Ciminelli BM, Pignatti PF (March 2007). "Cystic fibrosis and lactase persistence: a possible correlation". European Journal of Human Genetics. 15 (3): 255–9. doi:10.1038/sj.ejhg.5201749. PMID 17180122. S2CID 4650571.
- ^ Poolman EM, Galvani AP (February 2007). "Evaluating candidate agents of selective pressure for cystic fibrosis". Journal of the Royal Society, Interface. 4 (12): 91–8. doi:10.1098/rsif.2006.0154. PMC 2358959. PMID 17015291.
- ^ Williams N (2006). "Footprint fears for new TB threat". Current Biology. 16 (19): R821–R822. doi:10.1016/j.cub.2006.09.009. S2CID 2346727.
- ^ Tobacman JK (June 2003). "Does deficiency of arylsulfatase B have a role in cystic fibrosis?". Chest. 123 (6): 2130–9. doi:10.1378/chest.123.6.2130. PMID 12796199.
- ^ a b c Busch R (1990). "On the History of Cystic Fibrosis". Acta Universitatis Carolinae. Medica. 36 (1–4): 13–15. PMID 2130674.
- ^ Fanconi G, Uehlinger E, Knauer C (1936). "Das coeliakiesyndrom bei angeborener zysticher pankreasfibromatose und bronchiektasien". Wien. Med. Wochenschr. 86: 753–756.
- ^ Di Sant'Agnese PA, Darling RC, Perera GA, Shea E (November 1953). "Abnormal electrolyte composition of sweat in cystic fibrosis of the pancreas; clinical significance and relationship to the disease". Pediatrics. 12 (5): 549–563. doi:10.1542/peds.12.5.549. PMID 13111855. S2CID 42514224.
- ^ Riordan JR, Rommens JM, Kerem B, Alon N, Rozmahel R, Grzelczak Z, et al. (September 1989). "Identification of the cystic fibrosis gene: cloning and characterization of complementary DNA". Science. 245 (4922): 1066–1073. Bibcode:1989Sci...245.1066R. doi:10.1126/science.2475911. PMID 2475911.
- ^ Rommens JM, Iannuzzi MC, Kerem B, Drumm ML, Melmer G, Dean M, et al. (September 1989). "Identification of the cystic fibrosis gene: chromosome walking and jumping". Science. 245 (4922): 1059–1065. Bibcode:1989Sci...245.1059R. doi:10.1126/science.2772657. PMID 2772657.
- ^ Freudenheim M (22 December 2009). "Tool in Cystic Fibrosis Fight: A Registry". The New York Times. pp. D1. Archived from the original on 24 May 2013. Retrieved 21 December 2009.
- ^ Lee TW, Southern KW, Perry LA, Penny-Dimri JC, Aslam AA (June 2016). Southern KW (ed.). "Topical cystic fibrosis transmembrane conductance regulator gene replacement for cystic fibrosis-related lung disease". The Cochrane Database of Systematic Reviews. 2016 (6): CD005599. doi:10.1002/14651858.CD005599.pub5. PMC 8682957. PMID 27314455.
- ^ Alton EW, Armstrong DK, Ashby D, Bayfield KJ, Bilton D, Bloomfield EV, et al. (September 2015). "Repeated nebulisation of non-viral CFTR gene therapy in patients with cystic fibrosis: a randomised, double-blind, placebo-controlled, phase 2b trial". The Lancet. Respiratory Medicine. 3 (9): 684–691. doi:10.1016/S2213-2600(15)00245-3. PMC 4673100. PMID 26149841.
- ^ Ramalho AS, Beck S, Meyer M, Penque D, Cutting GR, Amaral MD (November 2002). "Five percent of normal cystic fibrosis transmembrane conductance regulator mRNA ameliorates the severity of pulmonary disease in cystic fibrosis". American Journal of Respiratory Cell and Molecular Biology. 27 (5): 619–27. doi:10.1165/rcmb.2001-0004oc. PMID 12397022. S2CID 8714332.
- ^ Tate S, Elborn S (March 2005). "Progress towards gene therapy for cystic fibrosis". Expert Opinion on Drug Delivery. 2 (2): 269–80. doi:10.1517/17425247.2.2.269. PMID 16296753. S2CID 30948229.
- ^ 온라인 Mendelian In Man (OMIM) : CASTIC FIBROSIS; CF - 219700
- ^ Schwank G, Koo BK, Sasselli V, Dekkers JF, Heo I, Demircan T, et al. (December 2013). "Functional repair of CFTR by CRISPR/Cas9 in intestinal stem cell organoids of cystic fibrosis patients". Cell Stem Cell. 13 (6): 653–8. doi:10.1016/j.stem.2013.11.002. PMID 24315439.
- ^ Hraiech S, Brégeon F, Rolain JM (2015). "Bacteriophage-based therapy in cystic fibrosis-associated Pseudomonas aeruginosa infections: rationale and current status". Drug Design, Development and Therapy. 9: 3653–63. doi:10.2147/DDDT.S53123. PMC 4509528. PMID 26213462.
- ^ Trend S, Fonceca AM, Ditcham WG, Kicic A, Cf A (November 2017). "The potential of phage therapy in cystic fibrosis: Essential human-bacterial-phage interactions and delivery considerations for use in Pseudomonas aeruginosa-infected airways". Journal of Cystic Fibrosis. 16 (6): 663–670. doi:10.1016/j.jcf.2017.06.012. PMID 28720345.
- ^ a b Ramsey BW, Downey GP, Goss CH (May 2019). "Update in Cystic Fibrosis 2018". American Journal of Respiratory and Critical Care Medicine. 199 (10): 1188–1194. doi:10.1164/rccm.201902-0310UP. PMC 6519861. PMID 30917288. ProQuest 2230820891.
- ^ Dietz HC (August 2010). "New therapeutic approaches to mendelian disorders". The New England Journal of Medicine. 363 (9): 852–63. doi:10.1056/NEJMra0907180. PMID 20818846. S2CID 5809127. 무료 전문
- ^ a b Office of the Commissioner (24 October 2019). "FDA approves new breakthrough therapy for cystic fibrosis". FDA. Retrieved 13 November 2019.
- ^ "CFTR Modulator Therapies". Bethesda, Md.: Cystic Fibrosis Foundation. Retrieved 13 November 2019.
- ^ Sherrard LJ, McGrath SJ, McIlreavey L, Hatch J, Wolfgang MC, Muhlebach MS, Gilpin DF, Elborn JS, Tunney MM (February 2016). "Production of extended-spectrum beta-lactamases and the potential indirect pathogenic role of Prevotella isolates from the cystic fibrosis respiratory microbiota". Int J Antimicrob Agents. 47 (2): 140–145. doi:10.1016/j.ijantimicag.2015.12.004. PMC 4746055. PMID 26774156.
인용된 작품
- Egan ME, Schechter MS, Voynow JA (2020). "Cystic Fibrosis". In Kliegman RM, St Geme JW, Blum NJ, Shah SS, Tasker RC, Wilson KM (eds.). Nelson Textbook of Pediatrics. Elsevier. pp. 2282–2297. ISBN 978-0-323-56890-6.
외부 링크
- 낭포성 섬유증과 관련된 유전자를 GeneCard 검색
- 낭포성 섬유증 돌연변이 데이터베이스
- "Cystic Fibrosis". MedlinePlus. U.S. National Library of Medicine.