낫세포병
Sickle cell disease| 낫세포병 | |
|---|---|
| 기타명 | 겸상적혈구장애; drepanocytosis (날짜) |
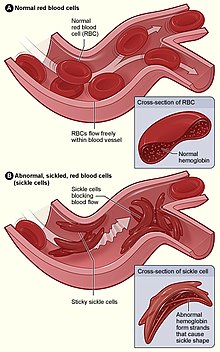 | |
| 그림 (A)는 혈관을 통해 정상적인 적혈구가 자유롭게 흐르는 것을 보여줍니다. 삽입물은 정상 적혈구와 정상 헤모글로빈의 단면을 보여줍니다. 그림 (B)는 혈관의 분기점에 달라붙는 비정상적인 낫 모양의 적혈구를 보여줍니다. 삽입된 이미지는 긴 중합된 낫 헤모글로빈(HbS) 가닥이 뻗어 있고 세포 모양이 초승달처럼 보이도록 왜곡된 낫 세포의 단면을 보여줍니다. | |
| 전문 | 혈액학, 의학유전학 |
| 증상 | 통증, 빈혈, 손발 붓기, 세균 감염, 뇌졸중의[1] 발작 |
| 합병증 | 만성 통증, 뇌졸중, 무균성 골괴사, 담석, 다리 궤양, 원위증, 폐 고혈압, 시력 문제, 신장 문제[2] |
| 통상발병 | 생후[1] 5~6개월 |
| 원인들 | 헤모글로빈 S 유전자의 유전적, 동형접합 돌연변이.[3] |
| 진단법 | 혈액검사[4] |
| 치료 | 예방접종, 항생제, 고수액 섭취, 엽산 보충, 진통제, 수혈[5][6] |
| 예후 | 기대수명 40~60세 (선진국)[2] |
| 빈도수. | 440만명 (2015년)[7] |
| 사망자 | 114,800 (2015)[8] |
낫세포 질환(SCD)은 단순히 낫세포라고도 불리며, 전형적으로 유전되는 헤모글로빈 관련 혈액 질환의 그룹입니다.[2] 가장 일반적인 유형은 낫 세포 빈혈로 알려져 있습니다.[2] 적혈구에서 발견되는 산소 운반 단백질 헤모글로빈에 이상이 생기게 됩니다.[2] 이로 인해 특정 상황에서는 경직되고 낫과 같은 모양이 됩니다.[2] 낫 세포 질환의 문제는 일반적으로 생후 5개월에서 6개월 사이에 시작됩니다.[1] 통증의 발작( 낫 세포 위기로 알려져 있음), 빈혈, 손발 붓기, 세균 감염, 뇌졸중과 같은 많은 건강 문제가 발생할 수 있습니다.[1] 사람들이 나이가 들면서 장기적인 통증이 생길 수 있습니다.[2] 선진국 평균 수명은 40~60세입니다.[2] 모든 주요 장기는 낫 세포 질환의 영향을 받습니다. 간, 심장, 신장 담낭, 눈, 뼈, 관절 등도 낫세포의 기능 이상과 작은 혈관을 제대로 흐르지 못해 손상을 입을 수 있습니다.
겸상적혈구질환은 헤모글로빈을 만드는 β-글로빈 유전자(HBB)의 비정상 복제물 2개를 부모로부터 각각 1개씩 물려받으면서 발생합니다.[3] 이 유전자는 11번 염색체에서 발생합니다.[9] 각 헤모글로빈 유전자의 정확한 돌연변이에 따라 여러 가지 아형이 존재합니다.[2] 공격은 온도 변화, 스트레스, 탈수 및 높은 고도에 의해 시작될 수 있습니다.[1] 한 장의 이상 사본이 있는 사람은 보통 증상이 없고 겸상적인 세포 형질이 있다고 합니다.[3] 이러한 사람들을 캐리어라고도 합니다.[5] 진단은 혈액 검사로 이루어지며, 일부 국가에서는 출생 시 모든 아기에게 질병을 검사합니다.[4] 임신 중 진단도 가능합니다.[4]
겸상적혈구질환자의 진료에는 예방접종과 항생제를 통한 감염예방, 고액수 섭취, 엽산 보충, 진통제 등이 포함될 수 있습니다.[5][6] 다른 조치로는 수혈 및 약물 하이드록시카바미드(하이드록시우레아)가 포함될 수 있습니다.[6] 2023년에는 새로운 유전자 치료제가 승인되었습니다.[10][11] 골수 세포를 이식하면 적은 비율의 사람들이 치료될 수 있습니다.[2]
2015년[update] 기준 약 440만 명이 낫세포 질환을 앓고 있는 반면, 추가로 4300만 명이 낫세포 형질을 가지고 있습니다.[7][12] 겸상적인 세포 질환의 약 80%는 사하라 사막 이남의 아프리카에서 발생하는 것으로 추정됩니다.[13] 또한 인도, 남유럽, 서아시아, 북아프리카의 일부 지역과 세계의 다른 지역에 사는 아프리카 출신(사하라 이남)의 사람들 사이에서 덜 발생합니다.[14] 2015년에는 약 114,800명의 사망자가 발생했습니다.[8] 이 질환은 미국 의사 James B에 의해 의학 문헌에 처음 기술되었습니다. 1910년 헤릭.[15][16] 1949년 E.A.에 의해 유전자 전달이 결정되었습니다. 비트와 J.[16]V.닐. 1954년 낫 세포 형질의 말라리아에 대한 보호 효과가 기술되었습니다.[16]
징후 및 증상

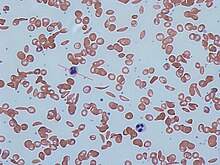

낫세포 질환의 징후는 대개 유아기에 시작됩니다. 증상의 심각성은 위기 사건의 빈도와 마찬가지로 사람마다 다를 수 있습니다.[17][13] 겸상적혈구질환은 다양한 급성 및 만성 합병증을 유발할 수 있으며, 그 중 몇몇은 사망률이 높습니다.[18]
첫번째 사건들
SCD 진단으로 이어지는 첫 번째 사건의 일반적인 특성은 아이의 나이에 따라 다릅니다. 생후 1년 이내에 병이 나타나면 손과 발에 통증이 생기고 붓는 증상이 나타나는데, 이를 악질염 또는 '손발증후군'이라고 합니다. 창백, 황달, 피로감 등도 겸상적인 세포질환으로 인한 빈혈로 초기 징후가 될 수 있습니다.[19]
전형적인 상염색체 열성 SCD 환자의 약 절반은 5세 이상이 될 때까지 위기를 겪지 않습니다.[19] 이러한 환자들 중 일부와 다른 유전자형을 가진 다른 사람들은 중등도에서 심각한 저산소증 상태에서만 증상을 보일 수 있으므로 나중까지 질병에 걸린 것을 모를 수 있습니다.[13] 2세 이상 소아 중 가장 빈번한 초성발현은 일반화형이나 가변형의 고통스러운 사건이며, 약간 덜 흔한 버전은 급성 흉통의 사건으로 나타납니다. 방선염은 2세 이상의 어린이에서는 거의 발생하지 않거나 전혀 발생하지 않습니다.[19]
낫세포 위기
"병든 세포 위기" 또는 "병든 위기"라는 용어는 혈관 폐쇄 위기, 플라스틱 위기, 비장 격리 위기, 용혈 위기 등을 포함하여 많은 유형이 될 수 있는 빈혈과 위기를 초래하는 SCD 환자에서 발생하는 여러 독립적인 급성 질환을 설명하는 데 사용될 수 있습니다. 초기 증상은[20] 피부가 누르스름하거나 눈의 흰자가 많은 수의 적혈구가 용혈될 때 나타나는 증상입니다. 낫 세포 위기의 대부분의 에피소드는 5일에서 7일 사이에 지속됩니다.[21] "감염, 탈수, 산증(모두 낫질을 선호함)이 유발 요인으로 작용할 수 있지만 대부분의 경우 소인이 확인되지 않습니다."[22]
폐색성 위기
혈관폐쇄성 위기는 낫 모양의 적혈구가 모세혈관을 막고 장기로 가는 혈류를 제한해 허혈, 통증, 괴사, 종종 장기 손상을 초래해 발생합니다. 이러한 위기의 빈도, 심각성 및 지속 기간은 상당히 다릅니다. 통증이 있는 위기는 수분 공급, 진통제, 수혈로 치료되며, 통증 관리는 위기가 진정될 때까지 일정한 간격으로 오피오이드 약물 투여가 필요합니다. 가벼운 위기의 경우 환자의 하위 그룹이 디클로페낙 또는 나프록센과 같은 비스테로이드성 항염증제를 관리합니다. 더 심각한 위기의 경우 대부분의 환자는 정맥 오피오이드에 대한 입원 관리를 필요로 합니다. 환자가 제어하는 진통제 장치는 일반적으로 이 환경에서 사용됩니다. 음경이나[23] 폐와 같은 장기가 관련된 혈관폐쇄성 위기는 응급상황으로 간주하여 적혈구 수혈로 치료합니다. 무기폐의 발생을 최소화하기 위해 심호흡을 장려하는 기술인 인센티브 스피로메트리가 권장됩니다.[24]
비장 격리 위기
낫 모양의 적혈구는 혈관이 좁아지고 결함이 있는 세포를 제거하는 기능이 저하되기 때문에 낫 모양의 적혈구가 자주 발생합니다.[25] 낫세포 빈혈이 있는 사람들은 보통 어린 시절이 끝나기 전에 경색됩니다. 이러한 비장 손상은 캡슐화된 유기체에 의한 감염 위험을 높입니다.[26][27] 적절한 비장 기능이 부족한 사람에게는 예방적 항생제와 예방접종이 권장됩니다.
비장 격리 위기는 비장 내 적혈구 포획으로 인한 비장의 급성 고통스러운 확장으로, 저혈량성 쇼크의 가능성과 함께 헤모글로빈 수치의 급격한 하락을 초래합니다. 격리 위기는 비상 사태로 간주됩니다. 치료하지 않을 경우 순환부전으로 1-2시간 이내에 환자가 사망할 수 있습니다. 관리는 때때로 수혈과 함께 도움이 됩니다. 이러한 위기는 일시적이며 3-4시간 동안 지속되며 하루 동안 지속될 수 있습니다.[28]
급성흉부증후군
급성 흉부 증후군은 가슴 통증, 발열, 폐 침윤 또는 초점 이상, 호흡기 증상 또는 저산소증과 같은 징후 또는 증상 중 적어도 두 가지로 정의됩니다.[24] 두 번째로 흔한 합병증이며 SCD 환자 사망의 약 25%를 차지합니다. 대부분의 경우 혈관 폐쇄성 위기를 경험한 후 급성 흉부 증후군이 발생합니다.[29][30] 그럼에도 불구하고 급성 흉부 증후군 동안 혈관 폐쇄성 위기를 겪는 사람은 약 80%에 달합니다.[citation needed]
플라스틱 위기
성형성 위기는 환자의 기저 빈혈이 급성으로 악화되어 창백한 외모, 빠른 심박수 및 피로를 유발하는 경우입니다. 이 위기는 보통 파보바이러스 B19에 의해 유발되는데, 파보바이러스 B19는 적혈구 전구체를 침범하여 증식하고 파괴함으로써 적혈구 생성에 직접적인 영향을 미칩니다.[31] 파보바이러스 감염증은 2~3일 동안 적혈구 생성을 거의 완벽하게 막아줍니다. 정상적인 사람의 경우, 이것은 거의 결과가 없지만 SCD 환자의 적혈구 수명이 짧아지면 갑자기 생명을 위협하는 상황이 발생합니다. 질병이 진행되는 동안 망상적혈구 수가 급격히 감소하고(망막구감소증을 유발), 적혈구의 빠른 회전은 헤모글로빈의 감소로 이어집니다. 이 위기는 사라지려면 4~7일이 걸립니다. 대부분의 환자는 지원적으로 관리할 수 있습니다. 일부는 수혈이 필요합니다.[32]
용혈성 위기
용혈성 위기는 헤모글로빈 수치가 급격히 가속화되는 것입니다. 적혈구는 더 빠른 속도로 분해됩니다. 이는 특히 G6PD 결핍이 공존하는 사람들에게 흔히 발생합니다.[33] 겸상적혈구 질환에서 용혈성 위기의 또 다른 영향은 적혈구, 백혈구 및 혈소판에 대한 산화 스트레스입니다. 골수에서 적혈구 생성이 충분하지 않을 때 몸이 공급받고 처리하며 운반하는 산소가 몸의 항산화 물질과 불균형하게 됩니다. 세포 내 산소 반응성 종의 불균형이 발생하여 산소가 제대로 공급되지 않거나 형성되지 않은 적혈구가 더 많이 생성됩니다. 산화 스트레스는 조직 내 산소의 불균형 때문에 빈혈을 유발할 수 있습니다.[34]
관리는 때때로 수혈과 함께 도움이 됩니다.[24]
다른.
가장 초기의 임상 증상 중 하나는 빠르면 생후 6개월에 나타나는 방선염이며 낫 세포 특성을 가진 어린이에게서 발생할 수 있습니다.[35] 위기는 한 달까지 지속될 수 있습니다.[36] 폐의 폐렴과 낫질이 모두 급성 흉부 증후군의 증상을 유발할 수 있다는 점을 감안할 때, 환자는 두 가지 상태 모두에 대해 치료를 받습니다.[37] 고통스러운 위기, 호흡기 감염, 골수 색전증 또는 무기폐, 아편 투여 또는 수술에 의해 유발될 수 있습니다.[38] 조혈성 궤양도 발생할 수 있습니다.[39] 가장 흔한 종류는 낫 세포 빈혈(SS), 낫 헤모글로빈-C병(SC), 낫 베타-플러스 탈라세미아, 낫 베타-제로 탈라세미아입니다.[40]
합병증
낫세포 빈혈은 다음과 같은 다양한 합병증을 유발할 수 있습니다.
- 심각한 세균 감염의 위험이 증가하는 것은 기능하는 비장 조직의 손실 때문입니다(그리고 수술로 비장을 제거한 후 감염될 위험과 맞먹습니다). 이러한 감염은 일반적으로 Streptococcus pneumoniae 및 Hemophilus influenzae와 같은 캡슐화된 유기체에 의해 발생합니다. 일일 페니실린 예방법은 소아기에 가장 많이 사용되는 치료법으로 일부 혈액내과 전문의는 무기한 치료를 계속하고 있습니다. 오늘날 환자들은 S. pneumoniae에 대한 일상적인 예방접종의 혜택을 받습니다.[41]
- 혈관이 점진적으로 좁아져 발생할 수 있는 뇌졸중은 산소가 뇌에 도달하지 못하게 합니다. 소아에서는 뇌경색이, 성인에서는 뇌출혈이 발생합니다.[citation needed]
- 조용한 뇌졸중은 즉각적인 증상을 일으키지 않지만 뇌 손상과 관련이 있습니다. 소리 없는 뇌졸중은 증상이 있는 뇌졸중의 5배 정도일 것입니다. SCD를 가진 어린이의 약 10-15%가 뇌졸중을 가지고 있으며, 어린 환자들에게서 무성 뇌졸중이 우세합니다.[42][43]
- 담석증(담석)과 담낭염은 빌리루빈의 과다 생성과 장기간의 용혈로 인한 침전으로 발생할 수 있습니다.[44]
- 허혈로 인해 고관절 및 기타 주요 관절의 혈관 괴사(무균성 골괴사)가 발생할 수 있습니다.[45]
- 비장 기능 저하로 인한 면역 반응 저하(비장 기능 이상)[46]
- 음경의[47] 원두통과 경색
- SCD에서 골수염의 가장 흔한 원인은 살모넬라(특히 비정형 혈청형 살모넬라 티피무륨, 살모넬라 엔테리티디스, 살모넬라 콜레라수이스 및 살모넬라 파라티피 B)이며, 황색포도상구균과 그람 음성 장내 간균이 뒤따르는 것은 아마도 장의 혈관 내 낫질이 패치성 허혈성 경색을 초래하기 때문일 것입니다.[48]
- 신장의[citation needed] 급성 유두 괴사
- 다리 궤양[49]
- 눈의 경우 배경망막병증, 증식망막병증, 유리체 출혈, 망막 박리 등으로 실명할 수 있습니다.[50] 정기적인 연간 시력 검사가 권장됩니다.
- 임신 중 자궁 내 성장 제한, 자연유산 및 자간전증
- 만성 통증: 급성 혈관폐쇄성 통증이 없는 경우에도 보고되지 않은 만성 통증이 있는 환자가 많습니다.[51]
- 폐고혈압(폐동맥에 대한 압력 증가)은 우심실에 무리를 주고 심부전의 위험을 초래할 수 있으며, 대표적인 증상은 호흡곤란, 운동내력 저하, 실신 에피소드입니다.[52] 어린이의 21%와 성인의 30%가 폐고혈압의 증거를 가지고 있습니다. 이는 보행 거리 감소와 사망률 증가와 관련이 있습니다.[53]
- 심장 조직의 섬유화 또는 흉터로 인한 심근병증 및 좌심실 이완기 기능 장애.[54][55] 이것은 또한 폐 고혈압, 운동 능력 감소 및 부정맥에 기여합니다.[56]
- 낫세포신병증에 의한 만성신부전은 고혈압, 소변의 단백질 소실, 소변의 적혈구 소실, 빈혈 악화 등으로 나타납니다. 말기 신부전으로 진행되면 좋지 않은 예후를 보입니다.[57]
유전학


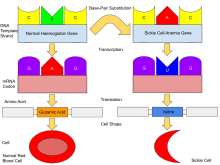
일반적으로 인간은 알파와 베타 사슬 2개로 구성된 헤모글로빈 A, 알파와 델타 사슬 2개로 구성된 헤모글로빈 A2, 알파와 감마 사슬 2개로 구성된 헤모글로빈 F(HbF)를 체내에 가지고 있습니다. 이 세 종류 중 헤모글로빈 F는 생후 6주 정도까지 지배적입니다. 그 후 헤모글로빈 A가 일생을 지배합니다.[58] 겸상적혈구병 진단을 받은 사람들은 헤모글로빈 A의 β-글로빈 소단위체 중 적어도 하나가 헤모글로빈 S로 대체됩니다. 겸상적인 겸상적인 겸상적인 형태의 겸상적인 겸상적인 겸상적인 겸상적인 세포혈증에서, 헤모글로빈 S는 헤모글로빈의 두 β-글로빈 소단위체를 대체합니다.[17]
겸상 적혈구 질환은 부모로부터 물려받는 상염색체 열성 패턴을 가지고 있습니다.[59] 적혈구에서 사람이 만드는 헤모글로빈의 종류는 부모로부터 어떤 헤모글로빈 유전자를 물려받느냐에 따라 달라집니다. 만약 한 부모가 낫세포 빈혈을 가지고 있고 다른 한 부모가 낫세포 특성을 가지고 있다면, 어떤 주어진 아이도 낫세포 질환을 가질 확률은 50%이고 낫세포 특성을 가질 확률은 50%입니다. 부모 모두 낫세포 특성을 가지고 있을 때, 어떤 주어진 아이도 낫세포 질환에 걸릴 확률은 25%, 낫세포 대립유전자가 없을 확률은 25%, 이형접합 상태일 확률은 50%입니다.[60][61][unreliable medical source?]
제한 엔도뉴클레아제 분석에 의해 제안된 [62]바와 같이 낫 세포 유전자 돌연변이는 아마도 다른 지리적 영역에서 자발적으로 발생했을 것입니다. 이러한 변종은 카메룬, 세네갈, 베냉, 반투 및 사우디-아시아로 알려져 있습니다. 그들의 임상적 중요성은 일부가 세네갈 및 사우디-아시아 변종과 같이 더 높은 HbF 수준과 관련이 있고 더 가벼운 질병을 가지고 있는 경향이 있기 때문입니다.[63]
유전자 결함은 β-글로빈 유전자의 단일 뉴클레오티드 돌연변이(단일 뉴클레오티드 다형성 – SNP 참조)(GAG 코돈이 GTG로 변경됨)이며, 이로 인해 글루타메이트(E/Glu)가 6번 위치(E6V 치환)에서 발린(V/Val)으로 치환됩니다.[64][note 1] 이 돌연변이를 가진 헤모글로빈 S는 정상적인 성인 HbA와 달리 HbS라고 합니다. 이것은 보통 양성 돌연변이이며, 정상 산소 농도 조건에서 헤모글로빈의 2차, 3차 또는 4차 구조에 명백한 영향을 미치지 않습니다. 그러나, 낮은 산소 농도에서는 헤모글로빈의 디옥시 형태가 E 나선과 F 나선 사이의 단백질에 소수성 패치를 노출시키기 때문에 HbS가 중합되어 섬유성 침전물을 형성합니다(Phe 85, Leu 88).[65]
HbS에 대한 이형접합(sickling hemoglobin의 운반체)이 있는 사람들의 경우 정상 대립유전자가 헤모글로빈의 절반을 생성할 수 있기 때문에 중합 문제는 경미합니다. HbS에 대해 동형 접합된 사람들에서 HbS의 긴 사슬 폴리머의 존재는 적혈구의 모양을 매끄럽고 도넛 같은 모양에서 너덜너덜하고 스파이크로 가득 찬 모양으로 왜곡하여 모세혈관 내에서 깨지기 쉽고 취약하게 만듭니다. 보균자는 산소를 빼앗기거나(예를 들어, 산을 오르는 동안) 심하게 탈수된 상태에서만 증상이 나타납니다.[citation needed]
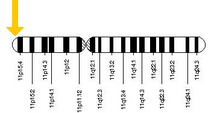
낫세포 빈혈의 원인이 되는 대립유전자는 11번 염색체의 짧은 팔, 보다 구체적으로 11p15.5에서 찾을 수 있습니다. 아버지와 어머니로부터 결함이 있는 유전자를 모두 받은 사람이 병에 걸리고, 하나의 결함이 있는 대립유전자와 하나의 건강한 대립유전자를 받은 사람은 건강을 유지하지만 병을 물려줄 수 있으며, 보균자 또는 이형접합자로 알려져 있습니다. 이형 접합체는 여전히 말라리아에 걸릴 수 있지만 일반적으로 증상이 덜 심각합니다.[66]
이형 접합체의 적응적 이점으로 인해, 이 질병은 특히 아프리카, 지중해, 인도 및 중동과 같은 말라리아에 걸린 지역에 최근 조상이 있는 사람들 사이에서 여전히 널리 퍼져 있습니다.[67] 말라리아는 역사적으로 남유럽의 토착종이었으나, 드물게 산발적으로 발생하는 사례를 제외하고는 20세기 중반에 퇴치가 선언되었습니다.[68]
말라리아 기생충은 복잡한 수명 주기를 가지고 있으며 그 일부를 적혈구에서 보냅니다. 운반체에서 말라리아 기생충이 존재하면 헤모글로빈에 결함이 있는 적혈구가 조기에 파열되어 열원충 기생충이 번식할 수 없게 됩니다. 또한 Hb의 중합은 기생충이 Hb를 소화하는 능력에 영향을 미칩니다. 따라서 말라리아가 문제가 되는 지역에서는 낫 세포 형질(이형 접합체에 대한 선택)을 가지고 있으면 실제로 사람들의 생존 가능성이 높아집니다.[citation needed]
풍토병 말라리아가 없는 미국의 경우 아프리카 혈통의 사람들 사이에서 낫세포 빈혈의 유병률은 서아프리카 사람들 사이(약 4.0%)보다 낮고(약 0.25%) 감소하고 있습니다. 풍토병 말라리아가 없으면 낫 세포 돌연변이는 순전히 불리하고 자연 선택에 의해 영향을 받는 개체군에서 감소하는 경향이 있으며, 현재는 출산 전 유전자 검사를 통해 인위적으로 발생합니다. 그러나 아프리카계 미국인 공동체는 미국인 노예를 포함한 몇몇 아프리카 민족과 비아프리카 민족의 후손입니다. 따라서 아프리카인이 아닌 사람들과의 교배를 통한 유전적 희석 정도와 노예제(특히 노예 무역과 종종 치명적인 중간 통로)를 통한 높은 건강 선택적 압력이 낫 세포 빈혈의 낮은 유병률에 대한 가장 그럴듯한 설명이 될 수 있습니다. 서아프리카인에 비해 아프리카계 미국인들 사이에서 다른 유전병). 북미에서 낫형 세포 유전자의 확산을 제한하는 또 다른 요인은 일부다처제가 상대적으로 없다는 점입니다. 일부다처제 사회에서 영향을 받은 남성은 여러 파트너와 함께 많은 자녀를 출산할 수 있습니다.[69]
병태생리학

적혈구 탄력성의 상실은 겸상적혈구 질환의 병태생리의 중심입니다. 정상 적혈구는 상당히 탄력적이고 쌍곡판 모양을 하고 있는데, 이를 통해 세포가 변형되어 모세혈관을 통과할 수 있습니다.[70] 낫세포 질환에서 낮은 산소 장력은 적혈구 낫질을 촉진하고 낫질의 반복적인 에피소드는 세포막을 손상시키고 세포의 탄력성을 떨어트립니다. 이 세포들은 정상적인 산소 장력이 회복되면 정상적인 모양으로 돌아가지 못합니다. 이 때문에 이들 강직한 혈구는 좁은 모세혈관을 통과하면서 변형되지 못해 혈관 폐색과 허혈을 일으킵니다.[citation needed]
이 질병의 실제 빈혈은 적혈구의 모양 때문에 적혈구가 파괴되는 용혈로 인해 발생합니다. 골수는 새로운 적혈구를 만들어 보상을 시도하지만 파괴 속도와 일치하지 않습니다.[71] 건강한 적혈구는 일반적으로 90-120일 동안 기능하지만 낫 세포는 10-20일 동안만 지속됩니다.[72]
진단.
HbS에서 전체 혈액 수는 높은 망상적혈구 수와 함께 6–8 g/dl 범위의 헤모글로빈 수치를 나타냅니다(골수가 더 많은 적혈구를 생성하여 병든 세포의 파괴를 보상하기 때문입니다). 다른 형태의 겸상적인 세포 질환에서는 Hb 수치가 더 높은 경향이 있습니다. 혈액 필름은 시상하부(표적 세포 및 하웰-졸리 신체)의 특징을 나타낼 수 있습니다.[73]
혈액막에 있는 적혈구의 낫질은 대사황산나트륨을 첨가함으로써 유도될 수 있습니다. 낫형 헤모글로빈의 존재는 "병든 용해도 테스트"("병든"이라고도 함)[74]로도 입증될 수 있습니다. 환원 용액(예: 나트륨 디티오나이트)에서 헤모글로빈 S(HbS)의 혼합물은 탁한 외관을 제공하는 반면, 정상 Hb는 명확한 용액을 제공합니다.[75]
다양한 종류의 헤모글로빈이 다양한 속도로 움직이는 겔 전기영동의 한 형태인 헤모글로빈 전기영동에서 비정상적인 헤모글로빈 형태를 감지할 수 있습니다. 가장 일반적인 두 가지 형태인 낫형 세포 헤모글로빈(HgbS)과 낫형 헤모글로빈 C(HgbSC)를 확인할 수 있습니다. 고성능 액체 크로마토그래피로 진단을 확인할 수 있습니다. 다른 조사는 HbS 및 HbC에 대한 특이성이 높기 때문에 유전자 검사는 거의 수행되지 않습니다.[76]
급성 낫 세포 위기는 종종 감염에 의해 촉발됩니다. 따라서 요로감염을 감지하기 위한 소변검사와 요로감염을 찾기 위한 흉부 X선 검사를 일상적으로 시행해야 합니다.[77]
병의 보균자로 알려져 있거나 낫세포 빈혈에 걸린 아이를 낳을 위험이 있는 사람은 유전자 상담을 받을 수 있습니다. 유전 상담사는 가족과 함께 유전자 검사 옵션의 이점, 제한 사항 및 물류뿐만 아니라 검사 및 검사 결과가 개인에게 미칠 수 있는 잠재적 영향에 대해 논의합니다.[78][79] 임신 중에는 태아의 혈액 샘플이나 양수 샘플에 대한 유전자 검사를 수행할 수 있습니다. 임신 첫 3개월 동안 융모막 융모 샘플링(CVS)은 SCD 산전 진단에 사용되는 기술이기도 합니다.[80] 태아의 혈액 샘플을 채취하는 것은 더 큰 위험이 있기 때문에 일반적으로 후자의 테스트를 사용합니다. 신생아 검진은 때때로 신생아 검진이라고도 불리며, 낫세포 질환을 가진 사람들에게 조기 발견 방법을 제공할 뿐만 아니라 낫세포 특성을 가진 사람들의 그룹을 식별할 수 있습니다.[81] 유전 상담사는 유색인종과 그 가족이 의료계에 존재하는 인종적, 인종적 차이를 해결하는 데 도움을 줄 수 있습니다.[82]
2010년에 미국에서는 SCD 선수들의 종합적인 심사를 둘러싸고 상당한 고민과 논쟁이 있었습니다.[83][84][85][86] 2012년 미국혈액학회는 과학적 근거 부족, 좋은 의료행위와의 불일치, 공중보건윤리와의 불일치 등을 이유로 낫형 세포 형질 상태의 검사나 공개를 운동활동 참여의 전제조건으로 지지하지 않는다고 결론내렸습니다. 그들은 낫 세포 상태와 상관없이 모든 운동 선수에게 효과적인 운동 관련 부상과 사망을 줄이기 위한 보편적인 개입을 권장했습니다.[87]
관리
치료에는 여러 가지 조치가 포함됩니다. 역사적으로 겸상적인 세포 질환이 있는 사람들은 운동을 피하는 것이 권장되어 왔지만, 규칙적인 운동은 사람들에게 도움이 될 수 있습니다.[88] 탈수는 피해야 합니다.[89] 칼슘이 많은 식단을 권장하지만[90] 비타민 D 보충의 효과는 여전히 불확실합니다.[91] L-글루타민 사용은 합병증을 줄여주기 때문에 5세부터 FDA의 지원을 받았습니다.[92]
엽산과 페니실린
생후부터 5세까지 매일 페니실린을 복용하는 것은 면역체계가 미숙해 유아기 질병에 걸리기 쉽기 때문입니다.[93] 엽산의 식이 보충은 이전에 WHO에 의해 권장되었습니다.[5] 2016년 Cochrane 사용에 대한 검토에 따르면 의학적 증거 부족으로 인해 "증강제가 빈혈 및 빈혈 증상에 미치는 영향은 불분명하다"고 합니다.[94]
말라리아 예방법

낫세포 형질의 보호 효과는 낫세포 질환을 가진 사람에게는 적용되지 않습니다. 실제로 말라리아 국가에서 고통스러운 위기의 가장 흔한 원인은 말라리아 감염이기 때문에 말라리아에 더 취약합니다. 말라리아 국가에 거주하는 겸상적혈구질환자는 예방을 위해 평생 약물치료를 받아야 합니다.[95]
폐색성 위기
겸상적인 세포 질환을 앓고 있는 대부분의 사람들은 혈관 폐쇄성 위기라고 불리는 극심하게 고통스러운 에피소드를 가지고 있습니다. 그러나 이러한 위기의 빈도, 심각성 및 기간은 매우 다양합니다. 통증이 있는 위기는 진통제로 증상을 치료합니다. 통증 관리는 위기가 해결될 때까지 일정한 간격으로 오피오이드 약물을 투여해야 합니다. 가벼운 위기의 경우 환자의 하위 그룹이 NSAID(예: 디클로페낙 또는 나프록센)를 관리합니다. 더 심각한 위기의 경우 대부분의 환자는 정맥 오피오이드에 대한 입원 관리가 필요합니다.[96]
경구 또는 정맥 주사로 투여되는 여분의 수액은 혈관 폐쇄성 위기를 치료하는 일상적인 부분이지만 가장 효과적인 수액 대체 경로, 양 및 유형에 대한 증거는 여전히 불확실합니다.[97]
2019년 미국에서 p-셀렉틴에 대한 단일클론항체 표적인 크리잔리주맙이 16세 이상의 혈관폐쇄성 위기 빈도를 줄이기 위해 승인되었습니다.[98]
뇌졸중 예방
경두개 도플러 초음파(TCD)는 뇌졸중 위험이 높은 낫세포 어린이를 탐지할 수 있습니다. 초음파 검사는 혈류 속도가 동맥 직경과 반비례하고 결과적으로 혈류 속도가 동맥 직경과 상관관계가 있으므로 낫 세포에 의해 부분적으로 막힌 혈관을 탐지합니다.[99] 2002년 미국 국립보건원(NIH)은 낫세포를 가진 어린이들에게 매년 경두개 도플러 초음파 검사를 받을 것을 권고하는 성명을 발표했고, 2014년에는 NIH가 소집한 전문가 패널이 같은 권고를 반복하는 지침을 발표했습니다. 버밍엄에 있는 앨라배마 대학의 혈액학자 줄리 칸터 박사가 의료기록을 검토한 결과, 낫 세포를 가진 어린이의 평균 48.4%만이 권장 초음파 검사를 받는 것으로 나타났습니다.[100]
1994년 NIH의 한 연구에 따르면 수혈을 받은 뇌졸중 위험에 처한 어린이의 뇌졸중 발병률은 연간 1% 미만인 반면 수혈을 받지 않은 어린이의 뇌졸중 발병률은 연간 10%였습니다. (New England Journal of Medicine 1998년 연구 참조)[99] 저렴한 제네릭 의약품 하이드록시우레아는 초음파와 수혈 외에도 비가역적 장기와 뇌 손상의 위험을 줄일 수 있습니다. 2014년 발표된 NIH의 지침에 따르면 모든 어린이와 청소년은 하이드록시 요소를 복용해야 하며, 심각한 합병증이나 1년에 3번 이상의 통증 위기를 겪는 성인도 마찬가지입니다.[100]
급성흉부증후군
관리는 혈관 폐쇄 위기와 유사하며, 항생제(일반적으로 퀴놀론 또는 마크로라이드, 세포벽 결핍["비형"] 박테리아가 증후군에 기여하는 것으로 생각되기 때문에),[101] 저산소증에 대한 산소 보충 및 면밀한 관찰이 추가됩니다. 낫세포질환자의 급성흉부증후군에 대한 항생제의 효과에 대한 양질의 근거가 없는 상황에서 2019년 현재 표준항생제 치료제는 없습니다.[102] 급성흉부증후군이 의심되는 사람은 중환자실 입원 적응증인 A-a 구배 악화로 입원하는 것이 좋습니다.[24]
폐 침윤이 악화되거나 산소 요구량이 증가하는 경우 단순 수혈 또는 교환 수혈을 지시합니다. 후자는 사람의 적혈구 질량의 상당 부분을 정상 적혈구로 교환하는 것을 포함하며, 이는 환자의 혈액 내 헤모글로빈 S의 수치를 감소시킵니다. 그러나, 낫 세포 질환을 가진 사람들의 급성 흉부 증후군에 대한 수혈의 가능한 이득 또는 해악에 대한 현재 불확실한 증거가 있습니다.[103]
히드록시우레아
하이드록시카바미드라고도 알려진 하이드록시우레아는 아마도 고통스러운 에피소드의 빈도와 생명을 위협하는 질병 또는 사망의 위험을 감소시키지만 부작용의 위험에 대한 증거는 현재 충분하지 않습니다.[104] 통증, 생명을 위협하는 질병 및 사망 위험 측면에서 수혈 및 킬레이션을 결합하는 것보다 하이드록시우레아와 정맥 절제술을 결합하는 것이 더 효과적일 수 있습니다.[104]
낫세포 빈혈 치료를 위해 승인된 최초의 약물이며, 1995년에[105] 공격 횟수와 중증도가 감소하는 것으로 나타났으며, 2003년의 한 연구에서 생존 시간이 증가할 가능성이 있는 것으로 나타났습니다.[106] 이것은 부분적으로 낫형 세포 빈혈을 유발하는 헤모글로빈 S 대신 태아 헤모글로빈 생성을 재활성화함으로써 달성됩니다. 하이드록시우레아는 이전에 화학요법제로 사용된 적이 있으며, 장기간 사용하면 해로울 수 있다는 우려도 있지만, 이 위험은 없거나 매우 작으며, 위험보다 이득이 더 클 수 있습니다.[18][107]
복셀로터는 2019년 미국에서 SS 질환자의 헤모글로빈 증가를 위해 승인되었습니다.[108]
수혈
수혈은 급성의 경우 낫세포 질환 관리에 많이 사용되며, 정상 적혈구를 추가하여 낫을 만들 수 있는 적혈구(RBC)의 수를 줄여 합병증을 예방하는 데 사용됩니다.[109] 소아에서 예방적 RBC 수혈요법은 경두개 도플러 초음파 검사에서 비정상적인 뇌 혈류를 보일 때 초발작이나 무음중풍의 위험을 감소시키는 것으로 나타났습니다.[6] 이전 뇌졸중 이벤트를 경험한 사람들의 경우 재발성 뇌졸중 및 추가 무음 뇌졸중의 위험도 줄어듭니다.[110][111]
골수이식
골수 이식은 어린이들에게 효과가 있는 것으로 입증되었습니다; 그것들은 SCD에 대한 유일한 알려진 치료법입니다.[112] 그러나 골수 이식은 필요한 특정 HLA 유형 때문에 얻기가 어렵습니다. 이상적으로 가까운 친척(동종)이 이식에 필요한 골수를 기증할 것입니다. 일부 유전자 치료법은 환자 자신의 골수 줄기세포를 생체 외에서 변화시킬 수 있으며, 이는 화학요법으로 원래의 변형되지 않은 세포를 제거한 후 환자에게 다시 이식될 수 있습니다.[113]
CRISPR-Cas9: 겸상세포 빈혈 유전체 편집
연구진은 낫세포 빈혈을 일으키는 유전적 오류를 바로잡기 위해 매우 특이적이고 강력한 DNA 도둑인 CRISPR-Cas9의 사용을 조사하고 있습니다. 이 기술을 일상적인 의료에 통합하기 전에 살아있는 배아에 대한 사용과 미래 세대에 미치는 영향에 대한 우려는 여전히 존재합니다.혈관괴사[114]
조혈모세포이식(HSCT)
겸상적혈구빈혈의 치료에는 암묵적으로 조혈모세포이식(HSCT)이 포함됩니다. 이것은 환자의 기능 장애 줄기 세포를 잘 맞는 기증자의 건강한 뼈로 대체하는 것을 의미합니다. 이상적인 고객(일반적으로 주식 또는 거의 일치하는 사람)을 찾는 것이 프로세스의 성공에 필수적입니다. 그러나 조혈모세포이식(HSCT)에는 민감한 시스템을 억제하기 위한 정확한 세부 정보가 필요하고 새로운 세포가 유지되지 않는 문제와 같은 몇 가지 단점이 여전히 있습니다. 그러나 성공적인 HSCT는 환자에게 낫세포 빈혈로부터 장기적인 치료를 가져올 수 있습니다.[115]
낫세포질환자의 뼈의 혈관성 괴사를 치료할 때 통증을 줄이거나 중단하고 관절 운동성을 유지하는 것이 치료의 목적입니다.[45] 현재 치료 옵션에는 관절 휴식, 물리 치료, 통증 완화제, 관절 대체 수술 또는 뼈 이식이 포함됩니다.[45] 가장 효과적인 치료 옵션을 평가하고 물리 치료와 수술의 조합이 물리 치료 단독보다 더 효과적인지 여부를 결정하기 위해서는 고품질의 무작위적이고 통제된 시험이 필요합니다.[45]
심리치료
현재의 의학적 치료를 보완하는 것을 목표로 하는 환자 교육, 인지 치료, 행동 치료 및 심리 역학 심리 치료와 같은 심리 치료는 그 효과를 결정하기 위해 추가 연구가 필요합니다.[25]
유전자 치료법
2023년 Exagamglogene autotemcel과 lovotibegene autotemcel 모두 낫세포질환 치료제로 승인되었습니다.[10][116]
예후
약 90%의 사람들이 20세까지 생존하고, 거의 50%가 50세를 넘어 생존합니다.[117] 2001년 자메이카에서 수행된 한 연구에 따르면, 사람들의 평균 생존 기간은 남성의 경우 53년, 여성의 경우 58년으로 추정되었습니다.[118] 대부분의 개발도상국의 기대 수명은 알려지지 않았습니다.[119] 1975년에는 SCD를 가진 사람들의 약 7.3%가 23세 생일 전에 사망했고, 1989년에는 SCD를 가진 사람들의 2.6%가 20세까지 사망했습니다.[120]: 348
역학
HbS 유전자는 모든 민족 집단에서 찾을 수 있습니다.[121] 낫 세포 질환의 가장 높은 빈도는 열대 지역, 특히 사하라 사막 이남의 아프리카, 인도의 부족 지역 및 중동에서 발견됩니다.[122] 이러한 유병률이 높은 지역에서 유럽의 유병률이 낮은 국가로 상당한 인구가 이동하는 것은 최근 수십 년 동안 극적으로 증가했으며 일부 유럽 국가에서는 낫 세포 질환이 혈우병 및 낭포성 섬유증과 같은 더 친숙한 유전적 조건을 추월했습니다.[123] 2015년에는 약 114,800명의 사망자가 발생했습니다.[8]
낫세포 질환은 말라리아가 있거나 흔했던 열대·아열대 사하라 사막 이남 지역에 조상이 살았던 사람들에게 더 흔하게 발생합니다. 말라리아가 흔한 곳에서, 하나의 낫 세포 대립 유전자( 형질)를 가지고 있는 것은 이형 접합체의 이점을 제공합니다; 낫 세포 질환의 두 대립 유전자 중 하나를 가진 인간은 말라리아에 감염되었을 때 덜 심각한 증상을 보입니다.[124]
이 상태는 상염색체 열성 패턴으로 유전되며, 이는 각 세포에 있는 유전자의 두 사본 모두에 돌연변이가 있음을 의미합니다. 부모는 각각 돌연변이 유전자의 사본 하나를 가지고 있지만, 일반적으로 그들은 그 상태의 징후와 증상을 보이지 않습니다.[125]
아프리카
낫 세포 사례의 4분의 3은 아프리카에서 발생합니다. 최근 WHO 보고서에 따르면 나이지리아 신생아의 약 2%가 낫세포 빈혈에 영향을 받아 나이지리아에서만 매년 총 150,000명의 어린이가 태어나는 것으로 추정됩니다. 캐리어 주파수는 적도 아프리카 전역에서 10~40% 사이이며 북아프리카 해안에서는 1~2%, 남아프리카에서는 1% 미만으로 감소합니다.[126] 아프리카의 연구들은 낫 세포 특성 때문에 2-16개월의 유아 사망률이 상당히 감소한다는 것을 보여줍니다. 이것은 말라리아 환자가 많은 지역에서 발생했습니다.[127]
우간다는 아프리카에서 다섯 번째로 낫 세포 질환 부담이 높습니다.[128] 한 연구에 따르면 연간 20,000명의 아기가 낫 세포 특성을 가진 낫 세포 질환을 가지고 태어나며 낫 세포 특성은 13.3%, 질병은 0.7%[129]입니다.
| 나라 | 인구(2020년) | 하위영역 | % 유행의 | 유행 | 인시던트 |
| 앙골라 | 32,866,272 | 중아프리카 | 0.09375 | 3,081,213 | 14,869 |
| 카메룬 | 26,545,863 | 중아프리카 | 0.117 | 3,105,866 | 11,826 |
| DR 콩고 | 89,561,403 | 중아프리카 | 0.1163333333 | 10,418,977 | 65,536 |
| 가나 | 31,072,940 | 서아프리카 | 0.09375 | 2,913,088 | 9,588 |
| 기니 | 13,132,795 | 서아프리카 | 0.139375 | 1,830,383 | 8,907 |
| 니제르 | 24,206,644 | 서아프리카 | 0.07025 | 1,700,517 | 8,756 |
| 나이지리아 | 206,139,589 | 서아프리카 | 0.1286666667 | 26,523,294 | 150,000 |
| 탄자니아 | 59,734,218 | 동아프리카 | 0.0545 | 3,255,515 | 19,585 |
| 우간다 | 45,741,007 | 동아프리카 | 0.07025 | 3,213,306 | 17,936 |
| 잠비아 | 18,383,955 | 동아프리카 | 0.082 | 1,507,484 | 9,958 |
| 알제리 | 43,851,044 | 북아프리카 | 0.029 | 1,271,680 | 6,624 |
| 베냉 | 12,123,200 | 서아프리카 | 0.1286666667 | 1,559,852 | 8,125 |
| 보츠와나 | 2,351,627 | 남아프리카 공화국 | 0.029 | 68,197 | 355 |
| 부르키나파소 | 20,903,273 | 서아프리카 | 0.07025 | 1,468,455 | 7,649 |
| 부룬디 | 11,890,784 | 동아프리카 | 0.023 | 273,488 | 1,425 |
| 카보베르데 | 555,987 | 서아프리카 | 0.023 | 12,788 | 67 |
| 중앙아프리카 공화국 | 4,829,767 | 중아프리카 | 0.082 | 396,041 | 2,063 |
| 차드 | 16,425,864 | 중아프리카 | 0.0585 | 960,913 | 5,005 |
| 코모로 | 869,601 | 동아프리카 | 0.023 | 20,001 | 104 |
| 콩고 | 5,518,087 | 중아프리카 | 0.1615 | 891,171 | 4,642 |
| Côte d'Ivoire | 26,378,274 | 서아프리카 | 0.07025 | 1,853,074 | 9,652 |
| 지부티 | 988,000 | 동아프리카 | 0.023 | 22,724 | 118 |
| 이집트 | 102,334,404 | 북아프리카 | 0.029 | 2,967,698 | 15,458 |
| 적도 기니 | 1,402,985 | 중아프리카 | 0.181 | 253,940 | 1,323 |
| 에리트레아 | 3,546,421 | 동아프리카 | 0.023 | 81,568 | 425 |
| 에스와티니 | 1,160,164 | 남아프리카 공화국 | 0.023 | 26,684 | 139 |
| 에티오피아 | 114,963,588 | 동아프리카 | 0.029 | 3,333,944 | 17,366 |
| 가봉 | 2,225,734 | 중아프리카 | 0.181 | 402,858 | 2,098 |
| 감비아 | 2,416,668 | 서아프리카 | 0.082 | 198,167 | 1,032 |
| 기니비사우 | 1,968,001 | 서아프리카 | 0.035 | 68,880 | 359 |
| 케냐 | 53,771,296 | 동아프리카 | 0.04675 | 2,513,808 | 13,094 |
| 레소토 | 2,142,249 | 남아프리카 공화국 | 0.023 | 49,272 | 257 |
| 라이베리아 | 5,057,681 | 서아프리카 | 0.07025 | 355,302 | 1,851 |
| 리비아 | 6,871,292 | 북아프리카 | 0.029 | 199,267 | 1,038 |
| 마다가스카르. | 27,691,018 | 동아프리카 | 0.04675 | 1,294,555 | 6,743 |
| 말라위 | 19,129,952 | 동아프리카 | 0.035 | 669,548 | 3,488 |
| 말리 | 20,250,833 | 서아프리카 | 0.082 | 1,660,568 | 8,650 |
| 모리타니 | 4,649,658 | 서아프리카 | 0.04675 | 217,372 | 1,132 |
| 모리셔스 | 1,271,768 | 동아프리카 | 0.023 | 29,251 | 152 |
| 모로코 | 36,910,560 | 북아프리카 | 0.029 | 1,070,406 | 5,576 |
| 모잠비크 | 31,255,435 | 동아프리카 | 0.035 | 1,093,940 | 5,698 |
| 나미비아 | 2,540,905 | 남아프리카 공화국 | 0.03883333333 | 98,672 | 514 |
| 르완다 | 12,952,218 | 동아프리카 | 0.035 | 453,328 | 2,361 |
| 상투메 프린시페 | 219,159 | 중아프리카 | 0.181 | 39,668 | 207 |
| 세네갈 | 16,743,927 | 서아프리카 | 0.07025 | 1,176,261 | 6,127 |
| 세이셸 | 98,347 | 동아프리카 | 0.023 | 2,262 | 12 |
| 시에라리온 | 7,976,983 | 서아프리카 | 0.1615 | 1,288,283 | 6,711 |
| 소말리아 | 15,893,222 | 동아프리카 | 0.029 | 460,903 | 2,401 |
| 남아프리카 공화국 | 59,308,690 | 남아프리카 공화국 | 0.029 | 1,719,952 | 8,959 |
| 남수단 | 11,193,725 | 동아프리카 | 0.04675 | 523,307 | 2,726 |
| 수단 | 43,849,260 | 북아프리카 | 0.03883333333 | 1,702,813 | 8,870 |
| 포장이요 | 8,278,724 | 서아프리카 | 0.09375 | 776,130 | 4,043 |
| 튀니지 | 11,818,619 | 북아프리카 | 0.023 | 271,828 | 1,416 |
| 짐바브웨 | 14,862,924 | 동아프리카 | 0.035 | 520,202 | 2,710 |
| 총 | 1,338,826,604 | 아프리카 | 91,868,664 | 495,726 |
미국
미국에서 이 병에 걸린 사람의 수는 약 10만 명(3,300명 중 1명)으로, 대부분 사하라 사막 이남의 아프리카 혈통의 미국인들에게 영향을 미칩니다.[130] 미국에서는 아프리카계 미국인 어린이 365명 중 1명, 히스패닉계 미국인 어린이 16,300명 중 1명이 낫세포 빈혈을 앓고 있습니다.[131] SCD를 가진 남성의 기대 수명은 약 42세인 반면 여성은 약 6년 더 오래 삽니다.[132] 추가적으로 200만 명이 낫 세포 형질의 보균자입니다.[133] 미국에서 태어난 SCD를 가진 대부분의 유아들은 정기적인 신생아 검진을 통해 식별됩니다. 2016년 기준으로 50개 주 모두 신생아 검진의 일환으로 낫세포 질환 검진을 포함하고 있습니다.[134] 신생아의 혈액은 힐 프릭을 통해 샘플링되고 검사를 위해 실험실로 보내집니다. 아기는 발뒤꿈치 통증 검사가 이루어지기 전에 최소 24시간 동안 식사를 하고 있었을 것입니다. 일부 주에서는 아기가 태어난 지 2주가 되었을 때 결과를 확인하기 위해 두 번째 혈액 검사를 하도록 요구하고 있습니다.[135]
낫세포 빈혈은 아프리카계 미국인들에게 가장 흔한 유전 질환입니다. 약 8%가 보균자이고 375명 중 1명이 이 질병을 가지고 태어납니다.[136] 겸상적혈구 질환의 환자 옹호자들은 낭포성 섬유증과 같은 유사한 희귀 질환보다 정부와 민간 연구비를 적게 받는다고 불평해 왔는데, 엘리엇 비친스키 연구원은 이것이 인종 차별이나 의료 옹호에서 부의 역할을 보여준다고 말했습니다.[137] 전체적으로 인종을 고려하지 않고 미국에서 태어난 유아의 약 1.5%가 돌연변이(질병 유발) 유전자의 적어도 한 사본을 운반하는 것으로 나타났습니다.[138]
프랑스.

해외 프랑스의 아프리카-카리브 지역의 인구 증가와 북 아프리카와 사하라 사막 이남의 아프리카에서 프랑스 본토로 이주한 결과, 낫 세포 질환이 프랑스의 주요 건강 문제가 되었습니다.[139] SCD는 같은 기준 기간 동안 페닐케톤뇨증(10,862명 중 1명), 선천성 갑상선 기능 저하증(3,132명 중 1명), 선천성 부신 비대증(19,008명 중 1명), 낭포성 섬유증(5,014명 중 1명)보다 앞서 프랑스 대도시에서 전체 출생 유병률이 2,415명 중 1명으로 가장 흔한 유전 질환이 되었습니다.[citation needed]

2000년부터 SCD의 신생아 검진은 민족적 기원(사하라 이남 아프리카, 북아프리카, 지중해 지역(남이탈리아, 그리스, 튀르키예), 아랍 반도, 프랑스 해외 섬에서 태어난 부모에게서 태어난 신생아로 정의됨)에 따라 국가 차원에서 실시되고 있습니다. 그리고 인도 아대륙.[140]
영국
영국에서는 12,000명에서 15,000명 사이의 사람들이 낫 세포 질환을 앓고 있는 것으로 추정되며, 영국에서만 약 250,000명의 낫 세포 질환 보균자가 있는 것으로 추정됩니다. 보균자 수는 추정치에 불과하기 때문에 영국의 모든 신생아는 정기적인 혈액 검사를 통해 상태를 검사합니다.[142] 고위험군 성인의 경우 보균자 여부를 모르는 경우가 많아 임산부와 부부 동반자 모두에게 검진을 제공하여 낫세포 특성이 있는지 상담을 받을 수 있습니다.[143] 또한 고위험군의 헌혈자도 선별하여 보균자인지, 혈액 필터가 제대로 되었는지 확인합니다.[144] 그리고 보균자로 밝혀진 기증자들에게 정보를 제공하고 그들의 혈액은 종종 같은 민족 집단의 사람들에게 사용되지만 수혈이 필요한 겸상적인 세포 질환을 가진 사람들에게는 사용되지 않습니다.[145][unreliable medical source?]
서아시아
사우디아라비아에서는 인구의 약 4.2%가 낫세포 특성을 가지고 있고 0.26%가 낫세포 질환을 가지고 있습니다. 인구의 약 17%가 유전자를 가지고 있고 1.2%가 낫 세포 질환을 가지고 있는 동부 지방에서 가장 높은 유병률을 보입니다.[146] 2005년, 사우디아라비아는 SCD와 말라리아의 발병률을 줄이기 위해 HB 전기영동을 포함한 의무적인 혼전 검사를 도입했습니다.[147]
1998년 바레인의 병원에서 약 56,000명의 사람들을 대상으로 발표된 바레인의 연구에 따르면 신생아의 2%가 낫세포 질환을 가지고 있고, 조사 대상자의 18%가 낫세포 특성을 가지고 있으며, 24%가 병을 일으키는 유전자 돌연변이의 보균자였습니다.[148] 이 나라는 1992년부터 모든 임산부에 대한 검진을 시작했고, 신생아는 산모가 보균자인지 검사를 받기 시작했습니다. 2004년, 결혼을 계획하고 있는 커플들이 무료로 혼전 상담을 받도록 하는 법이 통과되었습니다. 이러한 프로그램은 공교육 캠페인과 함께 진행되었습니다.[149]
인도 네팔
낫 세포 질환은 마디아 프라데시, 라자스탄 및 차티스가르의 풍토병 지역에서 9.4%에서 22.2%의 유병률을 보인 인도 중부의 일부 민족에서 흔히 발생합니다.[150][151] 네팔과 인도의 타루족 사이에서도 풍토병이지만 말라리아 감염 지역에 살고 있음에도 불구하고 말라리아 발병률이 7배나 낮습니다.[152]
카리브 제도
자메이카에서는 인구의 10%가 낫세포 유전자를 지니고 있어 이 나라에서 가장 흔한 유전 질환입니다.[153]
역사
낫 세포병에 대한 최초의 현대적인 보고는 처형된 도망친 노예의 부검이 논의되었던 1846년에 있었을 것입니다; 핵심적인 발견은 비장의 부재였습니다.[154][155] 보도에 따르면, 미국의 아프리카 노예들은 말라리아에 내성을 보였으나 다리 궤양에 걸리기 쉬웠다고 합니다.[155] 나중에 이 질환에 이름을 빌려준 적혈구의 비정상적인 특성은 어니스트 E에 의해 처음 기술되었습니다. 시카고의 심장내과 전문의이자 의학 교수인 아이언스(1877–1959). 헤릭 (1861–1954), 1910년. 아이언은 그레나다의 치과 1학년생인 20살 월터 클레멘트 노엘이라는 남자의 혈액에서 "특이하게 길고 낫 모양의" 세포를 보았습니다. 노엘은 1904년 12월 빈혈로 시카고 장로병원에 입원했습니다.[15][156] 노엘은 이후 3년 동안 "근육 류머티즘"과 "담즙 공격"으로 여러 번 재입원했지만, 학업을 마치고 그레나다(세인트)의 수도로 돌아갔습니다. George's) 치과를 개업합니다. 1916년 폐렴으로 세상을 떠났고 그레나다 북부 사우테우르스에 있는 가톨릭 공동묘지에 안장됐습니다.[15][16] 헤릭의 보도 직후 버지니아 메디컬 세미월간지에 같은 제목의 "심각한 빈혈의 경우 특이하게 길쭉하고 낫 모양의 적혈구"라는 또 다른 사례가 등장했습니다.[157] 이 기사는 1910년 11월 15일 버지니아 대학교 병원에 입원한 환자를 바탕으로 작성된 것입니다.[158] 1922년 베른 메이슨(Verne Mason)에 의해 나중에 기술된 '병세포 빈혈'이라는 이름이 처음 사용되었습니다.[16][159] 낫 세포 질환과 관련된 소아기 문제는 1930년대까지 보고되지 않았지만, 아프리카계 미국인 인구에서 드물지 않았을 것입니다.[155]
겸상적혈구병에 대한 다작 연구자인 멤피스 의사 레뮤엘 딕스(Lemuel Diggs)는 1933년 겸상적혈구병과 형질의 차이를 처음으로 소개했지만 1949년까지 제임스 5세에 의해 유전적 특성이 밝혀지지 않았습니다. Neel and E.A. 비트 [16]1949년은 리누스 파울링이 헤모글로빈 S의 특이한 화학적 거동을 기술한 해로, 이것을 분자 자체의 이상 때문으로 돌렸습니다.[16][160] HbS의 분자 변화는 1956년 버논 잉그램(Vernon Ingram)에 의해 설명되었습니다.[161] 1940년대 후반과 1950년대 초반에는 말라리아와 낫 세포 질환의 연관성에 대한 이해가 깊었습니다. 1954년 헤모글로빈 전기영동의 도입으로 HbSC 질환과 같은 특정 아형의 발견이 가능해졌습니다.[16]
1970년대와 1980년대에 대규모 자연사 연구와 추가 개입 연구가 도입되어 폐렴구균 감염에 대한 예방법이 널리 사용되었습니다. 빌 코스비(Bill Cosby)의 1972년 TV 영화인 해안가의 모든 나의 친구들에게(To All My Friends on Shore)는 낫 세포병을 앓고 있는 아이의 부모에 대한 이야기를 묘사했습니다.[162] 1990년대에는 하이드록시카바미드가 개발되었고, 2007년 골수 이식을 통한 완치 사례가 보고되었습니다.[16]
일부 오래된 문헌은 그것을 드레파노사이토시스라고 부릅니다.[163]
사회와 문화
미국
낫세포 질환은 장애로 자주 다툰다. [164] 2017년 9월 15일부터 미국 사회보장국은 낫 세포 질환에 대한 배경 정보와 장애 청구에 대한 판결 과정에서 사회보장국이 질병을 평가하는 방법에 대한 설명을 제공하는 정책 해석 판결을 발표했습니다.[165][166]
미국에는 SCD를 가진 사람들이 필요한 치료를 받지 못하게 하는 SCD를 둘러싼 낙인이 있습니다. 국립 심장, 폐, 혈액 연구소에 따르면 이러한 낙인들은 주로 아프리카계 미국인과 라틴 아메리카인 조상들에게 영향을 미친다고 합니다.[167] SCD를 가진 사람들은 질병의 낙인이 사회적, 심리적 행복을 포함한 삶의 여러 측면에 미치는 영향을 경험합니다. 연구에 따르면 SCD를 가진 사람들은 직장에서 그리고 관계에서 동료들 사이에서도 차별을 피하기 위해 진단을 비밀로 해야 한다고 종종 느낍니다.[168] 1960년대에 미국 정부는 SCD를 가진 사람들을 보호하기 위해 유전 질환에 대한 직장 검진 계획을 지원했습니다. 이러한 심사를 통해 직원들이 잠재적으로 유해하고 SCD를 유발할 수 있는 환경에 배치되지 않도록 의도했습니다.[169]
우간다
우간다는 세계에서 5번째로 높은 낫 세포 질환 (SCD) 부담을 가지고 있습니다.[170] 우간다에서는 낫 세포 질환에 대한 일반적인 지식이 부족하기 때문에 낫 세포 질환을 가진 사람들에게 사회적 낙인이 존재합니다. 낫세포 질환을 둘러싼 지식의 일반적인 격차는 문화적으로 승인된 질병에 대한 비밀주의로 인해 청소년과 젊은 성인 사이에서 주목됩니다.[170] 대부분의 사람들이 이 질병에 대해 일반적으로 들어본 적이 있지만, 인구의 많은 부분이 SCD가 어떻게 진단되거나 유전되는지에 대해 상대적으로 잘못 알고 있습니다. 질병에 대해 정보를 받은 사람들은 의료 전문가가 아닌 가족이나 친구로부터 질병에 대해 배웠습니다. 낫세포 질환에 대한 정보를 대중에게 제공하지 못하면 질병의 원인, 증상, 예방법에 대한 이해가 부족한 인구가 발생합니다.[171] 황달, 신체적 성장 둔화, 성 성숙 지연과 같은 낫 세포 질환을 가진 사람들에게 발생하는 신체적, 사회적 차이는 또한 그들을 괴롭힘, 거부 및 낙인의 대상으로 이끌 수 있습니다.[170]
우간다의 겸상적혈구병 발생률
우간다의 낫 세포 질환에 대해 수집된 데이터는 1970년대 초 이후로 업데이트되지 않았습니다. 우간다인들이 매일 SCD로 사망하고 있음에도 불구하고, 데이터의 부족은 정부 연구 자금의 부족 때문입니다.[172] 데이터에 따르면 겸상적인 세포 질환의 특성 빈도는 우간다 인구의 20%입니다.[172] 이는 6,600만 명이 낫 세포 질환을 가진 아이를 가질 위험에 처해 있다는 것을 의미합니다.[172] 또한 매년 약 25,000명의 우간다인들이 SCD를 가지고 태어나며 그들 중 80%가 5세 이상을 살지 않는 것으로 추정됩니다.[172] SCD는 또한 우간다의 어린이 사망률에 25%를 기여합니다.[172] 우간다의 남서쪽에 위치한 우간다의 밤바 사람들은 유전자의 45%를 가지고 있는데, 이는 세계에서 기록된 가장 높은 형질 빈도입니다.[172] 물라고에 있는 낫세포 클리닉은 전국에서 유일하게 낫세포 질환 클리닉이며 하루 평균 200명의 환자를 보고 있습니다.[172]
겸상적혈구질환에 대한 오해
질병 주변의 오명은 영향을 받지 않는 지역에서 특히 좋지 않습니다. 예를 들어, 동양 우간다인들은 낫 세포병이 신의 벌이나 마법의 결과라고 믿는 서양 우간다인들보다 병에 대해 더 잘 아는 경향이 있습니다.[173] SCD에 대한 다른 오해에는 환경적 요인에 의해 발생한다는 믿음이 포함되지만 실제로 SCD는 유전 질환입니다.[174] 우간다 전역에서 이 질병에 대한 사회적 오해를 해결하기 위한 노력이 있었습니다. 2013년에는 낫세포 질환에 대한 인식을 확산하고 병에 붙은 사회적 낙인을 퇴치하기 위해 우간다 낫세포구조재단을 설립했습니다.[175] 이 단체의 노력과 더불어 우간다에서 낫세포 질환의 오명을 줄이기 위해 기존 지역사회 보건교육 프로그램에 낫세포 질환 교육을 포함시킬 필요성이 있습니다.[171]
겸상적혈구질환자의 사회적 격리
사회로부터 뿌리 깊은 SCD의 낙인은 가족들로 하여금 꼬리표가 붙거나, 저주를 받거나, 사회 행사에서 소외되는 것을 두려워하여 종종 가족 구성원의 아픈 상태를 숨기게 합니다.[176] 우간다에서는 가족 중에 낫세포 질환이 있는 것이 확인되면 가족 모두와 친밀한 관계를 피하게 되는 경우가 있습니다.[176] 낫 세포 질환을 가진 사람들이 경험하는 오명과 사회적 고립은 종종 SCD를 가진 사람들이 질병에서 자유로운 사람들과 어울려서는 안 된다는 대중의 오해의 결과입니다. 이러한 사고방식은 SCD를 가진 사람들에게 다른[170] 모든 사람들처럼 지역사회 활동에 자유롭게 참여할 수 있는 권리를 빼앗고, 특히 학교에서의 사회적 고립은 낫세포 질환을 가진 젊은이들의 삶을 극도로 어렵게 만들 수 있습니다.[170] SCD를 가지고 생활하는 학령기 아동의 경우, 그들이 직면하는 낙인은 또래 거부로 이어질 수 있습니다.[170] 동료 거부는 사회적 그룹이나 모임에서 제외되는 것을 포함합니다. 그것은 종종 배제된 개인으로 하여금 정서적 고통을 경험하게 하며, 그들의 학업 부진, 학업 회피, 그리고 인생 후기의 직업적 실패를 초래할 수 있습니다.[170] 이러한 사회적 고립은 또한 SCD의 자존감과 전반적인 삶의 질을 가진 사람들에게 부정적인 영향을 미칠 가능성이 있습니다.[170]
낫세포 질환을 앓고 있는 아이들의 엄마들은 또래와 가족들로부터 불균형적인 양의 낙인을 받는 경향이 있습니다. 이 여성들은 종종 자녀의 SCD 진단에 대해 비난을 받을 것입니다. 특히 이전 세대에 SCD가 없는 경우 자녀의 건강이 좋지 않은 것은 어머니가 예방적 건강 조치를 시행하지 않거나 자녀가 건강하게 자랄 수 있는 환경을 촉진하지 않았기 때문일 수도 있다는 의심 때문입니다.[174] 어머니에게 책임을 돌리는 환경적 요인과 관련된 이론에 의존하는 것은 많은 우간다인들이 질병이 환경이 아닌 유전에 의해 결정되기 때문에 어떻게 획득되는지에 대한 부족한 지식을 반영합니다.[174] 겸상 적혈구 질환을 앓고 있는 아이들의 어머니들은 또한 종종 SCD에 걸린다는 오명으로부터 미래를 보호할 수 있는 매우 제한된 자원을 가지고 있습니다.[174] 이러한 자원에 대한 접근 부족은 가족 구조 내에서 종속적인 역할뿐만 아니라 많은 어머니들이 추가적인 보육 비용과 책임을 만족시키는 능력을 방해하는 계층 차이에서 비롯됩니다.[174]
임신을 한 SCD를 가지고 사는 여성들은 우간다에서 종종 극도의 차별과 낙담에 직면합니다. 이 여성들은 종종 동료들로부터 낫세포 질환을 앓고 있는 동안 아기를 낳거나 심지어 SCD를 앓고 있는 동안 성행위를 하는 것에 대해 무책임하다고 낙인 찍힙니다.[citation needed] 이 여성들이 의료 전문가뿐만 아니라 그들의 가족으로부터 받는 비판과 판단은 종종 그들을 외롭고, 우울하고, 불안하고, 부끄럽고, 사회적 지지가 거의 없는 상태로 만듭니다.[citation needed] SCD를 가진 대부분의 임신부들은 또한 미혼모가 되는데, 그들은 그들의 파트너의 SCD 상태를 몰랐다고 주장하는 그들의 남자 파트너에 의해 남겨지는 것이 일반적이기 때문입니다.[citation needed] 이러한 여성들이 경험하는 포기는 그들에게 정서적 고통을 줄 뿐만 아니라, 이러한 낮은 수준의 부모의 지지는 일단 태어나면 우울한 증상과 전반적으로 낮은 삶의 질로 연결될 수 있습니다.[177]
영국
2021년에 많은 환자들이 직원들의 무지 수준과 같이 병원을 방문하는 것을 두려워하는 것으로 밝혀져 NHS 밖에서 치료하기 위해 통증 완화제를 구입했습니다.[citation needed] 그들은 종종 통증 완화를 위해 오랜 시간을 기다렸고, 때때로 "약물을 찾는" 행동을 의심했습니다. 치료 지연, 병원 혈액내과 팀에 알리지 않음, 통증 관리 부실로 사망자가 발생했습니다. 혈액학 전문 직원들은 더 큰 교육 병원에서 일하는 것을 선호하여 다른 곳에서는 전문 지식이 부족합니다.[178] 2021년 NHS는 낫셀에 대해 20년 만에 처음으로 새로운 치료법을 시작했습니다. 여기에는 수혈 방울을 통해 투여되는 약물인 크리잔리주맙을 사용하는 것이 포함되어 있으며, 이는 환자의 A&E 방문 횟수를 줄여줍니다. 이 치료법은 컨설턴트를 통해 전국에 설치된 10개의 새로운 허브에서 액세스할 수 있습니다.[179] 그러나 같은 해, '아무도 듣지 않는다'는 제목의 낫셀과 탈라사미아에 대한 보고서를 올당 의회 그룹이 만들었습니다.[180][unreliable medical source?] 이에 부분적으로 대응하여 2022년 6월 19일 세계 낫 세포의 날에 NHS는 " 낫 세포라고 말할 수 있습니까?"라는 캠페인을 시작했습니다. 그 캠페인은 쌍둥이의 목적을 가지고 있었습니다. 하나는 혈액 장애의 주요 징후와 증상에 대한 인식을 높여 사람들이 임박한 심장마비나 뇌졸중만큼이나 낫 세포 위기의 징후에 대해 경각심을 갖도록 하는 것이었습니다. 두 번째 목표는 구급대원, 사고 및 응급 직원, 보호자 및 일반 대중이 위기에 처한 환자를 효과적으로 돌볼 수 있도록 돕기 위한 새로운 훈련 프로그램을 마련하는 것이었습니다.[181]
조사.
제대혈 이식
제대혈 이식은 잠재적으로 이 상태를 치료할 수 있지만 적합한 기증자는 10%의 사람들에게만 제공됩니다.[182] 또한 약 7%의 사람들이 시술로 인해 사망하고 이식 대 숙주 질환이 발생할 수 있습니다.[182]
유전자 치료법
변이된 유전자의 정상적인 복제에 의해 병에 걸린 세포에서 사람의 정상적인 표현형이나 세포 기능이 회복될 수 있는 겸상적인 세포 질환과 같은 질병이 유전자 치료의 좋은 후보가 될 수 있습니다. 겸상 적혈구 질환의 유전자 치료와 관련된 위험과 이점은 알려져 있지 않습니다.[183]
2001년에는 낫세포 질환을 유전자 치료법을 이용해 쥐를 대상으로 성공적으로 치료한 것으로 알려졌습니다.[184][185] 연구원들은 바이러스 벡터를 사용하여 사람의 낫 세포 질환을 유발하는 본질적으로 동일한 결함을 가진 쥐가 출생 직후에 일반적으로 생산을 중단하는 태아 헤모글로빈(HbF)의 생산을 발현하도록 했습니다. 인간의 경우 히드록시 요소를 사용하여 HbF의 생성을 자극하면 겸상적인 세포 질환 증상을 일시적으로 완화시키는 것으로 알려져 있습니다. 연구진은 이 유전자 치료법이 치료적 HbF 생성을 증가시키는 보다 영구적인 방법임을 입증했습니다.[186]
2014년 인간 대상 낫세포질환 유전자 치료제 임상 1상 시작 임상시험은 중증 낫세포질환 성인을 대상으로 렌티바이러스 벡터 변형 골수의 안전성을 평가했습니다.[187][188] 2017년 3월에 첫 번째 치료를 받은 사람에 대한 사례 보고서가 발표되었고, 이후 몇 명이 더 치료를 받았습니다.[189][190]
CRISPR/Cas9와 같은 유전자 편집 플랫폼을 사용하여 질환을 유발하는 사람으로부터 채취한 조혈모세포의 돌연변이를 수정했습니다.[191] 2019년 7월, 유전자 편집 도구 크리스퍼(CRISPR)는 BCL11A 유전자를 억제하여 태아 헤모글로빈을 증가시키기 위해 SCD를 가진 사람의 골수 세포를 편집하는 데 사용되었습니다.[192][193] 많은 연구자들은 의료 분야에서 아프리카계 미국인 공동체의 역사적 남용과 방치를 고려할 때 SCD의 윤리적 의미를 CRISPR 기술의 첫 번째 잠재적 응용 중 하나로 간주했습니다.[194]
2017년에는 낫세포 빈혈을 치료하기 위한 유전자 치료제를 중심으로 12건의 임상시험을 진행하고 있었습니다. 그 12개의 시험 중 4개는 돌연변이 HBB 유전자를 건강한 것으로 대체했습니다. 줄기세포의 증가가 유전자 치료에 사용될 수 있는지를 확인하기 위해 암의 종류를 치료하는 데 사용되는 약물인 모조빌을 세 번의 실험에서 사용했습니다. 한 시험은 낫세포 빈혈 환자의 골수 샘플을 분석하는 데 초점을 맞췄습니다. 또 다른 실험은 낫 세포 빈혈이 있거나 없는 아기의 제대혈을 유전자 치료법을 개발하기 위해 사용하는 실험을 했습니다.[195]
2023년 11월 영국 규제당국으로부터 낫세포질환 치료제와 혈액장애 수혈 의존성 베타탈라스혈증 치료제로 크리스퍼 유전자 편집 도구를 이용한 유전자 치료제가 승인되었습니다.[11][196]
조혈모세포이식
조혈모세포 이식으로 낫세포 질환자를 치료하는 것과 관련된 위험과 잠재적인 이점을 결정할 수 있는 강력한 의학적 증거는 없습니다.[197]
메모들
참고문헌
- ^ a b c d e "What Are the Signs and Symptoms of Sickle Cell Disease?". National Heart, Lung, and Blood Institute. 12 June 2015. Archived from the original on 9 March 2016. Retrieved 8 March 2016.
- ^ a b c d e f g h i j "What Is Sickle Cell Disease?". National Heart, Lung, and Blood Institute. 12 June 2015. Archived from the original on 6 March 2016. Retrieved 8 March 2016.
- ^ a b c "What Causes Sickle Cell Disease?". National Heart, Lung, and Blood Institute. 12 June 2015. Archived from the original on 24 March 2016. Retrieved 8 March 2016.
- ^ a b c "How Is Sickle Cell Disease Diagnosed?". National Heart, Lung, and Blood Institute. 12 June 2015. Archived from the original on 9 March 2016. Retrieved 8 March 2016.
- ^ a b c d "Sickle-cell disease and other haemoglobin disorders Fact sheet N°308". January 2011. Archived from the original on 9 March 2016. Retrieved 8 March 2016.
- ^ a b c d "How Is Sickle Cell Disease Treated?". National Heart, Lung, and Blood Institute. 12 June 2015. Archived from the original on 9 March 2016. Retrieved 8 March 2016.
- ^ a b Allen C, Arora M, Barber RM, Bhutta ZA, Brown A, Carter A, et al. (GBD 2015 Disease and Injury Incidence and Prevalence Collaborators) (October 2016). "Global, regional, and national incidence, prevalence, and years lived with disability for 310 diseases and injuries, 1990–2015: a systematic analysis for the Global Burden of Disease Study 2015". Lancet. 388 (10053): 1545–1602. doi:10.1016/S0140-6736(16)31678-6. PMC 5055577. PMID 27733282.
- ^ a b c Wang H, Naghavi M, Allen C, Barber RM, Bhutta ZA, Carter A, et al. (GBD 2015 Mortality and Causes of Death Collaborators) (October 2016). "Global, regional, and national life expectancy, all-cause mortality, and cause-specific mortality for 249 causes of death, 1980–2015: a systematic analysis for the Global Burden of Disease Study 2015". Lancet. 388 (10053): 1459–1544. doi:10.1016/S0140-6736(16)31012-1. PMC 5388903. PMID 27733281.
- ^ "Learning About Sickle Cell Disease". National Human Genome Research Institute. 9 May 2016. Archived from the original on 4 January 2017. Retrieved 23 January 2017.
- ^ a b "FDA Approves First Gene Therapies to Treat Patients with Sickle Cell Disease". U.S. Food and Drug Administration (FDA). 8 December 2023. Archived from the original on 8 December 2023. Retrieved 8 December 2023.
 이 문서에는 공개 도메인에 있는 이 출처의 텍스트가 포함되어 있습니다.
이 문서에는 공개 도메인에 있는 이 출처의 텍스트가 포함되어 있습니다. - ^ a b Wilkinson E (16 November 2023). "UK regulator approves "groundbreaking" gene treatment for sickle cell and β thalassaemia". BMJ. 383: 2706. doi:10.1136/bmj.p2706. ISSN 1756-1833. PMID 37973171. S2CID 265264939.
- ^ Vos T, Barber RM, Bell B, Bertozzi-Villa A, Biryukov S, Bolliger I, et al. (Global Burden of Disease Study 2013 Collaborators) (August 2015). "Global, regional, and national incidence, prevalence, and years lived with disability for 301 acute and chronic diseases and injuries in 188 countries, 1990–2013: a systematic analysis for the Global Burden of Disease Study 2013". Lancet. 386 (9995): 743–800. doi:10.1016/s0140-6736(15)60692-4. PMC 4561509. PMID 26063472.
- ^ a b c Rees DC, Williams TN, Gladwin MT (December 2010). "Sickle-cell disease". Lancet. 376 (9757): 2018–2031. doi:10.1016/s0140-6736(10)61029-x. PMID 21131035. S2CID 29909566.
- ^ Elzouki AY (2012). Textbook of clinical pediatrics (2 ed.). Berlin: Springer. p. 2950. ISBN 9783642022012.
- ^ a b c Savitt TL, Goldberg MF (January 1989). "Herrick's 1910 case report of sickle cell anemia. The rest of the story". The Journal of the American Medical Association. 261 (2): 266–271. doi:10.1001/jama.261.2.266. PMID 2642320.
- ^ a b c d e f g h i Serjeant GR (December 2010). "One hundred years of sickle cell disease". British Journal of Haematology. 151 (5): 425–429. doi:10.1111/j.1365-2141.2010.08419.x. PMID 20955412.
- ^ a b "Sickle cell disease: MedlinePlus Genetics". medlineplus.gov. Retrieved 22 October 2022.
- ^ a b Yawn BP, Buchanan GR, Afenyi-Annan AN, Ballas SK, Hassell KL, James AH, et al. (September 2014). "Management of sickle cell disease: summary of the 2014 evidence-based report by expert panel members". The Journal of the American Medical Association. 312 (10): 1033–1048. doi:10.1001/jama.2014.10517. PMID 25203083. S2CID 37681044.
- ^ a b c Gill FM, Sleeper LA, Weiner SJ, Brown AK, Bellevue R, Grover R, et al. (15 July 1995). "Clinical events in the first decade in a cohort of infants with sickle cell disease. Cooperative Study of Sickle Cell Disease [see comments]". Blood. 86 (2): 776–783. doi:10.1182/blood.v86.2.776.bloodjournal862776. ISSN 0006-4971.
- ^ "Sickle Cell Disease - Symptoms NHLBI, NIH". www.nhlbi.nih.gov. 30 August 2023. Retrieved 22 March 2024.
- ^ "BestBets: How long should an average sickle cell crisis last?". Archived from the original on 17 June 2010. Retrieved 27 November 2010.
- ^ Kumar V, Abbas AK, Fausto N, Aster J (28 May 2009). Robbins and Cotran Pathologic Basis of Disease (Professional Edition: Expert Consult – Online (Robbins Pathology) ed.). Elsevier Health. pp. Kindle Locations 33498–33499.
- ^ Olujohungbe A, Burnett AL (March 2013). "How I manage priapism due to sickle cell disease". British Journal of Haematology. 160 (6): 754–765. doi:10.1111/bjh.12199. PMID 23293942.
- ^ a b c d Glassberg J (August 2011). "Evidence-based management of sickle cell disease in the emergency department". Emergency Medicine Practice. 13 (8): 1–20, quiz 20. PMID 22164362.
- ^ a b Anie KA, Green J (May 2015). "Psychological therapies for sickle cell disease and pain". The Cochrane Database of Systematic Reviews. 2015 (5): CD001916. doi:10.1002/14651858.CD001916.pub3. PMC 7063720. PMID 25966336.
- ^ Pearson HA (August 1977). "Sickle cell anemia and severe infections due to encapsulated bacteria" (Free full text). The Journal of Infectious Diseases. 136 (Suppl): S25–S30. doi:10.1093/infdis/136.Supplement.S25. PMID 330779. Archived from the original on 27 May 2016.
- ^ Wong WY, Powars DR, Chan L, Hiti A, Johnson C, Overturf G (March 1992). "Polysaccharide encapsulated bacterial infection in sickle cell anemia: a thirty year epidemiologic experience". American Journal of Hematology. 39 (3): 176–182. doi:10.1002/ajh.2830390305. PMID 1546714. S2CID 19977178.
- ^ Khatib R, Rabah R, Sarnaik SA (January 2009). "The spleen in the sickling disorders: an update". Pediatric Radiology. 39 (1): 17–22. doi:10.1007/s00247-008-1049-9. PMID 19002450. S2CID 2547649.
- ^ Mekontso Dessap A, Leon R, Habibi A, Nzouakou R, Roudot-Thoraval F, Adnot S, et al. (March 2008). "Pulmonary hypertension and cor pulmonale during severe acute chest syndrome in sickle cell disease". American Journal of Respiratory and Critical Care Medicine. 177 (6): 646–653. CiteSeerX 10.1.1.504.790. doi:10.1164/rccm.200710-1606OC. PMID 18174543.
- ^ Paul RN, Castro OL, Aggarwal A, Oneal PA (September 2011). "Acute chest syndrome: sickle cell disease". European Journal of Haematology. 87 (3): 191–207. doi:10.1111/j.1600-0609.2011.01647.x. PMID 21615795. S2CID 40320701.
- ^ Kumar V, Abbas AK, Fausto N, Aster J (28 May 2009). Robbins and Cotran Pathologic Basis of Disease (Professional Edition: Expert Consult – Online (Robbins Pathology) ed.). Elsevier Health. pp. Kindle Location 33329.
- ^ Slavov SN, Kashima S, Pinto AC, Covas DT (August 2011). "Human parvovirus B19: general considerations and impact on patients with sickle-cell disease and thalassemia and on blood transfusions". FEMS Immunology and Medical Microbiology. 62 (3): 247–262. doi:10.1111/j.1574-695X.2011.00819.x. PMID 21585562.
- ^ Balgir RS (March 2012). "Community expansion and gene geography of sickle cell trait and G6PD deficiency, and natural selection against malaria: experience from tribal land of India". Cardiovascular & Hematological Agents in Medicinal Chemistry. 10 (1): 3–13. doi:10.2174/187152512799201190. PMID 22264009.
- ^ Fibach E, Rachmilewitz E (2008). "The Role of Oxidative Stress in Hemolytic Anemia". Current Molecular Medicine. 8 (7): 609–619. doi:10.2174/156652408786241384. PMID 18991647.
- ^ Jadavji T, Prober CG (April 1985). "Dactylitis in a child with sickle cell trait". Canadian Medical Association Journal. 132 (7): 814–815. PMC 1345873. PMID 3978504.
- ^ Worrall VT, Butera V (December 1976). "Sickle-cell dactylitis". The Journal of Bone and Joint Surgery. American Volume. 58 (8): 1161–1163. doi:10.2106/00004623-197658080-00024. PMID 1002763. Archived from the original on 23 September 2016.
- ^ Miller ST (May 2011). "How I treat acute chest syndrome in children with sickle cell disease". Blood. 117 (20): 5297–5305. doi:10.1182/blood-2010-11-261834. PMID 21406723. S2CID 206896811.
- ^ Friend A, Girzadas D (2021). "Acute Chest Syndrome". StatPearls. StatPearls Publishing. PMID 28722902. Retrieved 21 March 2021.
- ^ James WD, Berger TG, et al. (2006). Andrews' Diseases of the Skin: clinical Dermatology. Saunders Elsevier. p. 847. ISBN 978-0-7216-2921-6.
- ^ 오류 인용: 명명된 참조
online source호출되었지만 정의되지 않았습니다(도움말 페이지 참조). - ^ Kavanagh PL, Sprinz PG, Vinci SR, Bauchner H, Wang CJ (December 2011). "Management of children with sickle cell disease: a comprehensive review of the literature". Pediatrics. 128 (6): e1552–e1574. doi:10.1542/peds.2010-3686. PMID 22123880. S2CID 14524078. Archived from the original on 4 March 2016.
- ^ Adams RJ, Ohene-Frempong K, Wang W (2001). "Sickle cell and the brain". Hematology. American Society of Hematology. Education Program. 2001 (1): 31–46. doi:10.1182/asheducation-2001.1.31. PMID 11722977.
- ^ Adams RJ (November 2007). "Big strokes in small persons". Archives of Neurology. 64 (11): 1567–1574. doi:10.1001/archneur.64.11.1567. PMID 17998439.
- ^ "Cholelithiasis". The Lecturio Medical Concept Library. Retrieved 25 August 2021.
- ^ a b c d Martí-Carvajal AJ, Solà I, Agreda-Pérez LH (December 2019). "Treatment for avascular necrosis of bone in people with sickle cell disease". The Cochrane Database of Systematic Reviews. 2019 (12): CD004344. doi:10.1002/14651858.CD004344.pub7. PMC 6894369. PMID 31803937.
- ^ Kenny MW, George AJ, Stuart J (July 1980). "Platelet hyperactivity in sickle-cell disease: a consequence of hyposplenism". Journal of Clinical Pathology. 33 (7): 622–625. doi:10.1136/jcp.33.7.622. PMC 1146172. PMID 7430367.
- ^ Chrouser KL, Ajiboye OB, Oyetunji TA, Chang DC (April 2011). "Priapism in the United States: the changing role of sickle cell disease". American Journal of Surgery. 201 (4): 468–474. doi:10.1016/j.amjsurg.2010.03.017. PMID 21421100.
- ^ Almeida A, Roberts I (May 2005). "Bone involvement in sickle cell disease". British Journal of Haematology. 129 (4): 482–490. doi:10.1111/j.1365-2141.2005.05476.x. PMID 15877730. S2CID 908481.
- ^ Rudge FW (1991). "Hyperbaric oxygen therapy in the treatment of sickle cell leg ulcers". J. Hyperbaric Med. 6 (1): 1–4. Archived from the original on 15 April 2013. Retrieved 23 March 2011.
{{cite journal}}: CS1 maint : 잘못된 URL (링크) - ^ Elagouz M, Jyothi S, Gupta B, Sivaprasad S (July 2010). "Sickle cell disease and the eye: old and new concepts". Survey of Ophthalmology. 55 (4): 359–377. doi:10.1016/j.survophthal.2009.11.004. PMID 20452638.
- ^ Smith WR, Penberthy LT, Bovbjerg VE, McClish DK, Roberts JD, Dahman B, et al. (January 2008). "Daily assessment of pain in adults with sickle cell disease". Annals of Internal Medicine. 148 (2): 94–101. CiteSeerX 10.1.1.690.5870. doi:10.7326/0003-4819-148-2-200801150-00004. PMID 18195334. S2CID 34924760.
- ^ Lai YC, Potoka KC, Champion HC, Mora AL, Gladwin MT (June 2014). "Pulmonary arterial hypertension: the clinical syndrome". Circulation Research. 115 (1): 115–130. doi:10.1161/CIRCRESAHA.115.301146. PMC 4096686. PMID 24951762.
- ^ Caughey MC, Poole C, Ataga KI, Hinderliter AL (August 2015). "Estimated pulmonary artery systolic pressure and sickle cell disease: a meta-analysis and systematic review". British Journal of Haematology. 170 (3): 416–424. doi:10.1111/bjh.13447. PMID 25854714. S2CID 23920740.
- ^ Niss O, Quinn CT, Lane A, Daily J, Khoury PR, Bakeer N, et al. (March 2016). "Cardiomyopathy With Restrictive Physiology in Sickle Cell Disease". JACC. Cardiovascular Imaging. 9 (3): 243–252. doi:10.1016/j.jcmg.2015.05.013. PMC 4788530. PMID 26897687.
- ^ Niss O, Fleck R, Makue F, Alsaied T, Desai P, Towbin JA, et al. (July 2017). "Association between diffuse myocardial fibrosis and diastolic dysfunction in sickle cell anemia". Blood. 130 (2): 205–213. doi:10.1182/blood-2017-02-767624. PMC 5510791. PMID 28507082.
- ^ Rai P, Niss O, Malik P (November 2017). "A reappraisal of the mechanisms underlying the cardiac complications of sickle cell anemia". Pediatric Blood & Cancer. 64 (11): e26607. doi:10.1002/pbc.26607. PMID 28453224. S2CID 24444332.
- ^ Powars DR, Elliott-Mills DD, Chan L, Niland J, Hiti AL, Opas LM, et al. (October 1991). "Chronic renal failure in sickle cell disease: risk factors, clinical course, and mortality". Annals of Internal Medicine. 115 (8): 614–620. doi:10.7326/0003-4819-115-8-614. PMID 1892333.
- ^ Sankaran VG, Orkin SH (January 2013). "The switch from fetal to adult hemoglobin". Cold Spring Harbor Perspectives in Medicine. 3 (1): a011643. doi:10.1101/cshperspect.a011643. PMC 3530042. PMID 23209159.
- ^ "Sickle Cell Disease". NORD (National Organization for Rare Disorders). Retrieved 10 June 2019.
- ^ "sickle cell disease". Genetics Home Reference. Archived from the original on 15 May 2016. Retrieved 7 May 2016.
- ^ "Inheritance of Sickle Cell Anaemia". Sickle Cell Society. Archived from the original on 8 January 2024. Retrieved 8 January 2024.
- ^ "Sickle-Cell Anemia: Haplotype Learn Science at Scitable". www.nature.com. Retrieved 12 October 2023.
- ^ Green NS, Fabry ME, Kaptue-Noche L, Nagel RL (October 1993). "Senegal haplotype is associated with higher HbF than Benin and Cameroon haplotypes in African children with sickle cell anemia". American Journal of Hematology. 44 (2): 145–146. doi:10.1002/ajh.2830440214. PMID 7505527. S2CID 27341091.
- ^ Clancy S (2008). "Genetic mutation". Nature Education. 1 (1): 187.
- ^ Odièvre MH, Verger E, Silva-Pinto AC, Elion J (October 2011). "Pathophysiological insights in sickle cell disease". The Indian Journal of Medical Research. 134 (1): 532–537. doi:10.1007/bf00168807. PMC 3237253. PMID 22089617.
- ^ Allison AC (October 2009). "Genetic control of resistance to human malaria". Current Opinion in Immunology. 21 (5): 499–505. doi:10.1016/j.coi.2009.04.001. PMID 19442502.
- ^ Kwiatkowski DP (August 2005). "How malaria has affected the human genome and what human genetics can teach us about malaria". American Journal of Human Genetics. 77 (2): 171–192. doi:10.1086/432519. PMC 1224522. PMID 16001361.
- ^ Ponçon N, Toty C, L'Ambert G, Le Goff G, Brengues C, Schaffner F, et al. (February 2007). "Biology and dynamics of potential malaria vectors in Southern France". Malaria Journal. 6 (1): 18. doi:10.1186/1475-2875-6-18. PMC 1808464. PMID 17313664.
- ^ Lesi FE, Bassey EE (July 1972). "Family study in sickle cell disease in Nigeria". Journal of Biosocial Science. 4 (3): 307–313. doi:10.1017/S0021932000008622. PMID 5041262. S2CID 41719342.
- ^ Capriotti T, Frizzell JP (2016). Pathophysiology : introductory concepts and clinical perspectives. Philadelphia. ISBN 9780803615717. OCLC 900626405.
{{cite book}}: CS1 maint: 위치 누락 게시자(링크) - ^ "How Does Sickle Cell Cause Disease?". Archived from the original on 23 September 2010. Retrieved 27 November 2010.
- ^ "Sickle Cell Anemia: eMedicine Emergency Medicine". Archived from the original on 4 December 2010. Retrieved 27 November 2010.
- ^ Kruzliak P (19 July 2012), "Hematologic manifestations of celiac disease", Celiac Disease – From Pathophysiology to Advanced Therapies, InTech, doi:10.5772/31233, ISBN 978-953-51-0684-5
- ^ Atkinson K, Mabey D (23 May 2019). Revolutionizing Tropical Medicine: Point-of-Care Tests, New Imaging Technologies and Digital Health. Wiley. p. 227. ISBN 978-1-119-28265-5.
- ^ McPherson RA, Pincus MR (2017). Henry's Clinical Diagnosis and Management by Laboratory Methods (23 ed.). Elsevier Health Sciences. p. 578. ISBN 978-0-323-41315-2.
- ^ Clarke GM, Higgins TN (August 2000). "Laboratory investigation of hemoglobinopathies and thalassemias: review and update". Clinical Chemistry. 46 (8 Pt 2): 1284–1290. doi:10.1093/clinchem/46.8.1284. PMID 10926923. Archived from the original on 20 March 2008.
- ^ "BestBets: Does routine urinalysis and chest radiography detect occult bacterial infection in sickle cell patients presenting to the accident and emergency department with painful crisis?". Archived from the original on 17 June 2010. Retrieved 27 November 2010.
- ^ "National Society of Genetic Counselors : About Genetic Counselors". www.nsgc.org. Retrieved 24 February 2021.
- ^ "ABGC – Information for Certified Genetic Counselors ABGC". www.abgc.net. Archived from the original on 19 April 2021. Retrieved 23 February 2021.
- ^ Colah, R. B., Gorakshakar, A. C., & Nadkarni, A. H. (2011). 헤모글로빈 병증의 산전 진단을 위한 침습적 및 비침습적 접근법: 인도의 경험. 인도 의학 연구 저널, 134(4), 552-560.
- ^ Lee, C., Davies, S., & Dezatou, C. (2000). 낫 세포 질환에 대한 신생아 검진. 코크란 콜라보레이션. (주)존 와일리 & 선즈
- ^ Stallings E (27 July 2019). "Genetic Counselors Of Color Tackle Racial, Ethnic Disparities In Health Care". NPR. Retrieved 23 February 2021.
- ^ Goldsmith JC, Bonham VL, Joiner CH, Kato GJ, Noonan AS, Steinberg MH (March 2012). "Framing the research agenda for sickle cell trait: building on the current understanding of clinical events and their potential implications". American Journal of Hematology. 87 (3): 340–346. doi:10.1002/ajh.22271. PMC 3513289. PMID 22307997.
- ^ Bonham VL, Dover GJ, Brody LC (September 2010). "Screening student athletes for sickle cell trait--a social and clinical experiment". The New England Journal of Medicine. 363 (11): 997–999. doi:10.1056/NEJMp1007639. PMID 20825310.
- ^ Acharya K, Benjamin HJ, Clayton EW, Ross LF (November 2011). "Attitudes and beliefs of sports medicine providers to sickle cell trait screening of student athletes". Clinical Journal of Sport Medicine. 21 (6): 480–485. doi:10.1097/JSM.0b013e31822e8634. PMID 21959797. S2CID 11404187.
- ^ Ferrari R, Parker LS, Grubs RE, Krishnamurti L (December 2015). "Sickle Cell Trait Screening of Collegiate Athletes: Ethical Reasons for Program Reform". Journal of Genetic Counseling. 24 (6): 873–877. doi:10.1007/s10897-015-9849-1. PMID 26040250. S2CID 15889144.
- ^ "Statement on Screening for Sickle Cell Trait and Athletic Participation". American Society of Hematology. Archived from the original on 26 January 2021. Retrieved 24 February 2021.
- ^ Martin C, Pialoux V, Faes C, Charrin E, Skinner S, Connes P (February 2018). "Does physical activity increase or decrease the risk of sickle cell disease complications?". British Journal of Sports Medicine. 52 (4): 214–218. doi:10.1136/bjsports-2015-095317. PMID 26701924. S2CID 24464344.
- ^ "Keeping Well with Sickle Cell Disease - Brent Sickle Cell & Thalassaemia Centre". www.sickle-thal.nwlh.nhs.uk. Archived from the original on 3 October 2019. Retrieved 4 October 2019.
- ^ "Nutrition for the Child with Sickle Cell Anemia". www.eatright.org. Archived from the original on 19 June 2020. Retrieved 5 October 2019.
- ^ Soe HH, Abas AB, Than NN, Ni H, Singh J, Said AR, et al. (May 2020). "Vitamin D supplementation for sickle cell disease". The Cochrane Database of Systematic Reviews. 5 (9): CD010858. doi:10.1002/14651858.CD010858.pub3. PMC 7386793. PMID 32462740.
- ^ Office of the Commissioner (7 July 2017). "Press Announcements – FDA approves new treatment for sickle cell disease". www.fda.gov. Archived from the original on 10 July 2017. Retrieved 10 July 2017.
- ^ "Evidence-Based Management of Sickle Cell Disease" (PDF). 2014. Retrieved 16 November 2017.
twice-daily prophylactic penicillin beginning in early infancy and continuing through at least age 5
- ^ Dixit R, Nettem S, Madan SS, Soe HH, Abas AB, Vance LD, et al. (March 2018). "Folate supplementation in people with sickle cell disease". The Cochrane Database of Systematic Reviews. 3 (4): CD011130. doi:10.1002/14651858.CD011130.pub3. PMC 5440187. PMID 29546732.
- ^ Oniyangi O, Omari AA (November 2019). "Malaria chemoprophylaxis in sickle cell disease". The Cochrane Database of Systematic Reviews. 2019 (11). doi:10.1002/14651858.CD003489.pub2. PMC 6532723. PMID 31681984.
- ^ Carroll CP (January 2020). "Opioid treatment for acute and chronic pain in patients with sickle cell disease". Neuroscience Letters. 714. Elsevier BV: 134534. doi:10.1016/j.neulet.2019.134534. PMID 31593753. S2CID 203667575.
- ^ Okomo U, Meremikwu MM (July 2017). "Fluid replacement therapy for acute episodes of pain in people with sickle cell disease". The Cochrane Database of Systematic Reviews. 7 (4): CD005406. doi:10.1002/14651858.CD005406.pub5. PMC 6483538. PMID 28759112.
- ^ "FDA approves crizanlizumab-tmca for sickle cell disease". U.S. Food and Drug Administration. 15 November 2019. Retrieved 12 December 2023.
- ^ a b Adams RJ, McKie VC, Hsu L, Files B, Vichinsky E, Pegelow C, et al. (July 1998). "Prevention of a first stroke by transfusions in children with sickle cell anemia and abnormal results on transcranial Doppler ultrasonography". The New England Journal of Medicine. 339 (1): 5–11. doi:10.1056/NEJM199807023390102. PMID 9647873.
- ^ a b Kolata G (24 May 2021). "These Sisters With Sickle Cell Had Devastating, and Preventable, Strokes". The New York Times.
- ^ Aldrich TK, Nagel RL (1998). "Pulmonary Complications of Sickle Cell Disease.". In Reynolds HY, Bone RC, Dantzker DR, George RB, Matthay RA (eds.). Pulmonary and Critical Care Medicine (6th ed.). St. Louis: Mosby. pp. 1–10. ISBN 978-0-8151-1371-3.
- ^ Martí-Carvajal AJ, Conterno LO, Knight-Madden JM (September 2019). "Antibiotics for treating acute chest syndrome in people with sickle cell disease". The Cochrane Database of Systematic Reviews. 9 (4): CD006110. doi:10.1002/14651858.CD006110.pub5. PMC 6749554. PMID 31531967.
- ^ Dolatkhah R, Dastgiri S (January 2020). "Blood transfusions for treating acute chest syndrome in people with sickle cell disease". The Cochrane Database of Systematic Reviews. 1 (1): CD007843. doi:10.1002/14651858.CD007843.pub4. PMC 6984655. PMID 31942751.
- ^ a b Rankine-Mullings AE, Nevitt SJ (September 2022). "Hydroxyurea (hydroxycarbamide) for sickle cell disease". The Cochrane Database of Systematic Reviews. 2022 (10): CD002202. doi:10.1002/14651858.CD002202.pub3. PMC 9435593. PMID 36047926.
- ^ Charache S, Terrin ML, Moore RD, Dover GJ, Barton FB, Eckert SV, et al. (May 1995). "Effect of hydroxyurea on the frequency of painful crises in sickle cell anemia. Investigators of the Multicenter Study of Hydroxyurea in Sickle Cell Anemia". The New England Journal of Medicine. 332 (20): 1317–1322. doi:10.1056/NEJM199505183322001. PMID 7715639.
- ^ Steinberg MH, Barton F, Castro O, Pegelow CH, Ballas SK, Kutlar A, et al. (April 2003). "Effect of hydroxyurea on mortality and morbidity in adult sickle cell anemia: risks and benefits up to 9 years of treatment". The Journal of the American Medical Association. 289 (13): 1645–1651. doi:10.1001/jama.289.13.1645. PMID 12672732.
- ^ Platt OS (March 2008). "Hydroxyurea for the treatment of sickle cell anemia". The New England Journal of Medicine. 358 (13): 1362–1369. doi:10.1056/NEJMct0708272. PMID 18367739. S2CID 351061.
- ^ Center for Drug Evaluation and Research (25 November 2019). "FDA approves voxelotor for sickle cell disease". FDA. Retrieved 9 December 2019.
- ^ Drasar E, Igbineweka N, Vasavda N, Free M, Awogbade M, Allman M, et al. (March 2011). "Blood transfusion usage among adults with sickle cell disease – a single institution experience over ten years". British Journal of Haematology. 152 (6): 766–770. doi:10.1111/j.1365-2141.2010.08451.x. PMID 21275951. S2CID 44562296.
- ^ Gyang E, Yeom K, Hoppe C, Partap S, Jeng M (January 2011). "Effect of chronic red cell transfusion therapy on vasculopathies and silent infarcts in patients with sickle cell disease". American Journal of Hematology. 86 (1): 104–106. doi:10.1002/ajh.21901. PMID 21117059.
- ^ Mirre E, Brousse V, Berteloot L, Lambot-Juhan K, Verlhac S, Boulat C, et al. (March 2010). "Feasibility and efficacy of chronic transfusion for stroke prevention in children with sickle cell disease". European Journal of Haematology. 84 (3): 259–265. doi:10.1111/j.1600-0609.2009.01379.x. PMID 19912310. S2CID 24316310.
- ^ Walters MC, Patience M, Leisenring W, Eckman JR, Scott JP, Mentzer WC, et al. (August 1996). "Bone marrow transplantation for sickle cell disease". The New England Journal of Medicine. 335 (6): 369–376. doi:10.1056/NEJM199608083350601. PMID 8663884. S2CID 25256772.
- ^ Kaiser J (5 December 2020). "CRISPR and another genetic strategy fix cell defects in two common blood disorders". ScienceMag.org. Science. Retrieved 7 December 2020.
... teams report that two strategies for directly fixing malfunctioning blood cells have dramatically improved the health of a handful of people with these genetic diseases.
- ^ Dudi A (17 November 2023). "Unravelito the Quest: Is There a Cure for Sickle Cell Anemia? Introduction to Sickle Cell Anemia". Health aimed.
- ^ Dudi A (17 November 2023). "Unravelito the Quest: Is There a Cure for Sickle Cell Anemia? Introduction to Sickle Cell Anemia". Health aimed. Retrieved 17 November 2023.
- ^ "MHRA authorises world-first gene therapy that aims to cure sickle-cell disease and transfusion-dependent β-thalassemia". Medicines and Healthcare products Regulatory Agency (MHRA) (Press release). 16 November 2023. Archived from the original on 25 November 2023. Retrieved 8 December 2023.
- ^ Kumar V, Abbas AK, Fausto N, Aster J (28 May 2009). Robbins and Cotran Pathologic Basis of Disease (Professional Edition: Expert Consult – Online (Robbins Pathology) ed.). Elsevier Health. pp. Kindle Locations 33530–33531.
- ^ Wierenga KJ, Hambleton IR, Lewis NA (March 2001). "Survival estimates for patients with homozygous sickle-cell disease in Jamaica: a clinic-based population study". Lancet. 357 (9257): 680–683. doi:10.1016/s0140-6736(00)04132-5. PMID 11247552. S2CID 37012133.
- ^ Costa FF, Conran N (2016). Sickle Cell Anemia: From Basic Science to Clinical Practice. Springer. p. 35. ISBN 9783319067131. Retrieved 8 May 2016.
- ^ Prabhakar H, Haywood C, Molokie R (May 2010). "Sickle cell disease in the United States: looking back and forward at 100 years of progress in management and survival". American Journal of Hematology. 85 (5): 346–353. doi:10.1002/ajh.21676. PMID 20425797.
- ^ Medicine National Academies of Sciences, Engineering, and, Division Ha, Practice Bo, Action Co (2020). Addressing Sickle Cell Disease: A Strategic Plan and Blueprint for Action. Washington: National Academies Press. p. 1. ISBN 978-0-309-66960-3.
{{cite book}}: CS1 maint: 다중 이름: 작성자 목록(링크) - ^ Weatherall DJ, Clegg JB (2001). "Inherited haemoglobin disorders: an increasing global health problem". Bulletin of the World Health Organization. 79 (8): 704–712. PMC 2566499. PMID 11545326.
- ^ Roberts I, de Montalembert M (July 2007). "Sickle cell disease as a paradigm of immigration hematology: new challenges for hematologists in Europe". Haematologica. 92 (7): 865–871. doi:10.3324/haematol.11474. PMID 17606434.
- ^ Wellems TE, Hayton K, Fairhurst RM (September 2009). "The impact of malaria parasitism: from corpuscles to communities". The Journal of Clinical Investigation. 119 (9): 2496–2505. doi:10.1172/JCI38307. PMC 2735907. PMID 19729847.
- ^ United States National Library of Medicine. "Sickle cell disease: MedlinePlus Genetics".
- ^ WHO. "Sickle-cell anaemia – Report by the Secretariat" (PDF). Archived from the original (PDF) on 4 January 2011. Retrieved 27 November 2010.
- ^ Aidoo M, Terlouw DJ, Kolczak MS, McElroy PD, ter Kuile FO, Kariuki S, et al. (April 2002). "Protective effects of the sickle cell gene against malaria morbidity and mortality". Lancet. 359 (9314): 1311–1312. doi:10.1016/S0140-6736(02)08273-9. PMID 11965279. S2CID 37952036.
- ^ Tusuubira SK, Nakayinga R, Mwambi B, Odda J, Kiconco S, Komuhangi A (April 2018). "Knowledge, perception and practices towards sickle cell disease: a community survey among adults in Lubaga division, Kampala Uganda". BMC Public Health. 18 (1): 561. doi:10.1186/s12889-018-5496-4. PMC 5924488. PMID 29703184.
- ^ Ndeezi G, Kiyaga C, Hernandez AG, Munube D, Howard TA, Ssewanyana I, et al. (March 2016). "Burden of sickle cell trait and disease in the Uganda Sickle Surveillance Study (US3): a cross-sectional study". The Lancet. Global Health. 4 (3): e195–e200. doi:10.1016/S2214-109X(15)00288-0. PMID 26833239.
- ^ National Heart, Lung and Blood Institute. "Sickle cell anemia, key points". Archived from the original on 2 December 2010. Retrieved 27 November 2010.
- ^ "Data & Statistics on Sickle Cell Disease CDC". Centers for Disease Control and Prevention. 31 August 2016. Retrieved 13 December 2019.
- ^ "September is Sickle Cell Awareness Month". CDC. Archived from the original on 27 September 2010. Retrieved 6 February 2011.
- ^ "Sickle Cell Trait". American Society of Hematology. 8 September 2017. Retrieved 13 December 2019.
- ^ "Disorder Name: Sickle Cell Disease". New Born Screening. Archived from the original on 28 September 2016. Retrieved 11 October 2016.
- ^ "default – Stanford Children's Health". www.stanfordchildrens.org. Retrieved 14 March 2020.
- ^ Edwards QT, Seibert D, Macri C, Covington C, Tilghman J (November 2004). "Assessing ethnicity in preconception counseling: genetics—what nurse practitioners need to know". Journal of the American Academy of Nurse Practitioners. 16 (11): 472–480. doi:10.1111/j.1745-7599.2004.tb00426.x. PMID 15617360. S2CID 7644129.
- ^ "Sickle Cell Patients Endure Discrimination, Poor Care And Shortened Lives". NPR.org. 4 November 2017. Retrieved 12 November 2017.
- ^ Vlachadis N, Vrachnis N (15 November 2022). "A Review of Sickle Cell Disease". JAMA. 328 (19): 1979. doi:10.1001/jama.2022.16732. ISSN 0098-7484. PMID 36378213.
- ^ Bardakdjian J, Wajcman H (September 2004). "[Epidemiology of sickle cell anemia]". La Revue du Praticien (in French). 54 (14): 1531–1533. PMID 15558961.
- ^ Thuret I, Sarles J, Merono F, Suzineau E, Collomb J, Lena-Russo D, et al. (June 2010). "Neonatal screening for sickle cell disease in France: evaluation of the selective process". Journal of Clinical Pathology. 63 (6): 548–551. doi:10.1136/jcp.2009.068874. PMID 20498028. S2CID 22391674.
- ^ "Inheriting sickle cell anaemia – Live Well – NHS Choices". www.nhs.uk. 23 October 2017. Archived from the original on 2 December 2014.
- ^ "Sickle cell anaemia – NHS Choices". www.nhs.uk. 23 October 2017. Archived from the original on 13 December 2011.
- ^ "Who is offered screening and when?". screening.nhs.uk. Archived from the original on 31 December 2014.
- ^ "Give Blood – Resources – Sickle Cell and Blood Donation". Give Blood. Archived from the original on 31 December 2014.
- ^ "Why is Blood from Afro-Caribbean Donors Special?". sicklecellsociety.org. Archived from the original on 30 December 2014.
- ^ Jastaniah W (2011). "Epidemiology of sickle cell disease in Saudi Arabia". Annals of Saudi Medicine. 31 (3): 289–293. doi:10.4103/0256-4947.81540. PMC 3119971. PMID 21623060.
- ^ Memish ZA, Saeedi MY (2011). "Six-year outcome of the national premarital screening and genetic counseling program for sickle cell disease and β-thalassemia in Saudi Arabia". Annals of Saudi Medicine. 31 (3): 229–235. doi:10.4103/0256-4947.81527. PMC 3119961. PMID 21623050.
- ^ Al Arrayed S (1995). "Features of sickle-cell disease in Bahrain". Eastern Mediterranean Health Journal. 1 (1). Archived from the original on 8 October 2016.
- ^ Al Arrayed S, Al Hajeri A (2010). "Public awareness of sickle cell disease in Bahrain". Annals of Saudi Medicine. 30 (4): 284–288. doi:10.4103/0256-4947.65256. PMC 2931779. PMID 20622345.
- ^ "Sickle Cell Anemia". American Society of Hematology. 16 December 2014. Archived from the original on 25 June 2017. Retrieved 1 May 2017.
- ^ Awasthy N, Aggarwal KC, Goyal PC, Prasad MS, Saluja S, Sharma M (2008). "Sickle cell disease: Experience of a tertiary care center in a nonendemic area". Annals of Tropical Medicine and Public Health. 1 (1): 1–4. doi:10.4103/1755-6783.43069.
- ^ "Life with sickle cell – Nation – Nepali Times". Archived from the original on 24 June 2015.
- ^ Asnani MR, McCaw-Binns AM, Reid ME (2011). "Excess risk of maternal death from sickle cell disease in Jamaica: 1998–2007". PLOS ONE. 6 (10): e26281. Bibcode:2011PLoSO...626281A. doi:10.1371/journal.pone.0026281. PMC 3200316. PMID 22039456.
- ^ Lebby R (1846). "Case of absence of the spleen". Southern J of Med Pharmacol. 1: 481–3.
- ^ a b c Ballas SK, Gupta K, Adams-Graves P (November 2012). "Sickle cell pain: a critical reappraisal". Blood. 120 (18): 3647–3656. doi:10.1182/blood-2012-04-383430. PMID 22923496.
- ^ Herrick JB (1 November 1910). "Peculiar elongated and sickle-shaped red blood corpuscles in a case of severe anemia". Archives of Internal Medicine. 6 (5): 179–184. doi:10.1001/archinte.1910.00050330050003.Herrick JB (1 November 1910). "Peculiar elongated and sickle-shaped red blood corpuscles in a case of severe anemia". Archives of Internal Medicine. 6 (5): 179–184. doi:10.1001/archinte.1910.00050330050003.로 전재된.
- ^ Washburn RE (1911). "Peculiar elongated and sickle-shaped red blood corpuscles in a case of severe anemia". The Virginia Medical Semi-Monthly. 15 (21): 490–493.
- ^ "UVa Hospital Celebrating 100 Years". University of Virginia. Archived from the original on 31 January 2015. Retrieved 28 January 2015.
- ^ Mason VR (1922). "Sickle cell anemia". The Journal of the American Medical Association. 79 (16): 1318–1320. doi:10.1001/jama.1922.02640160038012. 재인쇄 대상
- ^ Pauling L, Itano HA (November 1949). "Sickle cell anemia a molecular disease". Science. 110 (2865): 543–548. Bibcode:1949Sci...110..543P. doi:10.1126/science.110.2865.543. PMID 15395398. S2CID 31674765.
- ^ Ingram VM (October 1956). "A specific chemical difference between the globins of normal human and sickle-cell anaemia haemoglobin". Nature. 178 (4537): 792–794. Bibcode:1956Natur.178..792I. doi:10.1038/178792a0. PMID 13369537. S2CID 4167855.
- ^ "Foster, Gloria". Facts On File History Database. Archived from the original on 5 March 2016. Retrieved 25 February 2015.
- ^ Richard-Lenoble D, Toublanc JE, Zinsou RD, Kombila M, Carme B (1980). "[Results of a systematic study of drepanocytosis in 1,500 Gabonese using hemoglobin electrophoresis]" [Results of a systematic study of drepanocytosis in 1,500 Gabonese using hemoglobin electrophoresis]. Bulletin de la Société de Pathologie Exotique et de ses Filiales (in French). 73 (2): 200–206. PMID 7460122.
- ^ Srikanthan S (2023). "Contested Disability: Sickle Cell Disease". Health & Social Work. 48 (3): 209–216. doi:10.1093/hsw/hlad014. PMID 37315205.
- ^ "Social Security Ruling: SSR 2017-3p". U.S. Social Security Administration. Retrieved 15 January 2018.
- ^ "Federal Register, Volume 82 Issue 178 (Friday, September 15, 2017)". U.S. Government Publishing Office (GPO). Retrieved 15 January 2018.
- ^ "Sickle Cell Disease National Heart, Lung, and Blood Institute (NHLBI)". www.nhlbi.nih.gov. Retrieved 4 July 2020.
- ^ Bulgin D, Tanabe P, Jenerette C (August 2018). "Stigma of Sickle Cell Disease: A Systematic Review". Issues in Mental Health Nursing. 39 (8): 675–686. doi:10.1080/01612840.2018.1443530. PMC 6186193. PMID 29652215.
- ^ Washington HA (2006). Medical apartheid : the dark history of medical experimentation on Black Americans from colonial times to the present (1st paperback ed.). New York: Harlem Moon. ISBN 978-0-7679-1547-2. OCLC 192050177.
- ^ a b c d e f g h Tusuubira SK, Naggawa T, Nakamoga V (October 2019). "To Join Or Not To Join? A Case Of Sickle Cell Clubs, Stigma And Discrimination In Secondary Schools In Butambala District, Uganda". Adolescent Health, Medicine and Therapeutics. 10: 145–152. doi:10.2147/AHMT.S223956. PMC 6778728. PMID 31632168.
- ^ a b Tusuubira SK, Nakayinga R, Mwambi B, Odda J, Kiconco S, Komuhangi A (April 2018). "Knowledge, perception and practices towards sickle cell disease: a community survey among adults in Lubaga division, Kampala Uganda". BMC Public Health. 18 (1): 561. doi:10.1186/s12889-018-5496-4. PMC 5924488. PMID 29703184.
- ^ a b c d e f g "Sickle Cell Association of Uganda". Sickle Cell Association of Uganda. Retrieved 7 April 2021.
- ^ Okwi AL, Byarugaba W, Ndugwa CM, Parkes A, Ocaido M, Tumwine JK (September 2009). "Knowledge gaps, attitude and beliefs of the communities about sickle cell disease in Eastern and Western Uganda". East African Medical Journal. 86 (9): 442–449. doi:10.4314/eamj.v86i9.54167. PMID 21644415.
- ^ a b c d e Marsh VM, Kamuya DM, Molyneux SS (August 2011). "'All her children are born that way': gendered experiences of stigma in families affected by sickle cell disorder in rural Kenya". Ethnicity & Health. 16 (4–5): 343–359. doi:10.1080/13557858.2010.541903. PMC 3534410. PMID 21797722.
- ^ "Our Vision and Mission – Uganda Sickle Cell Rescue Foundation". 13 May 2017. Retrieved 6 April 2021.
- ^ a b "Background – Uganda Sickle Cell Rescue Foundation". 13 May 2017. Retrieved 6 April 2021.
- ^ Sehlo MG, Kamfar HZ (April 2015). "Depression and quality of life in children with sickle cell disease: the effect of social support". BMC Psychiatry. 15 (1): 78. doi:10.1186/s12888-015-0461-6. PMC 4394397. PMID 25880537.
- ^ "London Eye: Shouldn't need an improvement programme". Health Service Journal. 27 July 2022. Retrieved 28 September 2022.
- ^ "Better protection and support for people with sickle cell disease". The Voice. October 2022. pp. 16–17. Retrieved 7 October 2022.
- ^ Rylatt A (7 October 2022). "No-one is Listening" (PDF).
- ^ "NHS launches lifesaving sickle cell campaign". 7 October 2022.
- ^ a b Kassim AA, Sharma D (December 2017). "Hematopoietic stem cell transplantation for sickle cell disease: The changing landscape". Hematology/Oncology and Stem Cell Therapy. 10 (4): 259–266. doi:10.1016/j.hemonc.2017.05.008. PMID 28641096.
- ^ Olowoyeye A, Okwundu CI (November 2020). "Gene therapy for sickle cell disease". The Cochrane Database of Systematic Reviews. 2020 (11): CD007652. doi:10.1002/14651858.CD007652.pub7. PMC 8275984. PMID 33251574.
- ^ Pawliuk R, Westerman KA, Fabry ME, Payen E, Tighe R, Bouhassira EE, et al. (December 2001). "Correction of sickle cell disease in transgenic mouse models by gene therapy". Science. 294 (5550): 2368–2371. Bibcode:2001Sci...294.2368P. doi:10.1126/science.1065806. PMID 11743206. S2CID 25607771.
- ^ Wilson JF (18 March 2002). "Murine Gene Therapy Corrects Symptoms of Sickle Cell Disease". The Scientist – Magazine of the Life Sciences. Retrieved 17 December 2014.
- ^ St. Jude Children's Research Hospital (4 December 2008). "Gene Therapy Corrects Sickle Cell Disease In Laboratory Study". ScienceDaily. Archived from the original on 13 December 2014. Retrieved 17 December 2014.
- ^ 겸상세포질환 줄기세포 유전자 치료제 임상시험번호 NCT02247843(ClinicalTrials.gov )
- ^ ' 겸상세포질환 치료용 탯줄 줄기세포 수집 및 보관' 임상시험번호 NCT00012545 ClinicalTrials.gov
- ^ Ribeil JA, Hacein-Bey-Abina S, Payen E, Magnani A, Semeraro M, Magrin E, et al. (March 2017). "Gene Therapy in a Patient with Sickle Cell Disease". The New England Journal of Medicine. 376 (9): 848–855. doi:10.1056/NEJMoa1609677. PMID 28249145. S2CID 5128871.
- ^ Kolata G (27 January 2019). "These Patients Had Sickle-Cell Disease. Experimental Therapies Might Have Cured Them". The New York Times. Retrieved 28 January 2019.
- ^ Dever DP, Bak RO, Reinisch A, Camarena J, Washington G, Nicolas CE, et al. (November 2016). "CRISPR/Cas9 β-globin gene targeting in human haematopoietic stem cells". Nature. 539 (7629): 384–389. Bibcode:2016Natur.539..384D. doi:10.1038/nature20134. PMC 5898607. PMID 27820943.
- ^ "In A 1st, Doctors In U.S. Use CRISPR Tool To Treat Patient With Genetic Disorder". NPR. Retrieved 31 July 2019.
- ^ Zipkin M (6 December 2019). "CRISPR's "magnificent moment" in the clinic". Nature Biotechnology. doi:10.1038/d41587-019-00035-2. PMID 33277639. S2CID 213060203.
- ^ Persaud A, Desine S, Blizinsky K, Bonham VL (August 2019). "A CRISPR focus on attitudes and beliefs toward somatic genome editing from stakeholders within the sickle cell disease community". Genetics in Medicine. 21 (8): 1726–1734. doi:10.1038/s41436-018-0409-6. PMC 6606394. PMID 30581191.
- ^ Walker M (15 January 2018). "Gene Therapy". Sickle Cell Disease News. Retrieved 14 March 2020.
- ^ "MHRA authorises world-first gene therapy that aims to cure sickle-cell disease and transfusion-dependent β-thalassemia". Medicines and Healthcare products Regulatory Agency (MHRA) (Press release). 16 November 2023. Archived from the original on 25 November 2023. Retrieved 8 December 2023.
- ^ Oringanje C, Nemecek E, Oniyangi O (July 2020). "Hematopoietic stem cell transplantation for people with sickle cell disease". The Cochrane Database of Systematic Reviews. 2020 (7): CD007001. doi:10.1002/14651858.CD007001.pub5. PMC 7390490. PMID 32617981.
추가읽기
- Brown RT, ed. (2006). Comprehensive handbook of childhood cancer and sickle cell disease: a biopsychosocial approach. Oxford University Press. ISBN 978-0-19-516985-0.
- Hill SA (2003). Managing Sickle Cell Disease in Low-Income Families. Temple University Press. ISBN 978-1-59213-195-2.
- Serjeant GR, Serjeant BE (2001). Sickle Cell Disease. Oxford University Press. ISBN 978-0-19-263036-0.
- Tapper M (1999). In the blood: sickle cell anemia and the politics of race. University of Pennsylvania Press. ISBN 978-0-8122-3471-8.


