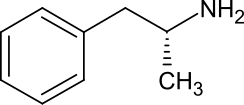
레보암페타민
Levoamphetamine
 | |
| 이름 | |
|---|---|
| 우선 IUPAC 이름 (2R)-1-페닐프로판-2-아민[2] | |
| 기타 이름 l-암페타민, 레밤페타민[1] | |
| 식별자 | |
3D 모델(JSmol) | |
| 2432739 | |
| 체비 | |
| 첸블 | |
| 켐스파이더 | |
| ECHA 정보 카드 | 100.005.320 |
| EC 번호 |
|
| 1125855 | |
PubChem CID | |
| 유니 | |
CompTox 대시보드 (EPA ) | |
| |
| |
| 특성. | |
| C9H13N | |
| 몰 질량 | 135.2062g몰−1 |
| 로그 P | 1.789 |
| 약리학 | |
| 경구(Adderall, Evkeo 및 일반 황산암페타민의[3][4] 일부) | |
| 법적 상태 |
|
달리 명시되지 않은 한 표준 상태(25°C[77°F], 100kPa)의 재료에 대한 데이터가 제공됩니다. | |
레보암페타민은[note 1] 식욕과 피로감퇴와 함께 각성과 집중력을 높이는 것으로 알려진 중추신경계(CNS) 자극제이다.현재 일부 국가에서는 주의력 결핍 과잉 행동 장애(ADHD), 비만 및 기면증 치료를 위해 레보암페타민이 함유된 약물이 표시 및 처방되고 있습니다.
레보암페타민은 암페타민 분자의 공중회전성 입체 이성질체이다.특발성 레보암페타민을 함유한 제제는 더 이상 제조되지 않지만, 레보메탐페타민(레보메탐페타민)은 여전히 시판되고 비강정맥 제거제로 판매된다.
화학
레보암페타민은 암페타민 분자의 공중회전성 입체 이성질체이다.라세미암페타민은 광학 이성질체인 덱스트로암페타민과 [6][7]레보암페타민을 함유하고 있다.
제제
라세미암페타민
최초의 특허받은 암페타민 브랜드인 벤제드린(Benzedrine)은 1934년 미국에서 코막힘 [3]치료용 흡입기로 도입된 암페타민 에난티오머(레보암페타민 및 덱스트로암페타민)의 활성 염기 또는 황산염을 혼합한 것이다.암페타민 에난티오머가 비만, 기면증,[3][4] ADHD를 치료할 수 있다는 것은 나중에 밝혀졌다.덱세드린(Dexedrine)으로 판매되는 덱스트로암페타민(dextroampotic enantiomer, 즉 덱스트로암페타민)의 중추신경계 효과가 더 크기 때문에 벤제드린 브랜드의 처방이 떨어졌고 결국 [8]중단되었다.그러나 2012년, 레이스미크 암페타민 황산염이 Evkeo 브랜드명으로 [4][9]재도입되었습니다.
애드럴
Adderall은 덱스트로암페타민 황산염, 암페타민 황산염, 덱스트로암페타민 사카레이트 및 암페타민(D,L)-아스파르트산염의 4가지 염분을 등량(중량 기준) 함유하는 덱스트로암페타민-레보-암페타민 염기당량 의약품 3.1:1 혼합물이다.이 결과는 76% 덱스트로암페타민 대 24% 레보암페타민 또는3/4 대 1/4 비율.[6][7]
이브키오
Evkeo는 라세미크 암페타민 황산염(레보암페타민 황산염 50%, 덱스트로암페타민 [4]황산염 50%)을 함유한 FDA 승인 의약품입니다.기면증, ADHD, 외인성 [4]비만 치료를 위해 승인되었습니다.경구 분해 정제는 6세에서 17세 [10]사이의 아동과 청소년의 주의력 결핍 과잉행동 장애(ADHD) 치료에 대해 승인되었습니다.
다른이들
현재 암페타민 베이스의 제품이 판매되고 있다.2015년에 출시된 액체 현탁제 형태인 디아나벨 XR은 약 24%의 [11]레보암페타민을 함유하고 있습니다.2016년 경구 분해성 태블릿인 Adzenys XR이 출시되었으며 레보암페타민 [12][13]함량은 25%입니다.
에난티오푸어 레보암페타민 숙신산염은 1952년부터 1955년 사이에 헝가리에서 Cydril이라는 [citation needed]상표명으로 판매되었다.
「 」를 참조해 주세요.
메모들
- ^ 동의어 및 대체 철자에는 (2R)-1-페닐프로판-2-아민(IUPAC명), 레밤페타민(International Nonpropetamine(INN; 국제 비특허명), (R)-암페타민, (-)-암페타민, l-암페타민 [2][5]및 L-암페타민이 포함된다.
레퍼런스
- ^ PubChem의 CID 32893
- ^ a b "L-Amphetamine". PubChem Compound. United States National Library of Medicine – National Center for Biotechnology Information. 30 December 2017. Retrieved 2 January 2018.
- ^ a b c Heal DJ, Smith SL, Gosden J, Nutt DJ (June 2013). "Amphetamine, past and present – a pharmacological and clinical perspective". J. Psychopharmacol. 27 (6): 479–496. doi:10.1177/0269881113482532. PMC 3666194. PMID 23539642.
- ^ a b c d e "Evekeo- amphetamine sulfate tablet". DailyMed. 14 August 2019. Retrieved 7 April 2020.
- ^ "R(-)amphetamine". IUPHAR/BPS Guide to Pharmacology. International Union of Basic and Clinical Pharmacology. Retrieved 2 January 2018.
- ^ a b "Adderall XR- dextroamphetamine sulfate, dextroamphetamine saccharate, amphetamine sulfate and amphetamine aspartate capsule, extended release". DailyMed. 17 July 2019. Retrieved 7 April 2020.
- ^ a b "Adderall- dextroamphetamine saccharate, amphetamine aspartate, dextroamphetamine sulfate, and amphetamine sulfate tablet". DailyMed. 8 November 2019. Retrieved 7 April 2020.
- ^ "Benzedrine: FDA-Approved Drugs". U.S. Food and Drug Administration (FDA). Retrieved 4 September 2015.
- ^ "Evekeo: FDA-Approved Drugs". U.S. Food and Drug Administration (FDA). Retrieved 11 August 2015.
- ^ "Evekeo ODT- amphetamine sulfate tablet, orally disintegrating". DailyMed. 20 February 2020. Retrieved 7 April 2020.
- ^ "Adzenys XR-ODT- amphetamine tablet, orally disintegrating". DailyMed. 22 January 2020. Retrieved 7 April 2020.
Adzenys XR-ODT (amphetamine extended-release orally disintegrating tablet) contains a 3 to 1 ratio of d- to l-amphetamine, a central nervous system stimulant.
- ^ "Adzenys ER- amphetamine suspension, extended release". DailyMed. 21 January 2020. Retrieved 7 April 2020.
외부 링크
- "Amphetamine". Drug Information Portal. U.S. National Library of Medicine.
- "Amphetamine sulfate". Drug Information Portal. U.S. National Library of Medicine.
- "Amphetamine aspartate". Drug Information Portal. U.S. National Library of Medicine.
- "Dextroamphetamine saccharate". Drug Information Portal. U.S. National Library of Medicine.
- "Amphetamine". MedlinePlus.


