PRNP
PRNPPRNP(프리온 단백질)는 CD230(분화 클러스터 230)[5][6][7][8]으로도 알려진 주요 프리온 단백질 PrP(프리온 단백질, 프리온 단백질, 단백질 P)를 코드하는 인간 유전자이다.단백질의 발현은 신경계에서 가장 우세하지만 [9][10][11]몸 전체의 많은 다른 조직들에서 일어난다.
단백질은 여러 개의 동질형태로 존재할 수 있다: 정상적인C PrP 형태, 그리고 질병을 유발하는Sc(scrapie) PrP와 미토콘드리아에 위치한 동질형태와 같은 프로테아제 내성 형태Res.그 misfolded 버전 PrPSc 인지적 장애와 같은 동물들에 신경 변성 질환:양의 스크래피, 광우병(BSE광우병), 고양이의 뇌 뇌증, 전염 밍크 뇌증(TME), 이국적인 유제 뇌병증, 만성을 낭비하고 병(CWD)은 affe의 다양성에 연관되어 있다.cts 자궁경부; 그리고 인간의 경우 크로이츠펠트-야콥병(CJD), 치명적 가족성 불면증(FFI), 게르스트만-슈트뢰슬러-샤인커 증후군(GSS), 쿠루 및 변종 크로이츠펠트-야콥병(vCJD)이다.병든 사람의 섭취에 의한 것으로 생각되는 쿠루와 광우병 감염 소 제품의 인간 섭취에 의한 것으로 생각되는 vCJD 사이에는 유사성이 존재한다.
진
인간 PRNP 유전자는 염기쌍 4,615,068에서 염기쌍 4,630,233까지 팔의 끝(말단)과 위치 13 사이의 염색체 20의 짧은 팔(p)에 위치한다.
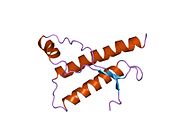
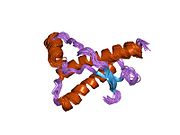
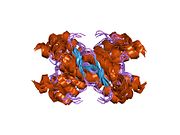
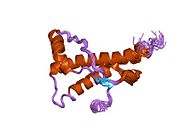
구조.
PrP는 포유류를 통해 고도로 보존되며,[12] 쥐와 같은 실험 동물의 결론 적용에 신빙성을 부여한다.영장류 간의 비교는 아미노산 배열에서 92.9-99.6%의 유사성으로 특히 유사하다.인간 단백질 구조는 세 개의 α-헬리체와 두 가닥 반평행 β-시트, NH2 말단 꼬리 및 짧은 COOH [13]말단 꼬리를 가진 구상 도메인으로 구성된다.COOH 말단 테더 PrP의 세포막 앵커에 있는 글리코포스파티딜이노시톨(GPI)막 앵커로, 이것은 배좌변화의 전달에 불가결함을 증명하는 앵커성분이 결여된 분비물 PrP는 감염성 아이소폼의 [14]영향을 받지 않는다.
PrP의 1차 배열은 번역 후 수정 훨씬 전에 253개의 아미노산이다.아미노말단 및 카르복시말단에서의 신호배열을 번역 후 제거함으로써 208개의 아미노산 성숙한 길이를 얻을 수 있다.인간과 황금햄스터 PrP의 경우, Asn181과 Asn197의 헬리클 2와 3에 2개의 글리코실화 부위가 존재한다.Murine PrP는 Asn180 및 Asn196으로 글리코실화 부위를 가지고 있다.두 번째 나선의 Cys179와 세 번째 나선의 Cys214 사이에는 디술피드 결합이 존재한다(인간C PrP 번호부여).
PrP 메신저 RNA는 PrP 단백질 [15]번역 조절에 관여하는 것으로 생각되는 의사 노트 구조(프리온 의사 노트)를 포함한다.
배위자 결합
스크래피 아이소폼으로의 배위 변환 메커니즘은 이해하기 어려운 리간드 단백질로 추측되지만, 지금까지 그러한 화합물은 확인되지 않았다.그러나 후보자들과 그들의C [16]PRP와의 상호작용에 대한 많은 연구가 발전했다.
구리, 아연, 망간 및 니켈은 옥타레피트 [17]영역에 결합하는 확인된 PrP 리간드이다.배위자 결합은 알 수 없는 효과와 함께 구조 변화를 일으킨다.PrP에서 중금속 결합은 중금속 [17][18]독성으로 인한 산화 응력에 대한 저항성과 관련이 있습니다.
PrPC(표준 세포) Isoform
PrP의 정확한 기능은 아직 알려지지 않았지만, 아마도 주변 환경에서 세포로 이온 구리를 운반하는 것과 관련이 있을 수 있습니다.연구자들은 또한 세포 신호 전달이나 시냅스 [19]형성에 있어 PrP의 역할을 제안했다.PrP는C C 말단 Ser231에서 글리코실포스파티딜이노시톨 앵커에 의해 세포막 외면에 부착된다.
프리온 단백질은 염기서열 PHGGGGGQ와 함께 5개의 옥타펩타이드 반복체를 포함하고 있다(단, 첫 번째 염기서열은 약간 변형된 히스티딘 결핍 염기서열 PQGGGGQ를 가진다).이는 히스티딘 이미다졸 측쇄의 질소 원자와 2차 및 3차 글리신으로부터의 탈양성아미드 니트로겐을 통해 구리 결합 도메인을 생성하는 것으로 생각된다.따라서 구리를 결합하는 능력은 pH에 의존합니다.NMR은 N-terminus에서 구리 결합의 결과로 Configuration이 변경되었음을 나타냅니다.
PrPSc(스크래피) 아이소폼
PrP는Sc PrP의C 입체 동질 형태이지만, 이러한 방향은 신경 [20]조직 내의 작고 단백질 분해효소 저항성 골재에 축적되는 경향이 있다.비정상적인Sc PrP Isoform은 PrP와C 2차 및 3차 구조는 다르지만 1차 배열은 동일하다.원형 이분법은 정상 PrP가C 알파 나선형 42%, 베타 시트 3%인 반면Sc, PrP는 알파 나선형 30%, 베타 [21]시트 43%에 불과하다.그러나, 감염성Sc PrP에서 알파 나선형의 존재에 의문이 제기되었고, 현재 모델은 알파 나선형의 부족을 제안하고 대신 전체 베타 시트 [22]조성으로 대체되었다.이 리폴딩은 PrPSc 동질체를 단백질 분해에 극도로 내성을 갖게 합니다.
PrP의Sc 축적은 신경 퇴화의 병리적인 원인이기 때문에, PrP의 전파는 매우 흥미로운 주제이다.해면상뇌병증의 진행성에 기초하여, 지배적인 가설은 정상적인 PrP로부터의C 변화가 PrP의Sc [23]존재와 상호작용에 의해 발생한다고 가정한다.이에 대한 강력한 지지는 PRNP 녹아웃 [24]생쥐가 PrP의Sc 도입에 저항하는 연구로부터 얻어진다.형상 변환 가설을 널리 수용함에도 불구하고, 일부 연구는 PrP와 세포독성 [25]사이의 직접적인Sc 연관성에 대한 주장을 완화한다.
부위 136, 154, 171에서의 다형은 난소 스크래피에 대한 다양한 감수성과 관련되어 있다.(이러한 난소 사이트는 인간 사이트 133, 151, 168에 해당합니다.)PrP-VRQ 형식과 PrP-ARQ 형식의 다형성은 감수성 증가와 관련이 있으며, PrP-ARR은 저항성과 관련이 있습니다.영국의 National Scrapie Plan은 내성 대립 유전자의 [26]빈도를 증가시킴으로써 이러한 스크래피 다형성을 배양하는 것을 목표로 하고 있다.그러나 PrP-ARR 다형은 비정형 스크래피에 취약하기 때문에 불충분할 수 있다.
기능.
신경계
신경변성 질환과의 강한 연관성은 뇌의 PrP 기능에 대해 많은 의문을 제기한다.일반적인 접근법은 결핍과 [27]차이를 조사하기 위해 PrP-knockout과 트랜스제닉 마우스를 사용하는 것이다.초기 시도에서는 일련의 테스트를 받았을 때 생리학적 또는 발달적 차이를 보이지 않는 두 종류의 PrP-null 생쥐가 생성되었다.그러나 최근 변종들은 상당한 인지 [16]이상을 보이고 있다.
늘 마우스가 노화됨에 따라 소뇌의 퍼킨제 세포가 현저하게 손실되면 운동 협응이 저하됩니다.그러나 이 효과는 PrP의 부재로 인한 직접적인 결과가 아니라 도플 유전자 [28]발현 증가에서 발생한다.관찰된 다른 차이점으로는 스트레스 반응 감소와 새로운 [29][30]환경의 탐색 증가가 있다.
null [11]마우스에서는 일주기 리듬이 변화합니다.치명적인 가족성 불면증은 코돈 178에서 PRNP의 포인트 돌연변이의 결과로 생각되며, 이는 수면-각성 [31]주기에 PrP의 관여를 입증한다.또한 주간-야간에 [32]정기적으로 순환하는 PrP mRNA에서 일주기 조절이 입증되었다.
기억
null 마우스는 정상적인 학습 능력과 단기 기억력을 보이는 반면, 장기 기억력 통합 결손이 입증되었다.그러나 운동실조증과 마찬가지로 이것은 도플 유전자 발현에 기인한다.그러나, 주로 해마 기능인 공간 학습은 null 마우스에서는 감소하며, 뉴런에서 PrP의 회복으로 회복될 수 있다. 이는 PrP 기능의 상실이 [33][34]원인임을 나타낸다.해마 PrP와 라미닌(LN)의 상호작용은 기억 처리에 중추적이며 키나아제 PKA와 ERK1/[35][36]2에 의해 조절될 수 있습니다.
기억 형성에 있어 PrP의 역할에 대한 추가 지원은 여러 모집단 연구에서 도출된다.건강한 젊은 사람들을 대상으로 한 테스트에서는 [37]VV에 비해 MM 또는 MV 유전자형과 관련된 장기 기억 능력이 향상되었습니다.단일 발린 치환으로 다운증후군 환자들은 초기 인지력 [38]저하와 관련이 있다.PRNP의 몇 가지 다형성은 노인의 인지장애와 초기 인지력 [39][40][41]저하와 관련이 있다.이러한 모든 연구는 코돈 129의 차이를 조사했으며, 특히 기억과 관련하여 PrP의 전체 기능에서 코돈 129의 중요성을 나타냈다.
뉴런과 시냅스
PrP는 시냅스 전 및 시냅스 후 구획에 모두 존재하며 시냅스 전 [42]부분에서 가장 농도가 높다.이것과 PrP의 일련의 행동적 영향을 고려하면, 신경세포의 기능과 상호작용은 특히 흥미롭다.구리배위자에 기초하여 하나의 제안된 함수는 시냅스 균열을 위한 구리 완충제로서 PrP를 주조한다.이 역할에서 단백질은 구리 항상성 메커니즘, 칼슘 조절기 또는 구리 또는 산화 [43]스트레스에 대한 센서 역할을 할 수 있습니다.PrP 기능의 상실은 장기전위화(LTP)와 관련되어 있습니다.이 효과는 긍정적일 수도 있고 부정적일 수도 있으며 신경 흥분성과 해마의 시냅스 [44][45]전달의 변화 때문이다.
일부 연구에 따르면 신경 발달, 분화 및 신경암 발육에 PrP가 관여하는 것으로 나타났다.PrP 활성화 신호 전달 경로는 축삭 및 일련의 [25][46]키나아제와의 수지상 발육과 관련이 있다.
면역 체계
비록 대부분의 관심이 신경계에서 PrP의 존재에 집중되어 있지만, 그것은 또한 면역 체계 조직에도 풍부합니다.PrP 면역세포는 조혈모세포, 성숙한 림프구 및 골수구획, 특정 림프구를 포함하며, 또한 자연살해세포, 혈소판, 단구에서도 검출되었다.T세포 활성화는 반드시 필요한 것은 아니지만 PrP의 강력한 상향 조절을 수반한다.프리온에 의한 신경변성 질환인 전염성 해면상뇌병증(TSE)에 대한 면역반응이 부족한 것은 [47]PrP에 대한Sc 내성 때문일 수 있다.
근육, 간, 뇌하수체
PrP-null 마우스는 운동 활동이 감소된 것을 보여주는 강제 수영 테스트를 받았을 때 근육 생리학에서 역할에 대한 단서를 제공한다.PRNP가 과다 발현된 노화 생쥐는 근육 조직의 현저한 저하를 보였다.
존재하지만 간에는 매우 낮은 수준의 PrP가 존재하며 간 섬유화와 관련이 있을 수 있습니다.뇌하수체 내 존재는 양서류의 신경내크린 기능에 영향을 미치는 것으로 나타났지만 포유류의 뇌하수체 [16]PrP에 대해서는 알려진 바가 거의 없다.
무선 전화의
세포 주기 동안 PrP의 다양한 발현으로 인해 개발 관여에 대한 추측이 제기되고 있다.세포 증식, 분화, 죽음, [16]생존에 대한 다양한 연구가 수행되었다.PrP의 체결은 신호 전달 활성화와 연계되어 있습니다.
신호 전달 경로의 변조는 항체 및 리간드 결합(홉/STI1 또는 구리)[16]과의 가교에서 입증되었다.상호작용, 효과 및 분포의 다양성을 고려할 때, PrP는 신호 경로에서 기능하는 동적 표면 단백질로 제안되었다.단백질을 따라 있는 특정 부위는 다른 단백질, 생체 분자, 그리고 금속과 결합합니다.이러한 인터페이스를 통해 특정 셀 세트가 발현 수준 및 주변 미세 환경에 따라 통신할 수 있습니다.지질 이중층 내 GPI 뗏목에 고정하는 것은 세포외 비계 [16]기능의 주장을 뒷받침한다.
PrP가 잘못 접혀서 발생하는 질병
PRNP 유전자의 20개 이상의 돌연변이가 유전 프리온 질환을 가진 사람들에게서 확인되었으며,[48][49] 여기에는 다음이 포함된다.
- 크로이츠펠트-야콥병 – 발린이 아미노산 129에 존재하는 동안 글루탐산-200은 리신으로 대체된다.
- 게르스트만-슈트뢰슬러-샤인커 증후군 – 보통 코돈 102가 프롤린에서 류신으로의[50] 변화
- 치명적인 가족성 불면증 – 메티오닌이 아미노산[51] 129에 존재하는 동안 아스파라긴으로 아스파라긴을 대체한다.
PrP를C PrP로Sc 변환하는 것은 치명적인 신경변성 전염성 해면상뇌병(TSE)의 전염 메커니즘이다.이것은 유전적 요인, 외부 소스로부터의 감염 또는 알려지지 않은 이유로 인해 자연적으로 발생할 수 있습니다.PrP의Sc 축적은 신경 변성의 진행에 해당하며 제안된 원인이다.일부 PRNP 돌연변이는 프리온 단백질에서 단일 아미노산(단백질의 구성 블록)의 변화를 초래합니다.다른 사람들은 단백질에 추가적인 아미노산을 넣거나 비정상적으로 짧은 단백질을 만든다.이러한 돌연변이는 세포가 비정상적인 구조를 가진 프리온 단백질을 만들게 한다.비정상적인 단백질Sc PrP는 뇌에 축적되어 신경세포를 파괴하고 프리온 질환의 정신적, 행동적 특징을 이끈다.
PRNP 유전자의 몇 가지 다른 변화들은 프리온 질환을 일으키지 않지만 이러한 질병이 발병할 위험성에 영향을 미치거나 장애의 과정을 바꿀 수 있다.PRNP 변종인 G127V를 코드하는 대립 유전자가 쿠루에 [52]내성을 제공합니다.
또한 일부 프리온 질환은 PrP의Sc [53]외부 소스로부터 전염될 수 있다.
- 스크래피 – 사람에게 전염되지 않는 양의 치명적인 신경 변성 질환
- 소 해면상뇌증(광우병) – 감염된 소의 뇌, 척추 또는 소화관 조직을 섭취함으로써 사람에게 전염될 수 있는 소의 치명적인 신경변성 질환
- Kuru – TSE는 장례를 치르는 식인 풍습에 의해 전염됩니다.일반적으로, 영향을 받은 가족에게는 죽은 가족을 섭취할 때 의식에 따라 중추신경계의 일부가 주어졌다.
알츠하이머병
PrPC 단백질은 수용성 아밀로이드 베타(Aβ) 올리고머의 여러 세포 수용체 중 하나이며, 알츠하이머병을 일으키는 [54]데 규범적으로 관련되어 있다.이러한 올리고머는 더 작은 Aβ 플라크로 구성되어 있으며,[54] 뉴런의 무결성을 가장 손상시킨다.직접적으로 신경독성을 유도하는 용해성 Aβ 올리고머의 정확한 메커니즘은 알려지지 않았으며, 동물에서 PRNP의 실험적인 결실은 여러 가지 상반된 발견을 낳았다.Aβ 올리고머를 알츠하이머 마우스 모델의 뇌실에 주입했을 때, PRNP 결실은 보호를 제공하지 않았고, 오직C 항PrP 항체만이 장기 기억력과 공간 학습 [55][56]결함을 막았다.이는 PRNP와 Aβ 올리고머 매개 신경변성 또는 부위 특이적 관계 유의성 사이의 불평등한 관계를 시사한다.해마에 Aβ 올리고머를 직접 주입한 경우, PRNP 녹아웃 마우스는 신경사망률과 시냅스 가소성 [54][56]측정과 관련하여 대조군과 구별할 수 없는 것으로 밝혀졌다.또한 Aβ-올리고머는 시냅스 후 밀도로 PrP에C 결합하여 Fyn 효소를 통해 NMDA 수용체를 간접적으로 과활성화하여 흥분독성을 [55]초래하는 것으로 밝혀졌다.수용성 Aβ 올리고머는 또한 수상돌기에서 PrP와C 결합하여 Fyn과 복합체를 형성하고 알츠하이머에 [55]관여하는 또 다른 단백질인 타우를 과도하게 활성화시킨다.유전자 FYN 코드로서 FYN 녹아웃 마우스는 Aβ 올리고머 [55]주입 시 흥분독성 이벤트나 수지상 척추수축을 나타내지 않는다.포유동물에서 PRNP의 완전한 기능적 중요성은 명확하지 않다. PRNP 결실은 명백한 [54]위해 없이 축산업에 의해 예방적으로 구현되었기 때문이다.생쥐에서는 hAPPJ20 생쥐와 TgCRND8 생쥐가 간질 활성이 약간 증가하여 알츠하이머 생존율을 [54]검사할 때 상반된 결과에 기여하기 때문에 동일한 결손이 알츠하이머 생쥐 라인 간에 표현형으로 변화한다.주목할 점은 알츠하이머의 다른 두 유전자 변형 모델인 APPSwe와 SEN1dE9 모두에서 PRNP의 결실은 이러한 [54]동물들의 하위 집합에서 볼 수 있는 간질 유발 사망 표현형을 약화시켰다 뇌전증종합적으로 볼 때, 최근의 증거는 PRNP가 수용성 Aβ-올리고머의 신경독성 효과와 알츠하이머의 [54][55][56]응급 질환 상태를 전도하는 데 중요할 수 있다는 것을 시사한다.
사람의 경우, PRNP(rs179990)의 코돈 129에 있는 메티오닌/발린 다형성은 알츠하이머병과 [57]가장 밀접하게 관련되어 있다.변종V형알레르담체(VV, MV)는 메티오닌호모 접합체(MM)에 비해 알츠하이머 발병위험이 13% 감소하였으나 변종V형알레르담체의 보호효과는 백인에게만 나타났다.V 대립 유전자 보균자의 위험 감소는 말기 알츠하이머병( 65 65년)[57]에만 국한된다.PRNP는 알츠하이머병과 산발성 크로이츠펠트-야콥병의 [54]위험을 복합하기 위해 알츠하이머병과 관련된 두 개의 다른 유전자, PSEN1과 APOE의 다형성과 기능적으로 상호작용할 수 있다.PRNP의 코돈 102에 대한 점 돌연변이는 적어도 부분적으로 동일한 패밀리 내에서 3명의 개별 환자의 비정형 전두엽 치매에 기여했으며, 게스트만-슈트뢰슬러-셰인커 [54][58]증후군에 대한 새로운 표현형을 제안했다.같은 연구는 치매의 다양한 형태가 차별적인 [58]진단이 어려울 수 있기 때문에 애매하게 진단된 치매의 경우 PRNP를 시퀀싱할 것을 제안했다.
상호 작용
PrP와 코치페론 홉(Hsp70/Hsp90 구성 단백질, STI1(스트레스 유도 단백질 1)[59][60]이라고도 함) 사이에는 강한 상호작용이 존재합니다.
레퍼런스
- ^ a b c GRCh38: 앙상블 릴리즈 89: ENSG00000171867 - 앙상블, 2017년 5월
- ^ a b c GRCm38: 앙상블 릴리즈 89: ENSMUSG000079037 - 앙상블, 2017년 5월
- ^ "Human PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ "Mouse PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ Kretzschmar HA, Stowring LE, Westaway D, Stubblebine WH, Prusiner SB, Dearmond SJ (August 1986). "Molecular cloning of a human prion protein cDNA". DNA. 5 (4): 315–24. doi:10.1089/dna.1986.5.315. PMID 3755672.
- ^ Sparkes RS, Simon M, Cohn VH, Fournier RE, Lem J, Klisak I, Heinzmann C, Blatt C, Lucero M, Mohandas T (October 1986). "Assignment of the human and mouse prion protein genes to homologous chromosomes". Proc. Natl. Acad. Sci. U.S.A. 83 (19): 7358–62. Bibcode:1986PNAS...83.7358S. doi:10.1073/pnas.83.19.7358. PMC 386716. PMID 3094007.
- ^ Liao YC, Lebo RV, Clawson GA, Smuckler EA (July 1986). "Human prion protein cDNA: molecular cloning, chromosomal mapping, and biological implications". Science. 233 (4761): 364–7. Bibcode:1986Sci...233..364L. doi:10.1126/science.3014653. PMID 3014653.
- ^ Robakis NK, Devine-Gage EA, Jenkins EC, Kascsak RJ, Brown WT, Krawczun MS, Silverman WP (October 1986). "Localization of a human gene homologous to the PrP gene on the p arm of chromosome 20 and detection of PrP-related antigens in normal human brain". Biochem. Biophys. Res. Commun. 140 (2): 758–65. doi:10.1016/0006-291X(86)90796-5. PMID 2877664.
- ^ Prusiner SB (2001). "Shattuck lecture--neurodegenerative diseases and prions". N Engl J Med. 344 (20): 1516–26. doi:10.1056/NEJM200105173442006. PMID 11357156.
- ^ Weissmann C (2004). "The state of the prion". Nat Rev Microbiol. 2 (11): 861–71. doi:10.1038/nrmicro1025. PMID 15494743. S2CID 20992257.
- ^ a b Zomosa-Signoret V, Arnaud JD, Fontes P, Alvarez-Martinez MT, Liautard JP (2008). "Physiological role of the cellular prion protein" (PDF). Vet. Res. 39 (4): 9. doi:10.1051/vetres:2007048. PMID 18073096.
- ^ Damberger FF, Christen B, Pérez DR, Hornemann S, Wüthrich K (October 2011). "Cellular prion protein conformation and function". Proc. Natl. Acad. Sci. U.S.A. 108 (42): 17308–13. Bibcode:2011PNAS..10817308D. doi:10.1073/pnas.1106325108. PMC 3198368. PMID 21987789.
- ^ Schätzl HM, Da Costa M, Taylor L, Cohen FE, Prusiner SB (January 1995). "Prion protein gene variation among primates". J. Mol. Biol. 245 (4): 362–74. doi:10.1006/jmbi.1994.0030. PMID 7837269.
- ^ Chesebro B, Trifilo M, Race R, Meade-White K, Teng C, LaCasse R, Raymond L, Favara C, Baron G, Priola S, Caughey B, Masliah E, Oldstone M (June 2005). "Anchorless prion protein results in infectious amyloid disease without clinical scrapie". Science. 308 (5727): 1435–9. Bibcode:2005Sci...308.1435C. CiteSeerX 10.1.1.401.781. doi:10.1126/science.1110837. PMID 15933194. S2CID 10064966.
- ^ Barrette I, Poisson G, Gendron P, Major F (2001). "Pseudoknots in prion protein mRNAs confirmed by comparative sequence analysis and pattern searching". Nucleic Acids Res. 29 (3): 753–758. doi:10.1093/nar/29.3.753. PMC 30388. PMID 11160898.
- ^ a b c d e f Linden R, Martins VR, Prado MA, Cammarota M, Izquierdo I, Brentani RR (April 2008). "Physiology of the prion protein". Physiol. Rev. 88 (2): 673–728. doi:10.1152/physrev.00007.2007. PMID 18391177.
- ^ a b Prčina M, Kontseková E, Novák M (2015). "Prion protein prevents heavy metals overloading of cells and thus protects them against their toxicity". Acta Virol. 59 (2): 179–84. doi:10.4149/av_2015_02_179. PMID 26104335.
- ^ Brown DR, Clive C, Haswell SJ (January 2001). "Antioxidant activity related to copper binding of native prion protein". J. Neurochem. 76 (1): 69–76. doi:10.1046/j.1471-4159.2001.00009.x. PMID 11145979. S2CID 45647133.
- ^ Kanaani J, Prusiner SB, Diacovo J, Baekkeskov S, Legname G (December 2005). "Recombinant prion protein induces rapid polarization and development of synapses in embryonic rat hippocampal neurons in vitro". Journal of Neurochemistry. 95 (5): 1373–86. doi:10.1111/j.1471-4159.2005.03469.x. PMID 16313516. S2CID 24329326.
- ^ Ross CA, Poirier MA (July 2004). "Protein aggregation and neurodegenerative disease". Nat. Med. 10 Suppl (7): S10–7. doi:10.1038/nm1066. PMID 15272267. S2CID 205383483.
- ^ Pan KM, Baldwin M, Nguyen J, Gasset M, Serban A, Groth D, Mehlhorn I, Huang Z, Fletterick RJ, Cohen FE (December 1993). "Conversion of alpha-helices into beta-sheets features in the formation of the scrapie prion proteins". Proc. Natl. Acad. Sci. U.S.A. 90 (23): 10962–6. Bibcode:1993PNAS...9010962P. doi:10.1073/pnas.90.23.10962. PMC 47901. PMID 7902575.
- ^ Baskakov, Ilia V.; Caughey, Byron; Requena, Jesús R.; Sevillano, Alejandro M.; Surewicz, Witold K.; Wille, Holger (2019-01-01). "The prion 2018 round tables (I): the structure of PrPSc". Prion. 13 (1): 46–52. doi:10.1080/19336896.2019.1569450. ISSN 1933-6896. PMC 6422368. PMID 30646817.
- ^ Sandberg MK, Al-Doujaily H, Sharps B, Clarke AR, Collinge J (February 2011). "Prion propagation and toxicity in vivo occur in two distinct mechanistic phases". Nature. 470 (7335): 540–2. Bibcode:2011Natur.470..540S. doi:10.1038/nature09768. PMID 21350487. S2CID 4399936.
- ^ Büeler H, Aguzzi A, Sailer A, Greiner RA, Autenried P, Aguet M, Weissmann C (July 1993). "Mice devoid of PrP are resistant to scrapie". Cell. 73 (7): 1339–47. doi:10.1016/0092-8674(93)90360-3. PMID 8100741.
- ^ a b Aguzzi A, Baumann F, Bremer J (2008). "The prion's elusive reason for being". Annu. Rev. Neurosci. 31: 439–77. doi:10.1146/annurev.neuro.31.060407.125620. PMID 18558863.
- ^ Atkinson M (October 2001). "National scrapie plan". The Veterinary Record. 149 (15): 462. PMID 11688751.
- ^ Weissmann C, Flechsig E (2003). "PrP knock-out and PrP transgenic mice in prion research". Br. Med. Bull. 66: 43–60. doi:10.1093/bmb/66.1.43. PMID 14522848.
- ^ Katamine S, Nishida N, Sugimoto T, Noda T, Sakaguchi S, Shigematsu K, Kataoka Y, Nakatani A, Hasegawa S, Moriuchi R, Miyamoto T (December 1998). "Impaired motor coordination in mice lacking prion protein". Cell. Mol. Neurobiol. 18 (6): 731–42. doi:10.1023/A:1020234321879. PMID 9876879. S2CID 23409873.
- ^ Nico PB, de-Paris F, Vinadé ER, Amaral OB, Rockenbach I, Soares BL, Guarnieri R, Wichert-Ana L, Calvo F, Walz R, Izquierdo I, Sakamoto AC, Brentani R, Martins VR, Bianchin MM (July 2005). "Altered behavioural response to acute stress in mice lacking cellular prion protein". Behav. Brain Res. 162 (2): 173–81. doi:10.1016/j.bbr.2005.02.003. PMID 15970215. S2CID 37511702.
- ^ Roesler R, Walz R, Quevedo J, de-Paris F, Zanata SM, Graner E, Izquierdo I, Martins VR, Brentani RR (August 1999). "Normal inhibitory avoidance learning and anxiety, but increased locomotor activity in mice devoid of PrP(C)". Brain Res. Mol. Brain Res. 71 (2): 349–53. doi:10.1016/S0169-328X(99)00193-X. PMID 10521590.
- ^ Medori R, Tritschler HJ, LeBlanc A, Villare F, Manetto V, Chen HY, Xue R, Leal S, Montagna P, Cortelli P (February 1992). "Fatal familial insomnia, a prion disease with a mutation at codon 178 of the prion protein gene". N. Engl. J. Med. 326 (7): 444–9. doi:10.1056/NEJM199202133260704. PMC 6151859. PMID 1346338.
- ^ Cagampang FR, Whatley SA, Mitchell AL, Powell JF, Campbell IC, Coen CW (1999). "Circadian regulation of prion protein messenger RNA in the rat forebrain: a widespread and synchronous rhythm". Neuroscience. 91 (4): 1201–4. doi:10.1016/S0306-4522(99)00092-5. PMID 10391428. S2CID 42892475.
- ^ Criado JR, Sánchez-Alavez M, Conti B, Giacchino JL, Wills DN, Henriksen SJ, Race R, Manson JC, Chesebro B, Oldstone MB (2005). "Mice devoid of prion protein have cognitive deficits that are rescued by reconstitution of PrP in neurons". Neurobiol. Dis. 19 (1–2): 255–65. doi:10.1016/j.nbd.2005.01.001. PMID 15837581. S2CID 2618712.
- ^ Balducci C, Beeg M, Stravalaci M, Bastone A, Sclip A, Biasini E, Tapella L, Colombo L, Manzoni C, Borsello T, Chiesa R, Gobbi M, Salmona M, Forloni G (February 2010). "Synthetic amyloid-beta oligomers impair long-term memory independently of cellular prion protein". Proc. Natl. Acad. Sci. U.S.A. 107 (5): 2295–300. Bibcode:2010PNAS..107.2295B. doi:10.1073/pnas.0911829107. PMC 2836680. PMID 20133875.
- ^ Coitinho AS, Freitas AR, Lopes MH, Hajj GN, Roesler R, Walz R, Rossato JI, Cammarota M, Izquierdo I, Martins VR, Brentani RR (December 2006). "The interaction between prion protein and laminin modulates memory consolidation". Eur. J. Neurosci. 24 (11): 3255–64. doi:10.1111/j.1460-9568.2006.05156.x. PMID 17156386. S2CID 17164351.
- ^ Shorter J, Lindquist S (June 2005). "Prions as adaptive conduits of memory and inheritance". Nat. Rev. Genet. 6 (6): 435–50. doi:10.1038/nrg1616. PMID 15931169. S2CID 5575951.
- ^ Papassotiropoulos A, Wollmer MA, Aguzzi A, Hock C, Nitsch RM, de Quervain DJ (August 2005). "The prion gene is associated with human long-term memory" (PDF). Hum. Mol. Genet. 14 (15): 2241–6. doi:10.1093/hmg/ddi228. PMID 15987701.
- ^ Del Bo R, Comi GP, Giorda R, Crimi M, Locatelli F, Martinelli-Boneschi F, Pozzoli U, Castelli E, Bresolin N, Scarlato G (June 2003). "The 129 codon polymorphism of the prion protein gene influences earlier cognitive performance in Down syndrome subjects". J. Neurol. 250 (6): 688–92. doi:10.1007/s00415-003-1057-5. PMID 12796830. S2CID 21049364.
- ^ Berr C, Richard F, Dufouil C, Amant C, Alperovitch A, Amouyel P (September 1998). "Polymorphism of the prion protein is associated with cognitive impairment in the elderly: the EVA study". Neurology. 51 (3): 734–7. doi:10.1212/wnl.51.3.734. PMID 9748018. S2CID 11352163.
- ^ Croes EA, Dermaut B, Houwing-Duistermaat JJ, Van den Broeck M, Cruts M, Breteler MM, Hofman A, van Broeckhoven C, van Duijn CM (August 2003). "Early cognitive decline is associated with prion protein codon 129 polymorphism". Ann. Neurol. 54 (2): 275–6. doi:10.1002/ana.10658. PMID 12891686. S2CID 31538672.
- ^ Kachiwala SJ, Harris SE, Wright AF, Hayward C, Starr JM, Whalley LJ, Deary IJ (September 2005). "Genetic influences on oxidative stress and their association with normal cognitive ageing". Neurosci. Lett. 386 (2): 116–20. doi:10.1016/j.neulet.2005.05.067. PMID 16023289. S2CID 23642220.
- ^ Herms J, Tings T, Gall S, Madlung A, Giese A, Siebert H, Schürmann P, Windl O, Brose N, Kretzschmar H (October 1999). "Evidence of presynaptic location and function of the prion protein". J. Neurosci. 19 (20): 8866–75. doi:10.1523/JNEUROSCI.19-20-08866.1999. PMC 6782778. PMID 10516306.
- ^ Kardos J, Kovács I, Hajós F, Kálmán M, Simonyi M (August 1989). "Nerve endings from rat brain tissue release copper upon depolarization. A possible role in regulating neuronal excitability". Neurosci. Lett. 103 (2): 139–44. doi:10.1016/0304-3940(89)90565-X. PMID 2549468. S2CID 24917999.
- ^ Bailey CH, Kandel ER, Si K (September 2004). "The persistence of long-term memory: a molecular approach to self-sustaining changes in learning-induced synaptic growth". Neuron. 44 (1): 49–57. doi:10.1016/j.neuron.2004.09.017. PMID 15450159. S2CID 2637074.
- ^ Barco A, Bailey CH, Kandel ER (June 2006). "Common molecular mechanisms in explicit and implicit memory". J. Neurochem. 97 (6): 1520–33. doi:10.1111/j.1471-4159.2006.03870.x. PMID 16805766. S2CID 26307975.
- ^ Laurén J, Gimbel DA, Nygaard HB, Gilbert JW, Strittmatter SM (February 2009). "Cellular prion protein mediates impairment of synaptic plasticity by amyloid-beta oligomers". Nature. 457 (7233): 1128–32. Bibcode:2009Natur.457.1128L. doi:10.1038/nature07761. PMC 2748841. PMID 19242475.
- ^ Isaacs JD, Jackson GS, Altmann DM (October 2006). "The role of the cellular prion protein in the immune system". Clin. Exp. Immunol. 146 (1): 1–8. doi:10.1111/j.1365-2249.2006.03194.x. PMC 1809729. PMID 16968391.
- ^ Castilla J, Hetz C, Soto C (2004). "Molecular mechanisms of neurotoxicity of pathological prion protein". Curr Mol Med. 4 (4): 397–403. doi:10.2174/1566524043360654. PMID 15354870.
- ^ Kovács GG, Trabattoni G, Hainfellner JA, Ironside JW, Knight RS, Budka H (2002). "Mutations of the prion protein gene phenotypic spectrum". J Neurol. 249 (11): 1567–82. doi:10.1007/s00415-002-0896-9. PMID 12420099. S2CID 22688729.
- ^ Collins S, McLean CA, Masters CL (2001). "Gerstmann-Straussler-Scheinker syndrome, fatal familial insomnia, and kuru: a review of these less common human transmissible spongiform encephalopathies". J Clin Neurosci. 8 (5): 387–97. doi:10.1054/jocn.2001.0919. PMID 11535002. S2CID 31976428.
- ^ Montagna P, Gambetti P, Cortelli P, Lugaresi E (2003). "Familial and sporadic fatal insomnia". Lancet Neurol. 2 (3): 167–76. doi:10.1016/S1474-4422(03)00323-5. PMID 12849238. S2CID 20822956.
- ^ Mead S, Whitfield J, Poulter M, Shah P, Uphill J, Campbell T, Al-Dujaily H, Hummerich H, Beck J, Mein CA, Verzilli C, Whittaker J, Alpers MP, Collinge J (2009). "A Novel Protective Prion Protein Variant that Colocalizes with Kuru Exposure" (PDF). The New England Journal of Medicine. 361 (21): 2056–2065. doi:10.1056/NEJMoa0809716. PMID 19923577.
- "Brain disease 'resistance gene' evolves in Papua New Guinea community; could offer insights into CJD". ScienceDaily (Press release). November 21, 2009.
- ^ Hwang D, Lee IY, Yoo H, Gehlenborg N, Cho JH, Petritis B, Baxter D, Pitstick R, Young R, Spicer D, Price ND, Hohmann JG, Dearmond SJ, Carlson GA, Hood LE (2009). "A systems approach to prion disease". Mol. Syst. Biol. 5 (1): 252. doi:10.1038/msb.2009.10. PMC 2671916. PMID 19308092.
- ^ a b c d e f g h i Laurén J (2014). "Cellular prion protein as a therapeutic target in Alzheimer's disease". Journal of Alzheimer's Disease. 38 (2): 227–244. doi:10.3233/JAD-130950. PMID 23948943.
- ^ a b c d e Zhou J, Liu B (May 2013). "Alzheimer's disease and prion protein". Intractable & Rare Diseases Research. 2 (2): 35–44. doi:10.5582/irdr.2013.v2.2.35. PMC 4204584. PMID 25343100.
- ^ a b c Laurén J, Gimbel DA, Nygaard HB, Gilbert JW, Strittmatter SM (Feb 2009). "Cellular prion protein mediates impairment of synaptic plasticity by amyloid-beta oligomers". Nature. 457 (7233): 1128–1132. Bibcode:2009Natur.457.1128L. doi:10.1038/nature07761. PMC 2748841. PMID 19242475.
- ^ a b He J, Li X, Yang J, Huang J, Fu X, Zhang Y, Fan H (Mar 2013). "The association between the methionine/valine (M/V) polymorphism (rs1799990) in the PRNP gene and the risk of Alzheimer disease: an update by meta-analysis". Journal of the Neurological Sciences. 326 (1–2): 89–95. doi:10.1016/j.jns.2013.01.020. PMID 23399523. S2CID 31070331.
- ^ a b Giovagnoli AR, Di Fede G, Aresi A, Reati F, Rossi G, Tagliavini F (December 2008). "Atypical frontotemporal dementia as a new clinical phenotype of Gerstmann-Straussler-Scheinker disease with the PrP-P102L mutation. Description of a previously unreported Italian family". Neurological Sciences. 29 (6): 405–10. doi:10.1007/s10072-008-1025-z. PMID 19030774. S2CID 20553167.
- ^ Americo TA, Chiarini LB, Linden R (June 2007). "Signaling induced by hop/STI-1 depends on endocytosis". Biochem. Biophys. Res. Commun. 358 (2): 620–5. doi:10.1016/j.bbrc.2007.04.202. PMID 17498662.
- ^ Zanata SM, Lopes MH, Mercadante AF, Hajj GN, Chiarini LB, Nomizo R, Freitas AR, Cabral AL, Lee KS, Juliano MA, de Oliveira E, Jachieri SG, Burlingame A, Huang L, Linden R, Brentani RR, Martins VR (Jul 2002). "Stress-inducible protein 1 is a cell surface ligand for cellular prion that triggers neuroprotection". EMBO J. 21 (13): 3307–16. doi:10.1093/emboj/cdf325. PMC 125391. PMID 12093732.
외부 링크
- GeneCard의 PRNP(PrP) 유전자
- PRNP+단백질+미국국립의학도서관 의학주제목(MeSH)의 인간
- Susan Lindquist의 세미나: "프리온 생물학의 놀라운 세계"