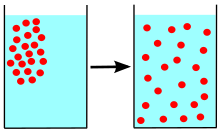
확산
Diffusion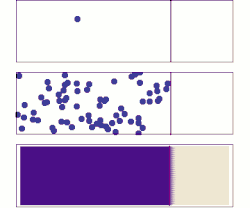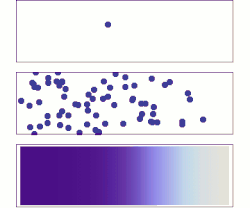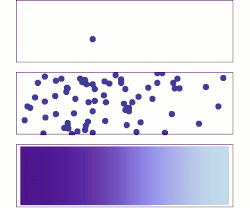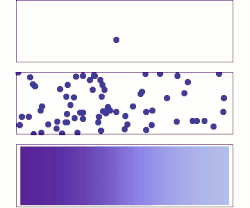
확산은 일반적으로 농도가 높은 영역에서 농도가 낮은 영역으로 모든 것(예를 들어 원자, 이온, 분자, 에너지)의 순이동입니다.확산은 깁스 자유 에너지 또는 화학적 전위의 기울기에 의해 추진된다.스피노달 분해와 같이 농도가 낮은 영역에서 농도가 높은 영역으로 "업힐"을 확산시킬 수 있다.
확산의 개념은 물리학, 화학, 생물학, 사회학, 경제학, 그리고 금융을 포함한 많은 분야에서 널리 사용된다.그러나 확산의 중심 개념은 이 모든 것에 공통적이다: 확산 중인 물질이나 수집물은 그 물질이나 수집물의 농도가 더 높은 지점이나 위치에서 확산된다.
구배는 농도, 압력 또는 온도와 같은 양의 값에서 다른 변수(일반적으로 거리)의 변화에 따른 변화입니다.거리에 걸친 집중력의 변화를 농도구배라고 하고, 거리에 따른 압력의 변화를 압력구배라고 하며, 거리에 따른 온도 변화를 온도구배라고 합니다.
확산이라는 단어는 "퍼지다"를 뜻하는 라틴어 diffundere에서 유래했다.
확산의 구별되는 특징은 입자 랜덤 워크에 의존하며, 따라서 직접적인 벌크 운동 없이 혼합 또는 대량 수송을 발생시킨다는 것이다.벌크 모션 또는 벌크 플로우는 [1]이류의 특성입니다.대류라는 용어는 두 운송 현상의 조합을 설명하기 위해 사용된다.
확산 과정을 Fick의 법칙으로 설명할 수 있다면, 그것은 정상 확산(또는 Fickian 확산)이라고 불립니다.그렇지 않으면 변칙 확산(또는 비-피키 확산)이라고 합니다.
확산 정도에 대해 설명할 때, 두 가지 다른 시나리오에서 두 가지 길이 척도를 사용한다.
- 임펄스 포인트 선원의 브라운 운동(예를 들어 향수 한 번 분무) - 이 지점으로부터의 평균 제곱 변위의 제곱근.Fickian 확산에서는 이것이 Dt\sqrt {입니다 서 n n은 이 브라운 운동의 치수입니다.
- 1차원에서의 일정한 농도원, 즉 확산 길이.Fickian 확산에서는 t(\ 2입니다.
확산 vs 벌크 플로우
"벌크 플로우"는 압력 경사(예: 수도꼭지에서 물이 나오는 것)로 인해 몸 전체가 움직이거나 흐르는 것입니다."확산"은 물질의 순 움직임 없이 농도 경사로 인해 신체 내에서 서서히 움직이거나 분산되는 것을 말한다.벌크 운동과 확산이 모두 일어나는 과정의 예로는 사람의 [2]호흡이 있습니다.
첫 번째로 '벌크 플로우' 프로세스가 있습니다.폐는 외부 호흡의 첫 단계로 확장되는 흉강 안에 위치합니다.이 팽창은 폐포의 부피의 증가로 이어져 폐포의 압력 감소를 일으킨다.이로 인해 상대적으로 높은 압력의 체외 공기와 상대적으로 낮은 압력의 폐포 사이에 압력 경사가 발생합니다.공기는 폐의 기도를 통해 압력 구배를 내려가고 폐포의 압력이 같아질 때까지 폐포 안으로 이동합니다. 즉, 압력 구배가 없어지면 폐포에 있는 공기의 움직임이 중단됩니다.
둘째, "확산" 프로세스가 있습니다.폐포에 도착하는 공기는 폐포에 있는 "몰래" 공기보다 더 높은 산소 농도를 가지고 있습니다.산소 농도의 증가는 폐포의 공기와 폐포를 둘러싼 모세혈관의 혈액 사이에 산소의 농도 구배를 생성합니다.산소는 확산에 의해 농도 구배를 따라 혈액으로 이동한다.공기가 폐포에 도달하는 또 다른 결과는 폐포의 이산화탄소 농도가 감소하는 것입니다.이것은 신선한 공기가 몸의 혈액에 비해 매우 낮은 이산화탄소 농도를 가지고 있기 때문에 이산화탄소가 혈액에서 폐포로 확산되는 농도 구배를 만듭니다.
셋째, 다른 '벌크 플로우' 프로세스가 있습니다.심장의 펌프 작용은 혈액을 몸으로 운반한다.심장의 좌심실이 수축하면 부피가 감소하여 심실의 압력이 높아집니다.이것은 심장과 모세혈관 사이에 압력 구배를 만들고 혈액은 압력 구배를 따라 대량으로 혈관을 통해 이동합니다.
다양한 분야의 맥락에서 확산

확산의 개념은 물리학(입자 확산), 화학, 생물학, 사회학, 경제학, 그리고 금융(사람, 아이디어, 가격 가치의 확산)에서 널리 사용된다.그러나 각각의 경우 확산되는 물질 또는 수집물은 해당 물질 또는 수집물의 농도가 높은 지점 또는 위치에서 "확산"되고 있다.
확산의 개념을 도입하는 방법에는 두 가지가 있다: Fick의 확산의 법칙과 그 수학적 결과에서 출발하는 현상학적 접근법, 또는 확산 [3]입자의 랜덤 워크를 고려함으로써 물리적이고 원자론적 접근법.
현상학적 접근에서 확산이란 물질이 고농도 영역에서 벌크 운동 없이 저농도 영역으로 이동하는 것을 말한다.Fick의 법칙에 따르면 확산 플럭스는 농도의 음의 구배에 비례합니다.농도가 높은 지역에서 농도가 낮은 지역으로 이동합니다.잠시 후, 픽의 법칙의 다양한 일반화가 열역학 및 비균형 열역학 [4]프레임에서 개발되었습니다.
원자론적 관점에서 확산입자의 랜덤워크 결과 확산이 고려된다.분자 확산에서, 움직이는 분자는 열에너지에 의해 스스로 추진된다.1827년 로버트 브라운은 액체 매체에 부유하고 광학 현미경으로 볼 수 있을 정도로 큰 미세 입자가 브라운 운동으로 알려진 입자의 빠르고 불규칙한 움직임을 보인다는 것을 발견했다.브라운 운동 이론과 확산의 원자론적 배경은 알버트 [5]아인슈타인에 의해 개발되었다.확산의 개념은 일반적으로 개인의 앙상블에서 랜덤 워크를 포함하는 모든 주제에 적용된다.
화학 및 재료 과학에서 확산은 다공질 [6]고체에서 유체 분자의 움직임을 말한다.분자 확산은 모공벽과의 충돌보다 다른 분자와 충돌할 가능성이 더 높을 때 발생합니다.이러한 조건 하에서 확산도는 비결합 공간에서의 확산도와 비슷하며 평균 자유 경로에 비례합니다.Knudsen 확산: 모공 직경이 모공을 통해 확산되는 분자의 평균 자유 경로와 같거나 작을 때 발생합니다.이 상태에서는 모공벽과의 충돌 가능성이 점차 높아져 확산도가 낮아진다.마지막으로, 만약 분자가 모공의 크기와 비슷한 크기를 가지고 있다면 일어나는 구성 확산이 있습니다.이 상태에서는 분자 확산에 비해 확산도가 훨씬 낮고 분자의 운동 직경의 작은 차이가 확산도에 큰 차이를 일으킨다.
생물학자들은 확산에 의한 이온이나 분자의 움직임을 묘사하기 위해 종종 "망 운동" 또는 "망 확산"이라는 용어를 사용합니다.예를 들어 산소는 세포 바깥에 산소 농도가 높은 한 세포막을 통해 확산될 수 있습니다.그러나 분자의 이동이 무작위적이기 때문에 때때로 산소 분자가 세포 밖으로 이동한다(농도 구배 반대).세포 밖에 산소 분자가 더 많기 때문에 산소 분자가 세포로 들어갈 확률은 산소 분자가 세포 밖으로 나갈 확률보다 높다.따라서 산소 분자의 "순" 이동은 세포 안으로 들어가거나 나가는 분자 수의 차이입니다.즉, 산소 분자의 순 이동이 농도 구배를 따라 내려가게 됩니다.
물리학에서의 확산의 역사
시간의 범위에서는, 확산 이론이 만들어지기 훨씬 전에 고체의 확산이 사용되었다.예를 들어, 대 플리니(Pliny the Elder)는 앞서 탄소 확산을 통해 철(Fe) 원소에서 강철을 생산하는 접합 공정을 설명했습니다.또 다른 예는 수세기 동안 잘 알려져 있는데 스테인드글라스나 토기, 중국 도자기의 색상의 확산이다.
현대 과학에서, 확산에 대한 최초의 체계적인 실험 연구는 토마스 그레이엄에 의해 수행되었다.그는 기체의 확산을 연구했고, 주요 현상은 1831–1833년에 [7]그에 의해 설명되었습니다.
서로 다른 성질을 가진 생물은 접촉했을 때 밀도, 가장 무거운 것, 가장 가벼운 것 순으로 배열하지 않지만, 자연히 서로 균등하게 퍼지기 때문에 오랜 시간 동안 혼합물의 밀착 상태를 유지합니다.
그레이엄의 측정은 제임스 클러크 맥스웰이 1867년에 대기 중 CO의 확산2 계수를 도출하는 데 기여했다.에러율이 5% 미만입니다.
1855년, 취리히 출신의 26세의 해부학자 아돌프 픽은 확산의 법칙을 제안했다.그는 그레이엄의 연구를 이용하여 "단일 공간 요소에서의 확산 작동을 위한 기본 법칙의 개발"이라고 말했다.그는 열이나 전기의 확산과 전도 사이의 깊은 유사성을 주장했고, 푸리에의 열 전도 법칙(1822)과 옴의 전류 법칙(1827)과 유사한 형식주의를 만들었다.
로버트 보일은 17세기에[8] 아연을 구리 동전에 침투시킴으로써 고형물의 확산을 증명했다.그럼에도 불구하고 고체의 확산은 19세기 후반까지 체계적으로 연구되지 않았다.영국의 잘 알려진 야금학자이자 토마스 그레이엄의 전 조수였던 윌리엄 챈들러 로버츠 오스틴은 1896년에 납 속의 금의 예에 대해 체계적으로 고체 확산을 연구했습니다.[9]
"... 그레이엄의 연구와의 오랜 인연으로 인해 액체 확산에 대한 그의 연구를 금속으로 확장하는 것이 거의 의무처럼 되었습니다."
1858년, 루돌프 클라우시우스는 평균 자유 경로의 개념을 도입했다.같은 해에, 제임스 클럭 맥스웰은 기체 내 수송 과정에 대한 최초의 원자론적 이론을 개발했다.확산과 브라운 운동에 대한 현대 원자론은 알버트 아인슈타인, 마리안 스몰루쇼스키, 장 밥티스트 페랭에 의해 개발되었다.루드비히 볼츠만은 거시적 수송 과정의 원자론적 배경을 개발하면서 140년 [10]이상 수송 과정의 아이디어와 우려의 원천과 함께 수학과 물리학에 기여해 온 볼츠만 방정식을 도입했다.
1920-1921년 조지 드 헤베시는 방사성 동위원소를 사용하여 자기 확산을 측정했다.그는 액체 속의 납과 고체 납의 방사성 동위원소 자기 확산에 대해 연구했다.
야코프 프렌켈(때로는 야코프/야콥 프렌켈)은 1926년에 국소적인 결함(공기와 간질 원자)을 통해 결정으로 확산된다는 아이디어를 제안하고 상세하게 설명했다.그는 응집물질의 확산 과정은 입자와 결함의 기본 점프와 준화학 상호작용의 집합체라고 결론지었다.그는 확산의 여러 메커니즘을 도입했고 실험 데이터에서 속도 상수를 찾았다.
얼마 후, 칼 바그너와 월터 H. 쇼트키는 확산 메커니즘에 대한 프렌켈의 아이디어를 더욱 발전시켰다.현재,[9] 결정의 확산을 매개하기 위해 원자 결함이 필요하다는 것은 보편적으로 인식되고 있다.
헨리 아이링은 공저자들과 함께 그의 절대 반응 속도 이론을 프렌켈의 준화학 [11]확산 모델에 적용했다.반응 속도론과 확산 사이의 유사성은 다양한 비선형 버전의 픽 법칙으로 [12]이어집니다.
확산의 기본 모델
확산 플럭스
각 확산 모델은 농도, 밀도 및 그 유도체를 사용하여 확산 플럭스를 표현합니다.Flux는 전달량과 방향을 벡터J{입니다.작은 영역 S \ S에 통상적인\displaystyle\delta S가 있는 경우 N(\)이 S(\displaystyle \ S)를 통해 전송되는 시간은 tdisplaystyle \S
, ){ ( \ } , { \ \ } 、o ) notation notation notation notation notation notation notation notation notation notation notation notation o 입니다.벡터 영역 S S{ \\ } = bold symbol \ nu 、 \ S의 표기법을 사용하면 다음과 .
확산 플럭스의 치수는 [color] = [color]/([time]·[면적])이다.확산 N(\ N은 입자 수, 질량, 에너지, 전하 또는 기타 스칼라 광대한 양일 수 있습니다.밀도(\ n에 대해 확산방정식은 다음과 같은 형태를 갖는다.
서 W W는 이 양의 로컬 소스 강도(예: 화학 반응 속도)입니다.확산방정식의 경우 no-display boundary 조건은 경계에서 (( () ( {\ symbol 0 으로 공식화할 수 있으며, 서 symbol 은x stymbl}의 에서의 정규 표시이다
픽의 법칙과 방정식
Fick의 제1법칙: 확산 플럭스는 농도 구배의 음수에 비례합니다.
대응하는 확산 방정식(Fick의 제2법칙)은 다음과 같다.
여기서는 Laplace 연산자입니다.
다성분 확산 및 열확산에 대한 Onsager 방정식
픽의 법칙은 매질 속의 혼합물의 확산을 묘사한다.이 혼합물의 농도는 작아야 하며 이 농도의 경사도 또한 작아야 한다.Fick의 법칙에서 확산의 원동력은 집중력의 항방사성 물질이다 - \ \ n
1931년, 라스[13] 온사저는 선형 비균형 열역학의 일반적인 맥락에서 다성분 수송 과정을 포함시켰다.멀티 컴포넌트 수송의 경우,
서 스타일 })는 ih 물리량(성분)의 플럭스이고 X_는 j번째 열역학력입니다.
운송 과정의 열역학적 힘은 엔트로피 ss의 파생물 공간 구배로서 Onsager에 의해 도입되었다(따옴표 또는 "구동력"에서 "힘"이라는 용어를 사용).
서 n i{ style _ { are 、 "역학적 좌표"입니다.열 및 질량 전달의 경우 n 에너지 밀도)가 될 수 , 는 i 성분의 농도입니다.해당하는 추진력은 공간 벡터입니다.
- d = - i T i \ \} s
여기서 T는 , 는 i i 성분의 화학적 전위입니다.개별 확산 방정식은 벌크 운동 없이 혼합 또는 질량 수송을 설명한다는 점을 강조해야 한다.따라서 총 압력의 변동이 있는 항은 무시됩니다.작은 혼합제의 확산 및 작은 구배에도 가능합니다.
선형 Onsager 방정식의 경우, 평형에 가까운 선형 근사에서의 열역학적 힘을 구해야 합니다.
서 s{\ s의 도함수는 평형 n {\ n에서 계산됩니다. {displaystyle 의 행렬은 대칭(Onsager 상호관계) 및 양의(엔트로피 증가)이어야 합니다.
전송 방정식은
여기서 모든 지수 i, j, k = 0, 1, 2, ...는 내부 에너지(0) 및 다양한 성분과 관련이 있다.각 괄호 안의 식으로는 확산계수(i,k > 0), 열확산계수(i > 0, k = 0 또는 k > 0, i = 0) 및 열전도계수(i = k = 0)의 가 있다.
등온 조건에서 T = 상수.관련된 열역학 퍼텐셜은 자유 에너지(또는 자유 엔트로피)입니다.등온 확산의 열역학적 추진력은 화학 전위의 반방사성 물질-(/ ) j\ - _이며 확산 계수의 매트릭스는 다음과 같습니다.
(i,k > 0).
열역학적 힘과 운동 계수의 정의에 내재적 임의성이 있으며, 이는 개별적으로 측정할 수 없고, 그 조합 j j X \ _만 측정할 수 있기 때문이다.예를 들어, Onsager의[13] 원래 작업에서 열역학 힘은 추가 승수 T를 포함하지만, 이론 물리학[14] 과정에서는 이 승수는 생략되지만 열역학 힘의 부호는 반대입니다.이러한 모든 변경은 해당 계수의 변경으로 보완되며 측정 가능한 양에는 영향을 미치지 않습니다.
비직각 확산은 비선형이어야 합니다.
선형 비가역 열역학(Onsager)의 형식주의는 다음과 같은 형태의 선형 확산 방정식의 시스템을 생성한다.
확산 계수의 행렬이 대각선인 경우, 이 방정식 시스템은 다양한 성분에 대한 분리된 Fick의 방정식의 집합일 뿐입니다.확산이 0 0이라고 가정하고 (\} =\{n} = 이 상태에서는/ t 1DISPLAY)로 합니다. 1() < \ D _ { } , \ c{ () } c c c c c c c c c c c c c c c c c c c c c c c c c c )는 단시간에 음이 됩니다.따라서 선형 비대각 확산은 농도의 양성을 보존하지 않는다.다성분 확산의 비대각 방정식은 [12]비선형이어야 합니다.
아인슈타인의 이동성과 테오렐 공식
아인슈타인 관계(운동학 이론)는 확산 계수와 이동성(적용된 [15]힘에 대한 입자의 종단 드리프트 속도의 비율)을 연결한다.
여기서 D는 확산 상수, μ는 "이동성", k는B 볼츠만 상수, T는 절대 온도, q는 기본 전하, 즉 한 전자의 전하이다.
아래에서는 화학 퍼텐셜 μ와 이동성을 동일한 공식으로 조합하기 위해 m 를 이동성에 사용합니다.
이동성 기반 접근방식은 T에 의해 더욱 적용되었습니다.티렐.[16]1935년, 그는 막을 통한 이온의 확산을 연구했다.그는 자신의 접근법의 본질을 다음 공식으로 공식화했다.
- 플럭스는 이동성 × 농도 × 그램당 힘과 같다.
이것은 소위 '테오렐 공식'입니다."그램-이온"이라는 용어는 아보가드로의 이온 수(입자)를 포함하는 물질의 양을 의미한다.일반적인 현대 용어는 두더지입니다.
등온 조건에서의 힘은 다음 두 부분으로 구성됩니다.
- 농도 구배에 의한 확산력 - 1 n - ( ( / - RT { \ } { n } , \ n = - , \ ( \ / { \ { } )} )
- 전위 구배에 의해 발생하는 : ∇、 \ q , \ \ }
여기서 R은 기체 상수, T는 절대 온도, n은 농도, 평형 농도는 "eq"로 표시되며 q는 전하, θ는 전위이다.
Teorell 공식과 Onsager 법칙의 간단하지만 결정적인 차이는 Teorell 식에서 플럭스에 대한 농도 계수입니다.아인슈타인에서...Teorell 접근법, 만약 유한한 힘에 대해 농도가 0이 되는 경향이 있다면, 플럭스도 0이 되는 경향이 있는 반면 Onsager 방정식은 이 간단하고 물리적으로 명백한 규칙을 위반합니다.
등온 조건 하에서[12] 불완전 시스템에 대한 Teorell 공식의 일반적인 공식은 다음과 같습니다.
여기서 μ는 화학0 퍼텐셜, μ는 화학 퍼텐셜의 표준값입니다. ( - RT) { a = \ \ left } \ { \ _ { } {RT는 이른바 액티비티입니다.이상적이지 않은 혼합물에서 종의 "유효한 농도"를 측정합니다.이 표기법에서, 플럭스에 대한 Teorell 공식은 매우 단순한 형태를[12] 가지고 있다.
활성의 표준 유도체에는 정규화 인자가 포함되며, 의 경우 a / nµ + (n / µ ){ a = / { \ } + ( / ^ { \ )( n \ n ^ { \ minus } ) ) 。따라서 플럭스 공식은 정규화된 무차원량 {\ { n의 플럭스를 나타낸다.
변동-분산 정리
아인슈타인 모델을 탄도 시간 [17]척도로 확장하기 위해 랑게뱅 방정식에 기초한 변동-분산 정리를 개발한다.Langevin에 따르면, 이 방정식은 뉴턴의 제2운동법칙에 기초하고 있다.
어디에
- x는 위치입니다.
- μ는 유체 또는 기체 내 입자의 이동성으로, 아인슈타인 관계(운동학 이론)를 사용하여 계산할 수 있습니다.
- m은 입자의 질량입니다.
- F는 입자에 가해지는 임의의 힘이다.
- t는 시간입니다.
이 방정식을 풀면 오랜 시간 한계에서 시간의존성 확산 상수를 얻을 수 있고 입자가 주변 [17]유체보다 상당히 밀도가 높을 때,
어디에
- k는B 볼츠만의 상수이다.
- T는 절대 온도입니다.
- μ는 유체 또는 기체 내 입자의 이동성으로, 아인슈타인 관계(운동학 이론)를 사용하여 계산할 수 있습니다.
- m은 입자의 질량입니다.
- t는 시간입니다.
다성분 확산 Teorell 공식
Onsager의 확산력에 대한 정의를 조합한 Teorell 공식은 다음과 같다.
서 m은 ih 구성요소의 이동성, 는 활동, })는 계수의 ,({X_j})}는 열역학 확산력, j - 등온완벽시스템에 는 Xj = - jn j \ _ { j } - { \ { \ { n { } { _ { j } 。그래서 아인슈타인은...Teorell 접근법은 다성분 확산에 대한 Fick의 법칙을 다음과 같이 일반화한다.
서 는 계수의 매트릭스입니다.기체 확산에 대한 채프먼-엔스코그 공식은 정확히 같은 용어를 포함한다.앞서 이러한 용어는 맥스웰-스테판 확산 방정식에 도입되었다.
표면과 고체에서 점프합니다.
촉매 표면에서의 시약 확산은 이종 촉매 작용에 중요한 역할을 할 수 있습니다.이상적인 단분자층의 확산 모델은 가장 가까운 자유 장소에서의 시약 점프를 기반으로 합니다.이 모델은 낮은 가스 압력에서 Pt 산화 시 CO에 사용되었습니다.
이 시스템에는 표면에 여러 의 {{2},\m}이(가) 포함되어 있습니다.표면 농도는 {입니다.} 표면은 흡착부위의 격자이다각 시약 분자는 표면의 한 부분을 채운다.몇 군데는 무료입니다.빈 영역의 농도는 z 0 z입니다. 공간 포함의 합계는 일정하며 흡착 밀도 b입니다.
점프 모델은 i = 1, ..., n):
해당하는 확산 방정식은 다음과 같습니다.[12]
z - i ,{ z _의 보존법칙에 의해 m확산방정식이 성립한다.한 성분에 대해 Fick의 법칙과 선형 방정식을 얻을 수 있습니다 왜냐하면 ( ) - -c ) c 、 \ style ( b - c ) , \ displayla c - c , \ ( b - c ) , \ c , \ la , \ lac. 이상의 성분에 대해 방정식이 비선형이기 때문입니다.
만약 모든 입자가 가장 가까운 입자와 위치를 교환할 수 있다면, 간단한 일반화는 다음과 같다.
서 j i0 { }= 0은 점프의 강도를 특징짓는 계수의 대칭 행렬이다.빈 공간(공백)은 0의 특수 "입자"로 간주해야 합니다.
이러한 점프 모델의 다양한 버전은 고체에서 단순한 확산 메커니즘에도 적합합니다.
다공질 매체 내 확산
다공질 매체의 확산에 대한 기본 방정식은 다음과 같습니다(δ가 일정할 경우).[18]
여기서 D는 확산 계수, δ는 다공성, n은 농도, m > 0이다(일반적으로 m > 1, 대문자 m = 1은 픽의 법칙에 해당한다).
다공질 매체의 다공성(δ)을 플럭스 조건과 축적 [19]조건 모두에서 적절하게 고려하도록 주의해야 합니다.예를 들어 다공성이 0이 되면 다공질 매체 내의 몰 플럭스는 소정의 농도 구배만큼 0이 된다.플럭스의 분산을 적용하면 다공성 항이 소거되고 위의 두 번째 방정식이 형성된다.
다공질 매체에서 기체의 확산에 대해 이 방정식은 다공질 매체에서 기체의 부피 측정 플럭스는 Darcy의 법칙을 공식화한 것입니다.
여기서 k는 매체의 투과성, μ는 점도, p는 압력이다.
이류성 어금니 플럭스는 다음과 같이 주어진다.
J = nq
~ n { n}} Darcy의 법칙은 다공질 매체에서의 확산 방정식을 m = γ + 1로 나타낸다.
다공질 매체에서 평균 선형 속도(θ)는 다음과 같이 체적 플럭스와 관련된다.
이류 몰 플럭스와 확산 플럭스를 결합하면 이류 분산 방정식을 얻을 수 있습니다.
지하수 침투의 경우, Bousinesq 근사치는 m = 2와 같은 방정식을 제공한다.
방사선이 높은 혈장의 경우 젤도비치-라이저 방정식은 열 전달을 위해 m > 4를 나타낸다.
물리학에서의 확산
기체운동이론의 확산계수
확산 DD})는 Fick의 J - Dn /x({ J,\n/\ x의 계수입니다. 여기서 J는 단위 시간당 단위 면적당 확산 플럭스(물질의 양)이고 n(이상 혼합물의 경우)은 x 길이입니다.
직경 d와 질량 m(자기 확산)이 같은 분자를 가진 두 기체를 생각해보자.이 경우, 확산의 기본 평균 자유 경로 이론은 확산 계수를 구한다.
여기서B k는 Boltzmann 상수, T는 온도, P는 압력, {은 평균 자유 경로, v는T 평균 열 속도입니다.
평균자유경로근사확산계수는 T가 되면3/2 커지고 P가 1/P이면 감소하는 것을 알 수 있다.P에 대해 이상적인 가스 법칙 P = RnT를 총 농도 n으로 사용하면, 주어진 농도 n에 대해 확산 계수가 T와1/2 함께 증가하고, 주어진 온도에 대해 총 농도 1/n과 함께 감소함을 알 수 있다.
분자 질량A m, mB 및 분자 지름A d, d를B 가진 두 개의 다른 기체 A와 B의 경우, B와 A의 확산 계수의 평균 자유 경로 추정치는 다음과 같다.
볼츠만 방정식에 기초한 기체 확산 이론
Boltzmann의 기체 혼합 동역학에서 각 기체는 자체 분포 , {, 를 가지고 있습니다. 여기서 t는 시간 모멘트, x는 위치, c는 혼합물의 ih 성분 분자 속도입니다.각 컴포넌트에는 ) f (x , , ) { _ { ( x , t )\_ { ( , t )cf ( x , t )。는 ( x
채프먼-엔스코그 근사에서 모든 분포 함수는 보존된 [10]양의 밀도를 통해 표현된다.
- 입자의 개별 농도, (x , ) ( , , ) c \ _ { } ( , , t ) = \_ { } _ { , ) , ( 볼륨당 최대)
- 운동량 밀도 i ( ,) { _ {m _ _ {i} _ { (, ) } (m은i ih 입자 질량),
- 운동 에너지 밀도
운동 온도 T와 압력 P는 3D 공간에서 다음과 같이 정의됩니다.
서 n in i { n = \_ {은 총 밀도입니다.
두 기체의 속도 인 C - 2 ({2}})는 다음과 같다.[10]
서 Fi는 ih성분의 분자에 가해지는 이고 kT(\k_{)입니다.는 열확산비입니다.
계수12 D는 양수이다.이것은 확산 계수입니다.C-C12 공식의 네 가지 항은 기체 확산에 대한 네 가지 주요 효과를 나타낸다.
- ( n ) { \ displaystyle \ \ , \ { n _ { n _ { } { n } \ right }는 n/n 비율이 높은1 영역에서 n/n2 값이 낮은 영역까지의 첫 번째 성분의 플럭스1(및 n/n = 1 ~ n이므로 두 번째 성분의 플럭스)를 나타낸다22
- 1 ( - ) n ( n + n ) nP \ display { { { n _ { - m {1 }{2}}}}}}\plass 영역과 무거운 분자의 영역을 나타냅니다.
- 1 2 P ( + 2 ) ( 1 - ) 。{ { _ { m _ {} n _ { {2} 2} {1} 1} + {2}} } } } ( ( - { } ) ) ) diffusion diffusion diffusion diffusion diffusion diffusion diffusion diffusion diffusion diffusion diffusion diffusion 。예를 들어, 지구의 중력장에서는, 무거운 분자가 아래로 내려가거나, 대전된 분자가 움직여야 합니다. 이 효과가 다른 용어의 합계에 의해 평형화되지 않을 때까지 말입니다.이 효과는 압력 경사로 인해 발생하는 압류 현상과 혼동해서는 안 됩니다.
- T는 온도 구배에 의한 확산 플럭스인 서모디퓨전(thermodiffusion)을 기술한다.
이 모든 효과는 혼합물 내 다른 성분들의 속도 차이를 설명하기 때문에 확산이라고 불립니다.따라서 이러한 효과는 벌크 운송으로 설명할 수 없으며 이류 또는 대류와는 다릅니다.
첫 번째 [10]근사치에서는
- 강체 구체의 경우
- § - . {\ _ { } { - \ }
A1 ( ) { A { 1 ( \ } } } is 、 atures 、 Chapman and Cowling[10] ))))) ))) ( 3 . 7 ) 、 ( 3 . 9 ) of 、 10 ) 。
강체 구에 대한 T 의존성은 단순 평균 자유 경로 이론과 동일하지만 전력 반발 법칙에 대한 지수는 다르다는 것을 알 수 있다.주어진 온도에서 총 농도 n에 대한 의존성은 항상 동일한 문자 1/n을 가집니다.
기체 역학을 적용할 때 확산 플럭스와 벌크 플로우는 하나의 수송 방정식에 결합되어야 한다.벌크 플로우는 질량 전달을 나타냅니다.그것의 속도 V는 질량 평균 속도이다.운동량 밀도와 질량 농도를 통해 정의됩니다.
여기서 i i \ _ {i} =} } i i { = \_{ \ _}}} where where where where where where where where where where where where where where where where where where where where where where where where where where where where where where where where where where
정의상, ih 성분의 확산 는 - ({{iV i 0(style \ _ _}=이다.ih 성분의 질량 전달은 연속성 방정식으로 설명됩니다.
서 })는 화학 반응의 순 대량 생산 속도이며, _})
이 식에서 용어 ( i) \ ( \_ { } )는 ih 성분의 이류를 나타내고 용어 ( i ( \_ {_ {는 이 성분의 확산을 나타낸다.
1948년 웬델 H. 퍼피는 기체 확산에 대한 새로운 현상학적 접근을 위한 틀로서 운동 이론에서 발견된 확산 속도의 형태를 사용하자고 제안했다.이 접근방식은 F.A.에 의해 추가로 개발되었다.윌리엄스와 S.H.[20] 램입니다다성분 가스(N개 성분)의 확산 속도에 대해 사용된
서 ij})는 확산계수 행렬,는 , 는 단위질량당 i종별 체력, 는 열확산계수 행렬이다.는 ith종의 분압분율( 는 분압분율), {}=\ _}는 ih종의 질량분율, x = = = = = = = = = }이다.
고체 중의 전자 확산
고체에서 전자의 밀도가 평형을 이루지 못하면 전자의 확산이 일어난다.예를 들어 반도체 덩어리의 양끝에 치우침이 가해지거나 한쪽 끝에 빛이 비칠 때(오른쪽 그림 참조), 전자는 고밀도 영역(중앙)에서 저밀도 영역(양끝)으로 확산되어 전자 밀도의 구배를 형성한다.이 프로세스는 확산 전류라고 하는 전류를 생성합니다.
확산 전류는 Fick의 제1법칙으로도 설명할 수 있습니다.
여기서 J는 단위시간당 단위면적당 확산전류밀도(물질의 양), n(이상혼합물의 경우)은 전자밀도, x는 위치[길이]이다.
지구물리학에서의 확산
서로 다른 초기 및 경계 조건에 대한 확산 방정식을 푸는 분석 및 수치 모형은 지구 표면의 다양한 변화를 연구하기 위해 인기를 끌었다.확산은 경사면 퇴각, 절벽 침식, 단층 스카프 열화, 파단 테라스/해안선 퇴각, 충적 수로 절개, 해안 선반 퇴각 및 델타 [21]순행의 침식 연구에 광범위하게 사용되어 왔다.비록 이러한 경우들 중 많은 경우에서 지구 표면이 문자 그대로 확산되지 않지만, 확산의 과정은 수십 년에서 수천 년에 걸쳐 일어나는 전체적인 변화를 효과적으로 모방한다.확산 모델은 또한 고환경 재구축에서 퇴적환경에 대한 일부 정보를 알고 확산방정식을 사용하여 지형변화의 [22]퇴적물 유입 및 시계열을 파악하는 역경계값 문제를 해결하기 위해 사용될 수 있다.
투석

투석은 용질의 확산과 반투과성 막을 통한 유체의 초여과 원리로 작용합니다.확산은 물 속 물질의 특성입니다. 물 속 물질은 고농도 영역에서 [23]저농도 영역으로 이동하는 경향이 있습니다.혈액은 반투과성 막의 한쪽에서 흐르고 투석액 또는 특수 투석액은 반대쪽에서 흐릅니다.반투과막은 다양한 크기의 구멍 또는 모공을 포함하는 얇은 재료 층이다.더 작은 용질과 액체는 막을 통과하지만, 막은 더 큰 물질의 통과를 막는다.이것은 혈액이 신장으로 들어갈 때 신장에서 일어나는 여과 과정을 재현하고 큰 물질은 사구체의 [23]작은 물질과 분리된다.
랜덤 워크(랜덤 모션)
한 가지 일반적인 오해는 개별 원자, 이온 또는 분자가 무작위로 움직인다는 것인데, 그렇지 않다.오른쪽 애니메이션에서 왼쪽 패널의 이온은 다른 이온이 없을 때 "랜덤" 운동을 하는 것으로 보입니다.그러나 오른쪽 패널에 나타나 있듯이 이 움직임은 무작위적인 것이 아니라 다른 이온과의 "충돌"의 결과입니다.이와 같이, 혼합물 내의 단일 원자, 이온 또는 분자의 움직임은 분리하여 볼 때 무작위로 나타난다."랜덤 워크"에 의한 혼합물 내 물질의 이동은 농도, 압력 또는 온도 변화에 의해 영향을 받을 수 있는 시스템 내 운동에너지에 의해 제어된다.(이것은 고전적인 설명입니다.작은 규모에서는 일반적으로 양자 효과는 무시할 수 없습니다.따라서, 그러한 작은 규모의 입자는 위치와 속도의 결정론적 측정이 아닌 확률적 진폭으로 묘사되기 때문에 단일 원자의 움직임에 대한 연구는 더 미묘해진다.)
기체 대류로부터의 확산 분리
브라운이 연구한 꽃가루 알갱이와 같은 다분자 메조스코프 입자의 브라운 운동은 광학 현미경으로 관찰할 수 있지만, 분자 확산은 신중하게 통제된 실험 조건에서만 탐색할 수 있습니다.Graham 실험 이후, 대류를 피하는 것이 필요하다는 것은 잘 알려져 있으며, 이것은 사소한 일이 아닐 수도 있다.
정상적인 조건에서는 분자 확산이 나노미터에서 밀리미터까지의 길이로만 지배적이다.더 큰 길이의 스케일에서 액체와 기체의 운송은 일반적으로 대류라는 또 다른 운송 현상에 기인합니다.이러한 경우의 확산을 분리하기 위해서는 특별한 노력이 필요하다.
따라서 종종 인용되는 확산의 예는 잘못된 것이다.향수를 한 곳에 뿌리면 방 전체에서 금방 냄새가 나지만, 간단한 계산으로는 확산 때문일 수 없다는 것을 알 수 있다.온도[불균질] 때문에 실내에서 대류 운동이 지속된다.잉크가 물에 떨어지면 공간 분포의 불균일한 진화를 관찰할 수 있는데, 이는 대류 현상을 명확하게 나타낸다(특히 이 [citation needed]낙하로 인해 발생).
반면, 고체 매체를 통한 열전도는 일상적인 일입니다(예를 들어 금속 스푼이 뜨거운 액체에 부분적으로 담그는 경우).이것은 왜 열의 확산이 질량의 확산 이전에 수학적으로 설명되었는지를 설명해준다.
기타 확산 유형
- Perona-Malik 방정식으로도 알려진 이방성 확산은 높은 구배를 강화합니다.
- 고체에서의 원자 확산
- Bohm 확산, 플라즈마의 자기장 간 확산
- 와류 확산(난류 흐름의 대략적인 설명)
- 작은 구멍을 통한 가스 유출
- 확산 전류라고 하는 전류를 발생시키는 전자 확산
- 일부 유기체에 존재하는 촉진 확산
- 동위원소 분리에 사용되는 기체 확산
- 열방정식, 열에너지 확산
- 이토 확산, 브라운 운동 수학화, 연속 확률 과정.
- 벽 충돌 빈도가 높은 긴 모공 내 가스 Knudsen 확산
- 레비 비행
- 분자 확산, 밀도가 높은 영역에서 밀도가 낮은 영역으로 분자의 확산
- 유체역학적 속도장의 확산 등 운동량 확산
- 광자 확산
- 플라즈마 확산
- 랜덤 워크,[24] 확산 모델
- 상분리 시 농도 구배에 대한 역확산
- 회전 확산, 분자의 무작위 방향 변경
- 표면확산, 표면상에서의 입자 확산
- 택시는 자극에 반응하는 동물의 방향성 운동이다.
- 키네시스는 자극에 반응하는 동물의 무방향 운동 활동이다
- 문화 간 확산, 지역 간 문화적 특성의 확산
- 난류 유체 내에서의 난류 확산, 질량, 열 또는 운동량의 운반
「 」를 참조해 주세요.
레퍼런스
- ^ J.G. 커크우드, R.L. 볼드윈, P.J. 던롭, L.J. 고스팅, G. 케겔스(1960)액체의 등온 확산에 대한 흐름 방정식 및 기준 프레임.화학물리학 저널 33(5): 1505–13.
- ^ Muir, D. C. F. (1966-10-01). "Bulk flow and diffusion in the airways of the lung". British Journal of Diseases of the Chest. 60 (4): 169–176. doi:10.1016/S0007-0971(66)80044-X. ISSN 0007-0971. PMID 5969933.
- ^ J. Philibert (2005).1세기 반의 확산: 픽, 아인슈타인 이전과 그 이후.2013-12-13년 Wayback Machine Diffusion Fundamentals, 2, 1.1–1.10에 보관.
- ^ S.R. 드 그루트, P. 마주르(1962)비균형 열역학.암스테르담의 노스홀랜드.
- ^ A. Einstein (1905). "Über die von der molekularkinetischen Theorie der Wärme geforderte Bewegung von in ruhenden Flüssigkeiten suspendierten Teilchen" (PDF). Ann. Phys. 17 (8): 549–60. Bibcode:1905AnP...322..549E. doi:10.1002/andp.19053220806.
- ^ Pescarmona, P.P. (2020). Gitis, V.; Rothenberg, G. (eds.). Handbook of Porous Materials. Vol. 4. Singapore: WORLD SCIENTIFIC. pp. 150–151. doi:10.1142/11909. ISBN 978-981-12-2328-0.
- ^ 확산 과정, 토마스 그레이엄 심포지엄, ED. J.N. 셔우드, A.V. 채드윅, W.M.1971년 런던, F.L. 스윈튼, 고든 앤 브레이크 뮤어
- ^ L.W. Bar(1997), In: Diffusion in Materials, DIMAT 96, ed.H.Merrer, Chr.Herzig, N.A. Stolwijk, H. Braacht, Scitec 출판물, Vol.1, 페이지 1~9.
- ^ a b H. Mehrer; N.A. Stolwijk (2009). "Heroes and Highlights in the History of Diffusion" (PDF). Diffusion Fundamentals. 11 (1): 1–32.
- ^ a b c d e S. Chapman, T. G. Cowling(1970) 불균일한 기체의 수학적 이론: 기체 내 점성, 열전도 및 확산의 운동 이론 설명, 케임브리지 대학 출판부 (3판), ISBN 052140844X.
- ^ J.F. Kincaid; H. Eyring; A.E. Stearn (1941). "The theory of absolute reaction rates and its application to viscosity and diffusion in the liquid State". Chem. Rev. 28 (2): 301–65. doi:10.1021/cr60090a005.
- ^ a b c d e A.N. Gorban, H.P. Sargsyan and H.A. Wahab (2011). "Quasichemical Models of Multicomponent Nonlinear Diffusion". Mathematical Modelling of Natural Phenomena. 6 (5): 184–262. arXiv:1012.2908. doi:10.1051/mmnp/20116509. S2CID 18961678.
- ^ a b Onsager, L. (1931). "Reciprocal Relations in Irreversible Processes. I". Physical Review. 37 (4): 405–26. Bibcode:1931PhRv...37..405O. doi:10.1103/PhysRev.37.405.
- ^ L.D. Landau, E.M. Lifshitz (1980). Statistical Physics. Vol. 5 (3rd ed.). Butterworth-Heinemann. ISBN 978-0-7506-3372-7.
- ^ S. Bromberg, K.A. Dill(2002), 분자 구동력: Garland Science, ISBN 0815320515 화학 및 생물학 통계 열역학.
- ^ T. Teorell (1935). "Studies on the "Diffusion Effect" upon Ionic Distribution. Some Theoretical Considerations". Proceedings of the National Academy of Sciences of the United States of America. 21 (3): 152–61. Bibcode:1935PNAS...21..152T. doi:10.1073/pnas.21.3.152. PMC 1076553. PMID 16587950.
- ^ a b Bian, Xin; Kim, Changho; Karniadakis, George Em (2016-08-14). "111 years of Brownian motion". Soft Matter. 12 (30): 6331–6346. Bibcode:2016SMat...12.6331B. doi:10.1039/c6sm01153e. PMC 5476231. PMID 27396746.
- ^ J. L. Vazquez (2006)다공질 매체 방정식입니다.옥스퍼드 대학의 수학 이론ISBN 0198569033을 누릅니다.
- ^ Stauffer, Philip H.; Vrugt, Jasper A.; Turin, H. Jake; Gable, Carl W.; Soll, Wendy E. (2009). "Untangling Diffusion from Advection in Unsaturated Porous Media: Experimental Data, Modeling, and Parameter Uncertainty". Vadose Zone Journal. 8 (2): 510. doi:10.2136/vzj2008.0055. ISSN 1539-1663. S2CID 46200956.
- ^ S. H. Lam (2006). "Multicomponent diffusion revisited" (PDF). Physics of Fluids. 18 (7): 073101–073101–8. Bibcode:2006PhFl...18g3101L. doi:10.1063/1.2221312.
- ^ Pasternack, Gregory B.; Brush, Grace S.; Hilgartner, William B. (2001-04-01). "Impact of historic land-use change on sediment delivery to a Chesapeake Bay subestuarine delta". Earth Surface Processes and Landforms. 26 (4): 409–27. Bibcode:2001ESPL...26..409P. doi:10.1002/esp.189. ISSN 1096-9837. S2CID 129080402.
- ^ Gregory B. Pasternack. "Watershed Hydrology, Geomorphology, and Ecohydraulics :: TFD Modeling". pasternack.ucdavis.edu. Retrieved 2017-06-12.
- ^ a b 모스비의 의학, 간호, 건강 직업 사전.제7판세인트루이스, 모스비: 2006
- ^ Weiss, G. (1994). Aspects and Applications of the Random Walk. North-Holland. ISBN 978-0444816061.


 이 브라운 운동의
이 브라운 운동의 

 통상적인
통상적인








 이 양의 로컬 소스 강도(예: 화학 반응 속도)입니다.확산방정식의 경우 no-display boundary 조건은 경계에서 (
이 양의 로컬 소스 강도(예: 화학 반응 속도)입니다.확산방정식의 경우 no-display boundary 조건은 경계에서 (














 i
i

 행렬은 대칭(
행렬은 대칭(![{\displaystyle {\frac {\partial n_{i}}{\partial t}}=-\operatorname {div} \mathbf {J} _{i}=-\sum _{j\geq 0}L_{ij}\operatorname {div} X_{j}=\sum _{k\geq 0}\left[-\sum _{j\geq 0}L_{ij}\left.{\frac {\partial ^{2}s(n)}{\partial n_{j}\,\partial n_{k}}}\right|_{n=n^{*}}\right]\,\Delta n_{k}\ .}](https://wikimedia.org/api/rest_v1/media/math/render/svg/f61d376b495038f57128d2c6ea83f733b7ae0b83)
 있다.
있다. 

 측정할 수 있기 때문이다.예를 들어, Onsager의
측정할 수 있기 때문이다.예를 들어, Onsager의



 단시간에 음이 됩니다.따라서 선형 비대각 확산은 농도의 양성을 보존하지 않는다.다성분 확산의 비대각 방정식은
단시간에 음이 됩니다.따라서 선형 비대각 확산은 농도의 양성을 보존하지 않는다.다성분 확산의 비대각 방정식은 









![{\displaystyle {\frac {\partial (n/n^{\ominus })}{\partial t}}=\nabla \cdot [{\mathfrak {m}}a(\nabla \mu -({\text{external force per mole}}))].}](https://wikimedia.org/api/rest_v1/media/math/render/svg/3f8ae11dd009457b8fd39d1a583ed5d4b3e30ab5)



 ih 구성요소의 이동성,
ih 구성요소의 이동성,  활동,
활동, 


 계수의 매트릭스입니다.
계수의 매트릭스입니다.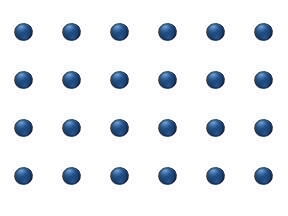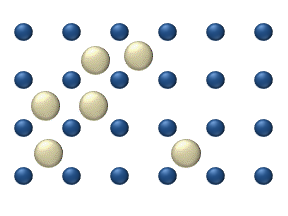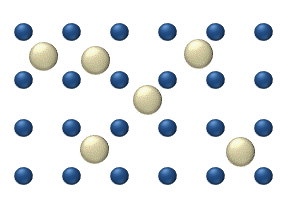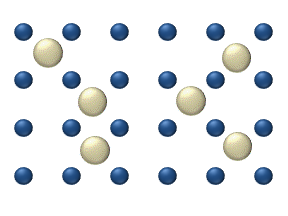





![{\displaystyle \mathbf {J} _{i}=-D_{i}[z\,\nabla c_{i}-c_{i}\nabla z]\,.}](https://wikimedia.org/api/rest_v1/media/math/render/svg/e62d2876591f6c0c24854dc77bd002742a487757)
![{\displaystyle {\frac {\partial c_{i}}{\partial t}}=-\operatorname {div} \mathbf {J} _{i}=D_{i}[z\,\Delta c_{i}-c_{i}\,\Delta z]\,.}](https://wikimedia.org/api/rest_v1/media/math/render/svg/59acf7a4d07ec81e21aec16a7dd999c091b60b79)
 보존법칙에 의해 m확산방정식이 성립한다.한 성분에 대해 Fick의 법칙과 선형 방정식을 얻을 수 있습니다
보존법칙에 의해 m확산방정식이 성립한다.한 성분에 대해 Fick의 법칙과 선형 방정식을 얻을 수 있습니다
![{\displaystyle \mathbf {J} _{i}=-\sum _{j}D_{ij}[c_{j}\,\nabla c_{i}-c_{i}\,\nabla c_{j}]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/aba83bc12bd5bab3419c70e17305975783df881d)
![{\displaystyle {\frac {\partial c_{i}}{\partial t}}=\sum _{j}D_{ij}[c_{j}\,\Delta c_{i}-c_{i}\,\Delta c_{j}]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/63b9c514f4d2f44400b6315598831cacc5edaee9)
 점프의 강도를 특징짓는 계수의 대칭 행렬이다.빈 공간(공백)은
점프의 강도를 특징짓는 계수의 대칭 행렬이다.빈 공간(공백)은 



















 총 밀도입니다.
총 밀도입니다. 

 ih성분의 분자에 가해지는
ih성분의 분자에 가해지는  열확산비입니다.
열확산비입니다. 


 온도 구배에 의한 확산 플럭스인 서모디퓨전(
온도 구배에 의한 확산 플럭스인 서모디퓨전(![{\displaystyle D_{12}={\frac {3}{2n(d_{1}+d_{2})^{2}}}\left[{\frac {kT(m_{1}+m_{2})}{2\pi m_{1}m_{2}}}\right]^{1/2}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/0f17effad1f63d0da95fb3082d73481f845e1785)
![{\displaystyle D_{12}={\frac {3}{8nA_{1}({\nu })\Gamma (3-{\frac {2}{\nu -1}})}}\left[{\frac {kT(m_{1}+m_{2})}{2\pi m_{1}m_{2}}}\right]^{1/2}\left({\frac {2kT}{\kappa _{12}}}\right)^{\frac {2}{\nu -1}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/a21bffa231a21e8104224bb96f51c7a59685b908)










 이 성분의 확산을 나타낸다.
이 성분의 확산을 나타낸다. 



 단위질량당 i종별 체력,
단위질량당 i종별 체력,  ith종의 분압분율(
ith종의 분압분율( 분압분율),
분압분율), 




