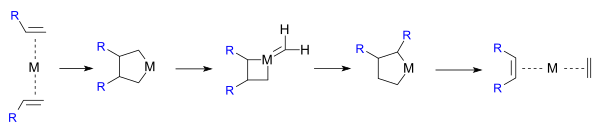올레핀 메타세시스
Olefin metathesis| 올레핀 메타세시스 | |
|---|---|
| 반응형 | 탄소-탄소 결합 형성 반응 |
| 식별자 | |
| 유기화학 포털 | 올레핀 메타제시스 |
| RSC 온톨로지 ID | RXNO:0000280 |
올레핀 메타테제스는 탄소-탄소 이중결합의 [1][2]스크리션 및 재생에 의해 알케인(올레핀) 조각의 재배포를 수반하는 유기 반응이다.올레핀 메타세시스는 비교적 단순하기 때문에 종종 다른 유기 반응보다 바람직하지 않은 부산물과 유해 폐기물을 덜 생성합니다.반응 메커니즘에 대한 설명과 다양한 고활성 촉매의 발견을 위해 이브 쇼빈, 로버트 H. 그럽스, 리처드 R. 슈록은 2005년 노벨 [3]화학상을 공동 수상했다.
촉매
반응에는 금속 촉매가 필요합니다.상업적으로 중요한 대부분의 공정은 이종 촉매를 사용합니다.이종 촉매는 유기 알루미늄 또는 유기소 화합물(예: MCl-EtAlCl2)을x 사용하여 금속 할로겐화물(MCLx)을 현장 활성화하여 제조되는 경우가 많습니다.대표적인 촉매 서포트는 알루미나입니다.상업용 촉매는 종종 몰리브덴과 루테늄을 기반으로 한다.잘 정의된 유기 금속 화합물은 주로 소규모 반응이나 학술 연구에서 연구되어 왔다.균질 촉매는 종종 Schrock 촉매와 Grubbs 촉매로 분류됩니다.슈록 촉매는 몰리브덴(VI) 및 텅스텐(VI) 기반의 중심을 알콕시드 및 이미도 [4]리간드로 지지합니다.
반면 그루브 촉매는 루테늄이다.II) 카르베노이드 [5]복합체Grubbs 촉매의 많은 변형이 알려져 있다.일부는 킬레이트 이소프로옥시벤질리덴 배위자로 변형되어 관련된 호베이다-그럽스 촉매를 형성한다.
적용들
올레핀 메타테제스는 몇 가지 산업 용도를 가지고 있다.거의 모든 상용 애플리케이션은 노벨상 수상 전에 개발된 촉매를 사용하여 균질 [6]복합체에 대한 작업을 수행했습니다.대표적인 프로세스는 다음과 같습니다.[1]
- 필립스 트리올레핀과 올레핀 변환 기술.이 과정은 프로필렌을 에틸렌 및 2-부텐과 상호 변환합니다.레늄 촉매와 몰리브덴 촉매가 사용된다.그러나 [6]오늘날에는 역반응, 즉 에틸렌과 2-부텐을 프로필렌으로 변환하는 것만이 산업적으로 행해지고 있다.
- 쉘 상위 올레핀 공정(SHOP)은 세제로 변환하기 위한 (알파-올레핀)을 생성합니다.이 공정은 메타세시스를 [7]사용하여 특정 올레핀 분율을 재활용합니다.
- 이소부텐 이합체의 분해와 관련된 네오헥센 생산.촉매는 실리카 및 MgO에 지지된 삼산화 텅스텐에서 파생됩니다.
- 유용한 가교제 및 합성 중간체인 1,5-헥사디엔 및 1,9-데카디엔을 시판하여 제조한다.촉매는 알루미나의 ReO에서27 파생됩니다.
- 의약품의 [8]합성,
균질 촉매 전위
분자 촉매는 다양한 잠재적 [9]응용 프로그램의 준비를 위해 연구되어 왔다.고강도 재료의 제조, 암에 강한 나노 [10]입자의 제조, 재생 가능한 식물성 원료의 모발 및 피부 관리 [11]용품으로의 전환 등이 그것이다.
종류들
올레핀 메타제스의 일부 중요한 클래스는 다음과 같습니다.
메커니즘
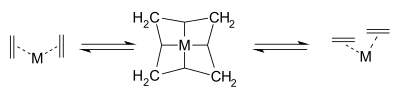
Herison과 Chauvin은 처음으로 전이 금속 알켄 [12]메타제스의 널리 받아들여지는 메커니즘을 제안했다.두 개의 알케인의 직접 [2+2] 사이클로드디션은 공식적으로 대칭이 금지되어 높은 활성화 에너지를 갖는다.Chauvin 메커니즘은 전이 금속 알킬리덴에 대한 알켄 이중 결합의 [2+2] 시클로디션을 통해 금속 사이클로부탄 중간체를 형성한다.생성된 메탈라시클로부탄은 시클로엘리미네이트를 통해 원종 또는 새로운 알켄과 알킬리덴을 얻을 수 있습니다.금속 촉매의 d-오비탈과의 상호작용은 적당한 온도에서 반응이 빠르게 진행될 수 있을 정도로 활성화 에너지를 낮춥니다.
올레핀 메타세시스는 변형되지 않은 알케인에 대한 엔탈피의 변화를 거의 수반하지 않는다.대신 제품 분포는 르 샤틀리에의 원리(엔트로피)에 의해 결정됩니다.
교차 메타세시스 및 링 클로징 메타세시스는 에틸렌 또는 프로필렌의 진화에 의해 구동되며, 이는 기체이기 때문에 시스템에서 제거될 수 있습니다.이러한 이유로 CM 및 RCM 반응은 종종 알파 올레핀을 사용합니다.두 개의 알파-올레핀 CM의 역반응인 에틸렌 분해가 바람직할 수 있지만 용액에서 에틸렌 농도를 높이기 위해서는 에틸렌의 높은 압력이 필요하다.RCM의 역반응(링 개방 메타제스)도 마찬가지로 알파 올레핀(종종 스티렌)이 많이 함유되어 있으면 선호될 수 있습니다.링 개방형 메타제스는 보통 변형된 알켄(종종 노르보르넨)을 포함하며 링 균주의 방출이 반응을 촉진합니다.반대로 링 클로징 메타제스는 일반적으로 엔탈피적으로 유리한 5원 또는 6원 고리의 형성을 수반한다. 그러나 이러한 반응은 앞서 설명한 바와 같이 에틸렌도 진화시키는 경향이 있다.RCM은 더 큰 매크로 사이클을 닫는 데 사용되었으며, 이 경우 [13]고희석 상태에서 반응을 실행함으로써 반응이 동적으로 제어될 수 있습니다.RCM을 통과하는 동일한 기판은 비순환식 디엔 메타세시스(admetesis)를 겪을 수 있으며, ADMET은 고농도로 선호됩니다.더 소프-잉골드 효과는 반응 속도와 제품 선택성을 향상시키기 위해 이용될 수도 있습니다.
크로스메타세스는 2개의 케톤 조각에 대해 알켄을 오존 분해한 후 그 중 하나를 위티그 시약과 반응시키는 절차와 합성적으로 동등하며, 현재 대체되어 있다.
이력 개요
"올레핀 메타제스는 산업의 산물이며, 많은 촉매 작용과 마찬가지로 [1]우연히 발견되었습니다."칼 지글러는 나중에 지글러-나타 촉매 작용으로 알려지게 되는 진행 중인 작업의 일부로 에틸렌이 포화 긴 사슬 탄화수소 대신 1-부텐으로 변환되는 것을 발견했다(니켈 [14]효과 참조).
1960년 Du Pont 연구 그룹은 리튬 알루미늄 테트라헵틸과 테트라클로로티타늄을[15] 사용하여 노르보르넨을 폴리노르보르넨으로 중합했다(이 주제에 대한 이 회사의 특허는 1955년으로[16] 거슬러 올라간다).
그 후 이른바 배위 중합으로 분류되는 반응다음으로 제안된 반응기구에 따르면 RTiX 티타늄 중간체는 파이 착체 내의 이중결합에 대해 우선 좌표를 맞춘다.두 번째 단계는 결합 SNi 반응으로 CC 결합을 깨고 새로운 알킬리덴-티타늄 결합을 형성합니다. 그런 다음 두 번째 단량체로 프로세스가 반복됩니다.
훨씬 후에야 폴리노르보르넨은 고리 개방 메타세시스 중합에 의해 생산될 예정이었다.DuPont의 작업은 Herbert S에 의해 주도되었다. 엘루테리오Giulio Natta는 1964년에 시클로펜텐을 텅스텐과 할로겐화 [17]몰리브덴으로 중합할 때 불포화 폴리머의 형성을 관찰했다.
제3개발 올레 음위 전환하고, 필립스 석유 회사에서 1964[18]의 연구원들은 촉매제 몰리브덴 hexacarbonyl, tungsten hexacarbonyl, 몰리브덴 산화 알루미나에 예를 들어 에틸렌과 2-butene의 이로 인해 그들은 propos 동등한 혼합물에 프로필렌을 지원을 받는 올레핀 불균화 반응을 묘사했다.ed사이클로부탄을 포함하는 반응 메커니즘(이것을 퀘시클로부탄이라고 함) – 금속 착화체:
이 특정 메커니즘은 2년 전에 처음 공식화된 우드워드-호프만 규칙에 따라 대칭성이 금지된다.시클로부탄은 메타제스 반응에서도 확인된 적이 없으며, 이것이 바로 시클로부탄이 빠르게 폐기된 또 다른 이유이다.
1967년 굿이어 타이어 앤 러버 컴퍼니의 닛심 칼데론이 이끄는 연구진은 6염화 텅스텐, 에탄올 및 유기 알루미늄2 화합물인 EtAlMe에 기초한 2-펜틴의 메타세제스를 위한 새로운 촉매 시스템을 설명했습니다.연구진은 이 반응 유형에 대해 올레핀 [19]메타세시스라는 이름을 제안했다.이전에는 이 반응을 "올레핀 불균형"이라고 불렀다.
이 반응에서 2-펜텐은 2-부텐 및 3-헥센과 빠른 화학적 평형을 형성한다.이중 결합 이동은 관찰되지 않으며, 부텐과 헥센에서도 반응을 시작할 수 있으며 메탄올을 첨가함으로써 반응을 멈출 수 있다.
Goodyear 그룹은 정규 2-부텐과 모든 가수분해 등방성 폴리그의 반응에서 중수소가 균등하게 [20]분포된 CHD가 생성되었음을444 입증했다.이러한 방식으로 그들은 트랜스알킬리덴화 메커니즘과 트랜스알킬화 메커니즘(룰 제외)을 구별할 수 있었다.
1971년 쇼빈은 특정 메타세시스 [21]반응에서 발견되는 생성물의 통계적 분포를 설명하기 위해 4원소 금속 중간체를 제안했다.이 메커니즘은 오늘날 올레핀 메타제시스에서 일어나는 실제 메커니즘으로 간주됩니다.
쇼빈의 실험 증거는 시클로펜텐과 2-펜텐이 균질 촉매 텅스텐(VI) 옥시테트라클로로라이드 및 테트라부틸틴과 반응하는 것을 기반으로 했다.
세 가지 주요 제품 C9, C10 및 C11은 변환에 관계없이 1:2:1로 나타납니다.올리고머가 높을수록 같은 비율이 나타난다.초빈은 또한 카벤이 어떻게 형성되는지를 설명했다: 탄소 금속 단결합에서 알파-수소화물을 제거함으로써.예를 들어 프로필렌(C3)은 2-부텐(C4)과 육염화 텅스텐 및 테트라메틸틴(C1)의 반응으로 형성된다.
몇 년 전에 사이클로부타디엔을 합성한 페티트는 같은 해에 독립적으로 경쟁 메커니즘을 [22]고안했다.그것은 다중 3중 2전자 결합을 가진 중심 금속 원자에 연결된 sp 하이브리드 탄소 원자를 가진3 테트라메틸렌 중간체로 구성되었다.
이 메커니즘에 대한 Pett의 실험적 지원은 텅스텐 금속 카르보닐과[23] 4-노넨의 특정 메타제스 반응에서 일산화탄소에 의한 관찰된 반응 억제에 기초했다.
로버트 H. 그럽스는 1972년에 메타세시스(metateshesis)에 관여했고 또한 고리 [24]안에 탄소 원자가 4개인 중간 금속을 제안했다.그가 연구한 그룹은 1,4-딜리시오부탄과 육염화 텅스텐을 반응시켜 중간체를 생성하는 사이클로메틸레네메탈라사이클을 직접 생산하고, 올레핀 메타세시스 반응에서 중간체에 의해 생성된 것과 동일한 제품을 생산하였다.이 메커니즘은 쌍으로 되어 있습니다.
1973년 Grubbs는 이러한 금속 중 하나를 텅스텐이 아닌 백금과 분리함으로써 시스비스(트리페닐포스핀) 디클로로플라티넘(dichlorplatinum)과의 반응에 의해 이 메커니즘에 대한 추가 증거를 발견했다.II)[25]
1975년 Katz는 또한[26] Chauvin이 제안한 것과 일치하는 메탈사이클로부탄 중간체에 도달하여 사이클로옥텐, 2-부텐 및 4-옥텐의 혼합물을 몰리브덴 촉매와 반응시키고 비대칭 C14 탄화수소 반응 생성물이 저환산 시 처음부터 존재함을 관찰하였다.
속도 결정 공정으로서 올레핀 페어링을 가지는 쌍방향 메커니즘 중 하나에서 이 화합물은 C12와 C6의 2차 반응 생성물인 C12와 C16을 형성한 후에 형성된다.
1974년 케이시는 최초로 카르벤을 메타제스 반응 [27]메커니즘에 구현했다.
1976년 Grubbs는 자신의 업데이트된 쌍별 메커니즘에 대한 증거를 제공했다.
4원 사이클 쇼빈 [28][29]메커니즘을 선호하는 또 다른 동위원소 라벨링 연구에서 5원 사이클을 사용한다.
이 반응에서 저환산 시 에틸렌 생성물 )({ (},},0})는 카르벤 메커니즘과 일치하는 것으로 밝혀졌다.한편, Grubbs는 테트라메틸렌 중간체의 가능성을 배제하지 않았다.
최초의 실용적인 메타제스 시스템은 1978년 Tebbe 시약([30]나중에 Tebbe 시약으로 알려짐)을 기반으로 Tebbe에 의해 도입되었습니다.모델 반응에서 이소부텐과 메틸렌시클로헥산의 동위원소 라벨이 부착된 탄소 원자는 다음과 같이 교환됩니다.
그럽스 그룹은 1980년에 제안된 메탈라시클로부탄 중간체를 3-메틸-1-부텐과 [31]함께 분리했다.
그들은 [32]1986년 카프넬렌의 전체 합성에서 유사한 화합물을 분리했다.
같은 해에는 그럽스 그룹 Tebbe의 시약에 의해 반면 슈록에 텅스텐과 몰리브덴은 촉매제에 대한 자신의 연구 초점을 두었다 살아 있는 중합 system[33]고 1년 뒤 그럽스와 슈록 기사를 텅스텐 카르빈 complex[34]와 함께 생활하고 중합을 설명하는 co-published norbornene의 음위 전환 중합을 증명했다. olefin m에타테제스, 그럽스는 루테늄을 기반으로 한 촉매의 개발을 시작했는데, 루테늄은 산소와 물에 덜 민감하고 따라서 기능성 기에 대한 내성이 더 강하다는 것이 증명되었다.
GRUBs 촉매
1960년대와 1970년대에 다양한 그룹은 극성 프로톤 [35][36][37]용제에서 루테늄과 기타 후기 전이 금속의 수화 트리염화물에 의해 촉매된 노르보넨의 고리 개방 중합이 보고되었다.이것은 Robert H. Grubbs와 동료들이 루테늄에 기초한 잘 정의된 기능성 기질 촉매들을 찾도록 자극했다.그럽스 그룹은 루테늄 삼염화물, 오스뮴 삼염화물 및 텅스텐 알킬리덴을 [38]사용하여 7-옥소 노르보넨 유도체를 성공적으로 중합했다.그들은 Ru(II) 카르벤을 효과적인 금속 중심이라고 식별하고 1992년에 루테늄 기반 올레핀 메타세시스 촉매인 (PPH3)2ClRu2=CHCH2=[39]CPH를 최초로 잘 정의된 최초의 올레핀 메타세시스 촉매는 다음과 같습니다.
해당 트리시클로헥실포스핀복합체(PCy3)2ClRu2=CHCH=CPH도2 활성으로 [40]나타났다.이 작업은 현재 상용화된 1세대 Grubbs [41][42]촉매로 정점을 찍었습니다.
슈록 촉매
슈록은 탄탈룸 알킬리덴에 [43]대한 연구의 연장선상에서 1979년에 올레핀 메타세시스 분야에 진출했다.첫 번째 결과는 실망스러운 반응이었다.CpTa(=CH-t-Bu)에틸렌을2 사용한 Cl은 메타세시스 [44]제품이 아닌 메탈사이클로펜탄만 산출했습니다.
단, 이 구조를 PRTa3(CHT-bu)(2Ot-bu)Cl(염화물을 t-부톡시드로 치환하고 시클로펜타디에닐을 유기인산으로 치환)로 조정함으로써 cis-2-펜텐으로 [45]메타세시스를 확립했다.또, W(O)(CHT-Bu)(Cl)(2PET)3형의 텅스텐 옥소 착화체도 유효하다는 것이 [46]판명되었다.
Mo(NAR)(CHC(CH3)2R){OC(CH3)(CH3)(CF)}22형 올레핀 메타세시스용 슈록 알킬리덴이 [47][48]1990년부터 상용화됐다.
최초의 비대칭 촉매는 1993년에[49] 도입되었습니다.
노르보르나디엔 ROMP에서 BINOL 배위자로 변형된 Schrock 촉매를 사용하여 고입체 조절 시스, 등방성 폴리머를 생성합니다.
「 」를 참조해 주세요.
레퍼런스
- ^ a b c Lionel Delaude, Alfred F. Noels (2005). "Metathesis". Kirk-Othmer Encyclopedia of Chemical Technology. Weinheim: Wiley-VCH. doi:10.1002/0471238961.metanoel.a01. ISBN 978-0471238966.
{{cite encyclopedia}}: CS1 maint: 작성자 파라미터 사용(링크) - ^ Astruc D. (2005). "The metathesis reactions: from a historical perspective to recent developments". New Journal of Chemistry. 29 (1): 42–56. doi:10.1039/b412198h. S2CID 98046245.
- ^ "The Nobel Prize in Chemistry 2005" (Press release). Nobelprize.org. 5 October 2005.
- ^ R.R. Schrock (1986). "High-oxidation-state molybdenum and tungsten alkylidene complexes". Accounts of Chemical Research. 19 (11): 342–348. doi:10.1021/ar00131a003.
- ^ Ileana Dragutan; Valerian Dragutan; Petru Filip (2005). "Recent developments in design and synthesis of well-defined ruthenium metathesis catalysts – a highly successful opening for intricate organic synthesis". Arkivoc: 105–129. Archived from the original on 12 May 2006. Retrieved 6 October 2005.
- ^ a b Ghashghaee, Mohammad (2018). "Heterogeneous catalysts for gas-phase conversion of ethylene to higher olefins". Reviews in Chemical Engineering. 34 (5): 595–655. doi:10.1515/revce-2017-0003. S2CID 103664623.
- ^ Klaus Weissermel, Hans-Jurgen Arpe (1997). Industrial Organic Chemistry (3rd ed.). John Wiley & Sons. ISBN 3-527-28838-4.
- ^ McCauley JA, McIntyre CJ, Rudd MT, Nguyen KT, Romano JJ, Butcher JW, Gilbert KF, Bush KJ, Holloway MK, Swestock J, Wan BL, Carroll SS, DiMuzio JM, Graham DJ, Ludmerer SW, Mao SS, Stahlhut MW, Fandozzi CM, Trainor N, Olsen DB, Vacca JP, Liverton NJ (March 2010). "Discovery of vaniprevir (MK-7009), a macrocyclic hepatitis C virus NS3/4a protease inhibitor". Journal of Medicinal Chemistry. 53 (6): 2443–63. doi:10.1021/jm9015526. PMID 20163176.
- ^ Kotha, S; Waghule GT (June 2012). "Diversity Oriented Approach to Crownophanes by Enyne Metathesis and Diels–Alder Reaction as Key Steps". The Journal of Organic Chemistry. 77 (14): 6314–6318. doi:10.1021/jo300766f. PMID 22731677.
- ^ Matson JB, Grubbs RH (2008). "Synthesis of Fluorine-18 Functionalized Nanoparticles for use as in vivo Molecular Imaging Agents" (PDF). Journal of the American Chemical Society. 130 (21): 6731–6733. doi:10.1021/ja802010d. PMID 18452296.
- ^ "Dow Corning and Elevance Announce Partnership to Market Naturally Derived Ingredients in Personal Care Applications" (Press release). Elevance Renewable Sciences. 9 September 2008. Retrieved 19 January 2012.
- ^ Jean-Louis Hérisson, Par; Chauvin, Yves (1971). "Catalyse de transformation des oléfines par les complexes du tungstène. II. Télomérisation des oléfines cycliques en présence d'oléfines acycliques". Die Makromolekulare Chemie (in French). 141 (1): 161–176. doi:10.1002/macp.1971.021410112.
- ^ Sambasivarao Kotha; Kuldeep Singh (2007). "Cross-enyne and ring-closing metathesis cascade: A building-block approach suitable for diversity-oriented synthesis of densely functionalized macroheterocycles with amino acid scaffolds". European Journal of Organic Chemistry. 2007 (35): 5909–5916. doi:10.1002/ejoc.200700744.
- ^ Ziegler, Karl; Holzkamp, E.; Breil, H.; Martin, H. (1955). "Polymerisation von Äthylen und anderen Olefinen". Angewandte Chemie. 67 (16): 426. Bibcode:1955AngCh..67..426Z. doi:10.1002/ange.19550671610.
- ^ Truett, W. L.; Johnson, D. R.; Robinson, I. M.; Montague, B. A. (1960). "Polynorbornene by Coördination Polymerization". Journal of the American Chemical Society. 82 (9): 2337–2340. doi:10.1021/ja01494a057.
- ^ A. W. Anderson and N. G. Merckling, 미국 특허 2,721,189(1955년 10월 18일)
- ^ Natta, G.; Dall'asta, G.; Mazzanti, G. (1964). "Stereospecific Homopolymerization of Cyclopentene". Angewandte Chemie International Edition in English. 3 (11): 723–729. doi:10.1002/anie.196407231.
- ^ Banks, R. L.; Bailey, G. C. (1964). "Olefin Disproportionation. A New Catalytic Process". Industrial & Engineering Chemistry Product Research and Development. 3 (3): 170–173. doi:10.1021/i360011a002.
- ^ Calderon, N; Chen, Hung Yu; Scott, Kenneth W. (1967). "Olefin metathesis – A novel reaction for skeletal transformations of unsaturated hydrocarbons". Tetrahedron Letters. 8 (34): 3327–3329. doi:10.1016/S0040-4039(01)89881-6.
- ^ Calderon, Nissim.; Ofstead, Eilert A.; Ward, John P.; Judy, W. Allen.; Scott, Kenneth W. (1968). "Olefin metathesis. I. Acyclic vinylenic hydrocarbons". Journal of the American Chemical Society. 90 (15): 4133–4140. doi:10.1021/ja01017a039.
- ^ Jean-Louis Hérisson, Par; Chauvin, Yves (1971). "Catalyse de transformation des oléfines par les complexes du tungstène. II. Télomérisation des oléfines cycliques en présence d'oléfines acycliques". Die Makromolekulare Chemie. 141 (1): 161–176. doi:10.1002/macp.1971.021410112.
- ^ S. Lewandos, G; Pettit, R. (1971). "A proposed mechanism for the metal-catalysed disproportionation reaction of olefins". Tetrahedron Letters. 12 (11): 789–793. doi:10.1016/S0040-4039(01)96558-X.
- ^ Lewandos, Glenn S.; Pettit, R. (1971). "Mechanism of the metal-catalyzed disproportionation of olefins". Journal of the American Chemical Society. 93 (25): 7087–7088. doi:10.1021/ja00754a067.
- ^ Grubbs, Robert H.; Brunck, Terence K. (1972). "Possible intermediate in the tungsten-catalyzed olefin metathesis reaction". Journal of the American Chemical Society. 94 (7): 2538–2540. doi:10.1021/ja00762a073.
- ^ Biefeld, Carol G.; Eick, Harry A.; Grubbs, Robert H. (1973). "Crystal structure of bis(triphenylphosphine)tetramethyleneplatinum(II)". Inorganic Chemistry. 12 (9): 2166–2170. doi:10.1021/ic50127a046.
- ^ Katz, Thomas J.; McGinnis, James (1975). "Mechanism of the olefin metathesis reaction". Journal of the American Chemical Society. 97 (6): 1592–1594. doi:10.1021/ja00839a063.
- ^ Casey, Charles P.; Burkhardt, Terry J. (1974). "Reactions of (diphenylcarbene)pentacarbonyltungsten(0) with alkenes. Role of metal-carbene complexes in cyclopropanation and olefin metathesis reactions". Journal of the American Chemical Society. 96 (25): 7808–7809. doi:10.1021/ja00832a032.
- ^ Grubbs, Robert H.; Burk, Patrick L.; Carr, Dale D. (1975). "Mechanism of the olefin metathesis reaction". Journal of the American Chemical Society. 97 (11): 3265–3267. doi:10.1021/ja00844a082.
- ^ Grubbs, Robert H.; Carr, D. D.; Hoppin, C.; Burk, P. L. (1976). "Consideration of the mechanism of the metal catalyzed olefin metathesis reaction". Journal of the American Chemical Society. 98 (12): 3478–3483. doi:10.1021/ja00428a015.
- ^ Tebbe, F. N.; Parshall, G. W.; Reddy, G. S. (1978). "Olefin homologation with titanium methylene compounds". Journal of the American Chemical Society. 100 (11): 3611–3613. doi:10.1021/ja00479a061.
- ^ Howard, T. R.; Lee, J. B.; Grubbs, R. H. (1980). "Titanium metallacarbene-metallacyclobutane reactions: stepwise metathesis". Journal of the American Chemical Society. 102 (22): 6876–6878. doi:10.1021/ja00542a050.
- ^ Stille, John R.; Grubbs, Robert H. (1986). "Synthesis of (.+-.)-.DELTA.9,12-capnellene using titanium reagents". Journal of the American Chemical Society. 108 (4): 855–856. doi:10.1021/ja00264a058.
- ^ Gilliom, Laura R.; Grubbs, Robert H. (1986). "Titanacyclobutanes derived from strained, cyclic olefins: the living polymerization of norbornene". Journal of the American Chemical Society. 108 (4): 733–742. doi:10.1021/ja00264a027.
- ^ Schrock, R. R.; Feldman, J.; Cannizzo, L. F.; Grubbs, R. H. (1987). "Ring-opening polymerization of norbornene by a living tungsten alkylidene complex". Macromolecules. 20 (5): 1169–1172. Bibcode:1987MaMol..20.1169S. doi:10.1021/ma00171a053.
- ^ Michelotti, Francis W.; Keaveney, William P. (1965). "Coordinated Polymerization of the Bicyclo-(2.2.1)-heptene-2 Ring System (Norbornene) in Polar Media". Journal of Polymer Science Part A: General Papers. 3 (3): 895–905. doi:10.1002/pol.1965.100030305.
- ^ Rinehart, Robert E.; Smith, Homer P. (1965). "The Emulsion Polymerization of the Norbornene Ring System Catalyzed by Noble Metal Compounds". Journal of Polymer Science Part B: Polymer Letters. 3 (12): 1049–1052. Bibcode:1965JPoSL...3.1049R. doi:10.1002/pol.1965.110031215.
- ^ Porri, Lido; Rossi, Renzo; Diversi, Pietro; Lucherini, Antonio (1974). "Ring-Opening Polymerization of Cycloolefins with Catalysts Derived from Ruthenium and Iridium". Die Makromolekulare Chemie. 175 (11): 3097–3115. doi:10.1002/macp.1974.021751106.
- ^ Novak, Bruce M.; Grubbs, Robert H. (1988). "The ring opening metathesis polymerization of 7-oxabicyclo[2.2.1]hept-5-ene derivatives: a new acyclic polymeric ionophore". Journal of the American Chemical Society. 110 (3): 960–961. doi:10.1021/ja00211a043.
- ^ Nguyen, Sonbinh T.; Johnson, Lynda K.; Grubbs, Robert H.; Ziller, Joseph W. (1992). "Ring-opening metathesis polymerization (ROMP) of norbornene by a Group VIII carbene complex in protic media" (PDF). Journal of the American Chemical Society. 114 (10): 3974–3975. doi:10.1021/ja00036a053.
- ^ Nguyen, Sonbinh T.; Grubbs, Robert H.; Ziller, Joseph W. (1993). "Syntheses and activities of new single-component, ruthenium-based olefin metathesis catalysts". Journal of the American Chemical Society. 115 (21): 9858–9859. doi:10.1021/ja00074a086.
- ^ Schwab, Peter; France, Marcia B.; Ziller, Joseph W.; Grubbs, Robert H. (1995). "A Series of Well-Defined Metathesis Catalysts–Synthesis of [RuCl2(CHR′)(PR3)2] and Its Reactions". Angewandte Chemie International Edition in English. 34 (18): 2039–2041. doi:10.1002/anie.199520391.
- ^ Schwab, Peter; Grubbs, Robert H.; Ziller, Joseph W. (1996). "Synthesis and Applications of RuCl2(=CHR')(PR3)2: The Influence of the Alkylidene Moiety on Metathesis Activity". Journal of the American Chemical Society. 118: 100–110. doi:10.1021/ja952676d.
- ^ Schrock, R. R.; Meakin, P. (1974). "Pentamethyl complexes of niobium and tantalum". Journal of the American Chemical Society. 96 (16): 5288–5290. doi:10.1021/ja00823a064.
- ^ McLain, S. J.; Wood, C. D.; Schrock, R. R. (1979). "Preparation and characterization of tantalum(III) olefin complexes and tantalum(V) metallacyclopentane complexes made from acyclic α olefins". Journal of the American Chemical Society. 101 (16): 4558–4570. doi:10.1021/ja00510a022.
- ^ Schrock, R; Rocklage, Scott; Wengrovius, Jeffrey; Rupprecht, Gregory; Fellmann, Jere (1980). "Preparation and characterization of active niobium, tantalum and tungsten metathesis catalysts". Journal of Molecular Catalysis. 8 (1–3): 73–83. doi:10.1016/0304-5102(80)87006-4.
- ^ Wengrovius, Jeffrey H.; Schrock, Richard R.; Churchill, Melvyn Rowen; Missert, Joseph R.; Youngs, Wiley J. (1980). "Multiple metal-carbon bonds. 16. Tungsten-oxo alkylidene complexes as olefins metathesis catalysts and the crystal structure of W(O)(CHCMe3(PEt3)Cl2". Journal of the American Chemical Society. 102 (13): 4515–4CF6. doi:10.1021/ja00533a035.
- ^ Schrock, Richard R.; Murdzek, John S.; Bazan, Gui C.; Robbins, Jennifer; Dimare, Marcello; O'Regan, Marie (1990). "Synthesis of molybdenum imido alkylidene complexes and some reactions involving acyclic olefins". Journal of the American Chemical Society. 112 (10): 3875–3886. doi:10.1021/ja00166a023.
- ^ Bazan, Guillermo C.; Oskam, John H.; Cho, Hyun Nam; Park, Lee Y.; Schrock, Richard R. (1991). "Living Ring-Opening Metathesis Polymerization of 2,3-Difunctionalized 7-Oxanorbornenes and 7-Oxanorbornadienes by Mo(CHCMe2R)(N-2,6-C6H3-i-Pr2)(O-t-Bu)2 and Mo(CHCMe2R)(N-2,6-C6H3-i-Pr2)(OCMe2CF3)2". 113 (18): 6899–6907. doi:10.1021/ja00018a028.
{{cite journal}}:Cite 저널 요구 사항journal=(도움말) - ^ McConville, David H.; Wolf, Jennifer R.; Schrock, Richard R. (1993). "Synthesis of chiral molybdenum ROMP initiators and all-cis highly tactic poly(2,3-(R)2norbornadiene) (R = CF3 or CO2Me)". Journal of the American Chemical Society. 115 (10): 4413–4414. doi:10.1021/ja00063a090.
추가 정보
- "Olefin Metathesis: Big-Deal Reaction". 80 (51). 2002: 29–33. doi:10.1021/cen-v080n016.p029.
{{cite journal}}:Cite 저널 요구 사항journal=(도움말) - "Olefin Metathesis: The Early Days". 80 (51). 2002: 34–38. doi:10.1021/cen-v080n029.p034.
{{cite journal}}:Cite 저널 요구 사항journal=(도움말) - Schrock, R. R. (1990). "Living ring-opening metathesis polymerization catalyzed by well-characterized transition-metal alkylidene complexes". Accounts of Chemical Research. 23 (5): 158–165. doi:10.1021/ar00173a007.
- Schrock, R. R.; Hoveyda, A. H. (2003). "Molybdenum and Tungsten Imido Alkylidene Complexes as Efficient Olefin-Metathesis Catalysts". Angewandte Chemie International Edition. 42 (38): 4592–4633. doi:10.1002/anie.200300576. PMID 14533149. S2CID 35370749.
- Samojłowicz, C.; Grela, K. (2009). "Ruthenium-Based Olefin Metathesis Catalysts Bearing N-Heterocyclic Carbene Ligands". Chemical Reviews. 109 (8): 3708–3742. doi:10.1021/cr800524f. PMID 19534492.
- Vougioukalakis, G. C.; Grubbs, R. H. (2010). "Ruthenium-Based Heterocyclic Carbene-Coordinated Olefin Metathesis Catalysts". Chemical Reviews. 110 (3): 1746–1787. doi:10.1021/cr9002424. PMID 20000700. S2CID 4589661.
- Trnka, T. M.; Grubbs, R. H. (2001). "The Development of L2X2Ru=CHR Olefin Metathesis Catalysts: An Organometallic Success Story". Accounts of Chemical Research. 34 (1): 18–29. doi:10.1021/ar000114f. PMID 11170353. S2CID 22145255.
- Grubbs, R. H.; Chang, S. (1998). "Recent advances in olefin metathesis and its application in organic synthesis". Tetrahedron. 54 (18): 4413–4450. doi:10.1016/S0040-4020(97)10427-6.
- Grubbs, R. H. (2004). "Olefin metathesis". Tetrahedron. 60 (34): 7117–7140. doi:10.1016/j.tet.2004.05.124.
- Grela, K. (2010). Grela, K. (ed.). "Progress in metathesis chemistry (Editorial for Open Access Thematic Series)". Beilstein Journal of Organic Chemistry. 6: 1089–1090. doi:10.3762/bjoc.6.124. PMC 3002079. PMID 21160917.