사이클로드디션
Cycloaddition사이클로드디션은 "두 개 이상의 불포화 분자(또는 동일한 분자의 일부)가 결합 다중성의 순 감소가 있는 순환 부가물의 형성과 결합하는 화학 반응이다.결과적으로 발생하는 반응은 환화 반응이다.모든 사이클로드 디케이션이 일치하는 것은 아니지만 많은 사이클로드 디케이션이 결합되어 있어 순환적입니다.[1]인증되지 않은 사이클로드 조건은 주순환 [2]상태가 아닙니다.부가 반응의 한 종류로서, 사이클로드 디젼은 친핵체나 전자 친위체를 사용하지 않고도 탄소-탄소 결합을 형성할 수 있다.
사이클로드 조건은 두 가지 표기법을 사용하여 설명할 수 있습니다.더 오래되었지만 여전히 일반적인 표기법은 반응 물질에 있는 원자의 선형 배열 크기에 기초합니다.괄호(i + j + ...)를 사용합니다.여기서 변수는 각 반응물질의 선형 원자의 수입니다.제품의 사이즈는 사이클(i+j+...)입니다.본 발명의 시스템에서 표준 다이엘스-알더 반응은 (4+2)-시클로디션이며, 1,3-디폴라 시클로디션은 알켄 a(2+1)-[1]시클로디션인 카르벤의 (3+2)-시클로피네이션이다.
보다 최근의 IUPAC 선호 표기법은 Woodward와 Hoffmann에 의해 처음 도입되었으며, 각 괄호를 사용하여 제품의 형성에 관여하는 탄소 원자가 아닌 전자 수를 나타냅니다.[i + j + ...] 표기법에서 표준 Diels-Alder 반응은 [4 + 2]-사이클로드디션이며, 1,3-다이폴라 사이클로드디션은 [4 + 2]-[1]사이클로드디션이기도 합니다.
열순환 및 그 입체화학
열 사이클로드디션은 반응물이 지면 전자 상태에 있는 사이클로드디션입니다.이들은 보통 (4n + 2) µ의 전자가 시작 물질에 참여하며, 일부 정수 n에 대해 있습니다.이러한 반응은 대부분의 경우 초안면-초안면(syn/syn 입체 화학)에서 궤도 대칭의 이유로 발생합니다.남극-대-대-아프리카(반/반입체화학) 반응의 극히 일부 사례도 보고되었다.4n µ 전자를 갖는 열 사이클로드디션의 몇 가지 예가 있습니다(예: [2 + 2]-사이클로드디션).이러한 반응은 [2s + 2a]로 π분석하더라도 p 오비탈의 직교 세트가 교차 전이 상태를 통해 반응이 진행되도록 하는 케틴과 알렌 유도체의 사이클로드 디션 반응과 같은 초안면-반입체 화학(syn/anti sterechemistry)으로 진행된다.트랜스-시클로헵텐 유도체와 같은 변형 알켄도 [2 + 2]-시클로디션 반응에서 남극면 방식으로 반응하는 것으로 보고되었다.
Doering은 (Woodward와 개인적인 통신에서) 헵타풀발렌과 테트라시아노에틸렌이 안면외반대아면 [14 + 2]-사이클로드 디지션에서 반응할 수 있다는 것을 발견했다.이 결과는 나중에 Erden과 Kaufmann에 의해 확인되고 확장되었으며, Erden과 Kaufmann은 N-페닐트리아졸리네디온과 [3]함께 헵타풀발렌의 초안면-안면 시클로디션을 보고했다.
광화학 사이클로드 디케이션 및 그 입체화학
광화학 활성화를 통해 4nµ 전자가 참여하는 사이클로드 현상도 발생할 수 있다.여기서 한 성분은 HOMO(δ결합)에서 LUMO(δ*항결합)로 촉진되는 전자를 가진다.그러면 궤도 대칭은 반응이 초면-초면 방식으로 진행될 수 있습니다.예를 들어 DeMayo 반응이 있습니다.또 다른 예는 [4]계피산의 광화학 이량화이다.두 개의 트랜스 알케인은 서로 마주보고 반응하며, 분리된 이성질체를 트룩실산이라고 합니다.
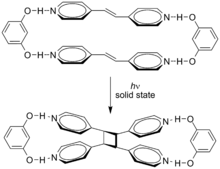
초분자 효과는 이러한 사이클로드 상태에 영향을 미칠 수 있습니다.트랜스-1,2-비스(4-피리딜)에텐의 시클로디션은 100% [5]수율에서 레조르시놀에 의해 유도된다.
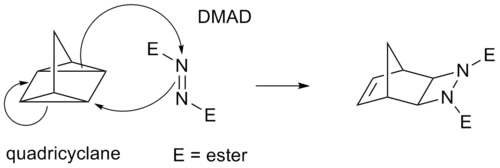
δ 결합 대신 일부 사이클로드디션은 δ 특성이 유의하기 때문에 변형된 사이클로프로판 고리를 통해 작동한다.예를 들어 Diels-Alder 반응의 아날로그는 4중 시크레인-DMAD 반응입니다.
(i+j+)로...cycloaddition 표기법 i와 j는 cycloaddition에 관여하는 원자의 수를 나타냅니다.이 표기법에서 Diels-Alder 반응은 (4+2)환부하량이고, 오존분해에서의 첫 단계와 같은 1,3-극첨가는 (3+2)환부하량이다.그러나 IUPAC는 [i+j+...]를 사용하는 표기법을 선호합니다.]는 원자가 아닌 전자를 고려합니다.이 표기법에서 DA 반응과 쌍극 반응은 모두 [4+2]사이클로드디션이 됩니다.노르보르나디엔과 활성 알킨 사이의 반응은 [2+2+2] 사이클로드 용량이다.
사이클로드 디케이션의 종류
디엘스-알더 반응
Diels-Alder 반응은 아마도 가장 중요하고 일반적으로 학습되는 사이클로드디션 반응이다.공식적으로는 [4+2] 사이클로드디션 반응이며, 역전자 요구 Diels-Alder 반응, 헥사데히드로 Diels-Alder 반응 및 관련 알킨 삼량화 등 다양한 형태로 존재한다.이 반응은 역방향-Diels-Alder 반응에서도 역방향으로 실행될 수 있다.
아자-딜-알더 반응과 이민-딜-알더 반응을 포함한 헤테로아톰과 관련된 반응들이 알려져 있다.
위스겐 사이클로드 디케이션
Huisgen 시클로디션 반응은 (2+3)시클로디션이다.
니트론-올레핀 환산
니트론-올레핀 시클로디션은 (3+2) 시클로디션입니다.
텔레트로피 반응
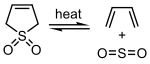
Celletropic 반응은 순환 부하의 하위 클래스이다.화학반응의 주요 특징 중 하나는 시약 중 하나에서 두 개의 새로운 결합이 동일한 원자에 만들어지고 있다는 것입니다.전형적인 예는 이산화황과 디엔의 반응이다.
다른.
다른 사이클로드디션 반응으로는 [4+3] 사이클로드디션, [6+4] 사이클로드디션, [2+2] 광사이클로드디션, 금속 중심 사이클로드디션 및 [4+4] 광사이클로드디션 등이 있습니다.
정식 사이클로드 조건
사이클로드디션은 종종 금속 촉매 및 단계적 래디칼 유사체를 가지지만, 엄밀하게 말하면 주순환 반응은 아니다.시클로디션 하전 또는 래디컬 중간체가 관여하거나 일련의 반응 단계에서 시클로디션 결과를 얻었을 때 실제 주순환 시클로디션과 구별하기 위해 형식 시클로디션이라고 부르기도 한다.
n-부틸리튬에 의해 촉매되는 고리형 에논과 에나민 사이의 공식 [3+3] 사이클로드량의 한 예는 황새 에나민 / 1,2-첨가 캐스케이드 [6]반응이다.
철촉매 2+2 올레핀 사이클로드디션
IronDiminopyridine 촉매는 중심 철 원자가 2개의 단순하고 기능화되지 않은 올레핀 이중 결합과 배위할 수 있는 레독스 활성 배위자를 포함한다.촉매는 II 산화 상태의 중심 철 원자와 짝을 이루지 않은 전자를 포함하는 구조와 0 산화 상태의 철 사이의 공진이라고 할 수 있습니다.이를 통해 C-C 환원 제거를 통해 사이클로부탄 구조를 생성하고, 또는 베타 수소 제거를 통해 사이클로부텐 구조를 생성하면서 이중 결합에 관여할 수 있는 유연성을 얻을 수 있다.반응 효율은 사용되는 알켄에 따라 크게 다르지만 합리적인 리간드 설계를 통해 [7][8]촉매될 수 있는 반응 범위를 확장할 수 있다.
레퍼런스
- ^ a b c "cycloaddition", IUPAC Compendium of Chemical Terminology, IUPAC, 2009, doi:10.1351/goldbook.C01496, ISBN 978-0-9678550-9-7, retrieved 2018-10-13
- ^ "pericyclic reaction", IUPAC Compendium of Chemical Terminology, IUPAC, 2009, doi:10.1351/goldbook.P04491, ISBN 978-0-9678550-9-7, retrieved 2018-10-13
- ^ Erden, Ihsan; KauFmann, Dieter (1981-01-01). "Cycloadditionsreaktionen des heptafulvalens". Tetrahedron Letters (in German). 22 (3): 215–218. doi:10.1016/0040-4039(81)80058-5. ISSN 0040-4039.
- ^ Hein, Sara M. (June 2006). "An Exploration of a Photochemical Pericyclic Reaction Using NMR Data". Journal of Chemical Education. 83 (6): 940–942. Bibcode:2006JChEd..83..940H. doi:10.1021/ed083p940.
- ^ L. R. MacGillivray; J. L. Reid; J. A. Ripmeester (2000). "Supramolecular Control of Reactivity in the Solid State Using Linear Molecular Templates". J. Am. Chem. Soc. 122 (32): 7817–7818. doi:10.1021/ja001239i.
- ^ Movassaghi, Mohammad; Bin Chen (2007). "Stereoselective Intermolecular Formal [3+3] Cycloaddition Reaction of Cyclic Enamines and Enones". Angew. Chem. Int. Ed. 46 (4): 565–568. doi:10.1002/anie.200603302. PMC 3510678. PMID 17146819.
- ^ Jordan M. Hoyt; Valeria A. Schmidt; Aaron M. Tondreau; Paul J. Chirik (2015-08-28). "Iron-catalyzed intermolecular [2+2] cycloadditions of unactivated alkenes". Science. 349 (6251): 960–963. Bibcode:2015Sci...349..960H. doi:10.1126/science.aac7440. PMID 26315433.
- ^ Myles W. Smith; Phil S. Baran (2015-08-28). "As simple as [2+2]". Science. 349 (6251): 925–926. Bibcode:2015Sci...349..925S. doi:10.1126/science.aac9883.


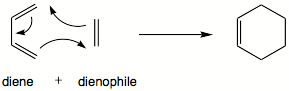


![Intermolecular Formal [3+3] Cycloaddition Reaction](http://upload.wikimedia.org/wikipedia/commons/thumb/2/26/3%2B3-cycloaddition.svg/600px-3%2B3-cycloaddition.svg.png)


