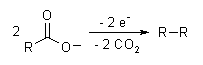콜베 전기 분해
Kolbe electrolysis그 마리아 콜베 전기 분해나 마리아 콜베 반응은 하나의 유기적 반응 헤르만 콜베의 이름을 딴 것이다.[1]두개의 카복실산 향료 또는 중간 염료의 제조(또는 이온 카르복시산염)의 마리아 콜베 반응은 공식적으로decarboxylative dimerisation.전체적인 반응:
만약 두개의 다른 carboxylates의 혼합물을 사용하고 있다면, 그들의 모든 조합이 일반적으로 유기농 제품 구조: 보인다.
- 3R1COO−+3R2COO− → R1−R1+R1−R2+R2−R2+6이산화 탄소 6e− 및.
이 반응 메커니즘:전기 화학 카르복시 이탈은 공유 결합을 형성할 수 근본적인 intermediate,을 주는 이단 급진적인 과정이 수반된다.[2]한 예로 아세트 산은 에탄과 이산화 탄소의 전기 분해:.
- CH3COOH → CH3COO− → CH3COO· → CH3·+CO2.
- 2CH3· → CH3CH3
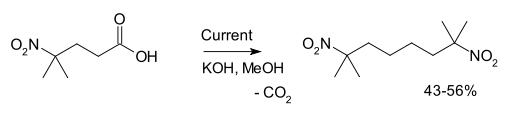
2,7-dimethyl-2,7-dinitrooctane의4-methyl-4-nitrovaleric 산성:[3]에서 또 다른 예는 합성.
추가 정보
- Kolbe, Hermann (1848). "Zersetzung der Valeriansäure durch den elektrischen Strom" [Decomposition of valeric acid by an electric current]. Annalen der Chemie und Pharmacie. 64 (3): 339–341. doi:10.1002/jlac.18480640346.
- Kolbe, Hermann (1849). "Untersuchungen über die Elektrolyse organischer Verbindungen" [Investigations of the electrolysis of organic compounds]. Annalen der Chemie und Pharmacie. 69 (3): 257–294. doi:10.1002/jlac.18490690302.
「 」를 참조해 주세요.
레퍼런스
- ^ Utley, James (1997). "Trends in Organic Electrosynthesis". Chemical Society Reviews. 26 (3): 157. doi:10.1039/cs9972600157.
- ^ Vijh, A. K.; Conway, B. E. (1967). "Electrode Kinetic Aspects of the Kolbe Reaction". Chem Rev. 67 (6): 623–664. doi:10.1021/cr60250a003.
- ^ 샤키는 W.H.;Langkammerer, CM.(1973년)."2,7-Dimethyl-2,7-dinitrooctane".유기 Syntheses.;집단적인 볼륨, 5vol. 페이지의 주는 445.
외부 링크
- "Kolbe Electrolysis". Organic Chemistry Portal. Retrieved 22 October 2007.