알돌 응축
Aldol condensation| 알돌 응축 | |
|---|---|
| 반응형 | 결합 반응 |
| 식별자 | |
| 유기화학 포털 | 알돌의 개재에 의한 |
| RSC 온톨로지 ID | RXNO:0000017 |
알돌축합이란 유기화학에서 에놀 또는 에놀라트이온이 카르보닐화합물과 반응하여 β-히드록시알데히드 또는 β-히드록시케톤(알돌반응)을 형성한 후 탈수하여 켤레 에논을 생성하는 축합반응이다.
알돌 축합은 탄소-탄소 [1][2][3][4]결합을 형성하는 방법으로서 유기 합성과 생화학에서 중요하다.
통상적인 형태에서는 알데히드에 케톤 에놀라트를 친핵적으로 첨가하여 β-히드록시 케톤, 즉 알돌(알데히드+알코올)[5][6][7]을 형성한다.
알돌 응축이라는 이름도 알돌라아제에 의해 촉매되는 과정의 첫 번째 단계인 알돌 반응 자체를 지칭하기 위해 특히 생화학에서 일반적으로 사용된다.그러나 알돌 반응은 작은 분자의 손실을 수반하지 않기 때문에 형식적으로는 응축 반응이 아니다.
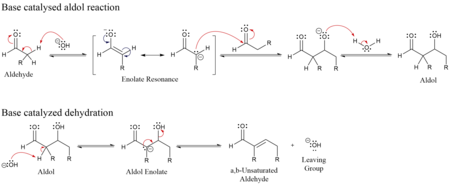
메커니즘
이 반응의 첫 번째 부분은 알돌 반응이고, 두 번째 부분은 탈수-제거 반응입니다(물 분자 또는 알코올 분자의 제거 포함).탈수는 활성 카르복실기가 존재할 때 탈탄산을 수반할 수 있다.알돌 첨가 생성물은 두 가지 메커니즘을 통해 탈수될 수 있습니다. 즉, t-부톡사이드 칼륨, 수산화칼륨 또는 수소화 나트륨과 같은 강한 염기는 에놀라트로 제품을 탈양성자로 만들고, 에놀라트는 [8][9]E1cB 메커니즘을 통해 제거되며, 산에서의 탈수는 E1 반응 메커니즘을 통해 진행됩니다.원하는 제품의 성질에 따라 알돌 축합은 운동 제어 또는 열역학 [10]제어의 두 가지 광범위한 조건에서 수행될 수 있다.
 |  |
| 애니메이션, Cataly | 애니메이션, 산촉매 |
교차 알돌 응축
교차 알돌 축합은 α-수소를 함유하는 2개의 이종 카르보닐 화합물이 알돌 축합된 결과이다.일반적으로 카르보닐 화합물 중 하나가 친핵체로 작용할 수 있고 자가 응축이 가능해 합성적으로 쓸모없는 혼합물을 만들 수 있기 때문에 4가지 가능한 생성물로 이어진다.그러나 화합물 중 하나가 α-수소를 포함하지 않아 분해할 수 없는 경우 이 문제를 피할 수 있다.알데히드와 케톤의 알돌축합에서 케톤은 +I효과와 입체장애에 의해 카르보닐카본이 높은 친전자성을 가지지 않기 때문에 친핵체로서 작용한다.보통 크로스 제품이 주요 상품입니다.먼저 적절한 베이스와 케톤의 혼합물을 조제하고 나서 해당 반응 혼합물에 천천히 알데히드를 첨가함으로써 알데히드로부터의 셀프알돌 생성물의 미량을 허용할 수 있다.너무 농축된 염기를 사용하면 경쟁적인 카니자로 [11]반응을 일으킬 수 있습니다.
응결 타입
알돌 축합은 카르보닐 화합물의 다른 부가 반응과 구별하는 것이 중요하다.
- 염기가 아민이고 활성 수소 화합물이 충분히 활성화되면 이 반응을 Knoevenagel 응축이라고 한다.
- Perkin 반응에서 알데히드는 방향족이며 무수물로부터 생성되는 에놀라트는 방향족이다.
- α-수소를 가진 알데히드 또는 케톤과 α-수소가 결핍된 방향족 카르보닐 화합물 사이의 클라이젠-슈미트 응축.
- 클라이젠 응축은 두 가지 에스테르 화합물을 포함한다.
- 디크만 응축은 동일한 분자에 두 개의 에스테르 그룹을 포함하며 순환 분자를 생성한다.
- 헨리 반응은 알데히드와 지방족 니트로 화합물을 포함한다.
- 로빈슨환에는 알돌축합 [2]전에 먼저 마이클반응에 관여하는 α,β-불포화케톤 및 카르보닐기가 포함된다.
- 게베트 반응에서는 알코올로부터 제자리 알데히드가 스스로 응축되어 이량화된 알코올이 됩니다.
- Japp-Maitland 응축수는 제거 반응이 아닌 친핵성 변위에 의해 제거된다.
예
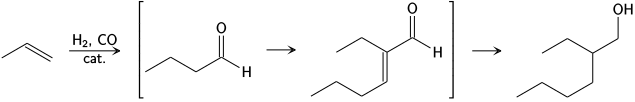
Royal Dutch Shell과 Exson이 개발한 Aldox 공정에서 프로펜과 신가스를 하이드로포메이션에서 부티알데히드로, 알돌 축합에서 2-에틸헥세날로,[12] 마지막으로 수소화를 통해 2-에틸헥산올로 변환한다.
아세트알데히드와 포름알데히드가 교차한 알돌축합과 3당량의 포름알데히드로부터 펜타에리톨을 대량으로 제조하여 펜타에리트로스를 얻을 수 있으며, 이 펜타에리톨은 카니자로 [13]반응으로 더욱 저감된다.
범위
에틸 2-메틸아세테이트와 캄폴렌 알데히드는 알돌 [14]축합에서 반응한다.합성[15] 절차는 이러한 유형의 반응에 대해 일반적으로 사용됩니다.이 과정에서 탈탄산화 시에는 물 외에 에탄올과 이산화탄소의 상당량이 손실된다.
에틸글리옥실산2 및 글루타콘산(디에틸-2-메틸펜트-2-에네디오산)1은 이소프렌메트릭카르본산3(이소프렌(2-메틸부타-1,3-디엔) 골격)과 에톡사이드나트륨으로 반응한다.이 반응 생성물은 이산화탄소의 초기 손실과 함께 매우 불안정하며 많은 2차 반응이 뒤따른다.이는 시스 디에노이드 [16]구조에서 메틸기와 카르본기로부터 발생하는 스테릭 균주 때문인 것으로 생각된다.
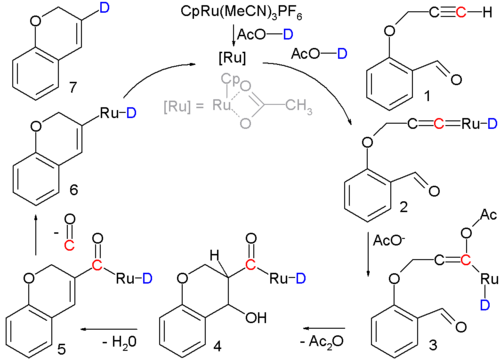
때때로 다음 예시와 같이 알돌 응축이 다단계 반응 또는 촉매 사이클에 묻힙니다.[17]
이 반응에서 알킬1은 루테늄 촉매에 의해 사이클로알켄7로 변환되어 실제 축합은 중간 3~5로 이루어진다.반응 메커니즘에 대한 지원은 동위원소 [18]라벨링에 기초한다.
멘톤(2S,5R)-2-이소프로필-5-메틸시클로헥사논)과 아니살알데히드(4-메톡시벤츠알데히드)의 반응은 케톤기의 입체 차폐로 인해 복잡하다.이 장애물은 [19]다음 반응에서 수산화칼륨과 같은 강한 염기 및 DMSO와 같은 극성 용매를 사용함으로써 극복됩니다.
제품은 공통 중간체(에놀레이트 A)를 통해 에피머라이징하여 원래(S,R) 에피머와 (R,R) 에피머를 변환할 수 있습니다.(R,R) 제품은 반응용매에 불용성인 반면 (S,R) 제품은 용해성이다.(R,R) 생성물의 침전에 의해 에피머화 평형 반응이 일어나 주요 생성물로 형성된다.
「 」를 참조해 주세요.
레퍼런스
- ^ Smith, M. B.; March, J. (2001). Advanced Organic Chemistry (5th ed.). New York: Wiley Interscience. pp. 1218–1223. ISBN 0-471-58589-0.
- ^ a b Carey, Francis A.; Sundberg, Richard J. (1993). Advanced Organic Chemistry Part B Reactions and Synthesis (3rd ed.). New York, NY: Plenum. pp. 55. ISBN 0-306-43440-7.
- ^ Wade, L. G. (2005). Organic Chemistry (6th ed.). Upper Saddle River, NJ: Prentice Hall. pp. 1056–1066. ISBN 0-13-236731-9.
- ^ Mahrwald, R. (2004). Modern Aldol Reactions. Vol. 1, 2. Weinheim, Germany: Wiley-VCH. pp. 1218–1223. ISBN 3-527-30714-1.
- ^ Heathcock, C. H. (1991). Additions to C-X π-Bonds, Part 2. Comprehensive Organic Synthesis. Selectivity, Strategy and Efficiency in Modern Organic Chemistry. Vol. 2. Oxford: Pergamon. pp. 133–179. ISBN 0-08-040593-2.
- ^ Mukaiyama T. (1982). "The Directed Aldol Reaction". Organic Reactions. 28: 203–331. doi:10.1002/0471264180.or028.03. ISBN 0471264180.
- ^ Paterson, I. (1988). "New Asymmetric Aldol Methodology Using Boron Enolates". Chemistry and Industry. London: Paterson Group. 12: 390–394.
- ^ Nielsen, A. T.; Houlihan., W. J. (1968). "The Aldol Condensation". Organic Reactions. 16: 1–438. doi:10.1002/0471264180.or016.01. ISBN 0471264180.
- ^ Perrin, C. L.; Chang, K. L. (2016). "The Complete Mechanism of an Aldol Condensation". J. Org. Chem. 81 (13): 5631–5. doi:10.1021/acs.joc.6b00959. PMID 27281298.
- ^ Carey, Francis A.; Sundberg, Richard J. (1993). Advanced Organic Chemistry Part A: Structure and Mechanisms (3rd ed.). New York, N.Y.: Plenum. pp. 458. ISBN 0-306-43440-7.
- ^ Sanyal, S.N. (2003). Reactions, Rearrangements and Reagents (4th ed.). Daryagunj, New Delhi: Bharati Bhavan Publishers (P&D). p. 80. ISBN 978-81-7709-605-7.
- ^ 예를들면,BG 881979
- ^ Schurink, H. B. J. (1925). "Pentaerythritol". Organic Syntheses. 4: 53. doi:10.15227/orgsyn.004.0053.; Collective Volume, vol. 1, p. 425
- ^ Badía, C.; Castro, J. M.; Linares-Palomino, P. J.; Salido, S.; Altarejos, J.; Nogueras, M.; Sánchez, A. (2004). "(E)-6-(2,2,3-Trimethyl-cyclopent-3-enyl)-hex-4-en-3-one". Molbank. 2004 (1): M388. doi:10.3390/M388.
- ^ 다이옥산 중 수소화나트륨 교반액에 2-메틸아세테이트(2)를 첨가한다.그런 다음 캄폴렌성 알데히드(1)를 첨가하고 혼합물을 15시간 동안 역류시킨다.그리고 2N 염산을 첨가하여 디에틸에테르로 추출한다.복합 유기층은 2N 염산, 포화 중탄산나트륨, 브라인으로 세척한다.유기상을 무수황산나트륨으로 건조시킨 후 감압상태에서 용매가 증발하여 진공증류에 의해 정제된 잔류물이 생성되어 3(58%)이 된다.
- ^ Goren, M. B.; Sokoloski, E. A.; Fales, H. M. (2005). "2-Methyl-(1Z,3E)-butadiene-1,3,4-tricarboxylic Acid, "Isoprenetricarboxylic Acid"". Journal of Organic Chemistry. 70 (18): 7429–7431. doi:10.1021/jo0507892. PMID 16122270.
- ^ Varela, J. A.; Gonzalez-Rodriguez, C.; Rubin, S. G.; Castedo, L.; Saa, C. (2006). "Ru-Catalyzed Cyclization of Terminal Alkynals to Cycloalkenes". Journal of the American Chemical Society. 128 (30): 9576–9577. doi:10.1021/ja0610434. PMID 16866480.
- ^ 루테늄 촉매인 [CpRu3(CHCN6)]3PF는 시클로펜타디에닐 리간드, 3개의 아세토니트릴 리간드 및 인 6불화물 대항체를 가지며, 용매(초산)의 산성 양성자는 동위원소 표기를 위해 중수소로 대체된다.반응 조건: 90°C, 24시간80%의 화학 수율.첫 번째 단계는 전이 금속 카르벤 복합체 2의 형성입니다.아세트산은 에놀레이트 3을 형성하기 위해 친핵성 첨가물로 이 중간체에 첨가되며, 그 후 알돌 축합이 5로 이루어지며, 이 단계에서 일산화탄소 분자는 6으로 소실된다.마지막 단계는 사이클로알켄을 형성하기 위한 환원적 제거이다.
- ^ Vashchenko, V.; Kutulya, L.; Krivoshey, A. (2007). "Simple and Effective Protocol for Claisen–Schmidt Condensation of Hindered Cyclic Ketones with Aromatic Aldehydes". Synthesis. 2007 (14): 2125–2134. doi:10.1055/s-2007-983746.
외부 링크