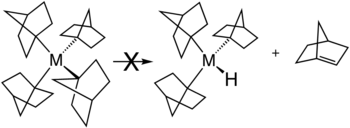베타-하이드라이드 제거
beta-Hydride elimination이 글은 검증을 위해 인용구가 추가로 필요하다.– · 신문 ·· 학자 · (2012년 8월 (이 템플릿 |
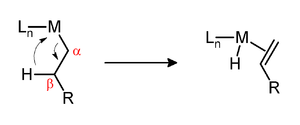
β-하이드라이드 제거는 금속 중심부에 접합된 알킬 그룹을 해당 금속 본드 하이드라이드와 알켄으로 변환하는 반응이다.[1]알킬에는 β-탄소 위에 하이드로겐이 있어야 한다.예를 들어, 부틸 그룹은 이 반응을 겪을 수 있지만 메틸 그룹은 할 수 없다.금속 단지는 알킬 그룹에 빈(또는 빈) 부위가 있어야 이 반응이 일어난다.또한 C-H 채권의 유연한 분할을 위해서는 C-H 채권의 궤도인 **에 d전자 쌍이 필요하다.따라서 d0 금속 알킬은 일반적으로2 d 및 상위 금속 알킬보다 β-하이드라이드 제거에 더 안정적이며, 빈 조정 부위가 있더라도 분리 가능한 불연속 복합체를 형성할 수 있다.[2]null
β-수소화물 제거는 반응에서 중요한 단계가 될 수도 있고 비생산적인 부작용일 수도 있다.셸 상위 올레핀 공정은 β-하이드라이드 제거에 의존하여 세제 생산에 사용되는 α-올레핀을 생산한다.지글러-나타 중합화에서 때때로 바람직하지 않은 β-히드라이드 제거, β-히드라이드 제거를 예증하면 분자량 감소의 고분자가 된다.아릴 할로겐화물과 알킬 그리그나드 시약의 니켈 및 팔라듐 측정 커플링의 경우 β-하이드라이드 제거는 수율을 낮출 수 있다.에틸렌으로부터 분기된 폴리머의 생산은 체인 보행에 의존하는데, 그 중 핵심 단계는 β-수소화물 제거다.null
β-수소화물 제거는 일련의 단계 중 첫 번째 단계인 경우도 있다.예를 들어, 루테늄 트리클로라이드, 트리페닐인산염 및 2-메톡시네탄올에서 RuHCl(CO)(PPH3)3의 합성에서 중간 알카산화물 복합체는 β-하이드라이드 리간드와 pi-본드 알데히드를 형성하여 나중에 카보닐(일산화탄소) 리간드로 변환한다.null
β-하이드라이드 제거 방지
β-히드라이드 제거를 피하기 위한 몇 가지 전략이 존재한다.가장 일반적인 전략은 수소 원자가 전혀 없는 알킬 리간드를 β 위치에 채용하는 것이다.일반적인 대체물로는 메틸과 네오펜틸이 있다.β-하이드라이드 제거는 반응으로 인해 알켄이 변형될 때도 억제된다.이러한 상황은 β-하이드라이드 제거 제품이 브레드의 규정을 위반할 수 있는 노르보닐 리간드를 함유한 금속 복합체의 안정성에 의해 설명된다.[3]null
테르트부틸이나 트리메틸실릴과 같은 부피가 큰 알킬 리간드는 수소 원자가 금속과 α 및 β 원자에 대해 공동선 구성에 접근하는 것을 금지할 수 있다.예를 들어 이미 18전자의 구성을 가진 단지에 의해 금속 센터에 빈 조정 부위가 없는 경우, β-수소화물 제거도 불가능하다.null
어떤 경우에, 콜리간드는 β-하이드라이드 제거를 억제하는 기하학적 형상을 부과할 수 있다.위의 예에서 원치 않는 β-히드라이드 제거는 두 개의 인 원자가 공간에 떨어져 고정되어 있는 디프인산(diphosphine)을 사용하여 방지한다.이것을 하는 한 가지 방법은 Xantphos와 같은 트랜스 스패닝 리간드를 사용하는 것이다.이러한 금속 단지는 전통적으로 사각 평면 기하학을 형성하기 때문에 알킬 그룹의 빈 부지는 형성될 수 없다.따라서 β-하이드라이드 제거를 방지한다.(전경간 리간드 참조)null
참조
- ^ Elschenbroich, C. (2006). Organometallics. Weinheim: Wiley-VCH. ISBN 978-3-527-29390-2.
- ^ Crabtree, Robert H. (2005). The organometallic chemistry of the transition metals (4th ed.). Hoboken, N.J.: John Wiley. p. 58. ISBN 0-471-66256-9. OCLC 61520528.
- ^ Bower, Barton K.; Tennent, Howard G. (1972). "Transition metal bicyclo[2.2.1]hept-1-yls". J. Am. Chem. Soc. 94: 2512–2514. doi:10.1021/ja00762a056.