엑셈스테인
Exemestane | |
 | |
| 임상 데이터 | |
|---|---|
| 발음 | /sncks,m,steadm(steen)/ EK-s--ME-stayn |
| 상호 | 아로마신 |
| 기타 이름 | FCE-24304 |
| AHFS/Drugs.com | 모노그래프 |
| Medline Plus | a607006 |
| 루트 행정부. | 입으로 |
| 약물 클래스 | 아로마타아제억제제, 항에스트로겐 |
| ATC 코드 | |
| 법적 상태 | |
| 법적 상태 |
|
| 약동학 데이터 | |
| 바이오 어베이러빌리티 | 최대 60 %[citation needed] |
| 단백질 결합 | 90% |
| 대사 | 간(CYP3A4, 알도케토환원효소) |
| 반감기 제거 | 24시간이 모자라 |
| 작업 기간 | 4[citation needed] ~ 5 일 |
| 배설물 | 소변 및 대변~1:1(주로 대사물) |
| 식별자 | |
| CAS 번호 | |
| PubChem CID | |
| IUPHAR/BPS | |
| 드러그뱅크 | |
| 켐스파이더 | |
| 유니 | |
| 케그 | |
| 체비 | |
| 첸블 | |
| CompTox 대시보드 (EPA ) | |
| ECHA 정보 카드 | 100.171.149 |
| 화학 및 물리 데이터 | |
| 공식 | C20H24O2 |
| 몰 질량 | 296.165g/140−1 |
| 3D 모델(JSmol) | |
| |
| |
| | |
아로마신 등의 브랜드명으로 판매되고 있는 엑셈스테인은 유방암 치료에 사용되는 의약품이다.그것은 아로마타아제 억제제로 알려진 항에스트로겐류의 구성원이다.어떤 유방암은 성장하기 위해 에스트로겐을 필요로 한다.그 암들은 에스트로겐 수용체를 가지고 있고, ER 양성이라고 불린다.그들은 또한 에스트로겐 반응성, 호르몬 반응성 또는 호르몬 수용체 양성이라고 불릴 수 있다.아로마타아제는 에스트로겐을 합성하는 효소이다.아로마타아제 억제제는 에스트로겐의 합성을 방해한다.이것은 에스트로겐 수치를 낮추고 암의 성장을 늦춘다.
의료 용도
폐경 후 에스트로겐 수용체 양성 조기 유방암에 걸린 여성의 보조요법으로서 타목시펜을 2~3년 투여받아 총 5년 연속 보조호르몬 [2]치료를 완료하기 위해 전환된다.미국 FDA의 허가는 1999년 [3]10월에 있었다.
엑셈스테인은 타목시펜 치료 [4]후 질병이 진행된 폐경 후 여성의 유방암 진행 치료에도 사용된다.
호르몬 수용체 양성 유방암을 가진 폐경 전 여성의 경우, 난소 억제제와 아로마타아제 억제제 엑셈스테인을 첨가한 보조 치료는 난소 억제제와 타목시펜과 비교하여 재발 위험을 감소시키는 새로운 치료 옵션을 제공한다.TEXT 및 SOFT 시험은 타목시펜 및 난소억제 그룹에 비해 엑셈스테인과 난소억제 치료를 받은 환자에서 무병 생존율이 향상되었음을 보여주었다.난소 억제를 받는 폐경 전 여성들은 이제 아로마타아제 억제제로부터 혜택을 받을 수 있다. 아로마타아제 억제제는 지금까지 폐경 [5]후 여성들에게만 권장되어 왔다.
금지 사항
이 약은 폐경 전 여성들에게 금지되어 있으며, 물론 임신과 수유 중인 [6]여성들도 포함되어 있다.
부작용
가장 흔한 부작용(환자의 10% 이상)은 엑시스테인에 의해 유발되는 에스트로겐 결핍과 불면증, 두통, 관절통으로 나타난다.메스꺼움과 피로는 주로 유방암 [6][7]말기 환자에게서 관찰된다.
아로마신을 투여하는 환자의 약 20%에서 림프구의 간헐적 감소가 관찰되었으며, 특히 기존 림프구 감소가 [8]관찰되었다.
엑셈스테인은 포름스테인과 유사한 안드로겐 특성을 가지고 있으며 여드름과 체중 증가와 같은 안드로겐 부작용을 일으킬 수 있다. 그러나 이러한 부작용은 일반적으로 [9]약물의 초치료 용량과 관련이 있다.
과다 복용
최소 32배(800mg)의 단일 용량과 평상시 하루 24배(600mg)의 지속적인 치료가 잘 허용된다.인간에게 생명을 위협하는 과다복용은 알려져 있지 않지만,[6] 동물 연구에서 (체표면적에 따라 조정된) 2000~4000배 용량만 알려져 있다.
상호 작용
exemestane은 간 효소 CYP3A4에 의해 대사된다.CYP3A4 억제제 케토코나졸은 임상시험에서 exemestane 수치에 유의미한 영향을 미치지 않았지만, 강한 CYP3A4 인덕터 리팜피신은 exemestane 수치를 약 절반으로 유의미하게 감소시켜(AUC -54max%, 1회 용량에 대해 C -41%) 효과를 저해할 수 있다.카바마제핀과 세인트존스워트와 같은 다른 3A4 인덕터들도 비슷한 [6][7]효과를 보일 것으로 예상된다.이 효과의 임상적 관련성은 [10]조사되지 않았다.
에스트로겐은 아마도 exemestane 효과를 [7]감소시킬 것입니다.인체의 에스트로겐 합성을 엑셈스테인으로 줄이고 에스트로겐을 의약품으로 대체하는 것은 보통 역효과를 낼 것이다.
약리학
약역학
Exemestane은 폐경 후 여성의 수술 및/또는 방사선 외에 ER 양성 유방암에 사용되는 경구 스테로이드 방향화효소 억제제이다.
에스트로겐의 주요 공급원은 폐경 전 여성의 난소인 반면, 폐경 후 여성의 경우 대부분의 신체 에스트로겐은 말초 조직(즉, 유방과 같은 지방 조직)과 뇌의 많은 부위에서 아로마타아제 효소에 의해 에스트로겐으로 전환됨으로써 생성된다.에스트로겐은 국소적으로 작용하는 이러한 말초 조직에서 방향분해효소의 작용을 통해 국소적으로 생산된다.폐경 후 여성뿐만 아니라 남성에게도 에스트로겐이 순환하는 것은 에스트로겐이 국소 대사를 벗어나 순환계로 [11]들어간 결과이다.
exemestane은 I형 스테로이드 방향분해효소 불활성제이며, 구조적으로 천연 기질 4-안드로스테디온과 관련이 있다.아로마타아제 효소에 대한 거짓 기질 역할을 하며, "자살 억제"라고도 알려진 효과인 효소의 불활성화를 일으키는 활성 부위에 불가역적으로 결합하는 중간체로 가공됩니다.효소 표적과 구조적으로 유사하기 때문에 엑세스테인은 효소와 영구적으로 결합하여 안드로겐이 [6]에스트로겐으로 변환되는 것을 방지한다.
반면, 아나스트로졸과 레트로졸과 같은 타입 II 방향분해효소 억제제는 스테로이드제가 아니며 방향분해효소의 [10]헴과 간섭하여 작용한다.
젊은 성인 남성을 대상으로 실시된 연구에 따르면 엑셈스테인의 에스트로겐 억제율은 에스트라디올(E2)의 35%에서 에스트론([12]E1)의 70%까지 다양했다.
| 시대 | 약 | 용량 | 억제율a | 클래스b | IC50c |
|---|---|---|---|---|---|
| 첫번째 | 테스토락톤 | 250밀리그램 4배속 | ? | 타입 I | ? |
| 100 mg 3배/주 | ? | ||||
| 로글레티미드 | 200 mg / 2 일 400 mg (1일 2배) 800 mg / 2 일 | 50.6% 63.5% 73.8% | 타입 II | ? | |
| 아미노글루테티미드 | 250mg 4배속 | 90.6% | 타입 II | 4,500 nM | |
| 둘째 | 포메스탄 | 125 mg (1일 1회) 125 mg / 2 일 250 mg (1일 1회) | 72.3% 70.0% 57.3% | 타입 I | 30nM |
| 250 mg 1x2 주간 500 mg 1 x 2주 500mg/1주일 | 84.8% 91.9% 92.5% | ||||
| 파드로졸레 | 1일 1mg 1일 2mg | 82.4% 92.6% | 타입 II | ? | |
| 셋째 | 엑셈스테인 | 25 mg (1일 1회 | 97.9% | 타입 I | 15nM |
| 아나스트로졸 | 1일 1mg 1일당 10mg / 10mg | 96.7–97.3% 98.1% | 타입 II | 10nM | |
| 레트로졸레 | 0.5mg/일 1배속 2.5mg/일 1회 | 98.4% 98.9%~99.1% | 타입 II | 2.5nM | |
| 각주: = 폐경 후 여성.b = Type I : 스테로이드, 불가역(결합부위)타입 II: 비스테로이드성, 가역성(시토크롬 P450 헴 부분과의 결합 및 간섭).c = 유방암 균질화물.출처:"템플릿"을 참조해 주세요. | |||||
약동학
엑셈스테인은 장에서 빠르게 흡수되지만 간에서 강한 퍼스트패스 효과를 일으킨다.가장 높은 혈장 농도는 유방암 환자에서 1.2시간 후, 건강한 환자에서 2.9시간 후에 도달한다.최대 방향화효소 억제는 2~3일 [10]후에 일어난다.흡수된 물질의 90%는 혈장 단백질에 결합되어 있다.간 효소 CYP3A4는 위치 6에서 메틸리덴기를 산화시키고, 알도케토 환원효소에 의해 알콜로 환원된다.생성된 대사물 중 40%는 소변을 통해, 40%는 대변을 통해 일주일 내에 배설된다.원래 물질은 소변에서 배설의 1%만을 차지한다.단말기의 반감기는 24시간입니다.[6][13]
화학
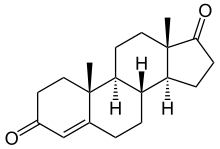
엑셈스테인은 화학적으로 6-메틸리덴안드로스타-1,4-디엔-3,17-디온으로 알려져 있다.포름스테인과 아탐스테인과 마찬가지로 엑셈스테인은 아로마타아제의 천연 기질인 4-안드로스테디온과 구조적으로 유사한 스테로이드이다.위치 6의 메틸리덴기와 위치 [14]1의 추가 이중 결합에 의해서만 천연 물질과 구별된다.
Pureexemestane은 DMSO에 최소 20 mg/mL까지 용해되는 백색에서 오프 화이트 분말이다.광학 회전 [α]D는 +250 ~ 300°(g/100cm³당, 589nm [15]파장에서 데시미터)입니다.
사회와 문화
퍼포먼스 향상
엑셈스테인은 황체화호르몬(LH)과 모낭자극호르몬(FSH) 수치를 높이기 위해 도핑에 사용돼 여성호르몬에 비해 남성의 비율을 증가시켜 성과를 향상시켰다.이 약은 또한 테스토스테론 [16]도핑으로 인한 과도한 방향분해효소 생성에 따른 지방과 수분 보유뿐만 아니라 여성유전증에도 작용한다.
엑셈스테인은 다른 아로마타아제 억제제와 함께 세계반도핑기구(WDA)의 금지 물질 목록에 [17]올라 있다.
조사.
2-3년간의 보조 요법 동안 매일 25mg의 경구 엑셈스테인은 일반적으로 잘 설계된[citation needed] 대규모 시험에서 조기 에스트로겐 수용체 양성/미지의 수용체 상태를 가진 폐경 후 여성의 치료에 5년 연속 보조 타목시펜보다 더 효과적이었다.2009년 exemestane과 타목시펜을 비교한 개방형 라벨 TEAM 시험의 예비 데이터는 exemestane이 폐경 [18]후 여성의 조기 유방암의 1차 보조 치료에도 효과적이라는 것을 나타냈다.
2011년 중간 단계 III 시험 결과에 따르면 진행성 유방암에 대한 exemestane 치료에 everolimus를 첨가하면 exemestane 치료 [19]단독에 비해 무진행 생존을 크게 개선할 수 있다.
폐경 후 유방암 위험이 높아진 여성들에게 엑셈스테인을 사용하면 침습성 유방암 발생률이 감소한다는 결론을 내린 3단계 임상시험이 2011년에 보고되었다.4,162명의 여성들에게 35개월 후, 25mg/일 용량으로 exemestane을 투여하면 위약과 비교하여 유방암 위험이 65% 감소하였다. 연간 발생률은 각각 0.19%와 0.55%였다. (위험비: 0.35; 95% CI [0.18-0.70]; p = 0.002).[20]
레퍼런스
- ^ ChEB의 Exemestane나
- ^ Coombes RC, Kilburn LS, Snowdon CF, Paridaens R, Coleman RE, Jones SE, et al. (February 2007). "Survival and safety of exemestane versus tamoxifen after 2-3 years' tamoxifen treatment (Intergroup Exemestane Study): a randomised controlled trial". Lancet. 369 (9561): 559–70. doi:10.1016/S0140-6736(07)60200-1. PMID 17307102. S2CID 38977099.
- ^ https://www.accessdata.fda.gov/drugsatfda_docs/nda/99/20-753_Aromasin_Approv.pdf[베어 URL PDF]
- ^ Aromasin for Advanced Break Cancer 2012-03-28 Wayback Machine Aromasin.com에 보관된 유방암 진단용 Aromasin
- ^ Pagani O, Regan MM, Walley BA, Fleming GF, Colleoni M, Láng I, et al. (July 2014). "Adjuvant exemestane with ovarian suppression in premenopausal breast cancer". The New England Journal of Medicine. 371 (2): 107–18. doi:10.1056/NEJMoa1404037. PMC 4175521. PMID 24881463.
- ^ a b c d e f Jasek, W, ed. (2007). Austria-Codex (in German) (62nd ed.). Vienna: Österreichischer Apothekerverlag. pp. 656–660. ISBN 978-3-85200-181-4.
- ^ a b c Drugs.com: exemestane에 관한 모노그래프.
- ^ "Aromasin - Summary of Product Characteristics (SMPC) - (Emc)".
- ^ Buzdar AU, Robertson JF, Eiermann W, Nabholtz JM (November 2002). "An overview of the pharmacology and pharmacokinetics of the newer generation aromatase inhibitors anastrozole, letrozole, and exemestane". Cancer. 95 (9): 2006–16. doi:10.1002/cncr.10908. PMID 12404296. S2CID 34798824.
- ^ a b c Dinnendahl V, Fricke U, eds. (2007). Arzneistoff-Profile (in German). Vol. 4 (21 ed.). Eschborn, Germany: Govi Pharmazeutischer Verlag. ISBN 978-3-7741-9846-3.
- ^ Simpson ER (September 2003). "Sources of estrogen and their importance". The Journal of Steroid Biochemistry and Molecular Biology. 86 (3–5): 225–30. doi:10.1016/S0960-0760(03)00360-1. PMID 14623515. S2CID 11210435.
- ^ Mauras N, Lima J, Patel D, Rini A, di Salle E, Kwok A, Lippe B (December 2003). "Pharmacokinetics and dose finding of a potent aromatase inhibitor, aromasin (exemestane), in young males". The Journal of Clinical Endocrinology and Metabolism. 88 (12): 5951–6. doi:10.1210/jc.2003-031279. PMID 14671195.
- ^ Mutschler E, Schäfer-Korting M (2001). Arzneimittelwirkungen (in German) (8 ed.). Stuttgart: Wissenschaftliche Verlagsgesellschaft. p. 904. ISBN 3-8047-1763-2.
- ^ Steinhilber D, Schubert-Zsilavecz M, Roth HJ (2005). Medizinische Chemie (in German). Stuttgart: Deutscher Apotheker Verlag. pp. 467f. ISBN 3-7692-3483-9.
- ^ Sigma-Aldrich Co., Exemestane, ( 98% (HPLC)
- ^ Sinner, D. (2007). Das Schwarze Buch – Anabole Steroide (in German). p. 133. ISBN 978-3-00-020944-4.
- ^ 2013-09-27 캐나다 스포츠 윤리 센터, 버전 4.0, 2009년 1월 웨이백 머신에 보관된 물질 분류 책자.
- ^ Deeks ED, Scott LJ (2009). "Exemestane: a review of its use in postmenopausal women with breast cancer". Drugs. 69 (7): 889–918. doi:10.2165/00003495-200969070-00007. PMID 19441873. Archived from the original on 2011-10-08. Retrieved 2010-03-29.
- ^ "Positive Trial Data Leads Novartis to Plan Breast Cancer Filing for Afinitor by Year End". 2011.
- ^ Goss, Paul E. (June 6, 2011). "Exemestane Offers New Option for Breast Cancer Prevention". American Society of Clinical Oncology. Archived from the original on July 11, 2011. Retrieved June 6, 2011.

