모노클로널 항체 치료
Monoclonal antibody therapy모노클로널 항체 치료는 모노클로널 항체(mAbs)를 이용해 특정 세포나 단백질에 특이적으로 결합하는 면역 요법의 한 형태다.목적은 이 치료법이 환자의 면역체계를 자극하여 그 세포들을 공격하는 것이다.또는 방사선 면역요법에서 방사성 선량은 표적 세포주를 국소화하여 치사 화학 [1]선량을 전달한다.항체는 T세포 반응을 차단하는 억제 경로를 제거하기 위해 T세포 조절에 관여하는 분자에 결합하는 데 사용되어 왔다.이것은 면역 검사점 [2]요법으로 알려져 있다.
거의 모든 세포 외/세포 표면 표적에 특정한 mAb를 생성할 수 있습니다.질병(류마티스 관절염, 다발성 경화증, 알츠하이머병[3], 에볼라 및 다양한 종류의 암)에 대한 항체를 만들기 위한 연구와 개발이 진행 중이다.
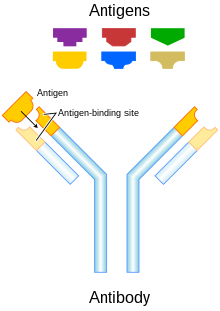
항체구조 및 기능
면역글로불린G(IgG) 항체는 약 150kDa의 큰 헤테로 이성질 분자이며 무거운(~50kDa)과 가벼운(~25kDa)이라고 불리는 두 종류의 폴리펩타이드 사슬로 구성되어 있다.경쇄에는 카파())와 람다(λ)가 있습니다.파파인 효소로 분해함으로써 Fab(파편-항원결합) 부분을 분자의 Fc(파편 상수) 부분에서 분리할 수 있다.Fab fragment는 항체 특이성을 담당하는 3개의 항체 초가변 아미노산 도메인으로 구성된 가변 도메인을 포함한다.알려진 4개의 IgG 서브클래스는 항체 의존성 세포독성에 [4]관여한다.항체는 적응 면역 반응의 핵심 요소이며, 외래 항원의 인식과 그에 대한 면역 반응의 자극 모두에서 중심 역할을 한다.모노클로널 항체 기술의 등장으로 [5]종양 표면에 나타나는 특정 항원에 대한 항체를 배양하는 것이 가능해졌다.모노클로널 항체는 면역 체계에서 수동 면역 또는 능동 면역으로 획득될 수 있다.활성 모노클로널 항체 치료의 장점은 면역체계가 이러한 반응을 유도하기 위한 단기 약물 투여만으로 항체를 장기적으로 생산한다는 사실이다.하지만, 특정 항원에 대한 면역 반응은 특히 노인들에게 불충분할 수 있습니다.또한 항원에 [6]대한 반응이 오래 지속되기 때문에 이러한 항체의 부작용이 발생할 수 있습니다.패시브 모노클로널 항체 치료는 항체 농도를 일정하게 유지할 수 있으며 투여를 중지하여 부작용을 억제할 수 있습니다.그러나 반복 투여와 그에 따른 높은 비용이 주요 [6]단점이다.
모노클로널 항체 치료는 암, 자가면역질환, 알츠하이머병과 같은 신체세포의 변성을 초래하는 신경학적 질환에 이로운 것으로 판명될 수 있다.선천적인 면역체계가 체세포에서 외부세포를 구별함으로써 발생하는 환경적 요인에 반응하기 때문에 모노클로널 항체 치료는 면역체계에 도움을 줄 수 있다.따라서, 빠른 속도로 증식하고 있는 종양 세포나 이후에 생리적 문제를 일으키는 신체 세포는 일반적으로 면역 체계에 의해 특별히 표적이 되지 않습니다. 종양 세포는 환자 자신의 세포이기 때문입니다.그러나 종양세포는 매우 이상하고 많은 세포들이 특이한 항원을 보인다.그러한 종양 항원 중 일부는 세포 유형이나 그 환경에 적합하지 않다.모노클로널 항체는 체세포로 인식되지만 건강을 해치는 종양세포나 이상세포를 노릴 수 있다.
★★★
면역요법은 1970년대에 항체 구조의 발견과 최초의 신뢰할 수 있는 모노클로널 [8][9]항체의 공급원을 제공한 하이브리드 도마 기술의 발달로 발전했다.이러한 발전은 체외 및 체내 종양의 특정 표적을 가능하게 했다.악성 종양에 대한 초기 연구는 혈액 악성 [10][11]종양에 대한 제한적이고 일반적으로 단기간에 성공하는 mAb 치료법을 발견했다.또한 치료는 개별 환자에 맞게 조정되어야 했고, 이는 일상적인 임상 환경에서는 실행 불가능했다.
개발된 네 가지 주요 항체 유형은 쥐, 키메라, 인간화 및 인간화이다.각 유형의 항체는 이름의 접미사로 구분됩니다.
초기 치료 항체는 쥐 유사체(suffix -omab)였다.이러한 항체는 짧은 반감기 체내(면역 복합체 형성에 의해), 종양 부위에 대한 제한된 침투 및 부적절한 숙주 이펙터 기능을 [12]가지고 있다.치료용 항체 [13]적용에서 키메라 및 인간화된 항체가 일반적으로 이들을 대체했다.프로테오믹스에 대한 이해는 새로운 종양 표적을 식별하는데 필수적인 것으로 입증되었다.
처음에 쥐 항체는 하이브리드 도마 기술에 의해 획득되었으며, 이 기술로 제른, 쾰러, 밀스타인은 노벨상을 받았다.그러나 쥐와 인간 면역체계의 차이는 일부 특정 상황을 제외하고 이러한 항체의 임상적 실패를 초래했다.쥐 항체와 관련된 주요 문제로는 세포독성 자극 감소와 반복 투여 후 복합체 형성이 포함되었으며, 이는 가벼운 알레르기 반응과 때로는 아나필락시 [12]쇼크를 초래했다.하이브리드 도마 기술은 재조합 DNA 기술, 트랜스제닉 마우스, 파지 [13]디스플레이로 대체되었다.
된 키메릭
쥐 항체 면역원성(항체에 대한 면역체계의 공격)을 줄이기 위해 쥐 분자는 면역원성 함량을 제거하고 면역학적 [12]효율을 높이기 위해 제작되었다.이것은 처음에 키메라(suffix -ximab)와 인간화된 항체(suffix -zumab)의 생산에 의해 달성되었다.키메라 항체는 인간의 일정한 영역에 융합된 쥐 가변 영역으로 구성됩니다.카파 경쇄와 IgG1 중쇄에서 인간 유전자 배열을 추출하면 약 65%가 인간인 항체가 생성된다.이것은 면역원성을 감소시키고, 따라서 혈청 반감기를 증가시킨다.
인간화된 항체는 아미노산 도메인 상의 뮤린 초가변 영역을 인간 항체에 접목함으로써 생산된다.이것은 약 95%의 인간 기원을 가진 분자를 낳는다.인간화된 항체는 항원을 부모 뮤린 모노클로널 항체보다 훨씬 더 약하게 결합하며, 친화력이 수백 [14][15]배까지 감소하는 것으로 보고되었다.antibody-antigen 바인딩 강도의 증가가 상호 보완성으로(사령관)[16]가변 지역 내 돌연변이error-prone PCR에 의해 유도와 chain-shuffling, complementarity-determining 지역 임의화나 항체 같은 기술을 사용하는 Emutator 변형 coli 지역을 결정하는 돌연변이를 도입함으로써 달성되었다.가 어떻게 되nd 사이트 고유의 돌연변이 유발.[1]
인간단일클로널항체
인간 모노클로널 항체(suffix - umab)는 인간 면역글로불린 유전자를 쥐 게놈에 전달하고 원하는 항원에 대해 해당 트랜스제닉 마우스를 백신접종함으로써 적절한 모노클로널 [13]항체를 제조한다.이것에 의해, 체외에서의 쥐 항체는 완전한 인간 [5]항체로 변환된다.
인간 IgG 단백질의 무겁고 가벼운 사슬은 구조적인 다형(allotype) 형태로 표현된다.인간 IgG 알로타입은 면역유전성에 [17][18]기여할 수 있는 많은 요인들 중 하나이다.
대상 조건
암
항암 모노클로널 항체는 몇 가지 메커니즘에 의해 악성 세포에 대한 표적이 될 수 있다.라무시루맵은 인간 모노클로널 재조합 항체로 진행성 악성종양 치료에 사용된다.[19]소아 림프종에서는 항체 [20]요법의 사용으로 인한 긍정적인 효과가 1상 및 2단계 연구에서 발견되었습니다.
자가면역질환
Monoclonal 항체 면역 질환에 사용되는 능력과 TNF-α.[21]Basiliximab과daclizumab 금지 IL-2 활성화 T세포에 억제하고 따라서 신장 이식의 급성 거부 반응 예방을 돕는으로 류머티스성 관절염에 효과적이다 infliximab과 adalimumab, 크론 병과 궤양성 대장염을 포함한다.[21]오말리주맵은 인간 면역글로불린E(IgE)를 억제하고 중간에서 심각한 알레르기 천식에 유용하다.
알츠하이머병
알츠하이머병(AD)은 다면적이고 연령에 따라 달라지는 진행성 신경변성 질환으로 [22]치매의 주요 원인이다.아밀로이드 가설에 따르면 세포외 아밀로이드 베타펩타이드(Aβ)가 올리고머화를 통해 플라크에 축적되는 것은 시냅스 기능 장애 및 신경 [23]변성을 통해 AD의 특징적인 증상 상태를 초래한다.외인성 모노클로널 항체(mAb) 투여에 의한 면역요법은 Aβ-올리고머화를 억제하여 신경독성을 예방함으로써 AD와 같은 다양한 중추신경장애를 치료하는 것으로 알려져 있다.그러나 mAb는 수동적 단백질 채널의 경우 크기 때문에 mAb가 뇌로 전달되는 것을 막는 혈액-뇌 장벽 때문에 비효율적이다.그러나 Peripheral Sink 가설은 mAb가 혈액-뇌 장벽을 [24]넘을 필요가 없는 메커니즘을 제안한다.따라서 과거에 [23]AD를 치료하기 위해 실패한 시도로부터 많은 연구가 이루어지고 있다.
단, 항Aβ 백신은 아밀로이드 전구 단백질(APP)을 가진 트랜스제닉 마우스 모델에서 Aβ 플라크의 항체 매개 클리어런스를 촉진할 수 있으며 인지 장애를 [22]줄일 수 있다.백신은 능동 면역으로 알려진 트랜스제닉 동물 모델에 Aβ를 도입함으로써 면역 체계를 자극하여 자체 [25]항체를 생산할 수 있습니다.그들은 또한 수동 면역으로 알려진 항체를 동물 모델에 도입할 수 있다.APP를 발현하는 생쥐에서는 항Aβ 항체의 능동적 및 수동적 면역이 플라크 제거에 효과적이며 인지 기능을 [23]향상시킬 수 있는 것으로 나타났다.현재 알츠하이머병에 대한 승인된 모노클로널 항체 치료법은 없지만, FDA가 승인한 특정 약물의 개발에 의한 수동적이고 능동적인 면역접종을 이용한 여러 임상시험이 진행 중이며, 몇 [23]년 후 결과가 나올 것으로 예상된다.이러한 약물의 실행은 AD가 시작되는 동안이다.조기 개입과 AD 예방을 위한 다른 연구 및 약물 개발이 진행 중이다.AD를 치료하기 위해 연구되고 있는 다양한 약물들은 바피뉴주맙, 솔라네주맙, 고테루맙, BAN2401 등이다.
바피누주맙
인간화된 항Aβ mAb인 Bapineuzumab은 Aβ의 N 말단에 대해 유도된다.경도에서 중간 정도의 AD 환자에 대한 Bapineuzumab 임상시험 2상에서는 뇌에서 Aβ 농도가 감소하였다.그러나 아폴리포단백질(APOE) e4 운반체가 증가한 환자에서는 Bapineuzumab 치료도 [27]혈중 뇌장벽이 파괴되어 뇌의 세포내 및 세포외 공간에 있는 모세혈관에서 과다한 액체의 축적으로 인한 백혈구에 영향을 미치는 세포독성 질환인 혈관성 [26]부종을 동반한다.3단계 임상시험에서 Bapineuzumab 처리는 APOE e4 환자의 뇌에서 Aβ의 축적 속도가 감소하고 APOE e4 환자 및 비 APOE e4 환자에서 Aβ 농도가 유의하게 감소하지 않는 것과 관련이 있다.따라서, Aβ 플라크 농도는 감소되지 않았으며, 인지 기능에 있어 유의미한 임상적 이점이 없다.Bapineuzumab은 3상 임상시험에서 [27]실패한 후 중단되었다.
솔라네즈마브
항Aβ mAb인 Solanzumab은 Aβ의 N 말단을 표적으로 한다.임상시험의 Phase I 및 Phase II에서 Solanezumab 처리는 Aβ의 뇌척수액 상승을 초래하여 Aβ 플라크의 저농도를 보였다.또한 관련 부작용은 없습니다.솔라네주맙의 3단계 임상시험은 경미한 AD 환자에서 인지장애를 유의하게 감소시켰지만 중증 AD 환자에서는 유의하지 않았다.그러나 Aβ 농도는 포스포-타우 발현과 해마 부피를 포함한 다른 AD 바이오마커와 함께 유의하게 변화하지 않았다.3단계 임상시험은 현재 [24]진행 중입니다.
BAN2401
BAN2401은 독성 수용성 Aβ 원섬유를 선택적으로 표적으로 하는 인체화 mAb로 현재 [28]3상 임상시험을 진행 중이며 2022년 [29]완료를 목표로 하고 있다.
예방 시험
3단계 임상시험에서 여러 약물의 실패는 AD 예방과 AD 치료 시작 노력에 대한 조기 개입으로 이어졌다.수동적 항Aβ mAb 치료는 광범위한 뇌 손상과 증상을 유발하기 전에 AD 진행을 수정하려는 예방적 시도에 사용될 수 있다.유전자 위험 인자에 양성인 환자 및 AD 지표에 양성인 노인 환자에 대해 mAb 치료를 사용하는 시도가 진행 중입니다.여기에는 무증상성 알츠하이머병(A4), 알츠하이머 예방 이니셔티브(API), DIAN-TU의 [24]항AB 치료가 포함됩니다.AD의 지표에는 긍정적이지만 유전적 위험 인자에 대해서는 음성인 노인을 대상으로 한 A4 연구는 이전 솔라네주맙 연구의 [24]후속 연구로서 단계 III 임상 시험에서 솔라네주맙을 테스트한다.2012년 12월에 출시된 DIAN-TU는 AD의 위험 요소인 유전자 돌연변이에 양성 반응을 보이는 젊은 환자들에 초점을 맞추고 있다.이 연구는 Solanesumab과 Gautenerumab을 사용합니다.뇌에서 올리고머화된 Aβ 플라크와 우선적으로 상호작용하는 최초의 완전 인간 MAB인 Gautenerumab은 1상 임상시험에서 Aβ 농도의 현저한 감소를 유발하여 뇌의 혈장 농도를 변경하지 않고 플라크 형성과 집중을 막았다.현재 2상 및 3상 임상시험이 [24]진행 중입니다.
치료 유형
방사선 면역 요법
방사성 면역 요법(RIT)은 세포 항원에 대한 방사성 결합 쥐 항체의 사용을 포함한다.대부분의 연구는 림프종에 대한 적용과 관련이 있는데, 이는 매우 방사선에 민감한 악성종양이기 때문이다.방사선 피폭을 제한하기 위해 높은 면역원성이 빠른 종양 제거를 촉진하기 때문에 쥐 항체가 선택되었다.토시투모맵은 비호지킨 림프종에 사용되는 예다.
항체지향효소프로드러그요법
항체방향효소프로드러그치료(ADEPT)는 약물활성화효소에 연결된 암관련 모노클로널 항체의 적용을 포함한다.무독성 약물을 전신 투여하면 항체가 독성 약물로 전환되어 악성 세포를 표적으로 삼을 수 있는 세포독성 효과가 발생한다.ADEPT 치료의 임상적 성공은 [30]제한적이다.
항체-약물 결합체
항체-약물결합체(ADC)는 하나 이상의 약물분자에 연결된 항체이다.일반적으로 ADC가 표적 세포(예: 암 세포)를 만나면 이를 죽이기 위해 약물이 방출된다.많은 ADC가 임상 개발 중입니다.2016년 현재[update] 일부 승인되었습니다.
임노리포좀 요법
면역리포좀은 항체결합 리포좀이다.리포좀은 약물이나 치료용 뉴클레오티드를 운반할 수 있으며 모노클로널 항체와 결합하면 악성 세포에 대항할 수 있다.면역리포좀은 인체 트랜스페린 수용체에 대한 항체 단편을 사용하여 종양 억제 유전자를 종양으로 전달하기 위해 생체 내에서 성공적으로 사용되어 왔다.면역리포좀을 이용한 조직 특이적 유전자 전달은 뇌와 유방암 [31]조직에서 이루어졌다.
체크 포인트 요법
검문소 치료는 항체와 다른 기술을 사용하여 종양들이 면역체계를 억제하기 위해 사용하는 방어 수단을 우회시킨다.각각의 방어를 검문소라고 합니다.복합요법은 항체를 결합하여 여러 방어층을 억제한다.알려진 체크포인트에는 ipilimumab 표적 CTLA-4, nivolumab 표적 PD-1 및 pembrolizumab 표적 PD-1 및 종양 미세환경이 [2]포함된다.
종양 미세 환경(TME) 기능은 종양에 T세포가 유입되는 것을 방지합니다.방법에는 스트로마에서 T세포를 가두는 케모카인 CCL2 질화가 포함됩니다.종양 혈관 구조는 부분적으로 FasL, ETRB 및 B7H3의 내피 세포(EC) 특이적 발현을 통해 종양이 T 세포 위에 다른 면역 세포를 우선적으로 모을 수 있도록 도와줍니다.골수구성세포 및 종양세포는 부분적으로 저산소 조건 및 사이토카인 생산(IFNβ 등)에 의해 구동되는 PD-L1의 발현을 상향조절할 수 있다.IDO에 의한 경로조절과 같은 TME에서의 이상대사물 생산은 T세포의reg 직간접적 기능에 영향을 미칠 수 있다.CD8 세포는 TAM 표현형의 B 세포 조절에 의해 억제될 수 있다.암 관련 섬유아세포(CAF)는 부분적으로 세포외 매트릭스(ECM) 매개 T세포 포획 및 CXCL12 조절 T세포 제외를 [32]통해 여러 TME 기능을 가진다.
FDA 승인 치료용 항체
이 섹션은 업데이트해야 합니다.(2021년 5월) |
최초의 FDA 승인 치료용 모노클로널 항체는 1986년 쥐 IgG2a CD3 특이 이식 거부제 OKT3(무로모나브라고도 함)였다.이 약은 스테로이드 [33]내성이 생긴 고형 장기 이식 환자들에게 사용되는 것으로 밝혀졌다.수백 가지 치료법이 임상시험을 거치고 있다.대부분은 면역학적 목표와 종양학적 목표와 관련이 있다.
| 항체 | 브랜드명 | 회사 | 승인일자 | 경로 | 유형 | 대상 | 표시 (대상 질환) | BLA STN | 약물 라벨 |
|---|---|---|---|---|---|---|---|---|---|
| abcximab | 리오프로 | 센토코 | 12/22/1994 | 정맥주사 | 키메라 팹 | GPIB/IIa | 경피적 관상동맥 개입 | 103575 | 링크 |
| 애드림마브 | 후미라 | 애비 | 12/31/2002 | 피하의 | 완전 인간적인 | TNF | 류마티스 관절염 | 125057 | 링크 |
| adalimumab-atto의 | 암제비타 | 암겐 | 9/23/2016 | 피하의 | 완전 인간, 바이오시밀러 | TNF | 류마티스 관절염 소아 특발성 관절염 건선성 관절염 강직성 척추염 크론병 궤양성 대장염 플라그 건선 | 761024 | 링크 |
| 아도트라스마브엠탄신 | 카드실라 | 제너텍 | 2/22/2013 | 정맥주사 | 인간화된 항체결합체 | HER2 | 전이성 유방암 | 125427 | 링크 |
| 알레무즈마브 | 캄파스 주, 렘트라다 | 젠자임 | 5/7/2001 | 정맥주사 | 인간화된 | CD52 | B세포만성림프구성백혈병 | 103948 | 링크 |
| 알리로쿠마브 | 프랄루엔트 | 사노피 아벤티스 | 7/24/2015 | 피하의 | 완전 인간적인 | PCSK9 | 헤테로 접합성 가족성 고콜레스테롤혈증 난치성 고콜레스테롤혈증 | 125559 | 링크 |
| 아테졸리주맙 | 테센트리크 | 제너텍 | 5/18/2016 | 정맥주사 | 인간화된 | PD-L1 | 요관암 | 761034 | 링크 |
| 아테졸리주맙 | 테센트리크 | 제너텍 | 10/18/2016 | 정맥주사 | 인간화된 | PD-L1 | 요관암 전이성 비소세포 폐암 | 761041 | 링크 |
| 아벨루마브 | 바벤시오 | EMD 세로노 | 3/23/2017 | 정맥주사 | 완전 인간적인 | PD-L1 | 전이성 메르켈 세포암 | 761049 | 링크 |
| 바실릭시마브 | 시뮬렉트 | 노바티스 | 5/12/1998 | 정맥주사 | 키메라 | IL2RA | 신장 이식의 급성 장기 거부 예방 | 103764 | 링크 |
| 벨리마바 | 벤리스타 | 인간 게놈 과학 | 3/9/2011 | 정맥주사 | 완전 인간적인 | 점멸 | 전신성 홍반성 낭창 | 125370 | 링크 |
| 베바시즈마브 | 아바스틴 | 제너텍 | 2/26/2004 | 정맥주사 | 인간화된 | VEGF | 전이성 대장암 | 125085 | 링크 |
| 베즐로톡스마브 | 진플라바 | 머크 | 10/21/2016 | 정맥주사 | 완전 인간적인 | 클로스트리듐디피실독소B | 클로스트리듐 디피실 감염 재발 방지 | 761046 | 링크 |
| 브리나툼마브 | 브린시토 | 암겐 | 12/3/2014 | 정맥주사 | 마우스, 2종류 | CD19 | 전구체B세포급성림프아구성백혈병 | 125557 | 링크 |
| 브렌턱시맙베도틴 | 아세트리스 | 시애틀 제네틱스 | 9/19/2011 | 정맥주사 | 키메라 항체결합체 | CD30 | 호지킨림프종 미분화대세포림프종 | 125388 | 링크 |
| 브로다루마브 | 실리크 | 발레안트 | 2/15/2017 | 피하의 | 키메라 | IL17RA | 플라그 건선 | 761032 | 링크 |
| 카나키무바 | 일라리 | 노바티스 | 6/17/2009 | 피하의 | 완전 인간적인 | IL1B | 크라이오피린관련주기증후군 | 125319 | 링크 |
| 카프로마브 펜데타이드 | 프로스타신트 | 세포진 | 10/28/1996 | 정맥주사 | 뮤린, 방사선 라벨 부착 | PSMA | 새로 진단된 전립선암 또는 항문절제술 후 영상검사제 | 103608 | 링크 |
| 케르토리주맙페골 | 킨지아 | UCB(회사) | 4/22/2008 | 피하의 | 인간화된 | TNF | 크론병 | 125160 | 링크 |
| cetuximab | Erbitux | ImClone 시스템 | 2/12/2004 | 정맥주사 | 키메라 | EGFR | 전이성 대장암 | 125084 | 링크 |
| 디스크리주맙 | 제나팍스 | 로체 | 12/10/1997 | 정맥주사 | 인간화된 | IL2RA | 신장 이식의 급성 장기 거부 예방 | 103749 | 링크 |
| 디스크리주맙 | 진브리타 | 바이오젠 | 5/27/2016 | 피하의 | 인간화된 | IL2R | 다발성 경화증 | 761029 | 링크 |
| 다라툼마브 | 다르잘렉스 | 얀센 바이오텍 | 11/16/2015 | 정맥주사 | 완전 인간적인 | CD38 | 다발성 골수종 | 761036 | 링크 |
| 데노스마브 | 프롤리아, 크제바 | 암겐 | 6/1/2010 | 피하의 | 완전 인간적인 | 랭클 | 폐경 후 골다공증 여성 | 125320 | 링크 |
| dinutuximab | 유니턱신 | 유나이티드 테라피유틱스 | 3/10/2015 | 정맥주사 | 키메라 | GD2 | 소아고위험신경아세포종 | 125516 | 링크 |
| 듀필루마브 | 듀픽슨트 | 레제논 제약 | 3/28/2017 | 피하의 | 완전 인간적인 | IL4RA | 아토피, 천식 | 761055 | 링크 |
| 두르바루마브 | 임핀지 | 아스트라제네카 | 5/1/2017 | 정맥주사 | 완전 인간적인 | PD-L1 | 요관암 | 761069 | 링크 |
| 에큘리주맙 | 솔리스 | 알렉시온 | 3/16/2007 | 정맥주사 | 인간화된 | 보완 컴포넌트 5 | 발작성 야행성 헤모글로빈뇨 | 125166 | 링크 |
| elotuzumab | 엠플리시티 | 브리스톨 마이어스 스퀴브 | 11/30/2015 | 정맥주사 | 인간화된 | 슬램프7 | 다발성 골수종 | 761035 | 링크 |
| 에볼로쿠마브 | 레파타 | 암겐 | 8/27/2015 | 피하의 | 완전 인간적인 | PCSK9 | 헤테로 접합성 가족성 고콜레스테롤혈증 난치성 고콜레스테롤혈증 | 125522 | 링크 |
| 골리마바 | 심포니 | 센토코 | 4/24/2009 | 피하의 | 완전 인간적인 | TNF | 류마티스 관절염 건선성 관절염 강직성 척추염 | 125289 | 링크 |
| 골리마바 | 심포니 아리아 | 얀센 바이오텍 | 7/18/2013 | 정맥주사 | 완전 인간적인 | TNF | 류마티스 관절염 | 125433 | 링크 |
| 이브리토마브티우세탄 | 제발린 | 스펙트럼 제약 | 2/19/2002 | 정맥주사 | 쥐, 방사선 면역 요법 | CD20 | 재발 또는 난치성 저급, 모낭 또는 변형된 B세포 비호지킨 림프종 | 125019 | 링크 |
| idarucizumab | 프락스바인드 | 베링거 잉겔하임 | 10/16/2015 | 정맥주사 | 인간화된 팹 | 다비가트란 | 항응고제 다비가트란 응급환원 | 761025 | 링크 |
| 인플릭스맵 | 레미케이드 | 센토코 | 8/24/1998 | 정맥주사 | 키메라 | TNF 알파 | 크론병 | 103772 | 링크 |
| 인플릭시맙 압다 | 렌플렉시스 | 삼성에피스 | 4/21/2017 | 정맥주사 | 키메라, 바이오시밀러 | TNF | 크론병 궤양성 대장염 류마티스 관절염 강직성 척추염 건선성 관절염 플라그 건선 | 761054 | 링크 |
| 인플릭시맙 다이브 | 굴절 | 셀트리온헬스케어 | 4/5/2016 | 정맥주사 | 키메라, 바이오시밀러 | TNF | 크론병 궤양성 대장염 류마티스 관절염 강직성 척추염 건선성 관절염 플라그 건선 | 125544 | 링크 |
| ipilimumab | 예르보이 | 브리스톨 마이어스 스퀴브 | 3/25/2011 | 정맥주사 | 완전 인간적인 | CTLA-4 | 전이성 흑색종 | 125377 | 링크 |
| ixekizumab | 탈츠 | 엘리 릴리 | 3/22/2016 | 피하의 | 인간화된 | IL17A | 플라그 건선 | 125521 | 링크 |
| 메폴리주맙 | 누칼라 | 글락소스미스클라인 | 11/4/2015 | 피하의 | 인간화된 | IL5 | 심한 천식 | 125526 | 링크 |
| 나탈리주맙 | 티사브리 | 바이오젠 IDEC | 11/23/2004 | 정맥주사 | 인간화된 | 알파-4 인테그린 | 다발성 경화증 | 125104 | 링크 |
| 니시투마브 | 초상화 | 엘리 릴리 | 11/24/2015 | 정맥주사 | 완전 인간적인 | EGFR | 전이성 편평상 비소세포 폐암 | 125547 | 링크 |
| 니볼루마브 | 옵디보 | 브리스톨 마이어스 스퀴브 | 12/22/2014 | 정맥주사 | 완전 인간적인 | PD-1 | 전이성 흑색종 | 125554 | 링크 |
| 니볼루마브 | 옵디보 | 브리스톨 마이어스 스퀴브 | 3/4/2015 | 정맥주사 | 완전 인간적인 | PD-1 | 전이성 편평상 비소세포 폐암 | 125527 | 링크 |
| 오빌톡시마브 | 노래 | 엘루시스 테라피유틱스 | 3/18/2016 | 정맥주사 | 키메라 | 탄저균 독소의 보호항원 | 흡입 탄저균 | 125509 | 링크 |
| 오비누투즈마브 | 가지바 | 제너텍 | 11/1/2013 | 정맥주사 | 인간화된 | CD20 | 만성 림프구성 백혈병 | 125486 | 링크 |
| 오크리즈마브 | 오크레부스 | 제너텍 | 3/28/2017 | 정맥주사 | 인간화된 | CD20 | 다발성 경화증 | 761053 | 링크 |
| 오오라무마브 | 아제르라 | 글락소그루프 | 10/26/2009 | 정맥주사 | 완전 인간적인 | CD20 | 만성 림프구성 백혈병 | 125326 | 링크 |
| olaratumab | 라르트루보 | 엘리 릴리 | 10/19/2016 | 정맥주사 | 완전 인간적인 | PDGFRA | 연조직육종 | 761038 | 링크 |
| 오마리즈마브 | 졸레르 | 제너텍 | 6/20/2003 | 피하의 | 인간화된 | IgE | 중등도에서 중도의 지속성 천식 | 103976 | 링크 |
| 팔리비즈마브 | 회당 | MedImmune | 6/19/1998 | 근육 내의 | 인간화된 | RSV의 F단백질 | 호흡합성세포바이러스 | 103770 | 링크 |
| 파니투마브 | 벡티빅스 | 암겐 | 9/27/2006 | 정맥주사 | 완전 인간적인 | EGFR | 전이성 대장암 | 125147 | 링크 |
| 펨보리주맙 | 키트루다 | 머크 | 9/4/2014 | 정맥주사 | 인간화된 | PD-1 | 전이성 흑색종 | 125514 | 링크 |
| 백일해 | 페르제타 | 제너텍 | 6/8/2012 | 정맥주사 | 인간화된 | HER2 | 전이성 유방암 | 125409 | 링크 |
| 라무시루마브 | 시람자 | 엘리 릴리 | 4/21/2014 | 정맥주사 | 완전 인간적인 | VEGFR2 | 위암 | 125477 | 링크 |
| 래니비즈마브 | 루센티스 | 제너텍 | 6/30/2006 | 체외 주입 | 인간화된 | VEGFR1 VEGFR2 | 습윤 노화로 인한 황반변성 | 125156 | 링크 |
| 락시바쿠마브 | 락시바쿠마브 | 인간 게놈 과학 | 12/24/2012 | 정맥주사 | 완전 인간적인 | 무연탄균의 보호항원 | 흡입 탄저균 | 125349 | 링크 |
| 리즈마브 | 싱카이르 | 테바 | 3/23/2016 | 정맥주사 | 인간화된 | IL5 | 심한 천식 | 761033 | 링크 |
| 리탁시마브 | 리투산 | 제너텍 | 11/26/1997 | 정맥주사 | 키메라 | CD20 | B세포 비호지킨림프종 | 103705 | 링크 |
| 세쿠키누마브 | 코센티엑스 | 노바티스 | 1/21/2015 | 피하의 | 완전 인간적인 | IL17A | 플라그 건선 | 125504 | 링크 |
| 실룩시마브 | 실반트 | 얀센 바이오텍 | 4/23/2014 | 정맥주사 | 키메라 | IL6 | 다심 캐슬맨 병 | 125496 | 링크 |
| 토실리주맙 | 액템라 | 제너텍 | 1/8/2010 | 정맥주사 | 인간화된 | IL6R | 류마티스 관절염 | 125276 | 링크 |
| 토실리주맙 | 액템라 | 제너텍 | 10/21/2013 | 정맥주사 피하의 | 인간화된 | IL6R | 류마티스 관절염 다관절성 소아특발성관절염 전신성 소아 특발성 관절염 | 125472 | 링크 |
| 트라스투즈마브 | 허셉틴 | 제너텍 | 9/25/1998 | 정맥주사 | 인간화된 | HER2 | 전이성 유방암 | 103792 | 링크 |
| 우스테키누마브 | 스테라라 | 센토코 | 9/25/2009 | 피하의 | 완전 인간적인 | IL12 IL23 | 플라그 건선 | 125261 | 링크 |
| 우스테키누마브 | 스테라라 | 얀센 바이오텍 | 9/23/2016 | 피하의 정맥주사 | 완전 인간적인 | IL12 IL23 | 플라그 건선 건선성 관절염 크론병 | 761044 | 링크 |
| 베도리즈마브 | 엔티비오 | 다케다 | 5/20/2014 | 정맥주사 | 인간화된 | 인테그린수용체 | 궤양성 대장염 크론병 | 125476 | 링크 |
| 사리루마브 | 케브자라 | 사노피 아벤티스 | 5/22/17 | 피하의 | 완전 인간적인 | IL6R | 류마티스 관절염 | 761037 | 링크 |
| 리턱시맙 및 히알루로니다아제 | 리투산 히셀라 | 제너텍 | 6/22/17 | 피하의 | 키메라, 공식화된 | CD20 | 모낭림프종 확산성 B세포 림프종 만성 림프구성 백혈병 | 761064 | 링크 |
| 구셀쿠마브 | 트렘피아 | 얀센 바이오텍 | 7/13/17 | 피하의 | 완전 인간적인 | IL23 | 플라그 건선 | 761061 | 링크 |
| 이노투즈마브오조가미신 | 베스폰사 | 와이스 | 8/17/17 | 정맥주사 | 인간화된 항체결합체 | CD22 | 전구체B세포급성림프아구성백혈병 | 761040 | 링크 |
| adalimumab-adbm | 시루테조 | 베링거 잉겔하임 | 8/25/17 | 피하의 | 완전 인간, 바이오시밀러 | TNF | 류마티스 관절염 소아 특발성 관절염 건선성 관절염 강직성 척추염 크론병 궤양성 대장염 플라그 건선 | 761058 | 링크 |
| 젬투주맙오즈가미신 | 마일로타그 | 와이스 | 9/1/17 | 정맥주사 | 인간화된 항체결합체 | CD33 | 급성 골수성 백혈병 | 761060 | 링크 |
| 베바시주맙-아워브 | 음바시 | 암겐 | 9/14/17 | 정맥주사 | 인간화, 바이오시밀러 | VEGF | 전이성 대장암 비편평성 비소세포 폐암 교아세포종 전이성 신세포암 자궁경부암 | 761028 | 링크 |
| 벤랄리주맙 | 파센라 | 아스트라제네카 | 11/14/17 | 피하의 | 인간화된 | 인터류킨-5수용체α서브유닛 | 심한 천식, 호산구 표현형 | 761070 | 링크 |
| emicizumab-kxwh | 헴리브라 | 제너텍 | 11/16/17 | 피하의 | 인간화된, 이특이 | 인자 IXa, 인자 X | 혈우병 A(공중 인자 VIII 결핍증) 및 인자 VIII 억제제. | 761083 | 링크 |
| 트라스투즈마브 dkst | 오기브리 | 마일란 | 12/1/17 | 정맥주사 | 인간화, 바이오시밀러 | HER2 | HER2-과잉 유방암, 전이성 위 또는 위 식도 접합부 선암 | 761074 | 링크 |
| infliximab-qbtx | Ixifi | 화이자 | 12/13/17 | 정맥주사 | 키메라, 바이오시밀러 | TNF | 크론병 궤양성 대장염 류마티스 관절염 강직성 척추염 건선성 관절염 플라그 건선 | 761072 | 링크 |
| 이발리주맙의이크 | 트로가르조 | 타이메드 바이오닉스 | 3/6/18 | 정맥주사 | 인간화된 | CD4 | HIV | 761065 | 링크 |
| 틸드라키즈마브 아스만 | 일루미야 | 머크 | 3/20/18 | 피하의 | 인간화된 | IL23 | 플라그 건선 | 761067 | 링크 |
| 부로수맵트자 | 크라이스비타 | 울트라제닉스 | 4/17/18 | 피하의 | 완전 인간적인 | FGF23 | X결합성 저인산혈증 | 761068 | 링크 |
| 에레누마바오에 | 아이모빅 | 암겐 | 5/17/18 | 피하의 | 완전 인간적인 | CGRP수용체 | 편두통 예방 | 761077 | 링크 |
Tositumomab – Bexar – 2003 – CD20
Moxetumomab pasudotox – 루목시티 – 2018년 9월 ~ CD22
Cemiplimab – Libtayo – 2018년 9월 – PD-1
Polatuzumab Vedotin – Polivy – 2019년 6월 – CD79B
이특이적 항체는 임상시험에서 유망한 결과를 얻었다.2009년 4월, 이원 [34][35]특이 항체 catumaxomab이 유럽연합에서 승인되었다.
경제학
2000년 이후, 모노클로널 항체의 치료 시장은 기하급수적으로 성장했다.2006년 시판된 치료용 항체는 베바시주맙, 트라스투주맙(종양학), 아달리맵, 인플릭시맵(자체면역 및 염증성 질환 모두 AIID), 리턱시맵(종양학 및 AIID)이 수익의 80%를 차지했다.2007년에 미국에서 가장 많이 팔린 20개의 생명공학 약 중 8개가 치료용 모노클로널 [36]항체이다.이러한 모노클로널 항체 생산 수요의 급격한 증가는 mAb [37]제조의 산업화에 의해 잘 수용되었다.
레퍼런스
- ^ a b Waldmann TA (March 2003). "Immunotherapy: past, present and future". Nature Medicine. 9 (3): 269–77. doi:10.1038/nm0303-269. PMID 12612576. S2CID 9745527.
- ^ a b Sharma P, Allison JP (April 2015). "The future of immune checkpoint therapy". Science. 348 (6230): 56–61. Bibcode:2015Sci...348...56S. doi:10.1126/science.aaa8172. PMID 25838373. S2CID 4608450.
- ^ Olinger GG, Pettitt J, Kim D, Working C, Bohorov O, Bratcher B, Hiatt E, Hume SD, Johnson AK, Morton J, Pauly M, Whaley KJ, Lear CM, Biggins JE, Scully C, Hensley L, Zeitlin L (October 2012). "Delayed treatment of Ebola virus infection with plant-derived monoclonal antibodies provides protection in rhesus macaques". Proceedings of the National Academy of Sciences of the United States of America. 109 (44): 18030–5. Bibcode:2012PNAS..10918030O. doi:10.1073/pnas.1213709109. PMC 3497800. PMID 23071322.
- ^ Janeway, Charles; Paul Travers; Mark Walport; Mark Shlomchik (2001). Immunobiology; Fifth Edition. New York and London: Garland Science. ISBN 978-0-8153-4101-7.
- ^ a b Janeway CA, Jr.; et al. (2005). Immunobiology (6th ed.). Garland Science. ISBN 978-0-443-07310-6.
- ^ a b Baxter, David (December 2007). "Active and passive immunity, vaccine types, excipients and licensing". Occupational Medicine. 57 (8): 552–6. doi:10.1093/occmed/kqm110. PMID 18045976.
- ^ 수정원
- ^ Prof FC Breedveld (2000). "Therapeutic monoclonal antibodies". Lancet. 355 (9205): 735–740. doi:10.1016/S0140-6736(00)01034-5. PMID 10703815. S2CID 43781004.
- ^ Köhler G, Milstein C (August 1975). "Continuous cultures of fused cells secreting antibody of predefined specificity". Nature. 256 (5517): 495–7. Bibcode:1975Natur.256..495K. doi:10.1038/256495a0. PMID 1172191. S2CID 4161444.
- ^ Nadler LM, Stashenko P, Hardy R, Kaplan WD, Button LN, Kufe DW, Antman KH, Schlossman SF (September 1980). "Serotherapy of a patient with a monoclonal antibody directed against a human lymphoma-associated antigen". Cancer Research. 40 (9): 3147–54. PMID 7427932.
- ^ Ritz J, Schlossman SF (January 1982). "Utilization of monoclonal antibodies in the treatment of leukemia and lymphoma". Blood. 59 (1): 1–11. doi:10.1182/blood.V59.1.1.1. PMID 7032624.
- ^ a b c Stern M, Herrmann R (April 2005). "Overview of monoclonal antibodies in cancer therapy: present and promise". Critical Reviews in Oncology/Hematology. 54 (1): 11–29. doi:10.1016/j.critrevonc.2004.10.011. PMID 15780905.
- ^ a b c Hudson PJ, Souriau C (January 2003). "Engineered antibodies". Nature Medicine. 9 (1): 129–34. doi:10.1038/nm0103-129. PMID 12514726. S2CID 19243664.
- ^ Carter P, Presta L, Gorman CM, Ridgway JB, Henner D, Wong WL, Rowland AM, Kotts C, Carver ME, Shepard HM (May 1992). "Humanization of an anti-p185HER2 antibody for human cancer therapy". Proceedings of the National Academy of Sciences of the United States of America. 89 (10): 4285–9. Bibcode:1992PNAS...89.4285C. doi:10.1073/pnas.89.10.4285. PMC 49066. PMID 1350088.
- ^ Presta LG, Lahr SJ, Shields RL, Porter JP, Gorman CM, Fendly BM, Jardieu PM (September 1993). "Humanization of an antibody directed against IgE". Journal of Immunology. 151 (5): 2623–32. PMID 8360482.
- ^ Chothia C, Lesk AM, Tramontano A, Levitt M, Smith-Gill SJ, Air G, Sheriff S, Padlan EA, Davies D, Tulip WR (1989). "Conformations of immunoglobulin hypervariable regions". Nature. 342 (6252): 877–83. Bibcode:1989Natur.342..877C. doi:10.1038/342877a0. PMID 2687698. S2CID 4241051.
- ^ Jefferis R, Lefranc MP (July–August 2009). "Human immunoglobulin allotypes: possible implications for immunogenicity". mAbs. 1 (4): 332–8. doi:10.4161/mabs.1.4.9122. PMC 2726606. PMID 20073133.
- ^ Chapman K, Pullen N, Coney L, Dempster M, Andrews L, Bajramovic J, Baldrick P, Buckley L, Jacobs A, Hale G, Green C, Ragan I, Robinson V (2009). "Preclinical development of monoclonal antibodies: considerations for the use of non-human primates". mAbs. 1 (5): 505–16. doi:10.4161/mabs.1.5.9676. PMC 2759500. PMID 20065651.
- ^ Vennepureddy A, Singh P, Rastogi R, Atallah JP, Terjanian T (June 2016). "Evolution of ramucirumab in the treatment of cancer – A review of literature". Journal of Oncology Pharmacy Practice. 23 (7): 525–539. doi:10.1177/1078155216655474. PMID 27306885. S2CID 21298489.
- ^ de Zwart, Verena; Gouw, Samantha C; Meyer-Wentrup, Friederike AG (2016-01-19). "Antibody therapies for lymphoma in children". Cochrane Database of Systematic Reviews. 2016 (1): CD011181. doi:10.1002/14651858.cd011181.pub2. ISSN 1465-1858. PMC 8719646. PMID 26784573.
- ^ a b Rang, H. P. (2003). Pharmacology. Edinburgh: Churchill Livingstone. p. 241. ISBN 978-0-443-07145-4.
- ^ a b Pul, Refik; Dodel, Richard; Stangel, Martin (March 2011). "Antibody-based therapy in Alzheimer's disease". Expert Opinion on Biological Therapy. 11 (3): 343–357. doi:10.1517/14712598.2011.552884. PMID 21261567. S2CID 19375883.
- ^ a b c d van Dyck, Christopher (August 24, 2017). "Anti-Amyloid-β Monoclonal Antibodies for Alzheimer's Disease: Pitfalls and Promise". Biological Psychiatry. 83 (4): 311–319. doi:10.1016/j.biopsych.2017.08.010. PMC 5767539. PMID 28967385.
- ^ a b c d e Panza, F.; Imbimbo, B. P.; Logroscino, G. (2014). "Amyloid-directed monoclonal antibodies for the treatment of Alzheimer's disease: The point of no return?". Expert Opinion on Biological Therapy. 14 (10): 1465–76. doi:10.1517/14712598.2014.935332. PMID 24981190. S2CID 26323381.
- ^ Hanan, Eilat; Solomon, Beka (January 1996). "Inhibitory effect of monoclonal antibodies on Alzheimer's P-amyloid peptide aggregation". Amyloid. 2 (3): 130–133. doi:10.3109/13506129609014365.
- ^ Goel, Ayush. "Vasogenic cerebral oedema". radiopaedia.org. Retrieved 2017-11-01.
- ^ a b Panza, F.; Imbimbo, B.P.; D'aOnofrio, G.; Pietrarossa, G.; Seripa, Davide; Frisardi, V. (November 2010). "Bapineuzumab: anti-β-amyloid monoclonal antibodies for the treatment of Alzheimer's disease". Immunotherapy. 2 (6): 767–82. doi:10.2217/imt.10.80. PMID 21091109.
- ^ Logovinsky, Veronika; Satlin, Andrew; Lai, Robert; Swanson, Chad; Kaplow, June; Osswald, Gunilla; Basun, Hans; Lannfelt, Lars (December 2016). "Safety and tolerability of BAN2401 – a clinical study in Alzheimer's disease with a protofibril selective Aβ antibody". Alzheimer's Research & Therapy. 8 (1): 14. doi:10.1186/s13195-016-0181-2. ISSN 1758-9193. PMC 4822297. PMID 27048170.
- ^ "A Study to Confirm Safety and Efficacy of BAN2401 in Participants With Early Alzheimer's Disease". Case Medical Research. 2019-03-25. doi:10.31525/ct1-nct03887455. ISSN 2643-4652. S2CID 242999976.
- ^ Francis RJ, Sharma SK, Springer C, Green AJ, Hope-Stone LD, Sena L, Martin J, Adamson KL, Robbins A, Gumbrell L, O'Malley D, Tsiompanou E, Shahbakhti H, Webley S, Hochhauser D, Hilson AJ, Blakey D, Begent RH (September 2002). "A phase I trial of antibody directed enzyme prodrug therapy (ADEPT) in patients with advanced colorectal carcinoma or other CEA producing tumours". British Journal of Cancer. 87 (6): 600–7. doi:10.1038/sj.bjc.6600517. PMC 2364249. PMID 12237768.
- ^ Krauss WC, Park JW, Kirpotin DB, Hong K, Benz CC (2000). "Emerging antibody-based HER2 (ErbB-2/neu) therapeutics". Breast Disease. 11: 113–24. doi:10.3233/bd-1999-11110. PMID 15687597.
- ^ Joyce JA, Fearon DT (April 2015). "T cell exclusion, immune privilege, and the tumor microenvironment". Science. 348 (6230): 74–80. Bibcode:2015Sci...348...74J. doi:10.1126/science.aaa6204. PMID 25838376. S2CID 11603692.
- ^ Hooks MA, Wade CS, Millikan WJ (1991). "Muromonab CD-3: a review of its pharmacology, pharmacokinetics, and clinical use in transplantation". Pharmacotherapy. 11 (1): 26–37. doi:10.1002/j.1875-9114.1991.tb03595.x (inactive 31 July 2022). PMID 1902291.
{{cite journal}}: CS1 유지 : 2022년 7월 현재 DOI 비활성화 (링크) - ^ Chames P, Baty D (2009). "Bispecific antibodies for cancer therapy: the light at the end of the tunnel?". mAbs. 1 (6): 539–47. doi:10.4161/mabs.1.6.10015. PMC 2791310. PMID 20073127.
- ^ Linke, Rolf; Klein, Anke; Seimetz, Diane (2010). "Catumaxomab: Clinical development and future directions". mAbs. 2 (2): 129–136. doi:10.4161/mabs.2.2.11221. PMC 2840231. PMID 20190561.
- ^ Scolnik PA (2009). "mAbs: a business perspective". mAbs. 1 (2): 179–84. doi:10.4161/mabs.1.2.7736. PMC 2725420. PMID 20061824.
- ^ Kelley B (2009). "Industrialization of mAb production technology: the bioprocessing industry at a crossroads". mAbs. 1 (5): 443–52. doi:10.4161/mabs.1.5.9448. PMC 2759494. PMID 20065641.
외부 링크
- 암관리 핸드북: 종양학적 약리요법의 원리 (등록 필요)