리툭시맙
Rituximab | |
| 단클론항체 | |
|---|---|
| 유형 | 전항체 |
| 원천 | 키메라(마우스/인간) |
| 대상 | CD20 |
| 임상자료 | |
| 상호 | 리툭산, 맛브테라, 맛브테라 SC 등 |
| 바이오시밀러 | rituximab-abbs,[1] rituximab-pvvr,[2] rituximab-arrx,[3] Riabni,[3] Riximyo,[4] Ruxience,[2] Truxima[1] |
| AHFS/Drugs.com | 모노그래프 |
| 메드라인 플러스 | a607038 |
| 라이센스 데이터 | |
| 임신 카테고리 |
|
| 경로 행정부. | 정맥주사 |
| 드럭 클래스 | 단클론항체 |
| ATC코드 | |
| 법적지위 | |
| 법적지위 | |
| 약동학적 자료 | |
| 생체이용률 | 100% (IV) |
| 제거 반감기 | 30~400시간 (용량별, 치료기간별 varies) |
| 배설 | 불확실: RES에서 식세포증 및 이화작용을 겪을 수 있음 |
| 식별자 | |
| CAS 번호 | |
| 드럭뱅크 | |
| 켐스파이더 |
|
| 유니아이 | |
| 케그 | |
| 쳄블 | |
| CompTox 대시보드 (EPA) | |
| ECHA 인포카드 | 100.224.382 |
| 화학 및 물리 데이터 | |
| 공식 | C6416H9874N1688O1987S44 |
| 어금니 질량 | 143860.04g·mol−1 |
| | |
리툭산이라는 브랜드명으로 판매되는 리툭시맙은 특정한 자가면역질환과 암의 종류를 치료하기 위해 사용되는 단일클론항체 약물입니다.[12]비호지킨림프종, 만성 림프구성 백혈병, 류마티스 관절염, 다발성 혈관염을 동반한 육아종증, 특발성 혈소판감소성 자반증, 펨피거스 벌리스, 빈혈성 그라비스 및 엡스타인-바 바이러스 양성 점막 피부 궤양에 사용됩니다.[12][13][14][15]느린 정맥 주사(IV 라인을 통해 천천히 주입)를 통해 투여됩니다.[12]리툭산의 바이오시밀러로는 블리츠시마, 리아브니, 리템비아, 리투엔차 등이 있습니다.턱셀라), 릭사톤, 룩시언스,[16][17] 트룩시마.
일반적인 부작용으로는 발진, 가려움, 저혈압, 호흡곤란 등이 있으며, 약을 복용한 후 2시간 이내에 흔히 발생합니다.감염도 흔합니다.[12]
심각한 부작용으로는 B형 간염의 재활성화, 진행성 다초점 백혈구 감소증, 독성 표피 괴사, 사망 등이 있습니다.[12][18]임신 중에 사용하는 것이 태아나 신생아에게 안전한지는 확실하지 않지만 유해하다고 증명되지는 않습니다.[5][12]
리툭시맙은 주로 면역체계 B 세포의 표면에서 발견되는 단백질 CD20에 대한 키메라 단클론 항체입니다.[19]이것이 이 단백질에 결합하면 세포 사멸을 유발합니다.[12]
리툭시맙은 1997년 의료용으로 승인되었습니다.[19]그것은 세계보건기구의 필수 의약품 목록에 올라있습니다.[20]리툭시맙은 미국 바이오젠과 제넨텍, 캐나다와 유럽연합(EU)의 호프만라로슈, 츄가이제약, 일본 젠야쿠코교, 이란 아료젠이 공동 판매하고 있습니다.[21]
의료용
리툭시맙(Rituximab)은 B 세포에 존재하는 표면 항원인 CD20을 표적으로 하는 키메라 단클론 항체입니다.따라서 CD20 표면항원이 발현되지 않아 혈장세포와 조혈모세포를 아끼지 않으면서 병원성 B세포 뿐만 아니라 정상세포를 고갈시키는 작용을 합니다.[22]
미국에서 리툭시맙은 다음을 치료하기 위해 표시됩니다.
- 비호지킨림프종(NHL)[10]
- 만성 림프구성 백혈병(CLL)[10]
- 하나 이상의 TNF 억제제에[10] 대한 반응이 부적절한 류마티스 관절염
- 다발혈관염을 동반한 육아종증이나 미세다기관염과[10] 같은 혈관염
- 중등도에서 중증의 페피구스속[10].
- 이전에 치료되지 않은, 진행 단계, CD20 양성 확산성 대규모 B세포 림프종(DLBCL), 버킷 림프종(BL), 버킷 유사 림프종(BLL) 또는 성숙 B세포 급성 백혈병(B-AL)과 함께 소아(≥ 6개월~<18세)의 항암 치료와 함께.
혈액암
리툭시맙은 비호지킨림프종, 만성 림프구성 백혈병, 결절성 림프구 우세 호지킨림프종 등 백혈구와 림프종 등의 암 치료에 사용됩니다.[24][25]여기에는 NHL의 일종인 Waldenström의 매크로글로불린혈증도 포함됩니다.[12]리툭시맙(Rituximab)은 히알루로니다제 휴먼(hyaluronidase human)과 병용하여 마브테라SC(MabTheraSC), 리툭산하이셀라(Rituxan Hycela)라는 브랜드명으로 판매되며,[26] 모낭림프종, 확산성큰B세포림프종, 만성림프구성백혈병 치료에 사용됩니다.[26]플루다라빈 및 사이클로포스파미드와 병용하여 이전에 치료되지 않은 CD20 양성 만성 림프구성 백혈병을 치료하는 방법.[10]
자가면역질환
리툭시맙은 세 번의 무작위 대조군 시험에서 효과적인 류마티스 관절염 치료제로 입증되었으며 현재 불응성 류마티스 질환에 사용할 수 있도록 허가되었습니다.[27]미국에서는 하나 이상의 항-TNF-알파 요법에 부적절한 반응을 보인 중간에서 심각한 활동성 류마티스 관절염(RA) 성인 환자의 징후와 증상을 줄이기 위해 메토트렉세이트(MTX)와 함께 사용하도록 FDA 승인을 받았습니다.유럽 연합에서는 라이센스가 약간 더 제한적입니다. 하나 이상의 항TNF 치료에 부적절한 반응을 보인 중증 활성 RA 환자에서 MTX와 함께 사용할 수 있도록 라이센스가 부여됩니다.[28]
다양한 다른 자가 면역 질환에서 효능에 대한 일부 증거가 있지만 반드시 안전성은 아닙니다. 리툭시맙은 다발성 경화증,[29][30] 전신 홍반성 루푸스, 만성 염증성 탈수성 다신경병증 및 자가 면역성 빈혈의 어려운 사례를 치료하기 위해 라벨 외로 널리 사용됩니다.[31]가장 위험하지만 부작용은 진행성 다초점 백혈구 증가증(PML) 감염으로 보통 치명적이지만 자가면역 질환에서 발생하는 사례는 극히 일부만 기록되어 있습니다.[31][32]
리툭시맙으로 치료된 다른 자가면역 질환으로는 자가면역용혈성 빈혈, 순수 적혈구형성증, 혈전성 혈소판감소성 자반증([33][34][35]TP), 특발성 혈소판감소성 자반증(ITP), 에반스 증후군,[36] 혈관염(다기관염을 동반한 육아종증), 황소 피부 질환(예: 펨피구스, 펨피구이드)이 있습니다.2006년 연구에 따르면, 우리의 노화 결과는 펨피거스에서 약 85%의 빠른 회복을 나타냄),[37] 제1형 당뇨병, 쇼그렌 증후군, 항-NMDA 수용체 뇌염 및 데빅스 질환(Anti-AQP4 질환, MOG 항체 질환),[38] 그레이브스 안과병증,[39] 자가면역 췌장염,[40] OMS(Opsoclonus myoclonus syndrome),[41] IgG4 관련 질환.[42]IgA 매개 자가면역질환 치료에 효과가 없다는 증거가 있습니다.[43]
유해사례
사망 및 장애를 유발할 수 있는 심각한 부작용은 다음과 같습니다.[10][12]
- 심각한 주입반응
- 심정지
- 사이토카인 방출 증후군
- 급성 신장 손상을 일으키는 종양 용해 증후군
- 감염증[44]
- JC 바이러스 재활성화에[45] 의한 진행성 다초점 백혈구증(PML)
- B형 간염 재활성화
- 기타 바이러스 감염[46]
- 림프종 환자의 70~80%에서 B세포가 고갈되는 면역 독성
- 폐독성[47]
- 장폐색 및 천공[48]
전신홍반 루푸스 환자 2명 리툭시맙 치료 후 진행성 다초점 백혈구감소증(PML)으로 사망PML은 보통 잠재되어 있는 뇌의 흔한 바이러스인 JC 바이러스의 활성화에 의해 발생합니다.JC 바이러스의 재활성화는 보통 사망이나 심각한 뇌 손상을 초래합니다.[49]
류마티스 관절염 환자 중 적어도 한 명은 리툭시맙으로 치료한 후 PML이 발생했습니다.[50]
리툭시맙은 림프종이 있는 사람의 만성 E형 간염 감염의 가능한 보조 인자로 보고되었습니다.E형 간염은 일반적으로 급성 감염이며, 림프종과 함께 이 약이 바이러스에 대한 신체의 면역 반응을 약화시켰을 수 있음을 시사합니다.[51]
지속적인 리툭시맙 치료의 주요 관심사는 적절한 백신 반응을 유도하기 어렵다는 것입니다.[52]이는 다발성 경화증과 리툭시맙 치료를 받는 사람들이 심각한 코로나19 위험이 더 높았던 코로나19 팬데믹 기간 동안 초점이 맞춰졌습니다.[53]다발성 경화증의 리툭시맙 치료를 받은 환자에서 B세포 수가 40/ µL 이상인 환자 10명 중 9명은 tozinameran으로 백신 접종 후 항체의 보호 수준이 생겼습니다.
작용기전
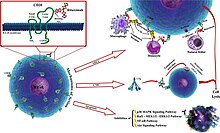

항체는 세포 표면 단백질 CD20에 결합합니다.CD20은 초기 전-B 세포에서 나중에 분화할 때까지 B 세포에서 광범위하게 발현되지만, 말단 분화된 혈장 세포에서는 없습니다.CD20의 기능은 알려져 있지 않지만, 세포 내 Ca 농도를2+ 유지하고 B 세포의 활성화를 가능하게 하는 플라즈마 막을 가로질러 Ca가2+ 유입되는 역할을 할 수 있습니다.
리툭시맙은 CD20 세포 표면 수준이 낮은 세포를 제거하는 데 상대적으로 효과적이지 않습니다.[56]그것은 CD20이 있는 B세포의 한쪽에 달라붙는 경향이 있고, 캡을 형성하고 그 쪽으로 단백질을 끌어당깁니다.모자의 존재는 이러한 B세포를 파괴하는 자연살해세포의 효과를 변화시킵니다.NK세포가 캡에 걸렸을 때 세포를 죽이는 데 80%의 성공률을 보였습니다.반면 B세포가 이 비대칭 단백질 클러스터를 결여하고 있을 때는 40%만 사멸했습니다.[57]
다음과 같은 효과가 있습니다.[58]
- 리툭시맙의 Fc 부분은 항체 의존성 세포 독성(ADCC)과 보체 의존성 세포 독성(CDC)을 매개합니다.[59]
- 리툭시맙은 세포 주기에 일반적인 조절 효과가 있습니다.
- 특히 만성 림프구성 백혈병(CLL)[56]에서 CD20 수치가 높고 BCR 신호전달 성향이 높은 악성 B세포의 우선적 제거.
- MHC II 및 부착 분자 LFA-1 및 LFA-3(림프구 기능-연관 항원)을 증가시킵니다.
- CD23의 유출을 유도합니다.
- 이것은 B세포 수용체를 억제합니다.
- CD20+ 세포의 사멸을 유도합니다.
- 리툭시맙은 또한 면역 니치로부터 일부 만성 림프구성 백혈병 세포의 방출을 유도하는데, 이것은 그들이 항-CD20 항체와 함께 사용되는 화학 요법에 더 민감하게 만들 수 있습니다.[59]
결합된 효과는 몸에서 B 세포 (암을 포함한)의 제거를 초래하여 림프 줄기 세포로부터 건강한 B 세포의 새로운 집단이 발달할 수 있게 합니다.
리툭시맙은 CD20에서 아미노산 170–173과 182–185에 결합하는데, 이들은 아미노산 167과 183 사이의 이황화 결합의 결과로 물리적으로 서로 가깝습니다.[60]
역사
리툭시맙은 IDEC-C2B8이라는 이름으로 IDEC Pharmaceuticals에 의해 개발되었습니다.이 약에 대한 미국의 특허는 1998년에 발급되었고 2015년에 만료되었습니다.[61]
리툭시맙은 임상시험에서 안전성과 효과를 바탕으로 1997년 미국 식품의약국에 의해 다른 화학요법 요법에 내성이 있는 B세포 비호지킨림프종을 치료하도록 승인되었습니다.[62][63]리툭시맙은 CHOP 화학요법과 함께 확산성 큰 B세포 림프종 및 다른 많은 B세포 림프종의 치료에 있어 CHOP 단독보다 우수합니다.[64]2010년 유럽연합 집행위원회로부터 엽상 림프종의 초기 치료 후 유지치료 승인을 받았습니다.[65]
그것은 세계보건기구의 필수 의약품 목록에 올라있습니다.[20]
2014년, 제넨텍은 리툭산을 전문의약품으로 재분류하였는데, 이는 미국 내 전문 유통업체를 통해서만 구입할 수 있는 의약품의 한 종류입니다.[66]도매상 할인과 리베이트가 더 이상 적용되지 않기 때문에 병원은 더 많은 비용을 지불할 것입니다.[66]
원래 정맥 주사(예: 2.5시간 이상)를 위해 사용할 수 있었으나, 2016년에 B-세포 CLL/림프종(CLL)에 대한 피하주사 제형으로 EU 승인을 받았습니다.[67]
사회와 문화
경제학
유럽에서는 2013년 2월에, 미국에서는 2016년 9월에 특허가 만료되었습니다.[failed verification][68]2018년[update] 11월까지 미국, 인도, 유럽 연합, 스위스, 일본 및 호주에서 여러 바이오시밀러가 승인되었습니다.미국 FDA는 2018년 트룩시마(리툭시맙-abbs), 2019년 룩시언스(리툭시맙-pvvr), 2020년 리아브니(리툭시맙-arx)를 승인했습니다.후자는 500mg 당 약 3600달러, 도매, 목록입니다.[69][68][70][71]
조사.
만성피로증후군
리툭시맙은 2019년 발표된 실험에서 만성피로증후군 환자의 증상이 개선되지 않았습니다.[72][73]22%의 참가자들이 심각한 사건을 겪었습니다.[72]리툭시맙으로 치료된 두 명의 암 환자들에게서 만성 피로 증후군의 개선이 나타난 후 이러한 잠재적인 사용이 조사되었습니다.[74]
추강내
CNS 질환의 경우 리툭시맙을 혈관 내에 투여할 수 있으며 이러한 가능성은 연구 중에 있습니다.[75]
기타 항CD20 단클론
리툭시맙의 효능과 성공은 일부 다른 항-CD20 단클론 항체를 개발하게 만들었습니다.
- Ocrelizumab, 인간화된 (90%-95% 인간) B 세포 파괴제.
- 완전한 인간 B 세포 파괴제인 ofatumumab (HuMax-CD20).[76]
- 오비누투주맙과 같은 3세대 항CD20은 Fc 감마 수용체에 대한 결합력이 강화된 글리코젠티드 Fc 단편(Fc)[77]을 가지고 있으며, 이는 ADCC(항체 의존성 세포 독성)를 증가시킵니다.[78]표시된 Fc 글리칸이 Fc 수용체에 대한 항체의 친화도를 조절한다는 점을 이용하여, 단일클론 항체의 ADCC 유도능을 향상시키기 위한 이 방법.[79]
참고문헌
- ^ a b c "Truxima- rituximab-abbs injection solution". DailyMed. Retrieved 26 March 2021.
- ^ a b c "Ruxience- rituximab-pvvr injection solution". DailyMed. Retrieved 26 March 2021.
- ^ a b c "Riabni- rituximab-arrx injection solution". DailyMed. Retrieved 26 March 2021.
- ^ "Summary Basis of Decision (SBD) for Riximyo". Health Canada. 23 October 2014. Retrieved 29 May 2022.
- ^ a b "Rituximab Use During Pregnancy". Drugs.com. 16 December 2019. Retrieved 2 February 2020.
- ^ Rituximab (rch) (CAS 등록번호: 174722-31-7) Wayback Machine에서 2015년 11월 30일 보관
- ^ 호주 제품 정보. MabThera® SC(리툭시맙)2021년 5월 13일 웨이백 머신(Wayback Machine)에서 보관됨
- ^ "MabThera 100 mg Concentrate for Solution for Infusion - Summary of Product Characteristics (SmPC)". (emc). 13 March 2021. Retrieved 26 March 2021.
- ^ "MabThera 1400 mg Solution for Subcutaneous Injection - Summary of Product Characteristics (SmPC)". (emc). 13 March 2021. Retrieved 26 March 2021.
- ^ a b c d e f g h "Rituxan- rituximab injection, solution". DailyMed. 6 November 2019. Retrieved 2 February 2020.
- ^ "MabThera EPAR". European Medicines Agency. 17 September 2018. Retrieved 8 September 2021.
- ^ a b c d e f g h i "Rituximab". The American Society of Health-System Pharmacists. Archived from the original on 27 March 2016. Retrieved 8 December 2016.
- ^ Tandan R, Hehir MK, Waheed W, Howard DB (August 2017). "Rituximab treatment of myasthenia gravis: A systematic review". Muscle & Nerve. 56 (2): 185–196. doi:10.1002/mus.25597. PMID 28164324. S2CID 19504332.
- ^ Singer O, McCune WJ (May 2017). "Update on maintenance therapy for granulomatosis with polyangiitis and microscopic polyangiitis". Current Opinion in Rheumatology. 29 (3): 248–253. doi:10.1097/BOR.0000000000000382. PMID 28306595. S2CID 35805200.
- ^ Dojcinov SD, Fend F, Quintanilla-Martinez L (March 2018). "EBV-Positive Lymphoproliferations of B- T- and NK-Cell Derivation in Non-Immunocompromised Hosts". Pathogens. 7 (1): 28. doi:10.3390/pathogens7010028. PMC 5874754. PMID 29518976.
- ^ "Rituximab Biosimilars Shown to Be Safe and Effective". www.medscape.com. Archived from the original on 15 March 2018. Retrieved 29 November 2017.
- ^ "rituximab Ligand page IUPHAR/BPS Guide to PHARMACOLOGY". www.guidetopharmacology.org.
- ^ "Boxed Warning and new recommendations to decrease risk of hepatitis B reactivation with the immune-suppressing and anti-cancer drugs Arzerra (ofatumumab) and Rituxan (rituximab)". U.S. Food and Drug Administration (FDA). 29 February 2016. Retrieved 2 February 2020.
- ^ a b Bosch X, Ramos-Casals M, Khamashta MA (2013). Drugs Targeting B-Cells in Autoimmune Diseases. Springer Science & Business Media. pp. 1–4. ISBN 9783034807067. Archived from the original on 5 November 2017.
- ^ a b World Health Organization (2019). World Health Organization model list of essential medicines: 21st list 2019. Geneva: World Health Organization. hdl:10665/325771. WHO/MVP/EMP/IAU/2019.06. License: CC BY-NC-SA 3.0 IGO.
- ^ "FDA Approves Rituxan Plus Chemotherapy for the Most Common Type of Adult Leukemia" (Press release). Biogen.
- ^ De A, Ansari A, Sharma N, Sarda A (2017). "Shifting Focus in the Therapeutics of Immunobullous Disease". Indian Journal of Dermatology. 62 (3): 282–290. doi:10.4103/ijd.IJD_199_17 (inactive 1 August 2023). PMC 5448263. PMID 28584371.
{{cite journal}}: CS1 메인 : 2023년 8월 기준 DOI 비활성화 (링크) - ^ "FDA approves rituximab plus chemotherapy for pediatric cancer indicati". U.S. Food and Drug Administration. 3 December 2021. Retrieved 4 December 2021.
 이 기사는 공용 도메인에 있는 이 소스의 텍스트를 통합합니다.
이 기사는 공용 도메인에 있는 이 소스의 텍스트를 통합합니다. - ^ Saini KS, Azim HA, Cocorocchio E, Vanazzi A, Saini ML, Raviele PR, et al. (August 2011). "Rituximab in Hodgkin lymphoma: is the target always a hit?". Cancer Treatment Reviews. 37 (5): 385–390. doi:10.1016/j.ctrv.2010.11.005. PMID 21183282.
- ^ Eichenauer DA, Engert A (December 2017). "Nodular lymphocyte-predominant Hodgkin lymphoma: a unique disease deserving unique management". Hematology. American Society of Hematology. Education Program. 2017 (1): 324–328. doi:10.1182/asheducation-2017.1.324. PMC 6142570. PMID 29222274.
- ^ a b "Rituxan Hycela- rituximab and hyaluronidase injection, solution". DailyMed. 3 December 2019. Retrieved 2 February 2020.
- ^ Edwards JC, Szczepanski L, Szechinski J, Filipowicz-Sosnowska A, Emery P, Close DR, et al. (June 2004). "Efficacy of B-cell-targeted therapy with rituximab in patients with rheumatoid arthritis". The New England Journal of Medicine. 350 (25): 2572–2581. doi:10.1056/NEJMoa032534. PMID 15201414.
- ^ Tak PP, Kalden JR (May 2011). "Advances in rheumatology: new targeted therapeutics". Arthritis Research & Therapy. 13 (Suppl 1): S5. doi:10.1186/1478-6354-13-S1-S5. PMC 3123966. PMID 21624184.
- ^ McGinley MP, Moss BP, Cohen JA (January 2017). "Safety of monoclonal antibodies for the treatment of multiple sclerosis". Expert Opinion on Drug Safety. 16 (1): 89–100. doi:10.1080/14740338.2017.1250881. PMID 27756172. S2CID 36762194.
- ^ He D, Guo R, Zhang F, Zhang C, Dong S, Zhou H (December 2013). "Rituximab for relapsing-remitting multiple sclerosis". The Cochrane Database of Systematic Reviews (12): CD009130. doi:10.1002/14651858.CD009130.pub3. PMID 24310855.
- ^ a b Paul M (20 May 2009). "Popular Cancer Drug Linked to Often Fatal 'Brain Eating' Virus". Northwestern University News and Information. Archived from the original on 29 May 2010. Retrieved 22 May 2009.
- ^ "FDA Warns of Safety Concern Regarding Rituxan in New Patient Population". U.S. Food and Drug Administration (FDA) (Press release). 18 December 2006. Archived from the original on 13 May 2009. Retrieved 29 April 2013.
- ^ Froissart A, Veyradier A, Hié M, Benhamou Y, Coppo P (November 2015). "Rituximab in autoimmune thrombotic thrombocytopenic purpura: A success story". European Journal of Internal Medicine. 26 (9): 659–665. doi:10.1016/j.ejim.2015.07.021. PMID 26293834.
- ^ Braendstrup P, Bjerrum OW, Nielsen OJ, Jensen BA, Clausen NT, Hansen PB, et al. (April 2005). "Rituximab chimeric anti-CD20 monoclonal antibody treatment for adult refractory idiopathic thrombocytopenic purpura". American Journal of Hematology. 78 (4): 275–280. doi:10.1002/ajh.20276. PMID 15795920. S2CID 42218074.
- ^ Patel V, Mihatov N, Cooper N, Stasi R, Cunningham-Rundles S, Bussel JB (2007). "Long-term responses seen with rituximab in patients with ITP" (PDF). Community Oncology. 4 (2): 107. doi:10.1016/s1548-5315(11)70061-4. Archived from the original (PDF) on 29 September 2007. Retrieved 18 April 2007.
- ^ Shanafelt TD, Madueme HL, Wolf RC, Tefferi A (November 2003). "Rituximab for immune cytopenia in adults: idiopathic thrombocytopenic purpura, autoimmune hemolytic anemia, and Evans syndrome". Mayo Clinic Proceedings. 78 (11): 1340–1346. doi:10.4065/78.11.1340. PMID 14601692.
- ^ Ahmed AR, Spigelman Z, Cavacini LA, Posner MR (October 2006). "Treatment of pemphigus vulgaris with rituximab and intravenous immune globulin". The New England Journal of Medicine. 355 (17): 1772–1779. doi:10.1056/nejmoa062930. PMID 17065638.
- ^ Jacob A, Weinshenker BG, Violich I, McLinskey N, Krupp L, Fox RJ, et al. (November 2008). "Treatment of neuromyelitis optica with rituximab: retrospective analysis of 25 patients". Archives of Neurology. 65 (11): 1443–1448. doi:10.1001/archneur.65.11.noc80069. PMID 18779415.
- ^ "Rituximab Treatment of Patients with Severe, Corticosteroid-Resistant Thyroid-Associated Ophthalmopathy". Archived from the original on 22 August 2017. Retrieved 19 October 2011.
- ^ Hart PA, Chari ST (11 June 2013). "Immunomodulators and Rituximab in the Management of Autoimmune Pancreatitis". Pancreapedia. doi:10.3998/panc.2013.20.
- ^ Pranzatelli MR, Tate ED, Travelstead AL, Longee D (January 2005). "Immunologic and clinical responses to rituximab in a child with opsoclonus-myoclonus syndrome". Pediatrics. 115 (1): e115–e119. doi:10.1542/peds.2004-0845. PMID 15601813.
- ^ Khosroshahi A, Wallace ZS, Crowe JL, Akamizu T, Azumi A, Carruthers MN, et al. (July 2015). "International Consensus Guidance Statement on the Management and Treatment of IgG4-Related Disease". Arthritis & Rheumatology. 67 (7): 1688–1699. doi:10.1002/art.39132. PMID 25809420. S2CID 39750214.
- ^ He Y, Shimoda M, Ono Y, Villalobos IB, Mitra A, Konia T, et al. (June 2015). "Persistence of Autoreactive IgA-Secreting B Cells Despite Multiple Immunosuppressive Medications Including Rituximab". JAMA Dermatology. 151 (6): 646–650. doi:10.1001/jamadermatol.2015.59. PMID 25901938.
- ^ Kyriakidis, Ioannis; Mantadakis, Elpis; Stiakaki, Eftichia; Groll, Andreas (October 2022). "Infectious Complications of Targeted Therapies in Children with Leukemias and Lymphomas". Cancers. 14 (20): 5022. doi:10.3390/cancers14205022. PMC 9599435. PMID 36291806.
- ^ Molloy ES, Calabrese LH (September 2012). "Progressive multifocal leukoencephalopathy associated with immunosuppressive therapy in rheumatic diseases: evolving role of biologic therapies". Arthritis and Rheumatism. 64 (9): 3043–3051. doi:10.1002/art.34468. PMID 22422012.
- ^ Grammatikos, Alexandros; Donati, Matthew; Johnston, Sarah L.; Gompels, Mark M. (30 August 2021). "Peripheral B Cell Deficiency and Predisposition to Viral Infections: The Paradigm of Immune Deficiencies". Frontiers in Immunology. 12. 731643. doi:10.3389/fimmu.2021.731643. PMC 8435594. PMID 34527001.
- ^ Burton C, Kaczmarski R, Jan-Mohamed R (June 2003). "Interstitial pneumonitis related to rituximab therapy". The New England Journal of Medicine. 348 (26): 2690–1, discussion 2690–1. doi:10.1056/NEJM200306263482619. PMID 12826649.
- ^ "Reports of Bowel Obstruction and Perforation with RITUXAN (rituximab)" (PDF). Roche Canada. 10 November 2006. Archived from the original (PDF) on 27 March 2014.
- ^ "Rituximab (marketed as Rituxan) Information". U.S. Food and Drug Administration (FDA). 23 July 2015. Archived from the original on 15 November 2009. Retrieved 15 November 2009.
- ^ "Rituximab, RA and PML" (PDF). U.S. Food and Drug Administration (FDA). Archived from the original (PDF) on 16 September 2008. Retrieved 14 September 2008.
- ^ Kriston L, Härter M, Hölzel L (March 2009). "Challenges in reporting meta-analyses of diagnostic accuracy studies". Annals of Internal Medicine. 150 (6): 430. doi:10.7326/0003-4819-150-6-200903170-00025. PMID 19293085.
- ^ Oren S, Mandelboim M, Braun-Moscovici Y, Paran D, Ablin J, Litinsky I, et al. (July 2008). "Vaccination against influenza in patients with rheumatoid arthritis: the effect of rituximab on the humoral response". Annals of the Rheumatic Diseases. 67 (7): 937–941. doi:10.1136/ard.2007.077461. PMID 17981914. S2CID 21878513.
- ^ Spelman T, Forsberg L, McKay K, Glaser A, Hillert J (June 2022) [EPub July 2, 2021 (date first published online - nearly a year earlier)]. "Increased rate of hospitalisation for COVID-19 among rituximab-treated multiple sclerosis patients: A study of the Swedish multiple sclerosis registry". Multiple Sclerosis. 28 (7): 1051–1059. doi:10.1177/13524585211026272. PMID 34212816. S2CID 235710318.
- ^ Tolf A, Wiberg A, Müller M, Nazir FH, Pavlovic I, Laurén I, et al. (May 2022). "Factors Associated With Serological Response to SARS-CoV-2 Vaccination in Patients With Multiple Sclerosis Treated With Rituximab". JAMA Network Open. 5 (5): e2211497. doi:10.1001/jamanetworkopen.2022.11497. PMC 9096596. PMID 35544139. S2CID 248695128.
- ^ Seyfizadeh N, Seyfizadeh N, Hasenkamp J, Huerta-Yepez S (January 2016). "A molecular perspective on rituximab: A monoclonal antibody for B cell non Hodgkin lymphoma and other affections". Critical Reviews in Oncology/Hematology. 97: 275–290. doi:10.1016/j.critrevonc.2015.09.001. PMID 26443686.
- ^ a b Pavlasova G, Borsky M, Svobodova V, Oppelt J, Cerna K, Novotna J, et al. (September 2018). "Rituximab primarily targets an intra-clonal BCR signaling proficient CLL subpopulation characterized by high CD20 levels". Leukemia. 32 (9): 2028–2031. doi:10.1038/s41375-018-0211-0. PMID 30030508.
- ^ Rudnicka D, Oszmiana A, Finch DK, Strickland I, Schofield DJ, Lowe DC, et al. (June 2013). "Rituximab causes a polarization of B cells that augments its therapeutic function in NK-cell-mediated antibody-dependent cellular cytotoxicity". Blood. 121 (23): 4694–4702. doi:10.1182/blood-2013-02-482570. PMID 23613524.
- ^ Shaw T, Quan J, Totoritis MC (November 2003). "B cell therapy for rheumatoid arthritis: the rituximab (anti-CD20) experience". Annals of the Rheumatic Diseases. 62 (Suppl 2): ii55–ii59. doi:10.1136/ard.62.suppl_2.ii55. PMC 1766758. PMID 14532151.
- ^ a b Borsky M, Hrabcakova V, Novotna J, Brychtova Y, Doubek M, Panovska A, et al. (December 2021). "Rituximab induces rapid blood repopulation by CLL cells mediated through their release from immune niches and complement exhaustion". Leukemia Research. 111: 106684. doi:10.1016/j.leukres.2021.106684. PMID 34438120.
- ^ Binder M, Otto F, Mertelsmann R, Veelken H, Trepel M (September 2006). "The epitope recognized by rituximab". Blood. 108 (6): 1975–1978. doi:10.1182/blood-2006-04-014639. PMID 16705086.
- ^ "Rituximab". go.drugbank.com. Archived from the original on 5 January 2014. Retrieved 14 March 2023.
- ^ Maloney DG, Grillo-López AJ, White CA, Bodkin D, Schilder RJ, Neidhart JA, et al. (September 1997). "IDEC-C2B8 (Rituximab) anti-CD20 monoclonal antibody therapy in patients with relapsed low-grade non-Hodgkin's lymphoma". Blood. 90 (6): 2188–2195. doi:10.1182/blood.V90.6.2188. PMID 9310469.
- ^ Scott SD (1998). "Rituximab: a new therapeutic monoclonal antibody for non-Hodgkin's lymphoma". Cancer Practice. 6 (3): 195–197. doi:10.1046/j.1523-5394.1998.006003195.x. PMID 9652253.
- ^ 해리슨의 내과학 원리, Longo et al.맥그로힐 메디컬 2011 페이지 931
- ^ "Roche Gets EC Nod for Follicular Lymphoma Maintenance Therapy". 29 October 2010. Archived from the original on 31 October 2010.
- ^ a b Saporito B (27 October 2014). "Hospitals Furious at Cancer-Drug Price Hikes". Time. Archived from the original on 20 October 2015. Retrieved 26 October 2015.
- ^ "EU approves second indication for subcutaneous form of Roche's rituximab". Archived from the original on 7 June 2016. Retrieved 9 June 2016.
- ^ a b "Biosimilars of Rituximab". Generics and Biosimilars Initiative. 14 April 2017. Archived from the original on 31 March 2017. Retrieved 29 April 2017.
- ^ "FDA approves first biosimilar for treatment of adult patients with non-Hodgkin's lymphoma". U.S. Food and Drug Administration (FDA) (Press release). 28 November 2018. Retrieved 11 November 2019.
- ^ Lahiri D, Osterman C (2 November 2018). "Novartis abandons effort for U.S. approval of biosimilar rituximab". Reuters. Retrieved 3 November 2018.
- ^ "Amgen Rituximab Biosimilar Gains FDA Approval". The Center For Biosimilars.
- ^ a b Fluge Ø, Rekeland IG, Lien K, Thürmer H, Borchgrevink PC, Schäfer C, et al. (May 2019). "B-Lymphocyte Depletion in Patients With Myalgic Encephalomyelitis/Chronic Fatigue Syndrome: A Randomized, Double-Blind, Placebo-Controlled Trial". Annals of Internal Medicine. 170 (9): 585–593. doi:10.7326/M18-1451. PMID 30934066. S2CID 91186383.
- ^ Tucker ME (2 April 2019). "Rituximab Fails to Improve Symptoms in ME/CFS". Medscape.
- ^ Castro-Marrero J, Sáez-Francàs N, Santillo D, Alegre J (March 2017). "Treatment and management of chronic fatigue syndrome/myalgic encephalomyelitis: all roads lead to Rome". British Journal of Pharmacology. 174 (5): 345–369. doi:10.1111/bph.13702. PMC 5301046. PMID 28052319.
- ^ Bonnan M, Ferrari S, Bertandeau E, Demasles S, Krim E, Miquel M, Barroso B (2014). "Intrathecal rituximab therapy in multiple sclerosis: review of evidence supporting the need for future trials". Current Drug Targets. 15 (13): 1205–1214. doi:10.2174/1389450115666141029234644. PMID 25355180.
- ^ "Genmab.com / HuMax-CD20 (ofatumumab)". Archived from the original on 11 September 2007. Retrieved 3 December 2007.
- ^ "Fc-structure". Archived from the original on 10 November 2007. Retrieved 3 December 2007.
- ^ Eccles SA (2001). "Monoclonal antibodies targeting cancer: 'magic bullets' or just the trigger?". Breast Cancer Research. 3 (2): 86–90. doi:10.1186/bcr276. PMC 138676. PMID 11250751.
- ^ Maverakis E, Kim K, Shimoda M, Gershwin ME, Patel F, Wilken R, et al. (February 2015). "Glycans in the immune system and The Altered Glycan Theory of Autoimmunity: a critical review". Journal of Autoimmunity. 57 (6): 1–13. doi:10.1016/j.jaut.2014.12.002. PMC 4340844. PMID 25578468.
외부 링크
- "Rituximab". Drug Information Portal. U.S. National Library of Medicine.
- "Discovery – Development of Rituximab". National Cancer Institute. 7 March 2014.