다비가트란
Dabigatran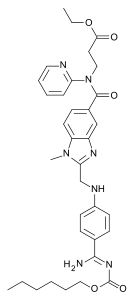 | |
| 임상자료 | |
|---|---|
| 상명 | 프라닥사, 프라닥사, 프라작사, 기타 |
| 기타 이름 | Dabigatran etexital (USAN ) |
| AHFS/Drugs.com | 모노그래프 |
| 메드라인플러스 | a610024 |
| 라이센스 데이터 | |
| 임신 범주 |
|
| 경로: 행정 | 입으로 |
| ATC 코드 | |
| 법적현황 | |
| 법적현황 | |
| 약동학 데이터 | |
| 생체이용가능성 | 3–7%[3] |
| 단백질 결합 | 35%[3] |
| 제거 반감기 | 12-17시간[3] |
| 식별자 | |
| |
| CAS 번호 | |
| 펍켐 CID | |
| 드러그뱅크 | |
| 켐스파이더 | |
| 유니 | |
| 케그 | |
| 체비 | |
| 켐벨 | |
| CompTox 대시보드 (EPA) | |
| 화학 및 물리적 데이터 | |
| 공식 | C34H41N7O5 |
| 어금질량 | 627.746 g·190−1 |
| 3D 모델(JSmol) | |
| |
| |
| | |
그중 프라닥사라는 상표명으로 판매되는 다비가트란은 혈액 응고를 치료하고 예방하며 심방세동 환자의 뇌졸중을 예방하는데 사용되는 항응고제다.[3][4] 특히 고관절이나 무릎 교체에 따른 혈액 응고 및 이전 응고 이력이 있는 혈액의 응고 예방을 위해 사용된다.[3] 와파린의 대안으로 사용되며 혈액검사에 의한 감시가 필요 없다.[3] 그것은 입으로 가져간다.[3]
일반적인 부작용으로는 출혈과 위염이 있다.[3] 다른 부작용으로는 척추 주변의 출혈과 과민증과 같은 알레르기 반응이 있을 수 있다.[3] 출혈이 심한 경우에는 해독제인 이다루치즈맙으로 되돌릴 수 있다.[3] 임신이나 모유 수유 중에는 사용을 권장하지 않는다.[3] 와파린에 비해 다른 약품과의 상호작용이 적다.[5] 그것은 직접적인 트롬빈 억제제다.[4]
다비가트란은 2010년 미국에서 의료용 허가를 받았다.[3] 그것은 세계보건기구의 필수 의약품 목록에 올라 있다.[6] 2017년에는 미국에서 가장 흔하게 처방된 302번째로 100만 개 이상의 처방전이 있었다.[7] 다비가트란 이텍스틸은 2020년 미국에서 일반 의약품으로 승인됐다.[8]
의학적 용법
다비가트란은 심방세동(심방세동)이 심방세동(심방세동)에 의한 뇌졸중을 예방하고, 종양항응고제(보통 분자량헤파린)로 5~10일 치료받은 사람의 심방혈전증, 폐색전증 등을 일부 회로에 방지하는 데 쓰인다.mstances[2]
판막문제로 인한 것이 아니라 심방세동이 있는 사람의 비혈성 뇌졸중과 색전증 예방에 와파린만큼 효과가 있는 것으로 보인다.[9][10]
콘트라인커뮤니케이션
다비가트란은 적극적인 병리학적 출혈이 있는 환자들에게 금지되는데, 다비가트란은 출혈 위험을 증가시킬 수 있고 또한 심각하고 잠재적으로 생명을 위협하는 출혈을 일으킬 수 있기 때문이다.[2] 다비가트란은 다비가트란에 대한 심각한 과민성 반응 이력이 있는 환자(예: 아나필락시스 또는 아나필락틱 쇼크)에서도 억제된다.[2] 또한 혈전증, 뇌졸중, 심근경색 등 혈전증 발병 위험이 증가하고 이 모집단의 다비가트란과 관련된 주요 출혈로 인해 기계식 보철 심장 판막이 있는 환자에서도 다비가트란의 사용을 피해야 한다.[2][11][12]
역효과
다비가트란의 가장 흔히 보고되는 부작용은 위장 장애다. 와파린으로 항응고된 환자와 비교해 볼 때, 다비가트란을 복용한 환자들은 생명을 위협하는 출혈이 적었고, 뇌내 출혈을 포함한 경증 및 주요 출혈이 적었지만, 위장 출혈의 비율은 현저하게 높았다. 다비가트란 캡슐에는 위 pH를 낮춰주고 적절한 흡수를 위해 필요한 타르타르산이 함유되어 있다. 낮은 pH는 이전에 난독증과 관련이 있었다; 어떤 사람들은 이것이 위장 출혈의 위험을 증가시키는 데 역할을 한다고 가정한다.[13]
여러 시험의 안전 결과 데이터를 결합할 때 심근경색(심장마비)의 위험은 작지만 현저하게 증가했다.[14]
신장 기능이 나쁜 사람에게는 감소된 선량을 사용해야 한다.[15]
약리학
작용기전
다비가트란은 역방향으로 트롬빈 분자의 활성 부위에 결합하여 혈빈 매개 응고 인자의 활성화를 방지한다. 게다가, 다비가트란은 트롬빈이 피브린에 묶여 있을 때에도 트롬빈을 불활성화할 수 있다; 그것은 피브리노리분해증의 트롬빈 매개 억제를 감소시키고, 따라서 피브리노리분해를 강화시킬 수 있다.[16]
약동학
다비가트란은 약 12~14시간 반감기를 가지고 있으며 섭취 후 2~3시간 이내에 최대 항응고 효과를 발휘한다.[citation needed] 지방성 식품은 약물의 생체이용성은 영향을 받지 않지만, 다비가트란의 장 흡수를 지연시킨다.[17] 한 연구는 양성자 펌프 억제제로 복용하면 흡수가 적당히 감소할 수 있다는 것을 보여주었다.[18] 키니딘, 베라파밀, 아미오다론 등 강력한 플리코프로틴 펌프 억제제를 복용하는 환자에게 P-글리코프로틴 펌프를 통한 다비가트란 배설이 느려져 다비가트란의 혈장 수치가 상승한다.[19]
다비가트란은 프로드약물 다비가트란 에텍스틸로 공식화되었다.[19]
역사
Dabigatran (then compound BIBR 953) was discovered from a panel of chemicals with similar structure to benzamidine-based thrombin inhibitor α-NAPAP (N-alpha-(2-naphthylsulfonylglycyl)-4-amidinophenylalanine piperidide), which had been known since the 1980s as a powerful inhibitor of various serine proteases, specifically thrombin, but also trypsin. 에틸 에스테르와 헥실록시카르보닐 카바미드 소수성 사이드 체인을 추가하면 구강 흡수 프로드러브, BIBR 1048(다비가트란 이텍시탈)이 나왔다.[20]
2008년 3월 18일, 유럽 의약청(EMA)은 고관절이나 무릎 교체 수술에 따른 혈전증 질환의 예방과 비혈관 심방세동 수술에 대한 Pradaxa의 마케팅 허가를 내주었다.[21]
영국의 NHS는 수술 환자의 고관절과 무릎 교체의 혈액 응고를 예방하는 데 사용할 다비가트란을 허가했다. 2008년 BBC 기사에 따르면, 다비가트란은 NHS에 하루 4.20파운드의 비용이 들 것으로 예상되었는데, 이것은 다른 몇몇 항응고제와 비슷했다.[22]
당초 와파린과 달리 [23]큰 출혈이 발생했을 때 다비가트란의 항응고 효과를 되돌릴 수 있는 구체적인 방법은 없었다.[24] 이후 정맥 투여를 위한 인체화 단핵항체인 다비가트란 특이 항체 이다루치즈맵이 개발돼 2015년 식품의약품안전청(FDA) 승인을 받았다.[25]
프라닥사는 2008년 6월 10일 캐나다 보건부로부터 총 고관절 또는 전체 무릎 교체 수술을 받은 환자의 혈액 응고 예방을 위한 준수 통지서(NOC)를 받았다.[26] 뇌졸중 위험이 있는 심방세동 환자에 대한 승인은 2010년 10월에 이루어졌다.[27][28]
미국 식품의약국(FDA)은 2010년 10월 19일 비발상 심방세동 환자의 뇌졸중 예방을 위해 프라닥사를 승인했다.[29][30][31][32] 이번[33] 승인은 2010년 9월 20일 외부 전문가들에 의해 여전히 주의가 요구되고 있지만 자문위원회가 승인할 것을 권고함에 따라 이루어졌다.[34]
2011년 2월 14일 미국심장학재단과 미국심장학회는 1급 추천으로 비발정 심방세동 관리에 대한 가이드라인에 다비가트란을 추가했다.[35]
2014년 5월 FDA는 13만4000명의 메디케어 환자를 대상으로 다비가트란을 와파린과 비교한 대규모 연구 결과를 발표했다. 그 기관은 다비가트란이 와파린보다 전반적인 사망률, 허혈성 뇌졸중, 뇌출혈의 위험성이 더 낮다고 결론지었다. 위장관 출혈은 와파린으로 치료받은 사람들보다 다비가트란으로 치료받은 사람들에게서 더 흔했다. 심장마비의 위험은 두 약 사이에 유사했다. FDA는 dabigatran의 전반적인 위험/효익비율이 유리하다는 의견을 되풀이했다.[36]
영국 의학저널(BMJ)은 2014년 7월 26일 보링거 인겔하임 제약그룹을 사적으로 보유하고 있는 보링거 인겔하임 제약그룹에 대해 고령자 특히 심각한 출혈로부터 환자를 보호하기 위한 모니터링의 필요성에 대해 비판적인 정보를 숨겼다고 고발하는 일련의 조사를 실었다. FDA와 EMA의 Boehringer 연구진과 직원들 간의 내부 커뮤니케이션에 대한 리뷰는 Boehringer 연구원들이 Dabigatran의 혈청 수치가 매우 다양하다는 증거를 발견했다고 밝혔다. BMJ 조사 결과 Boehringer는 모니터링이 필요 없는 항응고제로서 다비가트란을 광범위하게 마케팅하는 것과 상충되기 때문에 규제 보건 기관으로부터 이러한 우려를 보류할 수 있는 재정적 동기를 가지고 있는 것으로 나타났다.[37][38] 2012년 8월, 미국 연방법원에 제기된 프라닥사 주장은 데이비드 R 부장판사 이전에 일리노이주 남부지구의 다지역 소송으로 통합되었다. 헨든. 2014년 5월 28일, 보링거 인겔하임 제약사가 만든 약 3,900명의 청구인을 대신하여 6억 5천만 달러의 합의금이 발표되었다. 그 약은 심각한 출혈을 일으키거나 약을 복용하는 사람들에게 출혈을 일으킨다고 주장되었다.[39]
참조
- ^ "Dabigatran (Pradaxa) Use During Pregnancy". Drugs.com. 27 December 2018. Retrieved 16 May 2020.
- ^ a b c d e "Pradaxa- dabigatran etexilate mesylate capsule". DailyMed. 6 July 2020. Retrieved 13 November 2020.
- ^ a b c d e f g h i j k l "Dabigatran Etexilate Mesylate Monograph for Professionals". Drugs.com. American Society of Health-System Pharmacists. Retrieved 27 March 2019.
- ^ a b British national formulary : BNF 76 (76 ed.). Pharmaceutical Press. 2018. pp. 135–137. ISBN 9780857113382.
- ^ Kiser, Kathryn (2017). Oral Anticoagulation Therapy: Cases and Clinical Correlation. Springer. p. 11. ISBN 9783319546438.
- ^ World Health Organization (2019). World Health Organization model list of essential medicines: 21st list 2019. Geneva: World Health Organization. hdl:10665/325771. WHO/MVP/EMP/IAU/2019.06. License: CC BY-NC-SA 3.0 IGO.
- ^ "Dabigatran Etexilate Mesylate - Drug Usage Statistics". ClinCalc. Retrieved 11 April 2020.
- ^ "Office of Generic Drugs 2020 Annual Report". U.S. Food and Drug Administration (FDA). Retrieved 12 February 2021.
- ^ Gómez-Outes A, Terleira-Fernández AI, Calvo-Rojas G, Suárez-Gea ML, Vargas-Castrillón E (2013). "Dabigatran, Rivaroxaban, or Apixaban versus Warfarin in Patients with Nonvalvular Atrial Fibrillation: A Systematic Review and Meta-Analysis of Subgroups". Thrombosis. 2013: 640723. doi:10.1155/2013/640723. PMC 3885278. PMID 24455237.
- ^ Lowenstern A, Al-Khatib SM, Sharan L, Chatterjee R, Allen LaPointe NM, Shah B, et al. (December 2018). "Interventions for Preventing Thromboembolic Events in Patients With Atrial Fibrillation: A Systematic Review". Annals of Internal Medicine. 169 (11): 774–787. doi:10.7326/M18-1523. PMC 6825839. PMID 30383133.
- ^ "FDA Drug Safety Communication: Pradaxa (dabigatran etexilate mesylate) should not be used in patients with mechanical prosthetic heart valves". U.S. Food and Drug Administration (FDA). Retrieved 29 October 2014.
- ^ Eikelboom JW, Connolly SJ, Brueckmann M, Granger CB, Kappetein AP, Mack MJ, et al. (September 2013). "Dabigatran versus warfarin in patients with mechanical heart valves". The New England Journal of Medicine. 369 (13): 1206–14. doi:10.1056/NEJMoa1300615. PMID 23991661.
- ^ Blommel ML, Blommel AL (August 2011). "Dabigatran etexilate: A novel oral direct thrombin inhibitor". American Journal of Health-System Pharmacy. 68 (16): 1506–19. doi:10.2146/ajhp100348. PMID 21817082.
- ^ Uchino K, Hernandez AV (March 2012). "Dabigatran association with higher risk of acute coronary events: meta-analysis of noninferiority randomized controlled trials". Archives of Internal Medicine. 172 (5): 397–402. doi:10.1001/archinternmed.2011.1666. PMID 22231617.
- ^ "18/12/2014 Pradaxa -EMEA/H/C/000829 -II/0073".
- ^ Comin J, Kallmes DF (March 2012). "Dabigatran (Pradaxa)". AJNR. American Journal of Neuroradiology. 33 (3): 426–8. doi:10.3174/ajnr.A3000. PMC 7966436. PMID 22345499.
- ^ Pradaxa 전체 처방 정보 웨이백 머신에 2015-08-10년 보관. 보링거 인겔하임 2010년 10월.
- ^ Stangier J, Eriksson BI, Dahl OE, Ahnfelt L, Nehmiz G, Stähle H, et al. (May 2005). "Pharmacokinetic profile of the oral direct thrombin inhibitor dabigatran etexilate in healthy volunteers and patients undergoing total hip replacement". Journal of Clinical Pharmacology. 45 (5): 555–63. doi:10.1177/0091270005274550. PMID 15831779. S2CID 26441767.
- ^ a b "프라닥사 제품 특성 요약" (2018) 웨이백머신에 2019-07-05 보관 유럽의약국.
- ^ Hauel NH, Nar H, Priepke H, Ries U, Stassen JM, Wienen W (April 2002). "Structure-based design of novel potent nonpeptide thrombin inhibitors". Journal of Medicinal Chemistry. 45 (9): 1757–66. doi:10.1021/jm0109513. PMID 11960487. Lay summary.
{{cite journal}}: Cite는 사용되지 않는 매개 변수를 사용한다.lay-url=(도움말) - ^ "Pradaxa EPAR". European Medicines Agency. Archived from the original on 2 August 2012. Retrieved 30 January 2011.
- ^ "Clot drug 'could save thousands'". BBC News Online. 20 April 2008. Retrieved 21 April 2008.
- ^ van Ryn J, Stangier J, Haertter S, Liesenfeld KH, Wienen W, Feuring M, Clemens A (June 2010). "Dabigatran etexilate--a novel, reversible, oral direct thrombin inhibitor: interpretation of coagulation assays and reversal of anticoagulant activity". Thrombosis and Haemostasis. 103 (6): 1116–27. doi:10.1160/TH09-11-0758. PMID 20352166.
Although there is no specific antidote to antagonise the anticoagulant effect of dabigatran, due to its short duration of effect drug discontinuation is usually sufficient to reverse any excessive anticoagulant activity.
- ^ Hanley JP (November 2004). "Warfarin reversal". Journal of Clinical Pathology. 57 (11): 1132–9. doi:10.1136/jcp.2003.008904. PMC 1770479. PMID 15509671.
- ^ Syed YY (August 2016). "Idarucizumab: A Review as a Reversal Agent for Dabigatran". American Journal of Cardiovascular Drugs. 16 (4): 297–304. doi:10.1007/s40256-016-0181-4. PMID 27388764. S2CID 11596083.
- ^ "SBD(Summary Basis Canada. 2008-11-06.
- ^ Kirkey, Sharon (29 October 2010). "Approval of new drug heralds 'momentous' advance in stroke prevention". Montreal Gazette. Retrieved 29 October 2010.
- ^ "Pradax (Dabigatran Etexital) 심방세동에서의 뇌졸중 예방을 위해 캐나다에서 승인을 얻었다" 의학 뉴스 투데이. 2010년 10월 28일.
- ^ Connolly SJ, Ezekowitz MD, Yusuf S, Eikelboom J, Oldgren J, Parekh A, et al. (September 2009). "Dabigatran versus warfarin in patients with atrial fibrillation". The New England Journal of Medicine. 361 (12): 1139–51. doi:10.1056/NEJMoa0905561. hdl:11343/221723. PMID 19717844.
- ^ Turpie AG (January 2008). "New oral anticoagulants in atrial fibrillation". European Heart Journal. 29 (2): 155–65. doi:10.1093/eurheartj/ehm575. PMID 18096568.
- ^ "Boehringer wins first US OK in blood-thinner race". Reuters. 19 October 2010. Retrieved 20 October 2010.
- ^ "FDA approves Pradaxa to prevent stroke in people with atrial fibrillation" (Press release). U.S. Food and Drug Administration (FDA). 19 October 2010. Archived from the original on 20 October 2010.
- ^ Shirley S. Wang (20 September 2010). "New Blood-Thinner Recommended by FDA Panel". The Wall Street Journal. Retrieved 20 October 2010.
- ^ Merli G, Spyropoulos AC, Caprini JA (August 2009). "Use of emerging oral anticoagulants in clinical practice: translating results from clinical trials to orthopedic and general surgical patient populations". Annals of Surgery. 250 (2): 219–28. doi:10.1097/SLA.0b013e3181ae6dbe. PMID 19638915. S2CID 44917732.
- ^ Wann LS, Curtis AB, Ellenbogen KA, Estes NA, Ezekowitz MD, Jackman WM, et al. (March 2011). "2011 ACCF/AHA/HRS focused update on the management of patients with atrial fibrillation (update on Dabigatran): a report of the American College of Cardiology Foundation/American Heart Association Task Force on practice guidelines". Circulation. 123 (10): 1144–50. doi:10.1161/CIR.0b013e31820f14c0. PMID 21321155.
- ^ "FDA Drug Safety Communication: FDA study of Medicare patients finds risks lower for stroke and death but higher for gastrointestinal bleeding with Pradaxa (dabigatran) compared to warfarin". U.S. Food and Drug Administration (FDA). Retrieved 13 November 2020.
- ^ Cohen D (July 2014). "Dabigatran: how the drug company withheld important analyses". BMJ. 349: g4670. doi:10.1136/bmj.g4670. PMID 25055829.
- ^ Moore TJ, Cohen MR, Mattison DR (July 2014). "Dabigatran, bleeding, and the regulators". BMJ. 349: g4517. doi:10.1136/bmj.g4517. PMID 25056265. S2CID 29090410.
- ^ Thomas, Katie (28 May 2014). "$650 Million to Settle Blood Thinner Lawsuits". The New York Times.
외부 링크
- "Dabigatran". Drug Information Portal. U.S. National Library of Medicine.
- "Dabigatran etexilate". Drug Information Portal. U.S. National Library of Medicine.
- "Dabigatran etexilate mesylate". Drug Information Portal. U.S. National Library of Medicine.


