PD-L1
PD-L1분화 클러스터 274(CD274) 또는 B7 호몰로그 1(B7-H1)로도 알려진 프로그램 사망 리간드 1(PD-L1)은 CD274 [5]유전자에 의해 인체에서 암호화되는 단백질이다.
프로그램 사망 리간드 1(PD-L1)은 임신, 조직 동종이식, 자가면역질환 및 간염과 같은 기타 질병 상태와 같은 특정 사건에서 면역 시스템의 적응 팔을 억제하는 데 주요 역할을 하는 것으로 추측되는 40kDa 타입 1의 막 통과 단백질이다.일반적으로 적응형 면역체계는 외인성 또는 내인성 위험 신호에 의해 면역체계 활성화와 관련된 항원에 반응합니다.이어서 항원특이 CD8+T세포 및/또는 CD4+도우미세포의 클론팽창을 전파한다.억제성 체크포인트 분자 PD-1에 대한 PD-L1의 결합은 면역수용체 Tyrosine-Based Switch Motife(ITSM)[6]를 통해 포스파타아제(SHP-1 또는 SHP-2)와의 상호작용에 기초한 억제 신호를 전달한다.이는 림프절에서 항원 특이적 T세포의 증식을 감소시키는 동시에 조절 T세포(항염증, 억제 T세포)의 아포토시스(apoptosis)를 감소시키며, 이는 유전자 Bcl-2의 [citation needed]낮은 조절에 의해 더욱 매개된다.
역사
PD-L1은 Mayo Clinic에서 면역 조절 분자 B7-H1로[when?] 특징지어졌다.나중에[when?] 이 분자는 PD-1의[7] 배위자로 확인되었기 때문에 PD-L1로 이름이 바뀌었다. 몇몇 인간 암세포는 높은 수준의 B7-H1을 발현했고, B7-H1의 차단은 면역 세포의 존재에서 종양의 성장을 감소시켰다.당시 B7-H1은 종양세포가 항종양 [8]면역성을 회피하는 데 도움이 된다는 결론을 내렸다.2003년 B7-H1은 골수세포에서 체크포인트 단백질로 발현되는 것으로 나타났으며 인체클리닉 [9]암 면역치료의 잠재적 대상으로 제안되었다.
바인딩
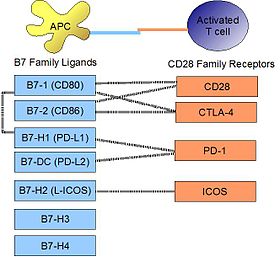
PD-L1은 활성화된 T세포, B세포 및 골수세포에서 발견된 수용체 PD-1에 결합하여 활성화 또는 억제를 조절한다.PD-L1과 PD-1의 친화력은 해리상수d K에 의해 정의된 바와 같이 770nM이다.PD-L1은 또한 늑장 자극 분자 CD80(B7-1)에 대해 현저한 친화력을 가지지만 CD86(B7-2)[10]은 가지지 않는다.PD-L1에 대한 CD80의 친화력 1.4µM은 CD28과 CTLA-4에 대한 친화력(각각 4.0µM과 400nM)의 중간이다.관련 분자 PD-L2는 CD80 또는 CD86에 대한 친화력은 없지만 수용체로서 PD-1을 공유한다(K가 140nM으로 더 강하다d).상기 등에서는 활성화된 CD4 T세포에서 상향조절된 PD-1이 단구 상에서 발현되는 PD-L1에 결합할 수 있으며 [11]후자에 의해 IL-10 생성을 유도할 수 있음을 보여주었다.
시그널링
PD-L1과 그 수용체 PD-1이 T세포에 결합하면 IL-2 생성 및 T세포 증식을 TCR 매개 활성화 억제하는 신호가 전달된다.이러한 메커니즘 ZAP70 인산화의 억제와 CD3ζ의 관계를 포함한다.[12]PD-1PKC-θ 활성화 루프 인산화(T세포 수용체 신호로 인한), 전사 요소 NF-κB과 AP-1의 활성화를 위하여 필요하고 IL-2. PD-L1의 생산 PD-1으로 결합 또한ligand-induced T세포 수용체 에 기여한다는 사실을 약화시키 신호이기도 하다.-E3 유비퀴틴 연결효소 CBL-b의 [13]상향조절을 유도하여 순진한 T세포에 항원 제시 중 조절.
규정
간섭에 의한
IFN-γ 자극 시 PD-L1은 T세포, NK세포, 대식세포,[14] 골수DC, B세포, 상피세포 및 혈관내피세포에서 발현된다.PD-L1 유전자 프로모터 영역은 간섭체 조절인자인 [15]IRF-1에 대한 반응 요소를 가지고 있다.I형 간섭자는 또한 쥐 간세포, 단구, 직류 및 종양 [16]세포에서 PD-L1을 상향조절할 수 있다.
대식세포 및 단구상
PD-L1은 특히 대식세포에서 발현된다.마우스에서는 고전적으로 활성화된 대식세포(I형 도우미 T세포 또는 LPS와 인터페론 감마의 조합에 의해 유도됨)가 PD-L1을 크게 [17]상향 조절하는 것으로 나타났다.또는 IL-4(대체 대식세포)에 의해 활성화된 대식세포는 PD-L1을 약간 상향 조절하고 PD-L2를 크게 상향 조절한다.STAT1 결핍 녹아웃 마우스는 STAT1이 LPS 또는 간섭체 감마에 의한 대식세포에 대한 PD-L1의 상향 조절에 대부분 책임이 있지만, 이러한 마우스에서 활성화되기 전 구성 발현에는 전혀 책임이 없다는 것을 보여주었다.또한 정상 상태에서 마우스 Ly6Clo 비클래식 [18]단구에서는 PD-L1이 구성적으로 발현되는 것으로 나타났다.
마이크로RNA의 역할
휴면인 담관세포는 microRNA miR-513에 [19]의한 번역 억제로 인해 단백질이 아닌 PD-L1 mRNA를 발현한다.interferon-gamma로 처리하면 miR-513이 하향 조절되어 PD-L1 단백질 억제가 해제된다.이와 같이 interferon-gamma는 mRNA 번역의 유전자 매개 억제를 억제함으로써 PD-L1 단백질 발현을 유도할 수 있다.엡스타인-바 바이러스(EBV) 잠막 단백질-1(LMP1)은 PD-L1의 알려진 잠재적 유도체인 반면, EBV miRNA miR-BamH1 단편 H 우측 개방 판독 프레임 1(BHRF1) 2-5p는 L-MP1을 조절하는 것으로 나타났다.
후생적 조절
PD-L1 프로모터 DNA 메틸화는 수술 [21]후 일부 암에서 생존을 예측할 수 있다.
임상적 의의
암
PD-L1의 상향 조절은 암이 숙주 면역 체계를 회피하도록 할 수 있다.신장세포암 환자의 종양 샘플 196개를 분석한 결과, PD-L1의 높은 종양 발현이 종양의 공격성 증가와 4.5배 사망 [22]위험 증가와 관련이 있는 것으로 나타났다.많은 PD-L1 억제제가 면역학 치료제로 개발되어 임상시험에서 [23]좋은 결과를 보이고 있다.임상적으로 이용 가능한 예로는 두르발루맙, 아테졸리주맙,[24] 아베루맙 등이 있다.정상 조직에서는 STAT3와 NF-δB와 같은 전사 인자 간의 피드백이 숙주 조직을 보호하고 염증을 제한하기 위한 면역 반응을 제한한다.암의 경우 전사인자 간의 피드백 제한 상실은 국소 PD-L1 발현을 증가시켜 PD-L1을 대상으로 하는 약물에[28] 대한 전신 치료의 효과를 제한할 수 있다[26][27].
면역 세포(특히 골수 세포)에 대한 PD-L1의 상향 조절은 또한 암세포가 [29]증식할 수 있게 하는 고도로 국소적인 방식으로 면역 억제 환경을 형성할 수 있습니다.
리스테리아단구균
세포내 감염 마우스 모델에서 L. 모노사이토제네스는 T세포, NK세포 및 대식세포에서 PD-L1 단백질 발현을 유도했다.PD-L1 차단(차단 항체 사용)은 감염된 생쥐의 사망률을 증가시켰다.차단은 대식세포에 의한 TNFα 및 일산화질소 생성을 감소시키고, NK세포에 의한 과립자임 B 생성을 감소시키며, L. 모노사이토겐 항원 특이 CD8 T 세포(CD4 T [30]세포는 아님)의 증식을 감소시켰다.이 증거는 PD-L1이 세포 내 감염에서 양성 늑장 자극 분자로 작용함을 시사한다.
자가면역
PD-1/PD-L1 상호작용은 여러 증거 행에서 자가면역성과 관련이 있다.NOD 마우스는 제1형 당뇨병과 다른 자가면역질환의 자발적 발병 가능성을 보이는 자가면역을 위한 동물모델로서 PD-1 또는 PD-L1(단, PD-L2는 [31]아님)의 차단으로부터 당뇨병의 급격한 발병을 일으키는 것으로 나타났다.
인체에서 PD-L1은 전신성 홍반성 루푸스(SLE) 소아 환자에서 발현이 변화한 것으로 밝혀졌다.건강한 어린이, 미성숙한 골수 수지상 세포 및 단구로부터 분리된 PBMC를 연구한 결과 초기 분리 시에는 PD-L1이 거의 발현되지 않았으나 24시간까지 자발적으로 상향 조절되었다.이와는 대조적으로 활성 SLE 환자의 mDC와 단구 모두 5일 동안 PD-L1을 상향 조절하지 못했고, 질병 [32]완화 중에만 이 단백질을 발현했다.이는 SLE에서 주변기기의 공차가 상실되는 메커니즘 중 하나일 수 있습니다.
「 」를 참조해 주세요.
참조
- ^ a b c GRCh38: 앙상블 릴리즈 89: ENSG00000120217 - 앙상블, 2017년 5월
- ^ a b c GRCm38: 앙상블 릴리즈 89: ENSMUSG000016496 - 앙상블, 2017년 5월
- ^ "Human PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ "Mouse PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ "Entrez Gene: CD274 CD274 molecule".
- ^ Chemnitz JM, Parry RV, Nichols KE, June CH, Riley JL (July 2004). "SHP-1 and SHP-2 associate with immunoreceptor tyrosine-based switch motif of programmed death 1 upon primary human T cell stimulation, but only receptor ligation prevents T cell activation". Journal of Immunology. 173 (2): 945–54. doi:10.4049/jimmunol.173.2.945. PMID 15240681.
- ^ Dong H, Zhu G, Tamada K, Chen L (December 1999). "B7-H1, a third member of the B7 family, co-stimulates T-cell proliferation and interleukin-10 secretion". Nature Medicine. 5 (12): 1365–9. doi:10.1038/70932. PMID 10581077. S2CID 21397460.
- ^ Dong H, Strome SE, Salomao DR, Tamura H, Hirano F, Flies DB, Roche PC, Lu J, Zhu G, Tamada K, Lennon VA, Celis E, Chen L (August 2002). "Tumor-associated B7-H1 promotes T-cell apoptosis: a potential mechanism of immune evasion". Nature Medicine. 8 (8): 793–800. doi:10.1038/nm730. PMID 12091876. S2CID 27694471.
- ^ Curiel TJ, Wei S, Dong H, Alvarez X, Cheng P, Mottram P, Krzysiek R, Knutson KL, Daniel B, Zimmermann MC, David O, Burow M, Gordon A, Dhurandhar N, Myers L, Berggren R, Hemminki A, Alvarez RD, Emilie D, Curiel DT, Chen L, Zou W (May 2003). "Blockade of B7-H1 improves myeloid dendritic cell-mediated antitumor immunity". Nature Medicine. 9 (5): 562–7. doi:10.1038/nm863. PMID 12704383. S2CID 12499214.
- ^ Butte MJ, Peña-Cruz V, Kim MJ, Freeman GJ, Sharpe AH (August 2008). "Interaction of human PD-L1 and B7-1". Molecular Immunology. 45 (13): 3567–72. doi:10.1016/j.molimm.2008.05.014. PMC 3764616. PMID 18585785.
- ^ Said EA, Dupuy FP, Trautmann L, Zhang Y, Shi Y, El-Far M, Hill BJ, Noto A, Ancuta P, Peretz Y, Fonseca SG, Van Grevenynghe J, Boulassel MR, Bruneau J, Shoukry NH, Routy JP, Douek DC, Haddad EK, Sekaly RP (April 2010). "Programmed death-1-induced interleukin-10 production by monocytes impairs CD4+ T cell activation during HIV infection". Nature Medicine. 16 (4): 452–9. doi:10.1038/nm.2106. PMC 4229134. PMID 20208540.
- ^ Sheppard KA, Fitz LJ, Lee JM, Benander C, George JA, Wooters J, Qiu Y, Jussif JM, Carter LL, Wood CR, Chaudhary D (September 2004). "PD-1 inhibits T-cell receptor induced phosphorylation of the ZAP70/CD3zeta signalosome and downstream signaling to PKCtheta". FEBS Letters. 574 (1–3): 37–41. doi:10.1016/j.febslet.2004.07.083. PMID 15358536. S2CID 85034305.
- ^ Karwacz K, Bricogne C, MacDonald D, Arce F, Bennett CL, Collins M, Escors D (October 2011). "PD-L1 co-stimulation contributes to ligand-induced T cell receptor down-modulation on CD8+ T cells". EMBO Molecular Medicine. 3 (10): 581–92. doi:10.1002/emmm.201100165. PMC 3191120. PMID 21739608.
- ^ Flies DB, Chen L (April 2007). "The new B7s: playing a pivotal role in tumor immunity". Journal of Immunotherapy. 30 (3): 251–60. doi:10.1097/CJI.0b013e31802e085a. PMID 17414316.
- ^ Lee SJ, Jang BC, Lee SW, Yang YI, Suh SI, Park YM, Oh S, Shin JG, Yao S, Chen L, Choi IH (February 2006). "Interferon regulatory factor-1 is prerequisite to the constitutive expression and IFN-gamma-induced upregulation of B7-H1 (CD274)". FEBS Letters. 580 (3): 755–62. doi:10.1016/j.febslet.2005.12.093. PMID 16413538. S2CID 11169726.
- ^ Yamazaki T, Akiba H, Iwai H, Matsuda H, Aoki M, Tanno Y, Shin T, Tsuchiya H, Pardoll DM, Okumura K, Azuma M, Yagita H (November 2002). "Expression of programmed death 1 ligands by murine T cells and APC". Journal of Immunology. 169 (10): 5538–45. doi:10.4049/jimmunol.169.10.5538. PMID 12421930.
- ^ Loke P, Allison JP (April 2003). "PD-L1 and PD-L2 are differentially regulated by Th1 and Th2 cells". Proceedings of the National Academy of Sciences of the United States of America. 100 (9): 5336–41. Bibcode:2003PNAS..100.5336L. doi:10.1073/pnas.0931259100. PMC 154346. PMID 12697896.
- ^ Bianchini M, Duchene J, Santovito D, Schloss MJ, Evrard M, Winkels H, Aslani M, Mohanta SK, Horckmans M, Blanchet X, Lacy M, von Hundelshausen P, Atzler D, Habenicht A, Gerdes N, Pelisek J, Ng LG, Steffens S, Weber C, Megens RT (June 2019). "PD-L1 expression on nonclassical monocytes reveals their origin and immunoregulatory function". Science Immunology. 4 (36): eaar3054. doi:10.1126/sciimmunol.aar3054. PMID 31227596. S2CID 195259881.
- ^ Gong AY, Zhou R, Hu G, Li X, Splinter PL, O'Hara SP, LaRusso NF, Soukup GA, Dong H, Chen XM (February 2009). "MicroRNA-513 regulates B7-H1 translation and is involved in IFN-gamma-induced B7-H1 expression in cholangiocytes". Journal of Immunology. 182 (3): 1325–33. doi:10.4049/jimmunol.182.3.1325. PMC 2652126. PMID 19155478.
- ^ Cristino AS, Nourse J, West RA, Sabdia MB, Law SC, Gunawardana J, Vari F, Mujaj S, Thillaiyampalam G, Snell C, Gough M, Keane C, Gandhi MK (December 2019). "EBV microRNA-BHRF1-2-5p Targets the 3'UTR of Immune Checkpoint Ligands PD-L1 and PD-L2". Blood. 134 (25): 2261–2270. doi:10.1182/blood.2019000889. PMC 6923667. PMID 31856276.
- ^ Gevensleben H, Holmes EE, Goltz D, Dietrich J, Sailer V, Ellinger J, Dietrich D, Kristiansen G (November 2016). "PD-L1 promoter methylation is a prognostic biomarker for biochemical recurrence-free survival in prostate cancer patients following radical prostatectomy". Oncotarget. 7 (48): 79943–79955. doi:10.18632/oncotarget.13161. PMC 5346762. PMID 27835597.
- ^ Thompson RH, Gillett MD, Cheville JC, Lohse CM, Dong H, Webster WS, Krejci KG, Lobo JR, Sengupta S, Chen L, Zincke H, Blute ML, Strome SE, Leibovich BC, Kwon ED (December 2004). "Costimulatory B7-H1 in renal cell carcinoma patients: Indicator of tumor aggressiveness and potential therapeutic target". Proceedings of the National Academy of Sciences of the United States of America. 101 (49): 17174–9. Bibcode:2004PNAS..10117174T. doi:10.1073/pnas.0406351101. PMC 534606. PMID 15569934.
- ^ Velcheti V, Schalper KA, Carvajal DE, Anagnostou VK, Syrigos KN, Sznol M, Herbst RS, Gettinger SN, Chen L, Rimm DL (January 2014). "Programmed death ligand-1 expression in non-small cell lung cancer". Laboratory Investigation; A Journal of Technical Methods and Pathology. 94 (1): 107–16. doi:10.1038/labinvest.2013.130. PMC 6125250. PMID 24217091.
- ^ "Immune checkpoint inhibitors to treat cancer". www.cancer.org. Retrieved 2017-03-27.
- ^ Vlahopoulos SA (August 2017). "Aberrant control of NF-κB in cancer permits transcriptional and phenotypic plasticity, to curtail dependence on host tissue: molecular mode". Cancer Biology & Medicine. 14 (3): 254–270. doi:10.20892/j.issn.2095-3941.2017.0029. PMC 5570602. PMID 28884042.
- ^ Xie YJ, Dougan M, Jailkhani N, Ingram J, Fang T, Kummer L, et al. (April 2019). "Nanobody-based CAR T cells that target the tumor microenvironment inhibit the growth of solid tumors in immunocompetent mice". Proceedings of the National Academy of Sciences of the United States of America. 116 (16): 7624–7631. doi:10.1073/pnas.1817147116. PMC 6475367. PMID 30936321.
- ^ Li, Dan; English, Hejiao; Hong, Jessica; Liang, Tianyuzhou; Merlino, Glenn; Day, Chi-Ping; Ho, Mitchell (2021-07-21). "A novel PD-L1-targeted shark VNAR single domain-based CAR-T strategy for treating breast cancer and liver cancer": 2021.07.20.453144. doi:10.1101/2021.07.20.453144. S2CID 236203365.
{{cite journal}}:Cite 저널 요구 사항journal=(도움말) - ^ Fabian KP, Padget MR, Donahue RN, Solocinski K, Robbins Y, Allen CT, et al. (May 2020). "PD-L1 targeting high-affinity NK (t-haNK) cells induce direct antitumor effects and target suppressive MDSC populations". Journal for Immunotherapy of Cancer. 8 (1): e000450. doi:10.1136/jitc-2019-000450. PMC 7247398. PMID 32439799.
- ^ Nirmal, Ajit J.; Maliga, Zoltan; Vallius, Tuulia; Quattrochi, Brian; Chen, Alyce A.; Jacobson, Connor A.; Pelletier, Roxanne J.; Yapp, Clarence; Arias-Camison, Raquel; Chen, Yu-An; Lian, Christine G. (2022-04-11). "The spatial landscape of progression and immunoediting in primary melanoma at single cell resolution". Cancer Discovery. 12 (6): 1518–1541. doi:10.1158/2159-8290.CD-21-1357. ISSN 2159-8290. PMC 9167783. PMID 35404441. S2CID 248083925.
- ^ Seo SK, Jeong HY, Park SG, Lee SW, Choi IW, Chen L, Choi I (January 2008). "Blockade of endogenous B7-H1 suppresses antibacterial protection after primary Listeria monocytogenes infection". Immunology. 123 (1): 90–9. doi:10.1111/j.1365-2567.2007.02708.x. PMC 2433284. PMID 17971153.
- ^ Ansari MJ, Salama AD, Chitnis T, Smith RN, Yagita H, Akiba H, Yamazaki T, Azuma M, Iwai H, Khoury SJ, Auchincloss H, Sayegh MH (July 2003). "The programmed death-1 (PD-1) pathway regulates autoimmune diabetes in nonobese diabetic (NOD) mice". The Journal of Experimental Medicine. 198 (1): 63–9. doi:10.1084/jem.20022125. PMC 2196083. PMID 12847137.
- ^ Mozaffarian N, Wiedeman AE, Stevens AM (September 2008). "Active systemic lupus erythematosus is associated with failure of antigen-presenting cells to express programmed death ligand-1". Rheumatology. 47 (9): 1335–41. doi:10.1093/rheumatology/ken256. PMC 2722808. PMID 18650228.
외부 링크
- CD274+단백질+미국국립의학도서관 의학 과목 제목(MeSH)
- PDB for UniProt: Q9NZQ7(프로그램된 세포사망 1배위자 1)에서 PDBe-KB에 사용 가능한 모든 구조 정보의 개요.