류마티스열
Rheumatic fever| 류마티스열 | |
|---|---|
| 기타 이름 | 급성 류마티스열(ARF) |
 | |
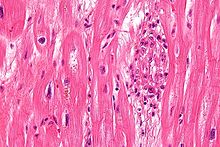
| 부검 시 류머티즘성 심장질환과 특징적인 소견(확대된 승모판, 두꺼워진 척색건조증, 비대해진 좌심실 심근) | |
| 전문 | 심장학 |
| 증상 | 발열, 다발성 관절 통증, 무의식적인 근육 운동, 홍반 여백[1] |
| 합병증 | 류마티스성 심장병, 심부전, 심방세동, 판막[1] 감염 |
| 통상적인 개시 | 연쇄상구균 인후 감염 후 2-4주 후 5-14세[2] |
| 원인들 | 스트렙토코커스 파요네스에[1] 의해 유발되는 자가면역질환 |
| 위험요소 | 유전학, 영양실조, 빈곤[1] |
| 진단 방법 | 증상 및 감염[3] 이력에 근거함 |
| 예방 | 인두염 항생제, 위생 개선[1][4] |
| 치료 | 항생제 장기 투여, 판막 교체 수술, 판막[1] 수리 |
| 빈도수. | 연간[1] 325,000명의 어린이 |
| 사망. | 319,400 (2015)[5] |
류마티스 열병은 심장, 관절, 피부, [1]뇌를 포함할 수 있는 염증성 질환이다.그 질병은 보통 연쇄상구균 인후염에 [2]감염된 후 2주에서 4주 후에 발병한다.징후와 증상에는 발열, 다발성 관절 통증, 무의식적인 근육 움직임, 그리고 때로는 [1]홍반으로 알려진 특징적인 가려움 없는 발진이 포함됩니다.심장은 [1]약 절반의 경우에 관여하고 있다.류마티스성 심장 질환으로 알려진 심장 판막의 손상은 보통 반복적인 발작 후에 발생하지만 때때로 [1]그 후에 발생할 수 있다.손상된 판막은 심부전, 심방세동 및 [1]판막 감염을 초래할 수 있습니다.
류머티즘 열은 스트렙토코커스 파요네스균에 [1]의한 인후 감염 후 발생할 수 있다.감염을 방치하면 류마티스열이 3%까지 발생한다.[6]기본 메커니즘은 개인의 [1]조직에 대한 항체의 생산을 수반하는 것으로 여겨진다.그들의 유전적 특성 때문에,[1] 어떤 사람들은 다른 사람들보다 박테리아에 노출되었을 때 그 병에 걸릴 가능성이 더 높다.다른 위험 요소로는 영양실조와 [1]빈곤이 있다.RF의 진단은 종종 최근 연쇄상구균 [3]감염의 증거와 함께 징후와 증상의 존재에 기초한다.
목에 연쇄상구균이 있는 사람들을 페니실린과 같은 항생제로 치료하면 류머티즘 [4]발열의 위험을 줄일 수 있다.항생제 오남용을 피하기 위해, 이것은 종종 목이 아픈 사람들에게 감염을 검사하는 것을 포함합니다; 하지만,[1] 개발도상국에서는 검사가 가능하지 않을 수 있습니다.다른 예방책으로는 위생 [1]개선 등이 있습니다.류머티즘 발열이나 류머티즘성 심장질환이 있는 사람은 항생제를 장기간 복용하는 것이 [1]권장될 수 있다.공격 [1]후 점차적으로 정상으로 복귀할 수 있습니다.RHD가 발병하면 치료가 [1]더 어려워진다.밸브 교체 수술이나 밸브 수리가 [1]필요할 수 있습니다.그렇지 않으면 합병증이 [1]정상적으로 처리됩니다.
류머티즘 열은 매년 약 325,000명의 아이들에게 발생하며 현재 약 3340만 명의 사람들이 류머티즘성 [1][7]심장병을 앓고 있다.RF가 발병하는 사람은 대부분 5세에서 [1]14세 사이이며, 최초 공격 중 20%는 [8]성인에게서 발생합니다.이 병은 개발도상국과 선진국의 [1]원주민들에게서 가장 흔하다.2015년에는 1990년의 [5][9]37만4천명에서 31만9천400명이 사망했다.대부분의 사망은 [1]매년 12.5%의 사람들이 사망할 수 있는 개발도상국에서 발생한다.이 상태에 대한 설명은 [10]히포크라테스의 글에서 적어도 기원전 5세기까지 거슬러 올라가는 것으로 여겨진다.그 병은 증상이 류마티스 질환의 [11]증상과 비슷하기 때문에 그렇게 이름 붙여졌다.
징후 및 증상

그 병은 보통 목 감염 [2]후 2주에서 4주 후에 발병한다.증상은 다음과 같습니다: 발열, 시간에 따라 영향을 받는 관절의 통증, 무의식적인 근육의 움직임, 그리고 때때로 홍반으로 알려진 특징적인 가려움증 없는 발진이 있습니다.심장은 약 절반의 경우에 관여하고 있다.심장 판막의 손상은 일반적으로 여러 번 발작을 일으킨 후에만 발생하지만 RF가 한 번 발생한 후에 발생할 수 있습니다.손상된 판막은 심부전을 초래할 수 있고 또한 [1]판막의 심방 세동 및 감염 위험을 증가시킵니다.
병태생리학
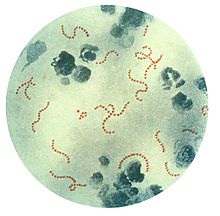
류머티즘 열은 동맥 주위의 결합 조직에 영향을 미치는 전신 질환으로, 치료되지 않은 인후염, 특히 A군 연쇄상구균(GAS), 연쇄상구균 파요겐에 의해 발생할 수 있습니다.스트렙토코커스 파요겐의 항원과 다발성 심장 단백질의 유사성은 생명을 위협하는 II형 과민반응을 일으킬 수 있다.[12]보통 자기반응성 B세포는 T세포 공동자극 없이 말초에서 아네르기성을 유지한다.연쇄상구균 감염 중에는 B세포 등의 성숙한 항원 제시세포가 CD42+T세포에 세균 항원을 제시하며 CD4+T세포는 도우미 T세포로 분화한다.그2 후 도우미 T세포는 B세포를 활성화시켜 혈장세포로 만들어 스트렙토코커스 세포벽에 대한 항체 생성을 유도한다.그러나 항체는 심근과 [13]관절에 반응하여 류마티스 발열 증상을 일으킬 수도 있다.S. pyogenes는 운동성이 없고 포자가 형성되지 않으며 사슬과 큰 [14]군집을 형성하는 유산소, 구균, 그램 양성 박테리아입니다.
S. pyogenes는 때로 높은 항원성 인자인 M 단백질을 포함하는 분기된 폴리머로 구성된 세포벽을 가지고 있습니다.면역 체계가 M 단백질에 대해 생성하는 항체는 심장 근육 세포 단백질 미오신,[15] 심장 근육 글리코겐 및 동맥의 평활근 세포와 교차 반응하여 사이토카인 방출과 조직 파괴를 유발할 수 있습니다.그러나 유일하게 검증된 교차반응은 혈관주위의 [citation needed]결합조직이다.이 염증은 보체의 직접 부착과 호중구 및 대식세포의 Fc 수용체 매개 모집을 통해 발생한다.림프구와 대식세포로 둘러싸인 부은 호산성 콜라겐으로 구성된 특징적인 아스호프체는 빛 현미경으로 관찰할 수 있다.더 큰 대식세포는 아니츠코우 세포나 애쉬오프 거대 세포가 될 수 있다.류마티스 판막 병변은 T-헬퍼 세포와 [16]대식세포를 주로 포함하고 있기 때문에 세포 매개 면역 반응을 수반할 수도 있다.
류머티즘 발열에서 이러한 병변은 다양한 종류의 심장염을 일으키는 심장의 어느 층에서나 발견될 수 있다.염증은 보통 후유증 없이 해결되는 "빵과 버터" 심막염으로 묘사되는 혈청성 심막 삼출액을 유발할 수 있습니다.심내막의 관여는 일반적으로 좌측 심장 판막의 폐쇄선을 따라 섬유소 괴사와 사마귀 형성을 일으킨다.심내막하 병변은 맥칼럼 [citation needed]플라크라고 불리는 불규칙한 비후를 유발할 수 있는 반면, 사마귀 돌기는 퇴적물로부터 생긴다.
류마티스성 심장병
만성 류머티즘성 심장병(RHD)은 섬유소 수복을 통해 반복적으로 염증을 일으키는 것이 특징이다.판막의 주요 해부학적 변화로는 리플릿 두께 증가, 교련성 융접, 힘줄의 [16]단축 및 두께 증가 등이 있습니다.판막 [17]손상을 일으키는 A군 β 용혈성 연쇄상구균(GAS)에 대한 자가면역 반응에 의해 발생한다.판막 리플릿, 교합 및 쿠스의 섬유화 및 흉터는 판막 협착 또는 [18]역류를 일으킬 수 있는 이상을 초래할 수 있습니다.류머티즘 발열로 인한 염증은 주로 소아기에 발생하는 류머티즘 판막염이라고 한다.류마티스 발열 환자의 절반 정도가 판막 [19]내피와 관련된 염증을 일으킨다.류마티스 열과 관련된 질병과 사망률의 대부분은 심장 판막 [18]조직에 대한 파괴적인 영향에 의해 발생한다.RHD의 병인은 복잡하고 완전히 이해되지 않지만, 자가면역반응을 [citation needed]일으키는 분자모방과 유전적 성향을 수반하는 것으로 알려져 있다.
분자 모방은 숙주 항원과 연쇄상구균 [20]항원 사이에 에피토프가 공유될 때 발생한다.이것은 에피토프 공유의 결과로 생성된 항체의 교차 반응으로 인해 "이물질"로 잘못 인식된 심장의 토종 조직에 대한 자가 면역 반응을 일으킨다.판막 내피는 림프구에 의해 유발되는 손상의 두드러진 부위이다.CD4+ T세포는 RHD에서 [21]심장조직 자가면역반응의 주요 효과인자이다.일반적으로 T세포 활성화는 박테리아 항원의 존재에 의해 유발된다.RHD에서, 분자 모방은 부정확한 T세포 활성화를 초래하고, 이러한 T림프구는 계속해서 자기 항원 특이 항체를 생성하기 시작하는 B세포를 활성화할 수 있다.이는 병원균으로 잘못 식별된 심장의 조직에 대한 면역 반응 공격을 일으킨다.류마티스 판막은 림프구의 [22]유착을 매개하는 단백질인 VCAM-1의 발현 증가를 나타낸다.인간단백질과 연쇄상구균항원 사이의 분자모방을 통해 생성된 자가항원특이항체는 판막내피결합 후 VCAM-1을 상향조절한다.이는 주로 CD4+ T 세포 [22]침윤에 의해 류마티스 판막염에서 관찰되는 염증과 판막 흉터로 이어진다.
유전적 소인의 메커니즘은 불분명하지만, 몇 가지 유전적 요인이 RHD에서 자가면역 반응에 대한 민감성을 증가시키는 것으로 밝혀졌다.주요 기여자는 림프구와 항원 제시 세포, 특히 인간 염색체 [23]6의 DR과 DQ 대립 유전자에서 발견되는 MHC 클래스 II 분자의 구성요소이다.특정 대립 유전자의 조합은 RHD 자가면역 감수성을 증가시키는 것으로 보인다.인간 백혈구 항원(HLA) 클래스 II 대립 유전자 DR7(HLA-DR7)은 RHD와 가장 자주 관련되며, 특정 DQ 대립 유전자와의 조합은 판막 [23]병변의 발달과 외견상 관련이 있다.MHC 클래스 II 분자가 RHD에서 자가면역 반응에 대한 숙주의 감수성을 증가시키는 메커니즘은 알려져 있지 않지만, 그것은 T 세포 수용체에 항원을 제시하는데 있어서 HLA 분자가 하는 역할과 관련이 있을 수 있으며, 따라서 면역 반응을 유발한다.인간 염색체 6에서도 RHD와 [23]관련된 사이토카인 TNF-α가 발견된다.TNF-α의 높은 발현 수치는 판막 조직 염증을 악화시켜 RHD 병리 형성에 기여할 수 있다.만노스 결합 렉틴(MBL)은 병원체 인식에 관여하는 염증 단백질이다.RHD에는 다양한 MBL2 유전자 영역이 관련되어 있습니다. RHD 유도 승모판 협착은 MBL의 [24]높은 생산을 위한 MBL2 대립 유전자 코드화와 관련되어 있습니다.RHD 환자들의 대동맥 판막 역류 현상은 MBL의 [25]낮은 생성을 코드화하는 다양한 MBL2 대립 유전자와 관련이 있다.다른 유전자들도 [citation needed]RHD에서 일어나는 자가면역반응의 복잡성을 더 잘 이해하기 위해 연구되고 있다.
진단.
수정된 존스 기준은 1944년에 T에 의해 처음 발표되었다.더킷 존스,[26] MD그것들은 미국 심장 협회에 의해 다른 [27]그룹들과 협력하여 정기적으로 개정되어 왔다.개정된 존스 기준에 따르면 류마티스 발열 진단은 연쇄상구균 감염의 증거와 함께 두 가지 주요 기준 또는 하나의 주요 기준과 두 가지 사소한 기준, 즉 항스트렙톨리신 O titre[28] 또는 항DNAase [29][8]B가 있을 때 이루어질 수 있다.세 가지 사소한 기준이 [30]있을 때 재발도 진단된다.예외적으로, 각각 류머티즘 [31][32][33]발열을 나타낼 수 있는 안무와 나태성 심장염은 예외이다.2013년 4월 인도 의학 연구 저널의 리뷰 기사에 따르면 심장초음파 및 도플러(E&D) 연구는 효용성에 대한 일부 의구심에도 불구하고 류마티스성 심장병의 엄청난 부담을 확인했으며, 이는 1992년 Jones의 기준의 부적절성을 시사한다.E&D 연구는 류머티즘 발열 환자뿐만 아니라 처음에 시덴햄의 [34]안무를 분리한 것으로 나타났던 류머티즘 심장병 환자의 후속 조치에서도 경미한 심장염을 확인했다.선행 연쇄상구균 감염의 징후는 최근의 성홍열, 항스트렙톨리신 O 또는 다른 연쇄상구균 항체 티트리 또는 양성 목 [35]배양이다.2015년 마지막 개정에서는 첫 번째 범주의 과잉진단과 마지막 [30]범주의 과소진단을 피하기 위해 저위험군과 고위험군의 가변진단 기준을 제시했다.저위험군은 급성 류머티즘 발열 연간 발병률이 10만 명당 2명 이하이거나 전 연령 류머티즘 심장병 유병률이 [30]1000명당 1명 이상인 집단으로 정의되었다.다른 모든 모집단은 중간 또는 높은 [30]위험을 가진 것으로 분류되었다.
주요 기준
- 다른population-risk 범주에 서로 다른 의미를 줍니다 합동적인 표현 있는 독특한 임상 징후:오직 polyarthritis[36](그 큰 관절의 임시migrating 염증은 보통 다리에 이상 이동하는 시작)주요 기준으로 위험이 낮은 인구에 반해, monoarthritis, polyarth으로 간주된다.ritis와 다관절통(부기가 없는 관절통)은 모두 고위험군의 [30]주요 기준으로 포함된다.
- 심장염: 심장염은 심막,[37] 심근의 일부 영역, 그리고 보다 일관되게 판막염의 형태로 심내막을 포함할 수 있습니다.심장염은 승모판막염 또는 대동맥판막염을 드러내는 심장초음파/도플러 연구에 의해 임상적으로 진단된다(두근거림, 호흡곤란, 심부전 또는 새로운 심장잡음)현재 임상적 심장염과 불치병적 심장염이 모두 [30][37]주요 기준으로 고려되고 있다.
- 피하결절: 뼈나 힘줄 위에 있는 무통하고 단단한 콜라겐 섬유 집합.그것들은 일반적으로 손목 뒤쪽, 바깥쪽 팔꿈치, 그리고 무릎 [citation needed]앞부분에 나타난다.
- 홍반 여백:몸통이나 팔에서 시작되는 붉은 발진. 몸통이나 팔에서 시작되어 가운데가 선명하게 퍼져 고리를 형성합니다.이 발진은 계속 퍼지고 다른 고리와 합쳐져 최종적으로 뱀처럼 보입니다.이 발진은 전형적으로 얼굴에 상처가 나고 열로 [citation needed]악화된다.
- 시덴햄의 안무(St. 바이서스의 춤)얼굴과 팔의 무의식적인 빠른 움직임의 특징적인 연속입니다.이것은 [citation needed]감염이 시작된 후 최소 3개월 동안 질병에서 매우 늦게 발생할 수 있다.
마이너 기준
- 관절통:저위험군에서는 다관절통, [30]다른 곳에서는 단관절통.그러나 관절의 징후는 같은 [30]환자의 주요 범주 및 부 범주에서 모두 고려될 수 없습니다.
- 발열: idence 38.5 °C (101.3 °F), 38 38 °C (100.4 °F) 고위험군.[30]
- 적혈구 침강속도 상승(lox-risk 모집단의 경우 최초 1시간 이내 60mm 이상, 기타의 경우 30mm/h 이하) 또는 C 반응단백질(> 3.0mg/[30]dL)
- 연령 변동을 고려한 후 PR[30][35][38] 간격이 길어지는 심전도(심장염이 주요 증상으로 있는 경우 포함 불가)
예방
류머티즘 발열은 항생제로 [39]인후염의 효과적이고 신속한 치료를 통해 예방할 수 있다.
류머티즘에 걸린 적이 있는 사람에게는 예방적인 항생제가 [39]권장되는 경우가 있습니다.2017년 현재 기저질환자의 장기 항생제를 뒷받침하는 증거는 불충분하다.[40]
미국 심장 협회는 치아 건강을 유지하고, 세균성 심내막염, 심장 이식, 인공 심장 판막, 또는 "일부 선천성 심장 결함"의 병력이 있는 사람들은 장기적인 항생제 [41]예방을 고려할 것을 제안합니다.
치료
류마티스열 관리는 아스피린이나 코르티코스테로이드와 같은 항염증 약물에 의한 염증 감소로 유도된다.인두염 양성 배양균을 가진 사람들은 항생제로 [36]치료받아야 한다.
아스피린은 선택약으로 높은 [42]용량으로 투여되어야 한다.
위염과 살리실산염 중독 같은 부작용을 조심해야 한다.어린이와 청소년들에게 아스피린과 아스피린이 함유된 제품의 사용은 심각하고 잠재적으로 치명적인 질환인 레이 증후군과 연관될 수 있습니다.어린이와 청소년에게 아스피린과 아스피린이 함유된 제품을 투여할 때는 항상 위험, 유익성 및 대체 치료법을 고려해야 합니다.어린이와 [citation needed]청소년은 통증과 불쾌감을 위한 이부프로펜과 류머티즘 열로 나타나는 중간에서 심각한 염증 반응을 위한 코르티코스테로이드를 고려해야 한다.
백신
현재 S. pyogenes 감염으로부터 보호할 수 있는 백신은 없지만,[43] 개발 연구가 진행 중이다.백신의 개발의 어려움은 환경에 존재하는 다양한 종류의 S. pyogenes와 [44]백신의 안전성과 효능을 위한 적절한 시험에 필요한 많은 시간과 사람들이다.
감염
스트렙토코커스 파요겐에 대한 양성 배양균을 가진 사람들은 알레르기가 없는 한 페니실린으로 치료해야 한다.항생제의 사용은 류머티즘 [36]발병에 대한 심장의 관여를 바꾸지 않을 것이다.벤자틴 벤질페니실린의 [citation needed]사용을 제안하는 사람도 있다.
류머티즘 발열 환자가 5년 동안 효과가 오래 지속되는 페니실린을 매달 주사해야 한다.만약 심장염의 증거가 있다면, 치료 기간은 최대 40년이 될 수 있다.류마티스 발열 치료에 있어 또 다른 중요한 초석은 재발 [citation needed]방지를 위해 저용량 항생제(예: 페니실린, 술파디아진, 에리트로마이신)의 지속적인 사용을 포함한다.
염증
코르티코스테로이드가 자주 사용되는 반면, 이를 뒷받침하는 증거는 [1]빈약하다.살리실산염은 [citation needed]통증에 유용하다.
스테로이드제는 심장 질환의 증거가 있는 경우를 위해 남겨져 있다.스테로이드제의 사용은 조직의 더 이상의 흉터를 예방할 수 있고 승모판 협착증과 [citation needed]같은 후유증의 발생을 예방할 수 있다.
심부전
몇몇 환자들은 울혈성 심부전으로 나타나는 심각한 심장염에 걸린다.이것은 심부전에 대한 일반적인 치료를 요구한다: ACE 억제제, 이뇨제, 베타 차단제, 그리고 디곡신.전형적인 심부전과 달리 류마티스성 심부전은 코르티코스테로이드에 잘 반응한다.
역학
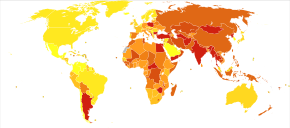
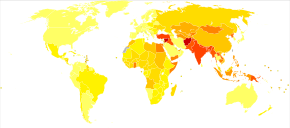
약 3천 3백만 명의 사람들이 류마티스성 심장병에 걸렸고, 추가로 4천 7백만 명의 사람들이 그들의 심장 [40]판막에 무증상적인 손상을 입었다.2010년 현재 전 세계적으로 사망자는 345,000명으로 [46]1990년의 463,000명에서 감소했다.
서양 국가들에서 류마티스 열은 1960년대 이후 상당히 드물어졌는데, 아마도 연쇄상구균 감염을 치료하기 위해 항생제가 널리 사용되었기 때문일 것이다.미국에서는 20세기 초부터 훨씬 덜 흔했지만 1980년대 이후 [47]발병은 거의 없었다.이 병은 호주 원주민들(특히 중부와 북부), 마오리족, 태평양 섬 주민들 사이에서 가장 흔하며 사하라 이남 아프리카, 라틴 아메리카, 인도 아대륙, 북아프리카에서도 [48]흔하다.
류머티즘 열은 주로 5세에서 17세 사이의 아이들에게 영향을 미치며 인후염 후 약 20일 후에 발생한다.3분의 1의 경우, 근본적인 연쇄상구균 감염은 어떠한 [citation needed]증상도 유발하지 않을 수 있다.
치료되지 않은 연쇄상구균 감염을 가진 사람들의 류마티스 열 발병률은 3%로 추정된다.후속 치료되지 않은 감염에 의한 재발률은 상당히 높다(약 50 [49]%)항생제 치료를 받은 사람들의 발병률은 훨씬 낮다.류머티즘 발열 증세를 보인 사람은 연쇄상구균 [citation needed]감염을 반복하면서 발진이 일어나는 경향이 있다.
류마티스열의 재발은 저용량 항생제가 유지되지 않을 때, 특히 첫 발병 후 처음 3~5년 동안 비교적 흔하다.류머티즘 발열이 재발하면 심장 판막 질환으로 이어질 수 있다.심장 합병증은 특히 판막과 관련된 경우 장기적이고 심각할 수 있다.동남아시아, 사하라 사막 이남 아프리카, 오세아니아 국가에서는 심장 소리를 듣고 류마티스성 심장질환을 발견한 비율이 어린이 1000명당 2.9명, 심장 초음파 검사에서는 어린이 [50][51][52][53]1000명당 12.9명이었다.소아 심장 초음파 검사와 류머티즘성 심장 질환의 초기 단계 징후가 있는 소아에서 2차 항생제 예방을 적시에 시작하는 것은 풍토 지역의 [54]류머티즘성 심장 질환의 부담을 줄이는데 효과적일 수 있다.
「 」를 참조해 주세요.
레퍼런스
- ^ a b c d e f g h i j k l m n o p q r s t u v w x y z aa ab ac Marijon, E; Mirabel, M; Celermajer, DS; Jouven, X (10 March 2012). "Rheumatic heart disease". Lancet. 379 (9819): 953–64. doi:10.1016/S0140-6736(11)61171-9. PMID 22405798. S2CID 20197628.
- ^ a b c Lee, KY; Rhim, JW; Kang, JH (March 2012). "Kawasaki disease: laboratory findings and an immunopathogenesis on the premise of a "protein homeostasis system"". Yonsei Medical Journal. 53 (2): 262–75. doi:10.3349/ymj.2012.53.2.262. PMC 3282974. PMID 22318812.
- ^ a b "Rheumatic Fever 1997 Case Definition". cdc.gov. 3 February 2015. Archived from the original on 19 February 2015. Retrieved 19 February 2015.
- ^ a b Spinks, Anneliese; Glasziou, Paul P.; Del Mar, Chris B. (9 December 2021). "Antibiotics for treatment of sore throat in children and adults". The Cochrane Database of Systematic Reviews. 12: CD000023. doi:10.1002/14651858.CD000023.pub5. ISSN 1469-493X. PMC 8655103. PMID 34881426.
- ^ a b GBD 2015 Mortality and Causes of Death, Collaborators. (8 October 2016). "Global, regional, and national life expectancy, all-cause mortality, and cause-specific mortality for 249 causes of death, 1980-2015: a systematic analysis for the Global Burden of Disease Study 2015". Lancet. 388 (10053): 1459–1544. doi:10.1016/S0140-6736(16)31012-1. PMC 5388903. PMID 27733281.
{{cite journal}}:first1=범용명(도움말)이 있습니다. - ^ Ashby, Carol Turkington, Bonnie Lee (2007). The encyclopedia of infectious diseases (3rd ed.). New York: Facts On File. p. 292. ISBN 9780816075072. Archived from the original on 21 November 2015.
The risk of severe complications is the primary concern with strep throat, and the reason why it is so important to be properly diagnosed and treated. One of the most serious complications is rheumatic fever, a disease that affects up to 3 percent of those with untreated strep infection. Rheumatic fever can lead to rheumatic heart disease.
- ^ GBD 2015 Disease and Injury Incidence and Prevalence, Collaborators. (8 October 2016). "Global, regional, and national incidence, prevalence, and years lived with disability for 310 diseases and injuries, 1990-2015: a systematic analysis for the Global Burden of Disease Study 2015". Lancet. 388 (10053): 1545–1602. doi:10.1016/S0140-6736(16)31678-6. PMC 5055577. PMID 27733282.
{{cite journal}}:first1=범용명(도움말)이 있습니다. - ^ a b Kumar, Vinay; Abbas, Abul K; Fausto, Nelson; Mitchell, Richard N (2007). Robbins Basic Pathology (8th ed.). Saunders Elsevier. pp. 403–6. ISBN 978-1-4160-2973-1.
- ^ GBD 2013 Mortality and Causes of Death, Collaborators (17 December 2014). "Global, regional, and national age-sex specific all-cause and cause-specific mortality for 240 causes of death, 1990–2013: a systematic analysis for the Global Burden of Disease Study 2013". Lancet. 385 (9963): 117–171. doi:10.1016/S0140-6736(14)61682-2. PMC 4340604. PMID 25530442.
{{cite journal}}:first1=범용명(도움말)이 있습니다. - ^ Quinn, RW (1991). "Did scarlet fever and rheumatic fever exist in Hippocrates' time?". Reviews of Infectious Diseases. 13 (6): 1243–4. doi:10.1093/clinids/13.6.1243. PMID 1775859.
- ^ 도란드 의학사전에 실린 '류마틱 열병'
- ^ "4.2 Biocompatibility and the Relationship to Standards: Meaning and Scope of Biomaterials Testing". Comprehensive Biomaterials II. Elsevier. 2017. pp. 7–29.
- ^ Abbas, Abul K.; Lichtman, Andrew H.; Baker, David L.; et al. (2004). Basic immunology: functions and disorders of the immune system (2 ed.). Philadelphia, Pennsylvania: Elsevier Saunders. ISBN 978-1-4160-2403-3.
- ^ "Streptococcus pyogenes – Pathogen Safety Data Sheets". Public Health Agency of Canada. 18 February 2011. Archived from the original on 17 January 2017. Retrieved 15 April 2017.
- ^ Faé KC, da Silva DD, Oshiro SE, et al. (May 2006). "Mimicry in recognition of cardiac myosin peptides by heart-intralesional T cell clones from rheumatic heart disease". J. Immunol. 176 (9): 5662–70. doi:10.4049/jimmunol.176.9.5662. PMID 16622036.
- ^ a b Cotran, Ramzi S.; Kumar, Vinay; Fausto, Nelson; Nelso Fausto; Robbins, Stanley L.; Abbas, Abul K. (2005). Robbins and Cotran pathologic basis of disease. St. Louis, Mo: Elsevier Saunders. ISBN 978-0-7216-0187-8. Archived from the original on 10 September 2005.
- ^ Kaplan, MH; Bolande, R; Rakita, L; Blair, J (1964). "Presence of Bound Immunoglobulins and Complement in the Myocardium in Acute Rheumatic Fever. Association with Cardiac Failure". The New England Journal of Medicine. 271 (13): 637–45. doi:10.1056/NEJM196409242711301. PMID 14170842.
- ^ a b Brice, Edmund A. W; Commerford, Patrick J. (2005). "Rheumatic Fever and Valvular Heart Disease". In Rosendorff, Clive (ed.). Essential Cardiology: Principles and Practice. Totowa, New Jersey: Humana Press. pp. 545–563. doi:10.1007/978-1-59259-918-9_30. ISBN 978-1-59259-918-9.
- ^ Caldas, AM; Terreri, MT; Moises, VA; Silva, CM; Len, CA; Carvalho, AC; Hilário, MO (2008). "What is the true frequency of carditis in acute rheumatic fever? A prospective clinical and Doppler blind study of 56 children with up to 60 months of follow-up evaluation". Pediatric Cardiology. 29 (6): 1048–53. doi:10.1007/s00246-008-9242-z. PMID 18825449. S2CID 13330575.
- ^ Guilherme, L; Kalil, J; Cunningham, M (2006). "Molecular mimicry in the autoimmune pathogenesis of rheumatic heart disease". Autoimmunity. 39 (1): 31–9. doi:10.1080/08916930500484674. PMID 16455580. S2CID 16987808.
- ^ Kemeny, E; Grieve, T; Marcus, R; Sareli, P; Zabriskie, JB (1989). "Identification of mononuclear cells and T cell subsets in rheumatic valvulitis". Clinical Immunology and Immunopathology. 52 (2): 225–37. doi:10.1016/0090-1229(89)90174-8. PMID 2786783.
- ^ a b Roberts, S; Kosanke, S; Terrence Dunn, S; Jankelow, D; Duran, CM; Cunningham, MW (2001). "Pathogenic mechanisms in rheumatic carditis: Focus on valvular endothelium". The Journal of Infectious Diseases. 183 (3): 507–11. doi:10.1086/318076. PMID 11133385.
- ^ a b c Stanevicha, V; Eglite, J; Sochnevs, A; Gardovska, D; Zavadska, D; Shantere, R (2003). "HLA class II associations with rheumatic heart disease among clinically homogeneous patients in children in Latvia". Arthritis Research & Therapy. 5 (6): R340–R346. doi:10.1186/ar1000. PMC 333411. PMID 14680508.
- ^ Schafranski, MD; Pereira Ferrari, L; Scherner, D; Torres, R; Jensenius, JC; De Messias-Reason, IJ (2008). "High-producing MBL2 genotypes increase the risk of acute and chronic carditis in patients with history of rheumatic fever". Molecular Immunology. 45 (14): 3827–31. doi:10.1016/j.molimm.2008.05.013. PMID 18602696.
- ^ Ramasawmy, R; Spina, GS; Fae, KC; Pereira, AC; Nisihara, R; Messias Reason, IJ; Grinberg, M; Tarasoutchi, F; Kalil, J; Guilherme, L. (2008). "Association of Mannose-Binding Lectin Gene Polymorphism but Not of Mannose-Binding Serine Protease 2 with Chronic Severe Aortic Regurgitation of Rheumatic Etiology". Clinical and Vaccine Immunology. 15 (6): 932–936. doi:10.1128/CVI.00324-07. PMC 2446618. PMID 18400978.
- ^ Jones, T Duckett (1944). "The diagnosis of rheumatic fever". JAMA. 126 (8): 481–4. doi:10.1001/jama.1944.02850430015005.
- ^ Ferrieri, P; Jones Criteria Working, Group (2002). "Proceedings of the Jones Criteria workshop". Circulation. Jones Criteria Working Group. 106 (19): 2521–3. doi:10.1161/01.CIR.0000037745.65929.FA. PMID 12417554. Archived from the original on 31 December 2005.
- ^ "Antistreptolysin O (ASO)". 24 July 2020.
- ^ "Anti-DNase B". 28 June 2021.
- ^ a b c d e f g h i j k Gewitz Michael H.; Baltimore Robert S.; Tani Lloyd Y.; Sable Craig A.; Shulman Stanford T.; Carapetis Jonathan; Remenyi Bo; Taubert Kathryn A.; Bolger Ann F.; Beerman Lee; Mayosi Bongani M. (19 May 2015). "Revision of the Jones Criteria for the Diagnosis of Acute Rheumatic Fever in the Era of Doppler Echocardiography". Circulation. 131 (20): 1806–1818. doi:10.1161/CIR.0000000000000205. PMID 25908771. S2CID 46209822.
- ^ Parrillo, Steven J. "Rheumatic Fever". eMedicine. DO, FACOEP, FACEP. Archived from the original on 8 July 2007. Retrieved 14 July 2007.
- ^ "Guidelines for the diagnosis of rheumatic fever. Jones Criteria, 1992 update". JAMA. Special Writing Group of the Committee on Rheumatic Fever, Endocarditis, and Kawasaki Disease of the Council on Cardiovascular Disease in the Young of the American Heart Association. 268 (15): 2069–73. 1992. doi:10.1001/jama.268.15.2069. PMID 1404745.
- ^ Saxena, Anita (2000). "Diagnosis of rheumatic fever: Current status of Jones criteria and role of echocardiography". Indian Journal of Pediatrics. 67 (4): 283–6. doi:10.1007/BF02758174. PMID 11129913. S2CID 23052280.
- ^ Kumar, RK; Tandon, R (2013). "Rheumatic fever & rheumatic heart disease: The last 50 years". The Indian Journal of Medical Research. 137 (4): 643–658. PMC 3724245. PMID 23703332.
- ^ a b Ed Boon, Davidson's General Practice of Medicine, 제20판.페이지 617
- ^ a b c "WHO Rheumatic fever and rheumatic heart disease". www.who.int. Archived from the original on 7 March 2017. Retrieved 1 February 2017.
- ^ a b Karthikeyan, Ganesan; Guilherme, Luiza (July 2018). "Acute rheumatic fever". The Lancet. 392 (10142): 161–174. doi:10.1016/s0140-6736(18)30999-1. ISSN 0140-6736. PMID 30025809. S2CID 51702921.
- ^ Aly, Ashraf (2008). "Rheumatic Fever". Core Concepts of Pediatrics. University of Texas. Archived from the original on 24 May 2011. Retrieved 6 August 2011.
- ^ a b Gerber, MA; Baltimore, RS; Eaton, CB; Gewitz, M; Rowley, AH; Shulman, ST; Taubert, KA (24 March 2009). "Prevention of rheumatic fever and diagnosis and treatment of acute Streptococcal pharyngitis: a scientific statement from the American Heart Association Rheumatic Fever, Endocarditis, and Kawasaki Disease Committee of the Council on Cardiovascular Disease in the Young, the Interdisciplinary Council on Functional Genomics and Translational Biology, and the Interdisciplinary Council on Quality of Care and Outcomes Research: endorsed by the American Academy of Pediatrics". Circulation. 119 (11): 1541–51. doi:10.1161/circulationaha.109.191959. PMID 19246689.
- ^ a b Nulu, S; Bukhman, G; Kwan, GF (February 2017). "Rheumatic Heart Disease: The Unfinished Global Agenda". Cardiology Clinics. 35 (1): 165–180. doi:10.1016/j.ccl.2016.08.006. PMID 27886787.
- ^ "What About My Child and Rheumatic Fever?" (PDF). American Heart Association. Archived (PDF) from the original on 6 April 2013. Retrieved 23 February 2014.
- ^ "Aspirin Monograph for Professionals - Drugs.com". Drugs.com. American Society of Health-System Pharmacists. Archived from the original on 25 April 2017. Retrieved 30 March 2017.
- ^ "Collaboration aims for rheumatic fever vaccine". sciencemediacentre.co.nz. 18 September 2014. Archived from the original on 15 April 2017. Retrieved 16 April 2017.
- ^ "Initiative for Vaccine Research (IVR) – Group A Streptococcus". World Health Organization. Archived from the original on 13 May 2012. Retrieved 15 June 2012.
- ^ "WHO Disease and injury country estimates". World Health Organization. 2009. Archived from the original on 2 February 2014. Retrieved 11 November 2009.
- ^ Lozano R, Naghavi M, Foreman K, Lim S, Shibuya K, Aboyans V, et al. (2012). "Global and regional mortality from 235 causes of death for 20 age groups in 1990 and 2010: a systematic analysis for the Global Burden of Disease Study 2010". Lancet. 380 (9859): 2095–128. doi:10.1016/S0140-6736(12)61728-0. hdl:10536/DRO/DU:30050819. PMID 23245604. S2CID 1541253.
- ^ "Rheumatic fever". Medline Plus Medical Encyclopedia. NLM/NIH. Archived from the original on 7 April 2016.
- ^ "Rheumatic heart disease". Menzies Institute for Medical Research. Retrieved 1 September 2018.
- ^ Porth, Carol (2007). Essentials of pathophysiology: concepts of altered health states. Hagerstown, MD: Lippincott Williams & Wilkins. ISBN 978-0-7817-7087-3.
- ^ Marijon, Eloi; Ou, Phalla; Celermajer, David S.; Ferreira, Beatriz; Mocumbi, Ana Olga; Jani, Dinesh; Paquet, Christophe; Jacob, Sophie; Sidi, Daniel (2 August 2007). "Prevalence of rheumatic heart disease detected by echocardiographic screening". The New England Journal of Medicine. 357 (5): 470–476. doi:10.1056/NEJMoa065085. ISSN 1533-4406. PMID 17671255. S2CID 28936439.
- ^ Rothenbühler, Martina; O'Sullivan, Crochan J.; Stortecky, Stefan; Stefanini, Giulio G.; Spitzer, Ernest; Estill, Janne; Shrestha, Nikesh R.; Keiser, Olivia; Jüni, Peter (1 December 2014). "Active surveillance for rheumatic heart disease in endemic regions: a systematic review and meta-analysis of prevalence among children and adolescents" (PDF). The Lancet Global Health. 2 (12): e717–726. doi:10.1016/S2214-109X(14)70310-9. ISSN 2214-109X. PMID 25433627.
- ^ Shrestha NR; Karki P; Mahto R; et al. (2 March 2016). "Prevalence of subclinical rheumatic heart disease in eastern nepal: A school-based cross-sectional study". JAMA Cardiology. 1 (1): 89–96. doi:10.1001/jamacardio.2015.0292. ISSN 2380-6583. PMID 27437661.
- ^ Beaton, Andrea; Okello, Emmy; Lwabi, Peter; Mondo, Charles; McCarter, Robert; Sable, Craig (26 June 2012). "Echocardiography screening for rheumatic heart disease in Ugandan schoolchildren". Circulation. 125 (25): 3127–3132. doi:10.1161/CIRCULATIONAHA.112.092312. ISSN 1524-4539. PMID 22626741.
- ^ Karki, Prahlad (2021). "Effectiveness of Systematic Echocardiographic Screening for Rheumatic Heart Disease in Nepalese Schoolchildren: A Cluster Randomized Clinical Trial". JAMA Cardiology. 6 (4): 420–426. doi:10.1001/jamacardio.2020.7050. ISSN 2380-6583. PMC 7818193. PMID 33471029.
외부 링크
- "Jones major criteria". Archived from the original on 4 August 2017.