자가면역질환
Autoimmune disease| 자가면역질환 | |
|---|---|
 | |
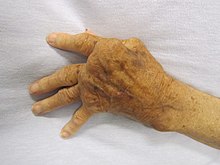
| 악성 발진이 있는 젊은 여성, 일반적으로 전신 홍반성 루푸스(SLE)에서 발견됨 | |
| 전문 | 류마티스, 면역학, 소화기내과, 신경학, 피부과, 내분비학 |
| 증상 | 광범위하고 상태에 따라 다릅니다. 일반적으로 낮은 등급의 열, 피로감을[1] 느끼는 것을 포함합니다. |
| 보통발병 | 성인기[1] |
| 종류들 | 자가면역질환 목록(알로페시아 부위, 백반증, 셀리악병, 당뇨병 1형, 하시모토병, 그레이브스병, 염증성 장질환, 다발성 경화증, 건선, 류마티스 관절염, 전신홍반성 루푸스 등)[1] |
| 약 | 비스테로이드성 항염증제, 면역억제제, 정맥면역글로불린[1][2] |
| 빈도수. | 10%(영국)[3] |
자가면역질환은 적응성 면역체계의 비정상적인 반응으로 인해 발생하는 질환으로, 신체의 건강하고 기능적인 부분을 마치 이물질인 것처럼 잘못 목표하고 공격합니다.[1] 알려진 자가면역질환만 80개가 넘는 것으로 추정되는데, 최근 과학적 증거에 따르면 100개 이상의 서로 다른 질환이 존재할 가능성이 있다고 합니다.[4][5][6] 거의 모든 신체 부위가 관련될 수 있습니다.[7]
자가면역질환은 자가염증질환과는 별개의 부류입니다. 둘 다 발진, 부종, 피로감 등 유사한 증상을 유발할 수 있는 면역체계 기능 이상이 특징이지만, 질병의 근본적인 원인이나 기전은 다릅니다. 자가 염증성 질환에서는 선천성 면역계의 기능 장애가 핵심적인 차이점인 반면, 자가 면역 질환에서는 적응성 면역계의 기능 장애가 있습니다.[8]
자가면역질환의 증상은 주로 질병의 특정 유형과 영향을 미치는 신체 부위에 따라 크게 달라질 수 있습니다. 증상은 종종 다양하고 일시적일 수 있으며 경미한 것에서 심각한 것까지 변동하며 일반적으로 저등급의 발열, 피로감 및 일반적인 불쾌감을 포함합니다.[1] 그러나 일부 자가 면역 질환은 관절통, 피부 발진(예: 두드러기) 또는 신경학적 증상과 같은 보다 구체적인 증상을 나타낼 수 있습니다.
자가면역질환의 정확한 원인은 불분명하며 유전적, 환경적 영향을 모두 수반하는 다인자일 가능성이 높습니다.[7] 루푸스와 같은 일부 질병은 유전적 소인을 암시하는 가족적 응집을 나타내는 반면, 다른 사례는 감염 유발 인자 또는 환경 요인에 대한 노출과 관련이 있으며, 이는 유전자와 환경 간의 복잡한 상호 작용을 의미합니다.
일반적으로 자가면역으로 분류되는 가장 흔한 질병으로는 셀리악병, 제1형 당뇨병, 그레이브스병, 염증성 장질환(크론병, 궤양성 대장염 등), 다발성 경화증, 탈모증,[9] 애디슨병, 악성 빈혈, 건선, 류마티스 관절염, 그리고 전신성 홍반성 루푸스. 자가면역질환의 진단은 다양한 양상과 많은 증상의 일시적인 특성으로 인해 어려울 수 있습니다.[1]
자가면역질환의 치료 양식은 질병의 종류와 중증도에 따라 다릅니다.[1] 치료적 접근은 주로 증상을 관리하고 면역 체계 활동을 줄이고 질병과 싸우는 신체의 능력을 유지하는 것을 목표로 합니다. 비스테로이드성 항염증제(NSAIDs)와 면역억제제는 일반적으로 염증을 줄이고 과활성 면역반응을 조절하기 위해 사용됩니다. 특정한 경우에는 면역체계를 조절하기 위해 정맥내 면역글로불린을 투여하기도 합니다.[2] 이러한 치료법이 증상 개선으로 이어지는 경우가 많음에도 불구하고, 대개 치료법을 제시하지 못하고 장기간의 관리가 필요한 경우가 많습니다.[1]
유병률에 있어서, 영국의 한 연구는 인구의 10%가 자가 면역 질환의 영향을 받고 있다는 것을 발견했습니다.[3] 여성이 남성보다 더 일반적으로 영향을 받습니다. 자가면역질환은 어느 연령에서나 발병할 수 있지만, 주로 성인기에 발병합니다.[1] 자가면역질환에 대한 초기 인식은 1900년대 초로 거슬러 올라가며, 그 이후로 이러한 질환에 대한 이해와 관리에 있어 상당한 발전이 이루어졌지만, 복잡한 병인과 병태생리를 완전히 밝히기 위해서는 훨씬 더 많은 것이 필요합니다.[10]
징후 및 증상
자가면역질환은 그 차이에도 불구하고 몇 가지 공통된 증상을 가지고 있는 광범위하고 다양한 질병 범주를 나타냅니다.[1] 이러한 공통된 증상은 우리 몸의 면역체계가 잘못해서 자신의 세포와 조직을 공격하여 염증과 손상을 일으키면서 발생합니다. 그러나 자가면역질환의 범위가 넓기 때문에 질병의 종류, 영향을 받는 장기 체계, 연령, 성별, 호르몬 상태, 환경적 영향 등 개인적 요인에 따라 증상의 구체적인 표현이 크게 달라질 수 있습니다.[1]
한 개인이 동시에 두 개 이상의 자가면역질환(다자가면역이라고 함)을 가질 수 있어 증상을 더욱 복잡하게 만듭니다.[1]
일반적인 증상
일반적으로 자가면역질환과 관련된 증상은 다음과 같습니다.[11]
- 피로감 자가면역질환을 앓고 있는 사람들의 가장 흔한 불만입니다.[12] 2015년 미국 조사에 따르면 자가면역질환을 가진 사람의 98%가 피로를 경험했고, 89%가 "주요 문제"라고 답했으며, 68%는 "피로는 정상과 전혀 다릅니다. 그것은 심오하고 [그들이] 가장 단순한 일상 업무를 할 수 없도록 합니다." 그리고 59%는 그것이 "아마도 AD를 가진 가장 쇠약한 증상"이라고 말했습니다.[13]
- 저열
- 권태감(일반적인 불편감이나 불안감)
- 근육통
- 관절통
- 피부 발진
특정 자가면역질환은 그 외에도 구강건조증, 안구건조증, 신체 일부의 얼얼함과 저림, 예상치 못한 체중감소 또는 증가, 설사 등 다양한 증상을 가지고 있습니다.
증상발생의 양상
이러한 증상은 종종 신체의 전신 염증 반응을 반영합니다. 그러나 이들의 발생과 강도는 시간이 지남에 따라 변동할 수 있으며, 이로 인해 질병 활동이 강화되는 기간(플레어업)과 완화 기간(완화 기간)이 상대적으로 비활성화되는 기간(완화 기간)이 발생할 수 있습니다.
증상의 구체적인 표현은 자가면역 반응의 위치와 유형에 크게 따라 달라집니다. 예를 들어, 관절에 주로 영향을 미치는 자가면역질환인 류마티스 관절염의 경우, 일반적으로 관절통, 부종, 경직 등의 증상이 나타납니다. 반면 췌장의 인슐린 생성 세포에 대한 자가면역 공격으로 발생하는 제1형 당뇨병은 주로 갈증 증가, 잦은 배뇨, 설명할 수 없는 체중 감소 등 고혈당과 관련된 증상을 나타냅니다.
일반적으로 영향을 받는 신체 부위
자가면역질환에서 일반적으로 영향을 받는 부위는 혈관, 결합조직, 관절, 근육, 적혈구, 피부, 갑상선(하시모토 갑상선염, 그레이브스병과 같은 질병에서), 췌장(제1형 당뇨병에서)과 같은 내분비선 등입니다. 이러한 질병의 영향은 특정 조직에 대한 국부적 손상, 장기 성장 및 기능의 변화, 신체 전체의 여러 조직이 영향을 받을 때 보다 전신적인 영향에 이르기까지 다양할 수 있습니다.[14]
추적 증상 발생값
이러한 징후와 증상의 출현은 종종 특정 생물학적 표지자에 대한 검사와 함께 자가면역 상태의 진단을 위한 단서를 제공할 뿐만 아니라 질병 진행과 치료에 대한 반응을 모니터링하는 데 도움이 될 수 있습니다.[15] 궁극적으로 자가면역질환의 다양한 특성으로 인해 이러한 질환의 관리를 위해서는 다양한 증상과 개인의 삶에 미치는 영향을 고려한 다차원적인 접근이 필요한 경우가 많습니다.
종류들
80종 이상의 자가면역질환이 존재하는 것으로 추정되지만, 이 섹션에서는 가장 일반적이고 잘 연구된 형태에 대한 개요를 제공합니다.[1][16][17]
실리아병
실리아병은 밀, 보리, 호밀에서 발견되는 단백질인 글루텐을 먹는 면역 반응입니다.[18] 이 질병에 걸린 사람들은 글루텐을 먹으면 소장에서 면역 반응이 일어나 소장에 줄을 잇고 영양소 흡수를 촉진하는 작은 손가락 모양의 돌기인 융모에 손상을 입습니다. [18] 이것은 위장관이 식도, 위, 소장, 대장, 직장, 항문을 포함하기 때문에 위장암의 위험이 증가하는 것을 설명합니다. 섭취한 글루텐이 소화 과정에서 통과하는 모든 영역입니다.[18] 환자가 식단에서 글루텐을 제거하면 위장암 발병률이 일부 감소하거나 제거될 수 있습니다.[18][19][20][21][22] 또한, 실장 질환은 림프증식 장애와 관련이 있습니다.[18]
그레이브스병
그레이브스병은 갑상선자극호르몬(TSH) 수용체(TRAb)에 대한 자가항체가 발달하는 것을 특징으로 하는 질환입니다. TRAb 자가항체가 TSH 수용체에 결합하면 조절되지 않는 갑상선 호르몬의 생성과 방출이 일어나며,[23] 이는 빠른 심박수, 체중 감소, 신경과민, 과민성과 같은 자극 효과를 초래할 수 있습니다. 그레이브스병에 더 특이한 다른 증상으로는 눈이 불룩하고 다리 아래가 붓는 것이 있습니다.
염증성 장질환
염증성 장질환(IBD)은 크론병, 궤양성 대장염 등 소화관의 만성 염증을 특징으로 하는 질환을 포괄합니다. 두 경우 모두 IBD를 가진 사람은 장내 미생물군집에 존재하는 정상적인 박테리아에 대한 면역 내성을 잃게 됩니다.[18] 증상으로는 심한 설사, 복통, 피로감, 체중 감소 등이 있습니다. IBD는 위장관의 암과 일부 림프증식성 암과 관련이 있습니다.[18]
다발성 경화증
다발성경화증(Multiple sclerosis, MS)은 중추신경계의 신경섬유의 보호 피복인 수초를 면역계가 공격하여 뇌와 신체의 나머지 부분 사이의 통신 문제를 일으키는 신경퇴행성 질환입니다. 증상으로는 피로감, 걷기 곤란, 저림이나 얼얼함, 근육 약화, 협응과 균형 문제 등이 나타날 수 있습니다. [24] MS는 주로 뇌에서 중추신경계 암의 위험 증가와 관련이 있습니다.[18]
류마티스 관절염
류마티스 관절염(RA)은 주로 관절을 표적으로 하여 지속적인 염증을 유발하여 관절 손상과 통증을 유발합니다. 한 손이나 무릎이 있으면 다른 한 손도 마찬가지라는 뜻으로 대칭적인 경우가 많습니다. RA는 또한 심장, 폐 및 눈에 영향을 미칠 수 있습니다. 또한, 만성 염증과 면역계의 과잉 활성화로 인해 다른 세포의 악성 변형을 촉진하는 환경이 형성되어 폐와 피부의 암과의 연관성 및 다른 혈액암의 위험 증가를 설명할 수 있습니다. 관절의 염증에 직접적인 영향을 받는 것은 없습니다.[25][26]
건선과 건선성 관절염
건선은 피부 세포가 빠르게 축적되어 피부 표면에 스케일링이 되는 것이 특징인 피부 상태입니다. 비늘 주변의 염증과 발적이 흔합니다.[27] 건선 환자 중에는 관절통, 뻣뻣함, 붓기를 유발하는 건선성 관절염이 발생하기도 합니다.[28]
쇼그렌 증후군
쇤그렌 증후군(SjS, SS)은 장기 자가면역질환으로, 인체의 수분을 생성하는 분비선에 영향을 미치고[4] 폐, 신장, 신경계 등 다른 장기계에도 종종 심각한 영향을 미칩니다.
전신성 홍반성 루푸스
전신성 홍반성 루푸스(SLE, systemic rulfus thematosus)는 단순히 루푸스라고 불리는 전신성 자가면역질환으로 피부, 관절, 신장, 신경계 등 여러 장기에 영향을 미칩니다. 면역 내성이 광범위하게 손실되는 것이 특징입니다.[29] 이 질병은 플레어와 완화 기간을 특징으로 하며 증상은 경미한 것부터 심각한 것까지 다양합니다. 여성들, 특히 가임기의 여성들은 불균형적으로 영향을 받습니다.[30]
제1형 당뇨병
제1형 당뇨병은 면역체계가 췌장에서 인슐린을 생성하는 베타세포를 공격해 혈당 수치가 높아지게 되면서 발생하는 질환입니다. 증상으로는 갈증 증가, 잦은 배뇨, 설명할 수 없는 체중 감소 등이 있습니다. 어린이와 젊은 성인에서 가장 흔하게 진단됩니다.[31]
미분화 결합조직질환
UCTD는 혈액검사 결과, 외부특성 등 결합조직질환의 특징을 가지고 있지만 어느 하나의 결합조직질환에 대해 확립된 진단기준을 충족하지 못하는 경우에 발생합니다. 시간이 지남에 따라 약 30-40%가 특정 결합 조직 질환으로 전환됩니다.
원인들
자가면역질환의 정확한 원인은 대부분 알려지지 않았지만,[7] 연구에 따르면 특정 감염뿐만 아니라 유전적, 환경적, 호르몬적 요인의 조합이 이러한 질병의 발병에 기여할 수 있다고 합니다.[1]
인간의 면역 체계는 외부 침입자로부터 방어하는 것과 자신의 세포를 보호하는 것 사이의 섬세한 균형을 유지하기 위한 여러 메커니즘을 갖추고 있습니다. 이를 위해 자가단백질과 반응할 수 있는 T세포와 B세포를 모두 생성합니다. 그러나 건강한 면역 반응에서 자가 반응성 세포는 일반적으로 활성화되기 전에 제거되거나, 에너지라는 과정을 통해 비활성화되거나, 조절 세포에 의해 활성이 억제됩니다.
유전학
자가면역질환이 발생하는 가족적인 경향은 유전적인 요소를 시사합니다. 루푸스나 다발성 경화증과 같은 일부 질환은 종종 같은 가족의 여러 구성원에게서 발생하며, 이는 잠재적인 유전적 연관성을 나타냅니다. 또 특정 자가면역질환 발병 위험을 높이는 특정 유전자도 확인됐습니다.
유전적 성향
자가면역질환 발병에 있어 강력한 유전적 요소를 제시하는 증거가 있습니다.[32] 예를 들어, 루푸스나 다발성 경화증과 같은 질환은 종종 같은 가족의 여러 사람에게서 나타나며, 이는 잠재적인 유전적 연관성을 나타냅니다. 또한 특정 자가면역 질환의 발병 위험을 증가시키는 특정 유전자가 확인되었습니다.[33]
유전체 전체 연관 연구(GWAS)와 같은 실험적 방법은 자가면역 질환의 잠재적 원인이 되는 유전적 위험 변이체를 정확하게 찾아내는 데 중요한 역할을 했습니다. 예를 들어, 이러한 연구는 제1형 당뇨병 및 류마티스 관절염과 같은 질병의 위험 변이를 식별하는 데 사용되었습니다.[34]
쌍둥이 연구에서 자가면역질환은 이란성 쌍둥이에 비해 일란성 쌍둥이에서 더 높은 일치율을 지속적으로 보여줍니다. 예를 들어, 다발성 경화증의 비율은 일란성 쌍둥이의 경우 35%인데 비해 이란성 쌍둥이의 경우 6%입니다.[35]
감염과 자가면역의 균형 잡기
진화 과정에서 선택된 특정 유전자가 감염에 대한 민감성과 자가면역 질환을 피할 수 있는 능력 사이의 균형을 제공한다는 증거가 증가하고 있습니다.[36] 예를 들어, ERAP2 유전자의 변이체는 자가면역(양성 선택)의 위험을 증가시킴에도 불구하고 감염에 대한 어느 정도의 내성을 제공합니다. 대조적으로, TYK2 유전자의 변이체는 자가면역질환으로부터 보호하지만 감염의 위험을 증가시킵니다(음성 선택). 이는 특히 역사적으로 높은 감염 위험을 고려할 때 감염 내성의 이점이 자가 면역 질환의 위험보다 클 수 있음을 시사합니다.[36]
유전체 전체 연관 연구(GWAS)와 같은 여러 실험 방법은 제1형 당뇨병 및 류마티스 관절염과 같은 질병의[37] 원인이 될 수 있는 유전적 위험 변이체를 식별하는 데 사용되었습니다.[38]
유사하게, 쌍둥이 연구에서 자가면역 질환은 이란성 쌍둥이에 비해 일란성 쌍둥이에서 더 높은 일치율을 지속적으로 보여줍니다. 예를 들어, 다발성 경화증에서 35% 대 6%입니다.[39]
환경적 요인
많은 환경적 요인들이 직접적으로 또는 촉매로서 다양한 자가면역질환의 개발과 진행에 관련되어 있습니다. 현재 연구에 따르면 자가면역질환의 최대 70%는 화학물질, 감염원, 식이 습관 및 장내세균불균형과 같은 일련의 요소를 포함하는 환경적 영향에 기인할 수 있습니다. 그러나 자가면역질환의 발병을 결정적으로 설명하는 통일된 이론은 여전히 모호하며, 이러한 조건의 복잡성과 다면적인 특성을 강조합니다.
다양한 환경 트리거가 식별되며, 그 중 일부는 다음과 같습니다.
우리의 즉각적인 환경의 일부이거나 약물에서 발견되는 화학 물질은 이러한 맥락에서 핵심적인 역할을 합니다. 이러한 화학 물질의 예로는 히드라진, 헤어 염료, 트리클로로에틸렌, 타르트라진, 유해 폐기물 및 산업 배출물이 있습니다.[41]
자외선(UV) 방사선은 피부근막염과 같은 자가면역 질환의 발병에 잠재적인 원인 인자로 연루되어 있습니다.[42] 또한, 살충제에 노출되는 것은 류마티스 관절염 발병 위험 증가와 관련이 있습니다.[43] 그러나 비타민 D는 특히 노인 인구에서 면역 기능 장애를 예방함으로써 보호 역할을 하는 것으로 보입니다.[44]
감염원은 또한 자가면역질환을 유발하는 데 중요한 단계인 T세포 활성화제로서의 역할을 점점 더 인정받고 있습니다. 그들이 질병 발병에 기여하는 정확한 메커니즘은 아직 완전히 이해되지 않았습니다. 예를 들어, 길랭-바레 증후군이나 류머티즘 열과 같은 특정 자가면역 질환은 감염에 의해 유발되는 것으로 알려져 있습니다.[45] 또한 대규모 데이터를 분석한 결과 SARS-CoV-2 감염(COVID-19의 원인균)과 광범위한 신종 자가면역질환 발병 위험 증가 사이에 중요한 연관성이 있는 것으로 나타났습니다.[46]
섹스.
자가면역질환 환자의 약 80%는 여성이 차지합니다.[47] 이러한 높은 가중치의 원인에 대해 많은 제안이 있었지만 명확한 설명은 없습니다.[48][49] 호르몬 인자에 대한 가능한 역할이 제시되었습니다.[50] 예를 들어, 일부 자가 면역 질환은 호르몬 수치가 높은 임신 기간([49]아마도 아이의 건강 보호를 증가시키기 위한 진화적 메커니즘으로)에 발광하고 호르몬 수치가 감소하는 폐경 후에 호전되는 경향이 있습니다. 여성들은 또한 자연적으로 자가면역질환이 사춘기와 임신에 유발될 수 있습니다.[47] 남성이 여성보다 의료 시스템과 덜 상호 작용할 수 있기 때문에 남성의 과소 보고도 한 요인이 될 수 있습니다.[51][52][53][54][55]
감염증
특정 바이러스 및 박테리아 감염은 자가 면역 질환과 관련이 있습니다.[56] 예를 들어, 연구에 따르면 인후염을 일으키는 박테리아인 화농성 연쇄상구균은 심장에 영향을 미치는 자가면역 반응인 류마티스열을 유발할 수 있다고 합니다.[57] 유사하게, 일부 연구들은 단핵증을 일으키는 Epstein-Barr 바이러스와 다발성 경화증 또는 루푸스의 후속 발병 사이의 연관성을 제안합니다.
조절되지 않는 면역반응
또 다른 관심 분야는 자가면역질환에서 손상되는 기능인 자가와 비자가를 구별하는 면역체계의 능력입니다. 건강한 개인의 경우 면역 관용은 면역 체계가 신체의 세포를 공격하는 것을 막습니다. 이 과정이 실패하면 면역체계는 자기 조직에 대한 항체를 생성하여 자가면역반응으로 이어질 수 있습니다.[58]
음의 선택과 흉선의 역할
자가 반응성 T 세포의 제거는 주로 T 세포의 성숙을 담당하는 기관인 흉선 내에서 "음성 선택"으로 알려진 메커니즘을 통해 이루어집니다.[59] 이 과정은 자가면역에 대한 방어의 핵심 라인 역할을 합니다. 이러한 보호 메커니즘이 실패하면 자가 반응성 세포의 풀이 면역계 내에서 기능하게 되어 자가 면역 질환의 발병에 기여할 수 있습니다.
분자 모방
캄필로박터 제주니와 같은 일부 감염원은 신체의 자가 분자와 유사하지만 동일하지 않은 항원을 가지고 있습니다. 분자 모방으로 알려진 이 현상은 교차 반응성으로 이어질 수 있는데, 이러한 감염에 대한 면역 반응은 무심코 자가 항원과도 반응하는 항체를 생성하게 됩니다.[60] 이것의 예는 C. jejuni 감염에 반응하여 생성된 항체가 말초 신경 축삭의 수초에 있는 강글리오사이드와 반응하는 길랭-바레 증후군입니다.[61]
진단.
자가면역질환 진단은 이 범주에 속하는 다양한 질병과 종종 중복되는 증상으로 인해 복잡할 수 있습니다. 정확한 진단은 적절한 치료 전략을 결정하는 데 중요합니다. 일반적으로 진단 프로세스에는 병력 평가, 신체 검사, 실험실 테스트 및 경우에 따라 이미징 또는 생검이 복합적으로 포함됩니다.[62]
병력 및 검사
자가면역질환 진단의 첫 단계는 일반적으로 환자의 병력에 대한 철저한 평가와 종합적인 신체검사입니다.[33] 임상의들은 종종 환자의 증상, 자가면역질환의 가족력, 자가면역반응을 유발할 수 있는 환경적 요인에 대한 노출에 세심한 주의를 기울입니다. 신체검사에서 자가면역질환의 일반적인 특징인 염증이나 장기손상의 징후가 드러날 수 있습니다.
실험실 테스트
실험실 테스트는 자가면역질환 진단에 중추적인 역할을 합니다. 이러한 테스트는 자기 주도 면역 반응을 나타내는 특정 자가 항체 또는 기타 면역 표지자의 존재를 식별할 수 있습니다.
- 자동 항체 테스트: 많은 자가면역질환은 자가항체가 존재하는 것이 특징입니다. 혈액 검사는 이러한 항체를 식별할 수 있으며, 이는 신체의 조직에 대해 지시됩니다.[63] 예를 들어, 항핵항체(ANA) 검사는 전신홍반성 루푸스(SLE) 및 기타 자가면역질환의 진단에 일반적으로 사용됩니다.
- 완전한 혈구 수 (CBC): CBC는 다양한 혈액 세포의 수와 특성에 대한 귀중한 정보를 제공할 수 있으며, 이는 일부 자가 면역 질환에 영향을 미칠 수 있습니다.[64][41][62]
- C-반응 단백질(CRP) 및 적혈구 침강 속도(ESR): 이 검사들은 자가면역질환에서 자주 높아지는 체내 염증 수치를 측정합니다.[62][41]
- 장기별 테스트: 특정 자가면역질환은 특정 장기를 대상으로 하므로 이러한 장기의 기능을 평가하기 위한 검사가 진단에 도움이 될 수 있습니다. 예를 들어 자가면역 갑상샘장애 진단에는 갑상선기능검사가 활용되고, 조직검사에서는 소장 손상을 확인해 셀리악병을 진단할 수 있습니다.
영상학 연구
경우에 따라 영상 연구를 사용하여 장기 침범 및 손상 정도를 평가할 수 있습니다. 예를 들어 흉부 엑스레이나 CT 촬영을 통해 류마티스 관절염이나 전신성 홍반성 루푸스 같은 질병에 폐가 관여하는 것을 확인할 수 있고, MRI를 통해 다발성 경화증에서 뇌와 척수에 염증이나 손상이 나타날 수 있습니다.
감별진단
자가면역질환과 연관될 수 있는 증상의 다양성과 비특이적인 특성을 고려할 때, 유사한 증상을 가진 여러 질병 중 어떤 것이 환자의 질병을 유발하는지를 결정하는 감별 진단은 진단 프로세스의 중요한 부분입니다. 이것은 종종 감염, 악성 종양 또는 유전적 장애와 같은 다른 잠재적인 증상의 원인을 배제하는 것을 포함합니다.
다학제적 접근
많은 자가면역 질환의 전신적 특성을 고려할 때, 이들의 진단과 관리를 위해서는 다학제적 접근이 필요할 수 있습니다. 여기에는 질병의 영향을 받는 기관이나 시스템에 따라 류마티스 전문의, 내분비 전문의, 소화기내과 전문의, 신경과 전문의, 피부과 전문의 및 기타 전문가가 참여할 수 있습니다.
요약하면 자가면역질환의 진단은 임상, 실험실, 영상 데이터에 대한 철저한 평가가 필요한 복잡한 과정입니다. 이러한 질병의 다양한 특성으로 인해 정확한 진단을 위해서는 종종 여러 전문가가 참여하는 개별화된 접근 방식이 중요합니다.
치료
치료는 질환의 종류와 중증도에 따라 다릅니다. 자가면역질환의 대부분은 만성이고 확실한 치료법은 없지만 치료로 증상을 완화하고 조절할 수 있습니다.[11] 표준 치료 방법은 다음과 같습니다.[11]
- 질병으로 인해 몸에 부족한 부분에 대한 비타민이나 호르몬 보충제(인슐린, 비타민B12, 갑상선호르몬 등)
- 혈액과 관련된 질병일 경우 수혈
- 질병이 뼈, 관절 또는 근육에 영향을 미칠 경우 물리치료
전통적인 치료 옵션에는 다음과 같은 신체 자체 조직에 대한 면역 반응을 줄이기 위한 면역 억제제가 포함됩니다.[65]
- 염증을 줄이기 위한 비스테로이드성 항염증제(NSAIDs)
- 염증을 줄이는 글루코코르티코이드
- 염증성 자가면역반응의 손상조직 및 장기효과를 감소시키기 위한 질병수정 항류마티스 약제(DMARDs)
면역 억제제는 전체적인 면역 반응을 약화시키기 때문에, 증상 완화는 잠재적으로 생명을 위협할 수 있는 감염과 싸우는 환자의 능력을 보존하는 것과 균형을 이루어야 합니다.[66]
비전통적 치료법은 특히 전통적 치료법이 실패했을 때 연구, 개발 및 사용되고 있습니다. 이러한 방법은 체내 병원성 세포의 활성화를 차단하거나, 이 세포를 자연적으로 억제하는 경로를 변경하는 것을 목표로 합니다.[66][67] 이러한 치료법은 환자에게 독성이 덜하고 더 구체적인 표적을 갖는 것을 목표로 합니다.[67] 이러한 옵션에는 다음이 포함됩니다.
- 친염증성 사이토카인을 차단하는 데 사용될 수 있는 단일클론항체
- 면역세포가 자가면역질환을[67] 일으키는 비정상적인 세포를 특이적으로 표적화할 수 있도록 하는 항원 특이적 면역요법
- 자가면역 반응으로 이어지는 경로를 차단하는 공동자극 차단 기능
- 자가면역반응을[66] 억제하기 위해 이 특수한 T세포를 이용하는 조절 T세포 치료
- Nigella sativa 꽃을 발견한 화합물인 Thymoquinone은 염증에 대한 영향으로 인해 여러 자가면역 질환을 치료할 가능성이 있는 것으로 연구되었습니다.[68][69]
역학
자가면역질환에 대한 미국의 집단 유병률에 대한 최초의 추정치는 1997년 Jacobson 등에 의해 발표되었습니다. 그들은 미국의 유병률이 약 9백만 명이라고 보고했고, 2억 7천 9백만 명의 미국 인구에게 24개 질병의 유병률 추정치를 적용했습니다.[70] 제이콥슨의 작업은 2012년 Hayter & Cook에 의해 갱신되었습니다.[71] 이 연구는 Rose & Bona가 수정한 [72]Witebsky의 가정을 사용하여 81개 질병으로 목록을 확장하고 81개 자가면역질환에 대한 전체 누적 미국 유병률을 5.0%로 추정했으며 남성은 3.0%, 여성은 7.1%였습니다.
자가면역질환을 한 개 이상 보유한 사람이 많다는 관측을 고려한 추정 지역사회 유병률은 남성이 2.7%, 여성이 6.4%로 전체적으로 4.5%였습니다.[71] 1980년대부터 2020년까지 미국에서 실시된 국민건강영양조사에서 자가면역질환의 일반적인 바이오마커인 항핵항체가 증가한 것으로 나타났습니다. 이는 자가면역질환의 위험요인으로 환경요인의 영향력이 더 강하다는 점을 지적하는 자가면역질환의 유병률이 증가했음을 보여줍니다.[73]
2024년 추산에 따르면 미국인 15명 중 1명은 자가면역질환을 하나 이상 갖고 있는 것으로 나타났습니다.ref>https://my.clevelandclinic.org/health/diseases/21624-autoimmune-diseases </ref>
조사.
이 질환은 자가면역질환과 염증질환 모두에서 인간의 적응성 또는 선천성 면역체계의 이상반응을 통해 발생합니다. 자가면역에서는 환자의 면역체계가 신체 자체의 단백질에 대항하여 활성화됩니다. 만성 염증성 질환에서 호중구 및 기타 백혈구는 사이토카인 및 케모카인에 의해 구성적으로 포섭되어 조직 손상이 발생합니다.[citation needed]
항염증 유전자의 활성화와 면역세포 내 염증 유전자의 억제에 의한 염증 완화는 유망한 치료적 접근법입니다.[74][75][76] 자가항체의 생산이 초기화되면 자가항체는 자체 생산을 유지할 수 있는 능력이 있다는 증거가 있습니다.[77]
줄기세포치료
줄기세포 이식은 연구되고 있으며 특정한 경우에 유망한 결과를 보여주었습니다.[78]
제1형 당뇨병에서 파괴되는 췌장 β세포를 대체하기 위한 의학 실험이 진행 중입니다.[79]
변형된 글리칸 이론
이 이론에 따르면 면역 반응의 이펙터 기능은 면역계의 세포와 체액 성분에 의해 나타나는 글리칸(다당류)에 의해 매개됩니다. 자가면역을 가진 사람들은 그들의 글리코실화 프로필에 변화가 있어서 전염증성 면역 반응을 선호합니다. 개별 자가면역질환은 특이한 글리칸 서명을 가질 것이라는 가설이 추가로 제기됩니다.[80]
위생가설
위생 가설에 따르면, 청결도가 높으면 아이들이 과거보다 적은 항원에 노출되어 면역체계가 과잉 활동하게 되고 자신의 조직을 외래 조직으로 오인할 가능성이 높아져 자가면역이나 천식과 같은 알레르기 질환이 발생합니다.[81]
비타민D가 면역반응에 미치는 영향
비타민 D는 적응적이고 선천적인 면역 반응을 돕는 면역 조절제로 알려져 있습니다.[82][83] 유전적 또는 환경적인 영향으로 비타민D가 결핍되면 면역반응이 더 비효율적이고 약화될 수 있으며 자가면역질환 발병의 한 원인으로 여겨집니다.[83] 비타민 D가 존재하면, 비타민 D 반응 요소(VDRE)는 패턴 인식 수용체(PRR) 반응과 그러한 반응과 관련된 유전자를 통해 암호화되고 발현됩니다.[82] 발현되는 특정 DNA 표적 서열은 1,25-(OH)2D3로 알려져 있습니다.[82] 1,25-(OH)2D3의 발현은 대식세포, 수지상세포, T세포, B세포에 의해 유도될 수 있습니다.[82] 1,25-(OH)2D3가 존재하는 경우, 면역계의 염증성 사이토카인 생성이 억제되고, 더 많은 내약성 조절 T-세포가 발현됩니다.[82] 이것은 비타민 D가 세포 성숙, 특히 T 세포 및 표현형 발현에 미치는 영향 때문입니다.[82] 1,25-(OH)2D3 발현의 부족은 덜 내성적인 조절 T 세포, 덜 내성적인 T 세포에 대한 항원의 더 큰 제시, 그리고 염증 반응의 증가로 이어질 수 있습니다.[82]
참고 항목
참고문헌
- ^ a b c d e f g h i j k l m n o "Autoimmune diseases". Office on Women's Health. U.S. Department of Health and Human Services. 22 February 2021. Archived from the original on 5 October 2016. Retrieved 5 October 2016.
- ^ a b Katz U, Shoenfeld Y, Zandman-Goddard G (2011). "Update on intravenous immunoglobulins (IVIg) mechanisms of action and off- label use in autoimmune diseases". Current Pharmaceutical Design. 17 (29): 3166–3175. doi:10.2174/138161211798157540. PMID 21864262.
- ^ a b Conrad N, Misra S, Verbakel JY, Verbeke G, Molenberghs G, Taylor PN, et al. (June 2023). "Incidence, prevalence, and co-occurrence of autoimmune disorders over time and by age, sex, and socioeconomic status: a population-based cohort study of 22 million individuals in the UK". Lancet. 401 (10391): 1878–1890. doi:10.1016/S0140-6736(23)00457-9. PMID 37156255. S2CID 258529606.
- ^ "List of Autoimmune Diseases". Autoimmune Registry Inc. Retrieved 2022-06-06.
- ^ Angum F, Khan T, Kaler J, Siddiqui L, Hussain A (May 2020). "The Prevalence of Autoimmune Disorders in Women: A Narrative Review". Cureus. 12 (5): e8094. doi:10.7759/cureus.8094. PMC 7292717. PMID 32542149. S2CID 219447364.
- ^ "Assessment of NIH Research on Autoimmune Diseases". www.nationalacademies.org. Retrieved 2022-06-13.
- ^ a b c Borgelt LM (2010). Women's Health Across the Lifespan: A Pharmacotherapeutic Approach. ASHP. p. 579. ISBN 978-1-58528-194-7. Archived from the original on 2017-09-08.
- ^ Zen M, Gatto M, Domeneghetti M, Palma L, Borella E, Iaccarino L, et al. (October 2013). "Clinical guidelines and definitions of autoinflammatory diseases: contrasts and comparisons with autoimmunity-a comprehensive review". Clinical Reviews in Allergy & Immunology. 45 (2): 227–235. doi:10.1007/s12016-013-8355-1. PMID 23322404. S2CID 23061331.
- ^ Erjavec SO, Gelfman S, Abdelaziz AR, Lee EY, Monga I, Alkelai A, et al. (February 2022). "Whole exome sequencing in Alopecia Areata identifies rare variants in KRT82". Nature Communications. 13 (1): 800. Bibcode:2022NatCo..13..800E. doi:10.1038/s41467-022-28343-3. PMC 8831607. PMID 35145093.
- ^ Ananthanarayan R, Paniker CK (2005). Ananthanarayan and Paniker's Textbook of Microbiology. Orient Blackswan. p. 169. ISBN 9788125028086. Archived from the original on 2017-09-08.
- ^ a b c "Autoimmune disorders". MedlinePlus, US National Library of Medicine. 16 July 2013. Retrieved 12 July 2023.
- ^ Zielinski MR, Systrom DM, Rose NR (2019-08-06). "Fatigue, Sleep, and Autoimmune and Related Disorders". Frontiers in Immunology. 10: 1827. doi:10.3389/fimmu.2019.01827. PMC 6691096. PMID 31447842.
- ^ Baumer K (2015-03-23). "Fatigue Survey Results Released". Autoimmune Association. Retrieved 2024-01-25.
- ^ Smith DA, Germolec DR (October 1999). "Introduction to immunology and autoimmunity". Environmental Health Perspectives. 107 (Suppl 5): 661–665. doi:10.1289/ehp.99107s5661. PMC 1566249. PMID 10502528.
- ^ National Research Council (US) Subcommittee on Immunotoxicology (1992). Autoimmune Diseases. National Academies Press (US).
- ^ "Autoimmune Disease List • AARDA". AARDA. 2016-06-01. Retrieved 2019-03-21.
- ^ Hohlfeld R, Dornmair K, Meinl E, Wekerle H (February 2016). "The search for the target antigens of multiple sclerosis, part 1: autoreactive CD4+ T lymphocytes as pathogenic effectors and therapeutic targets". The Lancet. Neurology. 15 (2): 198–209. doi:10.1016/S1474-4422(15)00334-8. PMID 26724103. S2CID 20082472.
- ^ a b c d e f g h Franks AL, Slansky JE (April 2012). "Multiple associations between a broad spectrum of autoimmune diseases, chronic inflammatory diseases and cancer". Anticancer Research. 32 (4): 1119–1136. PMC 3349285. PMID 22493341.
- ^ Meresse B, Ripoche J, Heyman M, Cerf-Bensussan N (January 2009). "Celiac disease: from oral tolerance to intestinal inflammation, autoimmunity and lymphomagenesis". Mucosal Immunology. 2 (1): 8–23. doi:10.1038/mi.2008.75. PMID 19079330. S2CID 24980464.
- ^ Green PH, Fleischauer AT, Bhagat G, Goyal R, Jabri B, Neugut AI (August 2003). "Risk of malignancy in patients with celiac disease". The American Journal of Medicine. 115 (3): 191–195. doi:10.1016/s0002-9343(03)00302-4. PMID 12935825.
- ^ Volta U, Vincentini O, Silano M (2011). "Papillary cancer of thyroid in celiac disease". Journal of Clinical Gastroenterology. 45 (5): e44–e46. doi:10.1097/mcg.0b013e3181ea11cb. PMID 20697293. S2CID 24754769.
- ^ Catassi C, Bearzi I, Holmes GK (April 2005). "Association of celiac disease and intestinal lymphomas and other cancers". Gastroenterology. 128 (4 Suppl 1): S79–S86. doi:10.1053/j.gastro.2005.02.027. PMID 15825131.
- ^ "Graves disease: MedlinePlus Genetics". MedlinePlus. 2013-07-01. Retrieved 2023-06-25.
- ^ Frohman EM, Racke MK, Raine CS (March 2006). "Multiple sclerosis--the plaque and its pathogenesis". The New England Journal of Medicine. 354 (9): 942–955. doi:10.1056/nejmra052130. PMID 16510748.
- ^ Turesson C, Matteson EL (2009). "Clinical Features of Rheumatoid Arthritis: Extra-Articular Manifestations". Rheumatoid Arthritis. Elsevier. pp. 62–67. doi:10.1016/b978-032305475-1.50014-8. ISBN 978-0-323-05475-1.
- ^ Khurana R, Berney SM (October 2005). "Clinical aspects of rheumatoid arthritis". Pathophysiology. 12 (3): 153–165. doi:10.1016/j.pathophys.2005.07.009. PMID 16125918.
- ^ "Psoriasis - Psoriatic Arthritis". National Library of Medicine. 2019-02-20. Retrieved 2023-06-25.
- ^ "Psoriatic Arthritis". National Library of Medicine. 2016-08-25. Retrieved 2023-06-25.
- ^ Tsokos GC (December 2011). "Systemic lupus erythematosus". The New England Journal of Medicine. 365 (22): 2110–2121. doi:10.1056/nejmra1100359. PMID 22129255.
- ^ "Lupus". Office on Women's Health. 2021-02-18. Retrieved 2023-06-25.
- ^ "Type 1 Diabetes - Juvenile Diabetes". National Library of Medicine. 2020-06-29. Retrieved 2023-06-25.
- ^ Antonelli A, Ferrari SM, Ragusa F, Elia G, Paparo SR, Ruffilli I, et al. (January 2020). "Graves' disease: Epidemiology, genetic and environmental risk factors and viruses". Best Practice & Research. Clinical Endocrinology & Metabolism. Elsevier BV. 34 (1): 101387. doi:10.1016/j.beem.2020.101387. PMID 32107168. S2CID 211555101.
- ^ a b Wang L, Wang FS, Gershwin ME (October 2015). "Human autoimmune diseases: a comprehensive update". Journal of Internal Medicine. Wiley. 278 (4): 369–395. doi:10.1111/joim.12395. PMID 26212387. S2CID 24386085.
- ^ Lettre G, Rioux JD (October 2008). "Autoimmune diseases: insights from genome-wide association studies". Human Molecular Genetics. Oxford University Press (OUP). 17 (R2): R116–R121. doi:10.1093/hmg/ddn246. PMC 2782355. PMID 18852199.
- ^ Willer CJ, Dyment DA, Risch NJ, Sadovnick AD, Ebers GC (October 2003). "Twin concordance and sibling recurrence rates in multiple sclerosis". Proceedings of the National Academy of Sciences of the United States of America. 100 (22): 12877–12882. Bibcode:2003PNAS..10012877W. doi:10.1073/pnas.1932604100. PMC 240712. PMID 14569025.
- ^ a b McKinney EF, Lee JC, Jayne DR, Lyons PA, Smith KG (July 2015). "T-cell exhaustion, co-stimulation and clinical outcome in autoimmunity and infection". Nature. Springer Science and Business Media LLC. 523 (7562): 612–616. Bibcode:2015Natur.523..612M. doi:10.1038/nature14468. PMC 4623162. PMID 26123020.
- ^ Gregersen PK, Olsson LM (2009). "Recent advances in the genetics of autoimmune disease". Annual Review of Immunology. 27: 363–391. doi:10.1146/annurev.immunol.021908.132653. PMC 2992886. PMID 19302045.
- ^ Hill NJ, King C, Flodstrom-Tullberg M (May 2008). "Recent acquisitions on the genetic basis of autoimmune disease". Frontiers in Bioscience. 13 (13): 4838–4851. doi:10.2741/3043. PMID 18508549.
- ^ Filippi M, Bar-Or A, Piehl F, Preziosa P, Solari A, Vukusic S, Rocca MA (November 2018). "Multiple sclerosis". Nature Reviews. Disease Primers. 4 (1): 43. doi:10.1038/s41572-018-0041-4. PMID 30410033. S2CID 53238233.
- ^ Vojdani A (2014). "A Potential Link between Environmental Triggers and Autoimmunity". Autoimmune Diseases. 2014: 437231. doi:10.1155/2014/437231. PMC 3945069. PMID 24688790.
- ^ a b c "Autoimmune Diseases: Symptoms & Causes". Boston Children's Hospital. Archived from the original on 7 April 2021. Retrieved 23 March 2020.
- ^ Shah M, Targoff IN, Rice MM, Miller FW, Rider LG (July 2013). "Brief report: ultraviolet radiation exposure is associated with clinical and autoantibody phenotypes in juvenile myositis". Arthritis and Rheumatism. 65 (7): 1934–1941. doi:10.1002/art.37985. PMC 3727975. PMID 23658122.
- ^ Meyer A, Sandler DP, Beane Freeman LE, Hofmann JN, Parks CG (July 2017). "Pesticide Exposure and Risk of Rheumatoid Arthritis among Licensed Male Pesticide Applicators in the Agricultural Health Study". Environmental Health Perspectives. 125 (7): 077010. doi:10.1289/EHP1013. PMC 5744649. PMID 28718769.
- ^ Meier HC, Sandler DP, Simonsick EM, Parks CG (December 2016). "Association between Vitamin D Deficiency and Antinuclear Antibodies in Middle-Aged and Older U.S. Adults". Cancer Epidemiology, Biomarkers & Prevention. 25 (12): 1559–1563. doi:10.1158/1055-9965.EPI-16-0339. PMC 5135624. PMID 27543618.
- ^ Wucherpfennig KW (October 2001). "Mechanisms for the induction of autoimmunity by infectious agents". The Journal of Clinical Investigation. 108 (8): 1097–1104. doi:10.1172/JCI14235. PMC 209539. PMID 11602615.
- ^ Sharma C, Bayry J (July 2023). "High risk of autoimmune diseases after COVID-19". Nature Reviews. Rheumatology. 19 (7): 399–400. doi:10.1038/s41584-023-00964-y. PMC 10096101. PMID 37046064.
- ^ a b Angum F, Khan T, Kaler J, Siddiqui L, Hussain A (May 2020). "The Prevalence of Autoimmune Disorders in Women: A Narrative Review". Cureus. 12 (5): e8094. doi:10.7759/cureus.8094. PMC 7292717. PMID 32542149.
- ^ Kronzer VL, Bridges SL, Davis JM (March 2021). "Why women have more autoimmune diseases than men: An evolutionary perspective". Evolutionary Applications. 14 (3): 629–633. Bibcode:2021EvApp..14..629K. doi:10.1111/eva.13167. PMC 7980266. PMID 33767739.
- ^ a b Moyer MW (September 1, 2021). "Why Nearly 80 Percent of Autoimmune Sufferers Are Female". Scientific American.
- ^ Moulton VR (2018-10-04). "Sex Hormones in Acquired Immunity and Autoimmune Disease". Frontiers in Immunology. Frontiers Media SA. 9: 2279. doi:10.3389/fimmu.2018.02279. PMC 6180207. PMID 30337927.
- ^ Schlichthorst M, Sanci LA, Pirkis J, Spittal MJ, Hocking JS (October 2016). "Why do men go to the doctor? Socio-demographic and lifestyle factors associated with healthcare utilisation among a cohort of Australian men". BMC Public Health. 16 (Suppl 3): 1028. doi:10.1186/s12889-016-3706-5. PMC 5103250. PMID 28185596.
- ^ "NCHS Pressroom - 2001 News Release - Women Visit Doctor More Often than Men". www.cdc.gov. 2019-05-24. Retrieved 2024-01-25.
- ^ "Pain bias: The health inequality rarely discussed". www.bbc.com. Retrieved 2024-01-25.
- ^ Hunt K, Adamson J, Hewitt C, Nazareth I (April 2011). "Do women consult more than men? A review of gender and consultation for back pain and headache". Journal of Health Services Research & Policy. 16 (2): 108–117. doi:10.1258/jhsrp.2010.009131. PMC 3104816. PMID 20819913.
- ^ Wang Y, Hunt K, Nazareth I, Freemantle N, Petersen I (August 2013). "Do men consult less than women? An analysis of routinely collected UK general practice data". BMJ Open. 3 (8): e003320. doi:10.1136/bmjopen-2013-003320. PMC 3753483. PMID 23959757.
- ^ Getts DR, Chastain EM, Terry RL, Miller SD (September 2013). "Virus infection, antiviral immunity, and autoimmunity". Immunological Reviews. Wiley. 255 (1): 197–209. doi:10.1111/imr.12091. PMC 3971377. PMID 23947356.
- ^ Karthikeyan G, Guilherme L (July 2018). "Acute rheumatic fever". Lancet. Elsevier BV. 392 (10142): 161–174. doi:10.1016/s0140-6736(18)30999-1. PMID 30025809. S2CID 51702921.
- ^ Conigliaro P, Triggianese P, Ballanti E, Perricone C, Perricone R, Chimenti MS (September 2019). "Complement, infection, and autoimmunity". Current Opinion in Rheumatology. Ovid Technologies (Wolters Kluwer Health). 31 (5): 532–541. doi:10.1097/bor.0000000000000633. hdl:2108/225709. PMID 31192812. S2CID 189813866.
- ^ Bruserud Ø, Oftedal BE, Wolff AB, Husebye ES (December 2016). "AIRE-mutations and autoimmune disease". Current Opinion in Immunology. Elsevier BV. 43: 8–15. doi:10.1016/j.coi.2016.07.003. PMID 27504588.
- ^ Rojas M, Restrepo-Jiménez P, Monsalve DM, Pacheco Y, Acosta-Ampudia Y, Ramírez-Santana C, et al. (December 2018). "Molecular mimicry and autoimmunity". Journal of Autoimmunity. Elsevier BV. 95: 100–123. doi:10.1016/j.jaut.2018.10.012. PMID 30509385. S2CID 54500571.
- ^ Jasti AK, Selmi C, Sarmiento-Monroy JC, Vega DA, Anaya JM, Gershwin ME (November 2016). "Guillain-Barré syndrome: causes, immunopathogenic mechanisms and treatment". Expert Review of Clinical Immunology. Informa UK Limited. 12 (11): 1175–1189. doi:10.1080/1744666x.2016.1193006. hdl:2434/424557. PMID 27292311. S2CID 45391831.
- ^ a b c "Autoimmune disorders". MedlinePlus Medical Encyclopedia. U.S. National Library of Medicine. Retrieved 23 March 2020.
- ^ "Antinuclear Antibody (ANA)". labtestsonline.org. Retrieved 14 April 2020.
- ^ "Complete blood count (CBC)". www.mayoclinic.org. 19 December 2018. Retrieved 14 April 2020.
- ^ Li P, Zheng Y, Chen X (2017). "Drugs for Autoimmune Inflammatory Diseases: From Small Molecule Compounds to Anti-TNF Biologics". Frontiers in Pharmacology. 8: 460. doi:10.3389/fphar.2017.00460. PMC 5506195. PMID 28785220.
- ^ a b c Rosenblum MD, Gratz IK, Paw JS, Abbas AK (March 2012). "Treating human autoimmunity: current practice and future prospects". Science Translational Medicine. 4 (125): 125sr1. doi:10.1126/scitranslmed.3003504. PMC 4061980. PMID 22422994.
- ^ a b c Smilek DE, Ehlers MR, Nepom GT (May 2014). "Restoring the balance: immunotherapeutic combinations for autoimmune disease". Disease Models & Mechanisms. 7 (5): 503–513. doi:10.1242/dmm.015099. PMC 4007402. PMID 24795433.
- ^ Ali MY, Akter Z, Mei Z, Zheng M, Tania M, Khan MA (February 2021). "Thymoquinone in autoimmune diseases: Therapeutic potential and molecular mechanisms". Biomedicine & Pharmacotherapy = Biomedecine & Pharmacotherapie. 134: 111157. doi:10.1016/j.biopha.2020.111157. PMID 33370631. S2CID 229714190.
- ^ Umar S, Hedaya O, Singh AK, Ahmed S (September 2015). "Thymoquinone inhibits TNF-α-induced inflammation and cell adhesion in rheumatoid arthritis synovial fibroblasts by ASK1 regulation". Toxicology and Applied Pharmacology. 287 (3): 299–305. doi:10.1016/j.taap.2015.06.017. PMC 4549173. PMID 26134265.
- ^ Jacobson DL, Gange SJ, Rose NR, Graham NM (September 1997). "Epidemiology and estimated population burden of selected autoimmune diseases in the United States". Clinical Immunology and Immunopathology. 84 (3): 223–243. doi:10.1006/clin.1997.4412. PMID 9281381.
- ^ a b Hayter SM, Cook MC (August 2012). "Updated assessment of the prevalence, spectrum and case definition of autoimmune disease". Autoimmunity Reviews. 11 (10): 754–765. doi:10.1016/j.autrev.2012.02.001. PMID 22387972.
- ^ Rose NR, Bona C (September 1993). "Defining criteria for autoimmune diseases (Witebsky's postulates revisited)". Immunology Today. 14 (9): 426–430. doi:10.1016/0167-5699(93)90244-F. PMID 8216719.
- ^ Dinse GE, Parks CG, Weinberg CR, Co CA, Wilkerson J, Zeldin DC, et al. (June 2020). "Increasing Prevalence of Antinuclear Antibodies in the United States". Arthritis & Rheumatology. 72 (6): 1026–1035. doi:10.1002/art.41214. PMC 7255943. PMID 32266792.
- ^ Mukundan L, Odegaard JI, Morel CR, Heredia JE, Mwangi JW, Ricardo-Gonzalez RR, et al. (November 2009). "PPAR-delta senses and orchestrates clearance of apoptotic cells to promote tolerance". Nature Medicine. 15 (11): 1266–1272. doi:10.1038/nm.2048. PMC 2783696. PMID 19838202.
- ^ Roszer T, Menéndez-Gutiérrez MP, Lefterova MI, Alameda D, Núñez V, Lazar MA, et al. (January 2011). "Autoimmune kidney disease and impaired engulfment of apoptotic cells in mice with macrophage peroxisome proliferator-activated receptor gamma or retinoid X receptor alpha deficiency". Journal of Immunology. 186 (1): 621–631. doi:10.4049/jimmunol.1002230. PMC 4038038. PMID 21135166.
- ^ Singh RP, Waldron RT, Hahn BH (July 2012). "Genes, tolerance and systemic autoimmunity". Autoimmunity Reviews. 11 (9): 664–669. doi:10.1016/j.autrev.2011.11.017. PMC 3306516. PMID 22155015.
- ^ Böhm I (May 2003). "Disruption of the cytoskeleton after apoptosis induction with autoantibodies". Autoimmunity. 36 (3): 183–189. doi:10.1080/0891693031000105617. PMID 12911286. S2CID 37887253.
- ^ Swart JF, Delemarre EM, van Wijk F, Boelens JJ, Kuball J, van Laar JM, Wulffraat NM (April 2017). "Haematopoietic stem cell transplantation for autoimmune diseases". Nature Reviews. Rheumatology. 13 (4): 244–256. doi:10.1038/nrrheum.2017.7. PMID 28228650. S2CID 21264933.
- ^ Drew L (2021-07-14). "How stem cells could fix type 1 diabetes". Nature. 595 (7867): S64–S66. Bibcode:2021Natur.595S..64D. doi:10.1038/d41586-021-01842-x. PMID 34262205. S2CID 235907766.
- ^ Maverakis E, Kim K, Shimoda M, Gershwin ME, Patel F, Wilken R, et al. (February 2015). "Glycans in the immune system and The Altered Glycan Theory of Autoimmunity: a critical review". Journal of Autoimmunity. 57: 1–13. doi:10.1016/j.jaut.2014.12.002. PMC 4340844. PMID 25578468.
- ^ Rook GA (February 2012). "Hygiene hypothesis and autoimmune diseases". Clinical Reviews in Allergy & Immunology. 42 (1): 5–15. doi:10.1007/s12016-011-8285-8. PMID 22090147. S2CID 15302882.
- ^ a b c d e f g Harrison SR, Li D, Jeffery LE, Raza K, Hewison M (January 2020). "Vitamin D, Autoimmune Disease and Rheumatoid Arthritis". Calcified Tissue International. 106 (1): 58–75. doi:10.1007/s00223-019-00577-2. PMC 6960236. PMID 31286174.
- ^ a b Lucas RM, Rodney Harris RM (August 2018). "On the Nature of Evidence and 'Proving' Causality: Smoking and Lung Cancer vs. Sun Exposure, Vitamin D and Multiple Sclerosis". International Journal of Environmental Research and Public Health. 15 (8): 1726. doi:10.3390/ijerph15081726. PMC 6121485. PMID 30103527.
더보기
- Vinay K, Abbas AK, Fausto M, Aster J (2010). Robbins and Cotran Pathologic Basis of Disease (8th ed.). Elsevier. p. 1464. ISBN 978-1-4160-3121-5.
- Asherson R (ed.). Handbook of Systemic Autoimmune Diseases. Elsevier.


