신생물
Neoplasm| 신생물 | |
|---|---|
| 기타 이름 | 종양, 종양, 카르키노사이트 |
 | |
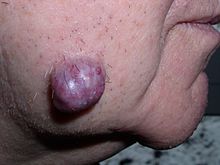
| 악성 종양, 즉 대장암의 침습적 예(분화구 모양, 불그스름, 불규칙한 형태의 종양)를 포함한 결장 절제 검체 | |
| 전문 | 종양학 |
| 증상 | 덩어리 |
| 합병증 | 암 |
| 원인들 | 방사선, 환경 요인, 특정 감염 |
신생물(/niː.oʊplézmm, niː)γ-/)[1][2]는 조직의 비정상적인 과도한 성장 형태이다.신생물질을 형성하거나 생성하는 과정을 신생물증이라고 한다.종양의 성장은 정상적인 주변 조직의 성장과 조화되지 않고, 원래의 방아쇠를 [3][4][5]제거해도 비정상적으로 계속 성장한다.이러한 비정상적인 성장은 [6]종양이라고 불릴 때 보통 덩어리를 형성한다.
ICD-10은 네 개의 주요 그룹으로 분류한다: 양성 종양, 현장 종양, 악성 종양, 불확실하거나 알려지지 않은 행동의 [7]종양.악성 종양은 암이라고도 하며 종양학의 초점이다.
조직이 비정상적으로 성장하기 전에, 종양으로서 세포는 종종 변형이나 [8]이형성과 같은 비정상적인 성장 패턴을 겪는다.그러나 메타플라시아 또는 이형성이 항상 신형성증으로 진행되는 것은 아니며 다른 [3]조건에서도 발생할 수 있다.이 단어는 고대 그리스어인 '신규'와 플라즈마 '형성, 창조'에서 왔다.
종류들
| -형성 및 -형성 |
|---|
종양은 양성, 잠재적으로 악성 또는 악성(암)[9]일 수 있습니다.
- 양성 종양에는 자궁 섬유종, 골생식물, 멜라노사이트네비(피부두더지)가 포함된다.그것들은 제한적이고 국소적이며 [8]암으로 변질되지 않는다.
- 잠재적으로 악성 종양은 제자리에 있는 암을 포함한다.그것들은 국소화되어 침입하거나 파괴하지는 않지만, 시간이 지나면 암으로 변할 수 있다.
- 악성 종양은 흔히 암이라고 불린다.그들은 주변 조직을 침범하여 파괴하고, 전이를 형성할 수 있으며, 치료하지 않거나 치료에 반응하지 않을 경우, 일반적으로 치명적인 것으로 판명될 것이다.
- 2차 종양은 1차 종양의 전이 분파이거나 화학요법이나 방사선 치료와 같은 특정 암 치료 후에 빈도가 증가하는 겉으로 보기에 관련이 없는 종양 중 하나를 말한다.
- 드물게 원발성 암의 알려진 부위가 없는 전이성 종양은 있을 수 있으며 이것은 알려지지 않은 원발성 암으로 분류된다.
클로날리티
종양은 종종 이질적이고 둘 이상의 세포를 포함하고 있지만, 그 시작과 지속적인 성장은 보통 하나의 종양 세포 집단에 의존합니다.이 세포들은 단일 클론성 즉, 같은 [10]세포에서 파생된 것으로 추정되며, 모두 같은 유전적 또는 후생학적 이상을 가지고 있는데, 이는 복제성을 분명히 보여준다.림프종 및 백혈병 등의 림프종 신생물에서는 클로날리티가 면역글로불린 유전자(B세포 병변용) 또는 T세포 수용체 유전자(T세포 병변용)의 단일 재배열로 증명된다.클로날리티의 증명은 림프세포의 증식을 종양으로 [11]식별하기 위해 필요한 것으로 간주되고 있다.
신생물종을 복제세포 증식으로 정의하는 것은 유혹적이지만 복제성의 증명은 항상 가능한 것은 아니다.따라서 종양의 정의에서 [citation needed]클로날리티는 필요하지 않다.
종양 대 종양
종양이라는 단어는 염증의 주요 징후 중 하나인 붓기를 뜻하는 라틴어에서 유래했다.그 단어는 원래 종양이든 아니든 어떤 형태의 종양이든 가리켰다.현대 영어에서 종양은 크기가 [12][13]커진 것처럼 보이는 신생물(신생물 세포의 비정상적인 성장에 의해 형성되거나 형성되지 않을 수 있는 고형 또는 액체로 채워진 낭포성 병변)의 동의어로 사용됩니다.일부 종양은 종양을 형성하지 않는다 - 백혈병과 대부분의 형태의 암종이 여기에 포함된다.종양은 또한 암과 동의어가 아니다.암은 당연히 악성이지만, 종양은 양성, 전암 또는 악성일 수 있습니다.
종괴와 결절이라는 용어는 종종 종양과 동의어로 사용된다.그러나 일반적으로 종양이라는 용어는 [3]병변의 물리적 크기에 관계없이 일반적으로 사용됩니다.보다 구체적으로, 질량이라는 용어는 병변의 최대 직경이 가장 큰 방향으로 최소 20mm(mm)인 경우에 자주 사용되며 결절이라는 용어는 일반적으로 병변의 크기가 가장 큰 치수(25.4mm =[3] 1인치)에서 20mm 미만일 때 사용됩니다.
원인들
인간의 종양은 단일 세포 내에서 축적된 유전적, 후생적 변화의 결과로 발생하는데, 이것은 세포를 통제 [14]불능으로 분열시키고 확장하게 만든다.종양은 조직의 비정상적인 증식에 의해 유발될 수 있으며, 이는 유전적 돌연변이에 의해 유발될 수 있다.모든 유형의 신생물종이 조직의 종양 과성장을 일으키는 것은 아니지만(예: 백혈병 또는 암종), 신생물 성장과 재생 과정 사이의 유사성(예: 탈분화 및 빠른 세포 증식)이 [15]지적되었다.
종양의 성장은 수학과 연속체 역학을 사용하여 연구되어 왔다.따라서 혈관종이나 림프관종과 같은 혈관종양은 끈적끈적한 세포와 [16]세포가 자랄 수 있는 공간을 채우는 유기액체로 이루어진 고체골격의 아말감이라고 볼 수 있다.이러한 유형의 모델에서는 기계적 스트레스와 균주가 처리될 수 있으며 종양과 주변 조직 및 혈관 구조에 미치는 영향을 설명할 수 있습니다.이 모델을 사용하는 실험의 최근 발견들은 종양의 활발한 성장이 종양의 바깥 가장자리로 제한되고 기초 정상 조직의 경직이 [17]종양의 성장을 억제한다는 것을 보여준다.
그러나 조직의 비정상적인 증식과 관련이 없는 양성 조건(예: 피지낭종)은 종양으로도 나타날 수 있지만 악성 가능성은 없다.유방 낭종(임신 중 및 다른 시기에 흔히 발생하는)은 다른 캡슐화된 선종(갑상선, 부신, 췌장)과 마찬가지로 또 다른 예이다.
캡슐화된 혈종, 캡슐화된 괴사 조직(곤충에 물린 상처, 이물질 또는 다른 유해한 메커니즘으로부터), 켈로이드(흉터 조직의 다른 과잉 성장) 및 육아종도 종양으로 존재할 수 있습니다.
유출 장애나 협착 또는 비정상적인 연결로 인해 정상 구조(요관, 혈관, 간내 또는 간외 담관, 폐포함물 또는 위장 복제)의 국소적인 이산적 확대도 종양으로 나타날 수 있다.예를 들어 동맥류 또는 동맥류(혈전 유무), 담도루 또는 동맥류, 경화성 담관염, 낭포성 낭종 또는 수화성 낭종, 장내 중복, 폐포함 등이 있다.내용물의 누출이 치명적일 수 있는 여러 종류의 종양을 조직 검사하는 것은 위험할 수 있습니다.그러한 유형의 종양이 발견되면, 그러한 심각한 [citation needed]합병증을 피하기 위해 조직검사 또는 외과적 탐색/절제 전에(또는 도중에) 초음파, CT 스캔, MRI, 혈관 조영 및 핵의학 스캔과 같은 진단적 양식이 사용된다.
악성 종양
DNA손상

DNA 손상은 [18]암으로 알려진 악성 종양들의 주된 근본 원인으로 여겨진다.암으로의 진행에 있어서의 그것의 중심적인 역할은, 이 섹션의 그림 상단의 상자안에 나타나 있다. (DNA 손상, 후생유전학적 변화 및 암으로의 진행에 있어서의 부족한 DNA 수복의 중심적인 특징은 빨간색으로 표시되어 있다.)DNA 손상은 매우 흔하다.자연적으로 발생하는 DNA 손상은 (대부분 세포 대사와 체온에서 물 속의 DNA 특성에 의해) 사람 세포당 평균 60,000개 이상의 새로운 손상의 속도로 매일 발생합니다[citation needed].외인성 물질에 노출되면 추가적인 DNA 손상이 발생할 수 있습니다.담배 연기는 외인성 DNA 손상을 증가시키고, 이러한 DNA 손상은 [19]흡연으로 인한 폐암의 원인일 수 있다.태양 방사선의 자외선은 흑색종에서 [20]중요한 DNA 손상을 일으킨다.헬리코박터균 감염은 DNA를 손상시키고 [21]위암의 원인이 되는 높은 수준의 활성산소를 생성한다.고지방 식단을 먹는 인간의 대장 내 높은 수준의 담즙산은 또한 DNA 손상을 일으키고 대장암에 [22]기여합니다.Katsurano 등은 염증이 있는 대장상피의 대식세포와 호중구가 대장 종양 [23][unreliable source?]발생을 시작하는 DNA 손상을 일으키는 활성산소의 원천이라고 밝혔다.DNA 손상의 원인은 이 섹션의 그림 상단에 있는 상자에 나와 있습니다.
34개의 DNA 복구 유전자 중 하나에 결핍을 일으키는 생식계 돌연변이를 가진 개인은 암 발병 위험이 증가한다.DNA 복구 유전자의 일부 생식계 돌연변이는 평생 암에 걸릴 확률을 100%까지 유발한다(예: p53 돌연변이).[24]이러한 생식선 돌연변이는 그림의 왼쪽에 있는 상자에 DNA 복구 결핍에 대한 기여도를 나타내는 화살표가 표시되어 있습니다.
악성 종양 중 약 70%는 유전적인 성분이 없고 "포자성 암"[25]이라고 불립니다.일부 산발성 암만이 DNA 수복 유전자의 돌연변이로 인한 DNA 수복에 결함이 있다.그러나 산발성 암의 대부분은 DNA 수복 유전자 발현을 감소시키거나 침묵시키는 후생유전학적 변화로 인해 DNA 수복에 결함이 있다.예를 들어, 113개의 순차 대장암 중 4개만이 DNA 복구 유전자 MGMT에서 미센스 돌연변이를 보였고, 대다수는 MGMT 프로모터 영역의 메틸화로 인해 MGMT 발현을 감소시켰다(후생유전자 변화).[26]대장암의 40%에서 90%가 MGMT 프로모터 [27][28][29][30][31]영역의 메틸화로 인해 MGMT 발현을 감소시켰다는 5가지 보고서가 있다.
마찬가지로 DNA수복유전자 PMS2 발현이 결여된 119건 중 PMS2는 PMS2 유전자의 돌연변이로 인해 6건에서 결핍된 반면, 103건에서는 짝짓기 파트너 MLH1이 프로모터 메틸화(PMS2 단백질 부재로 인해 억제됨)로 인해 PMS2 발현이 결핍된 것으로 나타났다.H1)[32] 다른 10가지 사례에서, PMS2 발현 손실은 MLH1을 [33]하향 조절하는 마이크로RNA, miR-155의 후생성 과발현에 의한 것일 수 있다.
또한 DNA 복구 유전자 BRCA1, WRN, FANCB, FANCF, MGMT, MLH1, MSH2, MSH4, ERCC1, XPF, NEIL1 및 ATM에 대해 13%-100%의 빈도에서 후생유전자 결함이 발견되었다.이러한 후생유전학적 결함은 다양한 암(예: 유방, 난소, 대장, 머리와 목)에서 발생했다.ERCC1, XPF 또는 PMS2 발현에서 2~3개의 결핍이 Facista 등에 [34]의해 평가된 49개의 대장암 중 대부분에서 동시에 발생한다.DNA 수복 유전자의 발현 저하를 일으키는 후생유전자의 변화를 본 섹션의 그림 상단에서 제3레벨의 중앙상자에 나타내고, 제4레벨의 DNA 수복결핍을 나타낸다.
DNA 수복 유전자의 발현이 감소하면 정상보다 높은 수준의 세포에 DNA 손상이 축적되고, 이러한 과도한 손상은 돌연변이나 발모 빈도를 증가시킨다.DNA 불일치[35][36] 복구 또는 상동 재조합 복구(HRR)[37]에서 결함이 있는 세포에서 돌연변이율이 크게 증가한다.
DNA 이중 가닥 절단 복구 또는 다른 DNA 손상 복구 중에, 복구 부위가 불완전하게 클리어되면 후생 유전자 침묵이 [38][39]발생할 수 있습니다.DNA 복구 결함(그림의 레벨 4)은 DNA 손상을 증가시켜(그림의 레벨 5), 체세포 돌연변이를 증가시키고 후생유전학적 변화(그림의 레벨 6)를 초래한다.
필드 결손은 여러 가지 변화가 있는 정상으로 나타나는 조직(및 아래 절에서 설명)으로 악성 종양에서 조직의 무질서하고 부적절하게 증식하는 클론의 발달에 대한 일반적인 전조이다.이러한 필드 결함(그림의 아래쪽에서 두 번째 레벨)은 다중 돌연변이와 후생유전학적 변화를 가질 수 있다.
일단 암이 형성되면 보통 게놈이 불안정해진다.이 불안정성은 DNA 복구가 감소하거나 과도한 DNA 손상이 원인일 수 있습니다.그러한 불안정성 때문에, 암은 계속 진화하고 서브 클론을 생산한다.예를 들어, 9개 영역에서 표본 추출된 신장암은 40개의 유비쿼터스 돌연변이를 가지고 있어 종양 이질성(즉, 암의 모든 영역에 존재하는 것), 59개의 돌연변이가 일부(전부는 아니지만)에 의해 공유되고 29개의 "개인" 돌연변이가 [40]암 영역 중 하나에만 존재했다.
필드 결함
"장 효과", "장 암화", "장 발암"을 포함한 다양한 용어들이 이 현상을 묘사하기 위해 사용되었다."장암화"라는 용어는 1953년에 상피의 한 영역 또는 "장"을 설명하기 위해 처음 사용되었으며, 상피가 [41]암 발병으로 발전하기 위해 (당시) 거의 알려지지 않은 과정에 의해 사전 조정되었다.그 이후로, "장암화"와 "장결함"이라는 용어는 새로운 [citation needed]암이 발생할 가능성이 있는 악성 조직 전(前) 조직을 설명하기 위해 사용되어 왔다.
암의 [42][43]진행에 있어 현장결함이 중요하다.그러나 루빈이 지적한 바와 같이[44] 대부분의 암 연구에서 암 연구의 대부분은 체내 또는 체외에서 잘 정의된 종양에 대해 수행되었다.그러나 돌연변이 표현형 인간 대장종양에서 발견된 체세포 돌연변이의 80% 이상이 말기 복제 [45]확장이 시작되기 전에 발생한다는 증거가 있다.마찬가지로, Vogelstein 외 [46]연구진은 종양에서 확인된 체세포 돌연변이의 절반 이상이 정상세포의 성장 중 종양이 생기기 전 단계(장결함)에서 발생했다고 지적한다.마찬가지로 종양에 존재하는 후생유전적 변화는 종양의 전장결함에서 발생할 [citation needed]수 있다.
전계효과에 대한 확장된 견해는 "생체학적 전계효과"라고 불리며, 이는 종양의 시작에서 [47]환자 사망에 이르는 국소 미세환경에서의 외인성 환경인자 및 분자변화의 영향을 포함한다.
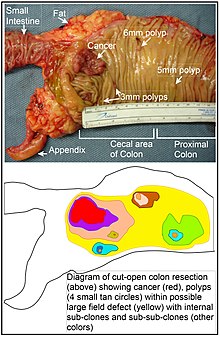
대장 내부 표면의 장내 크립트 중 하나의 기부에 있는 줄기세포 중 돌연변이 세포 또는 후생유전적으로 변경된 세포가 자연선택됨으로써 장내 결함이 발생할 수 있다.돌연변이 또는 후생유전적으로 변경된 줄기세포는 자연선택에 의해 근처의 다른 줄기세포를 대체할 수 있다.따라서 비정상적인 조직의 패치가 발생할 수 있습니다.이 섹션의 그림에는 대장암과 용종 4개를 보여주는 새로 절제된 세로 방향으로 열린 결장 부분의 사진이 포함되어 있습니다.사진 아래에는 돌연변이 세포 또는 후생유전적으로 변경된 세포의 큰 패치가 어떻게 형성되었는지에 대한 도식도가 있으며, 이 도표의 큰 면적이 노란색으로 표시되어 있습니다.이 다이어그램의 첫 번째 큰 패치(세포의 큰 클론) 내에서 주어진 줄기세포가 패치 내의 다른 줄기세포와 비교하여 이점을 획득하도록 두 번째 돌연변이 또는 후생유전적 변화가 발생할 수 있으며, 이 변경된 줄기세포는 원래 패치 내에서 2차 패치 또는 서브클론을 형성하면서 복제적으로 확장될 수 있다.이는 큰 노란색 원래 영역 내에 다른 색상의 4개의 작은 패치로 다이어그램에 나타나 있습니다.이러한 새로운 패치(서브클론) 내에서, 작은 용종 또는 악성 종양([citation needed]암)을 생성하는 줄기세포가 발생할 때까지 복제적으로 확장되는 4개의 2차 패치(그래픽에서 여전히 다른 색상으로) 내의 더 작은 패치로 나타나는 과정을 여러 번 반복할 수 있다.
사진에서 결장의 이 부분에서 명백한 필드 결손이 4개의 용종을 생성했습니다(용종의 크기, 6mm, 5mm, 3mm의 2개, 가장 긴 치수로 약 3cm의 암으로 라벨 표시됨).또한 이러한 종양은 사진 아래 다이어그램에서 4개의 작은 황갈색 원(용종)과 더 큰 빨간색 영역(암)으로 표시됩니다.사진 속 암은 대장이 소장과 결합하고(표지) 충수가 발생하는(표지) 결장의 맹장 부위에서 발생했다.사진 속의 지방은 결장의 외벽 바깥쪽에 있다.여기에 표시된 결장 부분에서는 결장 내면을 드러내고 [citation needed]결장 내피 내피 내에서 발생하는 암과 용종을 나타내기 위해 결장을 세로로 절단했다.
만약 산발적인 대장암이 발생하는 일반적인 과정이 자연선택에 의해 퍼지는 종양이 생기기 전 클론의 형성이고, 그 후 초기 클론 내의 내부 서브클론 및 그 내부의 서브클론의 형성이라면, 대장암은 일반적으로 비정상성 증가의 장과 관련되어야 하며, 그 앞에 와야 한다.y는 예감 이벤트의 연속을 반영합니다.가장 광범위한 이상 영역(도표에서 가장 바깥쪽 노란색 불규칙 영역)은 악성 종양 [citation needed]형성의 가장 이른 사건을 반영한다.
암의 특정 DNA 복구 결핍에 대한 실험 평가에서, 많은 특정 DNA 복구 결핍이 해당 암을 둘러싼 현장 결함에 발생하는 것으로 나타났다.아래 표는 암의 DNA 복구 결핍이 후생유전학적 변화에 의해 발생된 것으로 나타났으며, 주변 필드 결함에서 동일한 후생유전적으로 DNA 복구 결핍이 발견된 빈도가 다소 낮은 예를 보여준다.
| 암 | 진 | 암 발생 빈도 | 필드 결함의 빈도 | 레퍼런스 |
|---|---|---|---|---|
| 대장균 | 관리 | 46% | 34% | [27] |
| 대장균 | 관리 | 47% | 11% | [29] |
| 대장균 | 관리 | 70% | 60% | [48] |
| 대장균 | MSH2 | 13% | 5% | [29] |
| 대장균 | ERCC1 | 100% | 40% | [34] |
| 대장균 | PMS2 | 88% | 50% | [34] |
| 대장균 | XPF | 55% | 40% | [34] |
| 머리와 목 | 관리 | 54% | 38% | [49] |
| 머리와 목 | MLH1 | 33% | 25% | [50] |
| 머리와 목 | MLH1 | 31% | 20% | [51] |
| 배 | 관리 | 88% | 78% | [52] |
| 배 | MLH1 | 73% | 20% | [53] |
| 식도 | MLH1 | 77%-100% | 23%-79% | [54] |
개방된 대장 세그먼트의 사진에 나타난 필드 결함의 작은 용종 중 일부는 비교적 양성인 종양일 수 있다.대장내시경 검사에서 발견되고 3년 동안 반복 대장내시경 검사를 받은 10mm 미만의 용종 중 25%는 크기가 변하지 않았으며 35%는 크기가 퇴보 또는 축소된 반면 40%는 [55]크기가 커졌다.
게놈 불안정성
암은 게놈 불안정이나 돌연변이 표현형을 [56]보이는 것으로 알려져 있다.핵 내의 단백질 코드 DNA는 총 게놈 [57]DNA의 약 1.5%이다.이 단백질 코드 DNA (엑솜이라고 불림) 안에서, 유방 또는 결장의 평균 암은 약 60에서 70개의 단백질을 변화시키는 돌연변이를 가질 수 있으며, 그 중 약 3 또는 4개는 "운전자" 돌연변이일 수 있고, 나머지 것들은 "승객"[46] 돌연변이일 수 있다.그러나 유방암 조직 샘플 내 전체 게놈(비단백질 코드화 영역 포함)의 평균 DNA 염기서열 돌연변이 수는 [58]약 20,000개이다.평균 흑색종 조직 샘플에서(흑색종이 더 높은 엑솜 돌연변이[46] 빈도를 갖는 경우) 총 DNA 배열 돌연변이 수는 약 80,[59]000개입니다.이는 인간의 [60][61]세대 간(부모 대 자녀) 전체 게놈에서 약 70개의 새로운 돌연변이 빈도가 매우 낮은 것과 비교된다.
암 내 전체 뉴클레오티드 배열에서 높은 빈도의 돌연변이는 종종 암을 유발하는 필드 결함의 초기 변화(예: 이 섹션의 다이어그램의 노란색 영역)가 DNA 수복의 결핍임을 시사한다.결장암을 둘러싼 큰 필드 결함(암 양쪽에서 약 10cm까지 확장)은 필드 결함의 전체 영역에서 2개 또는 3개의 DNA 복구 단백질(ERCC1, XPF 또는 PMS2)에서 후생유전학적 결함을 자주 보이는 것으로 Facista [34]등에 의해 나타났다.DNA 수복의 결핍은 [35][36][37]돌연변이율을 증가시킨다.DNA 복구 자체의 결핍은 DNA 손상이 축적되도록 할 수 있으며, 그러한 손상 중 일부를 지나 오류 발생 가능성이 높은 트랜슬레이션 합성이 돌연변이를 일으킬 수 있다.또한 축적된 DNA 손상에 대한 잘못된 복구는 에피메이션이 발생할 수 있습니다.이러한 새로운 돌연변이 또는 에피메이션은 증식상의 이점을 제공하여 필드 결함을 발생시킬 수 있습니다.DNA 수복 유전자의 돌연변이/분열은 그 자체로 선택적인 이점을 부여하지는 않지만, 세포가 증식적 이점을 제공하는 추가적인 돌연변이/분열을 획득할 때 세포 내 이동자로서 운반될 수 있다.
어원학
종양이라는 용어는 종양과 동의어이다.신생물(Neoplasia)은 신생물/종양의 형성 과정을 의미하며, 이 과정을 신생물 과정이라고 한다.네오플라스틱이라는 단어 자체는 그리스어의 네오 'new'와 플라스틱 'formed, molded'[citation needed]에서 유래했다.
종양이라는 용어는 라틴어 명사 종양 'a spuling'에서 유래했고, 궁극적으로 동사 tum're 'to spuling'에서 유래했다.영국 연방에서는 철자 tumor가 일반적으로 사용되는 반면 미국에서는 보통 [citation needed]tumor라는 단어가 tumor로 쓰입니다.
의학적인 의미에서 종양은 전통적으로 살의 비정상적인 붓기를 의미해 왔다.로마의 의학 백과사전학자 셀수스 c.(기원전 30년–기원후 38년)는 급성 염증의 네 가지 주요 징후를 종양, 고로, 열, 그리고 루버라고 묘사했습니다.(그의 논문인 De Medicina는 가동 활자 인쇄기의 발명 이후 1478년에 인쇄된 최초의 의학 서적입니다.)
현대 영어에서 종양이라는 단어는 종종 낭포성(액체로 채워진) 성장 또는 고형 종양(암 또는 비암)[62]의 동의어로 사용되며, 다른 형태의 붓기는 종종 "스웰링"[63]이라고 한다.
관련 용어는 일반적으로 의학 문헌에서 발생하는데, 여기서 명사 tumefaction과 tumesence(형용사 [64]tumescent에서 파생)는 비종양성 부종을 나타내는 현재의 의학 용어이다.이런 종류의 붓기는 외상, 감염, 그리고 다른 요인들에 의해 야기되는 염증에 의해 가장 자주 발생한다.
그러나 종양은 종양세포의 과성장 이외의 조건에 의해 발생할 수 있다.낭종(예: 피지낭종)은 종양이라고 불리기도 하지만 종양은 종양세포가 없다.이는 의료비 청구 용어의 표준입니다(특히 아직 병리가 결정되지 않은 성장에 대해 청구하는 경우).
「 」를 참조해 주세요.
레퍼런스
- ^ "neoplasm". Lexico UK English Dictionary. Oxford University Press. n.d.
- ^ "neoplasm". Dictionary.com Unabridged (Online). n.d.
- ^ a b c d Birbrair A, Zhang T, Wang ZM, Messi ML, Olson JD, Mintz A, Delbono O (July 2014). "Type-2 pericytes participate in normal and tumoral angiogenesis". Am. J. Physiol., Cell Physiol. 307 (1): C25–38. doi:10.1152/ajpcell.00084.2014. PMC 4080181. PMID 24788248.
- ^ Cooper GM (1992). Elements of human cancer. Boston: Jones and Bartlett Publishers. p. 16. ISBN 978-0-86720-191-8.
- ^ Taylor, Elizabeth J. (2000). Dorland's Illustrated medical dictionary (29th ed.). Philadelphia: Saunders. p. 1184. ISBN 978-0721662541.
- ^ Stedman's medical dictionary (28th ed.). Philadelphia: Lippincott Williams & Wilkins. 2006. p. Neoplasm. ISBN 978-0781733908.
- ^ "II Neoplasms". International Statistical Classification of Diseases and Related Health Problems 10th Revision (ICD-10) Version for 2010. World Health Organization. Retrieved 19 June 2014.
- ^ a b Abrams, Gerald. "Neoplasia I". Retrieved 23 January 2012.
- ^ "Cancer - Activity 1 - Glossary, page 4 of 5". Archived from the original on 2008-05-09. Retrieved 2008-01-08.
- ^ "Medical Definition of Clone".
- ^ Lee ES, Locker J, Nalesnik M, Reyes J, Jaffe R, Alashari M, Nour B, Tzakis A, Dickman PS (January 1995). "The association of Epstein-Barr virus with smooth-muscle tumors occurring after organ transplantation". N. Engl. J. Med. 332 (1): 19–25. doi:10.1056/NEJM199501053320104. PMID 7990861.
- ^ "Pancreas Cancer: Glossary of Terms". Retrieved 2008-01-08.
- ^ "Tumor". Dorland's Illustrated Medical Dictionary (31st ed.). Saunders. 2007. ISBN 978-1-84972-348-0.
- ^ Tammela, Tuomas; Sage, Julien (2020). "Investigating Tumor Heterogeneity in Mouse Models". Annual Review of Cancer Biology. 4 (1): 99–119. doi:10.1146/annurev-cancerbio-030419-033413. PMC 8218894. PMID 34164589.
- ^ Asashima M, Oinuma T, Meyer-Rochow VB (1987). "Tumors in amphibia". Zoological Science. 4: 411–425.
- ^ Ambrosi D, Mollica F (2002). "On the mechanics of a growing tumor". International Journal of Engineering Science. 40 (12): 1297–316. doi:10.1016/S0020-7225(02)00014-9.
- ^ Volokh KY (September 2006). "Stresses in growing soft tissues". Acta Biomater. 2 (5): 493–504. doi:10.1016/j.actbio.2006.04.002. PMID 16793355.
- ^ Kastan MB (2008). "DNA damage responses: mechanisms and roles in human disease: 2007 G.H.A. Clowes Memorial Award Lecture". Mol. Cancer Res. 6 (4): 517–24. doi:10.1158/1541-7786.MCR-08-0020. PMID 18403632.
- ^ Cunningham FH, Fiebelkorn S, Johnson M, Meredith C (November 2011). "A novel application of the Margin of Exposure approach: segregation of tobacco smoke toxicants". Food Chem. Toxicol. 49 (11): 2921–33. doi:10.1016/j.fct.2011.07.019. PMID 21802474.
- ^ Kanavy HE, Gerstenblith MR (December 2011). "Ultraviolet radiation and melanoma". Semin Cutan Med Surg. 30 (4): 222–8. doi:10.1016/j.sder.2011.08.003. PMID 22123420.
- ^ Handa O, Naito Y, Yoshikawa T (2011). "Redox biology and gastric carcinogenesis: the role of Helicobacter pylori". Redox Rep. 16 (1): 1–7. doi:10.1179/174329211X12968219310756. PMC 6837368. PMID 21605492.
- ^ Bernstein C, Holubec H, Bhattacharyya AK, Nguyen H, Payne CM, Zaitlin B, Bernstein H (August 2011). "Carcinogenicity of deoxycholate, a secondary bile acid". Arch. Toxicol. 85 (8): 863–71. doi:10.1007/s00204-011-0648-7. PMC 3149672. PMID 21267546.
- ^ Katsurano M, Niwa T, Yasui Y, Shigematsu Y, Yamashita S, Takeshima H, Lee MS, Kim YJ, Tanaka T, Ushijima T (January 2012). "Early-stage formation of an epigenetic field defect in a mouse colitis model, and non-essential roles of T- and B-cells in DNA methylation induction". Oncogene. 31 (3): 342–51. doi:10.1038/onc.2011.241. PMID 21685942.
- ^ Malkin D (April 2011). "Li-fraumeni syndrome". Genes Cancer. 2 (4): 475–84. doi:10.1177/1947601911413466. PMC 3135649. PMID 21779515.
- ^ Lichtenstein P, Holm NV, Verkasalo PK, Iliadou A, Kaprio J, Koskenvuo M, Pukkala E, Skytthe A, Hemminki K (July 2000). "Environmental and heritable factors in the causation of cancer--analyses of cohorts of twins from Sweden, Denmark, and Finland". N. Engl. J. Med. 343 (2): 78–85. doi:10.1056/NEJM200007133430201. PMID 10891514.
- ^ Halford S, Rowan A, Sawyer E, Talbot I, Tomlinson I (June 2005). "O(6)-methylguanine methyltransferase in colorectal cancers: detection of mutations, loss of expression, and weak association with G:C>A:T transitions". Gut. 54 (6): 797–802. doi:10.1136/gut.2004.059535. PMC 1774551. PMID 15888787.
- ^ a b Shen L, Kondo Y, Rosner GL, Xiao L, Hernandez NS, Vilaythong J, Houlihan PS, Krouse RS, Prasad AR, Einspahr JG, Buckmeier J, Alberts DS, Hamilton SR, Issa JP (September 2005). "MGMT promoter methylation and field defect in sporadic colorectal cancer". J. Natl. Cancer Inst. 97 (18): 1330–8. doi:10.1093/jnci/dji275. PMID 16174854.
- ^ Psofaki V, Kalogera C, Tzambouras N, Stephanou D, Tsianos E, Seferiadis K, Kolios G (July 2010). "Promoter methylation status of hMLH1, MGMT, and CDKN2A/p16 in colorectal adenomas". World J. Gastroenterol. 16 (28): 3553–60. doi:10.3748/wjg.v16.i28.3553. PMC 2909555. PMID 20653064.
- ^ a b c Lee KH, Lee JS, Nam JH, Choi C, Lee MC, Park CS, Juhng SW, Lee JH (October 2011). "Promoter methylation status of hMLH1, hMSH2, and MGMT genes in colorectal cancer associated with adenoma-carcinoma sequence". Langenbecks Arch Surg. 396 (7): 1017–26. doi:10.1007/s00423-011-0812-9. PMID 21706233. S2CID 8069716.
- ^ Amatu A, Sartore-Bianchi A, Moutinho C, Belotti A, Bencardino K, Chirico G, Cassingena A, Rusconi F, Esposito A, Nichelatti M, Esteller M, Siena S (April 2013). "Promoter CpG island hypermethylation of the DNA repair enzyme MGMT predicts clinical response to dacarbazine in a phase II study for metastatic colorectal cancer". Clin. Cancer Res. 19 (8): 2265–72. doi:10.1158/1078-0432.CCR-12-3518. PMID 23422094.
- ^ Mokarram P, Zamani M, Kavousipour S, Naghibalhossaini F, Irajie C, Moradi Sarabi M, et al. (May 2013). "Different patterns of DNA methylation of the two distinct O6-methylguanine-DNA methyltransferase (O6-MGMT) promoter regions in colorectal cancer". Mol. Biol. Rep. 40 (5): 3851–7. doi:10.1007/s11033-012-2465-3. PMID 23271133. S2CID 18733871.
- ^ Truninger K, Menigatti M, Luz J, Russell A, Haider R, Gebbers JO, et al. (May 2005). "Immunohistochemical analysis reveals high frequency of PMS2 defects in colorectal cancer". Gastroenterology. 128 (5): 1160–71. doi:10.1053/j.gastro.2005.01.056. PMID 15887099.
- ^ Valeri N, Gasparini P, Fabbri M, Braconi C, Veronese A, Lovat F, et al. (April 2010). "Modulation of mismatch repair and genomic stability by miR-155". Proc. Natl. Acad. Sci. U.S.A. 107 (15): 6982–7. Bibcode:2010PNAS..107.6982V. doi:10.1073/pnas.1002472107. PMC 2872463. PMID 20351277.
- ^ a b c d e Facista A, Nguyen H, Lewis C, Prasad AR, Ramsey L, Zaitlin B, et al. (2012). "Deficient expression of DNA repair enzymes in early progression to sporadic colon cancer". Genome Integr. 3 (1): 3. doi:10.1186/2041-9414-3-3. PMC 3351028. PMID 22494821.
- ^ a b Narayanan L, Fritzell JA, Baker SM, Liskay RM, Glazer PM (April 1997). "Elevated levels of mutation in multiple tissues of mice deficient in the DNA mismatch repair gene Pms2". Proc. Natl. Acad. Sci. U.S.A. 94 (7): 3122–7. Bibcode:1997PNAS...94.3122N. doi:10.1073/pnas.94.7.3122. PMC 20332. PMID 9096356.
- ^ a b Hegan DC, Narayanan L, Jirik FR, Edelmann W, Liskay RM, Glazer PM (December 2006). "Differing patterns of genetic instability in mice deficient in the mismatch repair genes Pms2, Mlh1, Msh2, Msh3 and Msh6". Carcinogenesis. 27 (12): 2402–8. doi:10.1093/carcin/bgl079. PMC 2612936. PMID 16728433.
- ^ a b Tutt AN, van Oostrom CT, Ross GM, van Steeg H, Ashworth A (March 2002). "Disruption of Brca2 increases the spontaneous mutation rate in vivo: synergism with ionizing radiation". EMBO Rep. 3 (3): 255–60. doi:10.1093/embo-reports/kvf037. PMC 1084010. PMID 11850397.
- ^ O'Hagan HM, Mohammad HP, Baylin SB (2008). Lee JT (ed.). "Double strand breaks can initiate gene silencing and SIRT1-dependent onset of DNA methylation in an exogenous promoter CpG island". PLOS Genet. 4 (8): e1000155. doi:10.1371/journal.pgen.1000155. PMC 2491723. PMID 18704159.
- ^ Cuozzo C, Porcellini A, Angrisano T, Morano A, Lee B, Di Pardo A, Messina S, Iuliano R, Fusco A, Santillo MR, Muller MT, Chiariotti L, Gottesman ME, Avvedimento EV (July 2007). "DNA damage, homology-directed repair, and DNA methylation". PLOS Genet. 3 (7): e110. doi:10.1371/journal.pgen.0030110. PMC 1913100. PMID 17616978.
- ^ Gerlinger M, Rowan AJ, Horswell S, Larkin J, Endesfelder D, Gronroos E, et al. (March 2012). "Intratumor heterogeneity and branched evolution revealed by multiregion sequencing". N. Engl. J. Med. 366 (10): 883–92. doi:10.1056/NEJMoa1113205. PMC 4878653. PMID 22397650.
- ^ Slaughter DP, Southwick HW, Smejkal W (September 1953). "Field cancerization in oral stratified squamous epithelium; clinical implications of multicentric origin". Cancer. 6 (5): 963–8. doi:10.1002/1097-0142(195309)6:5<963::AID-CNCR2820060515>3.0.CO;2-Q. PMID 13094644. S2CID 6736946.
- ^ Bernstein C, Bernstein H, Payne CM, Dvorak K, Garewal H (February 2008). "Field defects in progression to gastrointestinal tract cancers". Cancer Lett. 260 (1–2): 1–10. doi:10.1016/j.canlet.2007.11.027. PMC 2744582. PMID 18164807.
- ^ Nguyen H, Loustaunau C, Facista A, Ramsey L, Hassounah N, Taylor H, Krouse R, Payne CM, Tsikitis VL, Goldschmid S, Banerjee B, Perini RF, Bernstein C (2010). "Deficient Pms2, ERCC1, Ku86, CcOI in field defects during progression to colon cancer". J Vis Exp (41): 1931. doi:10.3791/1931. PMC 3149991. PMID 20689513.
- ^ Rubin H (March 2011). "Fields and field cancerization: the preneoplastic origins of cancer: asymptomatic hyperplastic fields are precursors of neoplasia, and their progression to tumors can be tracked by saturation density in culture". BioEssays. 33 (3): 224–31. doi:10.1002/bies.201000067. PMID 21254148. S2CID 44981539.
- ^ Tsao JL, Yatabe Y, Salovaara R, Järvinen HJ, Mecklin JP, Aaltonen LA, Tavaré S, Shibata D (February 2000). "Genetic reconstruction of individual colorectal tumor histories". Proc. Natl. Acad. Sci. U.S.A. 97 (3): 1236–41. Bibcode:2000PNAS...97.1236T. doi:10.1073/pnas.97.3.1236. PMC 15581. PMID 10655514.
- ^ a b c Vogelstein B, Papadopoulos N, Velculescu VE, Zhou S, Diaz LA, Kinzler KW (March 2013). "Cancer genome landscapes". Science. 339 (6127): 1546–58. Bibcode:2013Sci...339.1546V. doi:10.1126/science.1235122. PMC 3749880. PMID 23539594.
- ^ Lochhead P, Chan AT, Nishihara R, Fuchs CS, Beck AH, Giovannucci E, Ogino S (2014). "Etiologic field effect: reappraisal of the field effect concept in cancer predisposition and progression". Mod Pathol. 28 (1): 14–29. doi:10.1038/modpathol.2014.81. PMC 4265316. PMID 24925058.
- ^ Svrcek M, Buhard O, Colas C, Coulet F, Dumont S, Massaoudi I, et al. (November 2010). "Methylation tolerance due to an O6-methylguanine DNA methyltransferase (MGMT) field defect in the colonic mucosa: an initiating step in the development of mismatch repair-deficient colorectal cancers". Gut. 59 (11): 1516–26. doi:10.1136/gut.2009.194787. PMID 20947886. S2CID 206950452.
- ^ Paluszczak J, Misiak P, Wierzbicka M, Woźniak A, Baer-Dubowska W (February 2011). "Frequent hypermethylation of DAPK, RARbeta, MGMT, RASSF1A and FHIT in laryngeal squamous cell carcinomas and adjacent normal mucosa". Oral Oncol. 47 (2): 104–7. doi:10.1016/j.oraloncology.2010.11.006. PMID 21147548.
- ^ Zuo C, Zhang H, Spencer HJ, Vural E, Suen JY, Schichman SA, Smoller BR, Kokoska MS, Fan CY (October 2009). "Increased microsatellite instability and epigenetic inactivation of the hMLH1 gene in head and neck squamous cell carcinoma". Otolaryngol Head Neck Surg. 141 (4): 484–90. doi:10.1016/j.otohns.2009.07.007. PMID 19786217. S2CID 8357370.
- ^ Tawfik HM, El-Maqsoud NM, Hak BH, El-Sherbiny YM (2011). "Head and neck squamous cell carcinoma: mismatch repair immunohistochemistry and promoter hypermethylation of hMLH1 gene". Am J Otolaryngol. 32 (6): 528–36. doi:10.1016/j.amjoto.2010.11.005. PMID 21353335.
- ^ Zou XP, Zhang B, Zhang XQ, Chen M, Cao J, Liu WJ (November 2009). "Promoter hypermethylation of multiple genes in early gastric adenocarcinoma and precancerous lesions". Hum. Pathol. 40 (11): 1534–42. doi:10.1016/j.humpath.2009.01.029. PMID 19695681.
- ^ Wani M, Afroze D, Makhdoomi M, Hamid I, Wani B, Bhat G, Wani R, Wani K (2012). "Promoter methylation status of DNA repair gene (hMLH1) in gastric carcinoma patients of the Kashmir valley". Asian Pac. J. Cancer Prev. 13 (8): 4177–81. doi:10.7314/APJCP.2012.13.8.4177. PMID 23098428.
- ^ Agarwal A, Polineni R, Hussein Z, Vigoda I, Bhagat TD, Bhattacharyya S, Maitra A, Verma A (2012). "Role of epigenetic alterations in the pathogenesis of Barrett's esophagus and esophageal adenocarcinoma". Int J Clin Exp Pathol. 5 (5): 382–96. PMC 3396065. PMID 22808291.
- ^ Hofstad B, Vatn MH, Andersen SN, Huitfeldt HS, Rognum T, Larsen S, Osnes M (September 1996). "Growth of colorectal polyps: redetection and evaluation of unresected polyps for a period of three years". Gut. 39 (3): 449–56. doi:10.1136/gut.39.3.449. PMC 1383355. PMID 8949653.
- ^ Schmitt MW, Prindle MJ, Loeb LA (September 2012). "Implications of genetic heterogeneity in cancer". Ann. N. Y. Acad. Sci. 1267 (1): 110–6. Bibcode:2012NYASA1267..110S. doi:10.1111/j.1749-6632.2012.06590.x. PMC 3674777. PMID 22954224.
- ^ Lander ES, Linton LM, Birren B, Nusbaum C, Zody MC, Baldwin J, Devon K, Dewar K, Doyle M, FitzHugh W, et al. (February 2001). "Initial sequencing and analysis of the human genome" (PDF). Nature. 409 (6822): 860–921. Bibcode:2001Natur.409..860L. doi:10.1038/35057062. PMID 11237011.
- ^ Yost SE, Smith EN, Schwab RB, Bao L, Jung H, Wang X, Voest E, Pierce JP, Messer K, Parker BA, Harismendy O, Frazer KA (August 2012). "Identification of high-confidence somatic mutations in whole genome sequence of formalin-fixed breast cancer specimens". Nucleic Acids Res. 40 (14): e107. doi:10.1093/nar/gks299. PMC 3413110. PMID 22492626.
- ^ Berger MF, Hodis E, Heffernan TP, Deribe YL, Lawrence MS, Protopopov A, et al. (May 2012). "Melanoma genome sequencing reveals frequent PREX2 mutations". Nature. 485 (7399): 502–6. Bibcode:2012Natur.485..502B. doi:10.1038/nature11071. PMC 3367798. PMID 22622578.
- ^ Roach JC, Glusman G, Smit AF, Huff CD, Hubley R, Shannon PT, et al. (April 2010). "Analysis of genetic inheritance in a family quartet by whole-genome sequencing". Science. 328 (5978): 636–9. Bibcode:2010Sci...328..636R. doi:10.1126/science.1186802. PMC 3037280. PMID 20220176.
- ^ Campbell CD, Chong JX, Malig M, Ko A, Dumont BL, Han L, et al. (November 2012). "Estimating the human mutation rate using autozygosity in a founder population". Nat. Genet. 44 (11): 1277–81. doi:10.1038/ng.2418. PMC 3483378. PMID 23001126.
- ^ 의학 백과사전의 종양
- ^ "Swelling". MedlinePlus Medical Encyclopedia. October 14, 2012.
- ^ "tumescence". Oxford English Dictionary (Online ed.). Oxford University Press. (가입 또는 참여기관 회원가입 필요)