5-HT3 수용체
5-HT3 receptor5-HT3 수용체는 리간드 게이트 이온 채널(LGICs)의 씨스루프 슈퍼패밀리에 속하므로 G 단백질 결합 수용체인 다른 모든 5-HT 수용체(5-hydroxytiptaine, 또는 세로토닌) 수용체와 구조적으로 기능적으로 차이가 있다.[1][2][3] 이 이온 채널은 양이온 선택적이며 중추신경계 및 말초신경계 내에서 뉴런의 탈극화와 흥분작용을 매개한다.[1]
5-HT 수용체는 다른 리간드 게이트 이온3 채널과 마찬가지로 나트륨(Na), 칼륨(K), 칼슘(Ca) 이온에 침투할 수 있는 중앙 이온 전도공 주위에 배열된 5개의 서브유닛으로 구성된다. 5-HT 수용체에3 신경전달물질 5-hydroxytryptamine(세로토닌)을 결합하면 채널이 열리고, 이는 다시 뉴런의 흥분반응으로 이어진다. 빠르게 활성화되고, 감압되고, 내부 전류는 주로 나트륨과 칼륨 이온에 의해 전달된다.[2] 5-HT3 수용체는 음이온에 대한 투과성이 미미하다.[1] 그것들은 니코틴 아세틸콜린 수용체와 가장 밀접한 관련이 있다.
구조
5-HT3 수용체는 G-단백 결합형인 다른 5-HT 수용체 하위 유형과 구조 및 메커니즘이 현저하게 다르다. 기능 채널은 5개의 동일한 5-HT3A 서브유닛(동형미) 또는 5-HT의3A 혼합물 및 다른 4개의 5-HT3B,[4][5][6][7] 5-HT3C, 5-HT3D 또는 5-HT3E 서브유닛 중 하나로 구성될 수 있다.[8] 오직 5-HT3A 서브유닛만이 기능적 동음이의 미국 채널을 형성하는 것으로 보인다. 다른 모든 서브유닛 하위유형은 기능 채널을 형성하기 위해3A 5-HT 하위유닛으로 이질화해야 한다. 또한, 현재 이형 5-HT3AC, 5-HT3AD, 5-HT3AE 및 동형 5-HT3A 수용체 간에 약리학적 차이가 발견되지 않았다.[9] 수용체 서브유닛의 N-단자 글리코실레이션은 서브유닛 조립체와 플라스마 멤브레인 밀거래에 매우 중요하다.[10]
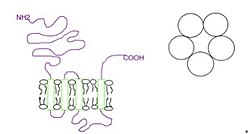
서브유닛은 의사대칭 방식으로 중앙 이온 채널을 둘러싸고 있다(그림.1). 각 하위 장치는 직교 리간드 바인딩 부위로 구성된 세포외 N-단자 영역, 4개의 상호연결된 알파 나선(M1-M4)로 구성된 투과형 영역, 게이트 메커니즘에 관여하는 세포외 M2-M3 루프, 수용체 밀거래와 규제에 관여하는 M3와 M4 사이의 큰 세포질 영역으로 구성된다.이온, 그리고 짧은 세포외 C-terminus (그림.1)[1] 세포외 영역은 작용제 및 경쟁적 길항제들의 작용장소인 반면, 투과영역은 중심 이온공극, 수용체 게이트, 이온이 세포막을 통과할 수 있는 원심 선택성 필터를 포함하고 있다.[2]
인간과 쥐의 유전자
인간 5-HT3 수용체를 부호화하는 유전자는 염색체 11(HTR3A, HTR3B)과 3(HTR3C, HTR3D, HTR3E)에 위치하기 때문에 유전자 중복으로 생긴 것으로 보인다. HTR3A와 HTR3B 유전자는 5-HT와3A 5-HT3B 서브유닛을 암호화하고 HTR3C, HTR3D, HTR3E는 5-HT3C, 5-HT3D3E 서브유닛을 암호화하고 있다. HTR3C와 HTR3E는 기능적인 동음이의어 채널을 형성하지 않는 것처럼 보이지만, HTR3A와 공동 표현하면 5-HT 효율이 감소하거나 증가하면서 이형성 복합체를 형성한다. 이러한 추가 하위 단위에 대한 병태생리학적 역할은 아직 확인되지 않았다.[11]
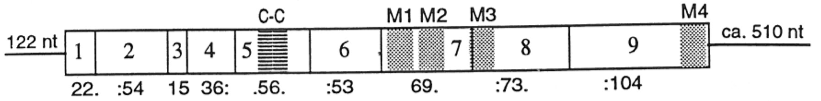
인간의 5-HT3A 수용체 유전자는 9 exon을 가지고 있고 13 kb에 걸쳐 퍼져 있는 마우스 유전자와 구조가 유사하다. 그것의 인트론 중 4개는 동질 α7-아세틸콜린 수용체 유전자의 인트론과 정확히 같은 위치에 있어 진화적 관계를 분명히 보여준다.[12][13]

표현. 5-HT3C, 5-HT3D, 5-HT3E 유전자는 주변적으로 제한된 발현 패턴을 보이는 경향이 있으며, 내장에서 높은 수치를 보인다. 예를 들어 인간의 십이지장과 위에서는 5-HT3C 및 5-HT3E mRNA가 5-HT3A 및 5-HT의3B 경우보다 클 수 있다.
다형성. 화학 요법 약물로 치료된 환자의 경우, HTR3B 유전자의 특정 다형성은 성공적인 항유전자 치료를 예측할 수 있다. 이는 5-HTR3B 수용체 서브유닛이 항임증 약물 효능의 바이오마커로 사용될 수 있음을 나타낼 수 있다.
조직 분포
5-HT3 수용체는 중추신경계와 말초신경계 전반에 걸쳐 발현되며 다양한 생리적 기능을 매개한다.[14] 세포 수준에서, 시냅스 후 5-HT3 수용체들은 랫드 신구체 내부 동맥류, 편도체, 해마, 페렛 시각피질에서 빠른 흥분 시냅스 전달을 중재하는 것으로 밝혀졌다.[15][16][17][18] 5-HT3 수용체들은 또한 사전 시냅스 신경 단자에도 존재한다. 신경전달물질 방출의 변조에 대한 약간의 증거가 있지만, 증거는 결론에 이르지 못한다.[19][20][21]
영향들
작용제에 의해 수용체가 활성화되어 이온 채널을 열면 다음과 같은 효과가 관찰된다.
- CNS: 뇌간에서 메스꺼움과 구토가 중심,[24][25] 불안,[22] 그리고 항경련제 및 친nociceptive 활동.
- PNS: 뉴런 배설(자율성, nociciceptive neuron), 에메시스[22]
고민자
수용체에 대한 작용제에는 다음이 포함된다.
- 세레울라이드
- 2-메틸-5-HT
- 알파메틸트립타민
- 부포테닌
- 클로로페닐비구아나이드[22]
- 에탄올
- 이보게인
- 페닐비구아나이드
- 퀴파진
- RS-56812: 잠재력3 및 선택적 5HT 부분작용제, 다른 세로토닌 수용체보다 1000배 선택성
- SR-57227
- 바레니클라인[26]
- YM-31636[27]
- S 21007[28](SAR C.f. CGS-12066A)
반목자
수용체에 대한 길항제(각각의 치료적 용도에 따라 선별)는 다음을 포함한다.
포지티브 알로스테릭 변조기
이러한 작용제는 수용체에서 작용하는 작용제가 아니라 작용제에 대한 수용체들의 친화력이나 유효성을 증가시킨다.
디스커버리
5-HT3 수용체 식별은 선택적 약리학적 도구가 결여되어 1986년까지 이루어지지 않았다.[14] 하지만,로 발견5-HT3 수용체를 중요한 역할에 chemotherapy-과 radiotherapy-induced 구토, 그리고 수반 개발의 선별적인5-HT3 수용체 길항제고픈 이러한 부작용을 불러일으켰다 강렬한 관심에서 제약 industry[2][33]고 따라서 식별의 5-HT3 수용체에서 '. 세포계s와 토종 조직들은 재빨리 따라왔다.[14]
참고 항목
참조
- ^ a b c d Barnes NM, Hales TG, Lummis SC, Peters JA (January 2009). "The 5-HT3 receptor--the relationship between structure and function". Neuropharmacology. 56 (1): 273–284. doi:10.1016/j.neuropharm.2008.08.003. PMC 6485434. PMID 18761359.
- ^ a b c d Thompson AJ, Lummis SC (2006). "5-HT3 Receptors". Current Pharmaceutical Design. 12 (28): 3615–3630. doi:10.2174/138161206778522029. PMC 2664614. PMID 17073663.
- ^ Reeves DC, Lummis SC (2002). "The molecular basis of the structure and function of the 5-HT3 receptor: a model ligand-gated ion channel (review)". Molecular Membrane Biology. 19 (1): 11–26. doi:10.1080/09687680110110048. PMID 11989819. S2CID 36985954.
- ^ Davies PA, Pistis M, Hanna MC, Peters JA, Lambert JJ, Hales TG, Kirkness EF (1999). "The 5-HT3B subunit is a major determinant of serotonin-receptor function". Nature. 397 (6717): 359–363. Bibcode:1999Natur.397..359D. doi:10.1038/16941. PMID 9950429. S2CID 4401851.
- ^ Dubin AE, Huvar R, D'Andrea MR, Pyati J, Zhu JY, Joy KC, Wilson SJ, Galindo JE, Glass CA, Luo L, Jackson MR, Lovenberg TW, Erlander MG (1999). "The pharmacological and functional characteristics of the serotonin 5-HT3A receptor are specifically modified by a 5-HT3B receptor subunit". J Biol Chem. 274 (43): 30799–30810. doi:10.1074/jbc.274.43.30799. PMID 10521471.
- ^ Monk SA, Desai K, Brady CA, Williams JM, Lin L, Princivalle A, Hope AG, Barnes NM (2001). "Generation of a selective 5-HT3B subunit-recognising polyclonal antibody; identification of immunoreactive cells in rat hippocampus". Neuropharmacology. 41 (8): 1013–1016. doi:10.1016/S0028-3908(01)00153-8. PMID 11747906. S2CID 10168401.
- ^ Boyd GW, Low P, Dunlop JI, Ward M, Vardy AW, Lambert JJ, Peters J, Conolly CN (2002). "Assembly and cell surface expression of homomeric and heteromeric 5-HT3 receptors: The role of oligomerisation and chaperone proteins". Mol Cell Neurosci. 21 (1): 38–50. doi:10.1006/mcne.2002.1160. PMID 12359150. S2CID 37832903.
- ^ Niesler B, Walstab J, Combrink S, Moeller D, Kapeller J, Rietdorf J, Boenisch H, Goethert M, Rappold G, Bruess M (2007). "Characterization of the Novel Human Serotonin Receptor Subunits 5-HT3C, 5- HT3D and 5-HT3E". Mol Pharmacol. 72 (Mar 28): 8–17. doi:10.1124/mol.106.032144. PMID 17392525. S2CID 40072549.
- ^ Niesler, Beate (February 2011). "5-HT3 receptors: potential of individual isoforms for personalised therapy". Current Opinion in Pharmacology. 11 (1): 81–86. doi:10.1016/j.coph.2011.01.011. PMID 21345729.
- ^ Quirk, Phillip L.; Rao, Suma; Roth, Bryan L.; Siegel, Ruth E. (2004-08-15). "Three putative N-glycosylation sites within the murine 5-HT3A receptor sequence affect plasma membrane targeting, ligand binding, and calcium influx in heterologous mammalian cells". Journal of Neuroscience Research. 77 (4): 498–506. doi:10.1002/jnr.20185. ISSN 0360-4012. PMID 15264219. S2CID 25811139.
- ^ Sanger GJ (September 2008). "5-hydroxytryptamine and the gastrointestinal tract: where next?". Trends in Pharmacological Sciences. 29 (9): 465–471. doi:10.1016/j.tips.2008.06.008. PMID 19086255.
- ^ a b c Uetz, P; Abdelatty, F; Villarroel, A; Rappold, G; Weiss, B; Koenen, M (1994). "Organisation of the murine 5-HT3 receptor gene and assignment to human chromosome 11". FEBS Letters. 339 (3): 302–306. doi:10.1016/0014-5793(94)80435-4. PMID 8112471. S2CID 28979681.
- ^ Uetz, P. (1992) Das 5HT3-Rezeptorgen der Maus. 하이델베르크 대학의 졸업장 논문, 143 페이지.
- ^ a b c Yakel, JL (2000). Endo, M; Kurachi, Y; Mishina, M (eds.). The 5-HT3 receptor channel: function, activation and regulation in Pharmacology of Ionic Channel Function: Activators and Inhibitors (Handbook of Experimental Pharmacology). Vol. 147. Berlin: Springer-Verlag. pp. 541–560. ISBN 3-540-66127-1.
- ^ Férézou I, Cauli B, Hill EL, Rossier J, Hamel E, Lambolez B (2002). "5-HT3 receptors mediate serotonergic fast synaptic excitation of neocortical vasoactive intestinal peptide/cholecystokinin interneurons". J Neurosci. 22 (17): 7389–7397. doi:10.1523/JNEUROSCI.22-17-07389.2002. PMC 6757992. PMID 12196560.
- ^ Kazuyoshi Kawa (1994). "Distribution and Functional Properties of 5HT3 Receptors in the Rat Hippocampus Dentate Gyrus". Journal of Neurophysiology. 71 (5): 1935–1947. doi:10.1152/jn.1994.71.5.1935. PMID 7520482.
- ^ Sugita S, Shen KZ, North RA (1992). "5-hydroxytryptamine is a fast excitatory transmitter at 5-HT3 receptors in rat amygdala". Neuron. 8 (1): 199–203. doi:10.1016/0896-6273(92)90121-S. PMID 1346089. S2CID 22554779.
- ^ Roerig B, Nelson DA, Katz LC (1992). "Fast synaptic signaling by nicotinic acetylcholine and serotonin 5-HT3 receptors in developing visual cortex". J Neurosci. 17 (21): 199–203. PMC 6573745. PMID 9334409.
- ^ Rondé P, Nichols RA (1998). "High calcium permeability of serotonin 5-HT3 receptors on presynaptic nerve terminals from rat striatum". J Neurochem. 70 (3): 1094–1103. doi:10.1046/j.1471-4159.1998.70031094.x. PMID 9489730.
- ^ Rondé P, Nichols RA (1997). "5-HT3 receptors induce rises in cytosolic and nuclear calcium in NG108-15 cells via calcium-induced calcium release". Cell Calcium. 22 (5): 357–365. doi:10.1016/S0143-4160(97)90020-8. PMID 9448942.
- ^ van Hooft JA, Vijverberg HP (2000). "5-HT3 receptors and neurotransmitter release in the CNS: a nerve ending story?". Trends Neurosci. 23 (12): 605–610. doi:10.1016/S0166-2236(00)01662-3. hdl:1874/7465. PMID 11137150. S2CID 36074796.
- ^ a b c d e Rang, H. P. (2003). Pharmacology. Edinburgh: Churchill Livingstone. ISBN 0-443-07145-4., 187페이지.
- ^ Gholipour T, Ghasemi M, Riazi K, Ghaffarpour M, Dehpour AR (January 2010). "Seizure susceptibility alteration through 5-HT(3) receptor: modulation by nitric oxide". Seizure. 19 (1): 17–22. doi:10.1016/j.seizure.2009.10.006. PMID 19942458.
- ^ Patel, Ryan; Dickenson, Anthony H. (September 2018). "Modality selective roles of pro-nociceptive spinal 5-HT2A and 5-HT3 receptors in normal and neuropathic states". Neuropharmacology. 143: 29–37. doi:10.1016/j.neuropharm.2018.09.028. ISSN 0028-3908. PMC 6277848. PMID 30240783.
- ^ Suzuki, Rie; Rahman, Wahida; Rygh, Lars J; Webber, Mark; Hunt, Stephen P; Dickenson, Anthony H (October 2005). "Spinal-supraspinal serotonergic circuits regulating neuropathic pain and its treatment with gabapentin". Pain. 117 (3): 292–303. doi:10.1016/j.pain.2005.06.015. ISSN 0304-3959. PMID 16150546. S2CID 6060490.
- ^ Mineur YS, Picciotto MR (December 2010). "Nicotine receptors and depression: revisiting and revising the cholinergic hypothesis". Trends Pharmacol. Sci. 31 (12): 580–586. doi:10.1016/j.tips.2010.09.004. PMC 2991594. PMID 20965579.
- ^ Imanishi, N.; Iwaoka, K.; Koshio, H.; Nagashima, S. Y.; Kazuta, K. I.; Ohta, M.; Sakamoto, S.; Ito, H.; Akuzawa, S.; Kiso, T.; Tsukamoto, S. I.; Mase, T. (2003). "New thiazole derivatives as potent and selective 5-hydroxytriptamine 3 (5-HT3) receptor agonists for the treatment of constipation". Bioorganic & Medicinal Chemistry. 11 (7): 1493–1502. doi:10.1016/S0968-0896(02)00557-6. PMID 12628674.
- ^ Delagrange, Philippe; Emerit, M.Boris; Merahi, Nacera; Abraham, Christine; Morain, Philippe; Rault, Sylvain; Renard, Pierre; Pfeiffer, Bruno; Guardiola-Lemaître, Béatrice; Hamon, Michel (1996). "Interaction of S 21007 with 5-HT3 receptors. In vitro and in vivo characterization". European Journal of Pharmacology. 316 (2–3): 195–203. doi:10.1016/S0014-2999(96)00680-2. ISSN 0014-2999. PMID 8982686.
- ^ Ashoor, A.; Nordman, J.; Veltri, D.; Susan Yang, K. -H.; Shuba, Y.; Al Kury, L.; Sadek, B.; Howarth, F. C.; Shehu, A.; Kabbani, N.; Oz, M. (2013). "Menthol Inhibits 5-Ht3 Receptor-Mediated Currents". Journal of Pharmacology and Experimental Therapeutics. 347 (2): 398–409. doi:10.1124/jpet.113.203976. PMID 23965380. S2CID 111928.
- ^ Newman, A. S.; Batis, N; Grafton, G; Caputo, F; Brady, C. A.; Lambert, J. J.; Peters, J. A.; Gordon, J; Brain, K. L.; Powell, A. D.; Barnes, N. M. (2013). "5-Chloroindole: A potent allosteric modulator of the 5-HT3 receptor". British Journal of Pharmacology. 169 (6): 1228–1238. doi:10.1111/bph.12213. PMC 3831704. PMID 23594147.
- ^ Davies, Paul A (2011). "Allosteric modulation of the 5-HT3 receptor". Current Opinion in Pharmacology. Elsevier BV. 11 (1): 75–80. doi:10.1016/j.coph.2011.01.010. ISSN 1471-4892. PMC 3072441.
- ^ a b c Solt, Ken; Stevens, Renna J.; Davies, Paul A.; Raines, Douglas E. (2005-08-04). "General Anesthetic-Induced Channel Gating Enhancement of 5-Hydroxytryptamine Type 3 Receptors Depends on Receptor Subunit Composition". Journal of Pharmacology and Experimental Therapeutics. American Society for Pharmacology & Experimental Therapeutics (ASPET). 315 (2): 771–776. doi:10.1124/jpet.105.090621. ISSN 0022-3565.
- ^ Thompson AJ, Lummis SC (2007). "The 5-HT3 receptor as a therapeutic target". Expert Opin Ther Targets. 11 (4): 527–540. doi:10.1517/14728222.11.4.527. PMC 1994432. PMID 17373882.