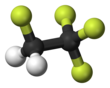
1,1,1,2-테트라플루오로에탄
1,1,1,2-Tetrafluoroethane
| | |||
| 이름 | |||
|---|---|---|---|
| 선호 IUPAC 이름 1,1,1,2-테트라플루오로에탄 | |||
| 기타 이름 프레온 134a 디멜 134a 포레인 134a 지네트로134a HFA-134a HFC-134a R-134a 수바 134a 노르플루레인 | |||
| 식별자 | |||
3D 모델(JSmol) | |||
| 켐벨 | |||
| 켐스파이더 | |||
| 드러그뱅크 | |||
| ECHA InfoCard | 100.011.252 | ||
| EC 번호 |
| ||
| 케그 | |||
펍켐 CID | |||
| RTECS 번호 |
| ||
| 유니 | |||
| UN 번호 | 3159 | ||
CompTox 대시보드 (EPA) | |||
| |||
| |||
| 특성. | |||
| CF3CH2F[1] | |||
| 어금질량 | 102.03 g/192 | ||
| 외관 | 무색가스 | ||
| 밀도 | 0.00425 g/cm3, 가스 | ||
| 녹는점 | -103.3°C(-153.9°F, 169.8K) | ||
| 비등점 | -26.3°C(-15.3°F, 246.8K) | ||
| 0.15wt% | |||
| 위험 | |||
| 주요 위험 | 질식성 물질 | ||
| 안전자료표 | 참고 항목: 데이터 페이지 | ||
| GHS 픽토그램 |  | ||
| GHS 시그널 워드 | 경고 | ||
| H280 | |||
| P410+403 | |||
| NFPA 704(화재 다이아몬드) | |||
| 플래시 포인트 | 250°C(482°F, 523K) | ||
| 관련 화합물 | |||
| 디플루오로메탄 펜타플루오로에탄 | |||
관련 화합물 | 2-클로로- 1,1,1,2-광화불화탄 1,1,1-트리클로로에탄 | ||
| 부가자료페이지 | |||
| 굴절률(n), 유전 상수(상수r) 등 | |||
열역학 자료 | 위상 거동 고체-기체-가스 | ||
| UV, IR, NMR, MS | |||
달리 명시된 경우를 제외하고, 표준 상태(25°C [77°F], 100 kPa)의 재료에 대한 데이터가 제공된다. | |||
| Infobox 참조 자료 | |||
1,1,1,2-Tetrafluoroethane (also known as norflurane (INN), R-134a, Freon 134a, Forane 134a, Genetron 134a, Green Gas, Florasol 134a, Suva 134a, or HFC-134a) is a hydrofluorocarbon (HFC) and haloalkane refrigerant with thermodynamic properties similar to R-12 (dichlorodifluoromethane) but with insignificant ozone depletion potential and a lower 100-연도별 지구온난화 잠재력(1,430, R-12의 GWP 10,900 대비)[2] CFCHF32 공식과 대기압에서 비등점은 -26.3°C(-15.34°F)이다. R-134a 실린더는 연한 파란색이다.[3] CO와2 유사한 GWP를 가진 HFO-1234yf 및 기타 냉매로의 단계적 폐기와 전환은 2012년 자동차 시장에서 시작되었다.[4]
사용하다
1,1,1,2-테트라플루오로에탄은 가정용 냉장 및 자동차 에어컨의 '고온' 냉매로 주로 사용되는 불연성 가스다. 이 장치들은 더 환경적으로 해로운 R-12를 대체하기 위해 1990년대 초에 1,1,1,2-테트라플루오로에탄을 사용하기 시작했다. 레트로핏 키트는 원래 R-12가 장착된 유닛을 변환할 수 있다.
다른 일반적인 용도로는 플라스틱 거품 불기, 세척 용제, 의약품 전달을 위한 추진제(예: 기관지염기), 와인 코르크 제거제, 가스 걸레("캔된 공기"), 압축 공기의 습기를 제거하기 위한 에어 드라이어 등이 있다. 1,1,1,1,2-테트라플루오로에탄은 일부 과부하 시도에서 컴퓨터를 식히는 데도 사용되었다.그것은 배관 파이프 동결 키트에 사용되는 냉매다. 에어소프트 공기총의 추진체로도 흔히 쓰인다. 이 가스는 실리콘 기반의 윤활유와 섞이는 경우가 많다.
희망 및 틈새 애플리케이션
1,1,1,2-테트라플루오로에탄은 다른 유기용매와 초임계 이산화탄소에 대한 가능한 대안으로 향미 및 향기 화합물 추출에 적합한 유기용매로도 검토되고 있다.[5][6] 또한 액체와 초임계액 모두 유기화학에서 용매로 사용할 수 있다.[7] 이 검출기는 Large Hadron Collider의 저항성 판실 입자 검출기에 사용된다.[8][9] 또한 일부 극저온 입자 검출기와 같은 다른 유형의 입자 검출기에도 사용된다.[10] 그것은 보호 가스로서 마그네슘 제련에서 육불화 황의 대안으로 사용될 수 있다.[11]
1,1,1,2-테트라플루오로에탄도 유전가스로서 육불화 황의 대안으로 검토되고 있다.[12] 호를 취입하는 성질은 열악하지만 유전적 성질은 상당히 양호하다.
역사 및 환경 영향
1,1,1,2-테트라플루오로에탄은 1990년대 초반 오존층 배출 특성이 큰 디클로로디플루오로메탄(R-12)의 대체품으로 도입됐다.[13] 오존층 파괴전위(오존층)가 미미하고 산성화전위(산비)가 미미하지만 지구온난화전위(GWP)는 100년, 대기수명은 대략 14년이다.[2] 대기 중 집중력과 복사력에 대한 기여도가 도입 이후 계속 높아지고 있다. 따라서 그것은 온실가스 IPCC 목록에 포함되었다.[14]
결과적으로 R-134a는 GWP가 100 이상인 에어컨 시스템의 가스를 금지하는 2006년의 지침에 의해 2011년 자동차를 시작으로 유럽연합에서 사용이 금지되었다. [15]
1,1,1,2-테트라플루오로에탄은 미국 및 다른 국가에서도 사용 제한을 받는다. 자동차공학회(SAE)는 자동차 에어컨 시스템에 새로운 불화학적 냉매 HFO-1234yf(CFCF3=CH2)로 대체하는 것이 가장 좋다고 제안했다.[16] 2021년 모델에 따라 미국에서 새로 제작된 경차들은 더 이상 R-134a를 사용하지 않을 것이다.[4]
캘리포니아는 또한 전문적이지 않은 에어컨 재충전을 피하기 위해 개인에게 R-134a 통조림을 판매하는 것을 금지할 수도 있다.[17] 1994년 10월부터 위스콘신 주에서는 ATCP 136에 따라 1,1,2-테트라플루오로에탄 15파운드 이하의 컨테이너 크기의 판매를 금지하고 있었으나, 이 제한은 이 화학물질이 냉매로 의도되었을 때만 적용되었다. 그러나 2012년 위스콘신에서 금지령이 해제됐다.[18] 그것이 활동했던 기간 동안, 위스콘신 특유의 금지는 허점을 포함하고 있었다. 예를 들어, 화학물질이 제7671a조 제1종 및 제2종 물질 목록에 포함되어 있지 않거나 냉매가 아닌 HFC-134a가 포함되어 있지 않기 때문에 화학물질이 어느 정도의 양으로도 가스 걸레 용기를 구매하는 것은 합법적이었다.[19]
생산 및 반응
테트라플루오로에탄은 일반적으로 트리클로로에틸렌과 불소화수소를 반응시켜 만들어진다.[20]
- CHCl=CCl2 + 4HF → CFCHF32 + 3HCl
그것은 부틸리튬과 반응하여 트리플루오로비닐 리튬을 준다.[21]
- CFCHF32 + 2 BuLi → CF2=CFLi + LiF + 2 Buh
안전
기체 1,1,1,2-테트라플루오로에탄의 공기와 혼합물은 대기압 및 최대 100 °C(212 °F)의 온도에서 인화성이 없다. 그러나 높은 압력 및/또는 온도에서 고농도의 공기를 혼합한 혼합물은 점화될 수 있다.[22] 1,1,1,2-tetrafluoroethane의 250°C(482°F)이상의 화염이나 뜨거운 표면과 접촉을 해 성서 분해 온도 위의 370°C,.[24]1,1,1,2-Tetrafluoroethane 자체가 있는 50%치사량 1,500g/m3에 보고되었던, 플루오르화 수소와 금속 카르보닐 fluoride,[23]을 포함한 증기 분해와 유독성 가스의 방출을 일으킬 수 있다.쥐, mak흡입제 남용에 내재된 위험과는 별도로 비교적 비흡수적이다. 그것의 기체 형태는 공기보다 밀도가 높으며 폐의 공기를 대신할 것이다. 이것은 과도하게 흡입하면 질식사 결과를 초래할 수 있다.[25][26] 이것은 흡입제 남용에 의한 대부분의 사망에 기여한다.
1,1,1,2-테트라플루오로에탄(tetrafluoroethane)을 함유한 에어로졸 캔은 뒤집으면 효과적인 동결 스프레이가 된다. 압력을 받으면 1,1,1,2-테트라플루오로에탄은 액체로 압축되며, 기화 시 상당한 양의 열 에너지를 흡수한다. 결과적으로, 그것은 그것이 증발할 때 접촉하는 물체의 온도를 크게 낮출 것이다.
의료용
의학적 용도를 위해 1,1,1,2-테트라플루오로에탄에는 노플루란이라는 총칭이 있다. 그것은 일부 계량된 흡입기의 추진제로 사용된다.[27] 이것은 이 용도에 안전한 것으로 여겨진다.[28][29][30] 펜타플루오로프로판과 결합하여 국소증기멸균 스프레이로 사용되어 완치 전 끓는 소리를 낸다.[31][32] 잠재적인 흡입 마취제로도 연구되어 왔지만,[33] 흡입기에 사용되는 용량에서는 비흡수적이다.[28]
참고 항목
참조
- ^ ODS 대체의 지구 온난화 가능성 오존층 보호 미국 EPA. Epa.gov (2006년 6월 28일) 2011년 8월 21일 회수
- ^ a b "Table 2.14 (Errata). Lifetimes, radiative efficiencies and direct (except for CH4) GWPs relative to CO2". Archived from the original on 6 July 2017. Retrieved 11 July 2017.
- ^ "Example image of a 30 lbs R134a bottle". budgetheating.com. Retrieved 26 March 2018.
- ^ a b "Refrigerant Transition & Environmental Impacts". U.S. Environmental Protection Agency. 6 August 2015. Retrieved 1 October 2020.
- ^ Corr, Stuart (2005). "1,1,1,2-Tetrafluoroethane (R-134a): A Selective Solvent for the Generation of Flavor and Fragrance Ingredients". Natural Flavors and Fragrances. ACS Symposium Series. 908. p. 41. doi:10.1021/bk-2005-0908.ch003. ISBN 0-8412-3904-5.
- ^ Abbott, Andrew P.; Eltringham, Wayne; Hope, Eric G.; Nicola, Mazin (2005). "Solubility of unsaturated carboxylic acids in supercritical 1,1,1,2-tetrafluoroethane (HFC 134a) and a methodology for the separation of ternary mixtures". Green Chemistry. 7 (4): 210. doi:10.1039/B412697A.
- ^ Abbott, Andrew P.; Eltringham, Wayne; Hope, Eric G.; Nicola, Mazin (2005). "Hydrogenation in supercritical 1,1,1,2 tetrafluoroethane (HFC 134a)" (PDF). Green Chemistry. 7 (10): 721. doi:10.1039/B507554H. hdl:2381/604. Archived from the original (PDF) on 19 July 2018. Retrieved 18 September 2019.
- ^ Anushree Ghosh 연구 - 유리 저항 플레이트 챔버(RPC) 및 웨이백 기계에 2011년 8월 7일 보관된 효율 계산 INO 대학원 교육 프로그램 DHEP, TIFR, 뭄바이.
- ^ 케이판스, I. 글루시코프, R. 귀다, F. Han, S. Haider(스위스 CERN) RPC 운영은 최적화된 폐쇄 루프 가스 시스템에서 LHC 실험에서 이루어진다. 메디컬 이미지 컨퍼런스. 2009년 10월 25일-31일.
- ^ Norbeck, E.; Olson, J. E.; Moeller, A.; Onel, Y. (2006). "Rad Hard Active Media For Calorimeters" (PDF). AIP Conference Proceedings. 867: 84. Bibcode:2006AIPC..867...84N. doi:10.1063/1.2396941. Archived from the original (PDF) on 23 March 2012.
- ^ 1998년 미국의 마그네슘 재활용. (PDF) USGS, 2011년 8월 21일 회수
- ^ 지구 온난화 가능성이 낮은 기체 유전체 – 미국 특허 애플리케이션 20080135817 Description 2012년 10월 13일 웨이백 머신에 보관. 아마존닷컴(2006년 12월 12일). 2011년 8월 21일 회수
- ^ Franklin J (1993). "The Atmospheric Degradation and Impact of 1,1,1,2-Tetrafluorethane (Hydrofluorocarbon 134a)". Chemosphere. 27 (8): 1565–1601. Bibcode:1993Chmsp..27.1565F. doi:10.1016/0045-6535(93)90251-Y.
- ^ Forster, P.; et al. (2007). "Changes in Atmospheric Constituents and in Radiative Forcing." (PDF). Climate Change 2007: The Physical Science Basis. Contribution of Working Group I to the Fourth Assessment Report of the Intergovernmental Panel on Climate Change. Archived (PDF) from the original on 24 July 2010.
- ^ "DIRECTIVE 2006/40/EC relating to emissions from air-conditioning systems in motor vehicles and amending Council Directive 70/156/EEC". eur-lex.europa.eu. 17 May 2006. Retrieved 29 May 2021.
- ^ HFO-1234yf MAC용 낮은 GWP 냉매 2009년 2월 27일 웨이백 머신에 보관. 아마존닷컴(2011년 8월 17일). 2011년 8월 21일 회수
- ^ 캘리포니아는 HFC-134a의 자동차 사용을 제한한다. 2007년 6월 27일. R744.com. 2011년 8월 21일 회수
- ^ a b ATCP 136. 모바일 에어컨, 냉매 회수 또는 재활용. State.wi.us. (PDF) 2011년 8월 21일 회수
- ^ 1등급 오존 퇴화 물질. EPA.gov. 2011년 8월 21일 회수
- ^ "Solvay in North America Solvay" (PDF).
- ^ Burdon, James; Coe, Paul L.; Haslock, Iain B.; Powell, Richard L. (1996). "The hydrofluorocarbon 1,1,1,2-tetrafluoroethane (HFC-134a) as a ready source of trifluorovinyllithium". Chemical Communications: 49. doi:10.1039/CC9960000049.
- ^ DuPont (2004). DuPont HFC-134a— Properties, Uses, Storage, and Handling (PDF) (Report). Archived from the original (PDF) on 4 October 2016. Retrieved 5 August 2016.
- ^ Honeywell International (December 2005). "MSDS # GTRN-0047 For Genetron 134aUV".
- ^ "SAFETY DATA SHEET according to Regulation (EU) 2015/8301/7 Harp® 134a" (PDF).
- ^ Alexander D. J.; Libretto S. E. (1995). "An overview of the toxicology of HFA-134a (1,1,1,2-tetrafluoroethane)". Hum. Exp. Toxicol. 14 (9): 715–20. doi:10.1177/096032719501400903. PMID 8579881. S2CID 19669317.
- ^ G. E. Millward; E. Tschuikow-Roux (1972). "Kinetic analysis of the shock wave decomposition of 1,1,1,2-tetrafluoroethane". The Journal of Physical Chemistry. 76 (3): 292–298. doi:10.1021/j100647a002.
- ^ Sellers, William F. S. (2017). "Asthma pressurised metered dose inhaler performance: Propellant effect studies in delivery systems". Allergy, Asthma & Clinical Immunology. 13: 30. doi:10.1186/s13223-017-0202-0. PMC 5492461. PMID 28670327.
- ^ a b Shah, S. B; Hariharan, U; Bhargava, A. K (2015). "Anaesthetic in the garb of a propellant". Indian Journal of Anaesthesia. 59 (4): 258–260. doi:10.4103/0019-5049.155011. PMC 4408662. PMID 25937660.
This propellant has been shown to be safe and nonanaesthetic in standard inhaler doses
- ^ Huchon, G; Hofbauer, P; Cannizzaro, G; Iacono, P; Wald, F (2000). "Comparison of the safety of drug delivery via HFA- and CFC-metered dose inhalers in CAO". The European Respiratory Journal. 15 (4): 663–9. doi:10.1034/j.1399-3003.2000.15d07.x. PMID 10780756.
- ^ "1,1,1,2-Tetrafluoroethane". Occupational Safety & Health Administration.
- ^ "Norflurane". DrugBank.
- ^ "Norflurane-Pentafluoropropane Aerosol, Spray". WebMD.
- ^ Shulman M, Sadove MS (1967). "1,1,1,2-tetrafluoroethane: an inhalational agent of intermediate potency". Anesthesia and Analgesia. 46 (5): 629–635. doi:10.1213/00000539-196709000-00029. S2CID 5868484.
외부 링크
| 위키미디어 커먼즈에는 테트라플루오로에탄과 관련된 미디어가 있다. |
- 국제 화학 안전 카드 1281
- 유럽불화탄소 기술위원회(EFCTC)
- 옥스퍼드 대학교 MSDS
- 간결한 국제 화학 평가 문서 11(inchem.org
- 압력 온도 계산기
- "The Coexisting Curve of the Refrigerant HFC 134a: Some Scaling Models" (PDF). Archived from the original (PDF) on 29 September 2006. Retrieved 11 September 2007.
- R134a 2상 컴퓨터 냉각