사이클린 의존키나제2
Cyclin-dependent kinase 2세포분열단백질키나아제2 또는 Cdk2라고도 알려진 사이클린 의존성 키나제2는 인간에서 CDK2 유전자에 의해 암호화된 효소다.[5][6]이 유전자에 의해 인코딩된 단백질은 Ser/Thr 단백질 키나제스의 사이클린 의존성 키나제 계열의 일원이다.이 단백질 키나제는 S. 세레비시아에 cdc28, 인간에게 cdk1로도 알려진 S. 퐁베 cdc2의 유전자 생성물과 매우 유사하다.세포가 유사분열에 필요한 단백질을 만들어 DNA를 복제하는 세포주기의 G1-S상(G1-S상)으로 활동이 제한되는 사이클린 의존성 키나아제 복합체의 촉매 서브단위다.이 단백질은 사이클린 E 또는 A를 포함한 단지의 규제 하위 단위에 의해 관련되고 규제된다.Cyclin E는 G1상 Cdk2를 바인딩하는데, Cyclin A와 바인딩하면 S상까지 진행해야 하는 반면 G1에서 S상으로의 전환에 필요하다.[7]그것의 활동도 인산화 작용에 의해 조절된다.이 유전자의 다중 대안으로 분할된 변종과 다중 전사 개시 부지가 보고되었다.[8]최근 G1-S 전환에서 이 단백질의 역할은 Cdk2가 부족한 세포가 이 전환 과정에서 아무런 문제가 없는 것으로 보고되면서 의문시되고 있다.[9]
정상적으로 작동하는 조직에서의 디스펜서빌리티
원래의 세포 배양 기반 실험은 Cdk2의 삭제에 따른 G1-S 전환에서 세포 주기 구속을 입증했다.[10]이후 실험에서 Cdk2 삭제를 통해 생쥐 배아 섬유질에서 세포 주기의1 G 단계가 길어진 것으로 나타났다.그러나 그들은 이 기간이 지난 후에도 여전히 S 단계로 진입하여 세포 주기의 나머지 단계를 완료할 수 있었다.[11]생쥐에서 Cdk2가 삭제되었을 때, 이 동물들은 몸집이 줄었음에도 불구하고 생존할 수 있었다.그러나 수컷 쥐와 암컷 쥐 모두의 감수성 기능은 억제되었다.이것은 Cdk2가 건강한 세포의 세포주기에 필수적이지는 않지만 감수분열과 생식에 필수적이라는 것을 암시한다.[10]Cdk2 녹아웃 생쥐의 세포는 더 적은 분열을 겪으며 신체 크기 감소에 기여한다.또한 생식세포는 감수분열의 프로 페이즈에서 분열을 멈추어 생식 불임으로 이어진다.[11]현재 cdk1은 감수기능을 제외한 cdk2 삭제의 많은 측면을 보상하는 것으로 알려져 있다.[10]
활성화 메커니즘
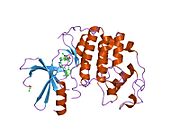
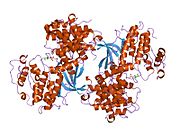
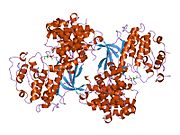
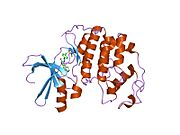
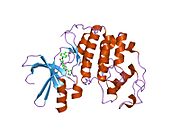
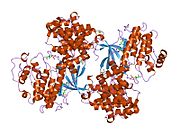
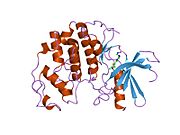
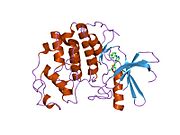
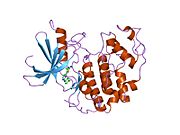
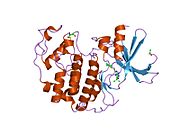
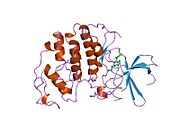
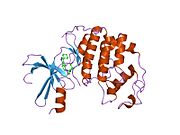
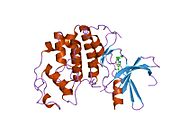
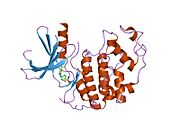
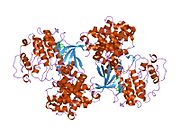
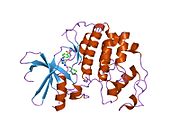
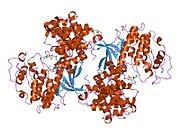
사이클린 의존성 키나아제 2는 두 개의 로브로 구성된다.N-terminus(N-lobe)에서 시작하는 로브에는 베타 시트가 많이 들어 있고, C-terminus 로브(C-lobe)에는 알파 헬리케스가 풍부하다.[7]Cdk2는 사이클린 A, B, E, 그리고 아마도 C를 포함한 많은 다른 사이클린들과 결합할 수 있다.[10]최근 연구에 따르면 Cdk2는 사이클린 A와 E에 우선적으로 결합하는 반면, Cdk1은 사이클린 A와 B를 선호한다.[12]
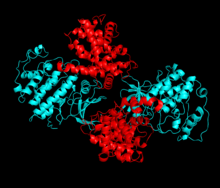
Cdk2는 키나아제의 N 로브와 C 로브 사이에 위치한 활성 부위에서 사이클린 단백질(A 또는 E)이 결합할 때 활성화된다.활성 사이트의 위치 때문에 파트너 사이클린은 Cdk2의 양쪽 로브와 상호 작용한다.Cdk2에는 키나아제의 C엽에 위치한 중요한 알파 나선형(C-헬릭스 또는 PSTARE-헬릭스)이 포함되어 있다.소수성 상호작용은 C-헬릭스가 활성 사이클린의 다른 나선과 연관되도록 한다.활성화는 나선이 회전하고 N-로브에 더 가깝게 이동하는 순응적 변화를 유도한다.[citation needed]이를 통해 C-헬릭스에 위치한 글루타민산이 가까운 리신 사이드 체인과 이온쌍을 형성할 수 있다.이 운동의 의의는 모든 진핵 키나아제에 보존되어 있는 촉매 현장 잔류물 3매드에 속하는 Glu 51의 측면 사슬을 촉매 현장으로 들여온다는 것이다.이 삼합체(Lys 33, Glu 51, Asp 145)는 ATP 인산염 방향과 마그네슘 조정에 관여하며, 촉매에 매우 중요한 것으로 생각된다.이러한 순응적 변화는 또한 활성화 루프를 C-러브에 다시 배치하여 현재 새로운 상호작용이 가능한 ATP 바인딩 사이트를 드러낸다.마지막으로, C-러브 활성화 세그먼트가 촉매 부위에서 이탈되고 트레오닌 잔여물이 더 이상 장력적으로 방해받지 않게 되면서 트레오닌-160 잔류물이 노출되고 인산염화된다.인산염화된 threonine 잔여물은 최종 효소 순응에서 안정성을 만들어낸다.이 활성화 프로세스 전체에 걸쳐 Cdk2에 바인딩된 사이클린은 어떠한 순응적 변화를 겪지 않는다는 점에 유의해야 한다.[14][7]

DNA 복제의 역할
세포분할 과정의 성공은 세포와 조직 수준에서 공정의 정확한 규제에 달려 있다.세포 내의 단백질과 DNA 사이의 복잡한 상호작용은 유전체 DNA가 딸 세포로 전달되도록 한다.세포와 세포외 매트릭스 단백질 사이의 상호작용은 새로운 세포가 기존 조직에 통합될 수 있도록 한다.세포 수준에서 이 과정은 다른 수준의 사이클린 의존적 키네즈(Cdks)와 그들의 파트너 사이클린에 의해 제어된다.셀은 결함을 고칠 수 있을 때까지 셀 주기 진행을 지연시키는 수단으로 다양한 체크포인트를 활용한다.[16]
Cdk2는 셀 사이클의 G1, S상 동안 활성화되어 있어 G-S상1 체크포인트 제어의 역할을 한다.G상1 이전에 Cyclin D와 함께 Cdk4와 Cdk6의 레벨이 증가한다.이를 통해 Rb의 부분 인산화, G상1 초기 E2F의 부분 활성화가 가능해져 사이클린 E 합성과 Cdk2 활성화가 촉진된다.G1 단계가 끝나면 Cdk2/Cyclin E 콤플렉스는 최대 활동에 도달하며 S 페이즈 개시 시 중요한 역할을 한다.[17]다른 비 Cdk 단백질도 G-S1 위상 전이 중에 활성화된다.예를 들어 레티노블레스토마(Rb)와 p27 단백질은 Cdk2 – 사이클린 A/E 콤플렉스에 의해 인산염화되어 완전히 비활성화된다.[18]이를 통해 E2F 전사 인자가 분열 전 DNA가 복제되는 S상 진입을 촉진하는 유전자를 표현할 수 있다.[19][20][18]또한, Cdk2-Cyclin E 콤플렉스의 알려진 기질인 NPAT는 인산화 시 히스톤 유전자 전사를 활성화하는 기능을 한다.[21]이것은 히스톤 단백질(크로마틴의 주요 단백질 성분)의 합성을 증가시키고, 이후 세포 주기의 DNA 복제 단계를 지원한다.마지막으로 S상 끝에서 유비퀴틴 프로테아솜은 사이클린 E를 분해한다.[11]
암세포증식
Cdk2는 정상적으로 기능하는 세포의 세포주기에 대부분 불필요한 것이지만, 암세포의 비정상적인 성장 과정에 매우 중요하다.CCNE1 유전자는 Cdk2의 양대 단백질 결합 파트너 중 하나인 사이클린 E를 생산한다.CCNE1의 과도한 압박은 많은 종양 세포에서 일어나 세포가 Cdk2와 사이클린 E에 의존하게 한다.[12]비정상적인 사이클린 E 활동은 백혈병, 림프종뿐만 아니라 유방, 폐, 대장암, 위암, 골암에서도 관찰된다.[17]마찬가지로 사이클린 A2의 비정상적인 발현도 염색체 불안정 및 종양 증식과 관련이 있는 반면 억제하면 종양의 성장 감소로 이어진다.[22]따라서 CDK2와 그 사이클린 결합 파트너는 새로운 암 치료법의 가능한 치료 목표를 나타낸다.[12]임상 전 모델은 종양 성장 제한에 사전 성공했으며, 기존 항암치료제의 부작용을 줄이는 효과도 관찰됐다.[23][24][25]
선택적 Cdk2 억제제를 식별하는 것은 Cdk2의 활성 사이트와 다른 Cdk들, 특히 Cdk1 간의 극단적인 유사성 때문에 어렵다.[12]Cdk1은 세포 주기에서 유일하게 필수 사이클린 의존성 키나아제로, 억제가 의도치 않은 부작용을 초래할 수 있다.[26]대부분의 CDK2 억제제 후보는 ATP 바인딩 사이트를 대상으로 하며, 두 가지 주요 하위 클래스, 즉 타입 I과 타입 II로 나눌 수 있다.제1형 억제제는 ATP 바인딩 사이트를 활성 상태로 경쟁적으로 겨냥한다.타입 II 억제제는 ATP 결합 사이트를 점유하거나 키나제 내의 소수성 포켓을 점유하여 결합되지 않은 상태에서 대상 CDK2를 억제한다.제2형 억제제는 보다 선택적인 것으로 여겨진다.[24]최근, 새로운 CDK 결정 구조물의 가용성은 C-헬릭스 근처의 잠재적 골격 결합 부지를 식별하게 했다.이 모든 부위의 억제제는 타입 III 억제제로 분류된다.[27]또 다른 가능한 대상은 CDK2의 T-루프다.사이클린 A가 CDK2에 바인딩되면 N단자엽이 회전하여 ATP 바인딩 사이트를 활성화하고 T-루프라고 하는 활성화 루프의 위치를 전환한다.[28]
억제제
동적 시뮬레이션과 결합 자유 에너지 연구의 해석에 따르면 리간드2(사내 합성 피롤론 퓨즈 벤조세베렌(PBS) 화합물 17개 중)는 플라보피리돌, SU9516, CVT-313 억제제에 안정적이고 동등한 자유 에너지를 가지고 있다고 밝혔다.리간드2는 리간드 효율성과 바인딩 친화력을 바탕으로 오프타깃 바인딩(CDK1과 CDK9)이 없는 CDK2의 선택적 억제제로서 면밀하게 검토했다.[29]
알려진 CDK 억제제는 p21Cip1(CDKN1A)과 p27Kip1(CDKN1B)이다.[30]
GW8510과 실험용 암 치료제 셀리시립과 같이 Cdk2를 억제하고 세포 주기를 구속하는 약물은 많은 세포 주기 활성 항균제에 대한 상피의 민감도를 감소시킬 수 있으므로 화학요법에 의한 탈모증 예방 전략을 나타낸다.[31]
로즈마린산 메틸에스테르는 식물에서 유래한 Cdk2 억제제로, 혈관 매끄러운 근육세포의 증식을 억제하고 생쥐의 재생 모델에서 네오티마 형성을 감소시키는 것으로 나타났다.[32]
많은 억제제(Purvalanol B 포함)와의 상호작용을 보여주는 아래의 PDB 갤러리를 참조하십시오.
유전자 조절
멜라노사이트 세포 유형에서 CDK2 유전자의 발현은 Michalmia 관련 전사 인자에 의해 조절된다.[33][34]
상호작용
Cyclin 의존성 키나제 2는 다음과 상호작용하는 것으로 나타났다.

참조
- ^ a b c GRCh38: 앙상블 릴리스 89: ENSG00000123374 - 앙상블, 2017년 5월
- ^ a b c GRCm38: 앙상블 릴리스 89: ENSMUSG000025358 - 앙상블, 2017년 5월
- ^ "Human PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ "Mouse PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ Tsai LH, Harlow E, Meyerson M (September 1991). "Isolation of the human cdk2 gene that encodes the cyclin A- and adenovirus E1A-associated p33 kinase". Nature. 353 (6340): 174–7. Bibcode:1991Natur.353..174T. doi:10.1038/353174a0. PMID 1653904. S2CID 4358953.
- ^ "Entrez Gene: CDK2 cyclin-dependent kinase 2".
- ^ a b c Echalier A, Endicott JA, Noble ME (March 2010). "Recent developments in cyclin-dependent kinase biochemical and structural studies". Biochimica et Biophysica Acta (BBA) - Proteins and Proteomics. 1804 (3): 511–9. doi:10.1016/j.bbapap.2009.10.002. PMID 19822225.
- ^ "Entrez Gene: CDK2 cyclin-dependent kinase 2".
- ^ Berthet C, Aleem E, Coppola V, Tessarollo L, Kaldis P (October 2003). "Cdk2 knockout mice are viable". Current Biology. 13 (20): 1775–85. doi:10.1016/j.cub.2003.09.024. PMID 14561402. S2CID 14320937.
- ^ a b c d Satyanarayana A, Kaldis P (August 2009). "Mammalian cell-cycle regulation: several Cdks, numerous cyclins and diverse compensatory mechanisms". Oncogene. 28 (33): 2925–39. doi:10.1038/onc.2009.170. PMID 19561645.
- ^ a b c Su TT, Stumpff J (March 2004). "Promiscuity rules? The dispensability of cyclin E and Cdk2". Science's STKE. 2004 (224): pe11. doi:10.1126/stke.2242004pe11. PMC 3242733. PMID 15026579.
- ^ a b c d Wood DJ, Korolchuk S, Tatum NJ, Wang LZ, Endicott JA, Noble ME, Martin MP (November 2018). "Differences in the Conformational Energy Landscape of CDK1 and CDK2 Suggest a Mechanism for Achieving Selective CDK Inhibition". Cell Chemical Biology. 26 (1): 121–130.e5. doi:10.1016/j.chembiol.2018.10.015. PMC 6344228. PMID 30472117.
- ^ PDB: 1FIN; Jeffrey PD, Russo AA, Polyak K, Gibbs E, Hurwitz J, Massagué J, Pavletich NP (July 1995). "Mechanism of CDK activation revealed by the structure of a cyclinA-CDK2 complex". Nature. 376 (6538): 313–20. Bibcode:1995Natur.376..313J. doi:10.1038/376313a0. PMID 7630397. S2CID 4361179.
- ^ Malumbres M (2014-06-30). "Cyclin-dependent kinases". Genome Biology. 15 (6): 122. doi:10.1186/gb4184. PMC 4097832. PMID 25180339.
- ^ PDB: 1W98; Honda R, Lowe ED, Dubinina E, Skamnaki V, Cook A, Brown NR, Johnson LN (February 2005). "The structure of cyclin E1/CDK2: implications for CDK2 activation and CDK2-independent roles". The EMBO Journal. 24 (3): 452–63. doi:10.1038/sj.emboj.7600554. PMC 548659. PMID 15660127.
- ^ Bartek J, Lukas C, Lukas J (October 2004). "Checking on DNA damage in S phase". Nature Reviews. Molecular Cell Biology. 5 (10): 792–804. doi:10.1038/nrm1493. PMID 15459660. S2CID 33560392.
- ^ a b Caruso JA, Duong MT, Carey JP, Hunt KK, Keyomarsi K (October 2018). "Low-Molecular-Weight Cyclin E in Human Cancer: Cellular Consequences and Opportunities for Targeted Therapies". Cancer Research. 78 (19): 5481–5491. doi:10.1158/0008-5472.can-18-1235. PMC 6168358. PMID 30194068.
- ^ a b Giacinti C, Giordano A (August 2006). "RB and cell cycle progression". Oncogene. 25 (38): 5220–7. doi:10.1038/sj.onc.1209615. PMID 16936740.
- ^ Cobrinik D (April 2005). "Pocket proteins and cell cycle control". Oncogene. 24 (17): 2796–809. doi:10.1038/sj.onc.1208619. PMID 15838516.
- ^ The molecular basis of cancer. Mendelsohn, John, 1936-, Gray, Joe W.,, Howley, Peter M.,, Israel, Mark A.,, Thompson, Craig (Craig B.) (Fourth ed.). Philadelphia, PA. 2015. ISBN 9781455740666. OCLC 870870610.
{{cite book}}: CS1 maint : 기타(링크) - ^ Zhao J, Kennedy BK, Lawrence BD, Barbie DA, Matera AG, Fletcher JA, Harlow E (September 2000). "NPAT links cyclin E-Cdk2 to the regulation of replication-dependent histone gene transcription". Genes & Development. 14 (18): 2283–97. doi:10.1101/gad.827700. PMC 316937. PMID 10995386.
- ^ Gopinathan L, Tan SL, Padmakumar VC, Coppola V, Tessarollo L, Kaldis P (July 2014). "Loss of Cdk2 and cyclin A2 impairs cell proliferation and tumorigenesis". Cancer Research. 74 (14): 3870–9. doi:10.1158/0008-5472.CAN-13-3440. PMC 4102624. PMID 24802190.
- ^ Xia P, Liu Y, Chen J, Coates S, Liu D, Cheng Z (October 2018). "Inhibition of cyclin-dependent kinase 2 protects against doxorubicin-induced cardiomyocyte apoptosis and cardiomyopathy". The Journal of Biological Chemistry. 293 (51): 19672–19685. doi:10.1074/jbc.ra118.004673. PMC 6314117. PMID 30361442.
- ^ a b Whittaker SR, Mallinger A, Workman P, Clarke PA (May 2017). "Inhibitors of cyclin-dependent kinases as cancer therapeutics". Pharmacology & Therapeutics. 173: 83–105. doi:10.1016/j.pharmthera.2017.02.008. PMC 6141011. PMID 28174091.
- ^ Cicenas J, Kalyan K, Sorokinas A, Stankunas E, Levy J, Meskinyte I, Stankevicius V, Kaupinis A, Valius M (June 2015). "Roscovitine in cancer and other diseases". Annals of Translational Medicine. 3 (10): 135. doi:10.3978/j.issn.2305-5839.2015.03.61. PMC 4486920. PMID 26207228.
- ^ Brown NR, Korolchuk S, Martin MP, Stanley WA, Moukhametzianov R, Noble ME, Endicott JA (April 2015). "CDK1 structures reveal conserved and unique features of the essential cell cycle CDK". Nature Communications. 6: 6769. Bibcode:2015NatCo...6.6769B. doi:10.1038/ncomms7769. PMC 4413027. PMID 25864384.
- ^ Rastelli G, Anighoro A, Chripkova M, Carrassa L, Broggini M (2014-06-09). "Structure-based discovery of the first allosteric inhibitors of cyclin-dependent kinase 2". Cell Cycle. 13 (14): 2296–305. doi:10.4161/cc.29295. PMC 4111683. PMID 24911186.
- ^ Pellerano M, Tcherniuk S, Perals C, Ngoc Van TN, Garcin E, Mahuteau-Betzer F, Teulade-Fichou MP, Morris MC (August 2017). "Targeting Conformational Activation of CDK2 Kinase". Biotechnology Journal. 12 (8): 1600531. doi:10.1002/biot.201600531. PMID 28430399.
- ^ a b Singh R, Bhardwaj VK, Sharma J, Das P, Purohit R (March 2021). "Identification of selective cyclin-dependent kinase 2 inhibitor from the library of pyrrolone-fused benzosuberene compounds: an in silico exploration". Journal of Biomolecular Structure and Dynamics: 1–9. doi:10.1080/07391102.2021.1900918. PMID 33749525. S2CID 232309609.
- ^ Levkau B, Koyama H, Raines EW, Clurman BE, Herren B, Orth K, Roberts JM, Ross R (March 1998). "Cleavage of p21Cip1/Waf1 and p27Kip1 mediates apoptosis in endothelial cells through activation of Cdk2: role of a caspase cascade". Molecular Cell. 1 (4): 553–63. doi:10.1016/S1097-2765(00)80055-6. PMID 9660939.
- ^ Davis ST, Benson BG, Bramson HN, Chapman DE, Dickerson SH, Dold KM, Eberwein DJ, Edelstein M, Frye SV, Gampe RT, Griffin RJ, Harris PA, Hassell AM, Holmes WD, Hunter RN, Knick VB, Lackey K, Lovejoy B, Luzzio MJ, Murray D, Parker P, Rocque WJ, Shewchuk L, Veal JM, Walker DH, Kuyper LF (January 2001). "Prevention of chemotherapy-induced alopecia in rats by CDK inhibitors". Science. 291 (5501): 134–7. Bibcode:2001Sci...291..134D. doi:10.1126/science.291.5501.134. PMID 11141566.
- ^ Liu R, Heiss EH, Waltenberger B, Blažević T, Schachner D, Jiang B, Krystof V, Liu W, Schwaiger S, Peña-Rodríguez LM, Breuss JM, Stuppner H, Dirsch VM, Atanasov AG (April 2018). "Constituents of Mediterranean Spices Counteracting Vascular Smooth Muscle Cell Proliferation: Identification and Characterization of Rosmarinic Acid Methyl Ester as a Novel Inhibitor". Molecular Nutrition & Food Research. 62 (7): e1700860. doi:10.1002/mnfr.201700860. PMID 29405576. S2CID 4634007.
- ^ Du J, Widlund HR, Horstmann MA, Ramaswamy S, Ross K, Huber WE, Nishimura EK, Golub TR, Fisher DE (December 2004). "Critical role of CDK2 for melanoma growth linked to its melanocyte-specific transcriptional regulation by MITF". Cancer Cell. 6 (6): 565–76. doi:10.1016/j.ccr.2004.10.014. PMID 15607961.
- ^ Hoek KS, Schlegel NC, Eichhoff OM, Widmer DS, Praetorius C, Einarsson SO, Valgeirsdottir S, Bergsteinsdottir K, Schepsky A, Dummer R, Steingrimsson E (December 2008). "Novel MITF targets identified using a two-step DNA microarray strategy". Pigment Cell & Melanoma Research. 21 (6): 665–76. doi:10.1111/j.1755-148X.2008.00505.x. PMID 19067971. S2CID 24698373.
- ^ Chen Y, Farmer AA, Chen CF, Jones DC, Chen PL, Lee WH (July 1996). "BRCA1 is a 220-kDa nuclear phosphoprotein that is expressed and phosphorylated in a cell cycle-dependent manner". Cancer Research. 56 (14): 3168–72. PMID 8764100.
- ^ Ruffner H, Jiang W, Craig AG, Hunter T, Verma IM (July 1999). "BRCA1 is phosphorylated at serine 1497 in vivo at a cyclin-dependent kinase 2 phosphorylation site". Molecular and Cellular Biology. 19 (7): 4843–54. doi:10.1128/MCB.19.7.4843. PMC 84283. PMID 10373534.
- ^ Wang H, Shao N, Ding QM, Cui J, Reddy ES, Rao VN (July 1997). "BRCA1 proteins are transported to the nucleus in the absence of serum and splice variants BRCA1a, BRCA1b are tyrosine phosphoproteins that associate with E2F, cyclins and cyclin dependent kinases". Oncogene. 15 (2): 143–57. doi:10.1038/sj.onc.1201252. PMID 9244350.
- ^ Shintani S, Ohyama H, Zhang X, McBride J, Matsuo K, Tsuji T, Hu MG, Hu G, Kohno Y, Lerman M, Todd R, Wong DT (September 2000). "p12(DOC-1) is a novel cyclin-dependent kinase 2-associated protein". Molecular and Cellular Biology. 20 (17): 6300–7. doi:10.1128/MCB.20.17.6300-6307.2000. PMC 86104. PMID 10938106.
- ^ a b Connor MK, Kotchetkov R, Cariou S, Resch A, Lupetti R, Beniston RG, Melchior F, Hengst L, Slingerland JM (January 2003). "CRM1/Ran-mediated nuclear export of p27(Kip1) involves a nuclear export signal and links p27 export and proteolysis". Molecular Biology of the Cell. 14 (1): 201–13. doi:10.1091/mbc.E02-06-0319. PMC 140238. PMID 12529437.
- ^ a b Rosner M, Hengstschläger M (November 2004). "Tuberin binds p27 and negatively regulates its interaction with the SCF component Skp2". The Journal of Biological Chemistry. 279 (47): 48707–15. doi:10.1074/jbc.M405528200. PMID 15355997.
- ^ Youn CK, Cho HJ, Kim SH, Kim HB, Kim MH, Chang IY, Lee JS, Chung MH, Hahm KS, You HJ (February 2005). "Bcl-2 expression suppresses mismatch repair activity through inhibition of E2F transcriptional activity". Nature Cell Biology. 7 (2): 137–47. doi:10.1038/ncb1215. PMID 15619620. S2CID 42766325.
- ^ Porter LA, Kong-Beltran M, Donoghue DJ (September 2003). "Spy1 interacts with p27Kip1 to allow G1/S progression". Molecular Biology of the Cell. 14 (9): 3664–74. doi:10.1091/mbc.E02-12-0820. PMC 196558. PMID 12972555.
- ^ a b Law BK, Chytil A, Dumont N, Hamilton EG, Waltner-Law ME, Aakre ME, Covington C, Moses HL (December 2002). "Rapamycin potentiates transforming growth factor beta-induced growth arrest in nontransformed, oncogene-transformed, and human cancer cells". Molecular and Cellular Biology. 22 (23): 8184–98. doi:10.1128/mcb.22.23.8184-8198.2002. PMC 134072. PMID 12417722.
- ^ Yeh CT, Lu SC, Chao CH, Chao ML (May 2003). "Abolishment of the interaction between cyclin-dependent kinase 2 and Cdk-associated protein phosphatase by a truncated KAP mutant". Biochemical and Biophysical Research Communications. 305 (2): 311–4. doi:10.1016/s0006-291x(03)00757-5. PMID 12745075.
- ^ Hannon GJ, Casso D, Beach D (March 1994). "KAP: a dual specificity phosphatase that interacts with cyclin-dependent kinases". Proceedings of the National Academy of Sciences of the United States of America. 91 (5): 1731–5. Bibcode:1994PNAS...91.1731H. doi:10.1073/pnas.91.5.1731. PMC 43237. PMID 8127873.
- ^ a b Harper JW, Adami GR, Wei N, Keyomarsi K, Elledge SJ (November 1993). "The p21 Cdk-interacting protein Cip1 is a potent inhibitor of G1 cyclin-dependent kinases". Cell. 75 (4): 805–16. doi:10.1016/0092-8674(93)90499-g. PMID 8242751.
- ^ Wang H, Iakova P, Wilde M, Welm A, Goode T, Roesler WJ, Timchenko NA (October 2001). "C/EBPalpha arrests cell proliferation through direct inhibition of Cdk2 and Cdk4". Molecular Cell. 8 (4): 817–28. doi:10.1016/s1097-2765(01)00366-5. PMID 11684017.
- ^ Sweeney C, Murphy M, Kubelka M, Ravnik SE, Hawkins CF, Wolgemuth DJ, Carrington M (January 1996). "A distinct cyclin A is expressed in germ cells in the mouse". Development. 122 (1): 53–64. doi:10.1242/dev.122.1.53. PMID 8565853.
- ^ Yang R, Morosetti R, Koeffler HP (March 1997). "Characterization of a second human cyclin A that is highly expressed in testis and in several leukemic cell lines". Cancer Research. 57 (5): 913–20. PMID 9041194.
- ^ Müller-Tidow C, Wang W, Idos GE, Diederichs S, Yang R, Readhead C, Berdel WE, Serve H, Saville M, Watson R, Koeffler HP (April 2001). "Cyclin A1 directly interacts with B-myb and cyclin A1/cdk2 phosphorylate B-myb at functionally important serine and threonine residues: tissue-specific regulation of B-myb function". Blood. 97 (7): 2091–7. doi:10.1182/blood.v97.7.2091. PMID 11264176.
- ^ Brown NR, Noble ME, Endicott JA, Johnson LN (November 1999). "The structural basis for specificity of substrate and recruitment peptides for cyclin-dependent kinases". Nature Cell Biology. 1 (7): 438–43. doi:10.1038/15674. PMID 10559988. S2CID 17988582.
- ^ a b c Shanahan F, Seghezzi W, Parry D, Mahony D, Lees E (February 1999). "Cyclin E associates with BAF155 and BRG1, components of the mammalian SWI-SNF complex, and alters the ability of BRG1 to induce growth arrest". Molecular and Cellular Biology. 19 (2): 1460–9. doi:10.1128/mcb.19.2.1460. PMC 116074. PMID 9891079.
- ^ a b McKenzie PP, Danks MK, Kriwacki RW, Harris LC (July 2003). "P21Waf1/Cip1 dysfunction in neuroblastoma: a novel mechanism of attenuating G0-G1 cell cycle arrest". Cancer Research. 63 (13): 3840–4. PMID 12839982.
- ^ Koff A, Giordano A, Desai D, Yamashita K, Harper JW, Elledge S, Nishimoto T, Morgan DO, Franza BR, Roberts JM (September 1992). "Formation and activation of a cyclin E-cdk2 complex during the G1 phase of the human cell cycle". Science. 257 (5077): 1689–94. Bibcode:1992Sci...257.1689K. doi:10.1126/science.1388288. PMID 1388288.
- ^ Mayer C, Zhao J, Yuan X, Grummt I (February 2004). "mTOR-dependent activation of the transcription factor TIF-IA links rRNA synthesis to nutrient availability". Genes & Development. 18 (4): 423–34. doi:10.1101/gad.285504. PMC 359396. PMID 15004009.
- ^ Boudrez A, Beullens M, Groenen P, Van Eynde A, Vulsteke V, Jagiello I, Murray M, Krainer AR, Stalmans W, Bollen M (August 2000). "NIPP1-mediated interaction of protein phosphatase-1 with CDC5L, a regulator of pre-mRNA splicing and mitotic entry". The Journal of Biological Chemistry. 275 (33): 25411–7. doi:10.1074/jbc.M001676200. PMID 10827081.
- ^ Henneke G, Koundrioukoff S, Hübscher U (July 2003). "Phosphorylation of human Fen1 by cyclin-dependent kinase modulates its role in replication fork regulation". Oncogene. 22 (28): 4301–13. doi:10.1038/sj.onc.1206606. PMID 12853968.
- ^ Méndez J, Zou-Yang XH, Kim SY, Hidaka M, Tansey WP, Stillman B (March 2002). "Human origin recognition complex large subunit is degraded by ubiquitin-mediated proteolysis after initiation of DNA replication". Molecular Cell. 9 (3): 481–91. doi:10.1016/s1097-2765(02)00467-7. PMID 11931757.
- ^ a b Yam CH, Ng RW, Siu WY, Lau AW, Poon RY (January 1999). "Regulation of cyclin A-Cdk2 by SCF component Skp1 and F-box protein Skp2". Molecular and Cellular Biology. 19 (1): 635–45. doi:10.1128/mcb.19.1.635. PMC 83921. PMID 9858587.
- ^ Ono T, Kitaura H, Ugai H, Murata T, Yokoyama KK, Iguchi-Ariga SM, Ariga H (October 2000). "TOK-1, a novel p21Cip1-binding protein that cooperatively enhances p21-dependent inhibitory activity toward CDK2 kinase". The Journal of Biological Chemistry. 275 (40): 31145–54. doi:10.1074/jbc.M003031200. PMID 10878006.
- ^ a b Cheng A, Kaldis P, Solomon MJ (November 2000). "Dephosphorylation of human cyclin-dependent kinases by protein phosphatase type 2C alpha and beta 2 isoforms". The Journal of Biological Chemistry. 275 (44): 34744–9. doi:10.1074/jbc.M006210200. PMID 10934208.
- ^ Leng X, Noble M, Adams PD, Qin J, Harper JW (April 2002). "Reversal of growth suppression by p107 via direct phosphorylation by cyclin D1/cyclin-dependent kinase 4". Molecular and Cellular Biology. 22 (7): 2242–54. doi:10.1128/mcb.22.7.2242-2254.2002. PMC 133692. PMID 11884610.
- ^ Lacy S, Whyte P (May 1997). "Identification of a p130 domain mediating interactions with cyclin A/cdk 2 and cyclin E/cdk 2 complexes". Oncogene. 14 (20): 2395–406. doi:10.1038/sj.onc.1201085. PMID 9188854.
- ^ Marti A, Wirbelauer C, Scheffner M, Krek W (May 1999). "Interaction between ubiquitin-protein ligase SCFSKP2 and E2F-1 underlies the regulation of E2F-1 degradation". Nature Cell Biology. 1 (1): 14–9. doi:10.1038/8984. PMID 10559858. S2CID 8884226.
추가 읽기
- Kaldis P, Aleem E (November 2005). "Cell cycle sibling rivalry: Cdc2 vs. Cdk2". Cell Cycle. 4 (11): 1491–4. doi:10.4161/cc.4.11.2124. PMID 16258277.
- Moore NL, Narayanan R, Weigel NL (February 2007). "Cyclin dependent kinase 2 and the regulation of human progesterone receptor activity". Steroids. 72 (2): 202–9. doi:10.1016/j.steroids.2006.11.025. PMC 1950255. PMID 17207508.
외부 링크
- Cyclin-dependent+Kinase+2 미국 국립 의학 도서관의 의료 과목 제목(MesH)
- UCSC 게놈 브라우저에서 CDK2 인간 유전자 위치.
- UCSC 게놈 브라우저의 CDK2 인간 유전자 세부 정보.