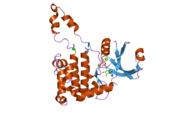CHEK2
CHEK2CHEK2(Checkpoint kinase 2)는 세린-트레오닌 키나제인 단백질 CHK2를 인코딩하는 종양 억제기 유전자다.CHK2는 DNA 손상에 대한 DNA 수리, 세포 주기 구속 또는 세포 사멸에 관여한다.CHEK2 유전자에 대한 돌연변이는 광범위한 암과 연관되어 있다.[5]
유전자위치
CEK2 유전자는 위치 12.1에서 22번 염색체의 긴 (q) 팔에 위치한다.22번 염색체의 위치는 염기쌍 28,687,742부터 염기쌍 28,741,[5]904까지 뻗어있다.
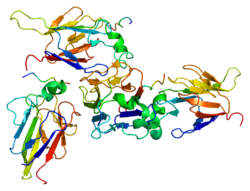
단백질 구조
CHEK2 유전자에 의해 인코딩된 CHEK2 단백질은 세린 threonine kinase이다.단백질은 543개의 아미노산과 다음과 같은 영역으로 구성된다.
SCD 영역에는 DNA 손상에 대응하여 인산화 부위의 역할을 하는 여러 SQ/TQ 모티브가 포함되어 있다.가장 주목할 만하고 자주 인지되는 부위는 Thr68이다.[6]
CHK2는 비활성 상태에서 모노머로 나타난다.그러나 DNA 손상 시 SCD인산화효소는 CHK2 조광화를 유발한다.인광 처리된 Thr68 (SCD에 위치)은 조광기를 형성하기 위해 FHA 도메인과 상호작용한다.단백질이 약해진 후 KD는 자가인산화를 통해 활성화된다.KD가 활성화되면 CHK2 다이머가 분리된다.[6]
기능 및 메커니즘
CHEK2 유전자는 종양 억제기를 작용하는 단백질인 체크포인트키나아제2(CHK2)를 위해 암호화된 것이다.CHK2는 세포 분열을 조절하며, 세포가 너무 빠르게 또는 통제되지 않는 방식으로 분열되는 것을 방지하는 능력을 가지고 있다.[5]
DNA가 이중 가닥이 끊어질 때 CHK2가 활성화된다.구체적으로는 DNA가 활성화된 인산염리노시톨키나아제(PIKK) ATM 인산염 사이트 Thr68을 손상시켜 CHK2를 활성화한다.[6]CHK2 인산염은 활성화되면 CDC25 인산염을 포함한 다운스트림 표적을 생성하며, CDK(Cyclin-dependent kinas)를 활성화한다.따라서 CHK2의 CDC25 인산염 억제제는 세포가 유사분열로 들어가는 것을 막는다.게다가, CHK2 단백질은 p53 (p53)을 포함한 몇몇 다른 단백질들과 상호작용한다.CHK2에 의한 p53의 안정화는 G1단계에서 세포주기 구속으로 이어진다.나아가 CHK2는 세포주기 전사인자 E2F1과 세포사멸(프로그래밍된 세포사망)에 관여하는 프로밀로시즘성 백혈병 단백질(PML)을 인산화시키는 것으로 알려져 있다.[6]
암과의 연관성
CHK2 단백질은 DNA 손상 검문소에서 중요한 역할을 한다.따라서, CHEK2 유전자에 대한 돌연변이는 광범위한 암의 원인이라는 꼬리표가 붙었다.
1999년, CHEK2의 유전적 변화는 유전적 암 감수성과 일치하는 것으로 밝혀졌다.[7]
벨 외 연구진(1999)은 4개의 Li-Fraumeni 증후군(LFS)과 18개의 Li-Fraumeni 유사(LFL) 가족 중에서 3개의 CHEK2 세균선 돌연변이를 발견했다.이 발견 이후, 세 가지 변종 중 두 가지 변종(exon 10의 키나제 영역 삭제와 exon 3의 FHA 영역의 오감 변이)은 다른 암뿐만 아니라 유방으로의 유전적 감수성과 연결되었다.[8]
초기 추측을 넘어, LFS와 LFL 환자들을 선별한 결과 CHEK2 유전자에서 개별적인 오식 변형이 발견되지 않았다.또한, exon 10의 키나세 도메인에서 삭제된 경우는 LFS/LFL 환자들 사이에서 드물게 발견되었다.이러한 연구에서 나온 증거는 CHEK2가 Li-Fraumeni 증후군에 대한 소인 유전자가 아니라는 것을 보여준다.[8]
유방암
CHEK2 유전자의 유전적 돌연변이는 유방암의 특정 사례와 연관되어 있다.가장 주목할 만한 것은 exon 10(1100dLC)의 위치 1100에서 단일 DNA 뉴클레오티드를 삭제하면 키나제 영역에서 잘린 CHK2 단백질의 비기능 버전이 생성된다는 점이다.정상적인 CHK2 단백질 기능의 상실은 규제되지 않은 세포분열을 초래하고, DNA에 누적된 손상을 초래하며, 많은 경우에 종양 발달을 초래한다.[5]CHEK2*1100del 돌연변이는 동유럽과 북유럽 혈통의 개인들에게서 가장 흔히 나타난다.이러한 개체군 내에서 CHEK2*1100delC 돌연변이는 200명 중 100명 중 1명에서 1명은 CHEK2*1100delC 돌연변이는 200명 중 1명꼴이다.그러나 북아메리카에서는 333개 중 1개에서 500개 중 1개로 빈도가 떨어진다.이 돌연변이는 스페인과 인도에서 거의 없다.[9]연구 결과에 따르면 CHEK2 1100델C는 유방암 발병률이 2배 증가하고 남성은 유방암 발병률이 10배 증가하는 것과 일치한다.[10]
exon 3에서 FHA 영역의 I157T 변종이라고 알려진 CHEK2 돌연변이도 유방암과 연관되었지만 CHEK2*1100delC 돌연변이보다 더 낮은 위험에 처해 있다.이 변종에서 비롯된 유방암의 추정 분율은 미국에서 약 1.2%로 보고되고 있다.[8]
두 개의 CHEK2 유전자 돌연변이, exon 11의 키나제 영역에 대한 아미노산 대체인 CHEK2*S428F와 N-단자 지역의 아미노산 대체인 CEK2*P85L가 아슈케나지 유대인 인구에서 추가로 발견되었다.[9]히스패닉 창시자 돌연변이 제안도 기술됐다.[11]
기타암
CHEK2에 대한 돌연변이는 유전적, 비 유전적 암 사례에서 발견되었다.연구는 이 돌연변이를 전립선, 폐, 대장, 신장, 갑상선암의 사례와 연관시킨다.특정 뇌종양과 골육종에도 연관성이 있다.[5]
BRCA1과 BRCA2 돌연변이와 달리 CEK2 돌연변이는 난소암에 걸릴 위험이 높아지는 것으로 보이지 않는다.[10]그러나, 편평한 폐암에 대한 큰 효과의 게놈 광범위한 연관성은 CHEK2 (p)에서 희귀한 변종에 대해 설명되어 왔다.Ile157Thr, rs17879961, OR = 0.38).[12]
감수분열
CHEK2는 생쥐 난모세포 성숙과 초기 배아 발달 동안 세포 주기 진행과 스핀들 조립을 조절한다.[13][14]CHEK2는 ATM 키나아제의 다운스트림 이펙터로서 이중 스트랜드 파손에 주로 반응하는 ATM 키나아제(ataxia-telangectasia and Rad3 관련) 키나아제로도 활성화할 수 있다.생쥐의 경우 CHEK2는 여성의 감수분열에서 DNA 손상 감시를 위해 필수적이다.난모세포가 DNA 이중 가닥과 파괴 손상에 반응하는 경로 계층 구조는 ATR 키나아제가 CHEK2에 신호를 보내 p53과 p63 단백질을 활성화시키는 것이다.[15]
초파리인 드로소필라에서는 세균선 세포의 조사로 이중 가닥이 끊어져 세포주기가 정지되고 세포사멸이 발생한다.드로소필라 CHEK2 정형외과적 mnk와 p53 정형외과적 dp53은 난모세포 선택과 감수재조합이 발생할 때 초기 난형 발생에서 관찰된 세포 사망의 상당 부분을 위해 필요하다.[16]
상호작용
CHEK2는 다음과 상호작용하는 것으로 나타났다.
참조
- ^ a b c GRCh38: 앙상블 릴리스 89: ENSG00000183765 - 앙상블, 2017년 5월
- ^ a b c GRCm38: 앙상블 릴리스 89: ENSMUSG000029521 - 앙상블, 2017년 5월
- ^ "Human PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ "Mouse PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ a b c d e "CHEK2". Genetics Home Reference. August 2007.
- ^ a b c d Cai Z, Chehab NH, Pavletich NP (September 2009). "Structure and activation mechanism of the CHK2 DNA damage checkpoint kinase". Molecular Cell. 35 (6): 818–29. doi:10.1016/j.molcel.2009.09.007. PMID 19782031.
- ^ Bell DW, Varley JM, Szydlo TE, Kang DH, Wahrer DC, Shannon KE, et al. (December 1999). "Heterozygous germ line hCHK2 mutations in Li-Fraumeni syndrome". Science. 286 (5449): 2528–31. doi:10.1126/science.286.5449.2528. PMID 10617473.
- ^ a b c Nevanlinna H, Bartek J (September 2006). "The CHEK2 gene and inherited breast cancer susceptibility". Oncogene. 25 (43): 5912–9. doi:10.1038/sj.onc.1209877. PMID 16998506.
- ^ a b Offit K, Garber JE (February 2008). "Time to check CHEK2 in families with breast cancer?". Journal of Clinical Oncology. 26 (4): 519–20. doi:10.1200/JCO.2007.13.8503. PMID 18172189.
- ^ a b Meijers-Heijboer H, van den Ouweland A, Klijn J, Wasielewski M, de Snoo A, Oldenburg R, et al. (May 2002). "Low-penetrance susceptibility to breast cancer due to CHEK2(*)1100delC in noncarriers of BRCA1 or BRCA2 mutations". Nature Genetics. 31 (1): 55–9. doi:10.1038/ng879. PMID 11967536. S2CID 195216803.
- ^ Weitzel JN, Neuhausen SL, Adamson A, Tao S, Ricker C, Maoz A, et al. (August 2019). "Pathogenic and likely pathogenic variants in PALB2, CHEK2, and other known breast cancer susceptibility genes among 1054 BRCA-negative Hispanics with breast cancer". Cancer. 125 (16): 2829–2836. doi:10.1002/cncr.32083. PMC 7376605. PMID 31206626.
- ^ Wang Y, McKay JD, Rafnar T, Wang Z, Timofeeva MN, Broderick P, et al. (July 2014). "Rare variants of large effect in BRCA2 and CHEK2 affect risk of lung cancer". Nature Genetics. 46 (7): 736–41. doi:10.1038/ng.3002. PMC 4074058. PMID 24880342.
- ^ Dai XX, Duan X, Liu HL, Cui XS, Kim NH, Sun SC (February 2014). "Chk2 regulates cell cycle progression during mouse oocyte maturation and early embryo development". Molecules and Cells. 37 (2): 126–32. doi:10.14348/molcells.2014.2259. PMC 3935625. PMID 24598997.
- ^ Ruth KS, Day FR, Hussain J, Martínez-Marchal A, Aiken CE, Azad A, et al. (August 2021). "Genetic insights into biological mechanisms governing human ovarian ageing". Nature. 596 (7872): 393–397. Bibcode:2021Natur.596..393R. doi:10.1038/s41586-021-03779-7. ISSN 0028-0836. PMC 7611832. PMID 34349265.
- ^ Bolcun-Filas E, Rinaldi VD, White ME, Schimenti JC (January 2014). "Reversal of female infertility by Chk2 ablation reveals the oocyte DNA damage checkpoint pathway". Science. 343 (6170): 533–6. Bibcode:2014Sci...343..533B. doi:10.1126/science.1247671. PMC 4048839. PMID 24482479.
- ^ Shim HJ, Lee EM, Nguyen LD, Shim J, Song YH (2014). "High-dose irradiation induces cell cycle arrest, apoptosis, and developmental defects during Drosophila oogenesis". PLOS ONE. 9 (2): e89009. Bibcode:2014PLoSO...989009S. doi:10.1371/journal.pone.0089009. PMC 3923870. PMID 24551207.
- ^ Lee JS, Collins KM, Brown AL, Lee CH, Chung JH (March 2000). "hCds1-mediated phosphorylation of BRCA1 regulates the DNA damage response". Nature. 404 (6774): 201–4. Bibcode:2000Natur.404..201L. doi:10.1038/35004614. PMID 10724175. S2CID 4345911.
- ^ Chabalier-Taste C, Racca C, Dozier C, Larminat F (December 2008). "BRCA1 is regulated by Chk2 in response to spindle damage". Biochimica et Biophysica Acta (BBA) - Molecular Cell Research. 1783 (12): 2223–33. doi:10.1016/j.bbamcr.2008.08.006. PMID 18804494.
- ^ Matsuoka S, Ballif BA, Smogorzewska A, McDonald ER, Hurov KE, Luo J, et al. (May 2007). "ATM and ATR substrate analysis reveals extensive protein networks responsive to DNA damage". Science. 316 (5828): 1160–6. Bibcode:2007Sci...316.1160M. doi:10.1126/science.1140321. PMID 17525332. S2CID 16648052.
- ^ Lou Z, Minter-Dykhouse K, Wu X, Chen J (February 2003). "MDC1 is coupled to activated CHK2 in mammalian DNA damage response pathways". Nature. 421 (6926): 957–61. Bibcode:2003Natur.421..957L. doi:10.1038/nature01447. PMID 12607004. S2CID 4411622.
- ^ Adamson AW, Beardsley DI, Kim WJ, Gao Y, Baskaran R, Brown KD (March 2005). "Methylator-induced, mismatch repair-dependent G2 arrest is activated through Chk1 and Chk2". Molecular Biology of the Cell. 16 (3): 1513–26. doi:10.1091/mbc.E04-02-0089. PMC 551512. PMID 15647386.
- ^ Brown KD, Rathi A, Kamath R, Beardsley DI, Zhan Q, Mannino JL, Baskaran R (January 2003). "The mismatch repair system is required for S-phase checkpoint activation". Nature Genetics. 33 (1): 80–4. doi:10.1038/ng1052. PMID 12447371. S2CID 20616220.
- ^ Chen XB, Melchionna R, Denis CM, Gaillard PH, Blasina A, Van de Weyer I, et al. (November 2001). "Human Mus81-associated endonuclease cleaves Holliday junctions in vitro". Molecular Cell. 8 (5): 1117–27. doi:10.1016/s1097-2765(01)00375-6. PMID 11741546.
- ^ Tsvetkov L, Xu X, Li J, Stern DF (March 2003). "Polo-like kinase 1 and Chk2 interact and co-localize to centrosomes and the midbody". The Journal of Biological Chemistry. 278 (10): 8468–75. doi:10.1074/jbc.M211202200. PMID 12493754.
- ^ Bahassi EM, Conn CW, Myer DL, Hennigan RF, McGowan CH, Sanchez Y, Stambrook PJ (September 2002). "Mammalian Polo-like kinase 3 (Plk3) is a multifunctional protein involved in stress response pathways". Oncogene. 21 (43): 6633–40. doi:10.1038/sj.onc.1205850. PMID 12242661.
추가 읽기
- Caspari T (April 2000). "How to activate p53". Current Biology. 10 (8): R315-7. doi:10.1016/S0960-9822(00)00439-5. PMID 10801407. S2CID 17342787.
- McGowan CH (June 2002). "Checking in on Cds1 (Chk2): A checkpoint kinase and tumor suppressor". BioEssays. 24 (6): 502–11. doi:10.1002/bies.10101. PMID 12111733. S2CID 6654874.
- Honrado E, Osorio A, Palacios J, Benitez J (September 2006). "Pathology and gene expression of hereditary breast tumors associated with BRCA1, BRCA2 and CHEK2 gene mutations". Oncogene. 25 (43): 5837–45. doi:10.1038/sj.onc.1209875. PMID 16998498. S2CID 20960561.
- Nevanlinna H, Bartek J (September 2006). "The CHEK2 gene and inherited breast cancer susceptibility". Oncogene. 25 (43): 5912–9. doi:10.1038/sj.onc.1209877. PMID 16998506.
- Peng CY, Graves PR, Thoma RS, Wu Z, Shaw AS, Piwnica-Worms H (September 1997). "Mitotic and G2 checkpoint control: regulation of 14-3-3 protein binding by phosphorylation of Cdc25C on serine-216". Science. 277 (5331): 1501–5. doi:10.1126/science.277.5331.1501. PMID 9278512.
- Lykidis A, Jackson PD, Rock CO, Jackowski S (December 1997). "The role of CDP-diacylglycerol synthetase and phosphatidylinositol synthase activity levels in the regulation of cellular phosphatidylinositol content". The Journal of Biological Chemistry. 272 (52): 33402–9. doi:10.1074/jbc.272.52.33402. PMID 9407135.
- Lindsay HD, Griffiths DJ, Edwards RJ, Christensen PU, Murray JM, Osman F, et al. (February 1998). "S-phase-specific activation of Cds1 kinase defines a subpathway of the checkpoint response in Schizosaccharomyces pombe". Genes & Development. 12 (3): 382–95. doi:10.1101/gad.12.3.382. PMC 316487. PMID 9450932.
- Matsuoka S, Huang M, Elledge SJ (December 1998). "Linkage of ATM to cell cycle regulation by the Chk2 protein kinase". Science. 282 (5395): 1893–7. Bibcode:1998Sci...282.1893M. doi:10.1126/science.282.5395.1893. PMID 9836640.
- Martinho RG, Lindsay HD, Flaggs G, DeMaggio AJ, Hoekstra MF, Carr AM, Bentley NJ (December 1998). "Analysis of Rad3 and Chk1 protein kinases defines different checkpoint responses". The EMBO Journal. 17 (24): 7239–49. doi:10.1093/emboj/17.24.7239. PMC 1171070. PMID 9857181.
- Blasina A, de Weyer IV, Laus MC, Luyten WH, Parker AE, McGowan CH (January 1999). "A human homologue of the checkpoint kinase Cds1 directly inhibits Cdc25 phosphatase". Current Biology. 9 (1): 1–10. doi:10.1016/S0960-9822(99)80041-4. PMID 9889122. S2CID 18008732.
- Brown AL, Lee CH, Schwarz JK, Mitiku N, Piwnica-Worms H, Chung JH (March 1999). "A human Cds1-related kinase that functions downstream of ATM protein in the cellular response to DNA damage". Proceedings of the National Academy of Sciences of the United States of America. 96 (7): 3745–50. Bibcode:1999PNAS...96.3745B. doi:10.1073/pnas.96.7.3745. PMC 22365. PMID 10097108.
- Chaturvedi P, Eng WK, Zhu Y, Mattern MR, Mishra R, Hurle MR, et al. (July 1999). "Mammalian Chk2 is a downstream effector of the ATM-dependent DNA damage checkpoint pathway". Oncogene. 18 (28): 4047–54. doi:10.1038/sj.onc.1202925. PMID 10435585. S2CID 23907734.
- Ouyang B, Li W, Pan H, Meadows J, Hoffmann I, Dai W (October 1999). "The physical association and phosphorylation of Cdc25C protein phosphatase by Prk". Oncogene. 18 (44): 6029–36. doi:10.1038/sj.onc.1202983. PMID 10557092.
- Dunham I, Shimizu N, Roe BA, Chissoe S, Hunt AR, Collins JE, et al. (December 1999). "The DNA sequence of human chromosome 22". Nature. 402 (6761): 489–95. Bibcode:1999Natur.402..489D. doi:10.1038/990031. PMID 10591208.
- Bell DW, Varley JM, Szydlo TE, Kang DH, Wahrer DC, Shannon KE, et al. (December 1999). "Heterozygous germ line hCHK2 mutations in Li-Fraumeni syndrome". Science. 286 (5449): 2528–31. doi:10.1126/science.286.5449.2528. PMID 10617473.
- Chehab NH, Malikzay A, Appel M, Halazonetis TD (February 2000). "Chk2/hCds1 functions as a DNA damage checkpoint in G(1) by stabilizing p53". Genes & Development. 14 (3): 278–88. doi:10.1101/gad.14.3.278. PMC 316357. PMID 10673500.
- Hirao A, Kong YY, Matsuoka S, Wakeham A, Ruland J, Yoshida H, et al. (March 2000). "DNA damage-induced activation of p53 by the checkpoint kinase Chk2". Science. 287 (5459): 1824–7. Bibcode:2000Sci...287.1824H. doi:10.1126/science.287.5459.1824. PMID 10710310.
- Lee JS, Collins KM, Brown AL, Lee CH, Chung JH (March 2000). "hCds1-mediated phosphorylation of BRCA1 regulates the DNA damage response". Nature. 404 (6774): 201–4. Bibcode:2000Natur.404..201L. doi:10.1038/35004614. PMID 10724175. S2CID 4345911.
- Zhou BB, Chaturvedi P, Spring K, Scott SP, Johanson RA, Mishra R, et al. (April 2000). "Caffeine abolishes the mammalian G(2)/M DNA damage checkpoint by inhibiting ataxia-telangiectasia-mutated kinase activity". The Journal of Biological Chemistry. 275 (14): 10342–8. doi:10.1074/jbc.275.14.10342. PMID 10744722. S2CID 4240483.
외부 링크
- 교육 리소스 웨이백 머신에 2010-04-13 보관
- 진 리뷰
- 진 테스트
- CHEK2+단백질,+인간, 미국 국립 의학 도서관의 의학 과목 제목(MSH)
- UCSC 게놈 브라우저의 인간 CDS1 게놈 위치 및 CDS1 유전자 세부 정보 페이지.
- UCSC 게놈 브라우저의 인간 CHEK2 유전체 위치 및 CHEK2 유전자 세부 정보 페이지.
이 기사는 공공영역에 있는 미국 국립 의학 도서관의 텍스트를 통합하고 있다.