카로티노이드
Carotenoid테트라테페노이드라고도 불리는 카로티노이드(/kˈrttɪnɔd/)는 여러 박테리아와 [1]곰팡이뿐만 아니라 식물과 조류에 의해 생성되는 노란색, 주황색, 그리고 빨간색 유기 색소이다.카로티노이드는 호박, 당근, 파스닙, 옥수수, 토마토, 카나리아, 홍학, 연어, 바닷가재, 새우, 그리고 [1]수선화에 특징적인 색깔을 줍니다.카로티노이드는 이 모든 유기체들에 의해 지방과 다른 기본적인 유기 대사 요소로부터 생산될 수 있습니다.카로티노이드를 생성하는 것으로 알려진 절지동물은 [2][3][4]진딧물과 곰팡이로부터 능력과 유전자를 얻은 거미 진드기뿐이다.그것은 또한 흰파리의 [5]내생균에 의해 생성된다.식단에서 나오는 카로티노이드는 [1]동물의 지방조직에 저장되며, 육식동물만이 동물성 지방으로부터 이 화합물을 얻는다.인간의 식생활은 식사 [6]중 지방과 함께 섭취하면 카로티노이드의 흡수가 향상된다.카로티노이드가 함유된 채소를 기름으로 조리하고 채소를 채썰면 카로티노이드의 생물학적 [1][6][7]가용성이 높아진다.
1,100개 이상의 알려진 카로티노이드가[8] 있으며, 두 가지 등급으로 더 분류될 수 있습니다, 크산토필과 카로틴은 순수한 탄화수소로 [1]산소를 포함하지 않습니다.모두 테트라테펜의 유도체로, 8개의 이소프렌 분자에서 생성되며 40개의 탄소 원자를 포함하고 있습니다.일반적으로 카로티노이드는 400~550나노미터의 파장을 흡수한다.이로 인해 화합물이 노란색, 주황색 또는 빨간색으로 짙게 변합니다.카로티노이드는 나무 [1]종들의 약 15-30%의 가을 잎 색깔에서 지배적인 색소이지만, 많은 식물 색깔, 특히 빨강과 보라색은 폴리페놀 때문이다.
카로티노이드는 식물과 조류에서 두 가지 중요한 역할을 합니다: 그들은 광합성에 사용하기 위해 빛 에너지를 흡수하고, 그들은 비광화학 [9]담금질을 통해 광보호 기능을 제공합니다.치환되지 않은 베타 이오논 고리(β-카로틴, α-카로틴, β-크립톡산틴 및 β-카로틴 포함)를 포함하는 카로티노이드는 비타민 A 활성을 가지고 있다.눈에는 루테인, 메소-제아크산틴, 제아크산틴이 황반 색소로 존재하며 2016년 현재 시각 기능의 중요성이 임상 연구 [1][10]중에 남아있다.
생합성
카로티노이드의 기본 구성 요소는 이소펜테닐이인산(IPP)과 디메틸알릴이인산(DMAPP)[11]입니다.이 두 이소프렌 이성질체는 이성질체 [12]합성에 사용되는 생물학적 경로에 따라 다양한 화합물을 생성하기 위해 사용됩니다.식물은 IPP 생성을 위해 세포질 메발론산 경로(MVA)와 플라스티드 메틸에리톨 4-인산 경로(MEP)[11]의 두 가지 다른 경로를 사용하는 것으로 알려져 있다.동물에서 콜레스테롤의 생산은 MPA를 [12]사용하여 IPP와 DMAPP를 만드는 것으로 시작됩니다.카로티노이드 생산 공장에서는 IPP와 DMAPP를 [11]생성하기 위해 MEP를 사용합니다.MEP 경로에서는 IPP가 5:1로 혼합됩니다.DMAPP.[12] IPP 및 DMAPP는 여러 가지 반응을 거쳐 주요 카로티노이드 전구체인 제라닐게라닐이인산(GGPP)을 생성한다.GGPP는 카로티노이드 생합성 [11]경로 내에서 다양한 단계를 거침으로써 카로틴 또는 잔토필로 전환될 수 있다.
MEP 경로
광합성의 중간체인 글리세린알데히드 3-인산 및 피루브산을 촉매 DXP 합성효소(DXS)를 이용하여 디옥시-D-자일로오스 5-인산(DXP)으로 변환한다.DXP 환원 이소머라아제는 NADPH의 [12]존재 하에서 DXP 내의[11] 분자를 환원 및 재배열하여 MEP를 [11]형성하고 다음으로 MEP는 CTP를 통해 4-(시티딘 5'-디포스포)-2-C-메틸-D-에리트리톨(CDP-ME)로 변환한다.이어서 ATP의 존재 하에서 CDP-ME를 2-포스포-4-(시티딘 5'-디포스포)-2-C-메틸-D-에리트리톨(CDP-ME2P)로 변환한다.CDP-ME2P로의 전환은 CDP-ME 키나제 효소에 의해 촉매된다.다음으로 CDP-ME2P를 2-C-메틸-D-에리트리톨 2,4-시클로디인산(MECDP)으로 변환한다.이 반응은 MECDP 합성효소가 반응을 촉매하고 CMP가 CDP-ME2P 분자로부터 제거될 때 발생합니다.MECDP는 플라보독신 및 NADPH의 존재 하에서 HMBDP 합성효소를 통해 (e)-4-히드록시-3-메틸부트-2-en-1-일 이인산(HMBDP)으로 변환된다.HMBDP 환원효소에 의해 페레독신 및 NADPH의 존재 하에서 HMBDP는 IPP로 환원된다.HMBPD 합성효소와 환원효소를 포함하는 마지막 두 단계는 완전히 혐기적인 환경에서만 발생할 수 있습니다.IPP는 IPP 이성질화효소를 [12]통해 DMAPP로 이성화할 수 있습니다.
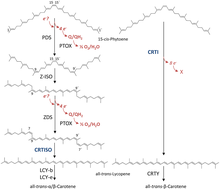
카로티노이드생합성경로
2개의 GGPP 분자는 피토엔 합성효소(PY)를 통해 응축되어 피토엔의 15-cison 이성질체를 형성한다.싸이는 스쿠알렌/피토엔 합성효소 계열에 속하며 스테로이드 생합성에 관여하는 스쿠알렌 합성효소와 상동한다.피토엔의 모든 트랜스 리코펜으로의 후속 전환은 유기체에 따라 달라진다.박테리아와 곰팡이는 촉매 작용을 위해 단일 효소인 박테리아 피토엔 불포화효소(CTI)를 사용합니다.그러나 식물과 시아노박테리아는 이 [13]과정을 위해 네 가지 효소를 사용한다.이들 효소 중 첫 번째는 식물성 피토엔 불포화효소로서 탈수소화에 의해 15-cis-phytoene에 2개의 추가 이중 결합을 도입하고 트랜스로부터 시스로의 기존 이중 결합 중 2개를 이성질화하여 9,15,9'-트리-cis-γ-카로틴을 생성한다.이 트리-시스-γ-카로텐의 중심 이중결합은 제타-카로텐 이성질화효소 Z-ISO에 의해 이성화되며, 결과적으로 생성된 9,9'-di-시스-γ-카로텐은 γ-카로텐 불포화효소(ZDS)에 의해 다시 탈수소된다.이것은 다시 두 개의 이중 결합을 도입하여 7,9,7',9'-테트라시스-리코펜을 생성한다.카로티노이드 이성질화효소인 CRTISO는 환원 FAD의 존재 하에서 시스-리코펜을 전 트랜스 리코펜으로 전환하기 위해 필요하다.
이 전 트랜스 리코펜은 환화된다; 환화는 카로티노이드 다양성을 발생시키며, 이는 말단 그룹에 따라 구별될 수 있다.각각 다른 효소(리코펜 베타-사이클라아제[베타-LCY] 또는 리코펜 엡실론-사이클라아제[엡실론-LCY])에 의해 생성되는 베타 고리 또는 엡실론 고리가 있을 수 있다. α-카로틴은 전 트랜스 리코펜이 엡실론-LCY와 첫 번째 반응을 거친 후 베타-CARY와 두 번째 반응을 보일 때 생성된다.β-LCY. α-와 β-카로틴은 식물 광계에서 가장 흔한 카로티노이드이지만, 그것들은 여전히 베타-히드로라아제와 엡실론-히드로라아제를 사용하여 크산토필로 [11]더 변할 수 있고, 다양한 크산토필로 이어질 수 있다.
규정
DXS와 DXR은 모두 속도 결정 효소로 카로티노이드 수치를 [11]조절할 수 있는 것으로 알려져 있다.이것은 DXS와 DXR이 유전적으로 과도하게 발현된 실험에서 발견되었고,[11] 결과 묘목에서 카로티노이드 발현을 증가시켰다.또한 J-단백질(J20) 및 열충격단백질(Hsp70) 샤페론은 DXS 활성의 전사 후 조절에 관여하는 것으로 생각되며, J20 활성이 결함이 있는 돌연변이가 비활성 DXS 단백질을 [14]축적하면서 DXS 효소 활성을 감소시킨다.조절은 또한 합성에 필요한 효소와 단백질에 영향을 미치는 외부 독소에 의해 야기될 수 있다.케토클로마존은 토양에 도포된 제초제에서 추출되어 DXP 합성효소에 [12]결합합니다.이는 DXP 합성효소를 억제하여 DXP 합성을 방해하고 MEP 경로를 [12]정지시킵니다.이 독소의 사용은 오염된 [12]토양에서 자란 식물에서 낮은 수준의 카로티노이드를 유도한다.포스미도마이신은 효소와 유사한 구조 때문에 [12]DXP 환원 이성질화효소의 경쟁적 억제제이다.상기 항생제를 도포하면 DXP의 감소를 방지하고 MEP 경로를 다시 정지한다.[12]
구조 및 기능
카로티노이드의 구조는 광합성, 광보호, 식물 착색, 그리고 세포 신호를 포함한 생물학적 능력을 허용합니다.
카로티노이드의 일반적인 구조는 9-11개의 이중 결합으로 구성되고 고리로 끝날 수 있는 폴리엔 사슬이다.이러한 켤레 이중 결합의 구조는 높은 환원 잠재력, [15]즉 분자 전체에 전자를 전달하는 능력으로 이어진다.카로티노이드는 1) 카로티노이드에서 클로로필로의 싱글릿 에너지 전달과 2) 클로로필에서 카로티노이드로의 트리플렛 에너지 전달의 두 가지 방법 중 하나로 들뜸 에너지를 전달할 수 있습니다.싱글릿-싱글릿 에너지 전달은 낮은 에너지 상태 전달이며 광합성 [16]중에 사용됩니다.폴리엔 꼬리의 길이는 광합성 범위에서 빛 흡수를 가능하게 합니다; 일단 에너지를 흡수하면, 그것은 흥분하게 되고, 광합성을 [15]위해 들뜬 전자를 엽록소로 전달합니다.트리플렛-트리플릿 전달은 더 높은 에너지 상태이며 [16]광보호에 필수적입니다.빛은 광합성을 하는 동안 해로운 종을 만들어내는데, 가장 해로운 것은 활성산소종이다.이러한 높은 에너지 ROS가 엽록소에서 생성됨에 따라 에너지는 카로티노이드의 폴리엔 꼬리로 전달되고 카로티노이드에 [15]대해 가장 균형 잡힌 상태(최저 에너지 상태)를 찾기 위해 카로티노이드 결합 사이에서 전자가 이동하는 일련의 반응을 겪습니다.
카로티노이드의 길이는 또한 식물이 흡수할 빛의 파장을 결정하기 때문에 식물 색채에 역할을 합니다.흡수되지 않은 파장은 반사되어 [15]식물의 색으로 보입니다.따라서, 다른 종들은 다른 [15]색깔들을 흡수하고 반사할 수 있도록 다른 꼬리 길이를 가진 카로티노이드를 포함할 것이다.
카로티노이드는 또한 다른 종류의 세포 [16]신호 전달에 참여합니다.그들은 식물의 성장, 종자의 휴면, 배아 성숙과 발아, 세포 분열과 신장, 꽃의 성장, 스트레스 [17]반응을 조절하는 압시시산의 생산을 신호로 전달할 수 있다.
특성.

카로티노이드는 테트라테페노이드의 범주에 속합니다(즉, 각각 10개의 탄소 원자를 포함하는 4개의 테르펜 단위에서 40개의 탄소 원자를 포함합니다).구조적으로, 카로티노이드는 때로 고리에 의해 종단되는 폴리엔 탄화수소 사슬의 형태를 취하며 추가적인 산소 원자가 부착될 수도 있고 부착되지 않을 수도 있다.
- 루테인이나 제아산틴과 같이 산소를 포함한 분자를 가진 카로티노이드는 크산토필로 알려져 있다.
- α-카로틴, β-카로틴, 리코펜과 같은 비산소화(산소가 없는) 카로티노이드는 카로틴으로 알려져 있다.카로틴은 일반적으로 탄소와 수소(즉, 탄화수소)만을 포함하고 있으며 불포화 탄화수소의 하위 등급에 속합니다.
옅은 노란색에서 밝은 오렌지색, 짙은 빨강색 등 다양한 색깔들은 그들의 구조와 직접적으로 연관되어 있다.크산토필은 종종 노란색이기 때문에 그들의 계급명은 노란색이다.이중 탄소-탄소 결합은 결합이라고 불리는 과정에서 서로 상호작용을 하는데, 이것은 분자의 전자가 분자의 이러한 영역들을 자유롭게 이동할 수 있게 해줍니다.켤레 이중 결합의 수가 증가함에 따라 켤레 시스템과 관련된 전자는 움직일 공간이 더 많아지고 상태를 변화시키기 위해 더 적은 에너지를 필요로 한다.이것은 분자가 흡수하는 빛의 에너지 범위를 감소시킨다.가시 스펙트럼의 긴 끝에서 더 많은 파장의 빛이 흡수됨에 따라 화합물은 점점 더 붉은 빛을 띠게 됩니다.
카로티노이드는 보통 지방산과 같이 긴 불포화 지방족 사슬의 존재로 인해 친유성이다.사람과 다른 유기체에서 이러한 지용성 비타민의 생리적인 흡수는 지방과 담즙염의 [1]존재에 직접적으로 의존한다.
식품
호박, 고구마, 당근 그리고 겨울 호박에서 발견되는 베타카로틴은 오렌지-노란색의 [1]원인이 된다.말린 당근은 레티놀 활성 당량(프로비타민 A 당량)[18]으로 측정되는 100그램 당 가장 많은 양의 카로틴을 함유하고 있습니다.베트남 가크 열매는 카로티노이드 리코펜의 [19]가장 높은 농도를 가지고 있습니다.비록 초록색이지만, 케일, 시금치, 콜라드 그린, 그리고 순무 채소는 베타카로틴을 [1]상당히 많이 함유하고 있습니다.플라밍고의 식단은 카로티노이드가 풍부하여 이 [20]새들의 오렌지색 깃털을 전해준다.
형태학
카로티노이드는 주로 세포핵 바깥에 다른 세포질 기관, 지질 방울, 세포질 및 과립에 위치합니다.그것들은 조류 [21]세포의 라만 분광법에 의해 시각화되고 정량화 되었다.
트랜스-리코펜에 대한 모노클로널 항체의 개발로 이 카로티노이드를 다른 동물과 인간 [22][23]세포에 위치시킬 수 있었다.
산소화
카로티노이드는 생물학적 산소화에 중요한 역할을 한다.식물 세포에서 그들은 광합성을 [24][25]통해 방출되는 분자 산소의 막 통과 수송의 제어에 관여한다.
동물에서 카로티노이드는 산소를 운반, 저장, 신진대사에 있어 중요한 역할을 한다.
운송
카로티노이드는 소수성이고 전형적으로 혈장 지질과 세포 지질 구조에 존재한다.[26]분자 산소 또한 소수성 분자이기 때문에, 지질은 수성 [27][28]매체에서보다 O 용해도에 더 유리한2 환경을 제공합니다.하전지질 과산화물 및 기타 산화유도체를 생성하는 유리방사성 손상으로부터 지질 보호함으로써 카로티노이드는 지질단백질 및 세포지질 구조의 결정구조 및 소수성을 지지하고, 따라서 산소용해성과 [29][30]그 확산성을 지지한다.
보관소
카로티노이드는 1973년 V.N. Karnaukhov에 [28]의해 세포 내 산소 저장에 관여할 수 있다는 것이 처음 제안되었다.나중에 카로티노이드는 또한 추가적인 [31]분자 산소를 저장할 수 있는 세포 내 지질 방울의 형성을 자극할 수 있다는 것이 발견되었다.카로티노이드의 이러한 특성은 동물들이 환경 스트레스, 높은 고도, 세포 내 감염 그리고 다른 저산소 [32][33]조건에 적응하도록 도와줍니다.
호흡
카로티노이드는, 산소 확산과 혈장 리포단백질의 산소 운반 능력을 증가시킴으로써, 신체 조직으로의 산소 공급을 자극할 수 있습니다.이것은 조직과 세포 산소화를 개선하고 미토콘드리아의 [34][35]성장과 호흡을 촉진합니다.
시너제틱 모달리티
산소는 비타민 D3와 같은 프로드루그와 프로호르몬의 대사 활성화에 중요한 히드록실화를 포함한 많은 세포 내 반응에서 필요합니다. 카로티노이드는 세포 내 산소화를 지원할 뿐만 아니라 이러한 분자의 효과도 향상시킬 수 있습니다.
카로티노이드는 다른 분자와 물리적 복합체를 형성할 수 있다.소수성 분자의 경우 이것은 자가 조립이 될 수 있다.양친매성 또는 친수성 화합물의 경우 라이코좀 또는 초임계2 CO 기술 또는 다른 방법을 사용해야 [35]][36]합니다.이러한 복합체의 카로티노이드는 조직의 산소화를 지지하고 촉진하는 새로운 형태를 제공하며, 이것은 다른 영양분자나 [36][37]제약분자의 치료 목적에 상승적으로 이롭습니다.
생리적 영향
식품에서 카로티노이드 소비와 임상 결과 사이의 상관관계를 모색하는 역학 연구의 검토는 다양한 결론에 도달했다.
- 카로티노이드가 전립선암을 예방할 수 있는지 여부를 조사하는 또 다른 2015년 리뷰에서는 여러 연구에서 카로티노이드가 풍부한 식단 간의 상관관계가 보호 효과가 있는 것으로 나타났지만, 이것이 [39]카로티노이드 그 자체 때문인지 여부를 결정하는 증거는 부족하다는 것을 발견했다.
- 2014년 리뷰에서는 카로티노이드와 비타민 A가 많이 함유된 음식을 섭취하는 것과 파킨슨병에 [40]걸릴 위험 사이에는 아무런 상관관계가 없는 것으로 나타났다.
- 또 다른 2014년 리뷰에서는 카로티노이드의 식사 섭취와 유방암에 [41]걸릴 위험성에 대한 연구에서 상반되는 결과가 발견되지 않았다.
카로티노이드는 또한 머리카락, 피부, 그리고 눈에서 발견되는 짙은 갈색 색소 멜라닌의 중요한 구성요소이다.멜라닌은 고에너지 빛을 흡수하고 이러한 장기를 세포 내 손상으로부터 보호합니다.
- 몇몇 연구는 고카로티노이드 식단이 [42][43][44]피부의 질감, 선명도, 색상, 힘, 그리고 탄력에 긍정적인 영향을 미치는 것을 관찰했다.
- 1994년 연구는 높은 카로티노이드 식단이 눈의 피로 증상을 줄이고 야간 [45][46]시력을 향상시키는데 도움을 준다고 언급했다.
인간과 다른 동물들은 대부분 카로티노이드를 합성할 수 없고, 그들의 식단을 통해 카로티노이드를 얻어야 한다.카로티노이드는 동물들에게 흔하고 종종 장식적인 특징이다.예를 들어, 연어의 분홍색, 조리된 바닷가재의 붉은색, 일반적인 벽 도마뱀의 노란 형태 비늘은 카로티노이드 [47][citation needed]때문이다.카로티노이드는 생리적, 화학적 특성을 감안할 때 개개인의 건강의 가시적인 지표로 사용될 수 있고, 따라서 잠재적 [48]짝을 선택할 때 동물에 의해 사용되기 때문에 관상적 특징(극단적인 예로는 복새 참조)에 사용된다고 제안되었다.
식물색

가장 일반적인 카로티노이드는 리코펜과 비타민 A 전구체 β-카로틴을 포함한다.식물에서 크산토필 루테인은 가장 풍부한 카로티노이드이며 노화와 관련된 눈병을 예방하는 역할을 현재 [10]연구 중이다.루테인과 성숙한 잎에서 발견되는 다른 카로티노이드 색소는 클로로필의 마스킹 존재 때문에 종종 명확하지 않다.가을 단풍처럼 엽록소가 없을 때는 카로티노이드의 노란색과 오렌지가 지배적이다.같은 이유로, 카로티노이드 색상은 엽록소의 소멸로 인해 탈이 벗겨진 후 익은 과일에 종종 우세합니다.
카로티노이드는 히코리, 애쉬, 단풍나무, 노란 포플러, 아스펜, 자작나무, 검은 체리, 무화나무, 목화나무, 사사프라, 그리고 올더와 같은 특정 단단한 나무 종들의 낙엽을 물들이는 선명한 노란색과 오렌지의 원인이 됩니다.카로티노이드는 나무 [49]종들의 약 15-30%의 가을 잎 색소의 지배적인 색소이다.하지만, 가을 단풍을 장식하는 붉은색, 보라색, 그리고 그들의 혼합된 조합은 보통 안토시아닌이라고 불리는 세포에 있는 다른 색소 그룹으로부터 옵니다.카로티노이드와는 달리, 이 색소들은 성장기 내내 잎에 존재하지 않지만,[50] 여름이 끝날 무렵에 활발하게 생산된다.
새의 색채와 성별 선택
식이 카로티노이드와 그 대사 유도체는 [51]조류에서 밝은 노란색에서 빨간색으로 변색되는 원인이 됩니다.연구에 따르면 약 2956종의 현대 조류들이 카로티노이드 색채를 나타내며, 외부 색채를 위해 이탤릭체를 사용하는 능력은 조류 진화 [52]역사에서 여러 번 독립적으로 진화한 것으로 추정됩니다.카로티노이드 색상은 높은 수준의 성적 이형성을 나타내는데, 이는 수컷 새들이 같은 [53]종의 암컷들보다 더 선명한 색채를 보이는 경향이 있다는 것을 의미합니다.
이러한 차이는 여성의 [54][53]선호도에 따라 남성의 노란색과 빨간색이 선택되기 때문에 발생한다.많은 종류의 조류에서 암컷은 수컷보다 새끼를 기르는 데 더 많은 시간과 자원을 투자한다.따라서 암컷 새들은 반드시 양질의 짝을 신중하게 선택해야 한다.현재의 문헌은 활발한 카로티노이드 착색이 면역 기능과 산화 [55][56][57]스트레스에 직접적인 영향을 미치거나 카로티노이드 대사 경로와 세포 [58][59]호흡을 위한 경로 사이의 연결을 통해 남성의 질과 상관관계가 있다는 이론을 뒷받침한다.
성적 신호
카로티노이드에 기초한 색채와 같이 성적으로 선택되는 특징들은 표현형과 유전적 품질의 정직한 신호이기 때문에 일반적으로 진화한다고 여겨진다.예를 들어, 큰조류의 수컷들 중에서, 화려하게 장식된 수컷들은 카로티노이드 항산화제의 [60]증가로 인한 산화 스트레스로부터 더 잘 보호되는 정자를 생산한다.그러나 매력적인 남성 착색은 남성 품질의 잘못된 신호일 수 있다는 증거도 있습니다.스틱백 물고기 중에서 카로티노이드 착색제 때문에 암컷에게 더 매력적인 수컷은 생식세포에 [61]카로티노이드를 적게 할당하는 것으로 보인다.카로티노이드는 유익한 항산화제이기 때문에, 생식 세포에 대한 그들의 낮은 할당은 이러한 [61]세포에 대한 산화적 DNA 손상을 증가시킬 수 있습니다.따라서, 암컷 스틱백은 더 붉은색을 선택함으로써 번식력과 그들의 자손의 생존 가능성을 위태롭게 할 수 있지만, 정자의 질이 떨어지는 더 나쁜 파트너를 선택할 수 있습니다.
아로마 케미컬
이오논, 다마스콘, 다마세논과 같은 카로티노이드 분해 제품도 향수와 향기 산업에서 널리 사용되는 중요한 향기 화학 물질이다.β-다마세논과 β-이오논은 모두 장미 증류액의 농도가 낮지만 꽃의 냄새를 유발하는 주요 화합물이다.사실, 홍차, 숙성된 담배, 포도, 그리고 많은 과일들에 존재하는 달콤한 꽃 냄새는 카로티노이드 분해로 인한 방향족 화합물 때문이다.
질병
몇몇 카로티노이드는 박테리아에 의해 산화 면역 공격으로부터 자신들을 보호하기 위해 생성된다.황색포도상구균의 몇몇 변종에게 그들의 이름을 주는 황색소는 포도상구균이라고 불리는 카로티노이드이다.이 카로티노이드는 숙주 [62]면역 체계에 의해 사용되는 활성 산소 종에 의해 미생물이 죽음을 피할 수 있도록 돕는 항산화 작용을 하는 독성 인자입니다.
자연발생 카로티노이드
- 탄화수소
- 알코올
- 알록산틴
- 박테리어우베린 2,2'-비스(3-히드록시-3-메틸부틸)-3,4,3',4'-테트라히드로-1,2,1',2'-테트라히드로-1,1'-디올
- 신시아산틴
- 펙테녹산틴
- 크립토모낙산틴(3R,3'R)-7,8,7',8'-테트라데히드로β,β-카로틴-3,3'-디올
- 크러스타크산틴β,-카로틴-3,4,3',4'-테트롤
- 가자니아크산틴(3R)-5'-cis-β,γ-카로텐-3-ol
- OH-클로로박텐1',2'-디히드로프,γ-카로텐-1'-ol
- 로록산틴β,γ-카로틴-3,19,3'-트리올
- 루테인(3R, 3′R, 6rR)-β, β-카로틴-3, 3--디올
- 리코산틴γ,γ-카로텐-16-ol
- 로도핀1,2-디히드로γ,γ-카로텐-l-ol
- 로도피놀 a.k.a.워밍올 13-cis-1,2-디히드로-γ-카로틴-1,20-디올
- 사프로산틴3',4'-디데히드로-1',2'-디히드로β,γ-카로틴-3,1'-디올
- 제아산틴
- 글리코사이드류
- 에테르
- 로도비브린1'-메톡시-3', 4'-디데히드로-1, 2, 1', 2'-테트라히드로-γ-카로텐-1-ol
- 스페로이덴1-메톡시-3,4-디데히드로-1,2,7',8'-테트라히드로-γ-카로틴
- 에폭시드
- 디아디녹산틴 5,6-에폭시-7', 8'-디데히드로-5,6-디히드로-카로틴-3,3-디올
- 루테옥산틴 5,6:5',8'-디폭시-5,6,5',8'-테트라히드로β,β-카로틴-3,3'-디올
- 뮤타톡산틴
- 시트로크산틴
- Zeaxantin franoxide 5,8-Epoxy-5,8-dihro-β,β-카로틴-3,3'-디올
- 네오크롬5',8'-에폭시-6,7-디데히드로-5,6,5',8'-테트라히드로β,β-카로틴-3,5,3'-트리올
- 폴리아크롬
- 트롤리크롬
- 보케리아크산틴5',6'-에폭시-6,7-디데히드로-5,6',5'-테트라히드로β,β-카로틴-3,5,19,3'-테트롤
- 알데하이드
- 로도피날
- 워밍온13-cis-1-히드록시-1, 2-디히드로-γ-카로텐-20-al
- 토룰라호디날데히드3',4'-디데히드로β,γ-카로텐-16'-알
- 산 및 산 에스테르
- 토룰라호딘3',4'-디데히드로β,γ-카로텐-16'-oic산
- 트룰라호딘메틸에스테르메틸3',4'-디데히드로β,γ-카로텐-16'-오트
- 케톤류
- 아스타센
- 아스타산틴
- 칸탁산틴[63] A.K.A.아프니킨, 클로렐락산틴β,β-카로틴-4,4'-디온
- 캡산틴(3R,3'S,5'R)-3,3'-디히드록시β,γ-카로텐-6'-온
- 캡소루빈(3S,5R,3'S,5'R)-3,3'-디히드록시-γ-카로틴-6,6'-디온
- 크립토캅신(3'R, 5'R)-3'-히드록시β,γ-카로텐-6'-온
- 2,2'-디케토스피릴옥산틴 1,1'-디메톡시-3,4,3',4'-테트라히드로-1,2,1',2'-테트라히드로-γ-카로틴-2,2'-디온
- 에키네논β,β-카로텐-4-온
- 3'-히드록시케논
- 플렉시산틴 3,1'-디히드록시-3', 4'-디드히드로-1', 2'-디히드로β, γ-카로텐-4-온
- 3-OH-칸탁산틴 a.k.a.아도니루빈 a.k.a.페니콕산틴3-히드록시β,β-카로틴-4,4'-디온
- 히드록시페리오데논1'-히드록시-1-메톡시-3,4-디데히드로-1,2,1',2',7',8'-헥사히드로-α-카로텐-2-온
- 옥케논1'-메톡시-1',2'-디히드로-c,γ-카로텐-4'-온
- 펙테놀론 3,3'-디히드록시-7', 8'-디데히드로β, β-카로텐-4-온
- 페니코논 a.k.a.데히드로니루빈 3-히드록시-2, 3-디데히드로β,β-카로틴-4,4'-디온
- 페니캅테론β,γ-카로텐-4-온
- 루빅산톤3-히드록시β,γ-카로텐-4'-온
- 시포낙산틴 3,19,3'-트리히드록시-7,8-디히드로β,γ-카로텐-8-온
- 알코올 에스테르
- 아스타세인 3,3'-비스팔미토일록시-2,3,2'-테트라디하이드로β,β-카로틴-4,4'-디온 또는 3,3'-디히드록시-2,3,2'-테트라디하이드로β,β-카로틴-4,4'-디온디온산염
- 푸콕산틴3'-아세톡시-5,6-에폭시-3,5'-디히드록시-6',7'-디데히드로-5,6'-헥사히드로β,β-카로텐-8-온
- 이소푸콕산틴3'-아세톡시-3,5,5'-트리히드록시-6',7'-디데히드로-5,8,5',6'-테트라히드로β,β-카로텐-8-온
- 물리학자
- 시폰인 3,3'-디히드록시-19-로록시-7,8-디히드로-β,γ-카로텐-8-온 또는 3,19,3'-트리히드록시-7,8-디히드로-β,γ-카로텐-8-온19-로레이트
- 아포카로테노이드
- β-Apo-2'-카로테날 3', 4'-디데히드로-2'-아포-b-카로텐-2'-al
- 아포-2-리코펜탈
- 아포-6'-리코펜탈 6'-아포이카로텐 6'-al
- 아자프리날데히드 5,6-디히드록시-5,6-디히드로-10'-아포-β-카로텐-10'-알
- 빅신6'-메틸수소9'-cis-6,6'-디아포카로틴-6,6'-디오네이트
- 시트라낙산틴 5', 6'-디히드로-5'-아포-β-카로텐-6'-온 또는 5'-디히드로-5'-아포-18'-노르-β-카로텐-6'-온 또는 6'-메틸-6'-아포-β-카로텐-6'-온
- 크로세틴 8,8'-디아포-8,8'-카로텐디오산
- 크로세틴세미알데히드8'-옥소-8,8'-디아포-8-카로텐산
- 크로신 디젠티오비오실 8,8'-디아포-8,8'-카로텐디오에이트
- 홉킨시아산틴 3-히드록시-7,8-디데히드로-7',8'-디히드로-7'-아포-b-카로틴-4,8'-디온 또는 3-히드록시-8'-메틸-7,8-디데히드로-8'-아포-브로틴-4,8'-디온
- 메틸아포-6'-리코페노에이트메틸6'-아포-y-카로텐-6'-오에이트
- 파라센트론 3,5-디히드록시-6,7-디드히드로-5,6,7',8'-테트라히드로-7'-아포-b-카로텐-8'-one 또는 3,5-디히드로-5,6-디드로-5,6-아포-8'-카로톤
- 신탁산틴7',8'-디히드로-7'-아포-b-카로텐-8'-온 또는 8'-메틸-8'-아포-b-카로텐-8'-온
- 노르카로테노이드 및 세코카로테노이드
- 악티니오에틸린 3,3'-비스실록시-2,2'-디노르-b,b-카로틴-4,4'-디온
- β-카로테논 5,6:5',6'-디세코-b,b-카로텐-5,6',6'-테트론
- 페리디닌3'-아세톡시-5,6-에폭시-3,5'-디히드록시-6',7'-디데히드로-5,6'-테트라히드로-12',13'-20'-트리노르-b,b-카로텐-19,11-올라이드
- 피록산티놀 5,6-에폭시-3,3'-디히드록시-7',8'-디데히드로-5,6-디히드로-12',13',20'-트리노르-b,b-카로텐-19,11-올라이드
- 세미α-카로테논 5,6-세코-b, e-카로텐 5,6-디온
- 반β-카로테논 5,6-seco-b, b-카로텐-5,6-디온 또는 5',6'-seco-b,b-카로텐-5',6'-디온
- 트리파시아산틴3-히드록시세미-b-카로테논3'-히드록시-5,6-세코-b,b-카로텐-5,6-디온 또는 3-히드록시-5',6'-세코-b,b-카로텐-5',6'-디온
- 레트로카로테노이드 및 레트로아포카로테노이드
- 고등 카로티노이드
- 노아프레녹산틴 2-(4-히드록시-3-메틸-2-부테닐)-7', 8', 11', 12'-테트라히드로-e, y-카로틴
- 데카프레녹산틴2,2'-비스(4-히드록시-3-메틸-2-부테닐)-e,e-카로틴
- C.p. 450 2-[4-히드록시-3-(히드록시메틸)-2-부테닐]-2'-(3-메틸-2-부테닐)-b,b-카로틴
- C.p. 473 2'-(4-히드록시-3-메틸-2-부테닐)-2-(3-메틸-2-부테닐)-3', 4'-디데히드로-l', 2'-디히드로β, γ-카로텐-1'-ol
- 박테리어우베린 2,2'-비스(3-히드록시-3-메틸부틸)-3,4,3',4'-테트라히드로-1,2,1',2'-테트라히드로-1,1'-디올
「 」를 참조해 주세요.
- 식품 내 식물 화학 물질 목록
- 카로티노이드의 생합성을 담당하는 유전자 클러스터인 CRT(유전자학)
- E 번호 E100 – E199 (컬러)
- 식물화학
레퍼런스
- ^ a b c d e f g h i j "Carotenoids". Micronutrient Information Center, Linus Pauling Institute, Oregon State University. 1 August 2016. Retrieved 17 April 2019.
- ^ Moran NA, Jarvik T (2010). "Lateral transfer of genes from fungi underlies carotenoid production in aphids". Science. 328 (5978): 624–7. Bibcode:2010Sci...328..624M. doi:10.1126/science.1187113. PMID 20431015. S2CID 14785276.
- ^ Boran Altincicek; Jennifer L. Kovacs; Nicole M. Gerardo (2011). "Horizontally transferred fungal carotenoid genes in the two-spotted spider mite Tetranychus urticae". Biology Letters. 8 (2): 253–257. doi:10.1098/rsbl.2011.0704. PMC 3297373. PMID 21920958.
- ^ Nováková E, Moran NA (2012). "Diversification of genes for carotenoid biosynthesis in aphids following an ancient transfer from a fungus". Mol Biol Evol. 29 (1): 313–23. doi:10.1093/molbev/msr206. PMID 21878683.
- ^ Sloan DB, Moran NA (2012). "Endosymbiotic bacteria as a source of carotenoids in whiteflies". Biol Lett. 8 (6): 986–9. doi:10.1098/rsbl.2012.0664. PMC 3497135. PMID 22977066.
- ^ a b Mashurabad, Purna Chandra; Palika, Ravindranadh; Jyrwa, Yvette Wilda; Bhaskarachary, K.; Pullakhandam, Raghu (3 January 2017). "Dietary fat composition, food matrix and relative polarity modulate the micellarization and intestinal uptake of carotenoids from vegetables and fruits". Journal of Food Science and Technology. 54 (2): 333–341. doi:10.1007/s13197-016-2466-7. ISSN 0022-1155. PMC 5306026. PMID 28242932.
- ^ Rodrigo, María Jesús; Cilla, Antonio; Barberá, Reyes; Zacarías, Lorenzo (2015). "Carotenoid bioaccessibility in pulp and fresh juice from carotenoid-rich sweet oranges and mandarins". Food & Function. 6 (6): 1950–1959. doi:10.1039/c5fo00258c. PMID 25996796.
- ^ Yabuzaki, Junko (2017-01-01). "Carotenoids Database: structures, chemical fingerprints and distribution among organisms". Database. 2017 (1). doi:10.1093/database/bax004. PMC 5574413. PMID 28365725.
- ^ Armstrong GA, Hearst JE (1996). "Carotenoids 2: Genetics and molecular biology of carotenoid pigment biosynthesis". FASEB J. 10 (2): 228–37. doi:10.1096/fasebj.10.2.8641556. PMID 8641556. S2CID 22385652.
- ^ a b Bernstein, P. S.; Li, B; Vachali, P. P.; Gorusupudi, A; Shyam, R; Henriksen, B. S.; Nolan, J. M. (2015). "Lutein, Zeaxanthin, and meso-Zeaxanthin: The Basic and Clinical Science Underlying Carotenoid-based Nutritional Interventions against Ocular Disease". Progress in Retinal and Eye Research. 50: 34–66. doi:10.1016/j.preteyeres.2015.10.003. PMC 4698241. PMID 26541886.
- ^ a b c d e f g h i Nisar, Nazia; Li, Li; Lu, Shan; Khin, Nay Chi; Pogson, Barry J. (2015-01-05). "Carotenoid Metabolism in Plants". Molecular Plant. Plant Metabolism and Synthetic Biology. 8 (1): 68–82. doi:10.1016/j.molp.2014.12.007. PMID 25578273.
- ^ a b c d e f g h i j KUZUYAMA, Tomohisa; SETO, Haruo (2012-03-09). "Two distinct pathways for essential metabolic precursors for isoprenoid biosynthesis". Proceedings of the Japan Academy. Series B, Physical and Biological Sciences. 88 (3): 41–52. Bibcode:2012PJAB...88...41K. doi:10.2183/pjab.88.41. ISSN 0386-2208. PMC 3365244. PMID 22450534.
- ^ Moise, Alexander R.; Al-Babili, Salim; Wurtzel, Eleanore T. (31 October 2013). "Mechanistic aspects of carotenoid biosynthesis". Chemical Reviews. 114 (1): 164–93. doi:10.1021/cr400106y. PMC 3898671. PMID 24175570.
- ^ Nisar, Nazia; Li, Li; Lu, Shan; ChiKhin, Nay; Pogson, Barry J. (5 January 2015). "Carotenoid Metabolism in Plants". Molecular Plant. 8 (1): 68–82. doi:10.1016/j.molp.2014.12.007. PMID 25578273.
- ^ a b c d e Vershinin, Alexander (1999-01-01). "Biological functions of carotenoids - diversity and evolution". BioFactors. 10 (2–3): 99–104. doi:10.1002/biof.5520100203. ISSN 1872-8081. PMID 10609869. S2CID 24408277.
- ^ a b c Cogdell, R. J. (1978-11-30). "Carotenoids in photosynthesis". Phil. Trans. R. Soc. Lond. B. 284 (1002): 569–579. Bibcode:1978RSPTB.284..569C. doi:10.1098/rstb.1978.0090. ISSN 0080-4622.
- ^ Finkelstein, Ruth (2013-11-01). "Abscisic Acid Synthesis and Response". The Arabidopsis Book / American Society of Plant Biologists. 11: e0166. doi:10.1199/tab.0166. ISSN 1543-8120. PMC 3833200. PMID 24273463.
- ^ "Foods Highest in Retinol Activity Equivalent". nutritiondata.self.com. Retrieved 2015-12-04.
- ^ Tran, X. T.; Parks, S. E.; Roach, P. D.; Golding, J. B.; Nguyen, M. H. (2015). "Effects of maturity on physicochemical properties of Gac fruit (Momordica cochinchinensis Spreng.)". Food Science & Nutrition. 4 (2): 305–314. doi:10.1002/fsn3.291. PMC 4779482. PMID 27004120.
- ^ Yim, K. J.; Kwon, J; Cha, I. T.; Oh, K. S.; Song, H. S.; Lee, H. W.; Rhee, J. K.; Song, E. J.; Rho, J. R.; Seo, M. L.; Choi, J. S.; Choi, H. J.; Lee, S. J.; Nam, Y. D.; Roh, S. W. (2015). "Occurrence of viable, red-pigmented haloarchaea in the plumage of captive flamingoes". Scientific Reports. 5: 16425. Bibcode:2015NatSR...516425Y. doi:10.1038/srep16425. PMC 4639753. PMID 26553382.
- ^ Timlin, Jerilyn A.; Collins, Aaron M.; Beechem, Thomas A.; Shumskaya, Maria; Wurtzel, Eleanore T. (2017-06-14), "Localizing and Quantifying Carotenoids in Intact Cells and Tissues", Carotenoids, InTech, doi:10.5772/68101, ISBN 978-953-51-3211-0, S2CID 54807067, retrieved 2021-03-28
- ^ Tsibezov, Valeriy V.; Bashmakov, Yuriy K.; Pristenskiy, Dmitry V.; Zigangirova, Naylia A.; Kostina, Ludmila V.; Chalyk, Natalya E.; Kozlov, Alexey Y.; Morgunova, Elena Y.; Chernyshova, Marina P.; Lozbiakova, Marina V.; Kyle, Nigel H. (2017). "Generation and Application of Monoclonal Antibody Against Lycopene". Monoclonal Antibodies in Immunodiagnosis and Immunotherapy. 36 (2): 62–67. doi:10.1089/mab.2016.0046. ISSN 2167-9436. PMID 28402743.
- ^ Petyaev, Ivan M.; Zigangirova, Naylia A.; Pristensky, Dmitry; Chernyshova, Marina; Tsibezov, Valeriy V.; Chalyk, Natalya E.; Morgunova, Elena Y.; Kyle, Nigel H.; Bashmakov, Yuriy K. (2018). "Non-Invasive Immunofluorescence Assessment of Lycopene Supplementation Status in Skin Smears". Monoclonal Antibodies in Immunodiagnosis and Immunotherapy. 37 (3): 139–146. doi:10.1089/mab.2018.0012. ISSN 2167-9436. PMID 29901405.
- ^ Siefermann, D.; Yamamoto, H. Y. (1975-01-20). "NADPH and oxygen-dependent epoxidation of zeaxanthin in isolated chloroplasts". Biochemical and Biophysical Research Communications. 62 (2): 456–461. doi:10.1016/s0006-291x(75)80160-4. ISSN 0006-291X. PMID 234228.
- ^ Karnaukhov, V.N. (1990). "Carotenoids: Recent progress, problems and prospects". Comparative Biochemistry and Physiology Part B: Comparative Biochemistry. 95 (1): 1–20. doi:10.1016/0305-0491(90)90241-K. PMID 2184985.
- ^ Gruszecki, Wieslaw I. (2004), Frank, Harry A.; Young, Andrew J.; Britton, George; Cogdell, Richard J. (eds.), "Carotenoids in Membranes", The Photochemistry of Carotenoids, Advances in Photosynthesis and Respiration, Dordrecht: Kluwer Academic Publishers, vol. 8, pp. 363–379, doi:10.1007/0-306-48209-6_20, ISBN 978-0-7923-5942-5, retrieved 2021-03-28
- ^ Bačič, G.; Walczak, T.; Demsar, F.; Swartz, H. M. (1988). "Electron spin resonance imaging of tissues with lipid-rich areas". Magnetic Resonance in Medicine. 8 (2): 209–219. doi:10.1002/mrm.1910080211. PMID 2850439. S2CID 41810978.
- ^ a b Windrem, David A.; Plachy, William Z. (1980). "The diffusion-solubility of oxygen in lipid bilayers". Biochimica et Biophysica Acta (BBA) - Biomembranes. 600 (3): 655–665. doi:10.1016/0005-2736(80)90469-1. PMID 6250601.
- ^ Carotenoids : physical, chemical, and biological functions and properties. John Thomas Landrum. Boca Raton: CRC Press. 2010. ISBN 978-1-4200-5230-5. OCLC 148650411.
{{cite book}}: CS1 유지보수: 기타 (링크) - ^ Petyaev, Ivan M.; Hunt, James V. (1997). "Micellar acceleration of oxygen-dependent reactions and its potential use in the study of human low density lipoprotein". Biochimica et Biophysica Acta (BBA) - Lipids and Lipid Metabolism. 1345 (3): 293–305. doi:10.1016/S0005-2760(97)00005-2. PMID 9150249.
- ^ Zigangirova, Naylia A.; Morgunova, Elena Y.; Fedina, Elena D.; Shevyagina, Natalia V.; Borovaya, Tatiana G.; Zhukhovitsky, Vladimir G.; Kyle, Nigel H.; Petyaev, Ivan M. (2017). "Lycopene Inhibits Propagation of Chlamydia Infection". Scientifica. 2017: 1–11. doi:10.1155/2017/1478625. ISSN 2090-908X. PMC 5602621. PMID 28948060.
- ^ Gordon, Gerald B.; Barcza, Maureen A.; Bush, Marilyn E. (1977). "Lipid Accumulation in Hypoxic Tissue Culture Cells". The American Journal of Pathology. 88 (3): 663–678. ISSN 0002-9440. PMC 2032384. PMID 196505.
- ^ Karnaukhov, V. N; Fedorov, G. G (1977-01-01). "The role of carotenoids and vitamin A in animal adaptation to high altitude". Comparative Biochemistry and Physiology Part A: Physiology. 57 (3): 377–381. doi:10.1016/0300-9629(77)90210-9. ISSN 0300-9629.
- ^ Gainer, John L.; Chisolm, G.M. (1974). "Oxygen diffusion and atherosclerosis". Atherosclerosis. 19 (1): 135–138. doi:10.1016/0021-9150(74)90049-5. PMID 4810465.
- ^ a b Petyaev, Ivan M.; Chalyk, Natalya E.; Klochkov, Victor A.; Pristensky, Dmitry V.; Chernyshova, Marina P.; Kyle, Nigel H.; Bashmakov, Yuriy K. (2018). "Pharmacokinetics and Oxidation Parameters in Volunteers Supplemented with Microencapsulated Docosahexaenoic Acid". International Journal of Applied & Basic Medical Research. 8 (3): 148–154. doi:10.4103/ijabmr.IJABMR_367_17. ISSN 2229-516X. PMC 6082003. PMID 30123743.
- ^ a b Petyaev, Ivan M.; Dovgalevsky, Pavel Y.; Klochkov, Victor A.; Chalyk, Natalya E.; Kyle, Nigel (2012). "Whey protein lycosome formulation improves vascular functions and plasma lipids with reduction of markers of inflammation and oxidative stress in prehypertension". TheScientificWorldJournal. 2012: 269476. doi:10.1100/2012/269476. ISSN 1537-744X. PMC 3541600. PMID 23326213.
- ^ Petyaev, Ivan M.; Dovgalevsky, Pavel Y.; Chalyk, Natalia E.; Klochkov, Victor A.; Kyle, Nigel H. (2019). "Reduction of elevated lipids and low-density lipoprotein oxidation in serum of individuals with subclinical hypoxia and oxidative stress supplemented with lycosome formulation of docosahexaenoic acid". Food Science & Nutrition. 7 (4): 1147–1156. doi:10.1002/fsn3.784. ISSN 2048-7177. PMC 6475726. PMID 31024687.
- ^ Leoncini; Sources, Natural; Head; Cancer, Neck; et al. (Jul 2015). "A Systematic Review and Meta-analysis of Epidemiological Studies". Cancer Epidemiol Biomarkers Prev. 24 (7): 1003–11. doi:10.1158/1055-9965.EPI-15-0053. PMID 25873578. S2CID 21131127.
- ^ Soares Nda, C; et al. (Oct 2015). "Anticancer properties of carotenoids in prostate cancer. A review". Histol Histopathol. 30 (10): 1143–54. doi:10.14670/HH-11-635. PMID 26058846.
- ^ Takeda, A; et al. (2014). "Vitamin A and carotenoids and the risk of Parkinson's disease: a systematic review and meta-analysis". Neuroepidemiology. 42 (1): 25–38. doi:10.1159/000355849. PMID 24356061. S2CID 12396064.
- ^ Chajès, V; Romieu, I (Jan 2014). "Nutrition and breast cancer". Maturitas. 77 (1): 7–11. doi:10.1016/j.maturitas.2013.10.004. PMID 24215727.
- ^ Schagen, SK; et al. (2012). ""Vasiliki A. Zampeli, Evgenia Makrantonaki, Christos C. Zouboulis, "Discovering the link between nutrition and skin aging". Dermatoendocrinol. 4 (3): 298–307. doi:10.4161/derm.22876. PMC 3583891. PMID 23467449.
- ^ Pappas, A (2009). "The relationship of diet and acne". Dermatoendocrinol. 1 (5): 262–267. doi:10.4161/derm.1.5.10192. PMC 2836431. PMID 20808513.
- ^ Zhi Foo, Y; Rhodes, G; Simmons, LW (2017). "The carotenoid beta-carotene enhances facial color, attractiveness and perceived health, but not actual health, in humans". Behavioral Ecology. 28 (2): 570–578. doi:10.1093/beheco/arw188. S2CID 90683989.
- ^ Roh S, Weiter JJ, 1994. 눈에 가벼운 손상을 입었습니다.J Fla Med Assoc, 1994년 4월 81(4):248-51.
- ^ Rozanowska M, et al., 빛으로 인한 망막 손상, http://photobiology.info/Rozanowska.html
- ^ Sacchi, Roberto (4 June 2013). "Colour variation in the polymorphic common wall lizard (Podarcis muralis): An analysis using the RGB colour system". Zoologischer Anzeiger. 252 (4): 431–439. doi:10.1016/j.jcz.2013.03.001.
- ^ Whitehead RD, Ozakinci G, Perrett DI (2012). "Attractive skin coloration: harnessing sexual selection to improve diet and health". Evol Psychol. 10 (5): 842–54. doi:10.1177/147470491201000507. PMID 23253790. S2CID 8655801.
- ^ Archetti, Marco; Döring, Thomas F.; Hagen, Snorre B.; Hughes, Nicole M.; Leather, Simon R.; Lee, David W.; Lev-Yadun, Simcha; Manetas, Yiannis; Ougham, Helen J. (2011). "Unravelling the evolution of autumn colours: an interdisciplinary approach". Trends in Ecology & Evolution. 24 (3): 166–73. doi:10.1016/j.tree.2008.10.006. PMID 19178979.
- ^ Davies, Kevin M., ed. (2004). Plant pigments and their manipulation. Annual Plant Reviews. Vol. 14. Oxford: Blackwell Publishing. p. 6. ISBN 978-1-4051-1737-1.
- ^ Delhey, Kaspar; Peters, Anne (2016-11-16). "The effect of colour‐producing mechanisms on plumage sexual dichromatism in passerines and parrots". Functional Ecology. 31 (4): 903–914. doi:10.1111/1365-2435.12796. ISSN 0269-8463.
- ^ Thomas, Daniel B.; McGraw, Kevin J.; Butler, Michael W.; Carrano, Matthew T.; Madden, Odile; James, Helen F. (2014-08-07). "Ancient origins and multiple appearances of carotenoid-pigmented feathers in birds". Proceedings of the Royal Society B: Biological Sciences. 281 (1788): 20140806. doi:10.1098/rspb.2014.0806. ISSN 0962-8452. PMC 4083795. PMID 24966316.
- ^ a b Cooney, Christopher R.; Varley, Zoë K.; Nouri, Lara O.; Moody, Christopher J. A.; Jardine, Michael D.; Thomas, Gavin H. (2019-04-16). "Sexual selection predicts the rate and direction of colour divergence in a large avian radiation". Nature Communications. 10 (1): 1773. doi:10.1038/s41467-019-09859-7. ISSN 2041-1723. PMC 6467902. PMID 30992444.
- ^ Hill, Geoffrey E. (September 1990). "Female house finches prefer colourful males: sexual selection for a condition-dependent trait". Animal Behaviour. 40 (3): 563–572. doi:10.1016/s0003-3472(05)80537-8. ISSN 0003-3472. S2CID 53176725.
- ^ Weaver, Ryan J.; Santos, Eduardo S. A.; Tucker, Anna M.; Wilson, Alan E.; Hill, Geoffrey E. (2018-01-08). "Carotenoid metabolism strengthens the link between feather coloration and individual quality". Nature Communications. 9 (1): 73. doi:10.1038/s41467-017-02649-z. ISSN 2041-1723. PMC 5758789. PMID 29311592.
- ^ Simons, Mirre J. P.; Cohen, Alan A.; Verhulst, Simon (2012-08-14). "What Does Carotenoid-Dependent Coloration Tell? Plasma Carotenoid Level Signals Immunocompetence and Oxidative Stress State in Birds–A Meta-Analysis". PLOS ONE. 7 (8): e43088. doi:10.1371/journal.pone.0043088. ISSN 1932-6203. PMC 3419220. PMID 22905205.
- ^ Koch, Rebecca E.; Hill, Geoffrey E. (2018-05-14). "Do carotenoid‐based ornaments entail resource trade‐offs? An evaluation of theory and data". Functional Ecology. 32 (8): 1908–1920. doi:10.1111/1365-2435.13122. ISSN 0269-8463.
- ^ Hill, Geoffrey E.; Johnson, James D. (November 2012). "The Vitamin A–Redox Hypothesis: A Biochemical Basis for Honest Signaling via Carotenoid Pigmentation". The American Naturalist. 180 (5): E127–E150. doi:10.1086/667861. ISSN 0003-0147. PMID 23070328. S2CID 2013258.
- ^ Powers, Matthew J; Hill, Geoffrey E (2021-05-03). "A Review and Assessment of the Shared-Pathway Hypothesis for the Maintenance of Signal Honesty in Red Ketocarotenoid-Based Coloration". Integrative and Comparative Biology. 61 (5): 1811–1826. doi:10.1093/icb/icab056. ISSN 1540-7063. PMID 33940618.
- ^ Helfenstein F, Losdat S, Möller AP, Blount JD, Richner H. 색채가 풍부한 남성의 정자는 산화 스트레스로부터 더 잘 보호된다.Ecol Lett. 2010년 2월 13일 (2) 213-22.doi: 10.11/j.1461-0248.2009.01419.x.2009년 1월 4일 PMID: 20059524
- ^ a b 김SY, 벨란도 A매력적인 수컷 스틱백은 소마와 생식선에서 더 많은 산화적 DNA 손상을 가지고 있습니다.제이 에볼 비올2020년 1월 33일 (1):121-126.doi:10.111/jeb.13552.Epub 2019 11월 7일 PMID : 31610052
- ^ Liu GY, Essex A, Buchanan JT, et al. (2005). "Staphylococcus aureus golden pigment impairs neutrophil killing and promotes virulence through its antioxidant activity". J. Exp. Med. 202 (2): 209–15. doi:10.1084/jem.20050846. PMC 2213009. PMID 16009720.
- ^ Choi, Seyoung; Koo, Sangho (2005). "Efficient Syntheses of the Keto-carotenoids Canthaxanthin, Astaxanthin, and Astacene". J. Org. Chem. 70 (8): 3328–3331. doi:10.1021/jo050101l. PMID 15823009.
외부 링크
- 카로티노이드 테르페노이드
- 향미 및 향기 전구체로서의 카로티노이드
- 진딧물의 카로티노이드 유전자
- 국제 카로티노이드 학회
- 미국 국립 의학 도서관 의학 주제 제목(MeSH)의 카로티노이드