페레독신
Ferredoxin페레독신(라틴 페럼: 철 + 레독스, 종종 "fd"로 약칭됨)은 다양한 대사 반응에서 전자 전달을 매개하는 철-황 단백질이다."페레독신"이라는 용어는 D.C.에 의해 만들어졌다.DuPont사의 와튼은 1962년 모텐슨, 발렌타인, 카르나한에 의해 혐기성 세균인 클로스트리디움 [1][2]파스퇴리아눔에서 정제된 철단백질에 적용됐다.
시금치 엽록체에서 분리된 또 다른 산화환원 단백질은 "클로로플라스 페레독신"[3]이라고 불렸다.엽록체 페레독신은 광합성의 순환적 및 비순환적 광인산화 반응에 모두 관여한다.비환식 광인산화에서 페레독신은 마지막 전자수용체이므로 NADP+ 환원효소를 환원시킨다.햇빛에 들뜬 엽록소에서 생성된 전자를 받아들여 페레독신 효소인 NADP+ 산화환원효소 EC 1.18.1.2로 전달합니다.
페레독신은 철-황 클러스터로 구성된 철과 황 원자를 포함하는 작은 단백질이다.이러한 생물학적 "용량체"는 +2와 +3 사이의 철 원자의 산화 상태 변화의 효과와 함께 전자를 받아들이거나 방출할 수 있습니다.이와 같이 페레독신은 생물학적 산화환원 반응에서 전자전달제로 작용한다.
다른 생물무기전자수송시스템은 루브레독신, 시토크롬, 청동단백질 및 구조적으로 관련된 리스케단백질을 포함한다.
페레독신은 철-황 클러스터의 특성과 배열 유사성에 따라 분류될 수 있다.
페레독신의 생물 에너지학
페레독신은 일반적으로 단일 전자 전달을 수행합니다.
Fd0
ox + e− - - { { < > } Fd−
red
그러나 일부 박테리아 페레독신(2[4Fe4S] 타입)은 2개의 철황 클러스터를 가지며 2개의 전자 전달 반응을 수행할 수 있다.단백질의 배열에 따라 두 전달은 거의 동일한 환원 전위를 가질 수도 있고, 유의하게 [4][5]다를 수도 있다.
Fd0
ox + e− - - { { < > } Fd−
red
Fd−
red + e− - - { { < > } Fd2−
red
페레독신은 가장 환원성이 높은 생물학적 전자 운반체 중 하나이다.일반적으로 중간점 전위는 [6]-420mV입니다.세포 내 물질의 환원 전위는 환원 및 산화 형태의 농도에 따라 중간점 전위와 다를 것이다.하나의 전자 반응의 경우, 농도 비율에서 10의 검정력이 변할 때마다 전위는 약 60mV씩 변화합니다.예를 들어 페레독신 풀이 약 95% 감소하면 감소 잠재력은 약 -500mV가 [7]된다.이에 비해, 다른 생물학적 반응들은 대부분 감소 잠재력이 적다. 예를 들어 세포의 일차 생합성 환원제는 NADPH의 세포 산화환원 전위는 -420mV이다(E
0 = -320mV).
지지 단백질의 배열에 따라 페레독신은 약 -500mv에서[6][8] -340mV의 [9]환원전위를 가진다.단일 세포는 여러 유형의 페레독신을 가질 수 있으며, 각 유형은 최적으로 다른 [10]반응을 수행하도록 조정됩니다.
페레독신 저감
고도로 환원되는 페레독신은 다른 강력한 환원제를 사용하거나 보다 적은 환원원으로부터 페레독신으로 [11]전자를 "부스트"하기 위해 에너지원을 사용하여 환원된다.
직접 삭감
Fd를 감소시키는 반응에는 알데히드가 글리세린산 반응(-580mV), 일산화탄소탈수소효소 반응(-520mV), 2-옥소산 등이 포함된다.피루브산 합성효소에 [7]의해 수행되는 반응과 같은 Fd 산화환원효소 반응(-500mV).[12][8]
막전위결합환원
페레독신은 NADH(-320mV) 또는
2 H(-414mV)를 사용하여 감소될 수 있지만, 이러한 과정은 전자의 "부스트"를 더 높은 에너지 [6]상태로 만들기 위해 막 전위의 소비와 결합됩니다.Rnf 복합체는 NADH와 페레독신 사이에서 전자를 가역적으로 전달하면서 막을 가로질러 Na 또는+
H 이온을 펌핑하는+
박테리아에 널리 퍼져 있는 막 단백질이다.막의 화학 삼투압 전위는 NADH에 의한 Fd의 바람직하지
ox 않은 감소에 전력을 공급하기 위해 소비된다.이 반응은 많은 자기영양 생물에서 Fd의 필수−
red 공급원이다.만약 세포가 여분의−
red Fd를 제공하는 기질 위에서 자라고 있다면, Rnf 복합체는 이러한 전자를 NAD로+
전달하여 막 [13]전위에 에너지를 저장할 수 있다.에너지 변환 하이드로게나아제(Ech)는 Fd와 H
2 사이의 전자 전달을 가역적으로 결합하는 효소 계열로, H 이온을 막에 걸쳐 펌핑하여 에너지 차이를 조정합니다.[14]
Fd0
ox + NADH + Na+
outside - ( style { < > } ) Fd2−
red + NAD+
+ Na+
inside
Fd0
ox + H
2 + H+
outside - ( { style { < > } ) Fd2−
red + H+
+ H+
inside
전자 분기
환원성이 낮은 전자공여체로부터의 Fd의 바람직하지 않은 감소는 전자 분기 [6]반응을 통한 산화제의 바람직한 감소와 동시에 결합될 수 있다.전자 분기 반응의 예로는 특정 호기성 디아조트로프에서의 질소 고정용 Fd 발생을−
red 들 수 있다.전형적으로 산화적 인산화에서 NADH에서 유비퀴논(Q)으로의 전자의 전달은 양성자 구동력을 충전하는 것과 결합된다.아조토박터에서는 1개의 전자를 NADH에서 Q로 전달함으로써 방출되는 에너지가 NADH에서 [15][16]Fd로의 1개의 전자의 전달을 동시에 촉진하기 위해 사용된다.
고전위 페레독신 직접 환원
일부 페레독신은 NADPH에 의해 직접 환원될 수 있을 정도로 충분히 높은 산화환원 잠재력을 가지고 있다.그러한 페레독신 중 하나는 많은 포유류의 스테로이드 [17]생합성에 관여하는 아드레독신(-274mV)이다.질산염과 아황산염을 감소시키는 식물의 뿌리에 함유된 페레독신 Fd3는 중간점 전위가 -337mV이며 NADPH에 [10]의해 환원된다.
FeS22 페레독신
| 2Fe-2S 철-황 클러스터 결합 도메인 | |||||||||
|---|---|---|---|---|---|---|---|---|---|
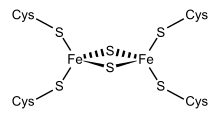 FeS22 페레독신의 구조적 표현. | |||||||||
| 식별자 | |||||||||
| 기호. | Fer2 | ||||||||
| 팜 | PF00111 | ||||||||
| 빠맘 클랜 | CL0486 | ||||||||
| 인터프로 | IPR001041 | ||||||||
| 프로 사이트 | PDOC00642 | ||||||||
| SCOP2 | 3fxc/SCOPe/SUPFAM | ||||||||
| OPM단백질 | 1kf6 | ||||||||
| |||||||||
2Fe–2S 페레독신 슈퍼 패밀리(InterPro: IPR036010)의 구성원은 β(2)-alpha-beta(2)로 구성된 일반 코어 구조를 가지고 있으며, 여기에는 푸티다레독신,[18][19][20][21] 테르프레독신 및 아드레노독신이 포함된다.이들은 2Fe–2S 클러스터가 결합되어 있는 4개의 보존된 시스테인 잔기를 가진 약 100개의 아미노산의 단백질이다.이러한 보존 영역은 또한 알데히드 산화환원효소(N 말단), 크산틴 산화효소(N 말단), 프탈레이트 디옥시게나아제 환원효소(C 말단), 숙신산 탈수소효소 철-술푸라아제(N 말단), 메탄 모노옥시게나아제 환원효소(N 말단)와 같은 다양한 대사 효소 및 멀티도메인 단백질에서 도메인으로 발견된다.
식물성 페레독신
원래 엽록체 막에서 발견된 페레독신 중 한 그룹은 "클로로플라스타형" 또는 "식물형"으로 불렸다(InterPro: IPR010241).활성 중심은 [FeS22] 클러스터이며, 철 원자는 무기 황 원자와 4개의 보존 시스테인(Cys) 잔류물의 황에 의해 사면체적으로 조정됩니다.
엽록체에서 FeS22 페레독신은 광합성 전자전달계의 전자담체 및 글루탐산합성효소, 아질산 환원효소, 아황산 환원효소 및 클로로필 [22]생합성의 사이클라아제와 같은 다양한 세포 단백질에 대한 전자공여체로서 기능한다.사이클라아제는 페레독신에 의존하는 효소이기 때문에 이것은 엽록소 생합성을 광합성 전자전달망에 연결시킴으로써 광합성과 엽록소에 필요한 엽록소 사이의 조정을 위한 메커니즘을 제공할 수 있다.히드록실화 세균성 디옥시게나아제 시스템에서 환원효소 플라보단백질과 산소가수분해효소 사이의 중간 전자전달 운반체 역할을 한다.
티오레독신류 페레독신류
Clostridium pastreianum(Cp2FeFd; P07324)의 FeS22 페레독신은 아미노산 배열, 철-황 클러스터의 분광학적 특성 및 [FeS22] 클러스터에 대한 두 개의 독특한 리간드 교환 능력에 기초하여 별개의 단백질 계열로 인식되었다.이 페레독신의 생리학적 역할은 아직 불분명하지만, Cp2FeFd와 질소분해효소의 몰리브덴-철 단백질의 강력하고 구체적인 상호작용이 밝혀졌다.Azotobacter vinelandii(Av2FeFdI; P82802)와 Aquifex aeolicus(AaFd; O66511)의 상동성 페레독신이 특징지어졌다.AaFd의 결정 구조가 해결되었습니다.AaFd는 다이머로 존재합니다.AaFd 모노머의 구조는 다른 FeS22 페레독신과는 다르다.폴드는 α+β 등급에 속하며, 처음 4개의 β-스트랜드와 2개의 α-헬리시스는 티오레독신 [23]폴드의 변종을 채택한다.UniProt는 이들을 "2Fe2S Shethna형 페레독신"[24] 패밀리로 분류합니다.
아드레노독신형 페레독신
| 페레독신 1 | |||||||
|---|---|---|---|---|---|---|---|
 인간 페레독신-1(FDX1)[25]의 결정 구조. | |||||||
| 식별자 | |||||||
| 기호. | FDX1 | ||||||
| Alt. | FDX | ||||||
| NCBI유전자 | 2230 | ||||||
| HGNC | 3638 | ||||||
| 옴 | 103260 | ||||||
| 참조 | NM_004109 | ||||||
| 유니프로트 | P10109 | ||||||
| 기타 데이터 | |||||||
| 궤적 | 제11장 문제 22.3 | ||||||
| |||||||
아드레노독신(부신 페레독신;InterPro: IPR001055), 푸티다레독신, 테르프레독신은 주로 진핵생물 미토콘드리아와 유사도모나도타에서 발견되는 단일 전자 운반체 역할을 하는 수용성22 FeS 단백질군을 구성합니다.아드레노독신의 인간 변종은 페레독신-1과 페레독신-2로 불린다.미토콘드리아 모노옥시게나아제 시스템에서 아드레노독신은 NADPH:아드레노독신 환원효소로부터 막결합 시토크롬 P450으로 전자를 전달한다.박테리아 중 푸티다레독신과 테르프레독신은 대응하는 NADH 의존성 페레독신 환원효소와 가용성 [26][27]P450 사이에서 전자를 전달한다.대장균 Fdx는 Fe–[28]S 클러스터의 생물 형성에 관여하는 것으로 나타나지만, 이 과의 다른 구성원의 정확한 기능은 알려져 있지 않다.아드레노독신과 식물성 페레독신 사이의 배열 유사성은 낮지만, 두 등급은 접힘 위상이 유사하다.
인간의 페레독신-1은 갑상선 호르몬 합성에 관여한다.또한 아드레노독신 환원효소의 전자를 콜레스테롤 측쇄 분열을 담당하는 CYP450 효소인 CYP11A1로 전달합니다.FDX-1은 금속과 [29]단백질에 결합하는 능력이 있다.페레독신-2는 헴 A와 철-술푸르 단백질 [30]합성에 관여한다.
FeS44 및 FeS34 페레독신
[FeS44] 페레독신은 저전위(세균형) 페레독신과 고전위(HiPIP) 페레독신으로 세분될 수 있다.
저전위 페레독신 및 고전위 페레독신은 다음과 같은 산화환원 방식으로 관련된다.
저전위 페레독신에서 철 이온의 공식 산화수는2+ [2Fe3+, 2Fe2+] 또는 [1Fe3+, 3Fe]일 수 있다.고잠재성 페레독신 중 철 이온의 산화수는 [3Fe3+, 1Fe2+] 또는 [2Fe3+, 2Fe2+]일 수 있다.
세균형 페레독신
| 3Fe-4S 바인딩 도메인 | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
 FeS34 페레독신의 구조적 표현. | |||||||||||
| 식별자 | |||||||||||
| 기호. | Fer4 | ||||||||||
| 팜 | PF00037 | ||||||||||
| 인터프로 | IPR001450 | ||||||||||
| 프로 사이트 | PDOC00176 | ||||||||||
| SCOP2 | 5fd1 / SCOPe / SUPFAM | ||||||||||
| OPM단백질 | 1kqf | ||||||||||
| |||||||||||
원래44 박테리아에서 발견되는 FeS 페레독신 그룹은 "박테리아형"이라고 불립니다.세균형 페레독신은 배열 특성에 따라 추가 그룹으로 세분될 수 있다.대부분은 [FeS44] 클러스터에 결합하는 4개의 시스테인 잔기를 포함하여 적어도 하나의 보존 도메인을 포함합니다.보존된 Cys 잔기 중 하나가 아스파르트산으로 치환된 Pyrococcus furiosus FeS44 페레독신.
세균형 페레독신의 진화 과정에서 효소 내 유전자 복제, 전위 및 융합 이벤트가 발생하여 여러 개의 철-황 중심을 가진 단백질이 나타났다.일부 세균성 페레독신에서 중복 도메인 중 하나가 보존된 4개의 Cys 잔류물 중 하나 이상을 잃었다.이러한 도메인은 철과 황의 바인딩 속성을 잃었거나 [FeS44]클러스터[31] [32]및 dicluster-type이 아닌 [FeS34]클러스터에 바인드되어 있습니다.
3-D 구조는 다수의 단클러스터 및 쌍클러스터 박테리아 유형 페레독신으로 알려져 있습니다.접힘은 α+β 등급에 속하며, 2-7개의 α-헬리체와 4개의 β-스트랜드가 배럴 모양 구조를 형성하고 철-황 클러스터의 "근접" Cys 리간드 3개를 포함하는 압출 루프가 있다.
고잠재성 철황단백질
고전위 철-황 단백질(HiPIPs)은 혐기성 전자 전달 사슬에서 기능하는 FeS 페레독신의 독특한44 군을 형성한다.일부 HiPIP는 알려진 다른 철-황 단백질보다 높은 산화환원 전위를 가진다(예: Rhodopila Globiformis의 HiPIP는 산화환원 전위가 ca. 450mV이다).몇몇 HiPIP는 구조적으로 특징지어졌으며, 그 접힘은 α+β 등급에 속한다.다른 세균성 페레독신과 마찬가지로 [FeS44] 단위는 큐반형 클러스터를 형성하고 4개의 Cys 잔기를 통해 단백질과 결합한다.
페레독신 계열의 인간 단백질
페레독신의 진화
이 섹션은 비어 있습니다.추가해서 도움을 드릴 수 있습니다. (2020년 7월) |
레퍼런스
- ^ Mortenson LE, Valentine RC, Carnahan JE (June 1962). "An electron transport factor from Clostridium pasteurianum". Biochemical and Biophysical Research Communications. 7 (6): 448–52. doi:10.1016/0006-291X(62)90333-9. PMID 14476372.
- ^ Valentine RC (December 1964). "Bacterial Ferredoxin". Bacteriological Reviews. 28 (4): 497–517. doi:10.1128/MMBR.28.4.497-517.1964. PMC 441251. PMID 14244728.
- ^ Tagawa K, Arnon DI (August 1962). "Ferredoxins as electron carriers in photosynthesis and in the biological production and consumption of hydrogen gas". Nature. 195 (4841): 537–43. Bibcode:1962Natur.195..537T. doi:10.1038/195537a0. PMID 14039612. S2CID 4213017.
- ^ Maiocco SJ, Arcinas AJ, Booker SJ, Elliott SJ (January 2019). "Parsing redox potentials of five ferredoxins found within Thermotoga maritima". Protein Science. 28 (1): 257–266. doi:10.1002/pro.3547. PMC 6295886. PMID 30418685.
- ^ Gao-Sheridan HS, Pershad HR, Armstrong FA, Burgess BK (March 1998). "Discovery of a novel ferredoxin from Azotobacter vinelandii containing two [4Fe-4S] clusters with widely differing and very negative reduction potentials". The Journal of Biological Chemistry. 273 (10): 5514–9. doi:10.1074/jbc.273.10.5514. PMID 9488675.
- ^ a b c d Buckel W, Thauer RK (2018). "Flavin-Based Electron Bifurcation, Ferredoxin, Flavodoxin, and Anaerobic Respiration With Protons (Ech) or NAD+ (Rnf) as Electron Acceptors: A Historical Review". Frontiers in Microbiology. 9: 401. doi:10.3389/fmicb.2018.00401. PMC 5861303. PMID 29593673.
- ^ a b Huwiler SG, Löffler C, Anselmann SE, Stärk HJ, von Bergen M, Flechsler J, et al. (February 2019). "One-megadalton metalloenzyme complex in Geobacter metallireducens involved in benzene ring reduction beyond the biological redox window". Proceedings of the National Academy of Sciences of the United States of America. 116 (6): 2259–2264. doi:10.1073/pnas.1819636116. PMC 6369795. PMID 30674680.
- ^ a b Li B, Elliott SJ (2016). "The Catalytic Bias of 2-Oxoacid:ferredoxin Oxidoreductase in CO2: Evolution and reduction through a ferredoxin-mediated electrocatalytic assay". Electrochimica Acta. 199: 349–356. doi:10.1016/j.electacta.2016.02.119.
- ^ Thamer W, Cirpus I, Hans M, Pierik AJ, Selmer T, Bill E, et al. (March 2003). "A two [4Fe-4S]-cluster-containing ferredoxin as an alternative electron donor for 2-hydroxyglutaryl-CoA dehydratase from Acidaminococcus fermentans". Archives of Microbiology. 179 (3): 197–204. doi:10.1007/s00203-003-0517-8. PMID 12610725. S2CID 23621034.
- ^ a b Hanke GT, Kimata-Ariga Y, Taniguchi I, Hase T (January 2004). "A post genomic characterization of Arabidopsis ferredoxins". Plant Physiology. 134 (1): 255–64. doi:10.1104/pp.103.032755. PMC 316305. PMID 14684843.
- ^ Boyd ES, Amenabar MJ, Poudel S, Templeton AS (February 2020). "Bioenergetic constraints on the origin of autotrophic metabolism". Philosophical Transactions. Series A, Mathematical, Physical, and Engineering Sciences. 378 (2165): 20190151. Bibcode:2020RSPTA.37890151B. doi:10.1098/rsta.2019.0151. PMC 7015307. PMID 31902344.
- ^ Gibson MI, Chen PY, Drennan CL (December 2016). "A structural phylogeny for understanding 2-oxoacid oxidoreductase function". Current Opinion in Structural Biology. 41: 54–61. doi:10.1016/j.sbi.2016.05.011. PMC 5381805. PMID 27315560.
- ^ Westphal L, Wiechmann A, Baker J, Minton NP, Müller V (November 2018). "The Rnf Complex Is an Energy-Coupled Transhydrogenase Essential To Reversibly Link Cellular NADH and Ferredoxin Pools in the Acetogen Acetobacterium woodii". Journal of Bacteriology. 200 (21). doi:10.1128/JB.00357-18. PMC 6182241. PMID 30126940.
- ^ Schoelmerich MC, Müller V (April 2020). "Energy-converting hydrogenases: the link between H2 metabolism and energy conservation". Cellular and Molecular Life Sciences. 77 (8): 1461–1481. doi:10.1007/s00018-019-03329-5. PMID 31630229. S2CID 204786346.
- ^ Ledbetter RN, Garcia Costas AM, Lubner CE, Mulder DW, Tokmina-Lukaszewska M, Artz JH, et al. (August 2017). "The Electron Bifurcating FixABCX Protein Complex from Azotobacter vinelandii: Generation of Low-Potential Reducing Equivalents for Nitrogenase Catalysis". Biochemistry. 56 (32): 4177–4190. doi:10.1021/acs.biochem.7b00389. PMC 7610252. PMID 28704608.
- ^ Poudel S, Colman DR, Fixen KR, Ledbetter RN, Zheng Y, Pence N, et al. (May 2018). "Electron Transfer to Nitrogenase in Different Genomic and Metabolic Backgrounds". Journal of Bacteriology. 200 (10). doi:10.1128/JB.00757-17. PMC 5915786. PMID 29483165.
- ^ Ewen KM, Ringle M, Bernhardt R (June 2012). "Adrenodoxin--a versatile ferredoxin". IUBMB Life. 64 (6): 506–12. doi:10.1002/iub.1029. PMID 22556163.
- ^ Armengaud J, Sainz G, Jouanneau Y, Sieker LC (February 2001). "Crystallization and preliminary X-ray diffraction analysis of a [2Fe-2S] ferredoxin (FdVI) from Rhodobacter capsulatus". Acta Crystallographica. Section D, Biological Crystallography. 57 (Pt 2): 301–3. doi:10.1107/S0907444900017832. PMID 11173487.
- ^ Sevrioukova IF (April 2005). "Redox-dependent structural reorganization in putidaredoxin, a vertebrate-type [2Fe-2S] ferredoxin from Pseudomonas putida". Journal of Molecular Biology. 347 (3): 607–21. doi:10.1016/j.jmb.2005.01.047. PMID 15755454.
- ^ Mo H, Pochapsky SS, Pochapsky TC (April 1999). "A model for the solution structure of oxidized terpredoxin, a Fe2S2 ferredoxin from Pseudomonas". Biochemistry. 38 (17): 5666–75. CiteSeerX 10.1.1.34.4745. doi:10.1021/bi983063r. PMID 10220356.
- ^ Beilke D, Weiss R, Löhr F, Pristovsek P, Hannemann F, Bernhardt R, Rüterjans H (June 2002). "A new electron transport mechanism in mitochondrial steroid hydroxylase systems based on structural changes upon the reduction of adrenodoxin". Biochemistry. 41 (25): 7969–78. doi:10.1021/bi0160361. PMID 12069587.
- ^ Stuart D, Sandström M, Youssef HM, Zakhrabekova S, Jensen PE, Bollivar DW, Hansson M (September 2020). "Aerobic Barley Mg-protoporphyrin IX Monomethyl Ester Cyclase is Powered by Electrons from Ferredoxin". Plants. 9 (9): 1157. doi:10.3390/plants9091157. PMC 7570240. PMID 32911631.
- ^ Yeh AP, Ambroggio XI, Andrade SL, Einsle O, Chatelet C, Meyer J, Rees DC (September 2002). "High resolution crystal structures of the wild type and Cys-55-->Ser and Cys-59-->Ser variants of the thioredoxin-like [2Fe-2S] ferredoxin from Aquifex aeolicus". The Journal of Biological Chemistry. 277 (37): 34499–507. doi:10.1074/jbc.M205096200. PMID 12089152.
- ^ 패밀리:"2fe2s 셰트나형 페레독신 패밀리"
- ^ PDB: 3P1M,
- ^ Peterson JA, Lorence MC, Amarneh B (April 1990). "Putidaredoxin reductase and putidaredoxin. Cloning, sequence determination, and heterologous expression of the proteins". The Journal of Biological Chemistry. 265 (11): 6066–73. doi:10.1016/S0021-9258(19)39292-0. PMID 2180940.
- ^ Peterson JA, Lu JY, Geisselsoder J, Graham-Lorence S, Carmona C, Witney F, Lorence MC (July 1992). "Cytochrome P-450terp. Isolation and purification of the protein and cloning and sequencing of its operon". The Journal of Biological Chemistry. 267 (20): 14193–203. doi:10.1016/S0021-9258(19)49697-X. PMID 1629218.
- ^ Tokumoto U, Takahashi Y (July 2001). "Genetic analysis of the isc operon in Escherichia coli involved in the biogenesis of cellular iron-sulfur proteins". Journal of Biochemistry. 130 (1): 63–71. doi:10.1093/oxfordjournals.jbchem.a002963. PMID 11432781.
- ^ "Entrez Gene: FDX1 ferredoxin 1".
- ^ "FDX2 ferredoxin 2 [Homo sapiens (human)] - Gene - NCBI". www.ncbi.nlm.nih.gov. Retrieved 8 April 2019.
- ^ Fukuyama K, Matsubara H, Tsukihara T, Katsube Y (November 1989). "Structure of [4Fe-4S] ferredoxin from Bacillus thermoproteolyticus refined at 2.3 A resolution. Structural comparisons of bacterial ferredoxins". Journal of Molecular Biology. 210 (2): 383–98. doi:10.1016/0022-2836(89)90338-0. PMID 2600971.
- ^ Duée ED, Fanchon E, Vicat J, Sieker LC, Meyer J, Moulis JM (November 1994). "Refined crystal structure of the 2[4Fe-4S] ferredoxin from Clostridium acidurici at 1.84 A resolution". Journal of Molecular Biology. 243 (4): 683–95. doi:10.1016/0022-2836(94)90041-8. PMID 7966291.
추가 정보
- Bruschi M, Guerlesquin F (1988). "Structure, function and evolution of bacterial ferredoxins". FEMS Microbiology Reviews. 4 (2): 155–75. doi:10.1111/j.1574-6968.1988.tb02741.x. PMID 3078742.
- Ciurli S, Musiani F (2005). "High potential iron-sulfur proteins and their role as soluble electron carriers in bacterial photosynthesis: tale of a discovery". Photosynthesis Research. 85 (1): 115–31. doi:10.1007/s11120-004-6556-4. PMID 15977063. S2CID 27768048.
- Fukuyama K (2004). "Structure and function of plant-type ferredoxins". Photosynthesis Research. 81 (3): 289–301. doi:10.1023/B:PRES.0000036882.19322.0a. PMID 16034533. S2CID 24574958.
- Grinberg AV, Hannemann F, Schiffler B, Müller J, Heinemann U, Bernhardt R (September 2000). "Adrenodoxin: structure, stability, and electron transfer properties". Proteins. 40 (4): 590–612. doi:10.1002/1097-0134(20000901)40:4<590::AID-PROT50>3.0.CO;2-P. PMID 10899784.
- Holden HM, Jacobson BL, Hurley JK, Tollin G, Oh BH, Skjeldal L, et al. (February 1994). "Structure-function studies of [2Fe-2S] ferredoxins". Journal of Bioenergetics and Biomembranes. 26 (1): 67–88. doi:10.1007/BF00763220. PMID 8027024. S2CID 12560221.
- Meyer J (November 2001). "Ferredoxins of the third kind". FEBS Letters. 509 (1): 1–5. doi:10.1016/S0014-5793(01)03049-6. PMID 11734195. S2CID 8101608.




