인디고 염료
Indigo dye | |
 | |
 | |
| 이름 | |
|---|---|
| 우선 IUPAC 이름 [2())E]-[2,2(-)-비인돌릴리덴]-3,3(1,1h)-디온 | |
| 기타 이름 2,2'-비스(2,3-디히드로-3-옥소인돌릴리덴),인고틴 | |
| 식별자 | |
3D 모델(JSmol) | |
| 첸블 | |
| 켐스파이더 | |
| ECHA 정보 카드 | 100.006.898 |
PubChem CID | |
| RTECS 번호 |
|
| 유니 | |
CompTox 대시보드 (EPA ) | |
| |
| |
| 특성. | |
| 채널161022 | |
| 몰 질량 | 262.27 g/g |
| 외모 | 짙은 청색의 결정성 분말 |
| 밀도 | 1.199g/cm3 |
| 녹는점 | 390~392°C(734~738°F, 663~665K) |
| 비등점 | 분해하다 |
| 990 µg/L (25 °C에서) | |
| 관련 화합물 | |
관련 화합물 | 인도옥실 타이리안 퍼플 인디칸 |
달리 명시되지 않은 한 표준 상태(25°C[77°F], 100kPa)의 재료에 대한 데이터가 제공됩니다. | |
인디고 염료는 독특한 파란색을 가진 유기 화합물이다.역사적으로, 인디고는 인디고페라속 식물의 잎에서 추출된 천연 염료였다; 염료를 함유한 인디고페라 식물은 세계적으로, 특히 아시아에서는, 특히, 인디고 염료의 생산은 이전 때문에 경제적으로 중요했다.청색 염료는 역사적으로 [1]보기 드문 것입니다.
오늘날 생산되는 대부분의 인디고 염료는 합성 염료로 매년 수천 톤을 구성하고 있다.이것은 데님 천과 청바지의 생산과 가장 일반적으로 연관되어 있으며, 돌세탁과 산세탁과 같은 효과를 빠르게 적용할 수 있는 특성을 가지고 있습니다.
사용하다
인디고의 주된 용도는 면사 염료로서 주로 청바지에 적합한 데님 천을 만드는 데 사용됩니다. 청바지는 평균적으로 3그램에서 12그램의 염료만 필요합니다.양털과 비단의 염색에는 소량이 사용된다.
인디고 카르민은 인디고라고도 하며 착색제로도 사용된다.연간 약 2만 톤이 생산되고 있으며, 이 역시 청바지의 [1]생산을 위해 생산되고 있다.식품 착색제로도 사용되며, 미국에서는 FD&C Blue No.2로 등록되어 있습니다.
원천
천연원
역사를 통틀어 다양한 식물들이 인디고를 제공했지만, 대부분의 천연 인디고는 열대지방, 특히 인도 아대륙이 원산지인 인디고페라속 식물들로부터 얻어졌습니다.아시아에서 가장 주요한 상업적인 인디고 종은 진정한 인디고였다.일본의 류큐 제도나 대만과 같이 비교적 추운 아열대 지역에서 사용되는 일반적인 대안은 스트로빌란테스 쿠시아이다.
남쪽에서 Indigofera 종이 도입되기 전까지, Polygonum tinctorum (Dyer's notweed)은 동아시아에서 가장 중요한 청색 염료였지만, 이 작물은 Indigo의 평균 작물보다 염료가 적게 생산되었고, 보다 경제적인 Indigofera tinctoria 식물에 빠르게 추월되었다.중남미에서 재배되는 종은 아닐이라고도 알려진 인디고페라 수프루티코사이고, 인도에서는 중요한 종이 인디고페라 아렉타 나탈 인디고였다.유럽에서, 일반적으로 와드로 알려진 이사티스 주석기는 인디고라고도 불리는 같은 염색 화합물을 포함하는 파란색 천을 염색하는 데 사용되었다.
몇몇 식물들은 대기 산소와 같은 산화원에 노출되었을 때 반응하여 인디고 염료를 생성한다; 그러나, 상대적으로 낮은 농도의 인디고 염료로 작업하기 어렵게 만들고, 색상은 이러한 식물에 존재하는 다른 염료 물질에 의해 더 쉽게 오염되어, 일반적으로 회색으로 이어진다.색조를 띠다
인디고의 전구체는 아미노산 트립토판의 무색, 수용성 유도체인 인디칸이다.인디칸은 쉽게 가수분해되어 β-D-포도당 및 인산화기를 방출한다.공기 노출에 의한 산화는 인디고 염료의 끝부분인 불용성 파란색 화학 물질인 인디고틴으로 인도옥시를 전환시킵니다.Indican은 식물의 잎을 가공하여 얻었으며, 이 화합물은 0.2~0.8%나 함유되어 있다.잎을 물에 담가 발효시켜 식물에 존재하는 글리코사이드 인디칸을 인디고틴으로 [2]전환시켰다.양잿물과 같은 강한[3] 베이스와 섞으면 발효된 잎 용액에서 침전되고, 케이크에 눌러 넣고, 말리고, 가루로 만듭니다.그리고 나서 그 가루는 다양한 다른 물질들과 섞여서 다른 색조의 파란색과 보라색들을 만들어냈다.
인디고의 자연적인 원천은 연체동물도 포함한다; 무렉스 골뱅이는 타이리안 퍼플이라고 알려진 다양한 보라색 색조를 내는 인디고와 6,6'-디브로모인디고의 혼합물을 생성한다.염색 과정의 일부에서 빛에 노출되면 디브로모인디고가 남색으로 바뀌어 로열 블루, 히야신스 퍼플 또는 테켈레트로 알려진 파란색 색조를 만들 수 있습니다.
화학 합성
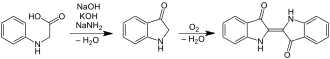
인디고는 경제적 중요성을 감안하여 여러 가지 방법으로 제조되어 왔다.베이어-드류슨 인디고 합성은 1882년으로 거슬러 올라간다.o-니트로벤츠알데히드를 아세톤과 함께 알돌 축합한 후 환화 및 산화 이량체를 통해 인디고로 환원합니다.이 경로는 실험실 규모에서 인디고와 그 유도체를 얻는 데 매우 유용하지만 산업 규모의 합성에는 실용적이지 않은 것으로 판명되었다.요하네스 플레거와[4] 카를 호이만(de)은 결국 산업적 대량생산 합성을 [5]고안했다.
인디고를 생산하는 최초의 상업적인 실용적인 경로는 1901년에 Pfleger에 의해 인정되었다.이 공정에서 N-페닐글리신은 수산화나트륨, 수산화칼륨 및 소다미드의 용융혼합물로 처리된다.이 매우 민감한 녹은 인산화기를 생성하며, 인산화기는 공기 중에 산화되어 인디고를 형성합니다.이 방법의 변형은 오늘날에도 여전히 사용되고 있습니다.1897년, 인디고의 대안이자 실행 가능한 경로가 Heumann에게 인정되었습니다.N-(2-카르복시페닐)글리신을 수산화나트륨을 사용하여 불활성 분위기에서 200°C(392°F)로 가열해야 합니다.공정은 Pfleger 방법보다 쉽지만 전구체가 더 비싸다.인도실-2-카르본산이 생성된다.이 물질은 쉽게 탈카복실화되어 공기 중에 산화되어 인디고를 [1]형성합니다.인디고 염료의 준비는 원래 Bayer-Drewsen [6]경로에 따라 대학 실험실 수업에서 실습된다.
인디고의 역사

페루 후아카 프리타에서 [7]6,000년 전으로 거슬러 올라가는 가장 오래된 남색으로 염색된 직물이 발견되었다.인도, 중국, 일본, 그리고 동남아시아 국가들과 같은 많은 아시아 국가들은 수 세기 동안 인디고를 염료로 사용해 왔다.이 염료는 메소포타미아, 이집트, 영국, 메소아메리카, 페루, 이란, 그리고 서아프리카의 고대 문명에도 알려져 있었다.인디고는 또한 인도에서 재배되었는데, 인도에서 생산과 [8]가공의 가장 초기 주요 중심지이기도 했다.I. tinctoria 종은 인도에서 [8]길들여졌다.염료로 쓰인 인디고는 그리스와 로마에 전해져 사치품으로 [8]평가되었다.
메소포타미아에서는 기원전 7세기의 신바빌로니아 설형편(,形 tablet)이 양모 염색의 레시피를 제공하고 있으며,[9] 이 경우 라피스색 양모(uqnatu)가 반복적으로 침지 및 통풍을 통해 생산된다.인디고는 아마 인도에서 수입되었을 것이다.로마인들은 남색을 그림이나 약품이나 화장품의 안료로 사용했다.그것은 아랍 상인들이 인도에서 지중해로 수입한 사치품이었다.
인도는 그리스-로마 시대에 유럽에 인디고의 주요 공급국이었다.The association of India with indigo is reflected in the Greek word for the dye, indikón (Ἰνδικόν, Indian).[9]로마인들은 이 용어를 indum으로 라틴어화했고, 이는 이탈리아 방언으로 전해졌고 결국 indigo라는 단어로 영어로 바뀌었다.
벵골의 인디고 재배업자들은 1859년 컴퍼니 통치 기간 동안 인디고 반란으로 알려진 유럽의 상인들과 농장주들에 의해 만들어진 착취적인 노동 조건에 저항했다.인도 극작가 디나반두 미트라의 벵골 희곡 닐 다판은 반란의 허구적인 개작이었다.
19세기에 인디고에 대한 수요는 1897년에 7,000km2(2,700평방마일)가 주로 인도에서 인디칸 생산 식물 재배에 바쳐졌다는 사실로 나타난다.이에 비해 룩셈부르크는 2,586km이다2.[1]
유럽에서 인디고는 중세 내내 희귀한 상품으로 남아있었다.대신 와드 식물에서 유래한 화학적으로 동일한 염료(Isatis tinctoria)가 사용되었습니다.15세기 후반에 포르투갈 탐험가 Vasco da Gama가 인도로 가는 뱃길을 발견했다.이것은 인도, 스파이스 제도, 중국, 일본과의 직거래를 확립하는 계기가 되었다.수입업자들은 이제 페르시아, 레반타인, 그리스 중개업자들이 부과하는 무거운 세금과 이전에 사용되었던 길고 위험한 육로를 피할 수 있었다.그 결과 유럽에서 인디고의 수입과 사용이 크게 증가했다.아시아에서 온 많은 유럽 인디고가 포르투갈, 네덜란드, 영국의 항구를 통해 도착했다.많은 인디고 농장은 열대 기후에 유럽 열강에 의해 세워졌다.스페인은 중남미의 식민지에서 염료를 수입했고, 아이티와 자메이카의 주요 작물이었고, 노예가 된 아프리카인들과 아프리카계 미국인들이 많은 혹은 모든 노동을 수행했다.스페인 식민지 시대에 현대 엘살바도르 지역에서 세계 시장을 위한 인디고의 집중 생산은 치명적인 환경에서 노동을 강요당한 지역 원주민들을 [10]죽일 정도로 건강하지 못한 조건을 수반했다.인디고 농장은 버진아일랜드에서도 번성했다.하지만, 프랑스와 독일은 16세기에 그 지역의 황토색소 산업을 보호하기 위해 수입 인디고를 불법화했다.
뉴턴은 1675년 [11]레티온스 옵티컬에서 무지개에 대한 그의 개정된 설명에서 그가 원래 이름 붙인 다섯 가지에 새로운 두 가지 원색 중 하나를 묘사하기 위해 "인디고"를 사용했습니다.
무역 상품으로서의 높은 가치 때문에, 인디고는 종종 블루 [12]골드라고 불렸습니다.
서아프리카 전역에서, 인디고는 수세기 동안 지속된 섬유 전통의 기반이었다.사하라의 투아레그 유목민에서 카메룬에 이르기까지 남색으로 물든 옷은 부를 상징했다.나이지리아 요루바와 말리의 만딩카 등 대부분의 지역에서 여성들이 옷을 염색했다.하우사 남성 염료업자들 사이에서는 공동 염료업자가 고대 도시 가노의 재산의 기초가 되어 오늘날에도 같은 [13]구덩이에서 장사를 하고 있는 것을 볼 수 있다.투아레그족은 때때로 그들의 전통적인 예복과 터번 천에 있는 인디고 색소가 피부를 짙은 파란색으로 [14]물들였기 때문에 "블루 피플"이라고 불립니다.
일본에서는 에도시대에 인디고가 특히 중요해졌다.이는 섬유 [15]산업이 성장하면서 일반인들이 [16]비단을 착용하는 것이 금지되었기 때문에 목화의 재배가 증가했고,[17] 결과적으로 염색을 할 수 있는 몇 안 되는 물질 중 하나인 인디고(indigo)가 증가했기 때문입니다.
북미에서 인디고는 Eliza Lucas에 의해 식민지 사우스 캐롤라이나에 도입되었고, 그곳에서 인디고는 식민지에서 [18]쌀 다음으로 중요한 현금 작물이 되었다.주요 수출 작물로서 인디고는 그곳의 [19]농장 노예제를 지지했다.젠틀맨즈 매거진의 1755년 5월과 6월호에는 사우스캐롤라이나주의 플랜터 찰스 우드메이슨이 작성한 필요한 장비의 도면과 그러한 작업을 시작하기 위한 예상 예산과 함께 인디고 재배에 대한 자세한 설명이 실렸다.그것은 나중에 책으로 출판되었다.[20] [21] 1775년까지 사우스 캐롤라이나에서 인디고 생산량은 1,222,000파운드를 넘었다.[22] 벤자민 프랭클린이 1776년 11월 미국 독립전쟁에 대한 프랑스의 지지를 얻기 위해 프랑스로 항해했을 때, 35 배럴의 인디고가 Reprisal에 실려 있었고, 이것은 전쟁 노력에 [23]자금을 대는데 도움이 될 것이다.북미 식민지에서는 세 가지 상업적으로 중요한 종이 발견됩니다: 토착종인 I. caroliniana와 도입된 I. tinctoria와 I. suffraticosa.[24]
합성 개발

1865년 독일의 화학자 아돌프 폰 바이어는 인디고의 합성에 대해 연구하기 시작했다.그는 1878년(이자틴으로부터) 인디고의 첫 합성, 1880년(2-니트로벤츠알데히드로부터) 두 번째 합성이라고 설명했다.(베이어는 1883년이 되어서야 마침내 남색의 구조를 알아냈다.)[25]인디고의 합성은 여전히 비현실적이었기 때문에 BASF(Badische Anilin-and Soda-Fabrik)와 Hoechst에서 대체 시작 재료를 찾는 작업이 계속되었다.요하네스 플레거와[4] 카를 호이만은 결국 산업적 대량생산 합성을 [5]고안했다.
아닐린을 쉽게 얻을 수 있는 N-(2-카르복시페닐)글리신의 합성은 새롭고 경제적으로 매력적인 경로를 제공했다.BASF는 1897년까지 상업적으로 실현 가능한 제조 공정을 개발했으며, 당시 19,000톤의 인디고가 식물에서 생산되었다.이것은 1914년까지 1,000톤까지 떨어졌고 계속해서 수축되었다.2011년까지,[26] 5만 톤의 합성 인디고가 전세계에서 생산되고 있었다.
염색 기술
인디고 화이트
인디고는 물에 녹지 않기 때문에 도전적인 색소이다.용해되려면 화학적 변화(환원)를 거쳐야 한다.축소는 남색을 흰 남색으로 변환한다.물에 잠긴 천을 염색욕에서 제거하면 흰색 인디고는 공기 중의 산소와 빠르게 결합되어 녹지 않고 강렬한 색상의 인디고로 되돌아갑니다.16세기에 처음 유럽에서 널리 보급되었을 때, 유럽의 염색공과 인쇄공들은 이 독특한 특성 때문에 인디고와 씨름했다.또한 몇 가지 화학적인 조작이 필요했고, 일부는 독성 물질을 포함하고 있었으며, 근로자들을 다치게 할 수 있는 많은 기회가 있었다.19세기 영국 시인 윌리엄 워즈워스는 자서전 시 서곡에서 고향인 코커머스의 남색 염료 노동자들의 곤경을 언급했다.그는 그들의 열악한 근무 환경과 그가 그들에게 느꼈던 공감에 대해 다음과 같이 썼다.
- 의심할 여지 없이, 나는 그 때 공동의 명분을 만들었어야 했다.
- 죽은 자들과 함께, 아마도 죽은 자들과 함께.
- 어처구니없는 오인
- 밀러 블루의 맨 영혼은 알 수 없다.
유럽에서 사용되는 인디고 화이트를 생산하기 위한 산업화 전 과정은 인디고를 암모니아가 함유된 퀴퀴한 소변에 녹이는 것이었다.더 편리한 환원제는 아연이다.일본에서 사용된 또 다른 산업화 이전의 방법은 인디고를 가열된 통에 녹여 호열성 혐기성 박테리아가 배양된 것이다.이러한 박테리아의 일부 종은 대사 산물로 수소를 생성하는데, 이것은 불용성 인디고를 가용성 인디고 화이트로 변화시킨다.이 통에 염색한 천은 시보리, 카스리, 가타조메, 쓰쓰가키 등의 기술로 장식되어 있었다.이러한 기법으로 염색한 의복이나 현수막의 예는 호쿠사이 등 예술가의 작품에서 볼 수 있다.
다이렉트 프린트
인디고의 직접 적용에 대한 두 가지 다른 방법이 18세기에 영국에서 개발되었고 19세기까지 잘 사용되었다.연필이나 붓으로 가장 자주 적용되었기 때문에 '연필 블루'로 알려진 첫 번째 방법은 어두운 색조를 얻기 위해 사용될 수 있다.인디고바트에는 삼황화비소와 증점제가 첨가됐다.비소 화합물은 직물에 염료를 칠할 수 있을 만큼 인디고의 산화를 지연시켰다.
두 번째 방법은 중국의 청화자기와 비슷하기 때문에 '차이나 블루'로 알려져 있다.남색 용액을 직접 사용하는 대신, 이 과정은 남색의 불용성 형태를 직물에 인쇄하는 것을 포함했다.그 후 인디고는 일련의 철욕으로 감소되었다.II) 황산염, 각 침지 사이에 공기 산화.차이나 블루 공정은 샤프한 디자인을 만들 수 있었지만 펜슬 블루 방식으로는 어두운 색조를 만들 수 없었습니다.
1880년경, '포도당 과정'이 개발되었다.그것은 마침내 직물에 인디고를 직접 인쇄할 수 있게 되었고 차이나 블루 방법으로는 얻을 수 없는 저렴한 짙은 인디고 프린트를 생산할 수 있었다.
2004년부터 즉석 인디고인 냉동건조 인디고가 출시되고 있다.이 방법에서는 이미 인디고를 환원하여 동결 건조하여 결정으로 한다.결정체를 따뜻한 물에 넣어 염료 냄비를 만듭니다.일반적인 인디고 염색 냄비와 마찬가지로 산소가 섞이지 않도록 주의해야 합니다.동결건조 인디고는 사용이 간편하고 [27]수분에 노출되지 않는 한 무기한 저장이 가능하다.
화학적 성질
인디고 염료는 390–392°C(734–738°F)에서 승화되는 짙은 파란색 결정성 분말이다.물, 알코올 또는 에테르에는 용해되지 않지만 DMSO, 클로로포름, 니트로벤젠 및 농축 황산에는 용해됩니다.인디고의 화학식은 CHNO입니다161022.
분자는 스펙트럼의 주황색 부분(광도 = 613 nm)[28]에서max 빛을 흡수한다.이 화합물은 이중 결합의 결합으로 인해 깊은 색을 띠게 된다. 즉, 분자 내의 이중 결합은 인접하고 분자는 평면이다.인디고 화이트에서는 분자가 평면이 아니기 때문에 결합이 중단된다.
인디고 유도체
인디고의 벤젠 고리는 다양한 관련 염료를 주기 위해 변형될 수 있습니다.두 NH 그룹이 S 원자로 대체되는 티오인디고는 진한 빨간색이다.티리안 퍼플은 지중해산 달팽이에서 분비되는 칙칙한 보라색 염료입니다.그것은 고대에 매우 귀중했다.1909년, 그것의 구조는 6,6'-디브로모인디고(빨간색)로 나타났다.6-브로모인디고([29]broomoindigo)도 성분이다.그것은 상업적으로 생산된 적이 없다.그러나 관련된 Ciba blue(5,7,5′,7--테트라브로모인디고)는 상업적인 가치가 있다.
Indigo 및 그 유도체는 분자 내 및 분자 간 수소 결합을 특징으로 하며 유기 용매 중 용해도가 매우 낮다.이들은 분자간 [30]결합을 억제하는 tBOC 그룹과 같은 과도적 보호 그룹을 사용하여 용해될 수 있습니다.tBOC 인디고를 가열하면 모체 H 결합 안료의 효율적인 열 탈보호 및 재생이 가능합니다.
황산으로 처리하면 인디고가 인디고 카르민(황산 처리된 인디고)이라는 청록색 유도체로 바뀝니다.그것은 18세기 중반에 이용 가능하게 되었다.그것은 식품, 의약품, 화장품의 착색제로 사용된다.
유기반도체로서의 인디고
인디고와 그 유도체는 진공증발로 [31]박막으로 퇴적되면 양극성 유기반도체가 되는 것으로 알려져 있다.
안전과 환경
인디고는 경구 독성이 낮으며,[1] 포유류의 LD는50 5000mg/kg입니다.2009년, Lesotho의 [32]한 청바지 제조업체 하류에서 대량의 청색 염료 유출이 보고되었습니다.
이 화합물은 아릴 탄화수소 [33]수용체의 작용제 역할을 하는 것으로 밝혀졌다.
레퍼런스
- ^ a b c d e Steingruber, Elmar (2004). "Indigo and Indigo Colorants". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a14_149.pub2.
- ^ Schorlemmer, Carl (1874). A Manual of the Chemistry of the Carbon compounds; or, Organic Chemistry. London. 옥스포드 영어사전 제2판, 1989년에 인용
- ^ "Indigo Dyeing". Coyuchi Inc. Retrieved 2019-05-24.
- ^ a b "Johannes Pfleger - Das Evonik Geschichtsportal - Die Geschichte von Evonik Industries". history.evonik.com. Retrieved Jun 7, 2020.
- ^ a b "The Synthesis of Indigo". Archived from the original on 2016-03-04. Retrieved 2015-01-05.
- ^ McKee, James R.; Zanger, Murray (1991). "A microscale synthesis of indigo: Vat dyeing". Journal of Chemical Education. 68 (10): A242. Bibcode:1991JChEd..68..242M. doi:10.1021/ed068pA242.
- ^ Splitstoser JC, Dillehay TD, Wouters J, Claro A (2016-09-14). "Early pre-Hispanic use of indigo blue in Peru". Science Advances. 2 (9): e1501623. Bibcode:2016SciA....2E1623S. doi:10.1126/sciadv.1501623. PMC 5023320. PMID 27652337.
- ^ a b c Kriger & Connah (120페이지
- ^ a b St. Clair, Kassia (2016). The Secret Lives of Colour. London: John Murray. p. 189. ISBN 9781473630819. OCLC 936144129.
- ^ 파울러, 월터(1991년 8월 6일).남동부 메소아메리카의 복잡한 사회 형성.CRC 프레스
- ^ 인용처:
- ^ "History of Indigo & Indigo Dyeing". wildcolours.co.uk. Wild Colours and natural Dyes. Retrieved 30 December 2015.
Indigo was often referred to as Blue Gold as it was an ideal trading commodity; high value, compact and long lasting
- ^ Kriger, Colen E. & Connah, Graham (2006).서아프리카 역사의 옷.Rowman Altamira.ISBN 0-7591-0422-0.
- ^ Gearon, Eamonn, (2011) The Sahara: 문화사 옥스퍼드 대학 출판부, 239페이지
- ^ Eiko Ikegami (28 February 2005). Bonds of Civility: Aesthetic Networks and the Political Origins of Japanese Culture. Cambridge University Press. p. 284. ISBN 978-0-521-60115-3.
- ^ John H. Sagers (20 July 2018). Confucian Capitalism: Shibusawa Eiichi, Business Ethics, and Economic Development in Meiji Japan. Springer. p. 27. ISBN 978-3-319-76372-9.
- ^ Trudy M. Wassenaar (3 November 2011). Bacteria: The Benign, the Bad, and the Beautiful. John Wiley & Sons. p. 105. ISBN 978-1-118-14338-4.
- ^ Eliza Layne Martin. "Eliza Lucas Pinckney:Indigo in the Atlantic World" (PDF). Archived from the original (PDF) on 2010-06-07. Retrieved 2013-08-24.
- ^ Andrea Feerser, Red, White 및 Black Make Blue: 사우스캐롤라이나 식민지 생활의 구조 속의 인디고(University of Georgia Press; 2013)
- ^ Jones, Claude E. (1958). "Charles Woodmason as a Poet". The South Carolina Historical Magazine. 59 (4): 189–194.
- ^ 데이비드 S.쉴드.제국의 신탁: 1690년-1750년, 영국의 시, 정치, 상업. (시카고:시카고 대학 출판부, 2010), 페이지 69, 249
- ^ 월터 B.에드거, ED사우스캐롤라이나 백과사전.Columbia, SC: University of South Carolina Press, 2006), 페이지 9.
- ^ Schoenbrun, David (1976). Triumph in Paris: The Exploits of Benjamin Franklin. New York: Harper & Row. p. 51. ISBN 978-0-06-013854-7.
- ^ David H. Rembert, Jr. (1979). "The indigo of commerce in colonial North America". Economic Botany. 33 (2): 128–134. doi:10.1007/BF02858281. S2CID 2488865.
- ^ 아돌프 바이어(1883) "Uber die Verbindungen der Indigroppe" (인디고군의 화합물에 대하여), Berichte der Deutschen Chemischen Gesellschaft zu Berlin, 16: 2188-2204; 특히 페이지 2204를 참조하십시오.
- ^ "Chemists go green to make better blue jeans". Nature. 553 (7687): 128. 2018. Bibcode:2018Natur.553..128.. doi:10.1038/d41586-018-00103-8.
- ^ Judith McKenzie McCuin. "Directions for Instant Indigo". Archived from the original on 2004-11-16. Retrieved 2008-05-06.
- ^ Wouten, J.; Verhecken, A. (1991). "High-performance liquid chromatography of blue and purple indigoid natural dyes". Journal of the Society of Dyers and Colourists. 107 (7–8): 266–269. doi:10.1111/j.1478-4408.1991.tb01351.x.
- ^ Ramig, Keith; Lavinda, Olga; Szalda, David J.; Mironova, Irina; Karimi, Sasan; Pozzi, Federica; Shah, Nilam; Samson, Jacopo; Ajiki, Hiroko; Massa, Lou; Mantzouris, Dimitrios; Karapanagiotis, Ioannis; Cooksey, Christopher (June 2015). "The nature of thermochromic effects in dyeings with indigo, 6-bromoindigo, and 6,6′-dibromoindigo, components of Tyrian purple". Dyes and Pigments. 117: 37–48. doi:10.1016/j.dyepig.2015.01.025.
- ^ Głowacki, Eric Daniel; Voss, Gundula; Demirak, Kadir; Havlicek, Marek; Sünger, Nevsal; et al. (2013). "A facile protection–deprotection route for obtaining indigo pigments as thin films and their applications in organic bulk heterojunctions". Chemical Communications. 49 (54): 6063–6065. doi:10.1039/C3CC42889C. PMID 23723050.
- ^ Irimia-Vladu, Mihai; Głowacki, Eric D.; Troshin, Pavel A.; Schwabegger, Günther; Leonat, Lucia; Susarova, Diana K.; Krystal, Olga; Ullah, Mujeeb; Kanbur, Yasin; Bodea, Marius A.; Razum, Vladimir F.; Sitter, Helmut; Bauer, Siegfried; Sarıçiftçi, Niyazi Serdar (2012). "Indigo - A Natural Pigment for High Performance Ambipolar Organic Field Effect Transistors and Circuits". Advanced Materials. 24 (3): 375–80. doi:10.1002/adma.201102619. PMID 22109816.
- ^ "Gap alarm". The Sunday Times. 2009-08-09. Retrieved 2011-08-16.
- ^ Denison MS, Nagy SR (2003). "Activation of the aryl hydrocarbon receptor by structurally diverse exogenous and endogenous chemicals". Annu. Rev. Pharmacol. Toxicol. 43: 309–34. doi:10.1146/annurev.pharmtox.43.100901.135828. PMID 12540743.
추가 정보
- Balfour-Paul, Jenny (2016). Indigo: Egyptian Mummies to Blue Jeans. London: British Museum Press. pp. 264 pages. ISBN 978-0-7141-1776-8.
- Ferreira, E.S.B.; Hulme A. N.; McNab H.; Quye A. (2004). "The natural constituents of historical textile dyes" (PDF). Chemical Society Reviews. 33 (6): 329–36. doi:10.1039/b305697j. PMID 15280965.
- Sequin-Frey, Margareta (1981). "The chemistry of plant and animal dyes" (PDF). Journal of Chemical Education. 58 (4): 301. Bibcode:1981JChEd..58..301S. doi:10.1021/ed058p301.