클로린
Chlorin | |
| 이름 | |
|---|---|
| 기타 이름 2,3-디히드로포르핀 | |
| 식별자 | |
3D 모델(JSmol) | |
| 체비 | |
| 켐스파이더 | |
PubChem CID | |
CompTox 대시보드 (EPA ) | |
| |
| |
| 특성. | |
| 채널20164 | |
| 몰 질량 | 312.36784 |
달리 명시되지 않은 한 표준 상태(25°C[77°F], 100kPa)의 재료에 대한 데이터가 제공됩니다. | |
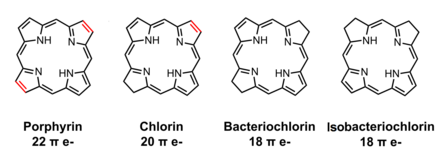
유기화학에서 클로로린은 부분적으로 수소화된 포르피린인 [1]테트라피롤 색소이다.모염소는 돼지에게 공기 산화를 거치는 불안정한 화합물이다.[2] 클로로린이라는 이름은 엽록소에서 유래되었다.클로로필은 마그네슘을 함유한 클로로핀으로 엽록체에서 광합성 색소로 발생합니다.환원된 염소 변종은 박테리오클로로필에 존재하며 '박테리오클로로린'과 '이소박테리오클로로린'으로 불린다.
클로로린은 뛰어난 광감작제이다.m-테트라히드록시페닐클로로린(mTHPC) 및 모노-L-아스파틸클로로인 e6 등의 각종 합성클로로인 유사물을 광감작제로서 [3]실험광역학적 치료에 효과적으로 이용한다.
클로로필류
가장 풍부한 클로로린은 광합성 색소 엽록소이다.클로로필은 클로로린과 달리 케톤이 함유된 다섯 번째 고리를 가지고 있다.클로로필 a, 클로로필 b, 클로로필 d, 클로로필 e, 클로로필 f, 클로로필 g와 같은 다양한 클로로필이 존재합니다.클로로필은 보통 마그네슘을 중심 금속 원자로 하여 [4]부모에 있는 두 개의 NH 센터를 대체한다.
합성 클로로린
수많은 합성 chlorins 검토되어 왔다.[5]Contracted chlorins B(3세)subporphyrin의 감소 또는 대응 B(3세)subbacteriochlorin의 산화에 의해 synthesised 수 있다.[6]그 B(3세)subchlorins 직접 meso-ester B(3세)subchlorin로 meso-diester tripyrromethane을 통해 합성되었다, 화합물의 이 수업은 매우 좋은 형광 양자 수량과 일중항 산소 생산 efficiency[7][8]을 보여 주었다.
「 」를 참조해 주세요.
추가 정보
- Juse´lius, Jonas; Sundholm, Dage (2000). "The aromatic pathways of porphins, chlorins and bacteriochlorins". Physical Chemistry Chemical Physics. 2 (10): 2145–2151. Bibcode:2000PCCP....2.2145J. doi:10.1039/b000260g.
레퍼런스
- ^ Gerard P. Moss (1988). "Nomenclature of Tetrapyrroles. Recommendations 1986". European Journal of Biochemistry. 178 (2): 277–328. doi:10.1111/j.1432-1033.1988.tb14453.x. PMID 3208761.
- ^ Battersby, Alan R. (2000). "Tetrapyrroles: The pigments of life". Natural Product Reports. 17 (6): 507–526. doi:10.1039/b002635m. PMID 11152419.
- ^ Spikes, John D. (July 1990). "New trends in photobiology". Journal of Photochemistry and Photobiology B: Biology. 6 (3): 259–274. doi:10.1016/1011-1344(90)85096-F. PMID 2120404.
- ^ K. Eszter, Borbas. Handbook of Porphyrin Science: 181: Chlorins. worldscientific. doi:10.1142/9789813149564_0001. ISBN 9814322326.
- ^ Taniguchi, Masahiko; Lindsey, Jonathan S. (2017). "Synthetic Chlorins, Possible Surrogates for Chlorophylls, Prepared by Derivatization of Porphyrins". Chemical Reviews. 117 (2): 344–535. doi:10.1021/acs.chemrev.5b00696. OSTI 1534468. PMID 27498781.
- ^ Osuka, Atsuhiro; Kim, Dongho (2008). "Synthesis and Characterization of meso-Aryl-Substituted Subchlorins". Journal of the American Chemical Society. 130 (2): 438–439. doi:10.1021/ja078042b. PMID 18095693.
- ^ Chandra, Brijesh; Soman, Rahul; Sathish Kumar, B.; Jose, K. V. Jovan; Panda, Pradeepta K. (3 Dec 2020). "Meso-Free Boron(III)subchlorin and Its μ-Oxo Dimer with Interacting Chromophores". Organic Letters. 22 (24): 9735–9739. doi:10.1021/acs.orglett.0c03813. PMID 33270460. S2CID 227282229.
- ^ Soman, Rahul; Chandra, Brijesh; Bhat, Ishfaq A.; Kumar, B. Sathish; Hossain, Sk Saddam; Nandy, Sridatri; Jose, K. V. Jovan; Panda, Pradeepta K. (15 Jul 2021). "A2B- and A3-Type Boron(III)Subchlorins Derived from meso-Diethoxycarbonyltripyrrane: Synthesis and Photophysical Exploration". The Journal of Organic Chemistry. 86 (15): 10280–10287. doi:10.1021/acs.joc.1c01001. PMID 34264670. S2CID 235959639.


