비메발론산 경로
Non-mevalonate pathway메발론산염 비의존 경로 및 2-C-메틸-D-에리스리톨 4-인산/1-디옥시-D-자일로오스 5-인산 경로(MEP/DOXP)로도 나타나는 비메발론산 경로는 이소프레노이드 전구체의 생합성을 위한 대체 대사 경로이다.MEP는 IPP로 가는 경로에서 첫 번째 커밋 대사물이기 때문에 현재 이 경로의 바람직한 이름은 MEP 경로이다.
이소프레노이드 전구체 생합성
고전적인 메발론산 경로(MVA 경로 또는 HMG-CoA 환원효소 경로)는 이소프레노이드 전구체(IPP 및 DMAPP)의 생합성을 위한 대사 경로이다.MVA 경로는 대부분의 진핵 생물과 일부 [citation needed]박테리아에 존재한다.IPP와 DMAPP는 단백질 프리닐화, 세포막 유지, 호르몬 합성, 단백질 고정 및 [citation needed]N-글리코실화와 같은 다양한 과정에서 사용되는 이소프레노이드(terpenoid) 분자의 생합성의 기초가 된다.
대부분의 박테리아, 식물 및 말라리아 기생충과 같은 아피콤플렉스 원생동물은 MEP 경로라고 불리는 대체 비메발론산 경로를 사용하여 이소프레노이드 전구체를 생성할 수 있다.식물과 많은 광합성 원생동물들은 MVA 경로와 MEP 경로를 모두 유지한다.MEP 경로를 통한 IPP/DMAPP 생합성은 플라스티드 오르가넬에서 일어나는 반면, MVA 경로를 통한 생합성은 세포질에서 [4]일어난다.대장균과 같은 박테리아는 MEP 경로와 MVA [5]경로를 동시에 발현하도록 설계되었다.MEP와 MVA 경로 사이의 대사 플럭스의 분포는 C-포도당 등방체를 사용하여 [6]연구할 수 있다.MEP 경로를 사용하는 박테리아는 결핵균과 [7]같은 중요한 병원균을 포함한다.
반응
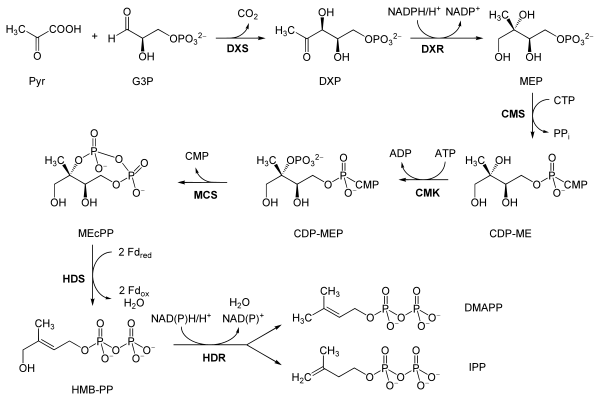
비메발론산 경로의 반응은 주로 아이젠라이히와 동료들로부터 얻은 것으로,[9][8] 단 굵은 글씨 라벨은 위의 체계에 표를 연결하는 데 도움이 되는 추가 로컬 약어이다.
| 반응물 | 효소 | 제품. | |
| 피루브산(Pyr) 및 글리세린알데히드 3-인산(G3P) | DOXP Synthase(Dx; DXP) | 1-디옥시-D-자일로오스5-인산(DOXP, DXP) | |
| DOXP(DXP) | DXP 환원 이성질화효소(Dxr, IspC, DXR) | 2-C-메틸에리톨 4-인산(MEP) | |
| MEP | 2-C-메틸-D-에리트리톨 4-인산시티딜전달효소(YgbP, IspD, CMS) | 4-디포스포시티딜-2-C-메틸에리트리톨(CDP-ME) | |
| CDP-ME | 4-디포스포시티딜-2-C-메틸-D-에리트리톨인산화효소(YchB, IspE, CMK) | 4-디포스포시티딜-2-C-메틸-D-에리스리톨 2-인산(CDP-MEP) | |
| CDP-MEP | 2-C-메틸-D-에리트리톨2,4-시클로디인산합성효소(YgbB, IspF, MCS) | 2-C-메틸-D-에리트리톨2,4-시클로디인산(MECPP) | |
| MECPP | HMB-PP Synthase(GcpE, ISPG, HDS) | (E)-4-히드록시-3-메틸-부트-2-에닐피로인산(HMB-PP) | |
| HMB-PP | HMB-PP 환원효소(LytB, ISPH, HDR) | 이소펜테닐피로인산(IPP) 및 디메틸알릴피로인산(DMAP) |
억제 및 기타 경로 연구
DXP 환원 이성질체 효소(DXR, DOXP 환원 이성질체 효소, IspC, MEP 합성효소라고도 함)는 MEP 경로의 핵심 효소이다.천연물인 포스미도마이신(fosmidomycin)에 의해 억제될 수 있으며, 이는 항균제 또는 항말라리아제 후보 개발의 출발점으로 [10][11][12]연구되고 있다.
중간체인 HMB-PP는 인간 V v9/V22 T 세포, 말초 혈액의 주요 majorT 세포군 및 "미생물 [13]병원균에 대한 면역 반응에 중요한 역할을 하는" 세포의 자연 활성제이다.
- ISPH 억제제: 대부분의 박테리아에는 필수적이지만 사람에게는 없는 비메발론산 대사 경로로 항생제 개발의 이상적인 표적이 됩니다.메틸-D-에리트리톨인산염(MEP) 또는 비메발론산 경로라고 불리는 이 경로는 대부분의 병원성 박테리아에서 세포 생존에 필요한 분자인 이소프레노이드의 생합성을 담당하며, 따라서 대부분의 항균성 박테리아에 도움이 될 것이다.
레퍼런스
- ^ Rohmer M; Rohmer, Michel (1999). "The discovery of a mevalonate-independent pathway for isoprenoid biosynthesis in bacteria, algae and higher plants". Nat Prod Rep. 16 (5): 565–574. doi:10.1039/a709175c. PMID 10584331.
- ^ W. Eisenreich; A. Bacher; D. Arigoni; F. Rohdich (2004). "Review Biosynthesis of isoprenoids via the non-mevalonate pathway". Cellular and Molecular Life Sciences. 61 (12): 1401–1426. doi:10.1007/s00018-004-3381-z. PMID 15197467. S2CID 24558920.
- ^ Hunter, WN (2007). "The Non-mevalonate Pathway of Isoprenoid Precursor Biosynthesis". Journal of Biological Chemistry. 282 (30): 21573–21577. doi:10.1074/jbc.R700005200. PMID 17442674.
- ^ Lichtenthaler H (1999). "The 1-Deoxy-D-xylulose-5-phosphate pathway of isoprenoid biosynthesis in plants". Annu Rev Plant Physiol Plant Mol Biol. 50: 47–65. doi:10.1146/annurev.arplant.50.1.47. PMID 15012203.
- ^ Martin MJ, Pitera DJ, Withers ST, Newman JD, Keasling JD (2003). "Engineering a mevalonate pathway in Escherichia coli for production of terpenoids". Nature Biotechnology. 21 (7): 796–802. doi:10.1038/nbt833. PMID 12778056. S2CID 17214504.
- ^ Orsi E, Beekwilder J, Peek S, Eggink G, Kengen SW, Weusthuis RA (2020). "Metabolic flux ratio analysis by parallel 13C labeling of isoprenoid biosynthesis in Rhodobacter sphaeroides". Metabolic Engineering. 57: 228–238. doi:10.1016/j.ymben.2019.12.004. PMID 31843486.
- ^ Wiemer, AJ; Hsiao, CH; Wiemer, DF (2010). "Isoprenoid Metabolism as a Therapeutic Target in Gram-Negative Pathogens". Current Topics in Medicinal Chemistry. 10 (18): 1858–1871. doi:10.2174/156802610793176602. PMID 20615187.
- ^ a b Qidwai T, Jamal F, Khan MY, Sharma B (2014). "Exploring Drug Targets in Isoprenoid Biosynthetic Pathway for Plasmodium falciparum". Biochemistry Research International. 2014: 657189. doi:10.1155/2014/657189. PMC 4017727. PMID 24864210.
{{cite journal}}: CS1 maint: 작성자 파라미터 사용(링크) - ^ a b Eisenreich W, Bacher A, Arigoni D, Rohdich F (2004). "Biosynthesis of Isoprenoids Via the Non-mevalonate Pathway". Cell. Mol. Life Sci. 61 (12): 1401–26. doi:10.1007/s00018-004-3381-z. PMID 15197467. S2CID 24558920.
- ^ Hale I, O'Neill PM, Berry NG, Odom A & Sharma R (2012). "The MEP pathway and the Development of Inhibitors as Potential Anti-Infective Agents". Med. Chem. Commun. 3 (4): 418–433. doi:10.1039/C2MD00298A.
{{cite journal}}: CS1 maint: 작성자 파라미터 사용(링크) - ^ Jomaa H, Wiesner J, Sanderbrand S, et al. (1999). "Inhibitors of the Nonmevalonate Pathway of Isoprenoid Biosynthesis as Antimalarial Drugs". Science (primary research report). 285 (5433): 1573–6. doi:10.1126/science.285.5433.1573. PMID 10477522.
{{cite journal}}:format=필요.url=(도움말) - ^ C. Zinglé; L. Kuntz; D. Tritsch; C. Grosdemange-Billiard; M. Rohmer (2010). "Isoprenoid Biosynthesis via the Methylerythritol Phosphate Pathway: Structural Variations around Phosphonate Anchor and Spacer of Fosmidomycin, a Potent Inhibitor of Deoxyxylulose Phosphate Reductoisomerase". J. Org. Chem. (primary research report). 75 (10): 3203–3207. doi:10.1021/jo9024732. PMID 20429517.
{{cite journal}}:format=필요.url=(도움말) - ^ Eberl M, Hintz M, Reichenberg A, Kollas AK, Wiesner J, Jomaa H (2003). "Microbial Isoprenoid Biosynthesis and Human γδ T cell Activation". FEBS Lett. 544 (1–3): 4–10. doi:10.1016/S0014-5793(03)00483-6. PMID 12782281. S2CID 9930822.
- ^ https://www.mdlinx.com/news/research-team-reports-new-class-of-antibiotics-active-against-a-wide-range-of-bacteria/1MbQ5xCs1oHgMqFGI8bYpj?show_order=4&ipost_environment=m3usainc&iqs=9z2ztpe37hi9sgpl3mtgomt0op2rcjjloh1vsoj0tro
추가 정보
- : CS1 maint: 작성자 파라미터(링크) RSC 리뷰를 사용하고 MAP Synthase 명명법을 사용합니다Hale I, O'Neill PM, Berry NG, Odom A & Sharma R (2012). "The MEP pathway and the Development of Inhibitors as Potential Anti-Infective Agents". Med. Chem. Commun. 3 (4): 418–433. doi:10.1039/C2MD00298A.
{{cite journal}}. - Qidwai T, Jamal F, Khan MY, Sharma B (2014). "Exploring Drug Targets in Isoprenoid Biosynthetic Pathway for Plasmodium falciparum". Biochemistry Research International. 2014: 657189. doi:10.1155/2014/657189. PMC 4017727. PMID 24864210.
{{cite journal}}: CS1 maint: 작성자 파라미터 사용(링크) - ISPH 억제제: 대부분의 박테리아에는 필수적이지만 사람에게는 없는 비메발론산 대사 경로로 항생제 개발의 이상적인 표적이 됩니다.메틸-D-에리트리톨인산(MEP) 또는 비메발론산 경로라고 불리는 이 경로는 대부분의 병원성 박테리아에서 세포 생존에 필요한 분자인 이소프레노이드의 생합성을 담당한다.