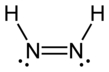다이미드
Diimide
| |||
| |||
| 이름 | |||
|---|---|---|---|
| IUPAC 이름 디아제네 | |||
| 기타 이름 다이미드 디이미네 | |||
| 식별자 | |||
| |||
3D 모델(JSmol) | |||
| 체비 | |||
| 켐스파이더 | |||
| 케그 | |||
| 메슈 | 디아제네 | ||
펍켐 CID | |||
| 유니 | |||
CompTox 대시보드 (EPA) | |||
| |||
| |||
| 특성. | |||
| H2N2 | |||
| 어금질량 | 30.030 g·190−1 | ||
| 외관 | 황색가스 | ||
| 녹는점 | -80°C(-112°F, 193K) | ||
| 관련 화합물 | |||
기타 음이온 | 디포스포네 이플루오르화 이산화 이질소 | ||
기타 양이온 | 아조 화합물 | ||
관련 바이너리 아잔 | 암모니아 디아제인 트라이아제인 | ||
관련 화합물 | 이소디아제네 트라이아젠 테트라젠 | ||
달리 명시된 경우를 제외하고, 표준 상태(25°C [77°F], 100 kPa)의 재료에 대한 데이터가 제공된다. | |||
| Infobox 참조 자료 | |||
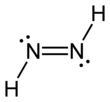
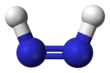
디아진 또는 디아민이라고도 불리는 디아미드는 공식(2NH)을 가진 화합물이다. 그것은 E(트랜스)와 Z(cis)라는 두 개의 기하학적 이소머로 존재한다. 디아진이라는 용어는 디아미드의 유기파생물에 더 흔하다. 따라서 아조벤젠은 유기체 디아진의 한 예다.
합성
디이미드로의 전통적인 경로로는 과산화수소나 공기에 의한 히드라진의 산화를 포함한다.[1] 대신 디에틸 아조디카르복실산염 또는 아조디카르보나미드의 가수분해효과는 다음과 같다.[2]
- (NCOOH)2 → (NH)2 + 2 CO2
오늘날, 디이미드는 2,4,6 – triisopropyl benzenesulfonylhydrazide의 열분해로 생성된다.[3]
불안정성 때문에 다이미드가 생성되어 현장에서 사용한다. CIS(Z-)와 Trans(E-) Isomer의 혼합물이 생성된다. 두 이소머는 모두 불안정하며, 느린 상호 변환을 겪는다. 트랜스 이소머는 더 안정적이지만, 시스 이소머는 불포화 기판과 반응하는 것이기 때문에 르 샤틀리에의 원리로 인해 그들 사이의 평형이 시스 이소머 쪽으로 이동한다. 일부 절차에서는 cis-trans Isomerization을 촉진하는 카르복실산을 추가해야 한다.[4] 다이미드는 쉽게 분해된다. 저온에서도 안정성이 높은 트랜스 이소머는 다양한 불균형 반응을 빠르게 일으키며, 주로 히드라진과 질소 가스를 형성한다.[5]
- 2 HN=NH → HN2–NH22 + N
이러한 경쟁적인 분해 반응 때문에 다이미드 감소는 전형적으로 전구시약을 크게 초과해야 한다.
유기합성에 대한 응용
디이미드는 유기합성에 있어서 시약으로서 유용할 때가 있다.[4] 기질 한쪽 면의 수소를 선택적으로 전달해 H의2 금속-카탈라이스 동기 첨가와 동일한 입체감을 유발하는 기질 한 면의 수소와 알키네를 수소화한다. 방출되는 유일한 화합물은 질소 가스다. 방법은 번거롭지만 디이미드를 사용하면 고압이나 수소 가스 및 금속 촉매가 필요 없어 비용이 많이 들 수 있다.[6] 수소화 메커니즘은 6-membed CHN222 전환 상태를 포함한다.
선택성
다이미드는 알케네와 알케인을 선택적으로 감소시키고 정상적인 촉매 수소화를 방해할 수 있는 많은 기능군에 비활성화되기 때문에 유리하다. 따라서 과산화물, 알킬 할로겐화물, 티올은 디이미드에 의해 용인되지만, 이와 같은 집단은 일반적으로 금속 촉매를 통해 분해된다. 시약은 알키네와 무힌드 또는 경화된[1] 알케인을 해당 알케인과 알칸으로 우선 감소시킨다.[4]
관련
도취 형태인 HNNH2+(Diprotonated dinitrogen)는 가장 강력한 알려진 화학 결합을 갖는 것으로 계산된다. 이 이온은 이중으로 양성된 질소 분자로 생각할 수 있다. 상대적 결합 강도 순서(RSO)는 3.38이다.[7] FNNH와2+ FNNF는2+ 강도 결합이 약간 낮다.[7]
참조
- ^ a b Ohno, M.; Okamoto, M. (1973). "cis-Cyclododecene". Organic Syntheses.; Collective Volume, vol. 5, p. 281
- ^ Wiberg, E.; Holleman, A. F. (2001). "1.2.7: Diimine, N2H2". Inorganic Chemistry. Elsevier. p. 628. ISBN 9780123526519.
- ^ Chamberlin, A. Richard; Sheppeck, James E.; Somoza, Alvaro (2008). "2,4,6-Triisopropylbenzenesulfonylhydrazide". Encyclopedia of Reagents for Organic Synthesis. doi:10.1002/047084289X.rt259.pub2. ISBN 978-0471936237.
- ^ a b c Pasto, D. J. (2001). "Diimide". Encyclopedia of Reagents for Organic Synthesis. John Wiley & Sons. doi:10.1002/047084289X.rd235. ISBN 0471936235.
- ^ Wiberg, Nils; Holleman, A. F.; Wiberg, Egon, eds. (2001). "1.2.7 Diimine N2H2 [1.13.17]". Inorganic Chemistry. Academic Press. pp. 628–632. ISBN 978-0123526519.
- ^ Miller, C. E. (1965). "Hydrogenation with Diimide". Journal of Chemical Education. 42 (5): 254–259. Bibcode:1965JChEd..42..254M. doi:10.1021/ed042p254.
- ^ a b Kalescky, Robert; Kraka, Elfi; Cremer, Dieter (12 September 2013). "Identification of the Strongest Bonds in Chemistry". The Journal of Physical Chemistry A. 117 (36): 8981–8995. Bibcode:2013JPCA..117.8981K. doi:10.1021/jp406200w. PMID 23927609.