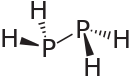디프인산
Diphosphane| | |||
| 이름 | |||
|---|---|---|---|
| IUPAC 이름 디프인산 | |||
| 체계적 IUPAC 이름 디프인산(대체) Tetrahydodiphosphorus(P—P) (가법) | |||
| 기타 이름 디프인산 | |||
| 식별자 | |||
3D 모델(JSmol) | |||
| 체비 | |||
| 켐스파이더 | |||
펍켐 CID | |||
CompTox 대시보드 (EPA) | |||
| |||
| |||
| 특성. | |||
| H4P2 | |||
| 어금질량 | 65.980 g·190−1 | ||
| 녹는점 | -99°C(-146°F, 174K) | ||
| 비등점 | 63.5°C(146.3°F, 336.6K) (추가 분해, 분해) | ||
| 관련 화합물 | |||
기타 음이온 | 암모니아 히드라진 트라이아제인 | ||
기타 양이온 | 쌍인산 | ||
| 인산염 테트라플루오르화물 인산 사트라클로라이드 인산염 사트라브로마이드 인산염 사차화 | |||
관련 화합물 | 인산염 삼인산 디포스포네 쌍두 동물 | ||
달리 명시된 경우를 제외하고, 표준 상태(25°C [77°F], 100 kPa)의 재료에 대한 데이터가 제공된다. | |||
| Infobox 참조 자료 | |||
디프인산(Diphosphane) 또는 디프인산(Diphosphine)은 화학적 공식 PH를24 가진 무기 화합물이다. 이 무색 액체는 여러 이항 인 하이드라이드 중 하나이다. 일반적으로 인산염 샘플이 공기 중에 발화하도록 하는 것은 불순물이다.
특성, 준비, 반응
Diphosphane은 P-P 거리 2.219 앙스트롬으로 가우슈 컨포메이션(이미지에 표시된 것보다 대칭이 덜한 히드라진 등)을 채택한다. 그것은 비기본적이고 상온에서 불안정하며 공기 중에 자연적으로 인화성이 있다. 그것은 물에 잘 녹지 않지만 유기 용제에 녹는다. 그것의 H NMR 스펙트럼은 AXX2'2A의 분할 시스템에서 발생하는 32개의 라인으로 구성된다.[1]
디프인산염은 모노인산칼슘의 가수분해에 의해 생성되는데, 이를 Ca파생물로2+ 설명할 수 있다. P4-2. 최적화된 절차에 따라 -30 °C에서 CaP 400 g을 가수 분해하면 인산염에 약간 오염된 약 20 g의 제품이 나온다.
부틸리튬에 대한 디프인산염의 반응은 다양한 응축된 폴리인산 화합물을 제공한다.
유기 인산염
디프인산(diphosphane)의 다양한 유기파생물이 알려져 있다. 이러한 종은 환원성 결합(예: 클로로디페닐인산염의 테트라페닐디프인산염)에 의해 준비된다.
- 2 ClPPh2 + 2 Na → PhP-PPh22 + 2 NaCl
메틸화합물 PMe는24 염화 티오포스포릴을 메틸마그네슘 브롬화물과 메틸마그네슘을 메틸화하여 생산되는 메틸화합물 MEP2(S)-P(S)Me의2 감소를 통해 제조된다.[2]
참고 항목
참조
- ^ Marianne Baudler, Klaus Glinka (1993). "Monocyclic and polycyclic phosphines". Chem. Rev. 93 (4): 1623–1667. doi:10.1021/cr00020a010.
- ^ Butter, S. A.; Chatt, J. (1974). "Ethylenebis(dimethylphosphine)". Inorg. Synth. 15: 185. doi:10.1002/9780470132463.ch41.