염화 메틸마그네슘
Methylmagnesium chloride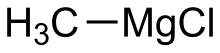 | |
| 이름 | |
|---|---|
| IUPAC 이름 클로로도(메틸)화 | |
| 기타 이름 (클로로마그네시오)methane | |
| 식별자 | |
3D 모델(JSmol) | |
| 체비 | |
| 켐스파이더 | |
| ECHA InfoCard | 100.010.573 |
| EC 번호 |
|
펍켐 CID | |
| 유니 |
|
CompTox 대시보드 (EPA) | |
| |
| |
| 특성. | |
| CH3MgCl | |
| 어금질량 | 74.79 g/190 |
| 외관 | 무색의 고체 |
| 물과 반응한다. | |
| 용해성 | 디에틸에테르와 THF에 녹는 |
| 위험 | |
| 산업안전보건(OHS/OSH): | |
주요 위험 | 인화성, 물과 반응 |
| GHS 라벨 표시: | |
  | |
| 위험 | |
| H225, H250, H260, H314 | |
| P210, P222, P223, P231+P232, P233, P240, P241, P242, P243, P260, P264, P280, P301+P330+P331, P302+P334, P303+P361+P353, P304+P340, P305+P351+P338, P310, P321, P335+P334, P363, P370+P378, P402+P404, P403+P235, P405, P422, P501 | |
| NFPA 704(화재 다이아몬드) | |
| 플래시 포인트 | -17°C(1°F, 256K) |
| 관련 화합물 | |
관련 화합물 | 페닐마그네슘브로미드, 디부틸마그네슘 |
달리 명시된 경우를 제외하고, 표준 상태(25°C [77°F], 100 kPa)의 재료에 대한 데이터가 제공된다. | |
| Infobox 참조 자료 | |
염화 메틸마그네슘(Methylmagnesium chlorgMagnesium)은 일반식 CHMgCl을3 포함한 유기농 화합물이다. 인화성, 무색, 습기에 민감한 이 물질은 가장 단순한 그리그나드 시약이며 통상적으로 테트라하이드로푸란 용액으로 상용화된다.
합성 및 반응
브롬화[1] 메틸마그네슘과 요오드화 메틸마그네슘에 비해 염화 메틸마그네슘은 저등가중과 저비용의 장점을 제공한다. 에틸에테르에 함유된 염화메틸과 마그네슘의 반응에 의해 준비된다.[2]
대부분의 그리냐드 시약과 마찬가지로 염화 메틸마그네슘은 두 개의 산소 원자의 조정을 통해 에테르 용제에 의해 고도로 용해되어 사면 접합 마그네슘 중심을 제공한다.
메틸리튬과 마찬가지로 메틸 카르바니온 신톤에 해당하는 합성물이다. 이 물질은 물과 다른 양성자 시약과 반응하여 다음과 같은 메탄을 공급한다.
- CHMgCl3 + ROH → CH4 + MgCl(OR)
디옥산염 처리 시 염화 메틸마그네슘은 슐렌크 평형을 통해 디메틸마그네슘으로 전환된다.
- 2 CHMgCl3 + 다이옥산 → (CH3)2Mg + MgCl2(다이옥산)
참고 항목
추가 읽기
- Sakai, Shogo; Jordan, K. D. (1982). "Ab initio study of the structure and vibrational frequencies of the Grignard reagent methylmagnesium chloride". Journal of the American Chemical Society. 104 (14): 4019. doi:10.1021/ja00378a047.
참조
- ^ Raymond Paul, Olivier Riobé, Michel Maumy (1976). "(E)-4-Hexen-1-ol". Org. Synth. 55: 62. doi:10.15227/orgsyn.055.0062.
{{cite journal}}: CS1 maint: 작성자 매개변수 사용(링크) - ^ E. R. Coburn (1947). "3-Penten-2-ol". Org. Synth. 27: 65. doi:10.15227/orgsyn.027.0065.




