저메인
Germane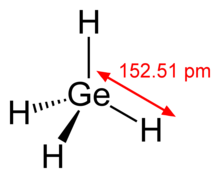 | |||
| | |||
| 이름 | |||
|---|---|---|---|
| IUPAC 이름 저메인 | |||
| 기타 이름 테트라히드화 게르마늄 게르마노메탄 모노게르만 | |||
| 식별자 | |||
3D 모델(JSmol) | |||
| 체비 | |||
| 켐스파이더 | |||
| ECHA 정보 카드 | 100.029.055 | ||
| EC 번호 |
| ||
| 587 | |||
| 케그 | |||
PubChem CID | |||
| RTECS 번호 |
| ||
| 유니 | |||
| UN 번호 | 2192 | ||
CompTox 대시보드 (EPA ) | |||
| |||
| |||
| 특성. | |||
| GeH4 | |||
| 몰 질량 | 76.62 g/g | ||
| 외모 | 무색 가스 | ||
| 냄새 | 톡[1] 쏘다 | ||
| 밀도 | 3.3 kg/m3 | ||
| 녹는점 | -165 °C (-265 °F, 108 K) | ||
| 비등점 | -88 °C (-126 °F, 185 K) | ||
| 낮다 | |||
| 증기압 | > 1 ATM[1] | ||
| 점성 | 17.21μPa/s (추정)[2] | ||
| 구조. | |||
| 사면체 | |||
| 0 D | |||
| 위험 요소 | |||
| 산업안전보건(OHS/OSH): | |||
주요 위험 요소 | 유독성, 인화성, 공기 중에 자연 발화할 수 있음 | ||
| GHS 라벨링: | |||
    | |||
| 위험. | |||
| H220, H280, H302, H330 | |||
| P210, , , , , , , , , , , , , , , , | |||
| NFPA 704(파이어 다이아몬드) | |||
| NIOSH(미국 건강 노출 제한): | |||
PEL(허용) | 없음[1] | ||
REL(권장) | TWA 0.2ppm(0.6mg/m3)[1] | ||
IDLH(즉시 위험) | N.D.[1] | ||
| 안전 데이터 시트(SDS) | ICSC 1244 | ||
| 관련 화합물 | |||
관련 화합물 | 메탄 실란 스타네인 플럼판 제르밀 | ||
달리 명시되지 않은 한 표준 상태(25°C[77°F], 100kPa)의 재료에 대한 데이터가 제공됩니다. | |||
제르메인은 GeH 공식의4 화합물이며, 메탄의 게르마늄 유사체이다.그것은 가장 단순한 수소화 게르마늄이며 게르마늄의 가장 유용한 화합물 중 하나이다.실란과 메탄과 마찬가지로 게르만은 사면체이다.그것은 공기 중에 타서 GeO와 물을 생성한다2.저메인은 14족 수소화물입니다.
발생.
합성
저메인은 일반적으로 게르마늄 산화물(특히 게르마늄산염)을 환원하여 제조되며, 수소화붕소나트륨, 수소화붕소나트륨, 수소화붕소나트륨, 수소화붕소나트륨 등의 수소화물 시약과 함께 제조됩니다.붕소수물과의 반응은 다양한 산들에 의해 촉매되며, 수성 또는 유기 용매에서 수행될 수 있습니다.실험실 규모에서 저메인은 Ge(IV) 화합물과 이러한 수소화물 시약을 [4][5]반응시켜 제조할 수 있다.전형적인 합성은 게르만산칼륨과 [6]수소화붕소나트륨의 반응을 수반했다.
- NaHGeO3 + KBH42 + HO → KGeH3 + KB(OH)4
- KGeH3 + HOCH23 → GeH4 + KOCH23
저메인의 합성을 위한 다른 방법으로는 전기화학적 환원 및 플라즈마 기반 [7]방법이 있다.전기화학적 환원방법은 전해액 수용액에 침지된 게르마늄 금속음극과 몰리브덴이나 카드뮴 등의 금속으로 이루어진 양극 대향전극에 전압을 가하는 것이다.이 방법에서는 양극이 반응하여 고체 몰리브덴 산화물 또는 카드뮴 산화물을 형성하면서 음극에서 제르만 및 수소가스가 진화한다.플라즈마 합성법은 게르마늄 금속에 고주파 플라즈마 소스를 이용해 생성되는 수소원자(H)를 충돌시켜 게르만과 디게르만을 생산하는 방식이다.
반응
저메인은 약산성이다.액체 암모니아4 중 GeH는 NH 및 GeH를3− [8]형성하여4+ 이온화된다.액체 암모니아4 속의 알칼리 금속과 GeH는 반응하여 백색 결정성 MGeH3 화합물을 생성한다.칼륨(칼륨 제르밀 KGeH3)과 루비듐 화합물(루비듐 제르밀 RbGeH3)은 염화나트륨 구조를 가지며, 세슘 화합물은 GeH3− 음이온, CsGeH는3 [8]TlI의 염화나트륨 구조를 가진다.
반도체 산업에서의 사용
이 가스는 약 600K(327°C; 620°F)에서 게르마늄과 수소로 분해됩니다.저메인은 열내성 때문에 MOVPE 또는 화학빔 에피택시에 [9]의해 게르마늄의 에피택시 성장을 위해 반도체 산업에서 사용된다.유기 제르마늄 전구체(예: 이소부틸제르만, 알킬제르마늄 삼염화물 및 디메틸아미노제르마늄 삼염화물)는 MOVPE에 [10]의해 Ge 함유 필름의 증착에 대한 저메인에 대한 덜 위험한 액체 대안으로 검토되었다.
안전.
저메인은 인화성이 높고 잠재적으로 발화성이 있으며 [11]독성이 강한 가스입니다.1970년, 미국 정부 산업 위생사 회의(ACGIH)는 최신 변경 사항을 발표하고 8시간 평균의 [12]직업 피폭 한계치를 0.2ppm으로 설정했다.1시간 노출 시 쥐의 LC50은 622ppm입니다.[13]흡입 또는 노출은 불안감, 두통, 어지럼증, 실신, 호흡곤란, 메스꺼움, 구토, 신장 손상 및 용혈 [14][15][16]효과를 초래할 수 있습니다.
미국 교통부의 위험 등급은 2.3 유독 [12]가스이다.
레퍼런스
- ^ a b c d e NIOSH Pocket Guide to Chemical Hazards. "#0300". National Institute for Occupational Safety and Health (NIOSH).
- ^ Yaws, Carl L. (1997), Handbook Of Viscosity: Volume 4: Inorganic Compounds And Elements, Gulf Professional Publishing, ISBN 978-0123958501
- ^ Kunde, V.; Hanel, R.; Maguire, W.; Gautier, D.; Baluteau, J. P.; Marten, A.; Chedin, A.; Husson, N.; Scott, N. (1982). "The tropospheric gas composition of Jupiter's north equatorial belt (NH3, PH3, CH3D, GeH4, H2O) and the Jovian D/H isotopic ratio". Astrophysical Journal. 263: 443–467. Bibcode:1982ApJ...263..443K. doi:10.1086/160516.
- ^ W. L. Jolly "수성 하이드로붕산염에 의한 IVA 및 VA의 휘발성 하이드라이드 준비" 미국화학회 저널 1961, 제83, 페이지 335-7.
- ^ 미국 특허 4,668,502
- ^ Girolami, G. S.; Rauchfuss, T. B.; Angelici, R. J. (1999). Synthesis and Technique in Inorganic Chemistry. Mill Valley, CA: University Science Books.
- ^ 미국 특허 7,087,102 (2006)
- ^ a b Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2nd ed.). Butterworth-Heinemann. ISBN 978-0-08-037941-8.
- ^ Venkatasubramanian, R.; Pickett, R. T.; Timmons, M. L. (1989). "Epitaxy of germanium using germane in the presence of tetramethylgermanium". Journal of Applied Physics. 66 (11): 5662–5664. Bibcode:1989JAP....66.5662V. doi:10.1063/1.343633.
- ^ Woelk, E.; Shenai-Khatkhate, D. V.; DiCarlo, R. L. Jr.; Amamchyan, A.; Power, M. B.; Lamare, B.; Beaudoin, G.; Sagnes, I. (2006). "Designing Novel Organogermanium MOVPE Precursors for High-purity Germanium Films". Journal of Crystal Growth. 287 (2): 684–687. Bibcode:2006JCrGr.287..684W. doi:10.1016/j.jcrysgro.2005.10.094.
- ^ 브루어, 1963년, 제1권, 제715호
- ^ a b Praxair MSDS 2012-05-08년 Wayback Machine에서 아카이브된 2011년 9월 액세스
- ^ NIOSH 제르만 화학물질 독성효과(RTECS) 등록부 2011년 9월 접속
- ^ Gus'kova, E. I. (1974). "K toksikologii Gidrida Germaniia" [Toxicology of germanium hydride]. Gigiena Truda I Professionalnye Zabolevaniia (in Russian). 18 (2): 56–57. PMID 4839911.
- ^ 미국 EPA 저메인
- ^ Paneth, F.; Joachimoglu, G. (1924). "Über die pharmakologischen Eigenschaften des Zinnwasserstoffs und Germaniumwasserstoffs" [About the pharmacological characteristics of tin hydride and germanium hydride]. Berichte der Deutschen Chemischen Gesellschaft (in German). 57 (10): 1925–1930. doi:10.1002/cber.19240571027.
외부 링크
- 메탈로이드(제조원) 데이터 시트
- Arkonic Specialty Gas China(제조업체) 데이터 시트
- Licensintorg Russia(프로세스 테크놀로지 판매) 2013-03-29 Wayback Machine에서 아카이브 완료
- 혼조케미칼재팬(제조업체) 2013-01-20 웨이백머신 아카이브
- Praxair 데이터 시트
- 공기 액화 가스 백과사전 엔트리
- CDC - 화학적 위험에 대한 NIOSH 포켓 가이드
- Voltaix(제조업체) 데이터시트 2011-07-17 Wayback Machine 아카이브 완료
- 포산화테가스(주)(제조업체)
- 러시아 호르스트 테크놀로지스(제조업체)





