간염
Hepatitis간염은 간조직의 염증이다.[5][3] 간염에 걸린 사람이나 동물은 아무런 증상이 없는 반면, 다른 사람은 피부나 눈의 흰자위가 노란색으로 변색되고 식욕부진, 구토, 피로, 복통, 설사 등이 나타난다.[1][2] 간염은 6개월 이내에 완치가 되면 급성이고, 6개월 이상 지속되면 만성적이다.[1][6] 급성 간염은 스스로 해결하거나 만성 간염으로 진전되거나 (급성적으로) 급성 간기능 장애를 일으킬 수 있다.[7] 만성간염은 간(순환), 간기능부전, 간암 등의 흉터로 진행될 수 있다.[3]
간염은 A, B, C, D, E형 간염에 의해 가장 흔하게 발생한다.[3][2] 다른 원인으로는 알코올 과다 사용, 특정 약물, 독소, 기타 감염, 자가면역질환,[2][3] 비알코올성 치주염(NASH) 등이 있다.[8] A형 간염과 E형 간염은 주로 오염된 음식과 물에 의해 전파된다.[3] B형 간염은 주로 성적으로 전염되지만 임신이나 출산 때 산모에서 아기에게로 옮겨져 감염된 혈액을 통해 전파되기도 한다.[3] C형 간염은 정맥주사 복용자의 주사바늘 공유 중 발생할 수 있는 등 감염된 혈액을 통해 전파되는 것이 일반적이다.[3] D형 간염은 B형 간염에 이미 감염된 사람만 감염시킬 수 있다.[3]
A, B, D형 간염은 예방접종으로 예방할 수 있다.[2] 만성 바이러스성 간염을 치료하기 위해 약을 사용할 수도 있다.[1] 항바이러스제는 기대수명을 제한하는 조건을 가진 것을 제외하고 만성 C형 간염과 함께 복용하는 것이 좋다.[9] NASH에 대한 특별한 치료법은 없지만, 신체 활동, 건강한 식단, 체중 감량이 권장된다.[8] 자가면역형 간염은 면역체계를 억제하는 약으로 치료할 수 있다.[10] 간 이식 수술은 급성 간기능 장애와 만성 간 기능 부전 둘 다의 선택사항일 수 있다.[4]
2015년 전 세계적으로 A형 간염은 약 1억 1,400만 명, 만성 B형 간염은 약 3억 4,300만 명, 만성 C형 간염은 약 1억 4200만 명에서 발생했다.[11] 미국에서 NASH는 약 1100만 명, 알코올성 간염은 약 500만 명에게 영향을 미친다.[8][12] 간염으로 인해 연간 100만 명 이상이 사망하는데, 이 중 대부분은 간 흉터나 간암으로 인해 간접적으로 발생한다.[3][13] 미국에서 A형 간염은 연간 약 2,500명에게서 발생하며 약 75명의 사망자가 발생하는 것으로 추정된다.[14] 이 단어는 '간'을 뜻하는 그리스 헤파(parparαἧ)와 '인플레이션'을 뜻하는 -itis(-ῖτ (-ς)[15]에서 유래되었다.
징후 및 증상
간염은 증상의 완전한 결핍에서 심각한 간 기능 부전에 이르는 광범위한 발현 범위를 가지고 있다.[16][17][18] 일반적으로 바이러스성 감염에 의해 발생하는 급성형 간염은 전형적으로 자가 제한적인 체질적 증상으로 특징지어진다.[16][17] 만성 간염은 유사하게 나타나지만 오랜 염증과 장기 손상으로 간 기능장애에 특유한 징후와 증상을 나타낼 수 있다.[18][19]
급성 간염
급성 바이러스성 간염은 세 가지 뚜렷한 단계를 따른다.
- 초기 프로드롬 단계(사전증상)는 많은 급성 바이러스 감염에 흔히 나타나는 특이하고 독감 같은 증상을 포함한다. 피로, 메스꺼움, 구토, 식욕부진, 관절통, 두통 등이 이에 해당한다.[16][17] 발열은 있을 때 A형, E형 간염의 경우 가장 흔하다 [16]이 단계 후반에는 담낭(어두운 소변)과 점토색 변소 등 간 특이 증상을 경험할 수 있다.[16][17]
- 피부와 눈의 흰자위가 노랗게 변하면 1~2주 정도 지나면 프로드롬을 따라가고 최대 4주까지 지속할 수 있다.[16][17] 비특이성 증상은 보통 이때쯤이면 해소되지만, 간 확대와 오른쪽 상복부 통증이나 불편함이 생기게 된다. 10~20%의 사람도 비장이 커지게 되며, 일부 사람들은 의도하지 않은 가벼운 체중 감량도 경험하게 된다.[16][16][18]
- 회복 단계는 간 연구실 값이 지속적으로 상승하고 잠재적으로 지속적으로 확대된 간염의 임상 증상을 해소하는 것이 특징이다.[16] A형, E형 간염은 모두 1~2개월이 지나면 완치될 것으로 보인다.[16] B형 간염 환자도 대부분 자가 제한돼 3~4개월 뒤 해소될 것으로 보인다. C형 간염의 경우 완치되는 경우는 거의 없을 것이다.[16]
약물유발형 간염과 자가면역형 간염은 모두 급성 바이러스성 간염과 매우 유사하게 나타날 수 있으며, 원인에 따라 증상이 약간씩 변화한다.[20][21] 약물에 의한 간염의 경우는 발진, 발열, 세로시스염(특정 장기에 안착하는 막의 팽창), 상승된 어시노필(백혈구의 일종), 골수활동 억제 등 알레르기 반응의 전신 징후로 나타날 수 있다.[20]
과민성 간염
과민성 간염, 즉 대규모 간세포 사망은 약물유발 및 자가면역형 간염 외에 B, D, E형 간염의 경우 발생할 수 있는 드물고 생명을 위협하는 합병증이다.[16][20][21] 합병증은 B형 간염과 D형 간염의 경우 2~20%의 비율로, E형 간염의 경우 15~20%의 비율로 임산부에게서 더 자주 발생한다.[16][17] 급성 간염의 징후 외에도 응고병증(타박상과 출혈이 쉬운 비정상적인 응고 연구)과 뇌병증(충돌, 방향감퇴, 졸림)의 징후를 보일 수 있다.[16][17] 완충성 간염으로 인한 사망률은 일반적으로 뇌부종, 위장 출혈, 패혈증, 호흡부전, 신부전 등 다양한 합병증의 결과물이다.[16]
만성간염
급성 간염은 6개월 내에 잘 해결되는 것으로 보인다. 간염이 6개월 이상 지속되면 만성간염이라고 한다.[22] 만성간염은 진로에 초기에 증상이 없는 경우가 많으며, 검사를 목적으로 하거나 비특정 증상을 평가하기 위해 간 실험실 연구에서만 발견된다.[18][19] 염증이 진행되면 급성 간염과 비슷한 체질적 증상이 나타나 피로, 메스꺼움, 구토, 식욕부진, 관절통 등이 생길 수 있다.[19] 황달은 또한 발생할 수 있지만, 훨씬 늦게 질병 과정에 발생하며, 전형적으로 발전된 질병의 징후다.[19] 만성간염은 간 호르몬 기능을 방해해 여성에게 여드름, 히르수티즘(이상 모발 성장), 아메노레아(월경기 부족) 등을 유발할 수 있다.[19] 시간이 지남에 따라 간에서 발생하는 광범위한 손상과 흉터는 간경변증을 정의하는데, 간기능 능력이 영구적으로 저해되는 질환이다.[18] 이로 인해 황달, 체중 감소, 응고병증, 복수증(악수액 채취), 말초부종(다리 붓기)이 발생한다.[19] 간경변은 간뇌증, 식도정맥증, 간막증후군, 간암과 같은 다른 생명을 위협하는 합병증으로 이어질 수 있다.[18]
원인들
간염의 원인은 감염성, 대사성, 허혈성, 자가면역, 유전성 등의 주요 범주로 나눌 수 있다. 전염성 물질은 바이러스, 박테리아, 기생충을 포함한다. 대사 원인으로는 처방약, 독소(주로 알코올), 비알코올성 지방간 질환 등이 있다. 간염의 자가면역 및 유전적 원인은 유전적 소인을 수반하며 특징적인 모집단에 영향을 미치는 경향이 있다.
전염성
바이러스성 간염
바이러스성 간염은 전 세계적으로 가장 흔한 유형의 간염이다.[23] 바이러스성 간염은 5가지 바이러스(Hepatitis A, B, C, D, E)에 의해 발생한다.[16] A형 간염과 E형 간염은 유사하게 행동한다. 둘 다 배설-구강 경로에 의해 전염되고 개발도상국에서 더 흔하며 만성 간염으로 이어지지 않는 자기제한성 질환이다.[16][24][25]
B형 간염, C형 간염, D형 간염은 정액, 질 분비물 등 감염된 혈액과 체액에 혈액이나 점막이 노출되면 전염된다.[16] 침과 모유에서도 바이러스 입자가 발견되었다. 그러나 키스, 공유기구, 모유수유 등은 이러한 액체가 열린 상처나 상처에 유입되지 않는 한 전염으로 이어지지 않는다.[26]
B형 간염과 C형 간염은 급성 또는 만성적으로 나타날 수 있다.[16] D형 간염은 B형 간염의 복제가 필요한 결함이 있는 바이러스로 B형 간염의 공동감염과 함께만 발견된다.[16] 성인의 경우 B형 간염 감염이 가장 흔하게 자가 제한되는데, 만성질환자는 5% 미만이 진행되며 만성질환자의 20~30%가 간경변이나 간암에 걸리게 된다.[27] 그러나 영유아 감염은 만성 감염으로 이어지는 경우가 많다.[27]
B형 간염과 달리 C형 간염은 만성 감염으로 이어지는 경우가 대부분이다.[28] C형 간염은 미국에서 간경변의 두 번째로 흔한 원인이다.[29] 1970년대와 1980년대에는 수혈이 C형 간염 바이러스를 확산시키는 주요 요인이 되었다.[28] 1992년 C형 간염에 대한 혈액제제의 광범위한 검진이 시작된 이후 수혈로 C형 간염에 걸릴 위험은 1970년대 약 10%에서 현재 200만분의 1로 줄었다.[16]
기생간염
기생충은 간을 감염시키고 면역반응을 활성화시켜 혈청 IgE가 증가된 급성간염 증상(만성간염은 만성감염으로 가능함)을 유발하기도 한다.[30] 원생동물 중 트라이파노소마 크루지, 라이프마니아종, 말라리아를 유발하는 플라스모듐종 등이 모두 간염증을 일으킬 수 있다.[30] 또 다른 원생동물인 엔타메바 히스토리티카는 간 종기가 뚜렷한 간염을 유발한다.[30]
지렁이 중에서 개 테이프벌레라고도 알려진 세스토드 에치노코쿠스 그라눌로수스는 간을 감염시켜 특징적인 간수성 낭종을 형성한다.[30] 간은 파시올라 간낭염과 클로노르치스 시넨시스는 담즙관에 살면서 진행성 간염과 간섬유화를 일으킨다.[30]
세균성 간염
간의 박테리아 감염은 일반적으로 화농성 간 종기, 급성 간염 또는 과립성 간질환을 유발한다.[31] 화인성 종기는 대장균, 클레브시엘라 진폐증과 같은 장내세균을 주로 포함하며, 최대 50%까지 복수의 박테리아로 구성된다.[31] 급성 간염은 네이세리아 메닌기티디스, 네이세리아 고노르후아, 바르토넬라 헨젤레, 보렐리아 버그도페리, 살모넬라 종, 브루셀라 종, 캠필로박터 종에 의해 발생한다.[31] 만성 또는 과립성 간염은 미코박테리아 종, 트로페리마 휘플피, 트레포네마 팔리디움, 코시엘라 버네티이, 리케치아 종에서 감염되어 나타난다.[31]
대사
알코올성 간염
과도한 알코올 섭취는 간염의 중요한 원인이며 미국에서 간경변의 가장 흔한 원인이다.[29] 알코올성 간염은 알코올성 간질환의 범위 내에 있다. 이는 알코올성 기질증(최소 중증, 가장 가역성), 알코올성 간염, 간경화증(최소 가역성), 간암(최소 가역성)으로부터 중증도와 가역성의 순서로 나타난다.[29] 간염은 보통 알코올에 수년 동안 노출되며 알코올 중독자의 10~20%에서 발생한다.[32] 알코올성 간염의 발달을 위해 가장 중요한 위험요인은 양과 알코올 섭취 기간이다.[32] 남성의 경우 하루 80g, 여성의 경우 하루 40g이 넘는 장기 알코올 섭취는 알코올성 간염(맥주 1개 또는 와인 4온스는 알코올 12g에 해당한다)[29] 발병과 관련이 있다. 알코올성 간염은 무증상 간염(간염에 걸리기)부터 급성 또는 만성 간염의 증상, 간 기능 부전에 이르기까지 다양할 수 있다.[29]
독성 및 약물유발성 간염
약물, 산업용 독소, 약초와 식이 보조제를 포함한 많은 화학 물질들은 간염을 일으킬 수 있다.[33][34] 약물에 의한 간 손상의 범위는 급성 간염부터 만성 간염까지 다양하다.[33] 독소와 약물은 직접 세포 손상, 세포 대사 방해, 구조적 변화 등 다양한 메커니즘을 통해 간 손상을 일으킬 수 있다.[35] 파라세타몰과 같은 약물은 예측 가능한 용량 의존성 간 손상을 보이는 반면 이소니아지드 같은 약물은 개인마다 다른 특이성과 예측 불가능한 반응을 일으킨다.[33] 간 손상과 잠복기의 메커니즘은 노출부터 임상 질환의 발달에 이르기까지 매우 큰 차이가 있다.[29]
Many types of drugs can cause liver injury, including the analgesic paracetamol; antibiotics such as isoniazid, nitrofurantoin, amoxicillin-clavulanate, erythromycin, and trimethoprim-sulfamethoxazole; anticonvulsants such as valproate and phenytoin; cholesterol-lowering statins; steroids such as oral contraceptives and anabolic steroids; and highlHIV/AIDS 치료에 사용되는 y 활성 항레트로바이러스 요법.[29] 이 중 아목시실린-클라불란산염은 약물유발성 간손상의 가장 흔한 원인이며 파라세타몰 독성은 미국과 유럽에서 가장 흔한 급성간 기능부전의 원인이다.[33]
약초요법과 식이 보조제는 간염의 또 다른 중요한 원인이다; 이것들은 한국에서 약물로 인한 간염의 가장 흔한 원인이다.[36] 미국계 약물유발 간손상 네트워크는 간독성 사례의 16% 이상을 약초 및 식이 보조제와 연계시켰다.[37] 미국에서는 약물과 달리 약초와 식이 보조식품은 식품의약품안전청에 의해 규제를 받지 않는다.[37] 그러나 국립보건원은 소비자가 간 손상과 관련된 모든 알려진 처방 및 비처방 화합물을 추적할 수 있도록 LiverTox 데이터베이스를 유지한다.[38]
다른 간독소에 대한 노출은 섭취, 흡입, 피부 흡수를 통해 우발적으로 또는 의도적으로 발생할 수 있다. 산업용 독소인 테트라클로라이드와 야생 버섯 아마니타 팔로이드는 다른 알려진 간독소들이다.[33][34][39]
비알코올성 지방간 질환
비알코올성 간염은 비알코올성 간질환(NAFLD)부터 비알코올성 지방간염(NASH)에서 간암에 이르는 간경변까지 심각성과 가역성이 범위인 비알코올성 간염(NALD)의 스펙트럼 내에 있는데, 이는 알코올성 간질환의 스펙트럼과 유사하다.[40]
비알코올성 간질환은 알코올 사용 이력이 거의 없거나 없는 사람에게 발생하며, 대신 대사증후군, 비만, 인슐린 저항성 및 당뇨, 고트리거성혈증 등과 강하게 연관된다.[29] 시간이 지나면서 비알코올성 지방간 질환은 비알코올성 지방간염으로 진행될 수 있으며, 이는 간세포 사망, 간염, 섬유화 가능성 등을 추가로 수반한다.[29] NAFLD에서 NASH로의 진행을 가속화하는 요인은 비만, 고령, 아프리카계 미국인이 아닌 민족, 여성, 당뇨병, 고혈압, ALT 또는 AST 수준, 높은 AST/ALT 비율, 낮은 혈소판 수, 초음파 기형성 점수 등이다.[29]
초기(NAFLD, 초기 NASH와 마찬가지로) 대부분의 환자는 증상이 없거나 가벼운 우측 상부 사분면 통증이 있으며, 이상 간 기능 검사를 근거로 진단이 의심된다.[29] 병이 진행되면 만성간염의 대표적인 증상이 나타날 수 있다.[41] 영상촬영은 지방간을 나타낼 수 있지만, 간 조직검사만이 NASH의 염증 및 섬유화 특성을 나타낼 수 있다.[42]NASH 환자의 9~25%가 간경변증을 일으킨다.[29] NASH는 미국에서 세 번째로 흔한 간질환의 원인으로 인정받고 있다.[41]
자가면역
자가면역형 간염은 간세포에 대한 면역반응이 비정상적으로 일어나면서 생기는 만성질환이다.[43] 이 질병은 면역 반응에 관여하는 특정한 인간 백혈구 항원과 연관되어 있기 때문에 유전적 소인이 있는 것으로 생각된다.[44] 다른 자가면역질환처럼 순환하는 자가면역체가 있을 수 있고 진단에 도움이 된다.[45] 자가면역형 간염 환자에게서 발견되는 자가항체로는 민감하지만 구체성이 떨어지는 항핵항체(ANA), 평활근항체(SMA), 비정형 과불핵항체 세포질항체(p-ANCA) 등이 있다.[45] 자가면역성 간염에 대한 일반성은 떨어지지만 자가면역성 간염에 더 특유한 다른 자가항체로는 간신장 마이크로썸 1(LKM1)과 수용성 간항원(SLA)에 대한 항체가 있다.[45] 자가면역형 간염은 간 이식 후 약물(니트로푸란토닌, 하이드랄라진, 메틸도파 등), 바이러스(A형 간염, 엡스타인-바르 바이러스, 홍역 등)에서도 유발할 수 있다.[29]
자가면역형 간염은 무증상, 급성 또는 만성 간염, 완전 간기능 장애에 이르기까지 스펙트럼 내 어디에나 나타날 수 있다.[29] 환자는 무증상 25~34%로, 이상 간 기능 검사를 근거로 진단이 의심된다.[45] 일부 연구는 25%에서 75% 사이의 급성 간염의 징후와 증상을 보이는 것을 보여준다.[29][46] 다른 자가면역질환과 마찬가지로 자가면역형 간염은 대개 젊은 여성들에게 영향을 미치며(어느 연령의 어느 성별이나 환자에게도 영향을 미칠 수 있지만), 환자는 피로, 빈혈, 거식증, 아메노레아, 여드름, 관절염, 늑막염, 갑상선염, 궤양성대장염, 신장염, 황혈성 r과 같은 자가면역증의 고전적인 징후와 증상을 나타낼 수 있다.재.[29] 자가면역 간염은 간경변 위험을 증가시키며, 간암에 걸릴 위험은 매년 약 1%씩 증가한다.[29]
자가면역 간염에 걸린 많은 사람들은 다른 자가면역 질환을 가지고 있다.[47] 자가면역형 간염은 간에서 발생하는 다른 자가면역질환인 1차 담도경변증, 1차 경화성 담낭염과는 구별된다. 그러나 이 모든 질병은 간장의 흉터, 섬유증, 간경변으로 이어질 수 있다.[29][45]
유전의
간염의 유전적 원인으로는 알파-1 항티트립신 결핍증, 헤모크롬증, 윌슨병 등이 있다.[29] 알파-1-항미트립신 결핍증에서는 알파-1-항미트립신 유전자의 공동지배인 돌연변이가 간세포 내에 돌연변이인 AAT 단백질이 비정상적으로 축적되어 간질환으로 이어진다.[48] 혈색소증과 윌슨병은 모두 광물의 비정상적인 저장을 수반하는 자가 열성 질환이다.[29] 혈색소증에서는 간을 포함한 여러 신체 부위에 철분의 과다량이 축적되어 간경변으로 이어질 수 있다.[29] 윌슨병에서는 과도한 양의 구리가 간과 뇌에 축적되어 간경변과 치매를 일으킨다.[29]
간이 관련되면 알파-1 항티트립신 결핍증, 윌슨병 등이 신생아기나 유년기에 간염으로 나타나는 경향이 있다.[29] 혈색소증은 일반적으로 성인기에 나타나며, 대개 50세 이후에 임상 질환이 시작된다.[29]
허혈성 간염
허혈성 간염(충격 간이라고도 한다)은 간으로 가는 혈류가 감소하여 쇼크, 심부전, 혈관부전 등의 증상이 나타난다.[49] 이 질환은 심부전과 가장 자주 연관되지만 충격이나 패혈증으로 인해 발생할 수도 있다. 허혈성 간염에 걸린 사람에 대한 혈액검사에서 매우 높은 수준의 트랜스아미노효소(AST와 ALT)가 나타날 것이다. 이 상태는 보통 근본 원인이 성공적으로 치료되었는지 여부를 해결한다. 허혈성 간염은 영구적인 간 손상을 거의 일으키지 않는다.[50]
기타
간염은 신생아에게도 발생할 수 있으며 다양한 원인에 기인하는데, 그 중 일부는 일반적으로 성인에게서 볼 수 없다.[51] 간염 바이러스, 톡소플라즈마, 풍진, 사이토메갈로바이러스, 매독에 의한 선천성 또는 근위기에 의한 감염은 신생아 간염을 유발할 수 있다.[51] 담도폐쇄증, 담도낭종 등 구조적 이상이 생기면 간염으로 인한 담수성 간 손상으로 이어질 수 있다.[51] 글리코겐 저장장애, 라이소솜 저장장애 등 대사질환도 연루돼 있다.[51] 신생아 간염은 특발성 간염일 수 있으며, 이런 경우 조직검사에서 간조직에 큰 다핵세포가 나타나는 경우가 많다.[52] 이 질병은 거대 세포간염이라고 불리며 바이러스 감염, 자가면역 장애, 약물 독성과 관련이 있을 수 있다.[53][54]
메커니즘
구체적인 메커니즘은 다양하며 간염의 근본적인 원인에 따라 달라진다. 일반적으로 간 손상과 염증반응의 활성화를 유발하는 초기 모독이 있는데 만성화돼 진행성 섬유화와 간경변으로 이어질 수 있다.[16]
바이러스성 간염
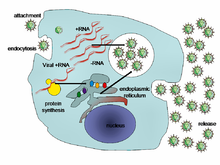
간염 바이러스가 바이러스성 간염을 일으키는 경로는 B형, C형 간염의 경우 가장 잘 이해된다.[16] 그 바이러스는 세포사멸을 직접적으로 활성화시키지 않는다.[16][55] 오히려 간세포의 감염은 면역체계의 선천적이고 적응적인 팔을 활성화시켜 세포 손상과 사망을 유발하는 염증반응을 일으키는데, 여기에는 사망수용체 매개 신호 경로 유도를 통한 바이러스성 사멸이 포함된다.[16][55][56][57] 면역반응의 강도, 관련 면역세포의 종류, 바이러스의 방어 회피 능력에 따라 감염은 바이러스의 간극(급성질환)이나 지속성(만성질환)으로 이어질 수 있다.[16] 간세포 내에 바이러스가 만성적으로 존재하게 되면 염증, 부상, 상처치유의 여러 파동이 일어나 시간이 흐르면서 흉터나 섬유증으로 이어지며 간세포암으로 절정에 이르게 된다.[55][58] 면역반응이 손상된 개인은 만성감염에 걸릴 위험이 더 크다.[16] 자연 킬러 세포는 초기 선천적 반응의 일차적 동인이며 CD4 T-헬퍼와 CD8 세포독성 T-세포의 모집을 초래하는 사이토카인 환경을 조성한다.[59][60] I형 인터페론은 항바이러스 반응을 일으키는 사이토카인이다.[60] 만성 B형 간염과 C형 간염에서는 자연적인 킬러 세포 기능이 손상된다.[59]
스테아토헤페티염
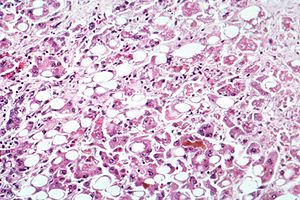
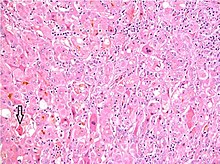
스테아토헤페염은 알코올성 간질환과 비알코올성 간질환 모두에서 볼 수 있으며, 부상과 함께 시작된 일련의 사건들의 정점이다. 비알코올성 치주염의 경우 비만, 인슐린 저항성, 지질 이상 조절과 관련된 신진대사의 변화에 의해 이 계단식 발작이 시작된다.[61][62] 알코올성 간염에서는 만성 과다 알코올 섭취가 원인이다.[63] 선동적인 사건은 다를 수 있지만 사건의 진행은 유사하며 스테아토시스라고 불리는 과정에서 자유지방산(FFA)과 그 분해물이 간세포에 축적되면서 시작된다.[61][62][63] 이 초기에는 되돌릴 수 있는 과정은 지방 분자가 축적되어 산화성 스트레스 반응의 설정에서 분해되면서 독성 효과로 이어지는 지방성 동점선을 유지하는 간세포의 능력을 압도한다.[61][62][63] 시간이 지남에 따라 이 비정상적인 지질 침착은 톨러이 같은 수용체 4(TLR4)를 통해 면역체계를 자극해 간세포 손상과 사망을 일으키는 TNF와 같은 염증성 사이토카인이 생성된다.[61][62][63] 이러한 사건들은 스테아토페염으로의 전환을 나타내며 만성적인 부상의 상황에서, 섬유증은 결국 간경변과 간세포암을 유발하는 사건들을 설정하게 된다.[61] 현미경적으로 볼 수 있는 변화로는 간세포가 크고 부은 기형성증(발기), 세포손상 및 세포사멸의 증거(절제, 괴사), 특히 간 3구역에서의 염증의 증거, 가변적인 정도의 섬유화 및 말로리 체질이 있다.[61][64][65]
진단
| 가장 높은 아미노트란스페라아제 | 원인 |
|---|---|
| ALT | 만성 B, C, D형 간염 |
| 비알코올성 간질환 | |
| 급성 바이러스성 간염 | |
| 약물/독신 | |
| 자가면역간염 | |
| 윌슨병 | |
| 알파-1-안티트립신 결핍증 | |
| 헤모크로마토증 | |
| 허혈성 간염(심각한 고도 수천까지) | |
| AST | 알코올성 간질환 |
| 간경변 |
간염 진단은 사람의 증상과 증상, 성·물질 사용 이력, 혈액검사, 영상검사, 간 생체검사 등 일부 또는 전부에 근거해 이루어진다.[29] 일반적으로 바이러스성 간염과 기타 급성 간염 원인에 대해서는 그 사람의 혈액검사와 임상사진으로 진단하기에 충분하다.[16][29] 간염의 다른 원인들, 특히 만성적인 원인에 대해서는 혈액 검사가 유용하지 않을 수 있다.[29] 이 경우 간 조직검사는 진단 확립의 금본위제다:조직병리학적 분석은 염증과 섬유화의 정확한 범위와 패턴을 밝혀낼 수 있다.[29] 그러나 간 조직검사는 침습적이고 간경변증 환자에게서 증가되는 출혈의 위험성이 작지만 유의한 것과 관련이 있기 때문에 일반적으로 초기 진단검사가 아니다.[66]
혈액 검사에는 간 효소, 세리학(즉 자가 항균의 경우), 핵산 검사(즉 간염 바이러스 DNA/RNA의 경우), 혈액 화학 및 완전 혈액수가 포함된다.[29] 간효소 기형의 특징적인 패턴은 간염의 특정 원인이나 단계를 가리킬 수 있다.[67][68] 일반적으로 AST와 ALT는 그 사람이 어떤 증상을 보이든 상관없이 대부분의 간염에서 상승한다.[29] 단, 고도 정도(즉, 수백 대 수천의 수준), AST 대 ALT 고도에 대한 우위, AST와 ALT의 비율이 진단에 유용하다.[29]
초음파, CT, MRI는 모두 간경변증을 암시하는 간조직의 기형성(지방 변화)과 결절성을 확인할 수 있다.[69][70] CT와 특히 MRI는 더 높은 수준의 디테일을 제공할 수 있어 간 내의 혈관이나 종양과 같은 구조를 시각화하고 특성화할 수 있다.[71] 스테아토시스나 간경변과 달리 간염(간염)이나 섬유증을 검출할 수 있는 영상검사는 없다.[29] 간 조직검사는 간의 염증과 섬유증을 평가할 수 있는 유일한 결정적인 진단검사다.[29]
바이러스성 간염
바이러스성 간염은 주로 바이러스 항원(B형 간염 표면 또는 코어 항원 등), 항바이러스 항체(B형 간염 표면 항체 또는 A형 항체 등) 또는 바이러스 DNA/RNA의 수준에 대한 혈액 검사를 통해 진단되며,[16][29] 조기 감염(즉 1주일 이내) 시 IgM 항체가 혈액에서 발견된다.[29] 늦은 감염과 회복 후에 IgG 항체는 존재하며 최대 몇 년 동안 체내에 남아 있다.[29] 따라서 환자가 IgG항체에는 양성이지만 IgM항체에는 음성이면 사전 감염과 회복 또는 사전 예방접종을 통해 바이러스에 면역된 것으로 간주된다.[29]
B형 간염의 경우 복수의 바이러스 항원(바이러스 입자의 다른 성분)과 항체에 대한 혈액 검사가 존재한다.[72] 항원과 항체 긍정의 결합은 감염 단계(급성 또는 만성), 바이러스 복제 정도, 바이러스의 감염성 등에 대한 정보를 제공할 수 있다.[72]
알코올 대 비알코올성
알코올성 치주염(ASH)과 비알코올성 치주염(NASH)의 가장 뚜렷한 구분 요인은 과도한 알코올 사용의 역사다.[73] 따라서 알코올 사용량이 없거나 무시해도 되는 환자의 경우 이 진단은 알코올성 간염일 가능성이 낮다. 그러나 알코올을 사용하는 사람들의 경우 특히 동시 비만, 당뇨병, 대사 증후군이 있는 경우 이 진단은 알코올성 간염이나 비알코올성 간염일 가능성이 있다. 이 경우 알코올성 간염과 비알코올성 간염은 간 효소 이상 패턴으로 구별할 수 있다. 특히, 알콜성 치주염 AST>ALT에서 AST 비율:ALT>2:1 비알코올성 치주염 ALT>AST:AST>1.5:1.[73]
특히 간 조직검사에서 ASH와 NASH 환자에게서 동일한 소견이 관찰되는데, 특히 다형질핵 침투, 간세포 괴사 및 사멸의 존재, 풍선 퇴화 형태의 간세포 괴사, 말로리체, 정맥과 시누스 주변의 섬유화 등이 나타난다.[29]
바이러스성 간염 검사
바이러스성 간염 검사의 목적은 증상과 트랜스미나제 상승이 나타나기도 전에 가능한 한 빨리 감염자를 가려내는 것이다. 이를 통해 조기 치료가 가능해져 질병 진행을 막고 다른 사람에게 전염될 가능성을 줄일 수 있다.
A형 간염
A형 간염은 만성 간질환으로 진행되지 않는 급성질환을 유발한다. 따라서 A형 간염의 감염이 간기능저하로 이어질 수 있는 알려진 간질환자뿐만 아니라 바이러스에 감염될 위험이 높은 사람에게도 면역 상태를 평가하는 것이 검진의 역할이다.[74][75] 이들 집단에서 아직 면역력이 없는 사람은 A형 간염 백신을 접종할 수 있다.
위험성이 높고 심사가 필요한 대상자는 다음과 같다.[76][77][78]
- 화장실 사용 후 손을 씻지 않거나 기저귀를 갈지 않는 등 위생습관이 나쁜 사람
- 깨끗한 물을 이용할 수 없는 사람들
- A형 간염에 걸린 사람과 밀접하게 접촉하는 사람(생존하거나 성적으로 접촉하는 사람)
- 불법 약물을 사용하는 사람들
- 간질환자
- 지방성 A형 간염 지역 여행자
혈액에 항혈당염 A IgG가 있다는 것은 과거 바이러스 감염이나 사전 예방접종을 했다는 것을 알 수 있다.[79]
B형 간염
CDC, WHO, USPSTF, ACOG는 특정 고위험군에 대해 정기적인 B형 간염 검진을 권고한다.[80][81][82][83] 특히 이러한 모집단에는 다음과 같은 사람들이 포함된다.
- B형 간염의 유병률이 높은 나라(인구 ≥2%로 정의됨), 예방접종[80][81] 여부와 관계없이 출생한다.
- 미국에서 태어나 B형 간염의 유병률이 매우 높은 나라(인구 of8%로 정의됨) 출신이며 예방접종을[80][81] 받지 않은 사람
- HIV 양성자[80][81][82]
- 정맥주사 약물 사용자[80][81][82]
- 남자들과 섹스를 하는 남자[80][81][82]
- B형[80][81][82] 간염에 걸린 것으로 알려진 사람들과 밀접하게 접촉(즉, 생활하거나 성관계를 갖는 것)한다.
- 임신한[80][81][83]
- 면역억제 또는 세포독성 치료[80] 시작
- 알려진 원인[80] 없이 간 효소가 증가된 것으로 확인됨
- 혈액, 장기 또는 조직 기증자[82]
- 투옥된[82]
- 혈액[80] 투석 시
검진은 B형 간염 표면항원(HBsAg)을 검출하는 혈액검사로 구성된다. HBsAg가 존재할 경우, B형간염 핵심항원(항-HBcAg)의 항체를 검출하는 두 번째 검사로 급성 감염과 만성 감염을 구별할 수 있다.[80][84] 혈액검사에서 HBsAg 음성 판정을 받은 고위험군은 B형 간염 백신을 접종해 향후 감염을 예방할 수 있다.[80][81][82][83]
C형 간염
CDC, WHO, USPSTF, AASLD, ACOG는 C형 간염에 걸릴 위험이 높은 사람들을 선별할 것을 권고한다.[83][85][86][87][9] 이러한 모집단에는 다음과 같은 사람들이 포함된다.
- 정맥주사 약물 사용자(과거 또는 현재)[85][86][87][9]
- 불법 마약 사용자[85][86][87][9]
- HIV[85][86][87][9] 양성자
- 남자들과[9] 섹스를 하는 남자
- 투옥되거나 과거에[85][86][87][9] 있었던 사람들
- 장기적 혈액투석 또는 과거에[85][86][87][9] 있었던 사람
- "비규제 설정"[87][9]의 문신 받는 사람
- 1992년 이전에 미국에서[85][87][9] 혈액제제 또는 장기를 받은 사람
- 1945년부터 1965년[87][9] 사이에 태어난 미국의 성인
- HCV 양성 엄마에게서[9] 태어났다.
- 임신 중이고 위험성이 높은 행동을[83] 하는 경우
- 의료 환경에서 바늘에 찔리는 부상을[9] 입은 근로자
- 혈액 또는 장기 기증자.[9]
- 성노동자[86]
USPSTF에 따르면, 연구는 최적의 선별 간격을 정의하지 않았지만, 노출이 진행 중인 위 그룹의 사람들에게 선별은 "주기적"이어야 한다.[87] AASLD는 매년 HIV 양성 남성과 성관계를 가진 남성을 선별할 것을 권고하고 있다.[9] 1945년부터 1965년 사이에 미국에서 태어난 사람들은 (다른 노출 위험이 없는 한) 한 번 검사를 받아야 한다.[85][87][9]
검진은 혈액검사에서 항혈당성 C형 바이러스 항체를 검출하는 방식으로 이뤄진다. 항혈당염 C 바이러스 항체가 존재할 경우 HCV RNA를 검출하기 위한 확인검사에서 만성질환이 나타난다.[86][9]
예방
백신
A형 간염
질병관리본부는 A형 간염 백신은 1세부터 시작하는 모든 어린이와 기존에 예방접종을 받지 않아 질병에 걸릴 위험이 높은 어린이에게 권장하고 있다.[76][77]
12개월 이상 어린이의 경우 6~18개월 간격으로 2회 복용 시 근육에 주사할 수 있으며 24개월 전에 예방접종을 시작해야 한다.[88] 성인은 백신 종류에 따라 복용량이 조금씩 다르다. 백신 접종이 A형 간염 전용일 경우 제조사에 따라 6~18개월 간격으로 2회 투여한다.[78] A형 간염과 B형 간염을 합친 경우 최대 4회까지 복용이 필요할 수 있다.[78]
B형 간염
질병관리본부는 B형 간염 백신을 19세 미만 모든 아동에게 정기적인 예방접종을 권고하고 있다.[89] 희망하거나 위험성이 높은 사람에게도 추천한다.[77]
B형 간염에 대한 정기적인 예방접종은 신생아가 병원에서 퇴원하기 전에 근육에 주사로 투여된 첫 번째 투여로 시작된다. 아이가 18개월이 되기 전에 2회 추가 투여해야 한다.[88]
B형 간염 표면 항원 긍정을 가진 산모에게서 태어난 아기들의 경우, 첫 번째 복용량은 독특하다. 백신 외에도, 간염 면역 글로불린도 생후 12시간 이내에 투여해야 한다. 이 신생아들은 또한 적어도 생후 1년 동안은 정기적으로 감염 검사를 받아야 한다.[88]
A형 간염과 B형 간염 백신을 모두 포함하는 복합제형도 있다.[90]
기타
현재 미국에는 C형 간염이나 E형 간염에 사용할 수 있는 백신이 없다.[86][91][92] 2015년 중국의 한 단체는 E형 간염 백신 개발 관련 기사를 실었다.[93] 2016년 3월 현재 미국 정부는 E형 간염 백신의 4단계 임상시험 참가자를 모집하는 중이었다.[94]
행동 변화
A형 간염
A형 간염은 주로 구강변통로를 통해 전염되기 때문에 예방접종 외에 예방의 주축은 위생상태가 양호하고 깨끗한 물을 접하고 하수처리도 제대로 하는 것이다.[77]
B·C형 간염
예방은 B형 간염과 C형 간염이 혈액과 여러 체액을 통해 전염되기 때문에 수혈 전 혈액검사와 주사제 사용 기권, 건강관리 환경에서의 안전한 바늘과 날카로운 시술, 안전한 성행위 등이 목적이다.[27][86]
D형 간염

D형 간염 바이러스는 우선 B형 간염 바이러스에 감염돼야 하므로 예방 노력은 B형 간염의 확산을 제한하는 데 집중해야 한다. 만성 B형 간염에 감염돼 D형 간염에 슈퍼감염될 위험이 있는 사람의 경우 예방전략은 B형 간염과 같다.[92]
E형 간염
E형 간염은 주로 구강혈통 경로를 통해 전파되지만 혈액 및 산모에서 태아로 전파될 수도 있다. E형 간염 예방의 주축은 A형 간염(명칭 위생과 깨끗한 물 사용)과 비슷하다.[91]
알코올성 간염
과도한 알코올 섭취는 간염과 간경변으로 이어질 수 있으므로 알코올 섭취에 대한 최대 권고는 다음과 같다.[96]
- 여성 – 주어진 날짜에 3잔, 주당 7잔
- 남자 – 주어진 날짜에 4잔, 주당 14잔
성공
A형 간염
미국에서는 보편적 면역으로 인해 A형 간염으로 병원 입원과 의료비가 3분의 2 수준으로 감소하고 있다.[97]
B형 간염
미국에서 B형 간염의 새로운 경우는 1990년부터 2004년까지 75% 감소했다.[98] 가장 큰 감소를 보인 집단은 1999년 가이드라인 시행을 반영했을 가능성이 높은 어린이와 청소년이었다.[99]
C형 간염
C형 간염은 1980년대 이후 매년 감소해 왔으나 2006년부터 다시 증가하기 시작했다.[100] 그 데이터는 그 감소가 바늘 교환 프로그램에 기인할 수 있는지에 대한 불확실하다.[101]
알코올성 간염
알코올성 간염에 걸린 사람들은 아무런 증상이 없을 수 있기 때문에 진단이 어려울 수 있고 그 병에 걸린 사람들의 수는 아마도 많은 추정치보다 많을 것이다.[102] 알코올 중독자 익명 등 프로그램은 간경변으로 인한 사망 감소에 성공했지만 알코올성 간염 발생률을 줄이는 데 성공했다고 평가하기는 어렵다.[103]
치료
간염의 치료는 급성이든 만성이든 종류에 따라, 병의 중증도에 따라 다르다.
- 활동: 간염에 걸린 많은 사람들은 회복하는 동안 모든 신체 활동을 피할 필요는 없지만, 침대 휴식을 선호한다.[16]
- 다이어트: 고칼로리 다이어트를 권장한다.[16] 많은 사람들이 메스꺼움을 느끼고, 늦은 시간에는 음식을 참지 못하기 때문에, 섭취량의 대부분이 이른 시간대에 집중될 수 있다.[16] 급성 질환 단계에서 환자가 음식을 참을 수 없고 구역질과 구토에 따른 구강 섭취가 불량할 경우 정맥주사가 필요할 수 있다.[16]
- 약물: 간염에 걸린 사람은 간에서 대사되는 약물을 복용하는 것을 피해야 한다.[16] 글루코코르티코이드는 급성 바이러스성 간염의 치료 옵션으로 권장되지 않으며 만성 간염의 발병 등 위해를 일으킬 수도 있다.[16]
- 주의사항: 일반적인 예방 조치를 준수해야 한다. 분변실실금증이 있는 A, E형 간염과 통제되지 않은 출혈이 있는 B, C형 간염의 경우를 제외하고는 대개 격리가 필요하지 않다.[16]
A형 간염
A형 간염은 보통 만성 상태로 진행되지 않고, 입원이 필요한 경우가 거의 없다.[16][76] 치료는 도움이 되며 정맥(IV) 수화 제공 및 적절한 영양 유지와 같은 조치를 포함한다.[16][76]
드물게 A형 간염 바이러스에 걸린 사람은 간기능저하로 불리며, 특히 노약자와 기존에 간질환이 있었던 사람, 특히 C형 간염으로 빠르게 발병할 수 있다.[16][76] 사망위험요인으로는 고령화와 만성 C형 간염 등이 있다.[16] 이런 경우 보다 적극적인 보조요법과 간 이식이 필요할 수 있다.[16]
B형 간염
급성
건강한 환자의 경우 95~99%는 오래 지속되는 효과가 없이 회복되며 항바이러스 치료는 보장되지 않는다.[16] 나이와 병세가 악화되면 질병이 더 길어지고 심각해질 수 있다. 특정 환자들은 입원을 보증하며, 특히 고환, 말초부종, 간뇌병증의 임상적 징후와 저혈당, 장기간의 프로트롬빈 시간, 낮은 혈청 알부민, 매우 높은 혈청 빌리루빈을 가지고 있는 환자들이다.[16]
이런 드물고 더 심각한 급성환자들은 엔테카비르나 테노포비르와 같은 뉴클레오사이드 유사성을 가지고 만성 B형 간염의 경우에서 사용되는 것과 유사한 항바이러스 요법으로 성공적으로 치료되어 왔다. 임상시험 자료가 부족하고 치료에 사용되는 약물은 내성이 생기기 쉬우므로 전문가들은 경증에서 중증까지가 아닌 중증 급성환자에 대해서는 치료비를 유보할 것을 권고한다.[16]
만성
만성 B형 간염 관리는 질병의 진행과 상관관계가 있는 바이러스성 복제를 억제하는 것이 목표다.[19] 미국에서는 7가지 약물이 승인된다.[19]
- 주사 가능한 인터페론 알파는 만성 B형 간염에 대해 승인된 첫 번째 치료법이었다.[19] 그것은 몇 가지 부작용을 가지고 있는데, 대부분은 치료의 제거로 되돌릴 수 있지만, 이 적응증에 대한 새로운 치료법으로 대체되었다.[19] 여기에는 폴리에틸렌 글리콜(피질화 인터페론)에 바인딩된 장작용 인터페론과 경구 뉴클레오시드 유사점이 포함된다.[19]
- 피하주사로 주 1회만 투여하는 PEG IFN(Pegulated Interferon, PEG IFN)은 표준 인터페론보다 편리하고 효과적이다.[19] 많은 구강 항바이러스제처럼 내성이 생기지는 않지만, 잘 견디지 못하고 면밀한 감시가 필요하다.[19] PEG IFN은 미국에서 연간 약 18,000달러가 소요될 것으로 추정되며, 경구용 약물의 경우 2,500달러–8,700달러가 소요된다. 그러나 치료 기간은 대부분의 환자에게 무기한 치료를 요구하는 경구용 항바이러스제(최소 1년)와는 대조적으로 48주이다.[19] PEG IFN은 바이러스 활동이 많은 환자에게는 효과가 없으며 면역억제 환자나 간경변 환자에게는 사용할 수 없다.[19]
- 라미부딘은 최초의 승인된 경구 뉴클레오사이드 아날로그였다.[19] 효과적이고 강력한 반면, 라미부딘은 서구 세계에서 더 새롭고 더 강력한 치료법으로 대체되었고 더 이상 첫 번째 치료로 추천되지 않는다.[19] 그러나 새로운 대리점이 승인되지 않았거나 비용이 너무 많이 드는 지역에서는 여전히 사용된다.[19] 일반적으로 치료 과정은 최소 1년, 최소 6개월의 '통합요법'이 추가된다.[19] 바이러스 반응에 기초해 보다 긴 치료가 필요할 수 있으며, 특정 환자는 무기한 장기 치료가 필요하다.[19] 아시아 환자들의 반응이 덜 건실해 통합요법은 최소 1년까지 연장하는 것이 좋다.[19] 모든 환자는 바이러스 재활성화를 모니터링해야 하며, 확인되면 치료를 다시 시작해야 한다.[19] 라미부딘은 일반적으로 안전하고 잘 용인된다.[19] 많은 환자들은 내성이 생기는데, 이것은 더 긴 치료 기간과 상관관계가 있다.[19] 이 경우 항바이러스제가 추가된다.[19] 단일 치료법으로서의 라미부딘은 저항력이 급속히 발달함에 따라 HIV에 동전으로 감염된 환자들에게 억제되지만, 다량의 약물 치료법의 일부로 사용될 수 있다.[19]
- 뉴클레오티드 아날로그인 아데포비르 디피폭실(Adefovir dipivoxil)은 저항력이 발달한 환자에게는 라미부딘을 보충하는 데 사용되어 왔으나, 더 이상 1선 치료로는 권장되지 않는다.[19]
- 엔테카비르는 안전하고, 잘 용인되며, 저항력이 덜하며, 현존하는 B형 간염 항바이러스 중 가장 강력한 치료제인 만큼, 1차 치료 선택이다.[19] 라미부딘 내성이 있는 환자나 HIV 양성 환자의 경우 단일요법으로 권장하지 않는다.[19]
- 텔비부딘은 효과적이지만 1차 치료로는 권장되지 않는다. 엔테카비르에 비해 효능이 떨어지고 저항력도 강하다.[19]
- 테노포비르(Tenofovir)는 뉴클레오티드 아날로그 물질이자 항레트로바이러스 약물로 HIV 감염 치료에도 쓰인다.[19] 라미부딘 내성이 있는 환자와 초기 치료 모두 아데포비르를 선호하는데, 이는 내성이 생길 가능성이 더 높고 덜 생기기 때문이다.[19]
현재 사용되는 1차 치료법으로는 환자 및 의사의 선호에 따라 PEG IFN, 엔테카비르, 테노포비르 등이 있다.[19] 치료 개시는 미국간질환연구협회(AASLD)와 유럽간연구협회(EASL)가 발표한 권고사항에 의해 안내되며, 검출 가능한 바이러스 수준, HBeAg 양 또는 음의 상태, ALT 수준, 그리고 특정 경우 HCC와 간 생체검사의 가족력 등을 기준으로 한다.[19] 보상성 간경변 환자의 경우 HBeAg 상태나 ALT 수준에 관계없이 치료를 권고하지만 HBV DNA 수준에 대해서는 권고사항이 다르다. AASLD는 2x103 IU/mL 이상에서 검출 가능한 DNA 수준에서 치료를 권고한다. EASL과 WHO는 HBV DNA 수치가 어떤 수준에서든 검출 가능한 경우 치료를 권고한다.[19][82] 간경변증 환자들의 경우 HBV DNA가 검출될 수 있는 경우라면 모든 경우에 간 이식에 대한 치료와 평가가 권장된다.[19][82] 현재 만성 HBV 치료에는 엔테카비르나 테노포비르를 사용한 개별 치료보다 장기적으로는 더 효과적이지 않기 때문에 다중 약물 치료가 권장되지 않는다.[19]
C형 간염
미국간질환연구회 및 전염병학회(AASLD-IDSA)는 기대수명을 제한하는 만성적인 만성질환자를 제외한 만성 C형 간염에 감염된 모든 환자에 대해 항바이러스 치료를 권고하고 있다.[9]
일단 획득되면 C형 간염 바이러스의 지속성이 원칙이어서 만성 C형 간염이 발생한다. 치료 목표는 간세포암(HCC) 예방이다.[104] HCC의 장기 위험을 줄이는 최선의 방법은 지속적인 바이러스 대응(SVR)을 달성하는 것이다.[104] SVR은 치료 완료 후 12주차에 감지할 수 없는 바이러스 부하로 정의되며 치료법을 나타낸다.[105][106] 현재 이용 가능한 치료법으로는 간접적이고 직접 작용하는 항바이러스제가 있다.[105][106] 간접 작용 항바이러스로는 피질화 인터페론(PEG IFN)과 리바비린(RBV)이 있는데, 역사적으로 결합하여 HCV 치료의 기초가 되어 왔다.[105][106] 이러한 치료의 지속 기간과 반응은 유전자형에 따라 다르다.[105][106] 이 요원들은 잘 견디지 못하지만 자원이 부족한 일부 지역에서 여전히 사용되고 있다.[105][106] 고자원 국가에서는 2011년에 처음 등장한 직접 작용 항바이러스제로 대체되었다. 이 작용제는 바이러스 복제를 담당하는 단백질을 대상으로 하며 다음 세 가지 등급이 포함된다.[105][106]
- NS3/4A 프로테아제 억제제(telaprevir, boceprevir, simeprevir 등)
- 레디파스비르, 다클라타스비르 등을 포함한 NS5A 억제제
- NS5B 중합효소 억제제(Sofosbuvir, dasabuvir 등)
이 약들은 다양한 조합으로 사용되며, 때로는 리바비린과 결합되어 환자의 유전자형에 기초하여 유전자형 1-6으로 디라인이 된다.[106] 미국과 전 세계에서 가장 보편적인 유전자형인 유전자형 1(GT1)은 이제 직접 작용하는 항바이러스 요법으로 치료할 수 있게 됐다.[106] GT1 1차 치료는 섬유증이나 간경변증이 진행된 환자를 포함해 대부분의 환자에게 12주 동안 소포스뷔르와 레디파스비르(SOF/LDV)를 혼합한 것이다.[106] 초기 질환을 앓고 있는 일부 환자는 8주만 치료를 받아야 하는 반면, 섬유증이나 간경변증이 진행된 환자는 사전 치료에 응하지 않은 경우 24주가 필요하다.[106] 비용은 특히 저자원 국가의 경우 이러한 약물에 대한 접근을 제한하는 주요 요인으로 남아있다; 12주간의 GT1 식사요법(SOF/LDV)의 비용은 미화 9만4,500달러로 추정되었다.[105]
D형 간염
D형 간염은 치료가 어렵고, 효과적인 치료법이 부족하다. 인터페론 알파는 바이러스 활동을 억제하는 데 효과적임이 증명되었지만 일시적 기준에서만 유효하다.[107]
E형 간염
A형 간염과 마찬가지로 E형 간염의 치료에도 도움이 되며 휴식과 적절한 영양과 수분이 보장된다.[108] 특히 심각한 경우나 임산부의 경우 입원이 필요할 수 있다.[108]
알코올성 간염
알코올성 간염의 첫 번째 치료는 알코올 중독 치료다.[32] 술을 완전히 삼가는 사람에게는 간질환의 역전이 가능하고 수명이 길어질 수 있으며, 모든 질환 단계의 환자들은 추가적인 간손상 예방으로 혜택을 보는 것으로 나타났다.[32][63] 치료는 심리치료와 다른 치료 프로그램에 대한 소개 외에도 영양학적, 심리학적 평가와 치료를 포함해야 한다.[32][63][109] 환자들은 또한 복통, 간뇌병증, 감염과 같은 관련 징후와 증상에 대해서도 적절하게 치료해야 한다.[63]
심각한 알코올성 간염은 예후가 좋지 않고 치료하기 힘들기로 악명 높다.[32][63][109] 어떤 치료도 받지 않으면 환자의 20-50%가 한 달 안에 사망할 수 있지만, 그 증거는 치료가 한 달 이상 수명을 연장할 수 있다는 것을 보여준다(즉, 단기 사망률을 감소시킨다).[32][109][110] 비특정 TNF 억제제인 펜톡시필린(PTX), 프레드니손이나 프레드니솔론(CS), 엔아세틸시스테인(NC와 함께 하는 CS), 펜톡시필린(PTX와 함께 하는 CS)[109]이 있는 코르티코스테로이드 등이 치료 옵션이다. 데이터에 따르면 CS 단독 또는 NAC와의 CS가 단기 사망률을 줄이는 데 가장 효과적이다.[109] 불행히도, 코르티코스테로이드들은 위장 출혈, 감염, 신장 기능 상실, 췌장염과 같은 몇몇 환자들에게 억제된다.[32][63] 이러한 경우 CS 대신 사례별로 PTX를 고려할 수 있다. 일부 증거는 PTX가 전혀 치료하지 않는 것보다 낫고 CS와 비교될 수 있다는 것을 보여주며, 다른 데이터는 위약보다 유익하다는 증거를 보이지 않는다.[109][110] 불행하게도, 현재 이러한 환자들의 장기적, 3-12개월 이상 사망 위험을 감소시키는 약물 치료는 없다.[109]
약한 증거는 밀크 엉겅퀴 추출물이 부작용을 일으키지 않고 알코올성 간 질환의 생존을 향상시키고 특정 간 검사(세럼 빌리루빈과 GGT)를 개선시킬 수 있다는 것을 암시하지만, 추가적인 연구 없이는 밀크 엉겅퀴에 대한 확실한 권고를 할 수 없다.[111]
자가면역간염
자가면역형 간염은 단독으로 또는 아자티오프린과 결합하여 간 합성이 필요 없는 활성판인 코르티코스테로이드 프리드니손이나 프레드니솔론과 같은 면역억제제에 의해 치료되는 것이 일반적이며, 일부에서는 코르티코스테로이드의 낮은 투여를 허용하기 위해 콤비네이션 요법이 선호된다는 의견을 제시하였다. 치료 효과의 결과가 비교적이긴 하지만 관련 부작용을 줄인다.[46][112]
자가면역 간염 치료는 초기 단계와 유지 단계라는 두 단계로 구성된다. 초기 단계는 더 많은 양의 코르티코스테로이드로 구성되며, 이 코르티코스테로이드들은 몇 주 동안 더 낮은 선량으로 줄였다. 조합하여 사용할 경우 초기 단계에서도 아자티오프린(Azathioprine)이 주어진다. 초기 단계가 완료되면 저선량 코르티코스테로이드로 구성된 유지단계, 그리고 결합요법에서는 간혈표지가 정상화될 때까지 아자티오프린으로 구성된다. 치료 결과 2년 만에 정상 간 검사값을 달성한 환자가 66~91%로 평균 22개월에 이른다.[46]
예후
급성 간염
거의 모든 A형 간염 환자들은 감염 전에 건강했다면 합병증 없이 완전히 회복된다. 마찬가지로 급성 B형 간염은 환자의 95~99%가 완치되는 데 유리한 코스를 가지고 있다.[16] 그러나, 어떤 요인들은 병세가 동반 악화되거나 복통, 부종 또는 뇌병증의 초기 증상을 보이는 것과 같은 더 나쁜 결과를 나타낼 수 있다.[16] 전체적으로 급성간염 사망률은 A, B형 간염의 경우 총 0.1%로 낮지만 특정 인구(B형, D형 간염, 임산부 등)에서는 사망률이 더 높아질 수 있다.[16]
A&B형 간염과 대조적으로 C형 간염은 만성간염으로 진행될 위험이 훨씬 높아 85~[113]90%에 육박한다. 간경변은 만성 C형 간염 환자의 20~50%에서 발병하는 것으로 보고되었다.
그 밖에 드물게 나타나는 급성간염 합병증으로는 췌장염, 재생불량성빈혈, 말초신경증, 심근염 등이 있다.[16]
과민성 간염
대부분의 바이러스성 간염의 비교적 양성인 과정에도 불구하고, 완충성 간염은 드물지만 두려운 합병증을 나타낸다. 과민성 간염은 B, D, E형 간염에서 가장 흔하게 발생한다. E형 간염의 약 1~2%는 완충성 간염으로 이어질 수 있지만 임신부는 특히 취약해 20%까지 발병한다.[114] 완충성 간염의 경우 사망률이 80% 이상 상승하지만 생존한 환자는 완치되는 경우가 많다. 간 이식 수술은 간기능 장애가 있는 환자에게는 생명을 구할 수 있다.[115]
D형 간염은 B형 간염의 양성 환자를 과민증이라고 알려진 중증 진행형 간염으로 변화시킬 수 있다.[116]
만성간염
급성 B형 간염은 환자의 연령이 높아질수록 만성적인 형태로 진행될 확률이 낮아지며, 유아의 경우 수직으로 전염되는 경우 진행률이 성인 위험률 1%에 비해 90%에 육박한다.[19] 전체적으로 만성 B형 간염의 5년 생존율은 경증의 경우 97%에서 간경변으로 심한 경우 55%에 이른다.[19]
B형 간염(공동감염)과 동시에 D형 간염에 걸리는 환자는 만성감염에 걸리지 않고 대부분 회복되지만, 나중에 D형 간염(과민감염)에 걸리는 B형 간염 환자의 경우 80~90%로 만성감염이 훨씬 흔하고 간질환 진행이 빨라진다.[107][117]
만성 C형 간염은 간경변으로 진행되는데, 간경변 유병률은 감염 후 20년이 되면 16%에 이른다고 추정한다.[118] C형 간염의 주요 사망원인은 말기 간질환이지만, 간세포암은 만성간염의 중요한 장기적 합병증이자 사망원인이다.
사망률은 기저 간질환의 진행에 따라 증가한다. HCV로 인한 보상형 간경변 환자는 35%, 10년 생존율은 각각 96%, 91%, 79%로 나타났다.[119] 간경변이 분해되면 5년 생존율이 50%로 떨어진다.
역학
바이러스성 간염
A형 간염
A형 간염은 전세계에서 발견되며 물과 식량의 배설물 오염과 관련된 대규모 발병과 전염병으로 나타난다.[99] 간염 A형 간염은 유아가 드물게 감염되는 5~14세 아동에게 주로 감염된다.[99] 감염된 아동은 뚜렷한 임상 질환이 거의 없으며, 80% 이상이 감염되면 증상이 나타나는 성인과 대조적으로 볼 수 있다.[120] 감염률은 공중위생과 인구집중도가 높은 저자원 국가에서 가장 높다.[16][121] 이런 지역에서는 10세 미만 아동의 90%가 감염돼 면역력이 있는 것으로 나타나 임상적 증상 질환과 발병률이 모두 낮아졌다.[99][121][122] 소아백신의 사용가능성은 2013년 현재 발병률이 95% 이상 감소하는 등 미국 내 감염을 크게 줄였다.[123] 역설적으로, 새로운 감염의 가장 높은 비율은 현재 더 나쁜 임상 질환을 가진 젊은 성인들과 성인들에게서 발생한다.[16] 가장 위험한 특정 개체군에는 여행자, 남성과의 성관계를 가진 남성, 비인간 영장류에 직업적으로 노출된 사람, 응고인자를 받은 응고장애가 있는 사람, A형 간염과의 공동감염이 완전 간염으로 이어질 수 있는 만성 간질환 이력이 있는 사람 등이 포함된다.정맥주사 약물 사용자(명사)이다.[99]
B형 간염
B형 간염은 만성적인 바이러스 보균자가 2억 4천만 명 이상으로 세계에서 가장 흔한 바이러스성 간염의 원인이며, 이 중 100만 명이 미국에 있다.[27][99] 급성 B형 간염에 감염된 환자의 약 3분의 2에서, 식별 가능한 노출은 명백하지 않다.[16] 급성 감염자 중 25%는 평생 바이러스의 보균자가 된다.[99] 감염 위험은 정맥내 약물 사용자, 고위험 성행위가 있는 개인, 의료 종사자, 복수 수혈 이력이 있는 개인, 장기 이식 환자, 투석 환자, 출산 과정 중 감염된 신생아 중에서 가장 높다.[99] 전 세계에서 78만 명에 가까운 사망자가 B형 간염에 의한 것으로 보고 있다.[27] 가장 풍토적인 지역은 사하라 이남 아프리카와 동아시아 지역인데, 성인의 10%가 만성 보균자다.[27] 선진국의 운송업체 요금은 인구의 1% 미만을 포함하여 상당히 낮다.[27] 고유 지역에서, 전염은 출생 중 노출과 어린 유아들 사이의 긴밀한 접촉과 관련이 있다고 생각된다.[16][27]
C형 간염
만성 C형 간염은 간경변과 간세포암의 주요 원인이다.[124] 합병증이 심해 간 이식 수술의 흔한 의학적 이유다.[124] 전 세계 인구의 3%를 약간 넘는 1억3000만~1억8000만 명이 이 병에 걸린 것으로 추정된다.[86][99][124] 아프리카, 아시아, 남아메리카의 개발 도상 지역에서는 유병률이 인구의 10%에 달할 수 있다.[99] 이집트에서는 C형 간염의 20%에 이르는 감염률이 기록되어 있으며 1950~1980년대 치스토노미아 치료와 관련된 이아토젠성 오염과 관련이 있다.[16][99] 현재 미국에서는 약 350만 명의 성인들이 감염된 것으로 추정된다.[125] C형 간염은 특히 1945년부터 1965년 사이에 태어난 사람들 사이에 만연되어 있으며, 약 80만 명의 사람들이 살고 있으며, 미국 일반 인구의 1.6% 대비 3.2%의 높은 유병률을 보이고 있다.[16] C형 간염의 만성 보균자들은 대부분 감염 상태를 모르고 있다.[16] C형 간염 바이러스의 가장 흔한 전염 방식은 수혈(1992년 이전)과 정맥주사를 통한 혈액제제 노출이다.[16][99] 정맥주사의 이력은 만성 C형 간염의 가장 중요한 위험인자다.[124] 또 다른 취약계층은 고위험성 성행위가 있는 개인, 감염된 산모의 유아, 건강관리 종사자 등이다.[99]
D형 간염
D형 간염 바이러스는 B형 간염과 공동감염의 맥락에서 만성 및 완전성 간염을 유발한다.[99] 그것은 주로 비성적인 접촉과 바늘을 통해 전달된다.[16][99] D형 간염에 대한 민감도는 지리적 지역에 따라 다르다.[16][99] 미국과 북유럽에서 위험에 처한 인구는 정맥주사 약물 사용자와 여러 번 수혈을 받는 개인이다.[16][99] 지중해에서 D형 간염은 B형 간염 바이러스에 공동 감염된 개인들 사이에서 우세하다.[16][99]
E형 간염
A형 간염과 유사하게 E형 간염은 수원의 대변 오염과 관련된 대규모 발생과 전염병으로 나타난다.[16] 그것은 전세계적으로 약 2천만 명의 사람들이 바이러스에 감염되었다고 생각되는 연간 55,000명 이상의 사망자를 차지한다.[91] 그것은 주로 젊은 성인들에게 영향을 미쳐 급성 간염을 유발한다.[16][126] 감염된 임산부의 경우 E형 간염은 3중 사망률이 30%에 [99][126]이르는 완전 간염으로 이어질 수 있다. 장기이식 수혜자 등 면역력이 약한 개인도 취약하다.[126] 미국에서는 감염이 드물지만 개발도상국(아프리카, 아시아, 중앙아메리카, 중동)에서는 감염률이 높다.[16][126] 많은 유전자형이 존재하며 전세계에 차등적으로 분포한다.[91] 동물의 E형 간염에 대한 몇가지 증거가 있는데, 이것은 인간 감염의 저장고 역할을 한다.[99]
알코올성 간염
심각한 형태의 알코올성 간염(AH)은 1개월 [63][64][127]치 사망률이 50%에 이른다. AH를 발병하는 대부분의 사람들은 남성이지만 여성은 AH의 발병 위험이 더 높으며, 그 합병증은 높은 체지방과 알코올 신진대사의 차이에 부차적인 것으로 보인다.[64] 그 밖에 젊은 나이 <60세>, 폭식, 영양상태 불량, 비만, C형 간염 공동감염 등이 기여요인으로 꼽힌다.[64] AH환자의 20%에 달하는 C형 간염도 감염된 것으로 추정된다.[128] 이 인구에서 C형 간염 바이러스의 존재는 간경변, 간세포암으로의 진행속도가 빨라지고 사망률이 증가하면서 더욱 심각한 질병으로 이어진다.[64][128][129] 비만은 알코올성 간염이 있는 개인에서 간경변으로 진행될 가능성을 높인다.[64] AH를 앓고 있는 개인(70%)의 높은 비율이 간경변으로 진행될 것으로 추정된다.[64]
비알코올성 치주염
비알코올성 치주염(NASH)은 C형 간염으로 인한 만성 간질환을 대체해 2020년까지 미국에서 간 이식 수술의 1위 이유가 될 것으로 전망된다.[130] 미국 인구의 약 20–45%가 NAFLD를 가지고 있고 6%는 NASH를 가지고 있다.[29][40] 전세계에서 NASH의 추정 유병률은 3–[131]5%이다. 간경화증이 발병하는 NASH 환자 중 연간 약 2%가 간세포암으로 진행될 가능성이 높다.[131] 전 세계적으로, NAFLD와 관련된 간세포암의 추정 유병률은 15~30%[132]이다. NASH는 미국 전체 환자의 약 25%에서 간경변의 주요 원인으로 생각되며, 이는 일반 인구의 1~2%를 대표한다.[132]
역사
초기 관측치
현재 우리가 간염일 가능성이 높다고 생각하는 증후군의 초기 설명은 기원전 3000년경에 발생하기 시작한다. 고대 수메르인들의 의학 핸드북 역할을 했던 점토판들은 황달의 첫 관찰을 묘사했다. 수메르인들은 간이 영혼의 본거지라고 믿었고, 황달의 발견을 아하즈라는 이름의 악마가 간을 공격한 탓으로 돌렸다.[133]
기원전 400년경, 히포크라테스는 전염병 황달에 대한 최초의 문서화를 기록했으며, 특히 2주 이내에 모두 사망한 환자 집단 특유의 완전한 진로에 주목했다. 그는 "간 속에 들어 있는 담즙이 가래와 피로 가득 차서 분출한다...그런 분화가 있은 후 환자는 곧 화를 내고 화를 내고 헛소리를 하며 개처럼 짖어댄다.[134]
전쟁의 열악한 위생 상태를 감안할 때 전염성 황달은 나폴레옹 전쟁, 미국 독립 전쟁, 그리고 두 번의 세계 대전에서 병력의 주요 사망 원인으로서 큰 역할을 했다.[135] 제2차 세계대전 당시 간염에 걸린 군인의 추정치는 1000만 명을 넘었다.
제2차 세계대전 당시 병사들은 황열병 등 질병에 대한 백신을 접종받았지만 이들 백신은 간염 바이러스에 오염된 것으로 추정되는 인간 혈청으로 안정화돼 간염 전염병이 자주 발생했다.[136] 총 3,100명의 백신을 접종한 환자 중 예방접종 후 몇 달 동안 89건의 황달 발생을 지적한 결과 황열 바이러스 자체 때문이 아닌 별도의 감염원 때문이라는 의심을 받았다. 종자 바이러스 변종을 바꾼 뒤 이어진 8000여 건의 예방접종에서 황달의 경우는 관찰되지 않았다.[137]
윌로우브룩 주립학교 실험
뉴욕대 연구원인 사울 크루그먼은 1950년대와 1960년대까지 이 연구를 계속했는데, 간염 감염이 학생에게 매우 만연해 있는 뉴욕의 윌로우브룩 주립학교에서 정신장애 아동을 대상으로 실험을 한 것이 가장 불명예스러운 일이다. 크루그먼은 학생들에게 항체의 일종인 감마 글로불린을 주사했다. 이 항체가 제공한 감염에 대한 일시적인 방어를 관찰한 후, 그는 학생들에게 살아있는 간염 바이러스를 주입하려고 시도했다. 크루그먼은 또 감염 학생들로부터 대변을 채취해 밀크쉐이크에 섞은 뒤 새로 입소한 아이들에게 먹였다.[138]
그의 연구는 사람들이 선택된 목표 인구를 둘러싼 의심스러운 윤리에 항의하면서 많은 논란과 함께 받아들여졌다. 헨리 비허는 1966년 뉴잉글랜드 의학저널의 기고문에서 부모가 동의의 위험을 알지 못하며, 그 연구는 아이들의 희생을 감수하고 다른 사람들에게 이익을 주기 위해 행해진 것이라고 주장하면서 최고의 비판자 중 한 명이었다.[139] 게다가 그는 정신장애 자녀를 둔 가난한 가정들이 학교 입학 허가를 받기 위해 연구과제에 참여해야 한다는 부담감을 느끼는 경우가 많으며, 이에 수반될 모든 교육 및 지원 자원이 포함되어 있다고 주장했다.[140] 의료계의 다른 사람들은 크루그먼의 연구에 대해 널리 퍼진 이익과 간염 바이러스에 대한 이해 면에서 지지의 목소리를 냈고, 윌로우브룩은 의료 윤리에 관한 논쟁에서 흔히 인용되는 사례로 계속 언급되고 있다.[141]
오스트레일리아 항원
B형 간염에 대한 다음 통찰력은 간염 연구에 착수하지 않고 오히려 지질단백유전학을 연구한 NIH 연구원인 바루치 블럼버그 박사가 우연히 발견한 것이다. 그는 전 세계를 돌아다니며 혈액 샘플을 채취했고, 질병, 환경, 유전학 사이의 상호작용을 조사했으며, 그들이 병에 걸리지 않도록 예방할 수 있는 위험에 처한 사람들을 위한 표적 개입을 설계하는 것을 목표로 했다.[142] 그는 수혈을 여러 번 받은 혈우병 환자의 혈액과 호주 원주민의 혈액에서 발견된 단백질 사이의 예기치 않은 상호작용을 알아차렸다.[143] 그는 이 단백질을 "호주 항원"이라고 명명하고 그것을 연구의 초점으로 삼았다. 그는 개발도상국 환자의 혈액에서 백혈병이나 다운증후군 같은 다른 질병과 항원의 연관성에 주목했다.[144] 결국 그는 호주의 항원이 바이러스성 간염과 연관되어 있다는 통일적인 결론에 도달했다.
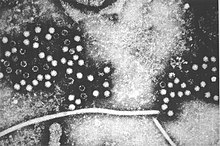
1970년 데이비드 데인은 런던 미들섹스 병원에서 B형 간염 바이러스(Virion)를 처음 격리시켜 42nm의 '데인 입자(Dane part)'[140]로 명명했다. B형 간염 바이러스의 표면과의 연관성을 바탕으로 호주 항원은 "Hepatitis B 표면 항원" 또는 HBsAg로 이름이 바뀌었다.
블럼버그는 항원을 계속 연구했고, 결국 1976년 노벨 의학상을 받은 HBsAg가 풍부한 혈장을 이용해 B형 간염 백신을 개발했다.[145]
사회와 문화
경제적 부담
전반적으로, 간염은 개발도상국과 선진국 모두에서 의료비 지출에서 상당한 부분을 차지하며, 몇몇 개발도상국에서는 증가할 것으로 예상된다.[146][147] A형 간염은 자가 제한적인 사건이지만, 미국에서는 상당한 비용과 관련이 있다.[148] 직간접 비용은 건당 각각 약 1817달러와 2459달러로, 감염 성인 1명당 평균 27일의 근무일이 손실되는 것으로 추산됐다.[148] 1997년 한 보고서는 A형 간염과 관련된 한 번의 입원 비용이 평균 6,900달러였으며 연간 총 5억 달러 정도의 의료비를 발생시켰다는 것을 보여주었다.[149] 비용 효과 연구에서는 성인에 대한 광범위한 예방접종이 불가능하다는 것을 발견했지만, 어린이와 위험군(내부성 지역 출신자, 의료 종사자)에 대한 A형 간염과 B형 간염 예방접종이 가능할 수 있다고 밝혔다.[150]
B형 간염은 아시아와 같은 고질적인 지역에서 의료비 지출에서 훨씬 더 큰 비중을 차지한다.[151][152] 1997년에 그것은 한국의 총 의료비 지출의 3.2%를 차지했고 6억 9600만 달러의 직접 비용을 초래했다.[152] 그 금액의 대부분은 질병 증상과 합병증을 치료하는 데 쓰여졌다.[153] 만성 B형 간염 감염은 미국에서만 볼 수 있는 만성은 아니지만 1990년 3억5천7백만 달러의 입원비를 차지했다.[146] 이 숫자는 2003년에 15억 달러까지 증가했지만 2006년 현재 안정세를 유지하고 있는데, 이는 효과적인 약물치료와 예방접종 캠페인의 도입에 기인할 수 있다.[146][147]
만성 C형 간염에 감염된 사람들은 세계적으로 건강관리 시스템의 빈번한 사용자인 경향이 있다.[154] 미국에서 C형 간염에 감염된 사람은 한 달에 691달러의 비용이 들 것으로 추정되었다.[154] 이 숫자는 보상형 간경변 환자의 경우 1,227달러로 두 배 가까이 늘어난 반면, 부패형 간경변 환자의 월 비용은 3,682달러로 거의 5배나 된다.[154] 간염의 영향이 광범위해 간접비용을 추정하기 어렵지만 미국에서는 연간 총 비용이 65억달러에 달한다는 연구결과가 나왔다.[146] 캐나다의 경우 HCV 관련 비용의 56%가 간경변으로 인한 것이며, 바이러스 관련 총 지출은 2032년에 3억9600만달러로 최고조에 달할 것으로 예상된다.[155]
주목할 만한 사례
미국 역사상 가장 큰 규모의 A형 간염 바이러스는 2003년 말 펜실베이니아 주 모나카에 위치한 지금은 없어진 멕시코 음식점에서 식사를 한 사람들 사이에서 발생했다.[156] 2003년 9월부터 10월 사이에 이 식당을 방문한 550명 이상의 사람들이 이 바이러스에 감염되었고, 이 중 3명은 직접적인 결과로 사망했다.[156] 군에서 A형 간염 환자가 크게 증가하는 것을 지역 응급의학과 의사들이 눈치채면서 이번 발병은 보건 관계자들의 주목을 받았다.[157] CDC는 조사를 벌인 뒤 발병의 원인을 오염된 원파를 사용한 것으로 보고 있다. 이 식당은 당시 멕시코의 농장에서 파 육수를 구입하고 있었다.[156] 대파는 농작물 관개, 헹굼 또는 결빙을 위해 오염된 물을 사용하거나 감염된 개인이 채소를 처리함으로써 오염되었을 수 있다고 여겨진다.[156] 대파는 이에 앞서 미국 남부에서 비슷한 규모의 A형 간염 발병을 일으켰지만 그 규모만큼은 아니었다.[156] CDC는 이 식당이 잘게 썬 생파용 대형 공동 양동이를 사용해 오염되지 않은 식물을 오염된 식물과 섞을 수 있게 해 감염 벡터를 늘리고 발생을 증폭시킨 것으로 보고 있다.[156] 이 식당은 일단 출처가 밝혀지자 문을 닫았고, 9,000명 이상이 식당에서 식사를 했거나 누군가와 밀접하게 접촉했다는 이유로 A형 면역 글로불린을 투여받았다.[156]
특수인구
HIV 공동 감염
HIV에 감염된 사람들은 특히 HIV-HCV의 공동 감염에 대한 부담이 크다.[158][159] 세계보건기구의 최근 연구에서, C형 간염 바이러스에 감염될 확률은 HIV에 감염된 사람들보다 6배 더 높았다.[159] 전 세계적으로 HIV-HCV 공동감염의 유병률은 220만 명 이상을 나타내는 6.2%로 추정되었다.[159] 정맥내 약물 사용은 HCV 감염의 독립적인 위험 요소였다.[124] 세계보건기구(WHO) 연구에서는 일반 인구(2.4%)[159]에 비해 약물을 투여한 사람의 HIV-HCV 공동감염 유병률이 82.4%로 눈에 띄게 높았다. 남성과의 성관계를 가진 HIV 양성 남성의 HIV-HCV 공동감염 연구(MSM)에서 전체 항혈당염 C항체 유병률은 8.1%로 추정됐으며 약물을 투여한 HIV 양성 MSM의 40%로 증가했다.[158]
임신
B형 간염
수직 전송은 매년 새로운 HBV 사례의 중요한 기여자로, 고유 국가에서 산모에서 신생아까지 35~50%의 전송이 이루어진다.[83][160] 수직적 전달은 신생아가 태어나는 동안 산모의 혈액과 질 분비물에 노출되는 것을 통해 주로 발생한다.[160] 바이러스에 감염된 성인의 경우 만성 감염으로 진행될 위험이 약 5%인 반면, 수직전송 대상 신생아의 경우 95%에 달한다.[83][161] 바이러스 전파 위험은 산모혈액이 HBsAg에 양성일 때 약 10~20%, HBeAg에도 양성일 때 최대 90%이다.[83]
CDC는 산전수신의 위험성이 높은 만큼 산전수신의 첫 방문 시 모든 임산부의 HBV 검사를 권고하고 있다.[83][162] 면역력이 없는 임산부들이 HBV 백신을 접종하는 것은 안전하다.[83][160] 미국간질환연구회(AASLD)는 이용 가능한 한정된 증거를 토대로 바이러스 부하가 20만 IU/mL를 넘는 임산부에게 항바이러스 치료를 권고하고 있다.[163] 세 번째 3개월에서 시작된 항바이러스 요법이 신생아로의 전달을 현저하게 감소시킨다는 증거가 증가하고 있다.[160][163] 항레트로바이러스 임신 등록 데이터베이스를 체계적으로 검토한 결과 테노포비르와 함께 선천성 기형의 위험이 증가하지 않은 것으로 확인되었으며, 이러한 이유로 AASLD는 이 약을 효능 및 저저항 위험과 함께 권장하고 있다.[163][164] 2010년 체계적 검토와 메타분석에 따르면, 라미부딘은 세 번째 3기 초기에 시작했으며, 알려진 부작용 없이 HBV의 모자 간 전송도 현저히 줄였다.[165]
ACOG는 이용 가능한 증거가 HBV를 가진 산모들의 수직 전달을 줄이는데 있어서 어떤 특정한 전달 방식(즉, 질 대 제왕절개)이 더 낫다는 것을 시사하지 않는다고 언급하고 있다.[83]
세계보건기구(WHO)와 CDC는 HBV를 가진 산모에게서 태어난 신생아는 생후 12시간 이내에 B형 면역 글로불린(HBIG) 간염과 HBV 백신을 맞도록 권고하고 있다.[80][82] HBIG와 HBV 백신을 접수한 유아에게는 모유 수유가 안전하다.[83][160]
C형 간염
2014년 체계적 검토 및 메타 분석 결과 HCV 양성, HIV 음성 여성에서 HCV 수직 전송률의 추정치는 5.8%로 나타났다.[83][166] 같은 연구에서는 HCV 양성, HIV 양성 여성에게서 수직 전파의 위험성이 10.8%로 나타났다.[166] 다른 연구들은 HIV 양성 여성들 사이에서 수직 전염의 위험성이 44%에 달한다는 것을 발견했다.[83] 산모의 혈액에서 바이러스를 검출할 수 있을 때 수직 전염의 위험성이 더 높다.[166]
증거는 전달 모드(즉 질 대 제왕)가 수직 전송에 영향을 미친다는 것을 나타내지 않는다.[83]
HCV 양성 및 HIV 음성인 여성의 경우 모유 수유는 안전하지만 CDC 지침에 따르면 여성의 젖꼭지가 "파열되거나 피가 나는" 경우 모유 수유를 피하는 것이 전염 위험을 줄일 수 있다.[83][85]
E형 간염
누가 하이브리드 카면 연락하는 임신한 여성들 모성 사망률 20–30%, 가장 보편적으로 세번째 3개월에서 3968 사람들이 포함되어 있47은 연구들이 2016년 체계적인 논평과 메타 분석 외 case-fatality율 20.8%그리고 태아기 CFR34.2%,시(CFR)을 발견했다 .[16][83][160]이 높고 격증 간염을 개발하는 중요한 위험에 있다.ong고 있는 여자 완전성 간 기능부전, CFR은 61.2%[167]로 나타났다.
참고 항목
참조
- ^ Jump up to: a b c d e f "Hepatitis". MedlinePlus. Archived from the original on 11 November 2016. Retrieved 10 November 2016.
- ^ Jump up to: a b c d e f g "What is hepatitis?". WHO. July 2016. Archived from the original on 7 November 2016. Retrieved 10 November 2016.
- ^ Jump up to: a b c d e f g h i j k l m "Hepatitis". NIAID. Archived from the original on 4 November 2016. Retrieved 2 November 2016.
- ^ Jump up to: a b "Liver Transplant". NIDDK. April 2012. Archived from the original on 11 November 2016. Retrieved 10 November 2016.
- ^ "Hepatitis". MedlinePlus. 2020-05-20. Retrieved 2020-07-19.
Your liver is the largest organ inside your body. It helps your body digest food, store energy, and remove poisons. Hepatitis is an inflammation of the liver.
- ^ "Hepatitis (Hepatitis A, B, and C) ACG Patients". patients.gi.org. Archived from the original on 2017-02-23.
- ^ Bernal W.; Wendon J. (2013). "Acute Liver Failure". New England Journal of Medicine. 369 (26): 2525–2534. doi:10.1056/nejmra1208937. PMID 24369077.
- ^ Jump up to: a b c "Fatty Liver Disease (Nonalcoholic Steatohepatitis)". NIDDK. May 2014. Archived from the original on 11 November 2016. Retrieved 10 November 2016.
- ^ Jump up to: a b c d e f g h i j k l m n o p q r AASLD/IDSA HCV Guidance Panel (2015-09-01). "Hepatitis C guidance: AASLD-IDSA recommendations for testing, managing, and treating adults infected with hepatitis C virus". Hepatology. 62 (3): 932–954. doi:10.1002/hep.27950. ISSN 1527-3350. PMID 26111063.
- ^ "Autoimmune Hepatitis". NIDDK. March 2014. Archived from the original on 11 November 2016. Retrieved 10 November 2016.
- ^ Vos, Theo; Allen, Christine; Arora, Megha; Barber, Ryan M.; Bhutta, Zulfiqar A.; Brown, Alexandria; Carter, Austin; Casey, Daniel C.; Charlson, Fiona J.; Chen, Alan Z.; Coggeshall, Megan; Cornaby, Leslie; Dandona, Lalit; Dicker, Daniel J.; Dilegge, Tina; Erskine, Holly E.; Ferrari, Alize J.; Fitzmaurice, Christina; Fleming, Tom; Forouzanfar, Mohammad H.; Fullman, Nancy; Gething, Peter W.; Goldberg, Ellen M.; Graetz, Nicholas; Haagsma, Juanita A.; Hay, Simon I.; Johnson, Catherine O.; Kassebaum, Nicholas J.; Kawashima, Toana; et al. (October 2016). "Global, regional, and national incidence, prevalence, and years lived with disability for 310 diseases and injuries, 1990–2015: a systematic analysis for the Global Burden of Disease Study 2015". The Lancet. 388 (10053): 1545–1602. doi:10.1016/S0140-6736(16)31678-6. PMC 5055577. PMID 27733282.
- ^ Basra, Sarpreet (2011). "Definition, epidemiology and magnitude of alcoholic hepatitis". World Journal of Hepatology. 3 (5): 108–13. doi:10.4254/wjh.v3.i5.108. PMC 3124876. PMID 21731902.
- ^ Wang, Haidong; Naghavi, Mohsen; Allen, Christine; Barber, Ryan M.; Bhutta, Zulfiqar A.; Carter, Austin; Casey, Daniel C.; Charlson, Fiona J.; Chen, Alan Zian; Coates, Matthew M.; Coggeshall, Megan; Dandona, Lalit; Dicker, Daniel J.; Erskine, Holly E.; Ferrari, Alize J.; Fitzmaurice, Christina; Foreman, Kyle; Forouzanfar, Mohammad H.; Fraser, Maya S.; Fullman, Nancy; Gething, Peter W.; Goldberg, Ellen M.; Graetz, Nicholas; Haagsma, Juanita A.; Hay, Simon I.; Huynh, Chantal; Johnson, Catherine O.; Kassebaum, Nicholas J.; Kinfu, Yohannes; et al. (October 2016). "Global, regional, and national life expectancy, all-cause mortality, and cause-specific mortality for 249 causes of death, 1980–2015: a systematic analysis for the Global Burden of Disease Study 2015". The Lancet. 388 (10053): 1459–1544. doi:10.1016/S0140-6736(16)31012-1. PMC 5388903. PMID 27733281.
- ^ "Statistics & Surveillance Division of Viral Hepatitis CDC". CDC. Archived from the original on 11 November 2016. Retrieved 10 November 2016.
- ^ "Online Etymology Dictionary". Etymonline.com. Archived from the original on 2012-10-20. Retrieved 2012-08-26.
- ^ Jump up to: a b c d e f g h i j k l m n o p q r s t u v w x y z aa ab ac ad ae af ag ah ai aj ak al am an ao ap aq ar as at au av aw ax ay az ba bb bc bd be bf bg bh bi bj bk bl Dienstag, JL (2015). "Chapter 360: Acute Viral Hepatitis". In Kasper, D; Fauci, A; Hauser, S; Longo, D; Jameson, J; Loscalzo, J (eds.). Harrison's Principles of Internal Medicine, 19e. New York, NY: McGraw-Hill. ISBN 978-0-07-180215-4.
- ^ Jump up to: a b c d e f g Rutherford, A; Dienstag, JL (2016). "Chapter 40: Viral Hepatitis". In Greenberger, NJ; Blumberg, RS; Burakoff, R (eds.). CURRENT Diagnosis & Treatment: Gastroenterology, Hepatology, & Endoscopy, 3e. New York, NY: McGraw-Hill. ISBN 978-0-07-183772-9.
- ^ Jump up to: a b c d e f Khalili, M; Burman, B (2013). "Chapter 14: Liver Disease". In Hammer, GD; McPhee, SJ (eds.). Pathophysiology of Disease: An Introduction to Clinical Medicine, 7e. McGraw-Hill. ISBN 978-1-25-925144-3.
- ^ Jump up to: a b c d e f g h i j k l m n o p q r s t u v w x y z aa ab ac ad ae af ag ah ai aj ak al am Dienstag, JL (2015). "Chapter 362: Chronic Hepatitis". In Kasper, D; Fauci, A; Hauser, S; Longo, D; Jameson, J; Loscalzo, J (eds.). Harrison's Principles of Internal Medicine, 19e. New York, NY: McGraw-Hill. ISBN 978-0-07-180215-4.
- ^ Jump up to: a b c Fontana, Robert; Hayashi, Paul (2014-05-01). "Clinical Features, Diagnosis, and Natural History of Drug-Induced Liver Injury". Seminars in Liver Disease. 34 (2): 134–144. doi:10.1055/s-0034-1375955. PMID 24879979.
- ^ Jump up to: a b Manns, Michael P.; Lohse, Ansgar W.; Vergani, Diego (2015). "Autoimmune hepatitis – Update 2015". Journal of Hepatology. 62 (1): S100–S111. doi:10.1016/j.jhep.2015.03.005. PMID 25920079.
- ^ Munjal, Y. P.; Sharm, Surendra K. (2012). API Textbook of Medicine, Ninth Edition, Two Volume Set. JP Medical Ltd. p. 870. ISBN 9789350250747. Archived from the original on 2017-09-10.
- ^ World Health Organization. "Hepatitis". World Health Organization. Archived from the original on 2 December 2013. Retrieved 25 November 2013.
- ^ "Hepatitis A Questions and Answers for the Public Division of Viral Hepatitis CDC". www.cdc.gov. Archived from the original on 2016-03-12. Retrieved 2016-03-14.
- ^ "Hepatitis E". World Health Organization. Archived from the original on 2016-03-12. Retrieved 2016-03-14.
- ^ Centers for Disease Control & Prevention (June 2010). "When Someone Close to You Has Hepatitis" (PDF). Archived (PDF) from the original on March 6, 2016. Retrieved March 14, 2016.
- ^ Jump up to: a b c d e f g h "Hepatitis B". World Health Organization. Archived from the original on 2014-11-09. Retrieved 2016-03-09.
- ^ Jump up to: a b "Hepatitis C FAQs for the Public Division of Viral Hepatitis CDC". www.cdc.gov. Archived from the original on 2016-03-15. Retrieved 2016-03-14.
- ^ Jump up to: a b c d e f g h i j k l m n o p q r s t u v w x y z aa ab ac ad ae af ag ah ai aj ak al am Friedman, Lawrence S. (2015). "Chapter 16: Liver, Biliary Tract, & Pancreas Disorders". In Papadakis, M; McPhee, SJ; Rabow, MW (eds.). Current Medical Diagnosis & Treatment 2016 55e. McGraw Hill. ISBN 978-0071845090.
- ^ Jump up to: a b c d e Harder, A; Mehlhorn, H (2008). "Diseases Caused by Adult Parasites or Their Distinct Life Cycle Stages". In Weber, O; Protzer, U (eds.). Comparative Hepatitis. Birkhauser. pp. 161–216. ISBN 978-3764385576.
- ^ Jump up to: a b c d Wisplinghoff, H; Appleton, DL (2008). "Bacterial Infections of the Liver". In Weber, O; Protzer, U (eds.). Comparative Hepatitis. Birkhauser. pp. 143–160. ISBN 978-3764385576.
- ^ Jump up to: a b c d e f g h Mailliard, ME; Sorrell, MF (2015). "Chapter 363: Alcoholic Liver Disease". In Kasper, D; Fauci, A; Hauser, S; Longo, D; Jameson, J; Loscalzo, J (eds.). Harrison's Principles of Internal Medicine 19e. McGraw-Hill. ISBN 978-0-07-180215-4.
- ^ Jump up to: a b c d e Lee, WM; Dienstag, JL (2015). "Chapter 361: Toxic and Drug-Induced Hepatitis". In Kasper, D; Fauci, A; Hauser, S; Longo, D; Jameson, J; Loscalzo, J (eds.). Harrison's Principles of Internal Medicine 19e. McGraw-Hill. ISBN 978-0-07-180215-4.
- ^ Jump up to: a b Malaguarnera, Giulia; Cataudella, E; Giordano, M; Nunnari, G; Chisari, G; Malaguarnera, M (2012). "Toxic hepatitis in occupational exposure to solvents". World Journal of Gastroenterology. 18 (22): 2756–66. doi:10.3748/wjg.v18.i22.2756. PMC 3374978. PMID 22719183.
- ^ Lee, William M. (31 July 2003). "Drug-Induced Hepatotoxicity". New England Journal of Medicine. 349 (5): 474–485. doi:10.1056/NEJMra021844. PMID 12890847.
- ^ Suk, Ki Tae; Kim, Dong Joon (2012). "Drug-induced liver injury: present and future". Clinical and Molecular Hepatology. 18 (3): 249–57. doi:10.3350/cmh.2012.18.3.249. PMC 3467427. PMID 23091804.
- ^ Jump up to: a b "Herbals_and_Dietary_Supplements". livertox.nih.gov. Archived from the original on 2016-05-08. Retrieved 2016-03-14.
- ^ "NIH launches free database of drugs associated with liver injury". National Institutes of Health (NIH). 2015-09-30. Retrieved 2018-09-18.
- ^ O'Mara SR, Gebreyes K (2011). "Chapter 83. Hepatic Disorders, Jaundice, and Hepatic Failure" (Online). In Cydulka RK, Meckler GD (eds.). Tintinalli's Emergency Medicine: A Comprehensive Study Guide (7th ed.). New York: McGraw-Hill. Archived from the original on 2 December 2013. Retrieved 26 November 2013.
- ^ Jump up to: a b Abdelmalek, MF; Diehl AM (2015). "Chapter 364: Nonalcoholic Liver Diseases and Nonalcoholic Steatohepatitis". In Kasper, D; Fauci, A; Hauser, S; Longo, D; Jameson, J; Loscalzo, J (eds.). Harrison's Principles of Internal Medicine 19e. McGraw-Hill. ISBN 978-0-07-180215-4.
- ^ Jump up to: a b National Digestive Diseases Information Clearinghouse (NDDIC). "Nonalcoholic Steatohepatitis". National Digestive Diseases Information Clearinghouse (NDDIC). Archived from the original on 2 December 2013. Retrieved 27 November 2013.
- ^ Masuoka, Howard C.; Chalasani, Naga (April 2013). "Nonalcoholic fatty liver disease: an emerging threat to obese and diabetic individuals". Annals of the New York Academy of Sciences. 1281 (1): 106–122. Bibcode:2013NYASA1281..106M. doi:10.1111/nyas.12016. PMC 3646408. PMID 23363012.
- ^ National Digestive Diseases Information Clearinghouse (NDDIC). "Autoimmune Hepatitis". National Digestive Diseases Information Clearinghouse (NDDIC). Archived from the original on 15 September 2010. Retrieved 27 November 2013.
- ^ Teufel, Andreas; Galle, PR; Kanzler, S (2009). "Update on autoimmune hepatitis". World Journal of Gastroenterology. 15 (9): 1035–41. doi:10.3748/wjg.15.1035. PMC 2655176. PMID 19266594.
- ^ Jump up to: a b c d e Czaja, Albert J (2016). "Diagnosis and Management of Autoimmune Hepatitis: Current Status and Future Directions". Gut and Liver. 10 (2): 177–203. doi:10.5009/gnl15352. PMC 4780448. PMID 26934884.
- ^ Jump up to: a b c Czaja, Albert J. (2016-03-15). "Diagnosis and Management of Autoimmune Hepatitis: Current Status and Future Directions". Gut and Liver. 10 (2): 177–203. doi:10.5009/gnl15352. ISSN 1976-2283. PMC 4780448. PMID 26934884.
- ^ Krawitt, Edward-L (2008). "Clinical features and management of autoimmune hepatitis". World Journal of Gastroenterology. 14 (21): 3301–5. doi:10.3748/wjg.14.3301. PMC 2716584. PMID 18528927.
- ^ Teckman, Jeffrey H. (2013-03-07). "Liver Disease in Alpha-1 Antitrypsin Deficiency: Current Understanding and Future Therapy". COPD: Journal of Chronic Obstructive Pulmonary Disease. 10 (sup1): 35–43. doi:10.3109/15412555.2013.765839. ISSN 1541-2555. PMID 23527737. S2CID 35451941.
- ^ Medline Plus (2012-08-10). "Hepatic ischemia". National Library of Medicine. Archived from the original on 8 December 2013. Retrieved 4 December 2013.
- ^ Feldman, Friedman; Feldman, Brandt, eds. (2010). "Chapter 83 Vascular Diseases of the Liver" (Online). Sleisenger and Fordtran's Gastrointestinal and Liver Disease. Saunders. ISBN 978-1416061892. Archived from the original on 4 March 2016. Retrieved 4 December 2013.
- ^ Jump up to: a b c d Samyn, M; Mieli-Vergani, G (November 2015). "Liver and Biliary Disease in Infancy". Medicine. 43 (11): 625–630. doi:10.1016/j.mpmed.2015.08.008.
- ^ Roberts, Eve A. (2003-10-01). "Neonatal hepatitis syndrome". Seminars in Neonatology. 8 (5): 357–374. doi:10.1016/S1084-2756(03)00093-9. ISSN 1084-2756. PMID 15001124.
- ^ Sokol, Ronald J.; Narkewicz, Michael R. (2012-06-21). "Chapter 22: Liver & Pancreas". In Hay, William W.; et al. (eds.). Current diagnosis & treatment: pediatrics (21st ed.). New York: McGraw-Hill Medical. ISBN 978-0-07-177970-8. Archived from the original on 10 December 2013. Retrieved 2 December 2013.
- ^ Alexopoulou, Alexandra; Deutsch, Melanie; Ageletopoulou, Johanna; Delladetsima, Johanna K.; Marinos, Evangelos; Kapranos, Nikiforos; Dourakis, Spyros P. (May 2003). "A fatal case of postinfantile giant cell hepatitis in a patient with chronic lymphocytic leukaemia". European Journal of Gastroenterology & Hepatology. 15 (5): 551–555. doi:10.1097/01.meg.0000050026.34359.7c. PMID 12702915.
- ^ Jump up to: a b c Nakamoto, Yasunari; Kaneko, Shuichi (2003-09-01). "Mechanisms of viral hepatitis induced liver injury". Current Molecular Medicine. 3 (6): 537–544. doi:10.2174/1566524033479591. ISSN 1566-5240. PMID 14527085.
- ^ Lin, Shaoli; Zhang, Yan-Jin (August 2017). "Interference of Apoptosis by Hepatitis B Virus". Viruses. 9 (8): 230. doi:10.3390/v9080230. PMC 5580487. PMID 28820498.
- ^ Cao, Lei; Quan, Xi-Bing; Zeng, Wen-Jiao; Yang, Xiao-Ou; Wang, Ming-Jie (2016). "Mechanism of Hepatocyte Apoptosis". Journal of Cell Death. 9: 19–29. doi:10.4137/JCD.S39824. PMC 5201115. PMID 28058033.
- ^ Wong, Grace Lai-Hung (2014-09-01). "Prediction of fibrosis progression in chronic viral hepatitis". Clinical and Molecular Hepatology. 20 (3): 228–236. doi:10.3350/cmh.2014.20.3.228. ISSN 2287-285X. PMC 4197170. PMID 25320725.
- ^ Jump up to: a b Rehermann, Barbara (2015-11-01). "Natural Killer Cells in Viral Hepatitis". Cellular and Molecular Gastroenterology and Hepatology. 1 (6): 578–588. doi:10.1016/j.jcmgh.2015.09.004. ISSN 2352-345X. PMC 4678927. PMID 26682281.
- ^ Jump up to: a b Heim, Markus H.; Thimme, Robert (2014-11-01). "Innate and adaptive immune responses in HCV infections". Journal of Hepatology. 61 (1 Suppl): S14–25. doi:10.1016/j.jhep.2014.06.035. ISSN 1600-0641. PMID 25443342.
- ^ Jump up to: a b c d e f Hardy, Timothy; Oakley, Fiona; Anstee, Quentin M.; Day, Christopher P. (2016-03-03). "Nonalcoholic Fatty Liver Disease: Pathogenesis and Disease Spectrum". Annual Review of Pathology. 11: 451–96. doi:10.1146/annurev-pathol-012615-044224. ISSN 1553-4014. PMID 26980160.
- ^ Jump up to: a b c d Yoon, Hye-Jin; Cha, Bong Soo (2014-11-27). "Pathogenesis and therapeutic approaches for non-alcoholic fatty liver disease". World Journal of Hepatology. 6 (11): 800–811. doi:10.4254/wjh.v6.i11.800. ISSN 1948-5182. PMC 4243154. PMID 25429318.
- ^ Jump up to: a b c d e f g h i j Chayanupatkul, Maneerat; Liangpunsakul, Suthat (2014-05-28). "Alcoholic hepatitis: a comprehensive review of pathogenesis and treatment". World Journal of Gastroenterology. 20 (20): 6279–6286. doi:10.3748/wjg.v20.i20.6279. ISSN 2219-2840. PMC 4033465. PMID 24876748.
- ^ Jump up to: a b c d e f g Basra, Sarpreet; Anand, Bhupinderjit S. (2011-05-27). "Definition, epidemiology and magnitude of alcoholic hepatitis". World Journal of Hepatology. 3 (5): 108–113. doi:10.4254/wjh.v3.i5.108. ISSN 1948-5182. PMC 3124876. PMID 21731902.
- ^ Haga, Yuki; Kanda, Tatsuo; Sasaki, Reina; Nakamura, Masato; Nakamoto, Shingo; Yokosuka, Osamu (2015-12-14). "Nonalcoholic fatty liver disease and hepatic cirrhosis: Comparison with viral hepatitis-associated steatosis". World Journal of Gastroenterology. 21 (46): 12989–12995. doi:10.3748/wjg.v21.i46.12989. ISSN 2219-2840. PMC 4674717. PMID 26675364.
- ^ Grant, A; Neuberger J (1999). "Guidelines on the use of liver biopsy in clinical practice". Gut. 45 (Suppl 4): 1–11. doi:10.1136/gut.45.2008.iv1. PMC 1766696. PMID 10485854.
The main cause of mortality after percutaneous liver biopsy is intraperitoneal haemorrhage as shown in a retrospective Italian study of 68 000 percutaneous liver biopsies in which all six patients who died did so from intraperitoneal haemorrhage. Three of these patients had had a laparotomy, and all had either cirrhosis or malignant disease, both of which are risk factors for bleeding.
- ^ Green, RM; Flamm, S (October 2002). "AGA technical review on the evaluation of liver chemistry tests". Gastroenterology. 123 (4): 1367–84. doi:10.1053/gast.2002.36061. PMID 12360498.
- ^ Pratt, DS; Kaplan, MM (Apr 27, 2000). "Evaluation of abnormal liver-enzyme results in asymptomatic patients". The New England Journal of Medicine. 342 (17): 1266–71. doi:10.1056/NEJM200004273421707. PMID 10781624.
- ^ Ito, Katsuyoshi; Mitchell, Donald G. (2004). "Imaging Diagnosis of Cirrhosis and Chronic Hepatitis". Intervirology. 47 (3–5): 134–143. doi:10.1159/000078465. PMID 15383722. S2CID 36112368.
- ^ Allan, Richard; Thoirs, Kerry; Phillips, Maureen (2010-07-28). "Accuracy of ultrasound to identify chronic liver disease". World Journal of Gastroenterology. 16 (28): 3510–3520. doi:10.3748/wjg.v16.i28.3510. ISSN 1007-9327. PMC 2909550. PMID 20653059.
- ^ Sahani, Dushyant V.; Kalva, Sanjeeva P. (2004-07-01). "Imaging the Liver". The Oncologist. 9 (4): 385–397. doi:10.1634/theoncologist.9-4-385. ISSN 1083-7159. PMID 15266092.
- ^ Jump up to: a b Villar LM, Cruz HM, Barbosa JR, Bezerra CS, Portilho MM, Scalioni Lde P (2015). "Update on hepatitis B and C virus diagnosis". World Journal of Virology. 4 (4): 323–42. doi:10.5501/wjv.v4.i4.323. PMC 4641225. PMID 26568915.
- ^ Jump up to: a b Neuman, Manuela G.; French, Samuel W.; French, Barbara A.; Seitz, Helmut K.; Cohen, Lawrence B.; Mueller, Sebastian; Osna, Natalia A.; Kharbanda, Kusum K.; Seth, Devanshi (2014-12-01). "Alcoholic and non-alcoholic steatohepatitis". Experimental and Molecular Pathology. 97 (3): 492–510. doi:10.1016/j.yexmp.2014.09.005. PMC 4696068. PMID 25217800.
- ^ "Guidelines For Viral Hepatitis Surveillance And Case Management". www.cdc.gov. Archived from the original on 2016-03-10. Retrieved 2016-03-12.
- ^ Longo DL, Fauci AS, Kasper DL, Hauser SL, Jameson J, Loscalzo J. eds. (2013). Harrison's Manual of Medicine, 18e, Chapter 164: Chronic Hepatitis. New York, NY: McGraw-Hill.CS1 maint: 복수 이름: 작성자 목록(링크) CS1 maint: 추가 텍스트: 작성자 목록(링크)
- ^ Jump up to: a b c d e "Hepatitis A Fact sheet N°328". WHO Media Centre. Archived from the original on February 21, 2014. Retrieved March 7, 2016.
- ^ Jump up to: a b c d Voise, Nathan (Oct 2011). "Advisory Committee on Immunization Practices (ACIP) of the Centers for Disease Control and Prevention. A shot at hepatitis prevention". J Am Osteopath Assoc. 111 (10 Suppl 6): S13–6. PMID 22086888.
- ^ Jump up to: a b c "Adult Immunization Schedule by Vaccine and Age Group". www.CDC.gov. Archived from the original on March 5, 2016. Retrieved March 7, 2016.
- ^ Longo, Dan L.; et al. (2013). Chapter 163: "Acute Hepatitis." Harrison's Manual of Medicine, 18e. New York, NY: McGraw-Hill.
- ^ Jump up to: a b c d e f g h i j k l m n "Recommendations for Identification and Public Health Management of Persons with Chronic Hepatitis B Virus Infection". www.cdc.gov. Archived from the original on 2016-03-06. Retrieved 2016-03-11.
- ^ Jump up to: a b c d e f g h i Chou, Roger; Dana, Tracy; Bougatsos, Christina; Blazina, Ian; Zakher, Bernadette; Khangura, Jessi (2014-01-01). Screening for Hepatitis B Virus Infection in Nonpregnant Adolescents and Adults: Systematic Review to Update the 2004 U.S. Preventive Services Task Force Recommendation. U.S. Preventive Services Task Force Evidence Syntheses, formerly Systematic Evidence Reviews. Rockville (MD): Agency for Healthcare Research and Quality (US). PMID 24921112.
- ^ Jump up to: a b c d e f g h i j k "Guidelines for the prevention, care and treatment of persons with chronic hepatitis B infection". World Health Organization. Archived from the original on 2016-02-20. Retrieved 2016-03-11.
- ^ Jump up to: a b c d e f g h i j k l m n o p q "ACOG Practice Bulletin: Clinical Management Guidelines for Obstetrician-Gynecologists: Viral Hepatitis in Pregnancy". www.acog.org. Retrieved 2016-03-12.
- ^ Esherick JS; Clark DS; Slater ED; et al. (2015). CURRENT Practice Guidelines in Primary Care 2015. New York, NY: McGraw-Hill.
- ^ Jump up to: a b c d e f g h i "Recommendations for Prevention and Control of Hepatitis C Virus (HCV) Infection and HCV-Related Chronic Disease". MMWR. 47 (RR-19): 1–39. October 16, 1998. PMID 9790221. Archived from the original on March 24, 2016. Retrieved March 16, 2016.
- ^ Jump up to: a b c d e f g h i j k "Hepatitis C". World Health Organization. Archived from the original on 2016-01-31. Retrieved 2016-03-08.
- ^ Jump up to: a b c d e f g h i j k "Final Recommendation Statement: Hepatitis C: Screening - US Preventive Services Task Force". www.uspreventiveservicestaskforce.org. Archived from the original on 2016-03-21. Retrieved 2016-03-21.
- ^ Jump up to: a b c "Birth-18 Years and Catchup Immunization Schedules for Providers". www.CDC.gov. Archived from the original on March 6, 2016. Retrieved March 7, 2016.
- ^ Centers for Disease Control (1999). "Update: recommendations to prevent hepatitis B virus transmission—United States. MMWR 1999". 48: 33–4. Archived from the original on May 14, 2016. Retrieved March 7, 2016. Cite 저널은 필요로 한다.
journal=(도움말) - ^ "Hepatitis A And Hepatitis B Vaccine (Intramuscular Route)". Mayo Clinic. Retrieved 25 January 2018.
- ^ Jump up to: a b c d "Hepatitis E". World Health Organization. Archived from the original on 2016-03-06. Retrieved 2016-03-09.
- ^ Jump up to: a b "WHO Hepatitis D". www.who.int. Archived from the original on 2016-03-08. Retrieved 2016-03-09.
- ^ Zhang; et al. (March 5, 2015). "Long-Term Efficacy of a Hepatitis E Vaccine". NEJM. 372 (10): 914–22. doi:10.1056/NEJMoa1406011. PMID 25738667.
- ^ "Phase IV Clinical Trial of Recombinant Hepatitis E Vaccine(Hecolin) - Full Text View - ClinicalTrials.gov". clinicaltrials.gov. Archived from the original on 2016-03-09. Retrieved 2016-03-09.
- ^ Rizzetto M (2020). "Epidemiology of the Hepatitis D virus". WikiJournal of Medicine. 7: 7. doi:10.15347/wjm/2020.001.
- ^ "Drinking Levels Defined National Institute on Alcohol Abuse and Alcoholism (NIAAA)". www.niaaa.nih.gov. 14 September 2011. Archived from the original on 2016-03-23. Retrieved 2016-03-09.
- ^ Franco, Elisabetta; Meleleo, Cristina; Serino, Laura; Sorbara, Debora; Zaratti, Laura (2012-03-27). "Hepatitis A: Epidemiology and prevention in developing countries". World Journal of Hepatology. 4 (3): 68–73. doi:10.4254/wjh.v4.i3.68. ISSN 1948-5182. PMC 3321492. PMID 22489258.
- ^ "Pinkbook Hepatitis B Epidemiology of Vaccine Preventable Diseases CDC". www.cdc.gov. Archived from the original on 2016-03-07. Retrieved 2016-03-09.
- ^ Jump up to: a b c d e f g h i j k l m n o p q r s t Carroll, Karen (2015). "Chapter 35: Hepatitis Viruses". Medical Microbiology. New York: McGraw-Hill. ISBN 978-0071824989.
- ^ "Commentary U.S. 2013 Surveillance Data for Viral Hepatitis Statistics & Surveillance Division of Viral Hepatitis CDC". www.cdc.gov. Archived from the original on 2016-03-05. Retrieved 2016-03-09.
- ^ 라이트 NMJ, 밀슨 CE, 톰킨스 CNE(2005) C형 간염의 감염을 줄이기 위한 개입의 효과와 관련 질병성의 증거는 무엇인가? 코펜하겐, WHO 유럽 지역 사무소(Health Invidence Network 보고서; CS1 maint: 제목(링크)으로 보관된 사본, 2016년 3월 9일에 액세스.
- ^ Basra, Sarpreet; Anand, Bhupinderjit S (2011-05-27). "Definition, epidemiology and magnitude of alcoholic hepatitis". World Journal of Hepatology. 3 (5): 108–113. doi:10.4254/wjh.v3.i5.108. ISSN 1948-5182. PMC 3124876. PMID 21731902.
- ^ "The Epidemiology of Alcoholic Liver Disease". pubs.niaaa.nih.gov. Archived from the original on 2016-03-03. Retrieved 2016-03-09.
- ^ Jump up to: a b Messori, Andrea; Badiani, Brigitta; Trippoli, Sabrina (2015-12-01). "Achieving Sustained Virological Response in Hepatitis C Reduces the Long-Term Risk of Hepatocellular Carcinoma: An Updated Meta-Analysis Employing Relative and Absolute Outcome Measures". Clinical Drug Investigation. 35 (12): 843–850. doi:10.1007/s40261-015-0338-y. ISSN 1179-1918. PMID 26446006. S2CID 41365729.
- ^ Jump up to: a b c d e f g Thiagarajan, Prarthana; Ryder, Stephen D. (2015-12-01). "The hepatitis C revolution part 1: antiviral treatment options". Current Opinion in Infectious Diseases. 28 (6): 563–571. doi:10.1097/QCO.0000000000000205. ISSN 1473-6527. PMID 26524328. S2CID 11926260.
- ^ Jump up to: a b c d e f g h i j Gogela, Neliswa A.; Lin, Ming V.; Wisocky, Jessica L.; Chung, Raymond T. (2015-03-01). "Enhancing our understanding of current therapies for Hepatitis C virus (HCV)". Current HIV/AIDS Reports. 12 (1): 68–78. doi:10.1007/s11904-014-0243-7. ISSN 1548-3568. PMC 4373591. PMID 25761432.
- ^ Jump up to: a b Abbas, Zaigham; Khan, Muhammad Arsalan; Salih, Mohammad; Jafri, Wasim (2011-12-07). "Interferon alpha for chronic hepatitis D". Cochrane Database of Systematic Reviews (12): CD006002. doi:10.1002/14651858.cd006002.pub2. PMC 6823236. PMID 22161394.
- ^ Jump up to: a b "HEV FAQs for Health Professionals Division of Viral Hepatitis CDC". www.cdc.gov. Archived from the original on 2016-03-08. Retrieved 2016-03-17.
- ^ Jump up to: a b c d e f g Singh, Siddharth; Murad, Mohammad Hassan; Chandar, Apoorva K.; Bongiorno, Connie M.; Singal, Ashwani K.; Atkinson, Stephen R.; Thursz, Mark R.; Loomba, Rohit; Shah, Vijay H. (2015-10-01). "Comparative Effectiveness of Pharmacological Interventions for Severe Alcoholic Hepatitis: A Systematic Review and Network Meta-analysis". Gastroenterology. 149 (4): 958–970.e12. doi:10.1053/j.gastro.2015.06.006. ISSN 1528-0012. PMID 26091937.
- ^ Jump up to: a b Thursz, Mark; Forrest, Ewan; Roderick, Paul; Day, Christopher; Austin, Andrew; O'Grady, John; Ryder, Stephen; Allison, Michael; Gleeson, Dermot (2015-12-01). "The clinical effectiveness and cost-effectiveness of STeroids Or Pentoxifylline for Alcoholic Hepatitis (STOPAH): a 2 × 2 factorial randomised controlled trial". Health Technology Assessment. 19 (102): 1–104. doi:10.3310/hta191020. ISSN 2046-4924. PMC 4781103. PMID 26691209.
- ^ Rambaldi, Andrea; Jacobs, Bradly P; Gluud, Christian (2007-10-17). "Milk thistle for alcoholic and/or hepatitis B or C virus liver diseases". Protocols (4): CD003620. doi:10.1002/14651858.cd003620.pub3. ISSN 1465-1858. PMID 17943794.
- ^ Summerskill, W. H.; Korman, M. G.; Ammon, H. V.; Baggenstoss, A. H. (1975-11-01). "Prednisone for chronic active liver disease: dose titration, standard dose, and combination with azathioprine compared". Gut. 16 (11): 876–883. doi:10.1136/gut.16.11.876. ISSN 0017-5749. PMC 1413126. PMID 1104411.
- ^ Bartenschlager, ed. (2013). Hepatitis C Virus: From Molecular Virology to Antiviral Therapy. Springer.
- ^ Khuroo, MS (1981). "Incidence and severity of viral hepatitis in pregnancy". Am J Med. 70 (2): 252–5. doi:10.1016/0002-9343(81)90796-8. PMID 6781338.
- ^ Gill, RQ (2001). "Acute Liver Failure". J Clin Gastroenterol. 33 (3): 191–8. doi:10.1097/00004836-200109000-00005. PMID 11500606.
- ^ Smedile, A; et al. (1981). "Infection with the delta agent in chronic HBsAg carriers". Gastroenterology. 81 (6): 992–7. doi:10.1016/S0016-5085(81)80003-0. PMID 7286594.
- ^ Abbas, Zaigham; Ali, Syed Salman; Shazi, Lubna (2015-06-02). "Interferon alpha versus any other drug for chronic hepatitis D". Cochrane Database of Systematic Reviews. doi:10.1002/14651858.cd011727.
- ^ Thein, Hla-Hla; Yi, Qilong; Dore, Gregory J.; Krahn, Murray D. (2008-08-01). "Estimation of stage-specific fibrosis progression rates in chronic hepatitis C virus infection: a meta-analysis and meta-regression". Hepatology. 48 (2): 418–431. doi:10.1002/hep.22375. ISSN 1527-3350. PMID 18563841. S2CID 20771903.
- ^ Fattovich, G (1997). "Morbidity and mortality in compensated cirrhosis type C: a retrospective follow-up study of 384 patients". Gastroenterology. 112 (2): 463–72. doi:10.1053/gast.1997.v112.pm9024300. PMID 9024300.
- ^ "Hepatitis A Information Division of Viral Hepatitis CDC". www.cdc.gov. Archived from the original on 2016-03-04. Retrieved 2016-03-08.
- ^ Jump up to: a b Aggarwal, Rakesh; Goel, Amit (2015). "Hepatitis A". Current Opinion in Infectious Diseases. 28 (5): 488–496. doi:10.1097/qco.0000000000000188. PMID 26203853. S2CID 22340290.
- ^ "WHO Hepatitis A". www.who.int. Archived from the original on 2014-02-21. Retrieved 2016-03-08.
- ^ "Hepatitis A Questions and Answers for Health Professionals Division of Viral Hepatitis CDC". www.cdc.gov. Archived from the original on 2016-03-06. Retrieved 2016-03-08.
- ^ Jump up to: a b c d e Rosen, Hugo R. (2011-06-23). "Clinical practice. Chronic hepatitis C infection". The New England Journal of Medicine. 364 (25): 2429–2438. doi:10.1056/NEJMcp1006613. ISSN 1533-4406. PMID 21696309.
- ^ Edlin, Brian R.; Eckhardt, Benjamin J.; Shu, Marla A.; Holmberg, Scott D.; Swan, Tracy (2015-11-01). "Toward a more accurate estimate of the prevalence of hepatitis C in the United States". Hepatology. 62 (5): 1353–1363. doi:10.1002/hep.27978. ISSN 1527-3350. PMC 4751870. PMID 26171595.
- ^ Jump up to: a b c d "HEV FAQs for Health Professionals Division of Viral Hepatitis CDC". www.cdc.gov. Archived from the original on 2016-03-08. Retrieved 2016-03-09.
- ^ Singal, Ashwani K.; Kamath, Patrick S.; Gores, Gregory J.; Shah, Vijay H. (2014-04-01). "Alcoholic hepatitis: current challenges and future directions". Clinical Gastroenterology and Hepatology. 12 (4): 555–564, quiz e31–32. doi:10.1016/j.cgh.2013.06.013. ISSN 1542-7714. PMC 3883924. PMID 23811249.
- ^ Jump up to: a b Shoreibah, Mohamed; Anand, Bhupinderjit S.; Singal, Ashwani K. (2014-09-14). "Alcoholic hepatitis and concomitant hepatitis C virus infection". World Journal of Gastroenterology. 20 (34): 11929–11934. doi:10.3748/wjg.v20.i34.11929. ISSN 2219-2840. PMC 4161778. PMID 25232227.
- ^ Singal, Ashwani K.; Anand, Bhupinder S. (2007-09-01). "Mechanisms of synergy between alcohol and hepatitis C virus". Journal of Clinical Gastroenterology. 41 (8): 761–772. doi:10.1097/MCG.0b013e3180381584. ISSN 0192-0790. PMID 17700425. S2CID 19482895.
- ^ Wree, Alexander; Broderick, Lori; Canbay, Ali; Hoffman, Hal M.; Feldstein, Ariel E. (2013-11-01). "From NAFLD to NASH to cirrhosis-new insights into disease mechanisms". Nature Reviews. Gastroenterology & Hepatology. 10 (11): 627–636. doi:10.1038/nrgastro.2013.149. ISSN 1759-5053. PMID 23958599. S2CID 6899033.
- ^ Jump up to: a b Weiß, Johannes; Rau, Monika; Geier, Andreas (2014-06-27). "Non-alcoholic fatty liver disease: epidemiology, clinical course, investigation, and treatment". Deutsches Ärzteblatt International. 111 (26): 447–452. doi:10.3238/arztebl.2014.0447. ISSN 1866-0452. PMC 4101528. PMID 25019921.
- ^ Jump up to: a b Michelotti, Gregory A.; Machado, Mariana V.; Diehl, Anna Mae (2013-11-01). "NAFLD, NASH and liver cancer". Nature Reviews. Gastroenterology & Hepatology. 10 (11): 656–665. doi:10.1038/nrgastro.2013.183. ISSN 1759-5053. PMID 24080776. S2CID 22315274.
- ^ Trepo, Christian (February 2014). "A brief history of hepatitis milestones". Liver International. 34 (Supplement s1): 29–37. doi:10.1111/liv.12409. PMID 24373076. S2CID 41215392.
- ^ Oon, GC (July 2012). "Viral hepatitis—the silent killer". Annals of the Academy of Medicine, Singapore. 41 (7): 279–80. PMID 22892603.
- ^ Lee, Christine A.; Thomas, Howard C., eds. (1988). Classic papers in viral hepatitis. Foreword by Dame Sheila Sherlock. London, England: Science Press. ISBN 978-1-870026-10-9.
- ^ Purcell, RH (April 1993). "The discovery of the hepatitis viruses". Gastroenterology. 104 (4): 955–63. doi:10.1016/0016-5085(93)90261-a. PMID 8385046.
- ^ Bradley, WH (1946). "Homologous Serum Jaundice". Proceedings of the Royal Society of Medicine. 39 (10): 649–654. doi:10.1177/003591574603901012. PMC 2181926. PMID 19993376.
- ^ Munson, Ronald (1996). Intervention and Reflection: Basic Issues in Medical Ethics. pp. 273–281.
- ^ Beecher, Henry (1966). "Ethics and Clinical Research". The New England Journal of Medicine. 274 (24): 1354–1360. doi:10.1056/nejm196606162742405. PMID 5327352.; 재인쇄
- ^ Jump up to: a b Purcell, RH (April 1993). "The discovery of the hepatitis viruses". Gastroenterology. 104 (4): 955–63. doi:10.1016/0016-5085(93)90261-a. PMID 8385046.
- ^ Emanuel, Ezekiel (2008). The Oxford Textbook of Clinical Research Ethics. Oxford University Press. pp. 80–85.
- ^ Odelberg, Wilhelm (1976). Les Prix Nobel.
- ^ Alter, Harvey J. (2014-01-01). "The road not taken or how I learned to love the liver: A personal perspective on hepatitis history". Hepatology. 59 (1): 4–12. doi:10.1002/hep.26787. ISSN 1527-3350. PMID 24123147.
- ^ Blumberg BS; Alter HJ (1965-02-15). "A "new" antigen in leukemia sera". JAMA. 191 (7): 541–546. doi:10.1001/jama.1965.03080070025007. ISSN 0098-7484. PMID 14239025.
- ^ "The Nobel Prize in Physiology or Medicine 1976". NobelPrize.org. Retrieved 2019-10-07.
- ^ Jump up to: a b c d Udompap, Prowpanga; Kim, Donghee; Kim, W. Ray (2015-11-01). "Current and Future Burden of Chronic Nonmalignant Liver Disease". Clinical Gastroenterology and Hepatology. 13 (12): 2031–2041. doi:10.1016/j.cgh.2015.08.015. ISSN 1542-7714. PMC 4618163. PMID 26291665.
- ^ Jump up to: a b Lemoine, Maud; Eholié, Serge; Lacombe, Karine (2015). "Reducing the neglected burden of viral hepatitis in Africa: Strategies for a global approach". Journal of Hepatology. 62 (2): 469–476. doi:10.1016/j.jhep.2014.10.008. PMID 25457207.
- ^ Jump up to: a b Koslap-Petraco, Mary Beth; Shub, Mitchell; Judelsohn, Richard (2008). "Hepatitis A: Disease Burden and Current Childhood Vaccination Strategies in the United States". Journal of Pediatric Health Care. 22 (1): 3–11. doi:10.1016/j.pedhc.2006.12.011. PMID 18174084.
- ^ Previsani, Nicoletta; Lavanchy, Daniel (2000). "Hepatitis A" (PDF). World Health Organization Global Alert and Response. World Health Organization. Retrieved March 5, 2016.
- ^ Anonychuk, Andrea M.; Tricco, Andrea C.; Bauch, Chris T.; Pham, Ba'; Gilca, Vladimir; Duval, Bernard; John-Baptiste, Ava; Woo, Gloria; Krahn, Murray (2008-01-01). "Cost-effectiveness analyses of hepatitis A vaccine: a systematic review to explore the effect of methodological quality on the economic attractiveness of vaccination strategies". PharmacoEconomics. 26 (1): 17–32. doi:10.2165/00019053-200826010-00003. ISSN 1170-7690. PMID 18088156. S2CID 46965673.
- ^ Chan, Henry Lik-Yuen; Jia, Jidong (2011-01-01). "Chronic hepatitis B in Asia—new insights from the past decade". Journal of Gastroenterology and Hepatology. 26: 131–137. doi:10.1111/j.1440-1746.2010.06544.x. ISSN 1440-1746. PMID 21199524. S2CID 23548529.
- ^ Jump up to: a b Dan, Yock Young; Aung, Myat Oo; Lim, Seng Gee (2008-09-01). "The economics of treating chronic hepatitis B in Asia". Hepatology International. 2 (3): 284–295. doi:10.1007/s12072-008-9049-2. ISSN 1936-0533. PMC 2716880. PMID 19669256.
- ^ Lavanchy, D. (2004-03-01). "Hepatitis B virus epidemiology, disease burden, treatment, and current and emerging prevention and control measures". Journal of Viral Hepatitis. 11 (2): 97–107. doi:10.1046/j.1365-2893.2003.00487.x. ISSN 1352-0504. PMID 14996343. S2CID 163757.
- ^ Jump up to: a b c Younossi, Z. M.; Kanwal, F.; Saab, S.; Brown, K. A.; El-Serag, H. B.; Kim, W. R.; Ahmed, A.; Kugelmas, M.; Gordon, S. C. (2014-03-01). "The impact of hepatitis C burden: an evidence-based approach". Alimentary Pharmacology & Therapeutics. 39 (5): 518–531. doi:10.1111/apt.12625. ISSN 1365-2036. PMID 24461160. S2CID 21263906.
- ^ Myers, Robert P.; Krajden, Mel; Bilodeau, Marc; Kaita, Kelly; Marotta, Paul; Peltekian, Kevork; Ramji, Alnoor; Estes, Chris; Razavi, Homie (2014-05-01). "Burden of disease and cost of chronic hepatitis C infection in Canada". Canadian Journal of Gastroenterology & Hepatology. 28 (5): 243–250. doi:10.1155/2014/317623. ISSN 2291-2797. PMC 4049256. PMID 24839620.
- ^ Jump up to: a b c d e f g Centers for Disease Control and Prevention (CDC) (2003-11-28). "Hepatitis A outbreak associated with green onions at a restaurant—Monaca, Pennsylvania, 2003". MMWR. Morbidity and Mortality Weekly Report. 52 (47): 1155–1157. ISSN 1545-861X. PMID 14647018.
- ^ Polgreen, Lydia (November 16, 2003). "Community Is Reeling From Hepatitis Outbreak". The New York Times. Archived from the original on March 22, 2016. Retrieved March 10, 2016.
- ^ Jump up to: a b Jordan, Ashly E.; Perlman, David C.; Neurer, Joshua; Smith, Daniel J.; Des Jarlais, Don C.; Hagan, Holly (2016-01-28). "Prevalence of hepatitis C virus infection among HIV+ men who have sex with men: a systematic review and meta-analysis". International Journal of STD & AIDS. 28 (2): 145–159. doi:10.1177/0956462416630910. ISSN 1758-1052. PMC 4965334. PMID 26826159.
- ^ Jump up to: a b c d Platt, Lucy; Easterbrook, Philippa; Gower, Erin; McDonald, Bethan; Sabin, Keith; McGowan, Catherine; Yanny, Irini; Razavi, Homie; Vickerman, Peter (2016-02-24). "Prevalence and burden of HCV co-infection in people living with HIV: a global systematic review and meta-analysis" (PDF). The Lancet. Infectious Diseases. 16 (7): 797–808. doi:10.1016/S1473-3099(15)00485-5. ISSN 1474-4457. PMID 26922272.
- ^ Jump up to: a b c d e f Cunningham, F. Gary; et al. (2013). "Hepatic, Biliary, and Pancreatic Disorders." Williams Obstetrics, Twenty-Fourth Edition. New York, NY: McGraw-Hill.
- ^ Tassopoulos, NC; et al. (June 1987). "Natural history of acute hepatitis B surface antigen-positive hepatitis in Greek adults". Gastroenterology. 92 (6): 1844–50. doi:10.1016/0016-5085(87)90614-7. PMID 3569758.
- ^ "A Comprehensive Immunization Strategy to Eliminate Transmission of Hepatitis B Virus Infection in the United States Recommendations of the Advisory Committee on Immunization Practices (ACIP) Part 1: Immunization of Infants, Children, and Adolescents". www.cdc.gov. Archived from the original on 2016-03-24. Retrieved 2016-03-16.
- ^ Jump up to: a b c Terrault, Norah A.; Bzowej, Natalie H.; Chang, Kyong-Mi; Hwang, Jessica P.; Jonas, Maureen M.; Murad, M. Hassan (2016-01-01). "AASLD guidelines for treatment of chronic hepatitis B". Hepatology. 63 (1): 261–283. doi:10.1002/hep.28156. ISSN 1527-3350. PMC 5987259. PMID 26566064.
- ^ Wang, Liming; Kourtis, Athena P.; Ellington, Sascha; Legardy-Williams, Jennifer; Bulterys, Marc (2013-12-01). "Safety of tenofovir during pregnancy for the mother and fetus: a systematic review". Clinical Infectious Diseases. 57 (12): 1773–1781. doi:10.1093/cid/cit601. ISSN 1537-6591. PMID 24046310.
- ^ Shi, Zhongjie; Yang, Yuebo; Ma, Lin; Li, Xiaomao; Schreiber, Ann (2010-07-01). "Lamivudine in late pregnancy to interrupt in utero transmission of hepatitis B virus: a systematic review and meta-analysis". Obstetrics and Gynecology. 116 (1): 147–159. doi:10.1097/AOG.0b013e3181e45951. ISSN 1873-233X. PMID 20567182. S2CID 41784922.
- ^ Jump up to: a b c Benova, Lenka; Mohamoud, Yousra A.; Calvert, Clara; Abu-Raddad, Laith J. (2014-09-15). "Vertical transmission of hepatitis C virus: systematic review and meta-analysis". Clinical Infectious Diseases. 59 (6): 765–773. doi:10.1093/cid/ciu447. ISSN 1537-6591. PMC 4144266. PMID 24928290.
- ^ Jin, H.; Zhao, Y.; Zhang, X.; Wang, B.; Liu, P. (2016-03-01). "Case-fatality risk of pregnant women with acute viral hepatitis type E: a systematic review and meta-analysis". Epidemiology & Infection. FirstView (10): 2098–2106. doi:10.1017/S0950268816000418. ISSN 1469-4409. PMID 26939626.