레디파스비르
Ledipasvir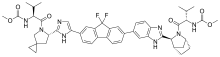 | |
| 임상자료 | |
|---|---|
| 상명 | 하보니 (소포스부비르와 결합) |
| 기타 이름 | GS-5885 |
| 라이센스 데이터 | |
| 경로: 행정 | 입으로 |
| ATC 코드 | |
| 법적현황 | |
| 법적현황 |
|
| 약동학 데이터 | |
| 생체이용가능성 | 76% |
| 단백질 결합 | >99% |
| 신진대사 | 시토크롬 대사 금지 |
| 제거 반감기 | 47시간 |
| 식별자 | |
| |
| CAS 번호 | |
| 펍켐 CID | |
| 드러그뱅크 | |
| 켐스파이더 | |
| 유니 | |
| 케그 | |
| 체비 | |
| CompTox 대시보드 (EPA) | |
| 화학 및 물리적 데이터 | |
| 공식 | C49H54F2N8O6 |
| 어금질량 | 889.018 g·1998−1 |
| 3D 모델(JSmol) | |
| |
| |
레디파스비르는 길리어드사이언스가 개발한 C형 간염 치료제다.[1] 3단계 임상시험을 마친 길리어드는 2014년 2월 10일 유전자형 1형 간염 C형 간염에 대한 ledipasvir/sofosbuvir 고정-dose 콤비네이션 태블릿의 미국 승인을 신청했다.[2][3] ledipasvir/sofosbuvir 조합은 HCV 복제를 방해하는 직접작용 항바이러스제로 PEG-인터페론이나 리바비린 없이 유전자형 1a 또는 1b로 환자를 치료하는 데 사용할 수 있다.
레디파스비르는 C형 간염 바이러스 단백질인 NS5A의 억제제다.
2013년 3월 제20차 레트로바이러스와 기회주의 감염에 관한 컨퍼런스에서 제시된 자료에 따르면 뉴클레오티드 아날로그 억제제 소포스부비르, 레디파스비르, 리바비린의 3중 요법은 치료감호 환자와 사전 반응자 모두에게 100%의 치료 후 지속적 바이러스 반응(SVR12)을 생성했다.CV 유전자형 1.[4][5] Sofosbuvir/ledipasvir 공식을 리바비린과 함께 또는 사용하지 않고 시험하고 있다. 2014년 2월 길리어드는 미국 식품의약국(FDA)에 인터페론과 리바비린 없이 레디파스비르/소포스부비르 구강 치료 승인을 요청했다.[6]
2014년 10월 10일 FDA는 하보니라는 복합 제품인 ledipasvir/sofosbuvir를 승인했다.[7]
의학적 용법
레디파스비르는 만성 C형 간염 1형 환자에서 치료를 위해 소포스뷔르와 함께 가장 많이 사용된다. 이 약은 검사하여 치료감호 및 치료경험이 있는 환자에게 효능을 보였다.[8]
역효과
임상 실험에 따르면, 레디파스비르/소포스부비르는 피로와 두통이라는 가장 흔한 부작용에 매우 잘 용인되어 왔다.[9]
상호작용
하보니와의 대부분의 약물-마약 상호작용은 세인트와 같은 Pgp 유도체를 포함한다. 존은 보트를 타거나 리팜피신을 타거나 한다. 병행 사용으로 하보니의 혈중 농도가 낮아져 치료 효과가 줄어든다.[9]
작용기전
레디파스비르는 바이러스 복제, 조립, 분비 등에 관여하는 중요한 바이러스 인산염, NS5A를 억제한다.[10]
반면 소포스부비르는 우리딘 삼인산 모방에 대사되어 NS5B 중합효소에 의해 RNA에 통합되었을 때 RNA 체인 터미네이터 역할을 한다.[10]
비용
소포스부비르와 마찬가지로 하보니 비용도 논란이 되고 있다. 미국에서는 약 한 알에 1,125달러, 8주 치료 코스는 6만 3천 달러, 12주 치료 코스는 9만 4천 500달러, 24주 치료 코스는 18만 9천 달러로 환산된다. 길리어드는 간 이식에 두 배의 비용을 지출하거나 일시적으로 간질환을 치료하는 비용보다 C형 간염 치료의 장점을 더 크게 부각시켜 비용을 정당화한다. 길리어드는 치료비를 감당할 수 없는 C형 간염 환자나 보험이 부족한 환자를 위해 레디파스비르/소포스부버비르 지원 프로그램을 제공했다.[10]
2015년 7월 길리어드는 미국에서 HCV 환자에 대한 지원 경로 혜택을 받기 위해 자격 기준을 수정했다.
참고 항목
참조
- ^ "Ledipasvir" (PDF). United States Adopted Name.
- ^ "Ledipasvir-submitted-to-FDA".
- ^ "GS-5885". Gilead Sciences. Archived from the original on 2013-04-10. Retrieved 2013-03-08.
- ^ Electron: Sofosbuvir + Ledipasvir (GS-5885) + Ribavirin 12주간의 치료 후 처리를 통한 바이러스 부하 100% 억제 및 -경험이 풍부한 C형 간염 바이러스 GT 1 환자 웨이백머신 보관 2013-03-23 제인, 에드워드 외 20차 레트로바이러스와 기회주의 감염에 관한 회의 2013년 3월 3일-6일. 추상 41LB.
- ^ CROI 2013: Sofosbuvir + Redipasvir + Ribavirin Combo for HCV, 웨이백 머신에서 100% 지속 응답 보관 2015-09-24 생산 하일리먼, 리즈 HIVandHepatitis.com. 2013년 3월 4일.
- ^ "Gilead Files for U.S. Approval of Ledipasvir/Sofosbuvir Fixed-Dose Combination Tablet for Genotype 1 Hepatitis C". Gilead Sciences. 10 February 2014.
- ^ "U.S. Food and Drug Administration Approves Gilead's Harvoni (Ledipasvir/Sofosbuvir), the First Once-Daily Single Tablet Regimen for the Treatment of Genotype 1 Chronic Hepatitis C". 10 October 2014. Retrieved 10 October 2014.
- ^ Afdhal N, Zeuzem S, Kwo P, Chojkier M, Gitlin N, Puoti M, et al. (May 2014). "Ledipasvir and sofosbuvir for untreated HCV genotype 1 infection". The New England Journal of Medicine. 370 (20): 1889–98. doi:10.1056/NEJMoa1402454. PMID 24725239.
- ^ a b "PRESCRIBING INFORMATION" (PDF). www.gilead.com. Retrieved 2019-06-12.
- ^ a b c "Ledipasvir-Sofosbuvir Harvoni - Treatment - Hepatitis C Online". www.hepatitisc.uw.edu.


