기흉
Pneumothorax| 기흉 | |
|---|---|
| 기타 이름 | 붕괴폐[1] |
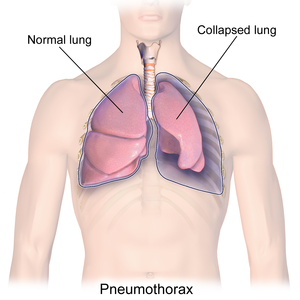 | |
| 붕괴된 폐 또는 기흉을 나타내는 그림 | |
| 전문 | 맥동학, 흉부외과 |
| 증상 | 가슴통증, 호흡곤란, 피로감[2] |
| 평상시 시작 | 갑자기[3] |
| 원인들 | 알 수 없음, 외상[3] |
| 위험요소 | COPD, 결핵, 흡연[4] |
| 진단법 | 흉부 X선, 초음파, CT 스캔[5] |
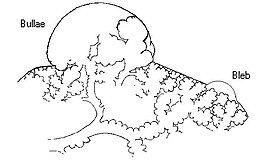
| 차등진단 | 폐불래,[3] 혈흉[2] |
| 예방 | 금연[3] |
| 치료 | 보수적, 바늘 흡인, 흉관, 늑막염[3] |
| 빈도 | 연간[3][5] 10만 명당 20명 |
기흉은 폐벽과 흉벽 사이의 흉막 공간에서 비정상적으로 공기를 모으는 것이다.[3]증상은 전형적으로 갑자기 날카롭고 한쪽으로 치우친 가슴통증과 호흡곤란이 있다.[2]소수의 경우, 손상된 조직의 영역에 의해 단방향 밸브가 형성되고 흉벽과 폐 사이의 공간에 있는 공기의 양이 증가하는데, 이를 장력 기흉이라고 한다.[3]이것은 산소 부족과 저혈압을 지속적으로 악화시킬 수 있다.이로 인해 폐쇄성 쇼크라고 하는 일종의 충격으로 이어지게 되는데, 이 충격은 되돌리지 않으면 치명적일 수 있다.[3]매우 드물게, 양쪽 폐가 기흉에 의해 영향을 받을 수 있다.[6]비록 그 용어가 식중독을 의미할 수도 있지만, 종종 "붕괴된 폐"라고 불린다.[1]
1차 자연발생성 기흉은 뚜렷한 원인 없이 중대한 폐질환이 없을 때 발생하는 기흉이다.[3]2차 자연발생적 기흉은 기존의 폐질환이 있는 곳에서 발생한다.[3][7]흡연은 1차 자연적 기흉의 위험을 증가시키는 반면 2차 기흉의 주요 근본 원인은 COPD, 천식, 결핵이다.[3][4]외상성 기흉은 신체적인 외상과 흉부(폭발성 부상 포함) 또는 의료 개입의 합병증에서 발생할 수 있다.[8][9]
신체검사만으로 기흉을 진단하는 것은 어려울 수 있다(특히 작은 기흉에서는 더욱 그러하다).[10]흉부 X선, 컴퓨터 단층 촬영(CT) 또는 초음파는 보통 그 존재를 확인하는 데 사용된다.[5]비슷한 증상을 일으킬 수 있는 다른 질환으로는 혈흉(흉막 공간에서의 혈액의 충혈), 폐색전증, 심장마비가 있다.[2][11]큰 불라는 흉부 엑스레이에서 비슷하게 보일 수 있다.[3]
작은 자발적 기흉은 일반적으로 치료 없이 해결되며 모니터링만 필요하다.[3]이러한 접근방식은 근본적인 폐질환이 없는 사람들에게 가장 적합할 수 있다.[3]더 큰 기흉에서 또는 호흡곤란이 있을 경우 단방향 밸브 시스템에 연결된 주사기나 흉관 등으로 공기를 제거할 수 있다.[3]간혹 튜브 배수가 성공하지 못한 경우 수술이 필요할 수도 있고, 반복적인 에피소드가 발생한 경우 예방책으로 수술이 필요할 수도 있다.[3]외과적 치료는 보통 흉막염(흉막의 층이 서로 붙도록 유도되는 것)이나 흉막절제술(흉막의 외과적 제거술)을 포함한다.[3]기흉은 연간 10만명당 약 17~23건이 발생한다.[3][5]그들은 여자보다 남자들에게 더 흔하다.[3]
징후 및 증상
일차적 자발적 기흉(PSP)은 젊은 성인에게서 근본적인 폐 질환이 없는 상태에서 발생하는 경향이 있으며, 대개는 제한된 증상을 일으킨다.가슴통증과 때로는 가벼운 호흡이 일반적인 특징이다.[12][13]PSP의 영향을 받는 사람들은 잠재적 위험을 알지 못하는 경우가 많으며 치료를 받기 전에 며칠을 기다릴 수도 있다.[14]PSP는 기압의 변화 동안에 더 흔히 발생하며 왜 기흉의 에피소드가 군집 내에서 발생할 수 있는지를 어느 정도 설명한다.[13]PSP가 장력 기흉을 일으키는 경우는 드물다.[12]
2차 자연적 기흉(SSP)은, 정의상, 중대한 기저 폐질환을 가진 개인에게서 발생한다.SSP의 증상은 PSP보다 더 심한 경향이 있는데, 일반적으로 영향을 받지 않는 폐는 영향을 받는 폐의 기능 상실을 대체할 수 없기 때문이다.저산소혈증(혈액-산소 수치의 저하)은 대개 존재하며 청색증(입술과 피부의 푸른색 변색)으로 관찰될 수 있다.과대마니아(혈중 이산화탄소 축적)는 때때로 마주친다. 이것은 혼란을 야기할 수 있고, 매우 심할 경우 혼동을 일으킬 수 있다.그러므로 만성폐쇄성폐질환(COPD), 낭포성 섬유증 또는 기타 심각한 폐질환을 가진 사람에게 갑자기 숨이 차게 되는 것은 기흉의 가능성을 확인하기 위한 신속한 조사를 해야 한다.[12][14]
외상성 기흉은 흉벽이 뚫렸을 때 가장 흔하게 발생한다. 예를 들어 찔린 상처나 총상으로 흉막 공간에 공기가 들어갈 수 있는 경우 또는 폐에 대한 다른 기계적 손상이 관련 구조물의 무결성을 손상시키기 때문이다.외상성 기흉은 전체 흉부외상 환자의 최대 절반에서 발생하는 것으로 나타났으며, 늑골 골절만이 이 집단에서 더 흔하다.기흉은 이러한 경우 절반으로 오컬트(흔히 드러나지 않음)할 수 있지만 특히 기계적 인공호흡이 필요한 경우 확대될 수 있다.[13]그것들은 또한 어떤 다른 이유로 이미 기계적인 환기를 받고 있는 사람들에게서 마주친다.[13]
신체검사 시, 늑막 공간의 공기가 소리의 전달을 축축하게 하기 때문에 (청진기로 듣는) 숨소리가 환부에 감소할 수 있다.가슴 표면으로의 성진동 전도 측정은 변경될 수 있다.가슴의 타악은 (북치는 소리처럼) 과음제로 인식될 수 있으며, 성악공명과 촉각공명 모두 눈에 띄게 감소할 수 있다.중요한 것은 기흉의 부피가 피해자가 경험하는 증상의 강도와 잘 상관되지 않을 수 있고,[14] 기흉이 상대적으로 작을 경우 신체적 징후가 뚜렷하지 않을 수 있다는 점이다.[13][14]
장력 기흉
장력 기흉은 일반적으로 기흉(일차적 자연발생적, 2차적 자연발생적 또는 외상적)이 호흡 및/또는 혈액순환의 현저한 손상을 초래할 때 존재하는 것으로 간주된다.[15]이것은 일종의 순환기충격을 유발하는데, 이를 '폐쇄충격'이라고 한다.장력 기흉은 통풍, 소생, 외상 등의 임상적 상황이나 폐질환자 등에서 발생하는 경향이 있다.[14]응급상황이며 추가 조사 없이 즉각적인 치료가 필요할 수 있다(치료 섹션 참조).[14][15]
장력 기흉이 있는 사람에게서 가장 흔히 발견되는 것은 가슴통증과 호흡곤란으로, 초기에는 심박수가 높아지고 호흡이 빠른 경우가 많다.다른 발견은 가슴 한쪽에서 더 조용한 숨소리, 낮은 산소 수준과 혈압, 그리고 기관지가 환부에서 멀리 떨어진 변위 등을 포함할 수 있다.드물게 청록증(산소 수치가 낮아 피부가 검게 변색됨), 의식의 변화된 수준, 팽창과 움직임이 감소된 환부를 검사할 때의 고엽제 타악기음, 후두부 통증(상복부), 정점박동(심장충동), 공명음 등이 있을 수 있다.흉골을 두드리는 것.[15]
장력 기흉은 기계적 인공호흡을 받는 사람에게도 발생할 수 있으며, 이 경우 일반적으로 진정제를 투여하고 있기 때문에 발견하기 어려울 수 있다. 기흉은 종종 급격한 상태 악화로 인해 나타난다.[15]최근의 연구는 긴장 기능의 발달이 항상 이전에 생각했던 것만큼 빠르지는 않을 수 있다는 것을 보여주었다.기관지가 한쪽으로 편차와 상승된 경정맥압(목 정맥)의 존재는 임상적 징후로서 신뢰할 수 없다.[15]
원인
일차 자연발생
자발적 기흉은 알려진 폐질환이 없을 때 발생하는 일차적 기흉과 기저적 폐질환이 있는 사람에게 발생하는 이차적 기흉으로 나뉜다.[16]1차적 자발적 기흉의 원인은 알려지지 않았지만, 확립된 위험 요소에는 남성 성, 흡연, 기흉 가족력이 포함된다.[17]대마초나 담배 중 하나를 피우면 위험성이 높아진다.[3]여러 가지 의심스러운 기저 메커니즘이 아래에 설명되어 있다.[12][13]
2차 자연발생
2차 자연적 기흉은 다양한 폐질환의 환경에서 발생한다.가장 흔한 질환은 만성폐쇄성폐질환(COPD)으로, 이 질환이 환자의 약 70%를 차지한다.[17]기흉의 위험을 크게 증가시킬 수 있는 알려진 폐질환은
| 유형 | 원인들 |
|---|---|
| 기도의[12] 질병 | COPD(특히 황소 폐기종이 있는 경우), 급성 중증 천식, 낭포성 섬유증 |
| 폐[12] 감염 | 폐렴성 폐렴(PCP), 결핵, 괴사성 폐렴 |
| 간막폐질환[12] | Sarcoidosis, 특발성 폐섬유화, 조직세포증 X, 림프강글레오미오마토시스(LAM) |
| 결합조직질환[12] | 류마티스 관절염, 안키로싱 스폰딜염, 다면염, 피부염, 전신 경화증, 마르판 증후군, 에를러스-댄로스 증후군 |
| 암[12] | 폐암, 폐와 관련된 사르코마 |
| 잡다한[13] | 카타멘성 기흉(월경 주기 및 흉부 자궁내막증 관련) |
어린이의 경우 홍역, 진폐증, 이물 흡입, 특정 선천성 기형(콩팥 폐 기도 기형과 선천성 로바 폐기종) 등이 추가 원인이다.[18]
자발적 기흉을 가진 사람의 11.5%는 기흉을 경험한 가족이 있다.유전적 조건인 마르판 증후군, 호모시스티누리아, 엘러스-단로스 신드롬, 알파 1-항티트리핀 결핍증(폐기물로 이어진다), 비르트-호그-두베 증후군은 모두 가족성 기흉과 연관되어 있다.[19]일반적으로 이러한 질환은 다른 징후와 증상도 유발하며 기흉은 보통 1차 발견이 아니다.[19]Birt-Hogg-Dubé 증후군은 엽록체라는 단백질을 인코딩하는 FLCN 유전자(17p11.2 염색체에 위치)의 돌연변이에 의해 발생한다.[18][19]FLCN 돌연변이와 폐 병변은 Birt-Hogg-Dubé 증후군의 다른 특징이 없는 기흉 가족 사례에서도 확인되었다.[18]HLA happlotype AB는240 유전적 연관성 외에도 PSP의 유전적 성향이다.[20][21]
트라우마
외상성 기흉은 둔기에 의한 외상이나 흉벽에 관통상을 입었을 수 있다.[13]가장 흔한 메커니즘은 폐 조직을 손상시키는 새로운 늑골 골절에서 날카로운 뼈의 점들이 침투하기 때문이다.[17]흉부에 외상을 입지는 않았지만 폭발에 노출된 사람들에게도 외상성 기흉이 관찰될 수 있다.[9]
"개방형" 또는 "폐쇄형"으로 분류할 수 있다.열린 기흉에는 외부환경에서 흉벽을 통해 흉막공간으로 들어가는 통로가 있다.이 통로를 통해 흉막 공간으로 공기가 빨려들면 '흉부 상처'로 알려져 있다.폐렴은 흉벽이 온전하게 남아 있을 때를 말한다.[22]
가슴 정맥 중 하나에 중추 정맥 카테터를 삽입하거나 폐 조직에서 조직 검사 샘플을 채취하는 등의 의료 절차는 기흉을 일으킬 수 있다.기계적 인공호흡기 또는 비침습적 인공호흡기를 투여하면 바로트라우마(압력 관련 상해)가 기흉으로 이어질 수 있다.[13]
수중 기기로 호흡하는 잠수부들은 주변 압력에서 호흡 가스를 공급받는데, 이는 대기 압력보다 높은 압력에서 가스를 포함한 폐를 발생시킨다.압축 공기를 마시는 잠수부들은 (스쿠버 다이빙과 같은) 폐를 완전히 부풀린 상태에서 숨을 참으면서 바로트라우마가 1미터(3피트)만 올라가면 기흉에 걸릴 수 있다.[23]이러한 경우에 또 다른 문제는 감압 질환의 다른 특징을 가진 사람들은 일반적으로 고압 요법으로 다이빙 방에서 치료된다는 것이다; 이것은 작은 기흉이 빠르게 커지고 긴장의 특징을 야기할 수 있다.[23]
신생아
저체중 생후 3~9일 사이의 신생아는 기흉 위험이 높다.[24]
메커니즘
흉곽은 폐, 심장, 그리고 수많은 주요 혈관을 포함하고 있는 가슴 내부의 공간이다.충치의 양쪽에 흉막은 폐표면(관측 흉막)을 덮고 흉벽 안쪽(정측 흉막)에도 선을 긋는다.일반적으로 두 층은 소량의 윤활 세러 액에 의해 분리된다.기도 내부의 압력(심폐압)이 흉막 공간 내부의 압력(심폐압)보다 높기 때문에 폐가 충치 내에서 완전히 팽창된다.흉막공간의 저기압에도 불구하고 공기가 포함된 통로로 자연적으로 연결되지 않아 공기가 들어가지 않고, 혈류 내 기체의 압력이 너무 낮아 흉막공간에 강제 투입될 수 없다.[13]따라서 기흉은 흉벽의 손상이나 폐 자체의 손상을 통해서, 또는 흉막 공간의 미생물이 가스를 생산하기 때문에 공기가 들어갈 수 있는 경우에만 발병할 수 있다.[13]일단 공기가 흉강으로 들어가면 경내 압력이 증가하여 심폐압과 경내압(전폐압으로 정의됨)의 차이가 0으로 나타나며, 이는 정상적인 심폐압인 ~4mmHg와 대조적으로 폐가 수축하게 한다.[25]
흉벽 결함은 흉벽에 자상이나 총상("열린 기흉")과 같은 부상을 입은 경우 대개 뚜렷하게 나타난다.2차 자연적 기흉에서 폐조직의 취약성은 다양한 질병 과정, 특히 폐기종이 심한 경우 황소(공기가 포함된 큰 병변)가 파열되면서 발생한다.괴사(사망)의 부위는 정확한 메커니즘은 불분명하지만 기흉의 증세를 촉진시킬 수 있다.[12]1차 자연 기흉(PSP)은 수년 동안 기계적 요인에 의해 기흉(키 큰 수컷)의 위험에 있는 고전적으로 더 흔한 것으로 추정된 "블럽"(흉막 표면 바로 아래의 작은 공기 주입 병변)에 의해 야기된 것으로 생각되어 왔다.PSP에서 표백은 77%의 사례에서 발견될 수 있으며, PSP의 이력이 없는 일반 인구의 6%에 비해 더 많다.[26]이러한 건강한 피험자가 나중에 모두 기흉이 생기는 것은 아니기 때문에, 그 가설은 모든 에피소드를 설명하기에 충분하지 않을 수 있다. 더욱이 기흉은 표백의 수술적 치료 후에도 재발할 수 있다.[13]따라서 PSP도 파열되기 쉬운 흉막층의 붕괴(포도) 영역으로 인해 발생할 수 있다는 의견이 제기되었다.[12][13][26]흡연은 추가적인 염증과 작은 기도의 방해로 이어질 수 있는데, 이는 흡연자들의 PSP 위험 증가가 두드러지게 증가하고 있다.[14]일단 흉강으로 공기가 들어가지 않게 되면 점차 다시 흡수된다.[14]
장력 기흉은 공기가 흉막 공간 안으로 들어갈 수 있는 개구부가 단방향 밸브로 기능할 때 발생하며, 숨을 쉴 때마다 더 많은 공기가 들어갈 수 있지만 빠져나갈 수는 없다.신체는 호흡수와 조수량을 증가시켜 문제를 악화시킴으로써 보상한다.고쳐지지 않는 한 저산소증(산소수치 저하)과 호흡기 정지 등이 결국 뒤따른다.[15]
진단
기흉의 증상은 특히 PSP가 작은 경우 모호하고 단정하지 못할 수 있다. 일반적으로 의료 영상과의 확인이 필요하다.[14]이와는 대조적으로, 장력 기흉은 의학적인 응급상황이며 특히 심각한 저산소증, 매우 낮은 혈압 또는 의식수준이 손상된 경우 영상촬영 전에 치료할 수 있다.장력 기흉에서는 기흉의 해부학적 위치에 대한 의심이 있을 경우 X선이 필요할 때가 있다.[15][17]
흉부 엑스레이
뒤쪽(후방 또는 "PA")에서 투사되는 X선 빔과 최대 영감(호흡을 참는 것) 동안 이상적으로 일반 흉부 방사선 촬영이 가장 적절한 첫 번째 조사다.[27]만료 기간 동안 일상적으로 이미지를 촬영하는 것이 어떤 이점도 줄 수 있다고 믿어지지 않는다.[28]그러나 임상적 의심이 높을 때 기흉을 검출하는 데 유용할 수 있지만 영감 방사선 촬영은 정상으로 나타난다.[29]또한 PA X선에 기흉이 나타나지 않지만 1에 대한 강한 의심이 있을 경우 측면 X선(옆에서 빔이 돌출된 상태)을 실시할 수 있으나 이는 일상적인 관행이 아니다.[14][18]
좌현 삽입으로 인한 미세한 좌측 기흉을 보이는 안테로포스테리어(Anteroposorior)가 X-ray에 영감을 주어
종격자(심장, 대혈관, 큰 기도가 들어 있는 폐 사이의 구조)가 기압 차이로 인해 영향을 받은 폐에서 멀어지는 것은 예사롭지 않다.이는 주로 증상의 별자리, 저산소증, 충격에 의해 결정되는 장력 기흉에 해당하지 않는다.[13]
기흉의 크기(즉 흉막 공간의 공기량)는 흉벽과 폐 사이의 거리를 측정하여 적당한 정확도로 결정할 수 있다.이것은 작은 기흉이 다르게 관리될 수 있기 때문에 치료와 관련이 있다.2 cm의 공기 림은 기흉이 혈흉의 약 50%를 차지하는 것을 의미한다.[14]영국 전문적인 지침 전통적으로 반면 미국 지침에 따르면 측정 값이 폐의 정점(최고)3)과" 작은"과 a을 차별 할 것이라고 측정은 배꼽(어디에 혈관과 기도 폐에 들어가)의 수준에서 2cm로 cutoff,[14]으로 수행해야 한다 언급된 것"나는기흉을 [30]일으키다후자의 방법은 기흉이 주로 정점에 위치한다면 기흉의 크기를 과대평가할 수 있는데, 이는 흔히 있는 일이다.[14]다양한 방법들은 상관관계가 좋지 않지만 기흉 크기를 추정하는 가장 쉽게 이용할 수 있는 방법이다.[14][18]CT 스캔(아래 참조)은 기흉 크기를 보다 정확하게 판단할 수 있지만 이 설정에서 기흉을 일상적으로 사용하는 것은 권장하지 않는다.[30]
모든 기흉이 균일한 것은 아니다; 어떤 기흉은 가슴의 특정 부위에만 공기 주머니를 형성한다.[14]흉부 X선(수압공압도압축)에 소량의 유체가 표시될 수 있으며, 이는 혈액(혈압도압도압)일 수 있다.[13]경우에 따라서는 유체의 이상 유무로 인해 흉벽과 횡격막 사이의 공간이 정상적으로 작아 보이는 '딥설커스 부호'만 유의미한 이상일 수 있다.[15]
컴퓨터단층촬영
기흉 진단에는 CT 스캔이 필요하지 않지만 특정 상황에서 유용할 수 있다.일부 폐질환, 특히 폐기종에서는 흉부 X선에 불래(공기충전주머니)와 같은 비정상적인 폐부위가 기흉과 같은 외관을 가질 수 있으며, 구별하기 전과 기흉의 정확한 위치와 크기가 결정되기 전에는 어떤 치료법도 적용하는 것이 안전하지 않을 수 있다.[14]직립필름을 시술할 수 없는 외상에서는 흉부 방사선 촬영이 기흉의 3분의 1까지 놓칠 수 있는 반면 CT는 매우 민감한 상태를 유지한다.[17]
CT의 추가 사용은 기저 폐병변의 식별에 있다.추정 1차 기흉에서는 표백이나 낭포성 병변을 식별하는 데 도움이 될 수 있으며(치료 예상 시, 아래 참조), 2차 기흉에서는 위에 열거된 원인 대부분을 식별하는 데 도움이 될 수 있다.[14][18]
초음파
초음파는 예를 들어 FAST 프로토콜과 같이 신체적 외상을 입은 사람들을 평가하는 데 일반적으로 사용된다.[31]흉부에 둔기에 의한 외상 후 기흉의 식별에 있어서 초음파는 흉부 X선보다 민감할 수 있다.[32]초음파는 또한 다른 응급 상황에서 신속한 진단을 제공할 수 있으며 기흉 크기를 정량화할 수 있다.흉부의 초음파 검사에 관한 몇 가지 특정한 특징을 사용하여 진단을 확인하거나 제외할 수 있다.[33][34]
치료
기흉의 치료는 여러 가지 요인에 따라 다르며 조기 사후관리 시 방전부터 즉시 바늘을 감압하거나 흉관을 삽입할 때까지 다양할 수 있다.치료는 급성 질환의 증상과 지표의 심각성, 기저 폐질환의 유무, X-ray 상의 기흉 추정 크기, 그리고 경우에 따라 관련자의 개인적 선호도에 따라 결정된다.[14]
외상성 기흉에서는 보통 흉관을 삽입한다.기계적 인공호흡이 필요할 경우 장력 기흉 위험이 크게 높아지고 흉관 삽입이 의무화된다.[13][37]열려 있는 흉부 상처는 긴장의 기흉으로 이어질 위험이 높으므로 밀폐된 밀봉으로 덮어야 한다.'애서맨 실'이라 불리는 드레싱은 표준 '3면' 드레싱보다 효과가 더 있어 보이는 만큼 이상적으로 활용해야 한다.애셔먼 밀봉은 흉벽에 달라붙어 밸브와 같은 메커니즘을 통해 공기가 빠져나오지만 가슴으로 들어가지 않는 특수 설계된 장치다.[38]
장력 기흉은 보통 급한 바늘 감압으로 치료된다.이는 병원으로 이송하기 전에 필요할 수 있으며 응급 의료 기술자 또는 기타 훈련된 전문가가 수행할 수 있다.[15][38]바늘이나 캐뉼라는 흉관을 삽입할 수 있을 때까지 제자리에 둔다.[15][38]중환자실 팀은 흉부 배수관을 삽입하지 않고 흉부를 절개하여 흉부 배수관을 배치할 때 수행되는 것처럼 더 큰 관을 만들 수 있다.이것은 단순한 흉곽 절제술이라고 불린다.[39]장력 기흉이 심장마비로 이어질 경우 심박출량을 회복할 수 있으므로 바늘의 감압 또는 단순 흉곽 절제술을 소생술의 일부로 수행한다.[40]
보수적인
작은 자발적 기흉은 호흡부전이나 긴장성 기흉으로 진행되지 않고 일반적으로 자연적으로 해결되기 어렵기 때문에 항상 치료가 필요한 것은 아니다.이 접근법은 기흉의 추정 크기가 작을 경우(<혈흉 부피의 50 %>로 정의), 호흡곤란이 없고, 기저 폐질환이 없는 경우에 가장 적합하다.[18][30]증상이 제한적일 경우 더 큰 PSP를 보수적으로 치료하는 것이 적절할 수 있다.[14]증상이 악화될 경우 병원에 복귀하라는 명확한 지시가 내려지는 한 입원은 필요 없는 경우가 많다.추가 조사는 외래환자로 실시할 수 있으며, 이때 개선확인을 위해 X선을 반복하고 재발방지에 관한 조언(아래 참조)[14]을 할 수 있다.예상 재흡수율은 1일 충치 부피 1.25%~2.2%이다.이것은 완전한 기흉도 약 6주 동안 자연적으로 해소된다는 것을 의미한다.[14]그러나 보수적인 경영과 비보수적인 경영을 비교하는 수준 높은 증거는 없다.[41]
2차 기흉은 크기가 매우 작고(1cm 이하 공기림) 증상이 제한적일 때만 보수적으로 치료한다.입원하는 것이 보통 권장된다.높은 유량으로 주어진 산소는 4배만큼 재흡수를 가속할 수 있다.[14][42]
흡인
대형 PSP(>50%)에서, 또는 호흡 곤란과 관련된 PSP에서, 일부 지침은 흡인하여 크기를 줄이는 것이 흉관 삽입과 동일하게 효과적이라고 권고한다.이것은 국소 마취제를 투여하고 3방향 수돗물에 연결된 바늘을 삽입하는 것과 관련이 있다; 최대 2.5리터의 공기가 제거된다.후속 X선 촬영 시 기흉 크기가 크게 줄어든 경우 나머지 치료는 보수적일 수 있다.이 접근방식은 50% 이상의 사례에서 효과가 있는 것으로 나타났다.[12][14][18]관배수에 비해 PSP의 1선 포부는 합병증의 위험을 높이지 않고 입원해야 하는 인원을 줄인다.[43]
또한 성공적인 시술 후에도 병원에서 지속적인 관찰이 필요하다는 차이와 함께 호흡이 없는 적당한 크기의 2차 기흉(공기 림 1-2cm)에서도 흡인을 고려할 수 있다.[14]미국의 전문지침은 PSP에 기인한 모든 큰 기흉은 흉관으로 치료해야 한다고 명시하고 있다.[30]적절한 크기의 이아트로겐성 외상성 기흉(의료 절차로 인한)은 초기에 흡인하여 치료할 수 있다.[13]
흉관
흉관(또는 비용간 배수구)은 기흉의 가장 확실한 초기 치료법이다.이것들은 일반적으로 "안전한 삼각형"이라고 불리는 축대 아래 영역에 삽입되는데, 이것은 젖꼭지 수준의 수평선과 흉벽의 두 근육에 의해 묘사된다.국소마취제를 투여한다.두 가지 유형의 튜브를 사용할 수 있다.자발적 기흉에서는 셀딩거 기법으로 소보어(소형 14F, 직경 4.7mm) 관을 삽입할 수 있으며, 큰 관은 유리하지 않다.[14][44]외상성 기흉에서는 더 큰 관(28F, 9.3 mm)을 사용한다.[38]무뎌지거나 관통하는 외상으로 인해 흉관을 놓을 때 항생제는 전염성 합병증의 위험을 감소시킨다.[45]
흉부 튜브는 바늘 흡기에 반응하지 않은 PSP, 대형 SSP(>50%) 및 장력 기흉의 경우에 필요하다.그것들은 공기가 빠져나갈 수는 있지만 가슴으로 다시 들어갈 수는 없는 단방향 밸브 시스템에 연결되어 있다.여기에는 워터 씰과 같은 기능을 하는 물이 들어 있는 병 또는 Heimlich 밸브가 포함될 수 있다.이들은 일반적으로 음압 회로에 연결되지 않는데, 이는 폐의 빠른 재확장 및 폐부종의 위험("재확장 폐부종")을 초래할 수 있기 때문이다.튜브는 일정 기간 동안 공기가 빠져나가지 않을 때까지 제자리에 방치되며, 엑스레이를 통해 폐의 재확장 여부를 확인하게 된다.[14][18][30]
만약 2-4일이 지난 후에도 여전히 공기 누출의 증거가 있다면, 다양한 옵션을 이용할 수 있다.특히 PSP에서는 높은 유량의 음압 흡인( –10 ~ –20 cmHO의2 저압)을 시도할 수 있으며, 이는 누출의 치유를 가속화할 수 있다고 생각된다.이것이 실패하면, 특히 SSP에서 수술이 필요할 수 있다.[14]
흉곽관은 AIDS 환자에게 기흉이 발생할 때 주로 기저폐렴성 폐렴(PCP)에 의한 것으로 장시간 공기누출과 관련이 있기 때문에 우선 사용된다.양쪽 기흉(양쪽 기흉)은 폐렴에 걸린 사람에게 비교적 흔하며 수술도 필요한 경우가 많다.[14]
흉부 관을 가진 사람이 하이믈리치 밸브를 사용하여 보행기 관리 환경에서 관리되는 것은 가능하지만, 입원 시 동등하다는 것을 증명하는 연구는 제한적인 품질을 가지고 있다.[46]
플뢰로데시스 및 수술
플뢰로데시스는 흉막 공간을 영구적으로 제거하고 폐를 흉벽에 붙이는 시술이다.그 결과에 대해 어떤 장기 연구(20년 이상)도 수행되지 않았다.단기적으로 좋은 결과는 공기 누출의 원인 파악과 표백의 스테이플링으로 개흉술(가슴의 수술적 개방)을 거쳐 외측 흉막의 흉막절제술(흉막절개술)과 내측막의 흉막마모술(흉막마모술)을 통해 달성된다.치유 과정에서 폐가 흉벽에 달라붙어 흉막 공간을 효과적으로 없앤다.재발률은 약 1%이다.[12][14]개흉 후 통증은 비교적 흔하다.
덜 침습적인 접근법은 대개 비디오 보조 흉곽 수술(VATS)이라고 불리는 절차의 형태로 흉곽내시경이다.VATS 기반 흉막 마멸의 결과는 단기적으로 개흉술을 사용하여 얻은 것보다 약간 더 나쁘지만 피부에 더 작은 흉터를 만들어 낸다.[12][14]VATS는 개흉술에 비해 입원 기간이 짧고, 수술 후 통증 조절 필요성이 적으며, 수술 후 폐 질환의 위험성이 줄어든다.[14]VATS는 또한 화학적 플레루로데시스(Pleurodesis)를 얻기 위해 사용될 수 있다; 이것은 폐가 흉벽에 붙게 하는 염증 반응을 활성화시키는 탈크를 절연하는 것을 포함한다.[12][14]
흉곽관이 이미 제자리에 있는 경우, 탈크, 테트라사이클린, 미노시클린 또는 독시사이클린과 같은 화학적 플레루로데시스를 얻기 위해 관을 통해 다양한 약물을 주입할 수 있다.화학적 늑막염의 결과는 외과적 접근법을 사용할 때보다 더 나쁜 경향이 있지만,[12][14] 탈크 늑막염은 젊은 사람들에게 부정적인 장기적 결과를 거의 가지고 있지 않은 것으로 밝혀졌다.[12]
애프터케어
기흉이 흡연자에게 발생할 경우, 이는 흡연을 계속하는 사람에게 현저하게 증가하는 재발 위험과 금연에 따른 많은 이점을 강조하는 기회로 여겨진다.[14]자발적 기흉이 발생한 후 일주일까지 일을 하지 않는 것이 바람직할 수 있다.만약 그 사람이 보통 심한 육체 노동을 한다면, 몇 주가 필요할 수 있다.늑막염을 앓은 사람들은 회복하기 위해 2~3주간의 휴가가 필요할지도 모른다.[47]
재발하지 않을 경우 기흉을 완전히 해결한 후 최대 7일간 항공여행이 금지된다.[14]수중 다이빙은 예방 절차가 수행되지 않는 한 기흉 발생 후 안전하지 않은 것으로 간주된다.전문지침은 양쪽 폐에 흉막절제술을 시행하고, 다이빙을 재개하기 전에 폐 기능검사와 CT스캔이 정상화된다는 내용을 담고 있다.[14][30]항공기 조종사들은 수술에 대한 평가를 요구할 수도 있다.[14]
신생아기
기흉이 있는 신생아의 경우 세심한 관찰, 흉곽(신경 흡인), 흉관 삽입 등 다양한 관리전략이 제시됐다.[24]바늘 흡인은 흉관의 필요성을 줄일 수 있지만, 두 침습적 시술의 효과와 안전성은 완전히 연구되지 않았다.[24]
예방
기흉 발생 후 재발방지를 위한 예방적 절차(흉막절개술 또는 흉막절개술을 통한 흉곽내시경)를 권고할 수 있다.가장 효과적인 치료법에 대한 증거는 여전히 일부 분야에서 상충되고 있으며 유럽과 미국에서 이용할 수 있는 치료법들 사이에 차이가 있다.[12]기흉의 모든 에피소드들이 그러한 개입을 필요로 하는 것은 아니다; 결정은 주로 재발의 위험의 추정에 달려 있다.이러한 절차는 종종 두 번째 기흉이 발생한 후에 권장된다.[48]만약 어떤 사람이 양쪽 기흉을 경험했다면("양면"), 양쪽이 관련된 순차적인 에피소드 또는 어떤 에피소드가 임신과 관련이 있다면 수술은 고려할 필요가 있을 것이다.[14]
역학
PSP의 연간 연령 조정 발병률(AAIR)은 남성이 여성보다 3배에서 6배 정도 높은 것으로 생각된다.피쉬맨은[49][50] AAIR의 경우 남성과 여성의 경우 각각 10만 명당 7.4건과 1.2건을 인용하고 있다.평균 높이보다 훨씬 높은 것은 PSP 위험 증가와도 관련이 있다 – 최소 76인치(1.93m)의 경우 AIR은 10만 명당 약 200건이다.슬림한 체격도 PSP의 위험을 높이는 것으로 보인다.[49]
남성 흡연자와 여성 흡연자의 첫 번째 자발적 기흉에 걸릴 위험은 같은 성별의 비흡연자와 비교했을 때 각각 약 22와 9의 요인에 의해 높아진다.[51]흡연율이 높은 개인은 "선형보다 더 큰" 효과로 더 높은 위험에 처해 있다. 하루에 10개 담배를 피우는 남성은 비흡연자에 비해 약 20배 더 높은 위험을 가지고 있는 반면, 하루에 20개 담배를 피우는 흡연자는 약 100배 더 높은 위험 증가를 보인다.[49]
2차 자연발생성 기흉에서 연간 AIR 추정치는 각각 남성과 여성의 10만 명당 6.3건과 2.0건으로, 기저 폐질환의 유무와 심각도에 따라 재발의 위험이 있다.[20][52]일단 두 번째 에피소드가 발생하게 되면 후속 에피소드가 이어질 가능성이 높다.[12]어린이의 발병률은 잘 연구되지 않았지만 10만 명당 5~10명 정도로 추정된다.[18][53]
기흉으로 인한 죽음은 매우 드물다(긴장 기흉 제외).영국의 통계에 따르면 남성과 여성의 연간 사망률은 각각 1.26명, 0.62명이다.[14]사망위험이 크게 증가한 것은 고령의 피해자와 2차 기흉을 가진 사람들에게서 볼 수 있다.[12]
역사
갈비뼈 골절에 대한 외상성 기흉 이차적 설명은 터키의 외과의사 에라페딘 사분쿠오울루(1385–1468)에 의한 임페리얼 수술에 나타나며, 이는 또한 단순한 흡인 방법을 추천한다.[54]
기흉은 1803년 르네 레이넥의 학생인 장 마르크 가스파드 이타르에 의해 묘사되었는데, 그는 1819년 임상 사진에 대한 광범위한 설명을 제공하였다.[55]Itard와 Laeneck은 일부 사례가 결핵(당시 가장 흔한 원인)에 기인한 것이 아니라는 것을 인식한 반면, 1932년 덴마크의 의사 한스 Kjærgaard에 의해 결핵(제1차 기흉)이 없을 때의 자발적 기흉의 개념이 다시 도입되었다.[14][26][56]1941년, 외과의사 타이슨과 크랜달은 기흉 치료를 위해 흉막 마모를 도입했다.[14][57]
기흉은 결핵에 걸린 사람들의 건강관리 제공자들에 의해 고의적으로 발생했는데, 이는 충치를 일으키는 병변 주위에 있는 로브, 즉 폐 전체를 쓰러뜨리기 위한 노력이었다.이것은 "폐를 고치는 것"으로 알려져 있었다.1888년 이탈리아의 외과의사 카를로 포를라니니가 도입하고, 20세기 초 미국의 외과의사 존 벤자민 머피(John Benjamin Murphy)가 독자적으로 같은 절차를 발견해 공표했다.머피는 최근 발견된 X선 기술을 이용해 정확한 크기의 기흉을 만들었다.[58]
어원
기흉이라는 단어는 그리스 기흉에서 유래했다. 기흉은 공기를 의미하고 흉부는 가슴을 의미한다.[59]그것의 복수형은 기흉이다.
다른동물
인간이 아닌 동물들은 자발적인 기흉과 외상적인 기흉을 모두 경험할 수 있다.자발적 기흉은 인간에서와 같이 일차적 또는 이차적으로 분류되는 반면 외상성 기흉은 개방적 기흉과 폐쇄적 기흉(가슴벽 손상이 있거나 없거나)으로 구분된다.[60]이 진단은 수의사에게 명백하게 나타날 수 있다. 왜냐하면 그 동물은 호흡이 곤란하거나 얕은 호흡을 가지고 있기 때문이다.기흉은 폐 병변(불래 등)이나 흉벽에 대한 외상으로부터 발생할 수 있다.[61]말에서 외상성 기흉은 양쪽 혈관이 모두 관여할 수 있는데, 종격막은 불완전하고 가슴의 두 반쪽 사이에 직접적인 관계가 있기 때문이다.[62]장력 기흉은 심장 기능이 급격히 저하되고 흉부 전체에 폐음이 없고, 통 모양의 흉부 등으로 인해 의심받을 수 있는 것으로 동물의 가슴을 절개하여 압력을 완화한 후 흉관을 삽입한다.[63]자발적 기흉의 경우 개와[64] 쿠네쿠네 돼지에 대해 CT를 진단에 사용하는 것이 설명되어 있다.[65]
참조
- ^ a b Orenstein DM (2004). Cystic Fibrosis: A Guide for Patient and Family. Lippincott Williams & Wilkins. p. 62. ISBN 9780781741521. Archived from the original on 31 October 2016.
- ^ a b c d "What Are the Signs and Symptoms of Pleurisy and Other Pleural Disorders". www.nhlbi.nih.gov. 21 September 2011. Archived from the original on 8 October 2016. Retrieved 31 October 2016.
- ^ a b c d e f g h i j k l m n o p q r s t u Bintcliffe O, Maskell N (May 2014). "Spontaneous pneumothorax". BMJ. 348: g2928. doi:10.1136/bmj.g2928. PMID 24812003. S2CID 32575512.
- ^ a b "What Causes Pleurisy and Other Pleural Disorders?". NHLBI. 21 September 2011. Archived from the original on 8 October 2016. Retrieved 31 October 2016.
- ^ a b c d Chen L, Zhang Z (August 2015). "Bedside ultrasonography for diagnosis of pneumothorax". Quantitative Imaging in Medicine and Surgery. 5 (4): 618–623. doi:10.3978/j.issn.2223-4292.2015.05.04. PMC 4559988. PMID 26435925.
- ^ Morjaria JB, Lakshminarayana UB, Liu-Shiu-Cheong P, Kastelik JA (November 2014). "Pneumothorax: a tale of pain or spontaneity". Therapeutic Advances in Chronic Disease. 5 (6): 269–273. doi:10.1177/2040622314551549. PMC 4205574. PMID 25364493.
- ^ Weinberger S, Cockrill B, Mandel J (2019). Principles of Pulmonary Medicine (7th ed.). Elsevier. pp. 215–216. ISBN 9780323523714.
- ^ Slade M (December 2014). "Management of pneumothorax and prolonged air leak". Seminars in Respiratory and Critical Care Medicine. 35 (6): 706–714. doi:10.1055/s-0034-1395502. PMID 25463161.
- ^ a b Wolf SJ, Bebarta VS, Bonnett CJ, Pons PT, Cantrill SV (August 2009). "Blast injuries". Lancet. 374 (9687): 405–415. doi:10.1016/S0140-6736(09)60257-9. PMID 19631372. S2CID 13746434.
- ^ Yarmus L, Feller-Kopman D (April 2012). "Pneumothorax in the critically ill patient". Chest. 141 (4): 1098–1105. doi:10.1378/chest.11-1691. PMID 22474153. S2CID 207386345.
- ^ Peters JR, Egan D, Mick NW (2006). Nadel ES (ed.). Blueprints Emergency Medicine. Lippincott Williams & Wilkins. p. 44. ISBN 9781405104616. Archived from the original on 1 November 2016.
- ^ a b c d e f g h i j k l m n o p q r s t Tschopp JM, Rami-Porta R, Noppen M, Astoul P (September 2006). "Management of spontaneous pneumothorax: state of the art". The European Respiratory Journal. 28 (3): 637–650. doi:10.1183/09031936.06.00014206. PMID 16946095.
- ^ a b c d e f g h i j k l m n o p q Noppen M, De Keukeleire T (2008). "Pneumothorax". Respiration; International Review of Thoracic Diseases. 76 (2): 121–127. doi:10.1159/000135932. PMID 18708734.
- ^ a b c d e f g h i j k l m n o p q r s t u v w x y z aa ab ac ad ae af ag ah ai aj ak al am an ao MacDuff A, Arnold A, Harvey J, et al. (BTS Pleural Disease Guideline Group) (August 2010). "Management of spontaneous pneumothorax: British Thoracic Society Pleural Disease Guideline 2010". Thorax. 65 (8 Suppl 2): ii18–ii31. doi:10.1136/thx.2010.136986. PMID 20696690.
- ^ a b c d e f g h i j Leigh-Smith S, Harris T (January 2005). "Tension pneumothorax--time for a re-think?". Emergency Medicine Journal. 22 (1): 8–16. doi:10.1136/emj.2003.010421. PMC 1726546. PMID 15611534.
- ^ Lyra RD (May–June 2016). "Etiology of primary spontaneous pneumothorax". Jornal Brasileiro de Pneumologia. 42 (3): 222–226. doi:10.1590/S1806-37562015000000230. PMC 5569604. PMID 27383937.
- ^ a b c d e Marx J (2010). Rosen's emergency medicine: concepts and clinical practice (7th ed.). Philadelphia, PA: Mosby/Elsevier. pp. 393–96. ISBN 978-0-323-05472-0.
- ^ a b c d e f g h i j Robinson PD, Cooper P, Ranganathan SC (September 2009). "Evidence-based management of paediatric primary spontaneous pneumothorax". Paediatric Respiratory Reviews. 10 (3): 110–7, quiz 117. doi:10.1016/j.prrv.2008.12.003. PMID 19651381.
- ^ a b c Chiu HT, Garcia CK (July 2006). "Familial spontaneous pneumothorax". Current Opinion in Pulmonary Medicine. 12 (4): 268–272. doi:10.1097/01.mcp.0000230630.73139.f0. PMID 16825879. S2CID 45908721.
- ^ a b Levine DJ, Sako EY, Peters J (2008). Fishman's Pulmonary Diseases and Disorders (4th ed.). McGraw-Hill. p. 1520. ISBN 978-0-07-145739-2.
- ^ Light RW (2007). Pleural diseases (5th ed.). Lippincott Williams & Wilkins. p. 307. ISBN 978-0-7817-6957-0.
- ^ Nicholas Rathert, W. Scott Gilmore, MD, EMT-P (19 July 2013). "Treating Sucking Chest Wounds and Other Traumatic Chest Injuries". www.jems.com. Journal of Emergency Medical Services. Archived from the original on 8 April 2015. Retrieved 28 September 2017.
- ^ a b Neuman TS (2003). "Arterial gas embolism and pulmonary barotrauma". In Brubakk AO, Neuman TS (eds.). Bennett and Elliott's physiology and medicine of diving (5th Rev ed.). United States: Saunders. pp. 558–61. ISBN 978-0-7020-2571-6.
- ^ a b c Bruschettini M, Romantsik O, Zappettini S, O'Donnell CP, Calevo MG (February 2019). "Needle aspiration versus intercostal tube drainage for pneumothorax in the newborn". The Cochrane Database of Systematic Reviews. 2: CD011724. doi:10.1002/14651858.CD011724.pub3. PMC 6357997. PMID 30707441.
- ^ Neupane K, Jamil R. "Physiology, Transpulmonary Pressure". NCBI National Center for Biotechnology Information. PMID 32644430.
- ^ a b c Grundy S, Bentley A, Tschopp JM (2012). "Primary spontaneous pneumothorax: a diffuse disease of the pleura". Respiration; International Review of Thoracic Diseases. 83 (3): 185–189. doi:10.1159/000335993. PMID 22343477.
- ^ Seow A, Kazerooni EA, Pernicano PG, Neary M (February 1996). "Comparison of upright inspiratory and expiratory chest radiographs for detecting pneumothoraces". AJR. American Journal of Roentgenology. 166 (2): 313–316. doi:10.2214/ajr.166.2.8553937. PMID 8553937.
- ^ MacDuff A, Arnold A, Harvey J (August 2010). "Management of spontaneous pneumothorax: British Thoracic Society Pleural Disease Guideline 2010". Thorax. 65 (Suppl 2): ii18–ii31. doi:10.1136/thx.2010.136986. PMID 20696690.
- ^ O'Connor AR, Morgan WE (June 2005). "Radiological review of pneumothorax". BMJ. 330 (7506): 1493–1497. doi:10.1136/bmj.330.7506.1493. PMC 558461. PMID 15976424.
- ^ a b c d e f Baumann MH, Strange C, Heffner JE, Light R, Kirby TJ, Klein J, et al. (February 2001). "Management of spontaneous pneumothorax: an American College of Chest Physicians Delphi consensus statement". Chest. 119 (2): 590–602. doi:10.1378/chest.119.2.590. PMID 11171742.
- ^ Scalea TM, Rodriguez A, Chiu WC, Brenneman FD, Fallon WF, Kato K, et al. (March 1999). "Focused Assessment with Sonography for Trauma (FAST): results from an international consensus conference". The Journal of Trauma. 46 (3): 466–472. doi:10.1097/00005373-199903000-00022. PMID 10088853. S2CID 19871141.
- ^ Wilkerson RG, Stone MB (January 2010). "Sensitivity of bedside ultrasound and supine anteroposterior chest radiographs for the identification of pneumothorax after blunt trauma". Academic Emergency Medicine. 17 (1): 11–17. doi:10.1111/j.1553-2712.2009.00628.x. PMID 20078434. S2CID 8184800.
- ^ Volpicelli G (February 2011). "Sonographic diagnosis of pneumothorax". Intensive Care Medicine. 37 (2): 224–232. doi:10.1007/s00134-010-2079-y. PMID 21103861. S2CID 24664490.
- ^ Staub LJ, Biscaro RR, Kaszubowski E, Maurici R (March 2018). "Chest ultrasonography for the emergency diagnosis of traumatic pneumothorax and haemothorax: A systematic review and meta-analysis". Injury. 49 (3): 457–466. doi:10.1016/j.injury.2018.01.033. PMID 29433802.
- ^ "UOTW #6 – Ultrasound of the Week". Ultrasound of the Week. 24 June 2014. Archived from the original on 8 September 2017. Retrieved 27 May 2017.
- ^ "UOTW #62 – Ultrasound of the Week". Ultrasound of the Week. 25 October 2015. Archived from the original on 9 May 2017.
- ^ Keel M, Meier C (December 2007). "Chest injuries - what is new?". Current Opinion in Critical Care. 13 (6): 674–679. doi:10.1097/MCC.0b013e3282f1fe71. PMID 17975389. S2CID 19317500.
- ^ a b c d Lee C, Revell M, Porter K, Steyn R (March 2007). "The prehospital management of chest injuries: a consensus statement. Faculty of Pre-hospital Care, Royal College of Surgeons of Edinburgh". Emergency Medicine Journal. 24 (3): 220–224. doi:10.1136/emj.2006.043687. PMC 2660039. PMID 17351237.
- ^ Mohrsen S, McMahon N, Corfield A, McKee S (December 2021). "Complications associated with pre-hospital open thoracostomies: a rapid review". Scandinavian Journal of Trauma, Resuscitation and Emergency Medicine. 29 (1): 166. doi:10.1186/s13049-021-00976-1. PMC 8643006. PMID 34863280.
- ^ Neumar RW, Otto CW, Link MS, Kronick SL, Shuster M, Callaway CW, et al. (November 2010). "Part 8: adult advanced cardiovascular life support: 2010 American Heart Association Guidelines for Cardiopulmonary Resuscitation and Emergency Cardiovascular Care". Circulation. 122 (18 Suppl 3): S729–S767. doi:10.1161/CIRCULATIONAHA.110.970988. PMID 20956224.
- ^ Ashby M, Haug G, Mulcahy P, Ogden KJ, Jensen O, Walters JA (December 2014). "Conservative versus interventional management for primary spontaneous pneumothorax in adults". The Cochrane Database of Systematic Reviews. 12 (12): CD010565. doi:10.1002/14651858.CD010565.pub2. PMC 6516953. PMID 25519778.
- ^ Light RW (2007). Pleural diseases (5th ed.). Lippincott Williams & Wilkins. p. 310. ISBN 978-0-7817-6957-0.
- ^ Carson-Chahhoud KV, Wakai A, van Agteren JE, Smith BJ, McCabe G, Brinn MP, O'Sullivan R (September 2017). "Simple aspiration versus intercostal tube drainage for primary spontaneous pneumothorax in adults". The Cochrane Database of Systematic Reviews. 9 (12): CD004479. doi:10.1002/14651858.CD004479.pub3. PMC 6483783. PMID 28881006.
- ^ Chang SH, Kang YN, Chiu HY, Chiu YH (May 2018). "A Systematic Review and Meta-Analysis Comparing Pigtail Catheter and Chest Tube as the Initial Treatment for Pneumothorax". Chest. 153 (5): 1201–1212. doi:10.1016/j.chest.2018.01.048. PMID 29452099. S2CID 4587316.
- ^ Ayoub F, Quirke M, Frith D (2019). "Use of prophylactic antibiotic in preventing complications for blunt and penetrating chest trauma requiring chest drain insertion: a systematic review and meta-analysis". Trauma Surgery & Acute Care Open. 4 (1): e000246. doi:10.1136/tsaco-2018-000246. PMC 6407548. PMID 30899791.
- ^ Brims FJ, Maskell NA (July 2013). "Ambulatory treatment in the management of pneumothorax: a systematic review of the literature". Thorax. 68 (7): 664–669. doi:10.1136/thoraxjnl-2012-202875. PMID 23515437.
- ^ Brown I, Palmer KT, Robin C (2007). Fitness for work: the medical aspects. Oxford: Oxford University Press. pp. 481–82. ISBN 978-0-19-921565-2.
- ^ Baumann MH, Noppen M (June 2004). "Pneumothorax". Respirology. 9 (2): 157–164. doi:10.1111/j.1440-1843.2004.00577.x. PMID 15182264. S2CID 222188018.
- ^ a b c Levine DJ, Sako EY, Peters J (2008). Fishman's Pulmonary Diseases and Disorders (4th ed.). McGraw-Hill. p. 1519. ISBN 978-0-07-145739-2.
- ^ Light RW (2007). Pleural diseases (5th ed.). Lippincott Williams & Wilkins. p. 306. ISBN 978-0-7817-6957-0.
- ^ Bense L, Eklund G, Wiman LG (December 1987). "Smoking and the increased risk of contracting spontaneous pneumothorax". Chest. 92 (6): 1009–1012. doi:10.1378/chest.92.6.1009. PMID 3677805. S2CID 16838594.
- ^ Light RW (2007). Pleural diseases (5th ed.). Lippincott Williams & Wilkins. p. 315. ISBN 978-0-7817-6957-0.
- ^ Sahn SA, Heffner JE (March 2000). "Spontaneous pneumothorax". The New England Journal of Medicine. 342 (12): 868–874. doi:10.1056/NEJM200003233421207. PMID 10727592.
- ^ Kaya SO, Karatepe M, Tok T, Onem G, Dursunoglu N, Goksin I (September 2009). "Were pneumothorax and its management known in 15th-century anatolia?". Texas Heart Institute Journal. 36 (2): 152–153. PMC 2676596. PMID 19436812.
- ^ Laennec RT (1819). Traité de l'auscultation médiate et des maladies des poumons et du coeur – part II (in French). Paris.
- ^ Kjærgard H (1932). "Spontaneous pneumothorax in the apparently healthy". Acta Medica Scandinavica. 43 (Suppl): 1–159. doi:10.1111/j.0954-6820.1932.tb05982.x.
- ^ Tyson MD, Crandall WB (1941). "The surgical treatment of recurrent idiopathic spontaneous pneumothorax". Journal of Thoracic Surgery. 10 (5): 566–70. doi:10.1016/S0096-5588(20)32206-6.
- ^ Herzog H (1998). "History of tuberculosis". Respiration; International Review of Thoracic Diseases. 65 (1): 5–15. doi:10.1159/000029220. PMID 9523361.
- ^ Stevenson A (2010). Oxford Dictionary of English. OUP Oxford. p. 1369. ISBN 9780199571123. Archived from the original on 14 September 2016.
- ^ Pawloski DR, Broaddus KD (2010). "Pneumothorax: a review". Journal of the American Animal Hospital Association. 46 (6): 385–397. doi:10.5326/0460385. PMID 21041331.
- ^ "Causes of Respiratory Malfunction". Merck Veterinary Manual, 9th edition (online version). 2005. Archived from the original on 26 November 2010. Retrieved 5 June 2011.
- ^ "Equine trauma and first aid: wounds and lacerations". Merck Veterinary Manual, 9th edition (online version). 2005. Archived from the original on 6 September 2009. Retrieved 5 June 2011.
- ^ "Primary survey and triage - breathing". Merck Veterinary Manual, 9th edition (online version). 2005. Archived from the original on 28 October 2011. Retrieved 5 June 2011.
- ^ Au JJ, Weisman DL, Stefanacci JD, Palmisano MP (March 2006). "Use of computed tomography for evaluation of lung lesions associated with spontaneous pneumothorax in dogs: 12 cases (1999-2002)". Journal of the American Veterinary Medical Association. 228 (5): 733–737. doi:10.2460/javma.228.5.733. PMID 16506938.
- ^ Smith J, Cuneo M, Walton R, White R, Busch R, Chigerwe M (April 2020). "Spontaneous Pneumothorax in a Companion Kunekune Pig due to Pulmonary Bullae Rupture". Journal of Exotic Pet Medicine. 34: 6–9. doi:10.1053/j.jepm.2020.04.001. S2CID 218806957.