대응물
Aprepitant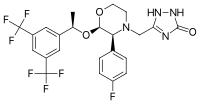 | |
 | |
| 임상 데이터 | |
|---|---|
| 상호 | 수정 |
| AHFS/Drugs.com | 모노그래프 |
| Medline Plus | a604003 |
| 라이선스 데이터 | |
| 임신 카테고리 |
|
| 루트 행정부. | 입으로 (캡슐) |
| ATC 코드 | |
| 법적 상태 | |
| 법적 상태 | |
| 약동학 데이터 | |
| 바이오 어베이러빌리티 | 60–65% |
| 단백질 결합 | 95% 이상 |
| 대사 | 간(대부분 CYP3A4 매개, CYP2C19 및 CYP1A2에 의한 일부 기여) |
| 반감기 제거 | 9~13시간 |
| 배설물 | 소변(57%), 대변(45%) |
| 식별자 | |
| |
| CAS 번호 | |
| PubChem CID | |
| IUPHAR/BPS | |
| 드러그뱅크 | |
| 켐스파이더 | |
| 유니 | |
| 체비 | |
| 첸블 | |
| CompTox 대시보드 (EPA ) | |
| ECHA 정보 카드 | 100.202.762 |
| 화학 및 물리 데이터 | |
| 공식 | C23H21F7N4O3 |
| 몰 질량 | 534.435 g/120−1 |
| 3D 모델(JSmol) | |
| |
| |
| (표준) | |
항진제(Aprepective)는 Emend라는 브랜드명으로 판매되며 화학요법으로 인한 메스꺼움과 구토(CINV)를 예방하고 수술 후 메스꺼움과 [1]구토를 예방하기 위해 사용되는 의약품입니다.온단셋론, 덱사메타손과 함께 [1]사용해도 좋다.입으로 [1]먹는 거예요.
일반적인 부작용으로는 피로감, 식욕부진, 설사, 복통, 딸꾹질, 가려움증, 폐렴, 혈압 변화가 [1]있다.다른 심각한 부작용에는 과민증이 [1]포함될 수 있다.임신 중 사용이 유해한 것으로 보이지는 않지만, 그러한 사용은 잘 [2]연구되지 않았다.항진제는 신경키닌-1 수용체 [1]길항제 약물에 속한다.물질 P가 [3]NK1 수용체에 부착되는 것을 차단함으로써 작용한다.
2003년 [1][3]유럽연합과 미국에서 의약품 사용이 승인되었다.그것은 Merck & Co.[1]에 의해 만들어졌다.그것은 세계보건기구의 필수 [4]의약품 목록에 있다.혈관에 주사함으로써 주어질 수 있는 형태, 즉 포사프립터라고 알려진 형태도 이용할 [1]수 있다.
의료 용도
항암제는 화학요법으로 인한 메스꺼움과 구토(CINV)를 예방하고 수술 후 메스꺼움과 [1]구토를 예방하기 위해 사용됩니다.장기 사용의 안전성과 유용성은 불명확하거나 이미 메스꺼움을 겪고 있는 사람들에게 명확하지 않다.[1]
온단셋론, 덱사메타손과 함께 [1]사용해도 좋다.입으로 [1]먹는 거예요.
작용 메커니즘
항진제는 NK 수용체에 의해1 전달되는 신호를 차단하기 때문에1 NK 길항제이다.따라서 이것은 환자의 구토 가능성을 감소시킨다.
NK는1 중추신경계와 말초신경계에 위치한 G단백질결합수용체이다.이 수용체는 물질 P로 알려진 지배적인 리간드를 가지고 있다. SP는 뇌에서 자극과 메시지를 보내는 11개의 아미노산으로 구성된 신경펩타이드이다.뇌의 구토 중추에서 고농도로 발견되며, 활성화되면 구토 반사를 일으킨다.이것 외에도, 그것은 또한 말초 수용체에서 중추 신경계로 통증 자극을 전달하는 데 중요한 역할을 한다.
세포독성 화학요법 약물에 의해 유발되는 급성 및 지연 구토를 뇌 신경세포 수용체에 물질 P가 착지하는 것을 차단함으로써 억제하는 것으로 나타났다.양전자방출단층촬영(PET) 연구는 혈액 뇌 장벽을 넘어 인간 [5]뇌의 NK 수용체와1 결합할 수 있다는 것을 보여주었다.또한 5-HT3 수용체 길항제 온단세트론과 코르티코스테로이드 덱사메타손의 활성을 증가시키는 것으로 나타났으며, 이들은 화학요법에 [6]의한 메스꺼움 및 구토 예방에도 사용된다.
항진제는 캡슐 형태로 경구 복용된다.임상시험 전에 새로운 종류의 치료제는 임상 전 대사 및 배설 연구의 관점에서 특징지어져야 한다.평균 생체 가용성은 약 60-65%인 것으로 밝혀졌다.어프리퍼틴은 주로 CYP3A4에 의해 대사되며, CYP1A2 및 CYP2C19에 의해 경미한 대사된다.사람의 혈장에서는 약하게만 활성인 7가지 항진제 대사물이 확인되었다.CYP3A4의 중간 억제제로서 CYP3A4를 통해 대사되는 공동 투여 의약품의 혈장 농도를 높일 수 있다.옥시코돈과의 특이적 상호작용은 억제작용이 효과를 증가시키고 옥시코돈의 부작용을 악화시키는 것으로 입증되었다. 그러나 이것이 CPY3A4 억제 때문인지 NK-1 길항제 [7]작용 때문인지는 불분명하다.C 라벨 부착 아프리퍼터 프로드러그(L-758298)를 IV 투여한 후, 총 방사능의 약 57%가 소변에 배설되고 45%가 대변에 배설된다.변함이 없는 물질은 [8]소변으로 배출되지 않는다.
구조 및 속성
항진제는 인접한 고리형 탄소에 2개의 치환기가 부착된 모르포린 코어로 구성된다.이들 치환기는 트리플루오로메틸화 1-페닐타놀기 및 플루오로페닐기이다.아프리퍼틴은 또한 모르포린 고리 질소에 결합되는 세 번째 치환기(트리아졸리논)를 가지고 있다.그것은 아미노 아세탈 배열을 만들기 위해 결합하는 세 개의 키랄 중심을 매우 가깝게 가지고 있습니다.그것의 경험식은 CHFNO이다2321743.
항산화제는 분자량이 약 534.53인 오프 화이트 결정성 고체입니다.물속에서는 용해도가 매우 제한적입니다.그것은 기름과 같은 비극성 분자에서 상당히 높은 용해도를 가지고 있다.따라서 이는 극성 성분이 있음에도 불구하고 전체적으로 무극성 물질임을 시사한다.
합성
Merck가 CINV의 심각성과 가능성을 줄이기 위한 연구를 시작한 지 얼마 지나지 않아, 연구원들은 대응제가 예방에 효과적이라는 것을 발견했다.연구원들은 적절한 물질을 만드는 과정을 고안해내는데 노력했고, 짧은 시간 안에 그들은 물질의 효과적인 합성을 생각해냈다.Merck는 이 원래의 합성은 실행 가능한 것으로 여겨졌고 상업화를 달성하는 데 중요한 단계로 판명되었다. 그러나 Merck는 이 과정이 환경적으로 지속 가능하지 않다고 결정했다.이것은 원래 합성이 6단계를 필요로 했기 때문인데, 그 중 다수는 시안화나트륨, 디메틸티탄세, 암모니아 가스 같은 위험한 화학물질을 필요로 했다.이 외에도, 효과적인 극저온 온도의 공정을 위해서는 일부 단계와 [9]메탄과 같은 유해 부산물이 생성되는 다른 단계가 필요했다.Merck 연구팀은 약물을 임상시험에서 철수시키고 다른 [10]약물의 합성을 시도하기로 결정할 정도로 환경적인 우려가 커졌다.
임상시험에서 약을 빼는 도박은 머크 연구팀이 대안적이고 환경친화적인 항진제 합성법을 고안해내면서 성공적이었다.새로운 공정은 크기와 복잡성이 비슷한 4가지 화합물이 융합되어 작용한다.따라서 이것은 훨씬 더 간단한 과정이며, 원래 합성의 절반인 3단계만 필요로 한다.
새로운 과정은 에난티오푸어 트리플루오로메틸화페닐에탄올이 라세믹 모르포린 전구체에 결합됨으로써 시작된다.그 결과 원하는 이성질체가 용액 위에 결정화되고 원치 않는 이성질체가 용액 안에 남게 됩니다.그런 다음 반응 조건을 제어하는 화학자에 의해 불필요한 이성질체가 원하는 이성질체로 전환되고 결정화 유도 비대칭 변환이 발생하는 과정으로 알려져 있다.이 공정의 종료에 의해 약물의 염기인 2차 아민이 형성된다.
두 번째 단계는 플루오로페닐기가 모르포린 고리에 부착되는 것을 포함한다.이 작업이 완료되면 세 번째 및 마지막 단계를 시작할 수 있습니다.이 단계는 트리아졸리논의 사이드 체인을 링에 추가하는 것을 포함했습니다.일단 이 단계가 성공적으로 완료되면 안정적인 분자의 항진제가 [11]생산됩니다.
이 보다 간소화된 루트는 원래 프로세스보다 약 76% 더 많은 대응력을 제공하며 운영 비용을 대폭 절감합니다.또한 새로운 공정은 필요한 용제 및 시약의 양을 약 80%까지 줄여 생산되는 [10]약 t당 약 340,000L를 절약합니다.
합성 공정의 개선은 또한 몇 가지 유해 화학 물질의 사용을 제거함으로써 원래 절차와 관련된 자연 환경에 대한 장기적인 피해를 줄였다.
역사
2003년 [12]미국 식품의약국(FDA)의 승인을 받았다.2008년 미국에서는 정맥주사 형태의 항진제인 항진제(fosaprepective)가 승인되었다.
조사.
주요 불황
항우울제로서 항응력을 개발하려는 계획은 [13]철회되었다.그 후, NK 수용체 길항제(casopitive 및 orveitant)를 사용한1 다른 시험들은 유망한 [14][15][16]결과를 보였다.
의견이 PET 수용체 점유 일상적으로 새로운 의료 지표로서 이 class,[17]> 또는 그들이 복용으로 사용되지 않다.;외에 99%인간의 수용체 점유 지속적인 또는psycho-pharmacological에 위의 데이터의 다른 치료 effects,[16]중요한 과학적 해부와 토론 ena하는데 필요할지도 모를 수 있습니다.aprepitbleCINV를 넘어 임상적으로1 예측된 효용(즉, 다른 정신 질환, 중독, 신경성 통증, 편두통, 골관절염, 과다 활성 방광, 염증성 장질환 및 염증성 성분이 의심되는 기타 장애)을 충족시키기 위해 개미와 NK 길항제 전체.그러나 대부분의 데이터는 소유권이므로, 즉응제와 같은 약물에 대한 확장된 임상 잠재력에 대한 검토는 낙관론에서[18] [19]빈곤론까지 다양하다.
레퍼런스
- ^ a b c d e f g h i j k l m "Aprepitant/Fosaprepitant Dimeglumine Monograph for Professionals". Drugs.com. Retrieved 13 October 2019.
- ^ "Aprepitant Use During Pregnancy". Drugs.com. Retrieved 13 October 2019.
- ^ a b "Emend". European Medicines Agency. 17 September 2018. Retrieved 13 October 2019.
- ^ World Health Organization (2019). World Health Organization model list of essential medicines: 21st list 2019. Geneva: World Health Organization. hdl:10665/325771. WHO/MVP/EMP/IAU/2019.06. License: CC BY-NC-SA 3.0 IGO.
- ^ Bergström, M; Hargreaves, RJ; Burns, HD; et al. (May 2004). "Human positron emission tomography studies of brain neurokinin 1 receptor occupancy by aprepitant". Biological Psychiatry. 55 (10): 1007–1012. doi:10.1016/j.biopsych.2004.02.007. PMID 15121485. S2CID 21071199.
- ^ Gralla R, de Wit R, Herrstedt J, Carides A, Ianus J, Guoguang-Ma J, Evans J, Horgan K (2005). "Antiemetic efficacy of the neurokinin-1 antagonist, aprepitant, plus a 5HT3 antagonist and a corticosteroid in patients receiving anthracyclines or cyclophosphamide in addition to high-dose cisplatin: analysis of combined data from two Phase III randomized clinical trials". Cancer. 104 (4): 864–8. doi:10.1002/cncr.21222. PMID 15973669. S2CID 24860776.
- ^ Walsh, S. L.; Heilig, M.; Nuzzo, P. A.; Henderson, P.; Lofwall, M. R. (2012). "Effects of the NK1 antagonist, aprepitant, on response to oral and intranasal oxycodone in prescription opioid abusers". Addiction Biology. 18 (2): 332–43. doi:10.1111/j.1369-1600.2011.00419.x. PMC 4354863. PMID 22260216.
- ^ FDA 자문위원회 배경 패키지
- ^ Hale, Jeffrey J. (1998). "Structural Optimization Affording 2-(R)-(1-(R)-3,5-Bis(trifluoromethyl)phenylethoxy)-3-(S)-(4-fluoro)phenyl-4- (3-oxo-1,2,4-triazol-5-yl)methylmorpholine, a Potent, Orally Active, Long-Acting Morpholine Acetal Human NK-1 Receptor Antagonist". Journal of Medicinal Chemistry. 41 (23): 4607–4614. doi:10.1021/jm980299k. PMID 9804700.
- ^ a b Hargreaves, Richard (2011). "Development of aprepitant, the first neurokinin-1 receptor antagonist for the prevention of chemotherapy-induced nausea and vomiting". Annals of the New York Academy of Sciences. 1222 (1): 40–48. Bibcode:2011NYASA1222...40H. doi:10.1111/j.1749-6632.2011.05961.x. PMID 21434941. S2CID 21202644.
- ^ Brands, Karel M. J. (2003). "Efficient Synthesis of NK1Receptor Antagonist Aprepitant Using a Crystallization-Induced Diastereoselective Transformation†". Journal of the American Chemical Society. 125 (8): 2129–2135. doi:10.1021/ja027458g. PMID 12590540.
- ^ "Drug Approval Package: EMEND (Aprepitant) NDA #21-549". Retrieved 2011-04-19.
- ^ Rupniak, NMJ; Kramer, MS (1 December 2017). "NK1 receptor antagonists for depression: Why a validated concept was abandoned". Journal of Affective Disorders. 223: 121–125. doi:10.1016/j.jad.2017.07.042. PMID 28753469.
- ^ Ratti, E; Bellew, K; Bettica, P; Bryson, H; Zamuner, S; Archer, G; Squassante, L; Bye, A; Trist, D; Krishnan, K. R.; Fernandes, S (2011). "Results from 2 randomized, double-blind, placebo-controlled studies of the novel NK1 receptor antagonist casopitant in patients with major depressive disorder". Journal of Clinical Psychopharmacology. 31 (6): 727–33. doi:10.1097/JCP.0b013e31823608ca. PMID 22020354. S2CID 24609826.
- ^ Trist, DG; Ratti, E; Bye, A (2013). "Why receptor reserve matters for neurokinin1 (NK1) receptor antagonists". J. Recept. Signal Transduct. Res. 33 (6): 333–7. doi:10.3109/10799893.2013.843194. PMID 24106886. S2CID 21799710.
- ^ a b Ratti, E; Bettica, P; Alexander, R; Archer, G; Carpenter, D; Evoniuk, G; Gomeni, R; Lawson, E; Lopez, M; Millns, H; Rabiner, E. A.; Trist, D; Trower, M; Zamuner, S; Krishnan, R; Fava, M (2013). "Full central neurokinin-1 receptor blockade is required for efficacy in depression: Evidence from orvepitant clinical studies". Journal of Psychopharmacology. 27 (5): 424–34. doi:10.1177/0269881113480990. PMID 23539641. S2CID 6523822.
- ^ Barrett, J. S.; McGuire, J; Vezina, H; Spitsin, S; Douglas, S. D. (2013). "PET measurement of receptor occupancy as a tool to guide dose selection in neuropharmacology: Are we asking the right questions?". Journal of Clinical Psychopharmacology. 33 (6): 725–8. doi:10.1097/JCP.0b013e3182a88654. PMID 24100788.
- ^ Herpfer, I; Lieb, K (2005). "Substance P receptor antagonists in psychiatry: rationale for development and therapeutic potential". CNS Drugs. 19 (4): 275–93. doi:10.2165/00023210-200519040-00001. PMID 15813642. S2CID 25497814.
- ^ Griebel, G; Holsboer, F (2012). "Neuropeptide receptor ligands as drugs for psychiatric diseases: the end of the beginning?". Nature Reviews Drug Discovery. 11 (6): 462–478. doi:10.1038/nrd3702. PMID 22596253. S2CID 10721248.
외부 링크
- "Aprepitant". Drug Information Portal. U.S. National Library of Medicine.


